pISSN: 0378-6471 eISSN: 2092-9374
http://dx.doi.org/10.3341/jkos.2013.54.1.170
= 증례보고 =
망막혈관증식성 종양 3예
노동현⋅사공민⋅장우혁 영남대학교 의과대학 안과학교실
목적: 망막혈관증식성 종양은 양성 종양이지만 여러 합병증을 동반할 수 있으며 동반되는 합병증에 따라 다양한 치료법이 보고되고 있다. 우연히 발견된 망막혈관증식성 종양 3예를 통해 임상적 특징 및 치료, 예후에 대해 알아보고자 한다.
증례요약: 안저검사상 주변부 망막에 융기된 종양이 관찰되었던 3명, 3안을 대상으로 하였다. 평균연령은 44.7세였고, 남자가 2명, 여자 가 1명이었다. 형광안저검사(FAG)와 인도사이아닌그린혈관조영검사(ICGA)를 통해 진단하였으며 1안에서 안구초음파검사, 2안에서는 안구자기공명촬영을 시행하였다. 경과관찰 중 1안에서 황반부종으로 테논낭하 트리암시놀론아세토나이드 주입술을 시행하였고, 1안에 서는 종양 주위의 삼출물 증가로 냉동치료를 시행하여 합병증을 조절할 수 있었다.
결론: 망막혈관증식성 종양의 정확한 진단을 위해 질환에 대해 의심을 갖고 주변부 안저를 철저히 관찰하고 FAG 및 ICGA, 안구초음파 검사를 통해 다른 망막종양과 감별하여 불필요한 치료를 피하는 것이 좋겠다. 또한 경과관찰 중 다양한 합병증이 발행할 수 있어 이에 따른 적절한 치료법을 선택하는 것이 중요하다.
<대한안과학회지 2013;54(1):170-175>
■ 접 수 일: 2012년 3월 30일 ■ 심사통과일: 2012년 8월 12일
■ 게재허가일: 2012년 12월 2일
■ 책 임 저 자: 장 우 혁
대구광역시 남구 현충로 170 영남대학교병원 안과
Tel: 053-620-3443, Fax: 053-620-5936 E-mail: changwh@ynu.ac.kr
* 이 논문의 요지는 2011년 대한안과학회 제105회 학술대회에서 포스터로 발표되었음.
망막혈관증식성 종양은 최근에 새롭게 분류된 질환으로 매우 드물고, 동반된 질환이 없는 건강한 사람에게서 주로 발견되는 질환으로 알려졌다.1,2붉은색을 띄는 노란색 또는 주황색을 띄는 노란색의 종양성 병변으로 주로 주변부 망 막에서 발견된다. 망막혈관증식성 종양이라고 명명되기 이 전에는 Shields et al1에 의해 후천망막혈관종(presumed acquired retinal hemangioma)으로 불리며 맥락막흑색종 또는 선천모세혈관종과는 다른 질환으로 분류되었으며 von Hippel-Lindau 증후군과의 연관성은 없는 것으로 알려졌 다. 이 후 Shields et al3은 이러한 혈관성 병변이 조직병리 학적으로 모세혈관종과 다르다는 것을 알게 되었고 이를 망막혈관증식성 종양이라고 명명하였다.
Shields et al3은 이러한 종양을 특발성 또는 이차성으로 분류하였으며 이차성의 경우 발생 원인에 따라 선천성, 염 증성, 혈관성, 외상성, 영양성 그리고 퇴행성으로 분류하였 다. 이 중 특발성이 가장 많다고 보고하였다. 이 종양은 특 징적으로 주변부 망막에서 관찰되며, 조직병리학적으로 양
성 종양의 특징을 나타내지만 시력저하를 유발하는 합병증 을 동반할 수 있으며 심한 경우 안구적출에 이르는 경우도 보고되고 있다.1,3-6
망막혈관증식성 종양의 치료는 경과관찰에서부터 수술 적 절제까지 다양하지만 어떠한 방법이 최선인가에 대해서 는 일치된 의견이 없어 종양의 크기, 동반되는 합병증에 따 라 경험적인 치료에 의존하고 있는 실정이다.
이러한 망막혈관증식성 종양은 해외에서 여러 차례 보고 되었으나 우리나라 환자들을 대상으로 한 임상적 특징과 적절한 치료법에 대한 보고는 없는 상황이다. 이에 저자들 은 최근 1년간 발견된 망막혈관증식성 종양 3예에 대한 경 과 관찰을 통해 임상적 특징 및 치료, 예후에 대해 보고하 고자 한다.
증례보고
증례 1
39세 남자가 2개월 전부터 시작된 좌안의 비문증을 주소 로 내원하였다. 과거력상 특이 사항은 없었으며 안질환의 과거력도 없었다. 안과적 검사상 최대교정시력은 양안 각각 1.0 이였으며 전안부의 특이소견은 관찰되지 않았다. 좌안 의 앞유리체에 2+ 정도의 염증성 변화가 관찰되었다. 안저 검사상 황반부의 병적 변화는 관찰되지 않았으나 하이측에 연노란색으로 보이는 균질성의 종양성 병변이 관찰되었다.
A
B
D
C
E
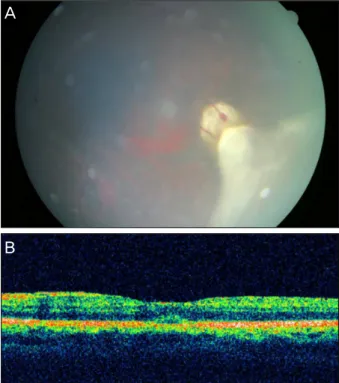
Figure 1. (A) Homogenous creamy yellow colored fine mass
in inferotemporal peripheral retina. (B) and (D) FAG finding.Dilated and obscured vessels with hyperfluorescence on mass lesion. There were neither abnormal feeding vessels nor di- lated vessels in surrounding mass lesion. (C) and (E) ICGA finding. Blocked fluorescence associated with tumor showing no abnormal choroidal vessels.
Figure 2. Optical coherence tomographic finding. Maular ede-
ma with thin epiretinal membrane.A
B
Figure 3. (A) W ell visualized retinal mass through relative
clear vitreous cavity 1 month after subtenon’s triamcinolone aceteonide injection. (B) Optical coherence tomographic finding. Absorbed macular edema one month after subtenon’s triamcinolone aceteonide injection.형광안저검사(FAG) 및 인도사이아닌그린혈관조영검사(ICGA) 를 시행하였으며 FAG에서 병변 부위 망막 혈관의 비정상적 확장 및 폐쇄 소견이 관찰되나, ICGA에선 맥락막혈관의 병 적인 변화는 없었다(Fig. 1). 또 병변 주위의 비정상적 혈관 확장이나 꼬임 소견도 관찰되지 않았다. 안구초음파 검사에 서 병변 내 균일한 반사도 증가를 보였으나 맥락막 침범 소 견은 없었다. 황반부로의 침범소견이나 시력 저하가 없어 경과 관찰하기로 하였다. 이후 3개월의 경과 관찰 기간 동 안 종양의 변화가 관찰되지 않았으며 시력 저하도 없었다.
진단 후 4개월이 지나서 좌안의 변형시가 발생하였으며 최 대교정시력이 0.8 로 저하되고 앞유리체의 염증성 반응이 증가하는 소견이 관찰되었다. 안저검사상 유리체 혼탁과 함
께 종양의 크기가 증가하면서 황반부종이 발생하기 시작하 였다. 그 후 1개월의 경과관찰기간 동안 황반부종이 점차 악화되었으며(Fig. 2) 다시 1개월이 지난 후 종양 위로 출 혈 소견과 함께 황반부종이 심해져 최대교정시력이 0.6으 로 저하되었다. 황반부종의 감소와 종양 위 출혈 감소를 목 적으로 유리체내 베바시주맙(Avastin®, Roche, Basel, Swiss, 0.05 ml)주입술을 시행하였다. 유리체내 베바시주 맙 주입술을 시행하고 1개월이 지난 후 경과 관찰에서 종양 위 출혈 소견은 사라졌으나 황반부종은 감소되지 않았다.
베바시주맙 주사 2개월째, 황반부종의 재발, 앞유리체의 염 증세포 증가와 유리체 혼탁의 악화로 교정시력은 0.2 로 저 하되어 테논낭하 트리암시놀론아세토나이드(Triam®, 신풍
A
B C
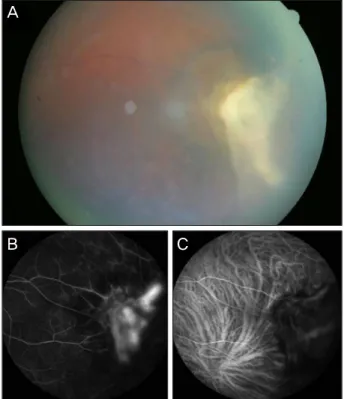
Figure 4. (A) Homogenous creamy yellow colored mass in in-
ferotemporal peripheral retina. (B) FAG finding. Dilated and obscure vessels with hyperfluorescence on mass lesion. There were neither abnormal feeding vessels nor dilated vessels in surrounding mass lesion. (C) ICGA finding. Blocked fluo- rescence associated with tumor showing no abnormal choroi-dal vessels.
Figure 5. Stable mass lesion without any complication for 6
months.제약, 0.1 ml) 주입술을 시행하였다. 주사 1주일 후 전방과 앞유리체의 염증성 반응이 감소하며 유리체 혼탁도 줄어드 는 소견을 보였으며 주사 1개월 후 유리체 혼탁은 사라지고 전방과 앞유리체의 염증은 1+ 정도로 관찰되었다. 최대 교정시력은 0.7로 회복되었으며 황반부종도 소실되었다 (Fig. 3).주사 후 3개월 동안 여전히 안정적인 경과를 유지 하고 있으며 최대교정시력도 0.9로 향상되었다.
증례 2
50세 남자가 6개월 전부터 시작된 좌안의 비문증을 주소 로 내원하였다. 과거력상 1년 전부터 고혈압 치료를 받고 있었으며, 안질환의 과거력은 없었다. 안과적 검사상 최대 교정시력은 1.0 이였으며 전안부의 특이소견은 관찰되지 않았다. 좌안의 앞유리체에 2+ 정도의 염증성 변화가 관찰 되었으며 안저검사상 황반부의 이상은 관찰되지 않았으나 유리체 혼탁과 하이측에 연노란색을 띄며 망막하출혈을 동 반하는 종양성 병변이 관찰되었다. 형광안저검사(FAG) 및 인도사이아닌그린혈관조영검사(ICGA)에서 병변 위의 망
막 혈관에서 비정상적 확장 및 폐쇄 소견이 관찰되나, 맥락 막혈관의 병적인 변화는 없었다(Fig. 4). 하지만 병변 주위 의 혈관 이상은 관찰되지 않았다. 안구자기공명촬영에서도 맥락막흑색종 같은 다른 질병의 증거는 관찰되지 않았다.
황반부로의 침범소견이나 시력 저하가 없어 경과 관찰하기 로 하였다. 6개월간의 경과 관찰 기간 동안 병변의 크기 증 가나 시력 저하를 초래하는 합병증이 발생하지 않았으며 지속적 경과 관찰 중이다(Fig. 5).
증례 3
45세 여자가 1개월 전부터 시작된 좌안의 비문증을 주소 로 내원하였다. 과거력상 특이 사항은 없었으며 같은 증상 으로 타 병원에서 레이저 치료를 받은 과거력이 있었다. 안 과적 검사상 최대교정시력은 1.0 이였으며 전안부에서 특 이소견은 관찰되지 않았다. 좌안 안저검사상 황반부의 이상 소견은 관찰되지 않았으나 하비측에 두꺼운 삼출과 혈관 확장을 동반하는 연노란색으로 보이는 종양성 병변과 주위 에 이전에 시행한 레이저 반흔이 관찰되었다. 형광안저검사 (FAG) 및 인도사이아닌그린혈관조영검사(ICGA)를 시행 하였으며 FAG에서 병변 부위 망막 혈관의 비정상적 확장 및 폐쇄 소견이 관찰되나, 종양성 병변 주위의 혈관의 확장 이나 굵은 영양혈관 등은 관찰되지 않았다. ICGA에선 맥락 막혈관의 병적인 변화는 없었다(Fig. 6). 병변 부위 망막 혈 관의 확장 소견과 함께 이로부터의 장액성 누출과 삼출물 이 관찰되어 유리체내 베바시주맙(Avastin®, 0.05 cc) 주 입술을 시행하였으며 주사 1개월 후 병변 부위 확장된 혈관 의 수축과 함께 망막하액의 감소 소견이 관찰되었다. 이후 2개월간의 경과 관찰 동안 병변의 크기 증가나 시력 저하를 초래하는 합병증이 발생하지 않았다. 3개월이 지난 후 환자 분의 증상은 없었으나 다시 병변 주위의 삼출물이 후극부
A
B
D
C
E
Figure 6. (A) Homogenous creamy yellow colored fine mass
with surrounding exudates and photocoagulation scar in in- feronasal peripheral retina. (B) and (C) Normal macular appearance. (D) FAG finding. Dilated and obscured vessels with hyperfluorescence on mass lesion and visible photo- coagulation scar. There were neither abnormal feeding vessels nor dilated vessels in surrounding mass lesion. (E) ICGA finding. Blocked fluorescence associated with subretinal exu- dates and photocoagulation scar showing no abnormal choroi- dal vessels.A
B
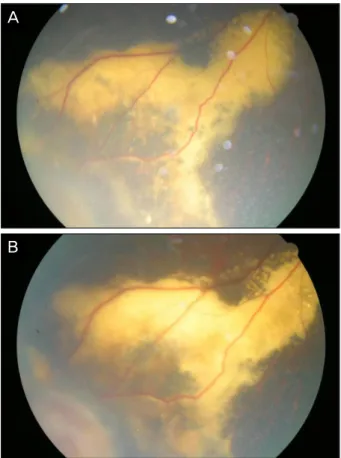
Figure 7. (A) Increased thick exudates toward optic disc but no
evidence of macular involvement. (B) One month after cry- otherapy, slightly decreased density of exudates toward optic disc.쪽으로 증가하는 소견이 관찰되어 유리체내 베바시주맙 (Avastin®, 0.05 cc) 주입술을 다시 시행하였다. 하지만 유리체내 베바시주맙 주입술 이후에도 지속적으로 병변 주위의 삼출물이 증가하여 병변 부위의 냉동치료를 결정 하였다. 냉동치료 후 2달간의 경과 관찰 기간 동안 병변 주위의 삼출물은 조금씩 흡수되는 양상을 보여주며 더 이상 삼출물의 증가 없이 안정적인 병변을 보여주고있 다(Fig. 7).
고 찰
망막혈관증식성 종양은 발병원인이 알려지지 않은 양성 종양으로 병리조직학적으로 반응성 혈관교질성 증식 소견 을 보인다.3-5고령의 환자에서 편측의 단일성 종양으로 발 견되는 경우가 많으며 특별한 가족력이나 과거력이 없는 경우가 많고 전신적 검사상에서도 특이소견이 관찰되지 않 는 것으로 알려졌다.2
Shields et al3은 망막혈관증식성 종양을 특발성과 이차 성으로 구분하였으며 특발성의 경우 작고 거상연 주위에 위치한 단일성 종양의 형태로 발견되며 하이측에 위치하는 경우가 많다고 보고하였다. 특발성 종양의 경우 망막삼출, 망막하액, 유리체출혈, 망막전막, 낭포성황반부종 등을 동 반하여 시력 저하에 영향을 줄 수 있다고 하였다. 안저검사 상 종양 주변의 혈관의 비정상적인 확장이나 꼬임이 관찰 되지 않으며 이는 von Hippel-Lindau 증후군에서 동반되 는 망막모세혈관종과는 다른 특징으로 알려졌다.
이차성 종양의 경우 대부분 망막색소변성증, 중간포도막 염, 미숙아망막증, 망막박리수술 후, 코우츠병 등과 연관이
있는 것으로 알려졌는데 이는 기존의 망막 질환으로 인한 이차적 망막색소상피와 혈관의 증식이 원인으로 여겨지고 있다. 대부분의 이차성 종양은 작고 증상이 없어 특별한 치 료 없이 경과 관찰만으로 충분한 것으로 보고되고 있다.
저자들의 증례에서 망막혈관증식성 종양은 임상적 소견, 안질환의 과거력, 형광안저검사(FAG), 인도사이아닌그린 혈 관조영검사(ICGA), 안구초음파, 안구자기공명촬영 등에 의 하여 진단되었으며 특별한 가족력이나 von Hippel-Lindau 증후군에 이환된 경우는 없었다.
증례 1에서 비문증을 제외한 다른 증상은 없었으나 경과 관찰 중 시력저하와 함께 변형시가 동반되는 망막전막과 황반부종을 관찰할 수 있었으며 종양 위 출혈 소견이 관찰 되었다. 황반부종을 감소시키고 시력 향상을 위하여 유리체 내 베바시주맙 주입술을 시행하였으나 호전을 보이지 않았 으며 앞유리체와 전방의 염증소견의 증가하고 유리체 혼탁 의 심해져 최대교정시력의 지속적 저하가 동반되었다. 염증 의 감소를 위해 시행한 테논낭하 트리암시놀론아세토나이 드 주입술 후 앞유리체와 전방의 염증은 조절되었으며 유 리체 혼탁이 감소하여 최대교정시력이 회복되었다. 증례 2 에서는 황반부를 침범하는 합병증을 동반하지 않고 종양이 안정적인 상태로 유지되어 별 다른 치료 없이 경과 관찰만 시행하고 있다. 증례 3에서 초기에는 유리체내 베바시주맙 주입술을 시행하여 병변 위 혈관의 확장을 조절할 수 있었 다. 경과관찰 중 종양 주위의 삼출물이 증가가 후극부 쪽으 로 진행되어 유리체내 베바시주맙 주입술을 추가로 시행하 였으나 호전을 보이지 않고 지속적 삼출물 증가가 관찰되 어 종양 부위의 냉동치료를 시행하였으며 이후 삼출물이 감소하고 안정적인 경과를 유지하고 있다. 임상양상을 토대 로 증례 2와 3의 경우 특발성 망막혈관증식성 종양으로 분 류하였다. 하지만 증례 1의 경우 비록 포도막염의 과거력은 없지만 망막혈관증식성 종양 진단 이후 임상양상이 전형적 인 중간포도막염의 경과를 보였고 테논낭하 트리암시놀론 아세토나이드 주사에 반응을 보인 점을 고려하여 중간포도 막염에 의한 이차성 종양으로 분류하였다.
저자들의 증례에서는 한 증례에서 망막전막을 동반하는 황반부종으로 인한 시력저하를, 한 증례에서는 안정적인 경 과, 나머지 한 증례에서는 종양 주위의 삼출물이 증가하는 합병증을 보여주었다. 하지만 황반삼출, 망막하액, 망막앞 섬유화, 유리체출혈, 삼출망막박리와 같은 합병증 그리고 신생혈관 형성으로 인해 안통을 유발하며 시력 소실을 유 발할 수 있는 이차성 녹내장 등의 합병증은 관찰되지 않았 다.
망막혈관증식성 종양의 치료는 정기적 경과 관찰만으로 충분한 경우가 많으며 합병증을 유발하는 경우 치료가 필
요하다. 대부분의 경우 결막을 경유한 냉동치료로 효과를 볼 수 있으며3 종양의 크기가 큰 경우 루테늄 106 또는 방 사성요오드근접치료를 시행하는 것이 도움이 될 수 있다.7,8 삼출이 동반되는 경우 광역학치료를 통해 병변을 안정화시 킬 수 있다고 알려졌다.9,10 수술적 치료로 유리체절제술을 통한 종양의 절제로 종양의 재발이나 합병증 발생을 막을 수 있다는 보고도 있으며11 유리체강내 베바시주맙 주입술 을 시행하는 것이 황반부종을 감소시킬 수 있는 것으로 알 려졌으나 장기적 치료 성적에 대해서는 알려져 있지 않다.12 망막전막을 동반한 황반부종이 시력 저하를 유발하는 경우 유리체절제술을 통한 망막전막의 제거가 효과적일 수도 있 다. 저자들의 증례 1에서 시행했던 테논낭하 트리암시놀론 아세토나이드 주입술도 치료법의 하나로 생각해 볼 수 있 는데 이는 망막혈관증식성 종양이 안내 염증을 동반하며 유리체 혼탁과 더불어 황반부종을 일으킬 수 있기 때문이 다. 테논낭하 트리암시놀론아세토나이드 주입술이 당뇨황 반부종이나 망막혈관폐쇄로 인한 이차적 황반부종을 감소 시키는 것처럼 안내 염증 반응을 억제하고 염증 전구물질 을 조절해 혈관내피세포인자의 유도를 감소시키며 혈관망 막경계를 안정화시켜13-15 망막혈관증식성종양에서 유발된 황반부종와 유리체 혼탁을 감소시킨다고 생각할 수 있다.
이처럼 여러 가지 치료 방법이 알려졌으나 아직 어떠한 방 법이 최선인가에 대한 일치된 의견이 없어 경험적인 치료 에 의존하고 있기 때문에 각각의 증례에 맞는 치료법을 선 택해야 한다.
결론적으로 망막혈관증식성 종양의 정확한 진단을 위해 서는 이 질환에 대해 의심을 갖고 주변부 안저를 철저히 관 찰하는 것이 중요하며, FAG 및 ICGA, 안구초음파검사 등 의 특징적 소견을 통해 다른 망막혈관종양과 감별 진단하 는 것이 필요하다. 또한 안구자기공명촬영을 통해 맥락막흑 색종이나 전신적 종양의 이차적 전이가 아님을 확인하는 것 또한 중요하다. 종양을 진단한 후에는 정기적 경과 관찰 을 통해 시력 상실을 유발할 수 있는 황반삼출, 망막하액, 망막앞 섬유화, 유리체출혈, 삼출망막박리, 이차성 녹내장 등의 발생을 미리 확인하고 각각의 증례에 맞는 치료를 선 택하는 것이 필요하다. 또한 망막혈관증식성 종양이 다른 혈관성 또는 종양성 질환과는 다른 질환의 경과를 보이며 치료법도 다양하다는 것을 인지할 필요가 있겠다.
참고문헌
1) Shields JA, Decker WL, Sanborn GE, et al. Presumed acquired ret- inal hemangiomas. Ophthalmology 1983;90:1292-300.
2) Jain K, Berger AR, Yucil YH, McGowan HD. Vasoproliferative tu- mours of the retina. Eye (Lond) 2003;17:364-8.
=ABSTRACT=
Three Cases of Vasoproliferative Tumor of the Retina
Dong Hyoun Noh, MD, Min Sagong, MD, PhD, Woo Hyok Chang, MD, PhD
Department of Ophthalmology, Yeungnam University College of Medicine, Daegu, Koera
Purpose: Vasoproliferative tumor of the retina (VPTR) is a histologically benign lesion that can lead to visual loss due to as- sociated complications. Herein, the authors report the clinical presentation, treatment, and prognosis of 3 VPTR cases.
Case summary: Three eyes of 3 patients with VPTR were enrolled in the present study. The patients’ fundoscopic feature showed characteristic elevated lesions of the peripheral retina without previous history of ocular disease. The patients in- cluded 2 males and 1 female, with an average age of 44.7 years. Fluorescein angiography (FAG) and indocyanine green angiography (ICGA) were helpful in establishing the diagnosis of VPTR. Additionally, 1 patient underwent ultrasonography and 2 patients underwent magnetic resonance imaging (MRI). During the follow-up period, subtenon triamcinolone aceto- nide injection was performed for 1 patient with macular edema, and cryotherapy was performed for 1 patient with in- creased peripheral exudation.
Conclusions: For an adequate diagnosis of VPTR, careful examination of the peripheral retina is important. In addition, FAG/ICGA and ultrasonography can be helpful in VPTR diagnosis. Furthermore, proper treatment according to each sub- set of complication during the follow-up period is recommended.
J Korean Ophthalmol Soc 2013;54(1):170-175
Key Words: Cryotherapy, Retina, Triamcinolone acetonide, Vasoproliferative tumors
Address reprint requests to Woo Hyok Chang, MD, PhD
Department of Ophthalmology, Yeungnam University Medical Center
#170 Hyeonchung-ro, Nam-gu, Daegu 705-703, Korea
Tel: 82-53-620-3443, Fax: 82-53-626-5936, E-mail: changwh@ynu.ac.kr 3) Shields CL, Shields JA, Barrett J, De Potter P. Vasoproliferative tu-
mors of the ocular fundus. Classification and clinical manifes- tations in 103 patients. Arch Ophthalmol 1995;113:615-23.
4) Smeets MH, Mooy CM, Baarsma GS, et al. Histopathology of a vasoproliferative tumor of the ocular fundus. Retina 1998;18:
470-2.
5) Heimann H, Bornfeld N, Vij O, et al. Vasoproliferative tumours of the retina. Br J Ophthalmol 2000;84:1162-9.
6) Irvine F, O'Donnell N, Kemp E, Lee WR. Retinal vasoproliferative tumors: surgical management and histological findings. Arch Ophthalmol 2000;118:563-9.
7) Anastassiou G, Bornfeld N, Schueler AO, et al. Ruthenium-106 plaque brachytherapy for symptomatic vasoproliferative tumours of the retina. Br J Ophthalmol 2006;90:447-50.
8) Cohen VM, Shields CL, Demirci H, Shields JA. Iodine I 125 pla- que radiotherapy for vasoproliferative tumors of the retina in 30 eyes. Arch Ophthalmol 2008;126:1245-51.
9) Saldanha MJ, Edrich C. Treatment of vasoproliferative tumors with photodynamic therapy. Ophthalmic Surg Lasers Imaging
2008;39:143-5.
10) Chan RP, Lai TY. Photodynamic therapy with verteporfin for vaso- proliferative tumour of the retina. Acta Ophthalmol 2010;88:711-2.
11) Yeh S, Wilson DJ. Pars plana vitrectomy and endoresection of a retinal vasoproliferative tumor. Arch Ophthalmol 2010;128:1196-9.
12) Kenawy N, Groenwald C, Damato B. Treatment of a vaso- proliferative tumour with intravitreal bevacizumab (Avastin). Eye (Lond) 2007;21:893-4.
13) McAllister IL, Vijayasekaran S, Chen SD, Yu DY. Effect of tri- amcinolone acetonide on vascular endothelial growth factor and occludin levels in branch retinal vein occlusion. Am J Ophthalmol 2009;147:838-46, 846.e1-2.
14) Hayashi K, Hayashi H. Intravitreal versus retrobulbar injections of triamcinolone for macular edema associated with branch retinal vein occlusion. Am J Ophthalmol 2005;139:972-82.
15) Byun YS, Park YH. Complications and safety profile of posterior subtenon injection of triamcinolone acetonide. J Ocul Pharmacol Ther 2009;25:159-62.