pISSN: 0378-6471 eISSN: 2092-9374 DOI : 10.3341/jkos.2011.52.2.197
= 증례보고 =
파스칼 레이저를 이용한 국소 및 격자 레이저 광응고술의 치료 효과
박재관⋅정우진 동아대학교 의과대학 안과학교실
목적: 당뇨황반부종에서 PASCALⓇ 레이저를 이용한 국소 및 격자 레이저 광응고술의 치료 효과를 알아보고자 하였다.
대상과 방법: 당뇨황반부종으로 진단된 환자들을 세군으로 나누어, 유리체강내 베바시주맙 주입술을 시행한 군 31명(31안) (1군), PASCALⓇ 레이저 광응고술을 시행한 군 17명(20안) (2군), 아르곤(Argon) 레이저 광응고술을 시행한 군 24명(24안) (3군)으로 정하고 치료 후의 시력과 황반부 두께의 변화를 분석하였다.
결과: 치료 후 시력변화에서 1군 중 16안(51.6%), 2군 중 13안(65.0%), 3군 중 10안(41.6%)에서 시력 상승을 보였으나 모두 통계적으로 유의하지 않았다. 치료 후 황반부 두께의 변화에서 1군 중 24안(77.4%), 2군 중 13안(65.0%), 3군 중 18안(75%)에서 황반두께의 감소를 보였으나, 치료 후 1개월의 결과만 통계학적으로 유의하였다(p<0.05).
결론: 당뇨황반부종에서, PASCALⓇ 레이저 광응고술은 유리체강내 베바시주맙 주입술 및 아르곤 레이저 광응고술에 근접할 만한 치료 효과를 가질 것으로 생각된다.
<대한안과학회지 2011;52(2):197-202>
■ 접 수 일: 2010년 7월 5일 ■ 심사통과일: 2010년 9월 24일
■ 게재허가일: 2010년 11월 29일
■ 책 임 저 자: 정 우 진
부산시 서구 동대신동 3-1 동아대학교병원 안과
Tel: 051-240-5227, Fax: 051-254-1987 E-mail: [email protected]
* 본 논문의 요지는 2009년 대한안과학회 제102회 학술대회에서 포스터로 발표되었음.
* 이 논문은 동아대학교 학술 연구비 지원에 의하여 연구되었음.
황반부종은 당뇨망막병증 환자에서 시력저하를 가져오 는 가장 흔한 원인으로, 대부분의 경우 내측혈액망막장벽이 소실되어 망막모세혈관의 투과성이 증가하게 되고 체액과 혈장성분이 누출되어 황반에 고임으로 인하여 발생되게 된 다.1 이러한 당뇨황반부종의 치료는 지금까지 약물요법, 고압 산소요법 등 여러가지 방법이 시도되었으나 좋은 결과를 얻지 못하였고, 조기 당뇨망막병증 치료연구팀(Early Treatment Diabebetic Retinopathy Study: ETDRS)에서 레이저 광응 고술의 효과를 보고한 이후 레이저 광응고술이 당뇨황반부 종의 치료에 이용되고 있다.2
이러한 레이저 광응고술 중 국소 및 격자 레이저 광응고 술은 당뇨황반부종 환자에 있어서 실명을 감소시키고, 시력 의 향상을 가져올 수 있으며, 지속적인 황반부 부종의 빈도 를 줄이면서도 단지 일부분만의 시야장애를 일으킨다고 하 였다.3또한 최근 안과 영역에서 유리체강내 베바시주맙 주
입술의 연령관련 황반변성과 증식당뇨망막병증에서 안구내 신생혈관의 억제 효과에 관한 많은 연구들이 보고되고 있 다.4-7
한편, 광응고술에 이용되는 레이저 중 비교적 최근에 나 온 PASCALⓇ레이저(Optimedia, Santa Clara, CA, USA)는 2005년에 소개된 새로운 레이저 치료방식으로, 반자동이며 망막에 한번의 빠른 선정된 순서(rapid predetermined se- quence)로 많은 레이저 광응고반(laser burns)을 만들어 낼 수 있다. 기존의 레이저 기기보다 조사 시간이 더 짧으 며 망막내막의 손상, 망막내경계막의 주름, 브루크막의 파 열 등의 부작용이 적은 것으로 보고된다.8,9 Cho et al10은 당뇨망막병증으로 범망막광응고술이 필요한 25명 29안을 대상으로 PASCALⓇ레이저를 이용하여 범망막광응고술을 시행한 결과 시력에 큰 영향을 주지 않으면서 특별한 단기 합병증이 없이 비교적 안전하고 효과적인 치료방법으로 보 고하였다.
또한 Sanghvi et al9은 황반부종의 치료에 PASCALⓇ레 이저를 이용한 국소 및 격자 레이저를 시도해서 75안의 pilot study를 한 결과 33안 중 29안에서 성공적인 결과를 보였고 부작용 또한 없었던 것으로 보고하였다.이에 저자 들은 당뇨황반부종 환자를 대상으로 PASCALⓇ 레이저를 이용한 국소 및 격자 레이저 광응고술을 시행하고 그 치료 효과에 대해 알아보고자 하였다.
Table 1. Characteristics of patients before treatments
Number of eyes 75
Gender
Male (eyes) 42
Female (eyes) 33
Age (yr, mean ± SD) 60.15 ± 8.73
Visual acuity (logMAR, mean ± SD) 0.72 ± 0.25 Macular thickness (µm, mean ± SD)) 362.04 ± 105.33
'A' advances to 'B'
A pattern B pattern
Figure 1. When the ‘A’ format of a grid pattern is selected it
will advance to the ‘B’ format automatically after firing. If a user start with the ‘B’ format, it will not advance to ‘A’ after firing.대상과 방법
2008년 6월에서 2010년 8월까지 본원에서 당뇨황반부 종으로 진단받고 6개월 이상 추적관찰이 가능하였던 환자 72명(75안) (남자 39명(42안), 여자 33명(33안))을 대상 으로 무작위로 3군으로 나누어, 유리체강 내로 베바시주맙 (AvastinⓇ, 1.25 mg/0.05 ml)을 주입한 군(1군) 31명(31 안), PASCALⓇ레이저를 이용하여 국소 및 격자 레이저 광 응고술을 시행한 군(2군) 17명(20안), Argon 국소 및 격 자 레이저 광응고술을 시행한 군(3군) 24명(24안)으로 정 하고, 치료 후 1개월, 3개월, 6개월의 시력과 황반부 두께의 변화를 분석하였다(Table 1).
유의한 황반부종(clinically significant macular edema, CSME)은 조기치료 당뇨망막병증연구(Early Treatment Diabetic Retinopathy Study, ETDRS)에서 제시한 다음과 같은 경우, 즉 두꺼워진 망막이 황반중심에서 반지름 500 μm의 원 안에 있거나 걸쳐 있을 때, 경성삼출물이 반지름 500 μm의 원 안에 있거나 걸쳐 있으면서 그와 인접한 망막 이 두꺼워져 있을 때, 1유두넓이 이상 크기의 두꺼워진 망 막이 있으면서 그 일부가 황반중심에서 반지름 1유두지름 (1500 μm)의 원 안에 있을 때로 정의하였다.2
모든 환자에서 연령, 당뇨병의 유병기간 등을 조사하였 으며 시술 전에 최대교정시력, 세극등 현미경검사, 안저검 사, 형광안저혈관조영술, OCT를 시행하였다.
당뇨 외에 망막혈관폐쇄, 고혈압망막증, 유리체염, 연령 관련황반변성 등 황반부종의 원인이 될 수 있는 질환이 동 반된 경우에는 연구 대상에서 제외되었으며, 시술 전 3개월 이내 또는 경과관찰 기간 동안에 동측 안에 한번 이상 수술 이나 유리체강내 트리암시놀론 주입술, 국소 또는 격자 레 이저 광응고술을 받은 대상 역시 연구에서 제외되었다.
레이저 광응고술을 시행한 환자들은 안과 외래에서 국소 점안마취(Proparacaine hydrochloride 0.5%) 후 Mainster 렌즈를 통해 PASCALⓇ 레이저와 Argon green 레이저를 각각 사용하여 국소 및 전체 격자 광응고하였다.
먼저, PASCALⓇ 레이저는 국소 광응고시 광속 직경은 100 μm, 에너지는 200 mW, 광속시간은 0.05초로 형광안
저혈관조영술상 유출이 의심되는 망막부위에 레이저를 조 사하였고, 전체 격자 광응고시에는 에너지 200 mW, 광속 시간 0.01초로 동심원에 지름이 200 μm인 56개의 점으로 구성된 패턴을 이용하여 ‘A’ 포맷의 격자 패턴이 선택되어 발사된 후에 자동으로 ‘B’ 포맷으로 진행되는 방식으로 레 이저를 조사하였다.
Argon green 레이저를 이용하여 국소 광응고시 광속 직 경은 100 μm, 에너지 200 mW, 광속시간은 0.1초로 시행 하였으며 형광안저혈관조영술상에서 확산형의 유출을 보 이는 경우에는 유출부위에서 유출의 시작점으로 생각되는 지점, 즉 최초의 과형광을 나타내는 부위에 레이저를 조사 하였고, 전체 격자 광응고시 광속 직경 200 μm, 에너지는 100~200 mW, 광속시간 0.05~0.1초로 레이저를 조사하 였다(Fig. 1).
시력측정은 각각의 치료 직전에 측정하여 이 시력을 기 준 시력으로 하였으며 치료 1달, 3달 그리고 6달 후에 다시 시력을 측정하였다. 시력은 logMAR scale을 이용하여 정량 적으로 비교 분석하였다. 황반부 두께는 OCT (STRATUS OCT model 3000, Carl Zeiss Meditec Inc. Jean, Germany) 를 이용하여 황반을 관통하는 6개의 방사상의 스캔으로 황 반두께를 측정하는 OCT retinal mapping program (ver.
4.0.2)을 이용하여 치료 직전과 치료 후 1개월, 3개월, 6개 월에 측정하였다. 이는 1인의 검사자에 의해 얻어진 황반부 단면 사진을 1인의 연구자가 분석하였다. 통계학적 분석은 Paired t-test, Wilcoxon signed rank test (SPSS v12.0) 를 이용하였고 p<0.05를 통계학적으로 유의하다고 판정하 였다.
결 과
1군 31명(31안), 2군이 17명(20안), 3군이 24명(24안) 이었으며, 남녀비는 1군에서 24:7, 2군에서 12:8, 3군에서 6:18이었고, 평균 연령은 각각 60.13 ± 7.29세, 58.11 ± 8.98세, 61.42 ± 9.61세로 평균 연령은 세 군 간에 차이는
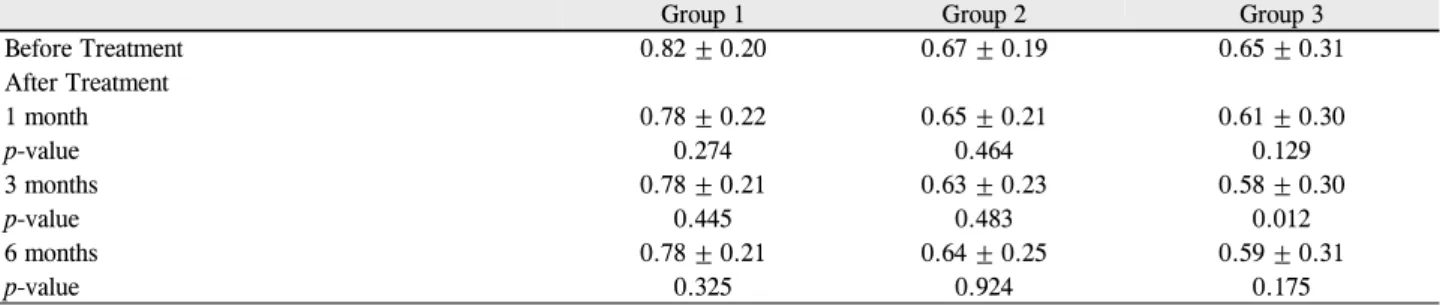
Figure 2. Visual acuity (logMAR).
Table 2. Visual acuity (logMAR)
Group 1 Group 2 Group 3
Before Treatment 0.82 ± 0.20 0.67 ± 0.19 0.65 ± 0.31
After Treatment
1 month 0.78 ± 0.22 0.65 ± 0.21 0.61 ± 0.30
p-value 0.274 0.464 0.129
3 months 0.78 ± 0.21 0.63 ± 0.23 0.58 ± 0.30
p-value 0.445 0.483 0.012
6 months 0.78 ± 0.21 0.64 ± 0.25 0.59 ± 0.31
p-value 0.325 0.924 0.175
Table 3. Macular thickness (µm)
Group 1 Group 2 Group 3
Before treatment 394.26 ± 325.58 354.75 ± 116.82 342.58 ± 93.26
After treatment
1 month 325.58 ± 121.74 281.40 ± 66.04 286.29 ± 104.49
p-value 0.002 0.001 0.006
3 months 355.50 ± 127.77 309.47 ± 71.56 302.93 ± 110.44
p-value 0.077 0.112 0.075
6 months 324.94 ± 86.90 320.75 ± 73.12 337.85 ± 86.90
p-value 0.003 0.313 0.221
Figure 3. Macular thickness (μm).
없었다.
시력은 1군에서 치료 전 평균 0.82 ± 0.20 (logMAR)에 서 치료 1달 후 0.78 ± 0.22 (logMAR), 치료 3달 후 0.78
± 0.21 (logMAR), 치료 6달 후 0.78 ± 0.21 (logMAR), 2 군에서 치료 전 평균 0.67 ± 0.19 (logMAR)에서 치료 1달 후 0.65 ± 0.21 (logMAR), 치료 3달 후 0.63 ± 0.23 (logMAR), 치료 6달 후 0.64 ± 0.25 (logMAR), 3군에서 치료 전 0.65
± 0.31 (logMAR)에서 치료 1달 후 0.61 ± 0.30 (logMAR), 치료 3달 후 0.58 ± 0.30 (logMAR), 치료 6달 후 0.59 ± 0.31 (logMAR)이었다. 치료 전과 비교하여 치료 6개월째 에 1군 중 16안(51.6%), 2군 중 13안(65.0%), 그리고 3군 중 10안(41.6%)에서 시력 상승을 보였으나 세 군 모두 통 계적으로 유의하지는 않았다(3군에서 치료 3달 후 결과는
통계적으로 유의하였음, p<0.05) (Table 2) (Fig. 2).
황반부 두께는 1군에서 치료 전 평균 394.26 ± 325.58 μm 에서 치료 1달 후 325.58 ± 121.74 μm, 치료 3달 후 355.50 ± 127.77 μm, 치료 6달 후 324.94 ± 86.90 μm, 2 군에서 치료 전 평균 354.75 ± 116.82 μm에서 치료 1달 후 281.40 ± 66.04 μm, 치료 3달 후 309.47 ± 71.56 μm, 치료 6달 후 320.75 ± 73.12 μm, 3군에서 치료 전 평균 342.58 ± 93.26 μm에서 치료 1달 후 286.29 ± 104.49 μm, 치료 3달 후 302.93 ± 110.44 μm, 치료 6달 후 337.85 ± 86.90 μm로 나타났다. 치료 전과 비교하여 치료 6개월째 에 1군 중 24안(77.4%), 2군 중 13안(65.0%), 3군 중 18 안(75%)에서 황반두께의 감소를 보였고, 1, 2, 3군 모두에 서 치료 후 1개월째 결과만 통계적으로 유의하였다(p<0.05)
(Table 3) (Fig. 3).
그밖에 치료 후 안내염, 망막박리, 새로운 홍채 신생혈관 이 생긴 경우 및 약물로 조절되지 않는 고안압 등의 다른 합병증은 관찰되지 않았다.
고 찰
최근 당뇨병 환자의 평균 연령이 증가함에 따라 당뇨망 막병증 환자도 늘어가고 있다. 당뇨황반부종은 이러한 당뇨 망막병증 환자에서 시력저하의 주요한 요인으로 모든 당뇨 망막병증 환자의 약 10%에서 발생하며 이중 40%는 황반 중심을 침범한다.11 병리생리학적인 기전으로는 망막허혈 에 의해 프로스타글란딘의 분비가 증가하고 혈관내피세포 성장인자나 섬유아세포성장인자와 같은 성장인자들이 상향 조절되어 혈관의 투과성 증가로 인해 황반부종이 발생하며, 또한 정상적인 혈액망막장벽이 손상되어 이에 따른 혈관투 과성 증대로 인해 황반부종이 발생하는 것으로 알려져 있 다. 그밖에 망막색소상피의 이상, 유리체 견인 등도 당뇨황 반부종의 발생에 관여할 것으로 생각한다.1,12
당뇨황반부종의 치료로써 당대사의 조절, 혈압 안정, 혈 청 지방 수치를 낮추는 등의 전신적인 치료와 레이저 광응 고술, 유리체 절제술이 알려져 있으나 레이저 광응고술이 주된 치료법이 되고 있으며 당뇨황반부종을 가진 안에서 레이저 광응고술을 실시함으로써 시력상실의 위험성을 감 소시킬 수 있다는 많은 보고가 있었다.3,13-15그 중 국소 레 이저 광응고술의 경우에는 안저검사에서 파악된 두꺼워진 망막에 대해, 형광안저혈관조영에서 파악된 치료가능한 병 변을 표적으로 레이저 조사를 하는데, 주로 형광안저혈관조 영상 명확한 과형광이나 누출점이 관찰되며 이것이 황반부 종의 원인으로 생각되는 경우에 치료효과가 있다. 국소 황 반부종에서는 국소누출을 일으키는 미세혈관류를 레이저로 직접 응고함으로써 누출점을 폐쇄하여 황반부종이 해소될 수 있으며 광범위 황반부종에서 누출 부위는 투과성이 비 정상적으로 항진된 미세혈관류, 망막내 모세혈관 병변, 확 장된 망막모세혈관 등에서 전반적인 누출이 일어나기 때문 에 부종이 있는 망막에 격자 레이저 광응고술을 시행해야 한다. 격자 레이저 광응고술이 광범위 황반부종의 해소에 작용하는 기전에 대해 몇 가지 가설들이 제기되고 있는데 대표적인 것으로 첫째, 병든 망막 색소 세포 상피들을 레이 저 광응고술로 제거하면 보다 젊고 건강한 세포로 대치되 며, 둘째, 산소 소비가 높은 광수용체를 파괴하여 내망막층 의 산소 농도를 증가시켜 망막의 혈류량을 감소시키면 망 막 혈관으로부터 삼출물이나 액체의 누출을 감소시킬 수 있으며, 셋째, 병변이 있는 망막 위의 망막 혈관에 크립톤
(Krypton) 레이저 조사 시 혈관 내피 세포의 증식을 유도 한다는 실험적 증거들이 있다.3,12,16
한 연구에 의하면 치료를 받지 않은 환자에서 5년 동안 5%의 시력개선을 보인데 반해 레이저 광응고술을 받은 군 에서는 5년간 17%의 시력개선을 보였다고 하였다.3 또한 레이저 광응고술의 효과에 대한 연구에서 Shahidi et al17이 Retinal thickness analyzer (RTA)를 사용하여 치료 4개월 후 50%에서 망막두께의 감소를 보였고 36%에서는 변화가 없었다고 보고하였다.
베바시주맙(AvastinⓇ; Genetech, San Francisco, CA, USA) 은 재조합 인간단일클론성 항체로 모든 혈관내피세포성장 인자의 아이소형에 결합하여 혈관내피세포성장인자를 억제 함으로써18당뇨황반부종에 적용할 수 있는데, 환자를 대상 으로 한 연구에서 황반부종을 동반한 당뇨망막병증에서 초 자체내 혈관내피세포성장인자가 증가되어 있음이 Brooks et al19에 의해 보고된 바 있다.
PASCALⓇ 레이저에 의한 레이저 광응고반은 10~100 msec에 이르기까지 비교적 짧은 조사시간으로 조직학적 손상 정도가 주로 손상이 망막외층과 망막색소상피에 국한 되어 망막내층과 브루크막 및 맥락막의 손상을 줄일 수 있 다.8 PASCALⓇ레이저를 이용하여 황반부 격자 레이저 광 응고술 시 망막중심오목을 둘러싸기 위한 4개의 동심원에 지름이 100 μm 또는 200 μm인 56개의 점으로 구성된 패 턴을 구성하여, 내부 원 지름은 2000 μm보다 커서 중심와 무혈관 부위(foveal avascular zone)를 침범하지 않으며 고 정 광원(fixation light)을 사용하여 환자에게 고정대상을 제공한다. 또한 ‘A’ 포맷의 격자 패턴이 선택된 경우 발사된 후에 자동으로 ‘B’ 포맷으로 진행하여, 치료하고자 하는 부 위가 빠짐이 없게끔 격자 패턴 밀도를 보다 정확하게 제어 할 수 있는 장점이 있다(Fig. 1).
본 연구는 당뇨황반부종 환자를 대상으로 기존의 아르곤 레이저나 유리체강내 베바시주맙 주입술에 비해 PASCALⓇ 레이저를 이용하여 치료를 했을 경우 그 임상적 효과에 대 해 알아 본 것으로 황반부종과 시력과의 관계를 알아보기 위해 시력을 logMAR scale로 환산하여 알아보았으나 유의 한 상관관계를 보이지 않았다. 또한 당뇨황반부종 환자를 대상으로 PASCALⓇ레이저를 이용한 국소 및 격자레이저 광응고술을 시행한 결과, 유리체강내 베바시주맙 주입술 및 아르곤 국소 및 격자레이저 광응고술에 근접할 만한 황반 두께감소 효과를 가진 것으로 나타났다. 이러한 PASCALⓇ 레이저는 그 특성상 망막내 손상이 기타 레이저에 비해 제 한적이고, 비교적 안전하며 또한 빠르고 정확하게 치료할 수 있는 장점이 있어 앞으로 그 유용성이 클 것으로 생각 한다.
본 연구 결과는 환자 수가 작고 경과관찰 기간이 짧아, 향후 더 많은 환자를 대상으로 장기간의 연구를 통해 확인 이 필요할 것으로 생각하고 기존의 여러가지 황반부종 치 료 형태에 따른 병합요법에 관한 연구도 필요할 것으로 생 각한다.
참고문헌
1) Ryan SJ. Nonproliferative diabetic retinopathy. In: Chew EY, Ferris FL III, eds. Retina, 4th ed. New York: Mosby, Elsevier Inc., 2006; v. 2. chap. 67.
2) Early Treatment Diabetic Retinopathy Study Research Group.
Treatment techniques and clinical guidelines for photocoagulation of diabetic macular edema: Early Treatment Diabetic Retinopathy Study report no 2. Ophthalmology 1987;94:761-74.
3) Early Treatment Diabetic Retinopathy Study Research Group.
ETDRS report no. 1: photocoagulation for diabetic macular edema.
Arch Ophthalmol 1985;103:1796-806.
4) Rosenfeld PJ, Moshfeghi AA, Puliafito CA. Optical coherence to- mography findings after an intravitreal injection of bevacizumab (Avastin) for neovascular age-related macular degeneration.
Ophthalmic Surg Lasers Imaging 2005;36:331-5.
5) Avery RL, Pieramici DJ, Rabena MD, et al. Intravitreal bevacizumab (Avastin) for neovascular age-related macular degeneration.
Ophthalmology 2006;113:363-72.
6) Avery RL. Regression of retinal and iris neovascularization after intravitreal bevacizumab (Avastin) treatment. Retina 2006;26:352-4.
7) Spaide RF, Fisher YL. Intravitreal bevacizumab (Avastin) treat- ment of proliferative diabetic retinopathy complicated by vitreous hemorrhage. Retina 2006;26:275-8.
8) Blumenkranz MS, Yellachich D, Andersen DE, et al. Semiautomated patterned scanning laser for retinal photocoagulation. Retina 2006;
26:370-6.
9) Sanghvi C, McLauchlan R, Delgado C, et al. Initial experience with the Pascal photocoagulator: a pilot study of 75 procedures. Br J Ophthalmol 2008;92:1061-4.
10) Cho BJ, Kim TW, Woo SJ, et al. Short-term clinical outcome of patterned scanning laser photocoagulation with short exposure time in diabetic retinopathy. J Korean Ophthalmol Soc 2009;50:
376-82.
11) Kim HK, Han YB. Laser photocoagulation in diabetic macular edema, J Korean Ophthalmol Soc 1992;33:759-63.
12) Bresnick GH. Diabetic maculopathy; a critical review highlighting diffuse macular edema. Ophthalmology 1983;90:1301-17.
13) Olk RJ. Modified grid argon (blue-green) laser photocoagulation for diffuse diabetic macular edema. Ophthalmology 1986;93:938-50.
14) Townsend C, Bailey J, Kohner E. Xenon arc photocoagulation for the treatment of diabetic maculopathy. Interim report of a multi- centre controlled clinical study. Br J Ophthalmol 1980;64:385-91.
15) Blankenship GW. Diabetic macular edema and argon laser photo- coagulation: a prospective randomized study. Ophthalmology 1979;86:69-78.
16) Bresnick GH. Nonproliferative diabetic retinopathy. In: Ryan SJ, ed. Retina, 2nd ed. St. Louis: CV Mosby, 1994;1277-318.
17) Shahidi M, Ogura Y, Blair NP, Zeimer R. Retinal thickness change after focal laser treatment of diabetic macular edema. Br J Ophthalmol 1994;78:827-30.
18) Hurwitz H, Fehrenbacher L, Novotny W, et al. Bevacizumab plus irinotecan, fluorouracil, and leucovorin for metastatic colorectal cancer. N Engl J Med 2004;350:2335-42.
19) Brooks HL, Caballero S, Newell CK, et al. Vitreous levels of vas- cular endothelial growth factor and stromal-derived factor 1 in pa- tients with diabetic retinopathy and cystoid macular edema before and after intraocular injection of triamcinolone. Arch Ophthalmol 2004;122:1801-7.
=ABSTRACT=
Effect of Focal and Grid Pattern PASCAL Photocoagulation Treatment in Diabetic Macular Edema
Jae Kwan Park, MD, Woo Jin Jeung, MD
Department of Ophthalmology, Dong-A University College of Medicine, Busan, Korea
Purpose: To investigate the effect of focal and grid pattern PASCAL photocoagulation treatment in diabetic macular ede- ma patients.
Methods: A total of 72 patients (75 eyes) who were diagnosed as diabetic macular edema were retrospectively analyzed.
The patients were divided into 3 groups as follows: group 1 (31 patients, 31 eyes) received an intravitreal bevacizumab in- jection, group 2 (17 patients, 20 eyes) underwent focal and grid pattern PASCAL photocoagulation treatment, and group 3 (24 patients, 24 eyes) underwent focal and grid pattern argon photocoagulation treatment. Macular thickness and visual acuity (logMAR) of 75 eyes were compared among groups before and after treatments.
Results: Visual acuity improved in 13 eyes (65.0%) in group 1, 16 eyes (51.6%) in group 2, and in 10 eyes (41.6%) in group 3; however, there was no statistical significance. Macular thickness reduction occurred in 24 eyes (77.4%) in group 1 and 13 eyes (65.0%) in group 2 which were statistically significant decreases at only 1 month after treatment (p < 0.05).
Conclusions: Focal and grid pattern PASCAL photocoagulation is a good therapeutic option for diabetic macular edema.
Focal and grid pattern PASCAL photocoagulation is as effective as intravitreal bevacizumab injection or focal and grid pat- tern argon photocoagulation treatment.
J Korean Ophthalmol Soc 2011;52(2):197-202
Key Words: Diabetic macular edema, Pascal photocoagulation
Address reprint requests to Woo Jin Jeung, MD
Department of Ophthalmology, Dong-A University Hospital
#3-1 Dongdaesin-dong, Seo-gu, Busan 602-715, Korea
Tel: 82-51-240-5227, Fax: 82-51-254-1987, E-mail: [email protected]