접수일:2010년 3월 31일, 수정일:2010년 4월 11일, 승인일:2010년 4월 16일
책임저자:차 영 주 156-755 서울시 동작구 흑석동 224-1 중앙대학교병원 진단검사의학과
TEL: 02) 6299-2720, FAX: 02) 6298-8630, E-mail: chayoung@cau.ac.kr 이 논문은 2007년도 중앙대학교 학술연구비 지원에 의한 것임.
혈액감염과 관련된 바이러스 검사의 외부정도관리 실태:
혈액전파감염을 방지하기 위한 헌혈혈액 선별검사의 품질보증프로그램 필요성
차 영 주
중앙대학교 의과대학 진단검사의학교실
= Abstract =
The Results of External Proficiency Tests to Prevent Transfusion-transmitted Virus Infection: There Is a Need for a Quality Assurance Program for
Donor Screening Tests to Prevent Blood-borne Virus Infections
Young Joo Cha
Department of Laboraotry Medicine, Chung-Ang University College of Medicine, Seoul, Korea
Background: We analyzed the results of external proficiency tests for HBsAg, anti-HCV and anti-HIV, and these tests are currently used for blood donor screening in Korea.
Methods: The external proficiency testing (EPT) data was retrospectively collected from 2001 to 2009 from the Korean Association of Quality Assurance for Clinical Laboratories, and this association includes those institutes that have blood centers. The pooled patient sera or converted sera from the plasma were used for EPT. The year 2004 data includes the Recombinant HBsAg variant (Gly/Arg 145).
Results: A total 806 institutes participated in this evaluation. The average discordant rate for HBsAg, anti-HCV and anti-HIV in the blood centers was 0.2%, 0.6% and 1.0%, respectively for the years 2001∼2009. For the HBsAg test, the discordant rate was less than 0.5% in 2009, yet there was a much higher rate (1.6∼22.2%) in 2004 when using the recombinant HBsAg variant.
Conclusion: HBV variants or low positive antigen or antibody titers were problematic in the current clinical laboratory, and so a systematic quality assurance program should be conducted with using control materials.
(Korean J Blood Transfus 2010;21:25-35)
Key words: Donor screening tests, Quality assurance program, Standard serum panel, Low titer panels, Genotype, HBV variants
서 론
현대의학에서 혈액 및 혈액제제를 사용하는 치 료는 꼭 필요한 의료행위로 자리잡았지만 수혈로 인하여 간염, 에이즈, 말라리아 등 여러 가지 혈 액전파감염이 발생할 가능성이 있다. 국내에서는 연간 약 350만 단위의 혈액제제가 환자에게 수혈 되고 있으며, 혈액전파감염을 방지하기 위하여 혈액관리법 시행규칙1) 제 8조에 의해 에이엘티 검사, 비(B)형간염검사, 씨(C)형간염검사, 매독검 사, 후천성면역결핍증검사 등을 실시하도록 정하 고 있지만, 검사를 실시한다고 하더라도 감염 후 항원이나 항체가 생기기 이전인 잠복기의 혈액을 검출할 수 없는 한계가 있다. 잠복기 감염의 검출 가능성을 높이기 위하여 2005년 2월부터 모든 헌 혈혈액에 대하여 C형간염(hepatitis C virus, HCV) 과 후천성면역결핍증(human immunodeficiency virus, HIV) 바이러스에 대한 핵산증폭검사가 실시되고 있어 수혈에 의한 C형간염과 후천성면역결핍증 이 전파될 가능성은 매우 감소되었지만, B형간염 바이러스(hepatitis B virus, HBV)의 경우에는 아 직까지 핵산증폭검사를 도입하고 있지 않아 감염 위험이 여전히 존재한다. 특히 HBV의 경우에는 잠복기가 길고, 혈액 중에 매우 낮은 농도의 바이 러스만이 존재하는 만성감염이 있으며, 기존의 항체와 반응하지 않는 변이가 유전자 및 조절요 소에서 다양하게 일어나고 있기 때문에 검출이 안 되는 경우가 있어 수혈로 인한 전파 위험이 높다.2) 국내에서 1999년 4월 1일∼2004년 4월 9일 사 이에 대한적십자사에서 출고된 혈액중 의심사례 에 대해서 전국적으로 조사한 결과 8명이 B형간 염에 감염된 것으로 확인되었으며, 감염은 되었 으나 명백한 인과관계가 입증되지 않은 경우가 9 명(B형간염 7명, C형간염 2명) 있었다.3) 2000년에 보고된 미국 American Association of Blood Banks
(AABB) 통계에 의하면 B형간염은 137,000 단위 당 한단위의 비율로 발생할 가능성이 있고, C형 간염은 1,000,000 단위, 에이즈는 1,900,000 단위 의 선별혈액이 수혈될 때마다 1회 발생하는 것으 로 보고되어 역시 수혈로 인한 감염 중 B형간염 의 발생이 가장 흔하게 발생함을 알 수 있다.
혈액전파감염을 방지하기 위하여서는 헌혈혈 액에 대하여 실시되고 있는 선별검사, 즉 B형간 염표면항원(hepatitis B surface antigen, HBsAg), C 형간염바이러스항체(anti-HCV) 및 후천성면역결 핍증바이러스항체(anti-HIV) 검사의 품질관리가 매우 중요하다. 혈액의 안전을 위하여 세계 각국 에서는 헌혈혈액 선별검사를 위한 별도의 품질보 증프로그램(quality assurance program)을 가지고 있지만, 우리나라에서는 별도의 헌혈혈액 선별검 사에 대한 품질보증프로그램은 없는 상황이고 사 단법인 대한임상검사정도관리협회에서 전국적 으로 연 2회 외부신빙도조사를 실시하여 바이러 스 검사결과의 정확도를 모니터링하고 있는 상황 이다.
따라서 본 연구에서는 현재 사단법인 대한임상 검사정도관리협회에서 실시하고 있는 바이러스 검사결과를 분석하여 우리나라 의료기관의 헌혈 혈액 선별검사 정확도 수준을 파악하고, 불일치 결과를 보고한 경우에 대해서는 그 원인을 분석 하여 이를 개선하며 현재 우리나라에 필요한 헌 혈혈액 선별검사의 품질보증 방안을 모색하고자 하였다.
대상 및 방법
1. 조사대상
사단법인 대한임상검사정도관리협회에서 면 역혈청분과에서 2001∼2009년까지 매년 2회씩
Table 1. Preparation of control materials used in external proficiency survey for donor screening tests
Control material Processing
Plasma sample 1. Prepare samples
2. After centrifugation (7,000 rpm, 30 minutes), remove precipitation and keep inactive for 3 hours at 56oC 3. Convert to serum by adding calcium chloride
4. Add 0.05% sodium azide
5. Do filtration once using each 0.8, 0.45, and 0.22 μm filters 6. After autoclaving vials and rubber stoppers, dry-heat sterilize
7. Dispense serum to each vial and put a rubber stopper under the clean bench 8. Seal the vials with aluminium cap
Pooled serum sample
1. Prepare samples
2. After centrifugation (7,000 rpm, 30 minutes), remove precipitation and keep inactive for 3 hours at 56oC 3. Convert to serum by adding calcium chloride
4. Add 0.05% sodium azide
5. After autoclaving vials and rubber stoppers, sterilize dry-heat
9. Dispense serum to each vial and put a rubber stopper under the clean bench 6. Seal the vials with aluminium cap
시행한 9년간의 외부신빙도조사 결과4-12) 및 보관 된 자료를 이용하여 바이러스 검사결과를 후향적 으로 분석하였다. 외부신빙도 조사는 2001년 1차 376기관, 2차 383기관, 2002년 1차 398기관, 2차 405기관, 2003년 1차 414기관, 2차 420기관, 2004 년 1차 435기관, 2차 447기관, 2005년 1차 465기 관, 2차 471기관, 2006년 1차 514기관, 2차 548기 관, 2007년 1차 615기관, 2차 637기관, 2008년 1차 691기관, 2차 706기관, 2009년 1차 777기관, 2차 806기관이 참여하였다. 바이러스 검사결과는 사 용하는 검사방법에 따라 그 예민도 및 특이도에 차이가 있으므로, 우선 외부신빙도조사에 참여하 는 전 기관의 검사방법의 추이를 조사하였고, 헌 혈혈액원이 개설되어 있어서 헌혈혈액 선별검사 를 실시하고 있는 기관의 검사방법을 조사하였 다.
2. 정도관리물질의 제조방법
사단법인 대한임상검사정도관리협회 면역혈
청분과에서 실시한 바이러스검사에 대한 외부신 빙도조사에 사용된 검체는 환자의 혼주혈청 및 대한적십자사 혈액수혈연구원에서 연구용으로 제공한 혈장으로서, 혼주혈청은 환자의 잔여 혈 청을 검사종목 별로 수집하여 저온냉동고(−70oC) 에 보관하였다가 필요에 따라 해동시켜 혼합하여 사용하였으며, 대한적십자사 혈액수혈연구원에 서 제공한 혈장은 calcium chloride를 첨가하여 혈 청으로 전환시켜 사용하였다. 각각의 검체 처리 방법은 Table 1과 같다. HBsAg의 경우에는 특별 히 변이형 검출을 위하여 HBsAg ‘a' 결정기 변이 중 가장 흔히 발생하는 변이인 Gly/Arg 145의 검 출을 조사하기 위하여 미국 애보트사(Abbott La- boratories, USA)에서 제공한 재조합 HBsAg 변이 (Gly/Arg 145)항원을 1회(2004년) 사용하였고, 저 농도 HBsAg, anti-HCV 및 anti-HIV 양성을 검출 하기 위하여 상품화된 관리물질인 ACCURUN 1R Multi-Marker Positive Control (Boston Biomedica Inc. USA)을 1회(2007년) 사용하였다.
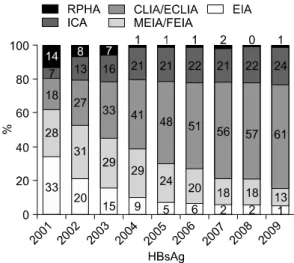
Fig. 1. Proportional changes of methods for mea- suring HBsAg.
3. 결과 분석
바이러스 검사결과 분석은 면역혈청분과에서 자체 제조한 정도관리물질의 경우에는 검체제조 과정에 문제가 있었던 1회를 제외(분석에서 제외 함)하고는 참여기관의 80% 이상이 보고한 결과 를 정답으로 판정하였고, 재조합항원과 상품화된 관리물질은 제조사에서 제시하는 결과를 정답으 로 판정하여 일치율을 분석하였는데, 정답과의 불일치율(이하 불일치율)은 gray zone이나 판정불 가(indeterminate) 결과는 양성(positive)으로 간주 하고 불일치한 기관수를 전체 참여기관수로 나눈 값으로 정의하였다. 바이러스 검사결과의 불일치 율은 외부신빙도조사에 참여하는 전 기관의 결과 를 검사방법 별로 분석하여 조사하였고, 헌혈혈 액원이 개설되어 있는 기관들의 불일치율을 조사 하여 비교하였다.
결 과
1. 외부신빙도조사에 참여하는 기관의 바이 러스 검사방법의 변화
HBsAg 검사방법의 경우 2001년에 효소면역검 사법(enzyme immunoassay, EIA)이 33%, 미세입자 효소면역검사법(microparticle EIA, MEIA)에 28%
로 HBsAg을 측정하는 방법으로 대세를 이루고 있었는데, 이 두 방법은 점차로 감소하여 2009년 에는 각각 1%와 13%의 검사실에서만 사용하는 방법이 되었고, 그 대신 2001년에는 18%를 차지 하고 있던 화학발광면역검사법(chemiluminescence immunoassay, CLIA)과 효소화학발광면역검사법 (enzyme chemiluminescence immunoassay, ECLIA) 이 2009년에는 61%를 차지하는 방법으로 증가하 였다(Fig. 1). 한편 장비를 사용하지 않고 HBsAg
을 측정하는 방법으로 전통적으로 사용하던 역수 동혈구응집법(reverse passive hemagglutination, RPHA) 은 2001년 14%에서 2009년 1%로 거의 사용하지 않는 검사법이 되었고, 그 대신 간이검사법인 면 역크로마토그래피법(immunochromatography assay, ICA)이 2001년 7%에서 2009년 24%로 크게 증가 하였다(Fig. 1).
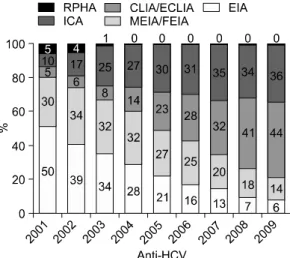
Anti-HCV와 anti-HIV를 측정하는 방법도 HBsAg 을 측정하는 방법의 변화와 유사한 변화를 보이 고 있는데, anti-HCV 측정의 경우 2001년 EIA법 이 50%, MEIA법이 30%로 약 80%를 차지하던 것 이 2009년에는 각각 6%와 14%로 감소되었고, CLIA와 ECLIA법이 2001년 5%에서 2009년 44%
로 크게 증가하였으며, 간이검사법인 ICA법이 2001 년 10%에서 2009년 36%로 증가하였다(Fig. 2).
Anti-HIV의 경우에는 2001년 EIA법이 47%, MEIA 법이 31%로 약 80%를 차지하던 것이 2009년에는 각각 5%와 16%로 감소되었고, CLIA와 ECLIA법 이 2001년 6%에서 2009년 52%로 크게 증가하였
Fig. 2. Proportional changes of methods for mea- suring anti-HCV.
Fig. 3. Proportional changes of methods for mea- suring anti-HIV.
Fig. 4. No. of blood centers using each method for donor screening tests in 2009.
으며, 간이검사법인 ICA법이 2001년 4%에서 2009 년 26%로 증가하였다(Fig. 3).
우리나라 헌혈혈액원 90기관에서 2009년 헌혈 혈액 선별검사를 위하여 사용하고 있는 검사방법 은 HBsAg의 경우 CLIA/ECLIA법이 83기관(92%),
MEIA/FEIA법이 7기관(8%)이었고, anti-HCV의 경우 CLIA/ECLIA법이 75기관(83%), MEIA/FEIA 법이 7기관(8%), EIA법이 8기관(9%)이었으며, anti- HIV의 경우 CLIA/ECLIA법이 73기관(81%), MEIA/
FEIA법이 9기관(10%), EIA법이 7기관(8%)이었다 (Fig. 4).
2. 검사방법 별 HBsAg 외부신빙도조사 검 사결과 불일치율
전국적인 규모로 실시되고 있는 HBsAg 외부신 빙도조사 결과 HBsAg 검사방법 별 불일치율을 2001년부터 분석한 결과 점차로 향상되어 2009년 RPHA법을 제외한 모든 검사방법에서 0.5% 이하 로 매우 좋은 일치율을 보였다. 하지만 2004년 외 부신빙도조사에서는 검체 중에 재조합 HBsAg 변 이(Gly/Arg 145)항원 검체가 포함되어 있어서 EIA법에서는 22.2%, CLIA/ECLIA법에서는 16.8%
로 불일치율이 매우 높았고, MEIA/FEIA법에서는 1.6%로 상대적으로 불일치율이 낮았다. 그리고 2007년 외부신빙도조사에서는 저농도 HBsAg 양
Table 2. Discordant rate (%) of external proficiency testing results according to methods measuring HBsAg
Methods Year
2001 2002 2003 2004* 2005 2006 2007† 2008 2009
EIA 0.8 2.0 1.3 22.2 0.0 0.0 15.0 0.0 0.0
MEIA/FEIA 1.0 0.0 0.8 1.6 0.8 0.4 2.7 0.4 0.4
CLIA/ECLIA 0.0 2.2 0.0 16.8 0.9 1.5 2.8 0.4 0.4
ICA 9.1 18.9 1.6 9.7 2.7 4.5 32.8 0.2 0.4
RPHA 23.1 3.8 0.0 10.0 0.0 5.0 24.1 0.0 10.0
Total 2.9 3.8 0.7 11.5 1.2 1.9 7.4 0.3 0.4
*Recombinant HBsAg mutant sample was included in 2004, †Commercial control material with low concentration of HBsAg, ACCURUN 1R Multi-Marker Positive Control (Boston Biomedica Inc. USA) was included in 2007.
Table 3. Discordant rate (%) of external proficiency testing results according to methods measuring anti-HCV
Methods Year
2001 2002 2003 2004 2005 2006 2007* 2008 2009
EIA 3.4 2.1 1.8 4.0 3.0 1.3 15.4 1.0 0.6
MEIA 0.0 0.0 0.5 0.7 0.9 0.4 3.8 1.2 0.0
CLIA/ECLIA 0.0 0.0 0.0 0.0 0.6 1.4 0.9 0.2 0.5
ICA 50.0 22.5 15.6 50.5 27.4 8.3 26.8 5.4 5.9
Total 6.9 4.4 4.6 13.9 9.1 3.2 12.4 2.2 2.3
*Commercial control material, ACCURUN 1R Multi-Marker Positive Control (Boston Biomedica Inc. USA) was included in 2007.
성 검체인 상품화된 관리물질을 사용하였기 때문 에 다른 검사방법에 비하여 예민도가 떨어지는 ICA법과 RPHA법에서의 불일치율이 각각 32.8%, 24.1%로 높았고, EIA법에서도 15.0%의 불일치율 을 보였으며, MEIA/FEIA법과 CLIA/ECLIA법에 서도 각각 2.7%, 2.8%로 다른 검체에 비하여 높은 불일치율을 보였다(Table 2).
3. 검사방법 별 Anti-HCV 외부신빙도조사 검사결과 불일치율
전국적인 규모로 실시되고 있는 anti-HCV 외부 신빙도조사 결과 anti-HCV 검사방법 별 불일치율 을 2001년부터 분석한 결과 점차로 향상되어
2009년 ICA법을 제외한 모든 검사방법에서 0.6%
이하로 매우 좋은 일치율을 보였다. 하지만 2007 년 외부신빙도조사에서는 저농도 양성 검체인 상 품화된 관리물질을 사용한 결과 다른 검사방법에 비하여 예민도가 떨어지는 ICA법에서는 불일치 율이 26.8%로 높았고, EIA법에서도 15.4%의 불 일치율을 보였으며, MEIA법에서도 3.8%로 다른 검체에 비하여 높은 불일치율을 보였다. Anti- HCV의 경우 ICA법을 사용하는 비율이 다른 검 사보다 높아서 약 36%의 검사실이 사용(Fig. 2)하 고 있는데, ICA법의 불일치율은 2001년과 2004년 약 50%로 매우 높았는데, 점차로 향상되어 최근 에는 약 5∼6% 정도를 보였다(Table 3).
Table 4. Discordant rate (%) of external proficiency testing results according to methods measuring anti-HIV
Methods Year
2001 2002 2003 2004 2005 2006 2007* 2008 2009
EIA 30.7 8.2 0.4 2.0 0.0 0.8 14.2 1.2 1.5
MEIA/FEIA 3.3 0.0 2.3 2.1 1.4 0.4 1.3 0.0 0.5
CLIA/ECLIA 5.6 29.4 0.0 1.2 4.0 0.7 0.5 0.3 0.5
ICA 46.2 16.2 2.7 11.6 2.1 1.3 32.4 3.0 2.9
Total 20.3 7.9 1.6 4.3 2.0 0.8 10.3 1.0 1.2
*Commercial control material, ACCURUN 1R Multi-Marker Positive Control (Boston Biomedica Inc. USA) was included in 2007.
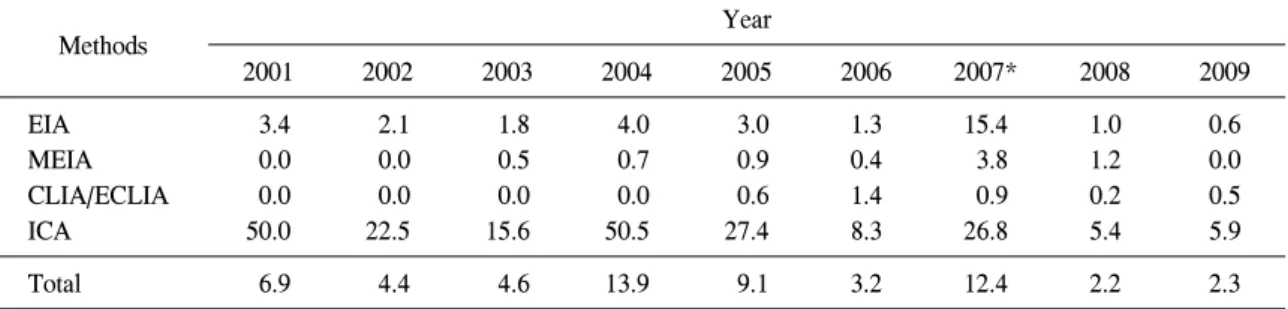
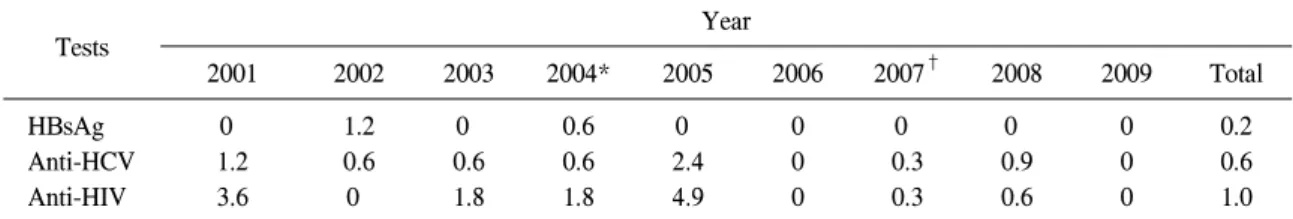
Table 5. Discordant rate (%) of external proficiency testing results for donor screening tests in blood centers
Tests Year
2001 2002 2003 2004* 2005 2006 2007† 2008 2009 Total
HBsAg 0 1.2 0 0.6 0 0 0 0 0 0.2
Anti-HCV 1.2 0.6 0.6 0.6 2.4 0 0.3 0.9 0 0.6
Anti-HIV 3.6 0 1.8 1.8 4.9 0 0.3 0.6 0 1.0
*Recombinant HBsAg mutant sample was included in 2004, †Commercial control material with low concentration of HBsAg, ACCURUN 1R Multi-Marker Positive Control (Boston Biomedica Inc. USA) was included in 2007.
4. 검사방법 별 Anti-HIV 외부신빙도조사 검사결과 불일치율
전국적인 규모로 실시되고 있는 anti-HIV 외부 신빙도조사 결과 2001년에 처음으로 anti-HIV 양 성검체가 외부신빙도조사에 도입됨에 따라 2001 년에는 EIA법의 불일치율이 30.7%, 2002년에는 CLIA/ECLIA법의 불일치율이 29.4%로 매우 높았 지만 점차 향상되어 2009년에는 EIA법, MEIA/
FEIA법, CLIA/ECLIA법의 불일치율이 각각 1.5%, 0.5%, 0.5%였다. Anti-HCV와 마찬가지로 2007년 외부신빙도조사에서는 저농도 양성 검체인 상품 화된 관리물질을 사용한 결과 다른 검사방법에 비하여 예민도가 떨어지는 ICA법에서는 불일치 율이 32.4%로 높았고, EIA법에서도 14.2%의 불 일치율을 보였다(Table 4).
5. 헌혈혈액원의 헌혈혈액 선별검사 외부신 빙도조사 검사결과 불일치율
우리나라 헌혈혈액원의 2001∼2009년 헌혈혈 액 선별검사 외부신빙도조사 검사결과 불일치율 을 조사한 결과 HBsAg의 경우에는 2002년과 2004년에 각각 1.2%, 0.6%의 불일치율을 보인 외 에는 모두 일치된 결과를 보였지만 anti-HCV의 경우에는 2006년과 2009년에만 일치된 결과를 보 였고, 다른 해에는 0.3∼2.4%의 불일치율을 보였 으며, anti-HIV의 경우에도 2002년, 2006년, 2009 년에만 일치된 결과를 보였고, 다른 해에는 0.3∼
4.9%의 불일치율을 보였으며, 2001∼2009년의 평 균 불일치율은 HBsAg, anti-HCV, anti-HIV 검사에 서 각각 0.2%, 0.6%, 1.0%였다(Table 5).
고 찰
헌혈혈액 선별검사로 시행되는 바이러스 검사 는 엄격한 정확도가 요구되는 검사로 위음성 결 과는 수혈감염으로 이어질 수 있는 위험성이 있 으며, 위양성 결과는 소중한 자원인 혈액의 불필 요한 폐기로 이어진다. 국내에서도 2003년 대한 적십자사가 실시한 역학조사에 의하면 초회 헌혈 혈액 선별검사 상 양성반응을 보였던 헌혈자가 이후 다시 실시한 검사결과가 음성이어서 출고된 혈액 2,550건에 대한 헌혈자 및 수혈자 추적조사 결과 B형 간염이 3건, C형 간염이 5건 감염되었 음이 확인된 바 있어13) 검사결과 위음성의 위험 성이 입증된 바 있다. 특히 HBV 변이형의 경우 일반적인 체외진단용의약품으로는 검출되지 않 을 가능성이 있는 바, 대한정도관리협회 면역혈 청분과위원회에서 2004년 HBV 변이형 검출을 위하여 재조합 HBsAg 변이(Gly/Arg 145)항원을 사용하여 외부신빙도조사를 실시한 결과 EIA법 과 CLIA/ECLIA법에서 각각 22.2%와 16.8%의 높 은 불일치율을 보여 HBV 변이형에 의한 위음성 가능성을 확인할 수 있었고, 실제로 2005년 2명 의 헌혈자에서 HBV 변이형으로 인하여 위음성 을 보여 환자에게 수혈된 바 있는데, 다행히 수혈 자가 anti-HBs 항체를 가지고 있어서 수혈감염은 일어나지 않았지만, 이와 같은 위험성은 늘 존재 한다고 생각된다.
또한 HBV 감염에서는 잠재HBV감염(occult HBV infection, OBI)14)이 있어서 이와 같은 경우 HBsAg 이 음성이기 때문에 검출되기 어렵지만 HBV DNA가 양성이므로 HBV핵산증폭검사를 실시하 지 않는 우리나라 현실에서는 수혈감염의 위험성 이 있다. 헌혈자에서 OBI의 빈도는 나라마다 차 이가 있어서 개별 헌혈혈액에 대한 NAT를 실시 하거나 6∼8개 혼주 NAT를 실시하는 유럽에서
는 7,500∼63,000 헌혈자 당 1명의 빈도로 발견되 고 있는 반면, 20개 혼주 NAT를 사용하고 있는 일본은 107,000 헌혈자 당 1명의 빈도로 보고되 고 있다. 우리나라에서의 OBI 빈도는 1,047명의 HBsAg 음성인 건강검진 환자 중 7명(0.7%)에서 발견됨이 보고15)된 바 있고, HBsAg이 음성인 12,435명의 헌혈자 중 2명(0.016%)에서 OBI가 발 견되었다.16)
따라서 HBsAg의 경우 매우 낮은 농도까지 예 민하게 측정하는 것이 필요한데, 대한정도관리협 회 면역혈청분과위원회에서 2007년 저농도 HBsAg 양성을 검출하기 위하여 상품화된 관리물질인 ACCURUN 1R Multi-Marker Positive Control (Boston Biomedica Inc. USA)을 사용하여 실시한 외부신 빙도조사 결과, EIA법에서 15.0%의 매우 높은 불 일치율을 보였고, MEIA/FEIA법과 CLIA/ECLIA 법에서도 각각 2.7%와 2.8%의 비교적 높은 불일 치율을 보여 낮은 농도의 HBsAg 검출이 취약함 을 알 수 있었다. ACCURUN 1R Multi-Marker Po- sitive Control을 사용한 anti-HCV와 anti-HIV 외부 신빙도조사에서도 EIA법의 경우 각각 15.4%, 14.2%
의 매우 높은 불일치율을 보여 HBsAg과 마찬가 지로 낮은 농도의 항체 검출에 문제가 있다고 생 각된다.
특히 헌혈혈액원을 운영하고 있는 기관의 바이 러스 표지자에 대한 외부신빙도조사 결과를 별도 로 분석한 결과 HBsAg은 과거에는 일부 불일치 가 있었지만 최근에는 모두 일치된 결과를 보였 지만, anti-HCV와 anti-HIV는 소수이기는 하지만 여전히 불일치된 결과가 나타나고 있어 더욱 주 의가 요구된다.
헌혈혈액 선별검사의 위양성 및 위음성 사례를 최소화하기 위해서는 우선 헌혈혈액 선별검사 체 외진단용의약품의 등록ㆍ허가 및 생산ㆍ유통 과 정의 품질관리가 요구되고, 검사실의 장비, 기구,
시설 및 검사자의 숙련도 등 사용 단계에서의 품 질관리가 필요하며, 검사결과의 정확도를 확인하 기 위한 체계적인 품질보증프로그램이 요구된다.
첫 번째 단계인 헌혈혈액 선별검사 체외진단용의 약품의 등록ㆍ허가 단계에서의 품질관리를 위하 여 미국이나 유럽의 경우 같은 바이러스 표지자 라 하더라도 헌혈혈액 선별검사로 사용하려면 임 상적 유효성을 검증한 후 별도의 허가를 받아야 하는데, 우리나라에서는 이와 같은 헌혈혈액 선 별검사 체외진단용의약품에 대한 별도의 허가 절 차가 없는 상황이다. 그리고 헌혈혈액 선별검사 체외진단용의약품의 생산ㆍ유통 과정의 품질관 리를 위하여서도 미국이나 유럽의 경우에는 제품 의 각 로트마다 검증하는 제도가 있는데, 우리나 라에는 이와 같은 로트검증도 없는 실정이다. 따 라서 헌혈혈액 선별검사 체외진단용의약품의 등 록ㆍ허가 및 생산, 유통 과정의 품질관리를 위한 제도 도입이 국가적으로 필요하다고 생각된다.
현재 국내에서는 헌혈혈액 선별검사를 수행하 면서 실시하여야 하는 사용단계의 품질관리로서 는 대한진단검사의학회에서 실시하는 ‘우수검사 실 인증’과 혈액관리법 시행령에 의하여 질병관 리본부 혈액안전감시팀에서 실시하고 있는 ‘혈 액관리업무 심사평가’가 있다.
마지막으로 헌혈혈액 선별검사의 검사결과 정 확도를 확인하기 위한 체계적인 품질보증프로그 램이 요구17)되는데, 현재 국내에서는 사단법인 대한임상검사정도관리협회에서 전 의료기관을 대 상으로 하는 외부신빙도조사 프로그램이 있지만 보다 정확한 품질관리가 요구되는 헌혈혈액원에 서의 선별검사를 위하여서는 다양한 검체 구성 및 상품화된 품질관리물질이 아닌 혈청으로부터 제조된 표준혈청패널이나 저역가패널 등을 이용 한 품질관리시스템이 요구된다. WHO에서는 가 능하면 자국민에 대한 선별검사에 활용할 국가표
준물질을 스스로 개발하여 품질평가에 활용하도 록 권고하고 있고, 영국이나 호주에서는 국가차 원의 생물의약품 국가표준물질을 확립하여 자국 내 검사실에서 사용하여 일관성 있게 품질관리를 시행할 수 있는 체계를 갖추고 있으며, 타국에서 요청할 경우에 이 품질관리물질을 판매하기도 한 다. 싱가폴에서는 호주의 국가표준검사실에서 제 조ㆍ공급하는 품질관리물질을 사용하여 외부 및 내부품질관리를 실시하고 있다. 국내에서도 체외 진단용의약품의 검증이나 헌혈혈액 선별검사에 필요한 안전하고 안정적인 국가표준품 및 품관리 물질의 필요성을 인식하고 식약청의 주도로 HBV 항원검사 표준품을 포함하여 바이러스검사에 대 한 표준품을 확립하거나 개발에 착수하고 있는 바, 이를 일회성으로 그치지 않고 체계적인 품질 보증프로그램과 연계하여 지속적으로 수행하는 것이 필요하다.
본 연구에서 나타난 바와 같이 헌혈혈액원의 선별검사 외부신빙도조사 결과에서 불일치 결과 가 지속되고 있고, 특히 HBV 변이형이나 저농도 항원/항체의 경우에는 검출율이 떨어지므로 다양 한 유전자형 및 변이형을 포함하는 신뢰도가 검 증된 품질관리물질과 상품화된 품질관리물질이 아닌 혈청으로부터 제조된 표준혈청패널이나 저 역가패널을 포함하는 품질관리물질을 사용하여 체계적인 품질보증프로그램을 운영하여야 할 것 이다.
요 약
배경: 헌혈혈액에 대하여 실시되고 있는 선별 검사, 즉 HBsAg, anti-HCV 및 anti-HIV 검사의 품 질관리 현황을 조사하고자 하였다.
방법: 사단법인 대한임상검사정도관리협회에 서 2001∼2009년까지 매년 2회씩 시행한 9년간의
외부신빙도조사 자료를 이용하였다. 환자의 혼주 혈청 및 대한적십자사에서 제공한 혈장을 혈청으 로 전환시켜 외부신빙도조사에 사용하였다. 2004 년에는 HBV 변이형 검출을 위하여 재조합 HBsAg 변이(Gly/Arg 145)항원을 이용하였다.
결과: 총 806기관이 이번 조사에 참여하였다.
우리나라 헌혈혈액원의 2001∼2009년의 HBsAg, anti-HCV 및 anti-HIV 외부신빙도조사 평균 불일 치율은 평균이 각각 0.2%, 0.6%, 1.0%였다. HBsAg 검사방법 별 불일치율은 2009년에는 0.5% 이하 로 좋은 일치율을 보였으나, 2004년 재조합 HBsAg 변이항원 검체가 포함된 경우에는 1.6∼22.2%의 높은 불일치율을 보였다.
결론: 현재 임상검사실에서는HBV 변이형이나 저농도 항원/항체의 항체 검출에 문제가 있다고 생각된다. 다양한 유전자형 및 변이형을 포함하 는 신뢰도가 검증된 품질관리물질과 상품화된 품 질관리물질이 아닌 혈청으로부터 제조된 표준혈 청패널이나 저역가패널을 포함하는 품질관리물 질을 사용하여 체계적인 품질보증프로그램을 운 영하는 것이 필요하다.
참고문헌
1. Korea Legislation Information Center. Enfor- cement Decree of the Blood Management Act.
http://www.law.go.kr/lsInfoP.do?lsiSeq=9144 0#0000 [Online] (last visited on 30 March 2010) 2. Cha YJ. Screening test for prevention of hepa- titis B due to transfusion. National Blood Sur- veillance Monthly Report 2007;1:2-5
3. Korea Center for Disease Control and Preven- tion, hemovigilance team. Comprehensive re- port on national surveillance of transfusion transmitted infection 2006. http://www.cdc.
go.kr/kcdchome/jsp/home/common/brd/C OMMBRD0200Detail.jsp?menuid=100039&boa
rdid=1002&pageNum=0&sub=0&boardseq=93 22 [Online] (last visited on 30 March 2010) 4. Cha YJ, Kum DG, Kim SW, Kim TY, Kim JR,
Kim HS, et al. Annual report on external quality assessment in immunoserology in Korea (2001). J Lab Med Qual Assur 2002;
24:27-38
5. Cha YJ, Kum DG, Kim SW, Kim TY, Kim JR, Kim HS, et al. Annual report on external quality assessment in immunoserology in Korea (2002). J Lab Med Qual Assur 2003;
25:51-71
6. Cha YJ, Kwon SY, Kum DG, Kim SW, Kim TY, Kim JR, et al. Annual report on external quality assessment in immunoserology in Korea (2003). J Lab Med Qual Assur 2004;
26:47-69
7. Cha YJ, Kwon SY, Kum DG, Kim SW, Kim TY, Kim JR, et al. Annual report on external quality assessment in immunoserology in Korea (2004). J Lab Med Qual Assur 2005;
27:37-57
8. Cha YJ, Kwon SY, Kim TY, Kim JR, Kim HS, Park MH, et al. Annual report on external quality assessment in immunoserology in Korea (2005). J Lab Med Qual Assur 2006;
28:41-61
9. Cha YJ, Kwon SY, Kim TY, Kim JR, Kim HS, Park MH, et al. Annual report on external quality assessment in immunoserology in Korea (2006). J Lab Med Qual Assur 2007;
29:45-64
10. Cha YJ, Kwon SY, Kim TY, Kim JR, Kim HS, Park MH, et al. Annual report on external quality assessment in immunoserology in Korea (2007). J Lab Med Qual Assur 2008;
30:49-74
11. Cha YJ, Kwon SY, Kim TY, Kim JR, Kim HS, Park MH, et al. Annual report on external quality assessment in immunoserology in
Korea (2008). J Lab Med Qual Assur 2009;
31:49-72
12. Cha YJ, Kwon SY, Kim TY, Kim JR, Kim HS, Park MH, et al. Annual report on external quality assessment in immunoserology in Korea (2009). J Lab Med Qual Assur 2010;32(In press)
13. Seo DH. Transfusion-transmitted diseases: cu- rrent state and recent countermeasures. J Korean Med Assoc 2006;49:410-5
14. Allain JP. Occult hepatitis B virus infection:
implications in transfusion. Vox Sang 2004;86:
83-91
15. Song EY, Yun YM, Park MH, Seo DH. Pre- valence of occult hepatitis B virus infection in a general adult population in Korea. Inter- virology 2009;52:57-62
16. Seo DH, Kim HS, Whang DH. Study on anti- HBc and HBV DNA positive rate among Korean Blood donors. Korean J Lab Med 2009 2009;
29:S346
17. Oh DJ, Cho YJ, Kwon SY, Cho NS, Kwon SW, Um TH, et al. A proposal for developing a national quality assurance program for donor blood assays. Korean J Blood Transfus 2008;19:
197-206