적복령 추출물이 파골세포의 분화와 골흡수 억제에 미치는 효과
원광대학교 의과대학 영상의학기반 폐 및 골질환 연구센터1, 원광대학교 의과대학 류마티스내과학교실2, 산본병원 마취통증의학교실3, 원광대학교 의과대학 해부학교실4, 원광대학교 의과대학 환경과학 연구소5,
골격계질환 연구소6, 원광대학교 의과대학 산부인과학교실7
김주영
1,6․김진숙
7․이승화
7․이명수
1,2,6․이창훈
1,2,6․문서영
3최민규
4,5․김정중
4,6․오재민
1,4,6․곽한복
1,4,6․조해중
7Inhibition of Osteoclast Differentiation and Bone Resorption by Poria cocos Wolf Extract
Ju-Young Kim
1,6, Jin Suk Kim
7, Seoung Hwa Lee
7, Myeung Su Lee
1,2,6, Chang Hoon Lee
1,2,6, Seo Young Moon
3, Min Kyu Choi
4,5, Jeong Joong Kim
4,6, Jae Min Oh
1,4,6, Han Bok Kwak
1,4,6, Hae Joong Cho
71Imaging Science based Lung and Bone Disease Research Center, College of Medicine, Wonkwang University,
2Department of Internal Medicine, Division of Rheumatology and Institute of Wonkwang Medical Science, College of Medicine, Wonkwang University, 3Division of Anesthesiology and Pain Medicine, Sanbon Medical Center,
4Department of Anatomy, College of Medicine, Wonkwang University,
5Institute for Environmental Science, College of Medicine, Wonkwang University, 6Institute for Skeletal Disease, College of Medicine, Wonkwang University, 7Department of Obstetrics and Gynecology, College of Medicine, Wonkwang University, Iksan, Korea
Objectives: Osteoclast differentiation and bone resorption are considered a potential therapeutic target to the treatment of erosive bone diseases, including osteoporosis and rheumatoid arthritis. Poria cocos Wolf (PCW), commonly used herbal medicine, has previously been reported to induce anti-inflammatory effect and anti-cancer effect, and to modulate immunologic responses. However, the effects of PCW on osteoclasts, and its detailed mechanisms are not proven. Therefore, we examined the inhibitory mechanism of PCW on osteoclast differentiation and bone resorption.
Materials and Methods: To analyze the effects of PCW on osteoclast differentiation, we examined osteoclast differentiation in bone marrow macrophages (BMMs) treated with or without of PCW by TRAP staining.
The expression of c-Fos, NFATc1, TRAP and OSCAR mRNA was determined by RT-PCR and the protein levels of c-Fos, NFATc1, p38, ERK, JNK, Akt and I
κ
B were assessed by western blot. Also, we evaluated the effect of PCW on bone resorption using hydroxyapatite plate.Results: PCW significantly inhibited RANKL-mediated osteoclast differentiation without any evidence of cytotoxicity. We founded that PCW strongly inhibited RANKL-induced osteoclast formation when added during the early stage of cultures, suggesting that PCW acts on osteoclast precursors to inhibit RANKL/RANK signaling. Among the RANK signaling pathways, PCW inhibited the phosphorylation of p38 and JNK, also inhibited RANKL-induced expression of c-Fos, NFATc1, TRAP and OSCAR. In addition, PCW suppressed the bone resorption of mature osteoclasts.
Conclusions: These findings suggest that PCW may be a potential novel drug for bone disorders by targeting the differentiation of osteoclasts as well as their functions.
Key Words: Bone resorption, Osteoclast differentiation, Poria cocos Wolf (PCW), RANKL/RANK signaling
Received: October 24, 2012 Revised: November 26, 2012 Accepted: December 20, 2012
Corresponding Author: Hae Joong Cho, Department of Obstetrics and Gynecology, College of Medicine, Wonkwang University, 460 Iksan-daero, Iksan 570-711, Korea
Tel: +82-63-859-1544, E-mail: chohj69@wku.ac.kr
* 이 논문은 2010년도 원광대학교 교비 지원에 의해 수행되었습니다.
골다공증(Osteoporosis)은 골밀도 감소에 의한 미 세구조의 변화와 골질(bone quality)의 저하로 인하여 골강도(bone strength)가 손상되어 가벼운 충격에도 골절이 쉽게 발생하는 질환이다.
1골다공증으로 인 한 고관절 및 척추골절은 현저히 나타나는 증상이 없을 수도 있지만 급성요통, 신경증상과 함께 직접 사망의 원인이 되기도 하며, 영구적인 장애가 동반 되고 많은 의료비가 소모되는 합병증이 흔히 발병되 고 있어 골다공증의 예방 및 치료는 중요하다고 할 수 있다.
2-4또한 골다공증은 연령증가에 비례하여 발병률이 상승되는 대표적인 질환으로, 인구의 고령 화가 진행될수록 이에 대한 관심이 증가되고 있는 추세이다.
5골조직은 고등 척추동물에서 지지역할을 하는 특 수하게 분화된 형태의 결합조직으로, 일생 동안 골 재형성(bone remodeling)이 일어나는 조직이다.
6,7골 재형성은 파골세포가 골에 붙어 산성화 및 단백질 분해작용에 의해 오래된 골을 제거하고 그 제거된 위치에 조골세포가 여러 종류의 단백질과 콜라겐으 로 이루어진 골기질을 분비하여 유골(osteoid)형성과 무기질 침착을 유도하여 새로운 골을 형성함으로 이 루어진다.
6,7골 재형성은 일정한 주기를 통해 일어나 며 국소적으로 좁은 부위에서 일어남으로써 골격계 의 구조가 유지되는데 이러한 골격계의 구조와 기능 은 전신적인 호르몬과 국소적 인자 사이의 복잡한 상호작용에 의해 조절된다.
6-8이러한 골조직의 대사 과정이 평형을 잃을 경우 여러 골질환이 발생될 수 있으며, 상대적으로 파골세포의 기능이 비정상적으 로 증가되면 골 흡수가 증가하여 골다공증이 야기된 다. 파골세포는 여러 단계를 거쳐 골을 흡수하는 파 골세포로 분화되는데, 단핵구/대식세포에서 발현하 는 receptor activator of NF-κB (RANK)에 RANK ligand (RNAKL)가 결합하면 TNF receptor-associated factor 6 (TRAF6)이 RANK의 세포질 부위와 결합하 고 다양한 신호전달 물질을 활성화시켜 파골세포의 분화에 중요한 전사인자 및 새로운 유전자 발현을 유도한다.
9,10특히, p-38, ERK, JNK와 같은 mitogen- activated protein kinases (MAPKs)와 전사인자 NF-κB 는 파골세포 분화에 중요한 전사인자 c-Fos와 nuclear factor activated T cells (NFAT)c1의 발현에 중
요하게 작용한다.
11,12NFATc1은 골세포 지표인 tartrate-resistant acid phosphatase (TRAP), cathepsin K, osteoclast-associated receptor (OSCAR) 등의 발현을 촉진하며,
13,14대식세포에 NFATc1을 과발현시키면 RANKL로 자극하지 않아도 파골세포로 분화된다고 보고되었다.
15이러한 연구결과에 의해 RANKL은 MAPKs, NF-κB, c-Fos와 NFATc1 등의 활성을 유도 하여 파골세포로의 분화를 촉진함을 알 수 있다.
현재, 골다공증의 치료방법으로서 완전하게 확립 된 것은 없으며 일단 손실된 골조직을 원상으로 재 생시키는 것은 어렵다. 따라서 가급적 조기에 발견 하고 골손실이 더 이상 증가되지 않도록 또는 진행 속도가 지연될 수 있도록 하는데 그 치료목표를 두 고 있다. 현재 파골세포의 분화 및 기능의 활성에 의 해 유발되는 골질환 치료나 예방의 목적으로 내인성 조절인자 외에도 여러 물질들이 연구되고 있다. 이 러한 목적으로 현재 사용되고 있는 약물들은 일정한 약리작용을 나타내고 있으나, 여러 가지 부작용과 복용상의 어려움을 갖고 있음으로써,
16-18부작용을 최소한으로 줄이기 위하여 천연자원으로부터 새로 운 작용 및 약물구조를 가지면서 독성과 부작용이 적은 골다공증의 예방 또는 치료에 효과적인 신물질 을 찾고자하는 시도가 계속해서 이루어지고 있는 실 정이다. 본 연구에 사용된 붉은색의 적복령(赤茯笭,
Poria cocos Wolf)은 소나무의 뿌리에 기생하며, 구멍장이버섯과에 속하는 버섯의 일종으로 흰색의 백복 령(白茯笭)과 함께 복령에 속한다. 이전 보고에 의하 면 복령은 이뇨, 진정, 심신수축 강화작용 등이 있으 며,
19항암, 항종양, 항구토, 항염증 기능도 알려져 있 다. 복령 균사체에서 분리한 U-pachymaran, pachy- maran, carboxymethylpachymaran 등은 항암 효과가
있으며,
20,21(1,3)-(1,6)-β-D-glucan은 강한 항종양성이
있다고 하였다.
22또한 복령 중의 triterpene성분은 항
구토, 항염증, 항피부암에 효과가 있다고 보고된 바
있다.
23최근 본 연구팀은 복령 중 백복령이 파골세
포의 분화에 중요한 NFATc1발현을 감소시킴으로써
파골세포의 분화를 억제하는 연구결과를 보고하였
다. 따라서 본 연구에서는 이전에 보고한 백복령의
파골세포에 미치는 영향과 비교하여, 적복령이 파골
세포의 분화 및 흡수에 미치는 효과를 검증하고 억
제 작용기전을 규명하고자 하였다.
대상 및 방법
1. 시약 및 실험재료
본 연구에 사용된 적복령 추출물은 ethanol 95~
95.5 v/v% 용매로 추출한 것으로 한국생명공학연구 원 한국식물추출물은행에서 구입하였다. 적복령 추 출물은 DMSO 용매를 사용하여 100 mg/mL로 -20
oC 저장하였고, 실험에는 25, 50, 100 μg/mL로 희석하여 분석에 사용하였다. TRAP 용액은 Sigma Aldrich (St. Louis, MO, USA) 제품을 사용하였고, XTT assay kit는 Roche (Indianapolis, IN, USA)에서 구입하였다. 세포배양 및 파골세포 분화를 위해 필 요한 α-minimum essential medium (α-MEM), fetal bovine serum (FBS) 및 penicillin-streptomycin 등은 Gibco-BRL (Grand Island, NT, USA)에서 구입하였고, Human RANKL와 Human M-CSF는 Peprotech (London, UK)의 제품을 사용하였다. Western blot을 위한 일차항체로 rabbit-anti-c-Fos, mouse-anti-NFATc1 (Santa Cruz Biotechnology; Santa Cruz, CA, USA), rabbit-anti-phospho-JNK, rabbit-anti-JNK, rabbit-anti- p h o s p h o - E R K , r a b b i t - a n t i - E R K , r a b b i t - a n t i - phospho-p38, rabbit-anti-p38, rabbit-anti-phospho-IκB, rabbit-anti-IκB (Cell Signaling Technology; Beverly, MA, USA) 및 mouse-anti-β-actin (internal control) (Sigma Aldrich) 등을 사용하였고, 이차항체는 Amer- sham Phamacia Biotechnology Inc. (Tokyo, Japan)구입 하여 사용하였다. 그 외 연구에 사용된 용매 및 시약 은 모두 일급 이상의 등급을 사용하였다.
2. 대식세포 획득 및 파골세포 분화
골수세포를 분리하기 위해 생후 5주령 ICR 마우 스를 경추 탈골법으로 희생시킨 후, 대퇴골과 경골 을 무균적으로 적출하고 연조직을 제거하였다. 장골 의 양끝을 절단한 후 양쪽 끝의 골수강에 1 mL의 주 사기를 이용하여 뼈의 속질을 수세함으로써 골수세 포를 얻었다. 분리된 골수세포는 10% FBS와 1%
penicillin/streptomycin이 포함된 α-MEM 배지에서 1 일간 배양한 후 미부착세포를 모았다. 파골세포의
전구세포가 되는 미부착세포를 10% FBS, 1% peni- cillin/streptomycin와 M-CSF (30 ng/mL)이 포함된 α- EM 배지에서 3일간 배양하였다. 3일 후, 부착된 대 식세포(bone marrow macrophage, BMM)를 사용하여 실험하였다. 대식세포는 M-CSF (30 ng/mL)와 RANKL (100 ng/mL)을 처리하여 배양하면서 적복령 추출물을 농도별로 각각 25, 50, 100μg/mL 처리하였 다. 분화유도 4일 후, 배양한 세포를 TRAP 용액으로 염색하고 붉은색으로 염색된 세포(성숙된 파골세포) 를 세어, 분화 정도를 분석하였다.
3. XTT 분석을 통한 세포 독성검사
대식세포를 96-well plate에 1x10
4/well로 분주하고, M-CSF (30 ng/mL), RANKL (100 ng/mL)와 적복령 추출물을 농도별로 첨가하여 3일간 배양하였다. 3일 후, XTT 용액 50μL를 각 well에 첨가하고 4시간 동 안 반응 후에 ELISA (Molecular Devices, CA, USA) 450 nm에서 분석하였다.
4. 역전사중합효소 연쇄반응(RT-PCR) 분석 세포 내 총 RNA는 QIAzol lysis reagent (QIAGEN, Valencia, CA, USA)로 설명서에 따라 추출하였다. 동 등한 양의 RNA는 TOPscript
TMcDNA synthesis kit (Enzynomics, Daejeon, Korea)를 사용하여 cDNA를 합 성하였다. cDNA 1μg은 다음과 같은 각각의 primer 를 이용하여 PCR을 수행하였다. c-Fos, forward 5'-ATCGGAGGAGGGAGCTGACA-3', reverse 5'- GGAACCGGACAGGTCCACAT-3'; NFATc1, forward 5'-CAACGCCCTGACCACCGATA-3', reverse 5'- GGCTGCCTTCCGTCTCATAG-3'; TRAP, forward 5'-ACTTCCCCAGCCCTTACTAC-3', reverse 5'-TCA- GCACATAGCCCACACCG-3'; OSCAR, forward 5'- AGGGAAACCTCATCCGTTTG-3', reverse 5'-GAGC- CGGAAATAAGGCACAG-3'; GAPDH, forward 5'- ACCACAGTCCATGCCATCAC-3', reverse 5'-TCCA- CCACCCTGTTGCTGTA-3'. PCR 조건은 94
oC에서 30초 동안 denaturation, 58
oC에서 30초 동안 annea- ling, 그리고 72
oC에서 30초 동안 extension 반응을 25
~30 cycles로 하여 증폭시켰다. PCR 산물은 1%
agarose gel에서 분리하였고, EtBr로 염색하여 자외선
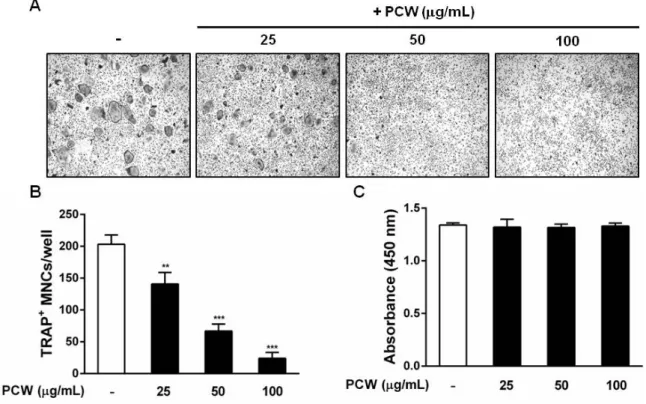
Fig. 1. Effects of Poria cocos Wolf (PCW) on RANKL-induced osteoclastogenesis in bone marrow macrophages (BMMs). (A) BMMs were cultured with PCW at 25, 50, 100 μg/mL for 4 days in the presence of M-CSF (30 ng/mL) and RANKL (100 ng/mL). After the 4 days culture, the cells were fixed and stained for TRAP.
TRAP-positive cells were photographed under a light microscope (x100). (B) TRAP-positive multinucleated cells containing three or more nuclei were counted as osteoclasts. The data shown are the mean±SD of three independent experiments. The asterisks indicate statistical significance compared with the control cells without PCW, **P<0.01, ***P<0.001 versus control. (C) Cell viability of the BMMs at 3 days of culture analyzed using the XTT assay kit.
파장에서 관찰하였다.
5. Western blot 분석
배양된 세포는 배지를 제거하고 PBS로 2회 세척한 후, lysis buffer (50 mM tris-Cl, 150 mM NaCl, 5 mM EDTA, 1% Triton X-100, 1 mM sodium fluoride, 1 mM sodium vanadate, 1% deoxycholate, protease inhibitors)로 용해시킨다. 용해된 단백질은 DC Protein assay kit (Bio-Rad, Hercules, CA, USA)를 사용하여 정량하고 동 량의 단백질(20μg)은 10% SDS- PAGE에서 분리하여 크기별로 분리된 단백질을 PVDF막(Amersham Pha- macia Biotechnology Inc.)으로 이동시켰다. 항체와 단백 질 간의 비특이적인 결합을 차단하기 위하여 blocking buffer (5% skim milk in TBST (0.01% tween 20 in TBS))에
서 실온, 1시간 동안 교반하였다. Blocking시킨 PVDF막 은 TBST로 10분 동안 2회 세척하고, 1차 항체를 4
oC, overnight 반응하였다. 반응 후, 10분씩 3회 세척하고 2차 항체는 blocking buffer에 1:3000 비율로 희석하여 실온에서 1시간 동안 반응하였다. TBST로 충분한 세척 후, 반응된 단백질은 HRP Chemiluminescent Substrate Reagent kit (Millipore Corp., Billerica, MA, USA)를 이용 하여 특이적 band를 확인하였다.
6. 골 흡수 분석
성숙한 파골세포를 얻기 위하여 collagen으로 코팅
한 90 mm 배양접시에 골수세포와 조골세포를 첨가
하고 1α, 25-dihydroxyvitamin D3 (VitD3)와 prosta-
glandin E2 (PGE2)를 처리하여 6일간 동조배양 하였
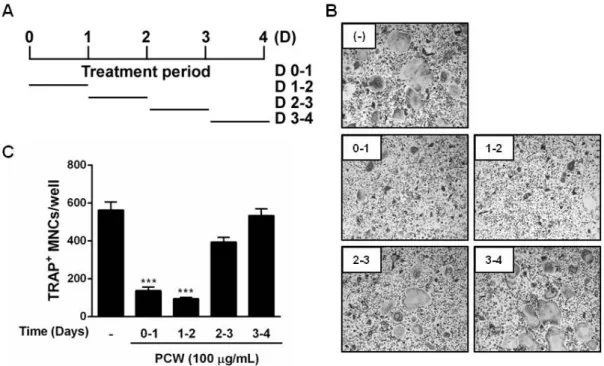
Fig. 2. Poria cocos Wolf (PCW) inhibits the early stage of osteoclast differentiation. (A) A diagram of the experimental design for PCW treatment. (B) Osteoclast was derived from BMM cells treated with RANKL (100 ng/mL) and M-CSF (30 ng/mL) in the presence of PCW. Osteoclasts was analyzed by TRAP staining an dphotographed (x 100). (C) TRAP-positive multinucleated cells counted as osteoclast. The results are expressed as mean ± SD of three cultures. ***P<0.001 versus control.
다. 배양한 후, 세포는 0.1% collagenase를 처리하여 떼어내고 hydroxyapatite-coated 96-well plate에 첨가 하였다. 동시에 적복령 추출물을 농도 별로 처리하 여 12시간 배양하였다. 12시간 배양 후, 세포는 증류 수로 수세하고 광학 현미경으로 사진을 찍었다.
Hydroxyapatite 흡수 영역은 Image Pro-Plus program version, 4.0 (Media Cybernetics)으로 정량화 하였다.
7. 통계분석
각 실험은 3회 이상 반복하였으며, 평균치 ± 표준 편차(SD)를 계산하였다. 각각의 조건에 따른 정량적 인 결과는 Student's t-test를 이용하여 분석하였고, 통 계적 유의성은 P<0.05 수준에서 평가하였다.
결 과
1. RANKL에 의해 유도된 파골세포 분화에 미치 는 적복령 추출물의 효과
RANKL에 의해 유도되는 전구세포에서 파골세포
로의 분화에 미치는 적복령 추출물의 효과를 확인하 기 위하여 마우스 골수에서 얻은 대식세포에 M-CSF 와 RNAKL을 처리하고 적복령 추출물을 농도별로 투여하여 4일간 배양 후, TRAP염색을 통해 파골세 포 분화능을 분석하였다. 그 결과, 적복령 추출물을 처리하지 않은 대조군은 붉은 색으로 염색된 TRAP 양성 다핵성 파골세포로 분화가 진행되었지만 적복 령 추출물을 처리한 실험군은 농도 의존적으로 파골 세포로의 분화가 억제됨을 형태학적으로 관찰할 수 있고(Fig. 1A), TRAP 양성 다핵성 파골세포의 수도 통계적으로 유의하게 억제되었다(Fig. 1B). 이러한 파골세포 분화에 대한 적복령 추출물의 효과가 세포 의 독성과 관련되는지 확인하기 위하여 XTT 분석을 실시하였다. Fig. 1C 결과와 같이, 파골세포 분화의 억제를 유도한 적복령 추출물의 농도에서 세포독성 은 나타나지 않았다. 따라서, 적복령 추출물에 의한 파골세포 분화 억제효과가 세포독성에 의한 것이 아 닌 적복령 자체의 효과임을 알 수 있다.
다음으로 적복령 추출물에 의한 파골세포의 분화
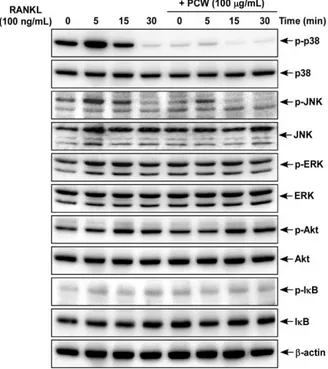
Fig. 4. Effects of Poria cocos Wolf (PCW) on RANKL- nducedsignaling pathways. (A) Mouse BMMs were pretreated with or without PCW (100 μg/
mL) for 1 h and then stimulated with RANKL (100 ng/mL) for the indicated time. The cell lysates were immunoblotted with specific antibodies. β-actin was used as an internal control.
Fig. 3. Effects of Poria cocos Wolf (PCW) on RANKL- mediated c-Fos, NFATc1, and osteoclast-related gene expression. (A) Mouse BMMs were cultured with PCW (100μg/mL) for the indicated time in the presence of M-CSF (30 ng/mL) and RANKL (100 ng/mL). mRNA expression for c-Fos, NFATc1, TRAP and OSCAR was analyzed by RT-PCR. GAPDH mRNA was used as an internal control. (B) Effect of PCW on the expression levels of NFATc1 and c-Fos during RANKL-induced osteoclastogenesis. The cells were incubated alone or in the presence of PCW and stimulated with RANKL (100 ng/mL) for the indicated time. The cell lysates were immunoblotted with specific antibodies. β-actin was used as an internal control.
억제 효과가 분화과정 중 어느 단계에서 작용하는지 여부를 확인하기 위하여 적복령 추출물 처리 시간을 달리하여 4단계로 구분하여 TRAP 양성 다핵성 염색 실험을 시행하였다. 실험결과 Fig. 2에서 보여주듯 이, 적복령 추출물을 D0-1, D1-2 단계에 처리했을 때 유의성 있게 분화가 억제되었지만, D2-3, D3-4 단계 에서는 분화 억제에 크게 변화를 주지 못하는 것을 확인할 수 있었다. 따라서 적복령 추출물에 의한 파 골세포의 분화 억제 효과는 분화 초기 단계에서 나 타남을 알 수 있었다.
2. RANKL과 관련된 유전자 발현에 미치는 적복 령 추출물의 효과
RANKL에 의해 발현되는 특정 유전자들은 파골세
포 분화를 조절하는 중요한 기능을 한다. 특히 c-Fos
는 파골세포 분화 초기단계에 중요한 전사인자로
NFATc1의 발현을 조절하고, 이 NFATc1은 TRAP와
OSCAR 유전자의 발현을 조절하여 파골세포 분화를
조절하게 된다. 따라서 파골세포 분화와 관련된 유
도인자에 적복령 추출물이 미치는 영향을 확인하기
위하여 RANKL로 유도되는 c-Fos, NFATc1, TRAP와
OSCAR의 mRNA 발현의 변화를 RT-PCR 방법으로
검증하였다. 그 결과, 적복령 추출물을 처리하지 않
은 경우에는 12시간에서 24시간 배양 시, 파골세포
의 분화에 중요한 역할을 하는 c-Fos, NFATc1,
TRAP, OSCAR mRNA 발현이 증가하였지만, 적복령
추출물을 함께 처리한 경우 c-Fos, NFATc1, TRAP,
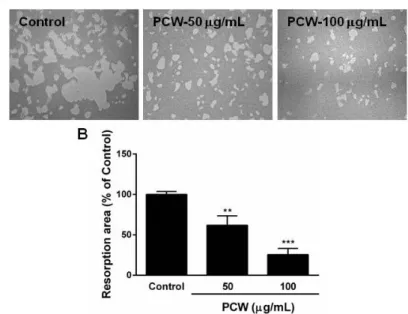
Fig. 5. Effect of Poria cocos Wolf (PCW) on bone resorption. Mature osteoclast were cultured on hydroxyapatite plates with increasing concentration of PCW for 24 h. (A) The cell were removed, and the resorbed pits were photographed. (B) Bone resorption was assessed by pit area measurement. **P<0.01, ***P<0.001 versus control.
OSCAR mRNA 발현이 모두 현저히 감소되는 것을 확 인하였다(Fig. 3A). RANKL에 의해 유도되는 c-Fos와 NFATc1 mRNA 발현에 적복령의 영향과 동일하게 c-Fos와 NFATc1 단백질 발현이 적복령 추출물에 의 해 현저히 감소되는 것을 관찰할 수 있었다(Fig. 3B).
3. RANKL에 의한 신호전달 체계에 미치는 적복 령 추출물의 효과
RANKL/RANK 상호작용에 의한 파골세포 분화는 다양한 신호전달 체계를 통해 조절되어진다. 특히 p38, ERK, JNK 등의 MAPK, Akt, 전사인자인 NF-κB 는 분화에 중추적인 역할을 하는 NFATc1과 c-Fos를 조절하는 중요한 신호전달 단백질로 알려져 있다.
따라서 RANKL신호 전달 경로에 적복령의 영향을 확인하였다. RANKL로 자극한 대조군과 비교했을 때, 적복령 추출물을 같이 처리한 군에서는 RANKL 에 의한 ERK, Akt, I-κB의 인산화 및 IκB의 분해에 차이를 관찰할 수 없었지만, p38, JNK의 인산화는 감소되는 것을 확인하였다(Fig. 4). 다음으로 저자는 파골세포 분화에 필수적인 c-Fos와 NFATc1의 발현 에 적복령 추출물의 영향을 실험하였다. 위 결과, 파
골세포 분화에 적복령 추출물의 억제 효과는 p38, JNK활성 억제에 의한 것임을 알 수 있었다.
4. 골 흡수능에 미치는 적복령 추출물의 효과 적복령 추출물이 파골세포의 분화에 미치는 효과 뿐만 아니라 뼈를 흡수하는 파골세포의 기능에도 영 향을 주는지 확인하기 위하여, 뼈의 주요 물질 중의 하나인 hydroxyapatite로 코팅된 plate에 파골세포를 배양하고 적복령 추출물의 처리 유무에 따라 흡수성 을 비교 분석하였다. 실험결과, 대조군의 파골세포 는 hydroxyapatite를 흡수하였지만, 적복령 추출물을 처리한 파골세포는 농도 의존적으로 hydroxyapatite 의 흡수현상이 감소하는 것을 확인할 수 있었다(Fig.
5). 따라서 적복령 추출물은 파골세포의 분화억제 효과뿐만 아니라 파골세포의 골 흡수 기능도 억제한 다는 것을 확인할 수 있었다.
고 찰