대한소화기학회지 1999;33:594 - 600
2)
접수: 1998년 2월 11일, 승인: 1998년 8월 28일
연락처: 김재준, 135-710, 서울특별시 강남구 일원동 50, 삼성서울병원 소화기내과 Tel: (02) 3410-3409, Fax: (02) 3410-3849
※ 본 논문은 삼성생명과학연구소 연구비와 영진약품주식회사의 연구비로 이루어졌음.
상부 위장관 질환에서 H elicob act er py lori cag A Gen e의 검출
성균관대학교 의과대학 삼성서울병원 소화기내과
손희정・김재준・이화영・김영호・이풍렬・고광철・백승운・이종철・최규완
D e t e c t i o n o f c a g A Ge n e i n H el i cob a c t er p yl o r i S t r a i n s Is o la t e d fro m G a s t r o d u d e n a l D i s e a s e s
He e J u n g S o n , M.D., J a e J u n Ki m , M.D., H w a Yo u n g Le e , M.D., You n g H o Ki m , M.D., P oo n g -Ly u l Rh e e , M.D., Kw a n g Ch e o l Ko h , M.D., S e u n g Wo o n P a i k , M.D., J on g Ch u l Rh e e , M.D. a n d Ky o o Wa n Ch o i , M.D.
Division of Gastroenterology, Samsung Medical Center, Sung Kyun Kwan University College of Medicine, Seoul, Korea
Background/Aims: It appeared to be geographic differences in the prevalence of cagA (cyto
toxin-associated gene A) positive strains. We investigated the relationship between cagA bearing H pylori strains and gastroduodenal diseases in Korea. Additionally we assessed the usefulness of reverse transcription-polymerase chain reaction (RT-PCR) for detecting cagA through comparison between RT-PCR of gastric biopsy specimens and PCR of bacterial isolates. Methods: Ninety-two patients were enrolled in this study. Antral biopsy specimens were taken for culture and RT-PCRResults: Culture or histology of antral biopsy specimens indicated that 82 (89.1%) of 92 patients
were infected with H. pylori. H. pylori was isolated from 69 patients (25 patients with gastritis, 29 patients with peptic ulcer disease, 15 patients with gastric cancer). CagA was detected by PCR in 61 (88.4%) of the 69 patients. The 61 patients included 20 patients (80.0%) with gastritis, 26 patient (89.7%) with peptic ulcer disease and 15 patients (100%) with gastric cancer (p>0.05). Of 92 patients, RT-PCR of biopsy specimens were performed in 22 patients. Detection rate of cagA gene by RT-PCR and PCR of bacterial genomic DNA were correlated by 78.6% (11/14). Conclusions:There was no relationship between cagA bearing H. pylori strains and gastroduodenal diseases Although cagA was rapidly detected by RT-PCR, it seemed to be less useful for diagnosing the presence of cagA gene than PCR of bacterial isolates. (Kor J Gastroenterol 1999;33:594 - 600)
Key Words: Helicobacter pylori, CagA, Gastroduodenal diseases
손희정 외 8인. 상부 위장관 질환과 Helicobacter pylori cagA Gene의 검출 595
서 론
1983년 Warren과 Marshall에 의하여 Helicobacter pylori (H. pylori)가 처음으로 분리 동정된 후 H.
pylori와 상부위장관 질환과의 연관성에 대한 많은 연구가 이루어져 왔다. 그러나 현재까지 H. pylori 감염이 상부위장관 질환을 유발하는 기전에 대해서 는 확실하게 알려진 바가 없는 실정이다.1-7 또한, H.
pylori의 감염 시 대부분의 경우에는 증상이 없으며 일부의 환자에서만 상부위장관 질환이 발생한다. 따 라서 어떤 독성인자를 가진 H. pylori에 감염된 경우 에 한하여 위장관 질환이 일어날 것이라는 가정하에 특정 독성인자를 가진 H. pylori와 상부위장관 질환 과의 연관성을 찾고자 하는 연구가 진행되어 왔다.
현재까지 알려진 여러 독성인자 중 대표적인 것 으로는 cytotoxin associated gene A (cagA)를 들 수 있는데 H. pylori의 60-70%에서 양성이라고 알려져 있다.8-10 CagA는 급성 염증과 밀접한 관련이 있어 in vitro 연구에서 cagA 양성인 H. pylori 균주로 자극하 면 cagA 음성인 경우보다 위 상피 조직세포의 interleukin-8의 생성이 현저히 증가되며 이는 생체에 서 발견되는 중성구의 침윤과 관계된다는 보고가 있 다.11 또한 위암 환자들에서 분리된 H. pylori 균주는 대조군에 비해 cagA의 양성률이 높게 보고되어 cagA와 위암과의 연관성이 제시되고 있다.9 그러나 cagA 양성률은 지역과 인종에 따라 차이를 보이고 있어12 우리 나라 나름대로의 연구가 필요한 실정이 다.
H. pylori의 독성인자를 확인하는 여러 방법 중 세 균배양법으로 균주를 얻어 확인하는 방법은 특이도 가 높고, 핵산을 추출하여 염기 서열을 알아낼 수 있 으며, H. pylori의 항생제에 대한 내성을 검사할 수 있는 장점이 있는 데 반하여, 배양 조건이 까다로우 며 단시간에 결과를 얻기 어려운 단점이 있다. 한편, 혈청학적 검사는 민감도는 높으나 과거와 현재 감염 사이의 분별력이 없어 특이도가 낮은 단점이 있다.13 최근 위점막의 생검 조직에서 직접 RNA를 추출하 여 역전사 중합효소 연쇄반응을 이용하여 cagA를 검출한 보고가 있었는데 이 방법은 세균 배양 없이
빠른 시간 내에 진단할 수 있다는 장점이 있다.13 그 러나 아직까지 우리 나라에는 이들 방법들의 유용 성에 대한 보고가 적은 실정이다.
이에 저자들은 상부위장관 질환 환자를 대상으로 하여 세균 배양을 통하여 H. pylori의 감염 여부와 cagA 유전자의 검출을 관찰하고 상부위장관 질환과 의 연관성을 알아보고자 하였으며, cagA 검출에 있 어 역전사 중합효소 연쇄반응법의 유용성을 알아보 고자 하였다.
대상 및 방법
1. 대 상
1995년 6월부터 1997년 2월까지 삼성서울병원 소 화기내과에 내원하여 상부 내시경검사를 시행받은 환자 중 H. pylori 세균 배양을 시행한 92명을 대상 으로 하였다. 평균 연령은 53.1세이고 남자 60명, 여 자 32명이었으며, 만성 위염이 32예, 소화성 궤양이 34예, 위암이 26예였다.
2. 방 법
1) 조직 생검 및 배양
내시경하에 위 전정부에서 3개의 조직 생검을 실 시하였다. 위 전정부 생검 조직 3개 중 1개는 조직 표본을 만들어 hematoxylin-eosin (H&E) 염색을 하 고, 1개는 세균 배양에 이용했고, 나머지 1개는 역전 사 중합효소 연쇄반응 방법에 이용하였다. 세균 배 양을 위한 조직은 다음 검사 때까지 4℃에서 냉장 보관하였고, 역전사 중합효소 연쇄반응을 위한 조직 은 -70℃에 보관하였다.
2) 세균 배양
쇄석된 생검 조직을 chocolate blood agar plate에 바르고 microaerophilic (5% O2, 10% CO2, 85% N2) 조건에서 5-7일간 배양하였다. H. pylori균의 동정은 urease, catalase와 oxidase 반응으로 관찰하였다.
3) 중합효소 연쇄반응
Chocolate blood agar plate에서 배양된 H. pylori 를 loop으로 채취하여 10,000 g에서 1분간 원심분리
596 The Korean Journal of Gastroenterology : Vol. 33, No. 5, 1999
한 후 세균 pellet을 150 μl의 phosphate-buffered- saline (pH 7.4)로 두 번 세척한 후, 50 μl 증류수에 세균 pellet을 부유시키고 10분간 끓인다. 이후 10,000 g로 원심분리하여 부유층을 얻어 중합효소 연쇄반응의 template로 쓰기 위해 -20℃에 보관하였 다.10
CagA 검출을 위한 중합효소 연쇄반응의 oligonu- cleotide primer는 기존의 염기 서열13에 따라 제작하 였으며(5' -GATAACAGGCAAGCTTTTGAGG-3' , 5' - CTGCAAAAGATT-GTTTGCGAGA-3' ) 298 bp 크 기의 생성물을 형성하였다. 중합효소 연쇄반응은 500 mmol/L KCl, 100 mmol/L Tris-HCl (pH 8.8), 15 mmol/L MgCl2, 1% Triton X-100을 포함하는 8 μl의 10X PCR reaction buffer (Perkin-Elmer-Cetus, Co., Norwalk, CT, USA)와 1 μl의 20 mM dNTP (Phar macia Biotech, Uppsala, Sweeden), 0.4 μl의 1.0 U Taq DNA polymerase (Amplitaq, Perkin-Elmer-Cetus Co., Norwalk, CT, USA), 증류수, 2.5 μl의 cagA specific primer, 그리고 DNA template를 포함하여 50 μl 부피의 반응 혼합물을 만든 후 25 μl의 mi neral oil을 첨가하였다. PCR 반응은 94℃에서 1분간 denaturation, 55℃에서 1분간 annealing, 72℃에서 1 분간 extension하는 cycle로 39회 시행하였다. 생성 물의 충분한 extension을 위하여 마지막 cycle은 7분 동안 72℃에서 시행하였다.
4) 역전사 중합효소 연쇄반응
생검 조직에서 mRNA extraction kit (Qiagen GmbH, Hilden, Germany)를 이용하여 mRNA를 추 출하였다. 방법은 분쇄한 생검 조직에 β-mercaptoe- thanol 15 μl와 700 mM Urea, 500 mM NaCl, 50 mM HEPES (pH 7.8), 1% SDS를 포함하는 lysis buffer 400 μl를 넣고 제작사의 지침대로 제작된 dilution buffer 800 μl를 넣은 후 상온에서 3분간 원 심분리하였다. 여기에 10 mM Tris-HCl (pH 7.5), 140 mM NaCl, 1 mM EDTA, 0.1% SDS, 0.1% NaN3 를 포함하는 oligotex suspension을 20 μl 넣고 상온 에서 10분간 방치한 후 5분간 원심분리하였다. 상층 액을 버린 후에 제작사의 지침대로 제작된 350 μl로 처리한 후 새 tube에 옮겨 30초간 14,000 g에서 원심
분리하였다. Wash buffer 처리 과정을 두 번 반복한 후 두 번에 걸쳐 5 mM elution buffer 10 μl를 넣고 30초간 원심분리하여 RNA를 추출하였다.
역전사 반응을 위해 9 μl의 RNA 수용액과 2 μl 의 100 mM random hexamer (Promega, Maidison, WI, USA), 4 μl의 5X buffer (Perkin-Elmer-Cetus Co.), 2 μl의 0.1 mM dithiothreitiol (Gibco/BRL, Gaithersburg, MD, USA), 1 μl의 20 mM dNTP (Pharmacia Biotech), 1 μl의 rRNAsin (recombinant ribonuclease inhibitor, Promega, Maidison, WI, USA) 및 1 μl의 200 U/μl moloney murine leukemia virus reverse transcriptase (Gibco/BRL, Gaithersburg, MD, USA)를 혼합하여 20 μl의 반응물을 만들었다. 이 반응물을 실온에서 10분, 42℃에서 1시간 반응시킨 후에 72℃에서 5분간 효소를 비활성화시켰다. 이후 3)과 같은 방법으로 중합효소 연쇄반응을 시행하였 다.
PCR 생성물은 ethidium bromide를 포함하는 2%
agarose gel젤 전기영동법을 이용하여 확인하였다.
5) 결과 분석
H. pylori의 존재 유무는 H&E 염색이나 세균배양 검사로 관찰하였으며 한 가지 검사에서라도 양성이 면 H. pylori 양성군으로 분류하였다. CagA 유무는 세균 배양에서 추출된 집락을 이용한 중합효소 연쇄 반응과 조직을 이용한 역전사 중합효소 연쇄반응에 서 관찰하였으며 한 가지 검사에서라도 양성이면 cagA 양성군으로 분류하였다.
통계는 Pearson chi-square test와 Fisher' s exact test를 이용하여 분석하였다.
결 과
1. H . p y lori의 감염률
세균 배양을 실시한 92명 중 69명에서 H. pylori 의 감염이 관찰되었으며, 세균 배양에서는 H. pylori 감염이 관찰되지 않았으나 조직 소견에서만 H.
pylori의 감염이 관찰된 경우가 13명으로 전체 92명 중 82명(89.1%)에서 H. pylori 감염이 관찰되었다.
질환별로 살펴보면 만성 위염 환자 32명 중 31명
Son et al. cagA Gene in Helicobacter pylori Strains Isolated from Gastrodudenal Diseases 597
(96.8%), 소화성 궤양 환자 34명 중 33명(97.1%), 위 암 환자 26명 중 18명(69.2%)에서 H. pylori 감염이 관찰되어 질환간에 H. pylori 감염의 유의한 차이는 없었다(p>0.05).
2. 상부위장관 질환에서 cag A 의 발현 검출 세균 배양에서 H. pylori 감염이 관찰되었던 69명 중 61명(88.4%)에서 cagA의 발현 검출을 관찰할 수 있었다(Fig. 1). 질환별로는 H. pylori 감염이 관찰된 만성 위염 환자 25명 중 20명(80.0%), 소화성 궤양 환자 29명 중 26명(89.7%), 위암 환자 15명 중 15명 (100.0%)에서 cagA의 검출이 관찰되었다. 질환군에 서 cagA 검출에는 통계적으로 유의한 차이는 없었 다(p>0.05).
3. 세균 배양 후 중합효소 연쇄반응법과 생검 조직에서의 역전사 중합효소 연쇄반응법에 의한 cag A 검출 발현 진단의 비교 대상 환자 92명 중 22명에서 중합효소 연쇄반응 법에 의한 cagA 검출과 생검 조직에서의 역전사 중 합효소 연쇄반응법에 의한 cagA mRNA 발현을 비 교하였다. 22명 중 H&E 염색 또는 세균 배양에서 H. pylori의 감염이 관찰된 경우는 18명(81.8%)이고, H&E 염색 또는 세균 배양에서 H. pylori의 감염이 관찰되지 않은 경우는 4명(18.2%)이었다. 22명 중 H&E 염색에서 H. pylori의 감염이 관찰된 경우는 14 명(63.6%)이고 이 중 세균 배양이 성공한 경우는 10 명이었으며, H&E 염색에서 H. pylori의 감염이 관찰 되지 않은 경우는 8명(36.4%)이었고 이 중 세균 배 양이 성공한 경우는 4명이었다. 22명 중 세균 배양 이 성공한 경우는 14명(63.6%)이었다. 세균배양이 성공한 14명 중 12명에서 중합효소 연쇄반응법에 의 해 cagA를 검출하였으며 12명 중 9명에서만 생검 조 직에서의 역전사 중합효소 연쇄반응법에 의해서 cagA mRNA 발현을 확인하였고(Fig. 2) 나머지 3명 에선 cagA mRNA 발현이 없었다. 세균 배양이 되지 않은 8명 중 H&E 염색으로 4명에서 H. pylori 감염 을 관찰할 수 있었으며, 감염이 관찰된 4명 중 1명에 서 역전사 중합효소 연쇄반응법에 의해 cagA mRNA 발현을 확인하였다.
고 찰
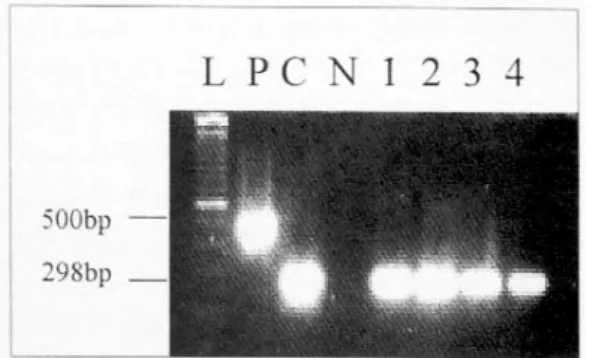
H. pylori가 사람의 위장관에 감염되어 어떠한 기 전으로 상부위장관 질환을 일으키는지에 관해서는 현재까지 정확하게 알려진 바가 없는 실정이다.1-7 최근 독성인자를 가진 H. pylori에 감염된 경우에 한 하여 위장관 질환이 일어날 것이라는 가정하에 특정 독성인자를 가진 H. pylori와 상부위장관 질환과의 연관성을 찾고자 하는 연구가 진행되어 왔다. 현재 까지 알려진 H. pylori의 주요 병독인자들을 살펴보 Fig. 1. RT-PCR using cagA primer pairs. PCR was performed on four different cDNA samples from mRNA of gastric tissue. The 298 bp cagA PCR product was demonstrated in all samples (lane1-4). A 100 bp size marker series was run in lane L as a reference. A 500 bp PCR product was run in lane P as a positive control for PCR. A 298 bp PCR product was run in lane C as a positive control for cagA. Negative control for cagA was run in lane N.
Fig. 2. PCR using cagA primer pairs. PCR was perfor- med on four different genomic DNA samples of bacterial isolates. The 298 bp cagA PCR product was demonstrated in all samples (lane1-4). Lane L, P, C, N are same as in Fig. 1.
598 대한소화기학회지 : 제 33 권 제 5 호 1999
면 flagella, urease, adhesin gene, vaculoating cyto- toxin 및 cytotoxin associated gene A (CagA) 단백질 을 들 수 있다. CagA는 96-138 kD의 다양한 분자량 을 갖는 surface immunodominant antigen으로 H.
pylori의 60-70%에서 cagA 유전자의 발현 검출이 보고되고 있다.8-10 이 cagA는 급성 염증과 밀접한 관련이 있고 따라서 cagA는 독성인자를 함유하는 H. pylori 균주를 동정하는 데 유용한 지표로 여겨지 고 있다. H. pylori의 위염 발병기전에 cagA의 중요 성을 보고한 연구 중 Crabtree 등11이 보고한 결과에 서 H. pylori에 의한 위염에서 cagA 양성인 경우가 음성인 경우보다 위 상피세포 interleukin-8의 발현 검출이 현저히 증가되어 있었다. 이들은 cagA에 의 해 유도된 interleukin-8의 증가는 중성구의 이동과 활성에 결정적인 역할을 하게 되며 활성화된 중성 구는 또다시 interleukin-8을 분비하게 되어 감염에 대한 염증이 계속되게 되며 이로 인해 점막 손상이 초래된다고 주장하였다. 실험실 결과 외에도 이들 병독인자를 갖고 있는 H. pylori와 소화성 궤양의 연 관을 조사한 보고에 따르면 소화성 궤양 환자의 100%에서 CagA에 대한 혈청 항체 양성률을 보이고 위염만 있는 환자는 60-62%에서만 혈청 항체 양성 률을 보인다는 보고가 있다.14-16 또한 nested case-control 연구를 포함한 역학조사에서 CagA에 대한 혈청 항체가 위암 환자에서 증가되어 있음을 관찰하였다.17-22 반면에 다른 연구12에 의하면, CagA 에 대한 혈청 항체 양성률이 호주의 십이지장궤양 환자와 비궤양성 소화불량증 환자에서 각각 89.6%
와 66.7%의 차이와는 달리, 중국인 위암 환자와 대 조군에서는 각각 83.3%와 85.7%로 보고하였다. 그 러나 이들 대부분의 연구는 H. pylori의 감염률이 40-50%인 선진국의 연구 결과로,23 CagA에 대한 혈 청 항체 양성률은 지역과 인종에 따라서도 다른 결 과를 보이고 있어 H. pylori의 감염률이 높은 우리 나라 나름대로의 결과가 필요한 실정이다. 우리 나 라 환자를 대상으로 연구24에서 CagA에 대한 혈청 항체를 측정한 결과 상부위장관 질환에서 CagA 발 현 검출률의 차이를 관찰할 수 없다고 하였다. 그러 나 혈청 항체 측정은 과거의 감염과 현재의 감염을 구분할 수 없는 단점이 있어 저자 등은 현재 감염을
반영하는 중합효소 연쇄반응법을 이용하여 cagA 양 성률을 조사하고자 하였다. 본 연구 cagA 양성률은 88.4%였으며, 서구와 달리 위염 환자와 소화성 궤 양 환자 및 위암 환자 간에 통계적인 차이를 발견할 수 없었다. 따라서 H. pylori의 감염률이 높은 우리 나라에서는 H. pylori의 병리기전에 있어 cagA 외에 다른 인자에 대한 연구가 필요하리라 생각된다.
CagA 진단 방법 중 세균 배양에 의한 검사는 그 특이도가 100%로, 염기 서열을 알아볼 수 있고 항생 제에 대한 감수성 검사가 가능하다는 장점이 있으나 배양 조건이 까다롭고 5일 내지 7일간의 시간이 걸 려 단시간에 결과를 알기 어려운 단점이 있다.25 이 에 반해 역전사 중합효소 연쇄반응법은 배양에 시간 이 필요 없다는 장점이 있다. 1992년 처음으로 역전 사 중합효소 연쇄반응법으로 위 점막에서 H. pylori 의 16S rRNA를 진단하였으며,26 이후 역전사 중합 효소 연쇄반응법으로 H. pylori를 진단하고 cagA mRNA 발현을 보고하였는데,13 역전사 중합효소 연 쇄반응법의 민감도는 96%, cagA의 양성률은 56%였 으며 역전사 중합효소 연쇄반응법과 세균의 geno- mic DNA로부터 중합효소 연쇄반응법에 의한 cagA 양성률이 100% 일치함을 보고하였다.12 그러나 본 연구 결과 cagA 양성이었던 12명 중 세균배양법과 역전사 중합효소 연쇄반응법에서 결과가 일치한 경 우는 9명이었으며 3명에서 서로 다른 결과가 나타나 본 연구 결과의 일치율은 78.6% (11/14)로 외국의 보고에 비해 낮았다. 역전사 중합효소 연쇄반응법의 결과가 배양에 의한 중합효소 연쇄반응법과 상이한 이유로는 조직을 조작할 때 mRNA의 파괴 등 기술 적인 면에서의 제약이 많은 역전사 중합효소 연쇄반 응법의 제한점을 생각할 수 있겠다. 세균 배양이 되 지 않은 1명에서 역전사 중합효소 연쇄반응법에 의 해 cagA를 검출할 수 있었다. 이는 H. pylori의 감염 이 첩포상으로 분포하여 역전사 중합효소 연쇄반응 을 위한 조직 생검에 H. pylori가 포함되어 양성으로 발현되었을 가능성을 생각할 수 있겠다.
중합효소 연쇄반응법은 세균배양법에 의한 중합 효소 연쇄반응법보다 신속하게 결과를 알 수 있는 장점이 있지만 세균배양법에 의한 중합효소 연쇄반 응법과의 일치율이 낮아 그 유용성이 떨어진다고 하
손희정 외 8인. 상부 위장관 질환과 Helicobacter pylori cagA Gene의 검출 599
겠다. 그러나 본 연구에서 역전사 중합효소 연쇄반 응법을 시행한 환자 수가 적었으며, 역전사 중합효 소 연쇄반응법이 기술적인 제약이 많다는 것을 고 려해 볼 때 앞으로 더 많은 수를 대상으로 한 연구 가 필요하리라 생각된다.
결론적으로 cagA 검출은 서구와는 달리 위암, 소 화성 궤양, 위염에서 모두 양성률이 높아서 상부위 장관 질환과 cagA와의 연관성을 발견할 수 없어 H.
pylori에 의한 위장관 질환의 병태생리에 있어서 cagA는 중요한 역할을 하지 않으리라 사료된다. 한 편, 역전사 중합효소 연쇄반응법에 의한 cagA 검출 은 세균 배양법에 의한 중합효소 연쇄반응법과의 일 치율이 낮아 그 유용성이 떨어진다고 생각된다. 그 러나 단시간에 병독인자를 검출할 수 있는 장점이 있으므로 앞으로 더 많은 환자를 대상으로 한 연구 가 필요하리라 사료된다.
요 약
목적: 상부위장관 질환 환자를 대상으로 하여 cagA와 상부위장관 질환과의 연관성을 알아보고자 하였다. 또한 세균배양법에 의한 중합효소 연쇄반응 법과 위점막 생검 조직의 역전사 중합효소 연쇄반응 법에 의한 cagA 검출을 비교하여 역전사 중합효소 연쇄반응법의 유용성을 알아보고자 하였다. 대상 및 방법: 1995년 6월부터 1997년 2월까지 삼성서울병 원 소화기내과에 내원하여 상부소화기 내시경검사 를 시행받은 환자 중 세균 배양이 가능했던 92명을 대상으로 하였다. 내시경 소견은 위염 32예, 소화성 궤양 34예, 위암 26예였다. CagA의 검출 유무는 세 균 배양에서 추출된 집락을 이용한 중합효소 연쇄반 응법과 역전사 중합효소 연쇄반응법으로 관찰하였 다. 결과: 92명 중 82명(89.1%)의 환자에서 H. pylori 감염이 관찰되었다. 세균 배양에서 H. pylori 감염이 관찰된 69명 중 61명(88.4%)에서 cagA 검출을 관찰 할 수 있었다. CagA 검출은 H. pylori 감염이 관찰된 위염 환자 25명 중 20명(80.0%), 소화성 궤양 환자 29명 중 26명(89.7%), 위암 환자 15명 중 15명 (100.0%)에서 관찰되었고, 각각의 질환군에서 cagA 양성률에는 유의한 차이가 없었다(p>0.05). 22명에
서 역전사 중합효소 연쇄반응법을 실시하였다. 세균 배양법에 의한 중합효소 연쇄반응법과 역전사 중합 효소 연쇄반응법에 의한 결과의 일치율은 14명 중 11명으로 78.6%였다. 결론: CagA 양성률은 서구와 는 달리 위암, 소화성 궤양, 위염에서 모두 양성률이 높아서 상부위장관 질환과 cagA와의 연관성을 발견 할 수 없었다. 또한 역전사 중합효소 연쇄반응법에 의한 cagA 검출은 중합효소 연쇄반응법과의 일치율 이 낮아 그 유용성이 떨어진다고 사료된다.
색인단어: Helicobacter pylori, cagA, 상부위장관 질환
감사의 글
본 연구에 도움을 준 삼성생명과학연구소 하혜영 씨에게 감사드립니다.
참 고 문 헌
1. Correa P. Human gastric carcinogenesis: a multistep and multifactorial process-first American cancer society award lecture on cancer epidemiology and prevention. Cancer Res 1992;52:6735-6740.
2. Cover TL, Blaser MJ. Helicobacter pylori and gast roduodenal disease. Annu Rev Med 1992;43:135- 145.
3. Jung HC, Kim WH, Song IS, Kim CY. Etiologic role of Helicobacter pylori in the pathogenesis o histologic chronic gastritis. Seoul J Med 1990;31 231-246.
4. 정현채, 최상운, 송영욱 등. 소화성 궤양, 위염 및 기능 성 위장장애 환자에서 Campylobacter pylori의 검출 과 이에 대한 혈청 IgG 항체가의 의미. 대한소화기학 회지 1988;20:47-56.
5. Kim NY, Oh HS, Jung HM, We SH, Choi JH, Le KH. The effect of eradication of Helicobacter pylor upon the duodenal ulcer recurrence. Korean J Intern Med 1994;92:72-79.
6. Rauws EA, Langenberg W, Houthoff HJ, Zanen HC Tytgat GN. Campylobacter pyloridis-associated chronic active antral gastritis. A prospective study of its pre
600 The Korean Journal of Gastroenterology : Vol. 33, No. 5, 1999
valence and the effects of antibacterial and antiul- cer treatment. Gastroenterology 1988;94:33-40.
7. Peterson WL. Helicobacter pylori and peptic ulcer disease. N Engl J Med 1991;324:1043-1048.
8. Apel I, Jacobs E, Kist M, Bredt W. Antibody res ponse of patients against a 120 kDa surface protein of Campylobacter pylori. Zentralbl Bakteriol Parasi teukd Infektionskr Hyg. Abt 1 Orig Reihe A 1988 268:271-276.
9. Blaser MJ, Perez-Perez IG, Kleanthous H, et al Infection with Helicobacter pylori strains possessing cagA is associated with an increased risk developing adenocacrcinoma of the stomach. Cancer Res 1995 55:2111-2115.
10. Yamaoka Y, Kita M, Kodama T, Sawai N, Imanish J. Helicobacter pylori cagA gene and expression o cytokine messenger RNA in gastric mucosa. Gastro enterology 1996;110:1744-1752.
11. Crabtree JE, Farmery SM, Lindley IJD, Figura N Peichl P, Tompkins DS. CagA/cytotoxin striains of Helicobacter pylori and interleukin-8 in gastric epithelial cell lines. J Clin Pathol 1994;47:945-950 12. Mitchell HM, Hazell SL, Li YY, Hu PJ. Serologica response to specific Helicobacter pylori antigens:
antibody against CagA antigen is not predictive o gastric cancer in a developing country. Am J Gastroenterol 1996;91:1785-1788.
13. Peek RM Jr, Miller GG, Tham KT, et al. Detection of Helicobacter pylori gene expression in human gastric mucosa. Jof Clin Microbiol 1995;33:28-32.
14. Covacci A, Censini S, Bugnoli M, et al. Molecula characterization of the 128 kDa immunodominant antigen of Helicobacter pylori associated with cytotoxicity and duodenal ulcer. Proc Natl Acad Sc USA 1993;90:5791-5795.
15. Cover TL, Dooley CP, Blaser MJ. Characterization of and human serologic response to proteins in Helicobacter pylori broth culture supernatants with vacuolizing cytotoxin activity. Infect Immun 1990;
58:603-610.
16. Crabtree JE, Taylor JD, Wyatt JI, et al. Mucosal IgA
recognition of Helicobacter pylori 120 kDa protein, peptic ulceration and gastric pathology. Lancet 1991; 338:332-335.
17. Parsonett J, Friedman GD, Vandersteen DP, et al Helicobacter pylori infection and the risk of gastric carcinoma. N Eengl J Med 1991;325:1127-1131.
18. Normura A, Stemmermann GN, Chyou P, Kato I Perez-Perez GI, Balser MJ. Helicobacter pylori infection and gastric carcinoma in a population o Japanese-Americans in Hawaii. N Engl J Med 1991 325:1132-1136.
19. EUROGAST Study Group. An international asso ciation between Helicobacter pylori infection and gastric cancer. Lancet 1993;341:1359-1362.
20. Asaka M, Kimura Tt, Kato M, et al. Possible role o Helicobacter pylori in early gastric cancer develop ment. Cancer (Phila.) 1994;73:2691-2694.
21. Sipponen P, Hyvarinen H. Role of Helicobacter pylori in the pathogenesis of gastritis, peptic ulcera tion and gatstric cancer. Scand J Gastroenterol 1993 196:S3-S6.
22. Forman D, Newell DG, Fullerton F, et al. Asso ciation between infection with Helicobacter pylori and risk of gastric cancer: evidence from a prospec tive investigation. Br Med J 1991;302:1302-1305.
23. NIH consensus development panel on Helicobacter pylori in peptic ulcer disease. JAMA 1994;272;65- 69.
24. 김경철, 박효진, 이홍우 등. Helicobacter pylori 감염 환자에서 CagA와 VacA의 혈청학적 인식과 혈청 gastrin 및 pesinogen 농도와의 관계. 대한소화기학회 지 1997;29:25-34.
25. 서정기, 심재건, 김의종. 소아 Helicobacter plyori 위 염의 혈청학적 진단: 정상 학동기 아동과 위장관 증상 환아에서의 유병실태 및 혈청학적 진단의 정확도에 관한 연구. 대한소화기내시경학회지 1993;13:673-684.
26. Engstrand L, Ngyyen AM, Graham DY, Zaatari FA Reverse transcription and polymerase chain reaction amplification of rRNA for detection of Helicobacter species. J Clin Microbiol 1992;30:2295-2301.