류마티스 관절염 환자에서 Antifilaggrin Antibody 검사의 진단적 유용성
최석우・임미경*・신동혁*・임춘화・심승철*
을지대학교 의과대학 진단검사의학교실, 내과학교실*
Diagnostic Performance of the Antifilaggrin Antibody in Rheumatoid Arthritis
Suk Woo Choi, Mi Kyoung Lim*, Dong Hyuk Sheen*, Chun Hwa Ihm, and Seung Cheol Shim*
Department of Laboratory Medicine and Internal Medicine*, Eulji University, School of Medicine, Daejeon, Korea
Backgrounds:Rheumatoid factor (RF) is common serological marker for the diagnosis of rheumatoid arthritis (RA), but its sensitivity and specificity are not satisfactory for the diagnosis of RA. Therefore, we investigated the diagnostic performance of a new antifilaggrin antibody test by enzyme linked immunosorbent assay (ELISA) in RA.
Methods:Recombinant human filaggrin was deiminated in vitro by peptidylarginine deiminase and used as the coating antigen for ELISA. We performed the RF and the antifilaggrin antibody for 324 RA patients, 251 non-RA patients (rheumatic diseases other than RA), and 286 normal individuals and evaluated the sensitivities and specificities of RF and antifilaggrin antibody. Optimal cut off values were calculated as mean+2SD in 95% confidence interval except 3SD for 286 normal individuals. Optimal cut off values of antifilaggrin antibody and RF were 9.6 U/ml and 12 U/ml, respectively.
Results:The sensitivities and specificities of antifilaggrin antibody were 44.8% and 89.2% at optimal cut off values. The sensitivity and specificity of RF were 75.0% and 83.3%. Combination of "antifilaggrin antibody and RF" showed significantly high specificity of 95.2% and that of
"antifilaggrin antibody or RF" showed slightly high sensitivity of 79.3% at optimal cut off values.
Antifilaggrin antibody was positive in 17.3% among 81 sero-negative RA patients.
Conclusion:We considered that antifilaggrin antibody could be used a supplementary test of RF for the diagnosis of RA, because "antifilaggrin antibody and RF" had higher diagnostic specificity than RF alone and antifilaggrin antibody test was easy, convenient ELISA method in performance.
Key Words:Rheumatoid arthritis, Antifilaggrin antibody, Rheumatoid factor
* 이 논문은 2002년도 범석학술장학재단 연구비 지원에 의한 것임 교신저자:최석우
우) 301-726 대전시 중구 목동 24-14 을지대학병원 진단검사의학과 전화:042-259-1481, FAX:042-259-1495 E-mail:drcsw@eulji.ac.kr
서 론
류마티스 관절염은 만성 전신성 염증성 질환이며 일차적
으로 임상증상에 의해 진단되어지고 일반적인 혈청학적 검 사로는 류마티스 인자(rheumatoid factor, RF)에 제한되 어 있었다. 그러나 RF는 류마티스 관절염 환자의 50-80%
에서 증가되어 있고[1], 특이도가 87%로 높지 않아 다른
자가 면역 질환이나 만성 염증, 악성종양, 건강한 노인에게
서도 나타나는 단점이 있다[2]. 류마티스 관절염에서 발견
되는 그 외의 자가 항체들로는 RA33 및 Sa, p68, calpa-
statin, perinuclear factor 등에 대한 자가 항체가 존재
한다[2].
Table 1. Characteristics of studied subjects
Group of Studies N Age
Mean Range
Reumatoid arthritis 324 50 4-83
Non-rheumatoid arthritis 251 55 22-90
Ankylosing spondylitis 6 26 22-47
Behcet's disease 16 44 22-61
Carpal tunnel syndrome 1 69
Fibromyalgia 24 45.5 23-63
Gout 12 52.5 40-72
Juvenile rheumatoid arthritis 15 22 13-60 Mixed connective tissue disease 1 65
Myofascial syndrome 1 55
Osteoarthritis 142 61 32-90
Reactive arthritis 3 43 29-59
Spondyloarthritis 7 48 42-55
Systemic lupus erythematosus 20 47 26-70
Systemic sclerosis 3 63 38-73
Healthy controls 286 50.4 16-72
류마티스 관절염에서 발견되는 자가항체중 인체 buccal keratinocytes내 perinuclear granules와 반응하는 an- tiperinuclear factor (APF)[3]와 쥐의 식도상피의 stra- tum corneum에 대한 항체인 antikeratin antibodies (AKA)[4]가 가장 특이적인 표식자로 알려져 있다. APF는 1964년 Nienhuis[3]에 의해 AKA는 1979년 Young[4]
에 의해 처음으로 기술되었다. AKA는 인체 상피세포내에 있는 filaggrin의 neutral-acidic isoform을 인지하며[5], APF는 epidermal (pro)filaggrin과 밀접한 단백질을 인 지하는 것[6]으로 비교적 특이도가 높은 것으로 알려져 있 다. 최근, APF와 AKA가 filaggrin에 반응하는 동일한 자 가항체임이 밝혀져 이 두 자가항체를 antifilaggrin auto- antibodies라 부르기도 한다[5, 6].
Vincent 등은 검사 방법에 따라 차이를 보이지만 AKA 와 APF의 민감도와 특이도를 각각 52%와 97%, 67%와 93%로 보고하기도 하였다[7]. 그러나 APF가 류마티스 관 절염 환자에서 특이도가 높은 검사임에도 제한되어 사용되 어 왔는데 그 이유는 주관적이고 간접 면역형광법으로 검사 가 이루어지며, 미리 선별된 구강 세포 공여자가 있어야 되 며, 검사실간 표준화가 문제가 되기 때문이다[8].
최근 peptidylarginine deiminase (PAD)에 의한 ar- ginines의 deimination에 의해 생성된 citrulline resi- dues를 포함하는 항원 결정기와 반응하는 자가항체가 류마 티스 관절염에 특이적으로 발견되었으며, 이 citrullinated residues에 대한 항체가 APF나 AKA와 동일한 항체라는 것이 증명되었고, 류마티스 관절염의 80% 이상에서 검출된
다고 보고되었다[9, 10]. 즉, citrulline이 류마티스 관절 염 환자들에서 특이적으로 가지는 자가항체가 인지하는 fi- laggrin epitope에 필수적인 물질임이 증명되었다[9].
이에 저자는 최근 유전자 재조합 기술에 의해 human filaggrin을 생성한 후 PAD에 의해 in vitro deimina- tion으로 제조된 citrullinated filaggrin 항원을 이용한 antifilaggrin antibody enzyme linked immunosor- bent assay (ELISA) 검사 방법이 개발됨에 따라 류마티 스 관절염 환자에서 새로운 혈청학적 검사로서 antifilag- grin antibody 검사의 진단적 유용성을 알아보고자 RF 함 께 antifilaggrin antibody 검사의 민감도, 특이도 등을 평가하고자 한다.
대상 및 방법 1. 연구 대상
2002년 1월부터 5월까지 류마티스 내과에 내원하는 환 자를 대상으로 검체를 수집하고 환자기록부를 조사하였다.
환자군은 American College of Rheumatology (ACR) 의 기준에[11] 맞는 류마티스 관절염 환자 324명과 대조 환자군으로 다른 류마티스 질환자 251명, 그리고 종합 건 강검진을 받는 일반인 중 다른 검사 소견상 이상이 없었던 286명을 건강대조군으로 하여 RF와 antifilaggrin anti- body 검사를 시행하였다. 류마티스 관절염 환자는 총 324 명(4-83세)으로 56.3%이었고, 남자는 49명, 여자는 275 명 이었으며 disease modifying antirheumatic drug (DMARD)으로 치료중인 환자이었다. 대조환자군은 총 251명(13-90세)이었고, 남자는 41명, 여자는 210명이었 다. 대조환자군의 질환에는 골관절염 환자가 142명으로 대 조환자군 중 56.2%이었고 섬유근육염증 24명, 루푸스 20 명, 베제씨 질환 16명, 소아성 류마티스 관절염 15명, 통 풍 12명, 척추관절염 7명, 강직성 척추염 6명, 전신 경화 증 3명, 반응성 관절염 3명, 그 외 수근 터널 증후군, 복합 성교원조직질환, 근육막동통증후군 각각 1명이었다(Table 1).
2. 연구 방법
2002년 1월부터 5월까지 을지대학병원 류마티스 내과에 내원한 환자의 모든 검체를 수집한 후 RF 및 antifila- ggrin antibody 검사를 위해 -70℃에 보관하였다. RF 정 량검사는 latex fixation test 원리로 Hitachi 7170 (Hi- tachi Co, Tokyo, Japan)으로 검사하였고, antifilagg- rin antibody 검사는 anti-citrullinated filaggrin ELI- SA kit (MBL Co., Nagoya, Japan)을 사용하였으며 microplate ELISA방법에 의한 효소면역 분석기기 MPR- A4iⅡ (Tosoh, Tokyo, Japan)를 이용하여 시행하였다.
Antifilaggrin antibody 검사의 원리는 혈청 중의 fila-
ggrin 항체를 검출하는 것으로 recombinant human cit-
rullinated filaggrin이 코팅된 microwell에 검체를 분주
한 후 고정된 anti-citrullinated filaggrin antibody를
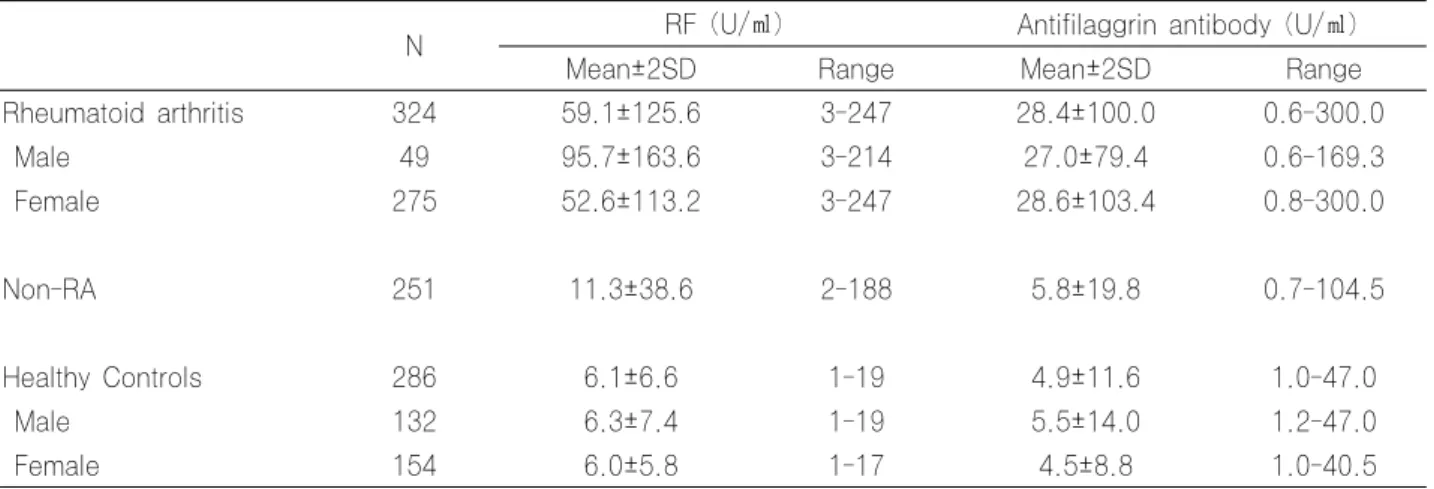
Table 2. Results of rheumatoid factor and antifilaggrin antibodies among the patients with or without rheumatoid arthritis and healthy controls
N RF (U/㎖) Antifilaggrin antibody (U/㎖)
Mean±2SD Range Mean±2SD Range
Rheumatoid arthritis 324 59.1±125.6 3-247 28.4±100.0 0.6-300.0
Male 49 95.7±163.6 3-214 27.0±79.4 0.6-169.3
Female 275 52.6±113.2 3-247 28.6±103.4 0.8-300.0
Non-RA 251 11.3±38.6 2-188 5.8±19.8 0.7-104.5
Healthy Controls 286 6.1±6.6 1-19 4.9±11.6 1.0-47.0
Male 132 6.3±7.4 1-19 5.5±14.0 1.2-47.0
Female 154 6.0±5.8 1-17 4.5±8.8 1.0-40.5
Abbreviations: Non-RA, disease other than rheumatoid arthritis;RF, rheumatoid factor;
SD, standard deviation.
효소표지된 항체와 반응시켜 발색시킨 후 450nm에서 흡광 도를 측정하는 것이다. 본 연구는 류마티스 관절염 환자와 대조환자군을 대상으로 antifilaggrin antibody 및 RF 검 사를 시행하여 남여에서의 분포 및 분별한계치에 따른 진단 적 민감도 및 특이도를 평가하였다. 분별한계치 설정은 286명의 건강대조군을 대상으로 3SD를 벗어나는 경우는 제외하고 95% 신뢰구간에서 얻은 평균+2SD를 적용하여 구하였다. 진단 정확도의 비교는 receiver operator cha- racteristics (ROC) curve를 이용하여 분석하였다. Anti- filaggrin antibody 검사는 microwell마다 음성 및 양성 대조 물질을 같이 검사하여 허용 범위 내에 있는 것을 확인 후 모든 결과를 얻었다.
3. 통계
통계처리는 SPSS version 11.0 (SPSS, Chicago, USA) 프로그램을 사용하였다. 환자군에서 평균값의 비교 는 Mann Whitney U test로 분석하였고, antifilaggrin antibody와 RF 검사의 비율 비교는 chi-square test로, ROC curve는 MedCalc software (Mariakerke, Bel- gium)로 처리하였다. 모든 분석 결과는 P value가 0.05 이하인 경우 유의하다고 판정하였다.
결 과
1. 건강 대조군에서의 antifilaggrin antibody 및 RF 검사 결과
건강 대조군은 총 286명으로 남자는 132명, 여자는 154명이었고, 연령은 평균 50.4 (16-72)세 이었고, anti- filaggrin antibody는 1.0-47.0 U/ml (평균±2SD, 4.9±
11.6 U/ml)의 값을 보였고, RF는 1-19 U/ml (6.1±6.6 U/ml)의 값을 보였다(Table 2). 건강대조군 중 antifi-
laggrin antibody 검사 양성은 21예로 7.3%로 나타났다.
2. 환자군에서 antifilaggrin antibody 및 RF 검사의 측정 결과
류마티스 관절염 환자 324명 중 남자는 49명, 여자는
275명으로 남, 여 비율은 1:5.6 이었으며, antifilaggrin
antibody는 0.6-300 U/ml (28.4±100.0 U/ml)의 값을
보였고 남(27.0±79.4 U/ml) 여(28.6±103.4 U/ml)간의
평균값의 차이는 없었다(P=0.723) (Table 2). 대조환자
군에서는 0.7-104.5 U/ml (5.8±19.8 U/ml)의 값을 보
였다. 류마티스 관절염 환자에서 RF는 3-247 U/ml
(59.1±125.6 U/ml)의 값을 보였고 남자에서 평균값
(95.7±163.6 U/ml)이 여자(52.6±113.2 U/ml)보다 높
아 남여 간 평균값의 유의한 차이가 있었다(P=0.009). 대
조환자군에서는 2-188 U/ml (11.3±38.6 U/ml)의 결과
를 나타냈다. 324예의 류마티스 관절염 환자중 131예가
antifilaggrin antibody 양성/RF 양성이었고, antifila-
ggrin antibody 양성/RF 음성이 14예, antifilaggrin
antibody 음성/RF 양성이 112예, antifilaggrin antibo-
dy 음성/RF 음성이 67예 이었다(Table 3). 류마티스 관
절염 환자에서 RF 음성 환자 중 antifilaggrin antibody
검사의 양성율은 분별한계치 9.6 U/ml에서 대상 환자 81
예중 14예가 antifilaggrin antibody 검사 양성을 보여
17.3% 양성율을 보였다(Table 3). 251예의 대조환자군중
13예가 antifilaggrin antibody 양성/RF 양성이었고,
antifilaggrin antibody 양성/RF 음성이 14예, antifila-
ggrin antibody 음성/RF 양성이 29예, antifilaggrin
antibody 음성/RF 음성이 195예 이었다(Table 3). An-
tifilaggrin antibody 위양성을 보인 예는 27예로 각각 베
제씨 질환 1예, 섬유근육염증 3예, 통풍 1예, 소아기 류마
티스 관절염 4예, 골관절염 10예, 척추관절염 1예, 루푸스
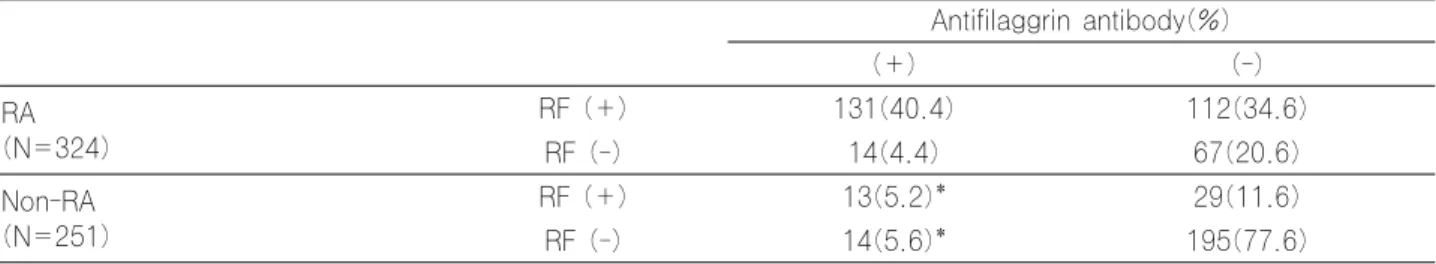
Table 3. Test results at optimal cut off values for the antifilaggrin antibody and rheumatoid factor in patients with or without rheumatoid arthritis
Antifilaggrin antibody(%)
(+) (-)
RA (N=324)
RF (+) 131(40.4) 112(34.6)
RF (-) 14(4.4) 67(20.6)
Non-RA (N=251)
RF (+) 13(5.2)* 29(11.6)
RF (-) 14(5.6)* 195(77.6)
Abbreviations: See Table 2.
*Diseases of antifilaggrin antibody (+) : Behcet's disease(N=1), fibromyalgia(N=3), gout(N=1), juvenile rheu- matoid arthritis(N=4), osteoarthritis(N=10), spondyloarthritis(N=1), systemic lupus erythematosus(N=6), and systemic sclerosis(N=1).
Table 4. Sensitivities and specificities of the antifilaggrin antibody and rheumatoid factor at optimal cut off values in the diagnosis for rheumatoid arthritis
Sensitivity(%) Specificity(%)
Antifilaggrin antibody 44.8 89.2
RF 75.0 83.3
Antifilaggrin antibody and RF 40.4 94.8
Antifilaggrin antibody or RF 79.3 77.6
Fig. 1. Receiver operator characteristics (ROC) curves of antifilaggrin antibody by ELISA and RF latex fixation test in patients with and without rheumatoid arthritis (P=0.000).
RF(Area=0.833)
Antifilaggrin antibody(Area=0.750)
0 20 40 60 80 100
100-Specificity 100
80
60
40
20
0
Sensitivity