Vol. 40, No. 1, March 2014, 1-10 http://dx.doi.org/10.15230/SCSK.2014.40.1.1
라만 분광 피부 측정기를 이용한 기능성 화장품 성분의 in vivo 피부 투과 측정 및 in vitro 비교 평가 연구
전 세 림*⋅한 민 희**⋅정 대 균*,**⋅황 재 성*,**†
*경희대학교 생명공학원, **피부생명공학센터
(2013년 8월 5일 접수, 2013년 8월 14일 수정, 2013년 9월 8일 채택)
The Study on the Skin Penetration of Cosmetic Ingredient with in vivo Raman Spectroscopy and in vitro Franz Cell
Serim Jeon*, MinHeeHan**, DaeKyunChung*,**, and JaeSungHwang*,**†
*Graduate School of Biotechnology, Kyung Hee University, Yongin, Korea
**Skin Biotechnology Center
(Received August 5, 2013; Revised August 14, 2013; Accepted September 8, 2013)
요 약: 현재, 기능성 화장품 성분의 피부흡수에 대한 연구 보고가 부족하며, 인체에서의 in vivo 피부 흡수는 거의 보고된 바 없다. 본 연구에서는 in vivo 라만 분광 피부 측정기를 이용하여 대표적 기능성 화장품 8종 성분 의 인체 표피 투과 데이터를 수집 및 분석하고, 이를 in vitro결과와 비교하여 주요 성분의 피부 흡수 자료를 확보하였다. 그리고 본 연구에 사용한 성분의 피부 투과도 측정한 결과를 보면, in vitro 평가에서 ascorb- yl-2-glucoside, retinol, retinyl palmitate, 그리고 kojic acid가 우수한 피부 투과율을 보였으며, in vivo 평 가에서는 retinol, vitamin C, 그리고 arbutin 이 우수한 것으로 나타났다. 반면, In vitro 평가와 in vivo 평가에 서 가장 우수한 투과율을 보인 성분은 각각 ascorbyl-2-glucoside와 retinol이었다. 이러한 차이점은 in vitro 평가의 경우 무모생쥐 모델의 피부를 모두 관통하는 물질을 평가하였고, 라만 분광 피부 측정기의 경우는 표피의 각질층을 평가하였으므로 물질의 특성에 따라서 표피 및 진피층의 영향에 민감할 수 있기 때문인 것으로 판단된 다. 그리고 대부분 물질의 투과 장벽은 각질층이므로 각질층에서 물질 이동을 살펴보는 것이 의미 있다고 생각된 다. 결론적으로, 본 연구에서는 라만 분광 피부 측정기를 이용하여 대표적 기능성 화장품 성분의 피부 흡수에 대한 기초적인 자료를 확보하였으며, 따라서 이들 자료는 추후 많은 연구에 활용될 수 있을 것으로 생각된다.
Abstract: At present, there are few research papers on skin penetration of cosmeceutical ingredients. What is worse is that in vivo studies are hard to find. In this study, we measured skin epidermal penetration of cosmeceutical ingredients using in vivo Raman spectroscopy and compared with the results obtained from experiments using in vitro franz cell.
Results showed that ascorbyl-2-glucoside, retinol, retinyl palmitate, and kojic acid were good for penetration ratio in measurement in vitro and retinol, vitamin C, and arbutin were good in measurement in vivo. Among them, retinol was best in skin penetration in vivo experiment using Raman spectroscopy and ascorbyl-2-glucoside was best in skin pene- tration in vitro experiment using Franz cell system. It is estimated that the differences were originated from the ex- perimental procedures of two different methods; in vivo Raman experiment can be sensitive to the effect of epidermis and dermis as characteristics of matter by estimating the stratum corneum and in vitro measurement is evaluation of material to penetrate skin of hairless mouse. However, most penetration barrier is the stratum corneum, thus it is im- portant to examine movement of material in the stratum corneum. We expect that these results provided useful in-
1)
† 주 저자 (e-mail: [email protected])
formation for many cosmetic related research.
Keywords: Skin penetration, in vivo, raman, franz cell, functional cosmetic ingredients
1. 서 론
피부에는 물질의 투과에 강력한 장벽인 각질층이 존 재하며[1], 피부 내에서 투과된 물질이 대사 되는 등 유 효성분이 작용부위인 세포층에 도달하는 농도가 적어 도포된 물질의 효과를 정확히 파악하기 위해서는 물질 의 피부 투과도를 정확히 파악하는 것이 중요하다.
유효성분의 피부 투과도는 물리 화학적 특성(pKa, 분자량, 안정성, 피부 내에서 결합특성, 용해도 분배계 수), 피부의 두께 및 구성요소, 피부 내 대사특성, 적용 부위, 적용시간, 피부투과, 제형 및 피부 내에 축적되 는 정도에 따라서 영향을 받는다. 기능성 화장품의 유 효성분이 높은 피부 흡수도를 가지기 위한 바람직한 물리화학적 특성은 분자량이 500 Da 이하인 분자, 분 배계수(Log octonol/water)가 1 - 3 사이, 용융점이 200
℃ 이하, 적당한 수용성(> 1 mg/mL), 분자 구조 내에 극성인 부분이 최소화인 분자와 같다[2].
기능성 화장품의 신 기능성 유효성분으로 광고되고 있는 효소, 펩타이드, 유전자, 단백질 등의 성분은 대 부분 수용성이고, 분자량이 크며, 분자 구조 내에 극 성인 부분이 대부분이어서 바람직한 피부 흡수도를 기대할 수 없는 물질들임을 고려 시, 재현성이 높고 간편한 피부 흡수도 평가법의 확립이 절실히 요구된 다. 화장품이 고 기능성으로 진화하면서, 소비자의 신 뢰와 안전에 대한 기대도 증대하고 있음에 따라 제품 의 성분 중 피부에 효과적인 성분은 가능한 피부 속으 로 침투시키고, 불필요한 성분은 가능한 피부 바깥에 서 머물 수 있기를 원한다. 화장품에는 이와 같은 선 택적 투과성이 요구될 것이며, 경피 흡수 연구의 중요 성은 나날이 증대되고 있다[3].
피부흡수도 평가에 크게 영향을 미치는 실험동물의 피부 흡수도 실험 치와 사람 피부의 피부흡수도의 연 관성 평가 확립과 체내와 체외 실험치의 연관성 지수 설정(in vivo와 in vitro 상관 인자)에 대한 자료가 보충 된 개선된 과학적 평가법 개발이 절실히 요구된다.
화장품에서 피부흡수 시험법은 전신순환계에 도달 을 목적으로 하는 의약품의 피부투과도 평가와는 달
라야 하며 기능성화장품(미백, 주름개선)의 작용부위 는 피부 세포로, 유효성분의 피부층으로의 흡수를 평 가하는 기술 개발이 필요하다. 현재 국내에서는 franz cell을 이용한 경피 투과기술은 있으나, in vivo 피부 흡수 측정은 전무한 상태이다.
라만 분광 피부 측정기는 기존의 in vivo 피부 흡수 측정법과는 달리 빛의 산란현상을 기초로 하여 피부 표면으로부터 수백 µm 아래까지 피부의 분자조성에 관한 정보와 피부 깊이에 따른 물질 투과도를 피부 손 상 없이 광학적인 방법으로 얻을 수 있다[4]. 이것은 산란 현상이 일어날 때 입사한 빛과 물질 사이에 상호 작용이 생기면서 에너지의 교환이 생겨 물질 분자 구 조에 따라 변하는 진동 에너지를 감지하는 원리이다 [5,6]. 물질마다 구성하는 분자구조가 다르고 피부 깊 이에 따라 분자조성이 다르기 때문에 측정을 원하는 물질을 피부에 도포한 후 라만 분광 피부 측정기를 이 용해 계측하면 특정한 파장에서 원하는 물질의 peak 를 발견할 수 있고, 이것을 토대로 특정 파장에서 피 부 깊이에 따른 물질의 투과도를 알 수 있다. 현재, 기 능성 화장품 성분의 피부흡수에 대한 연구 보고가 부 족하며, 인체에서의 in vivo 피부 흡수는 거의 보고된 바 없다. 따라서 본 연구에서는 in vivo 라만 분광 피부 측정기를 이용하여 기능성 화장품 성분의 인체 표피 투과 데이터를 수집, 분석하여 추론하고, 이를 in vitro 결과와 비교하여 라만 분광 피부 측정기의 응용가능 성을 확인하고, 주요 성분의 피부 흡수 자료를 확보하 고자 한다.
2. 재료 및 실험
2.1. in vitro 표준품(Standard compound) 및 매개체 (Vehicle)
시험물질에 따른 농도는 retinol (Sigma, USA), ret- inyl palmitate (Sigma, USA), kojic acid (Sigma, USA), arbutin (Sigma, USA), ascorbyl glucoside (Sigma, USA), niacinamide (Sigma, USA), vitamin C (Sigma, USA), ad- enosine (Sigma, USA)을 100 ppm 농도로 제조하였다.
Solvent Detector Retinol
Retinyl palmitate
100% ACN, 1.0 mL/min
100% ACN, 2.0 mL/min UV at 325 nm
Adenosine A: 20 mM Potassium phosphate / B: ACN
B 0% (0 min) → B 15% (15 min) UV at 254 nm Ascorbyl glucoside
Vitamin C
A: 20 mM Potassium phosphate / B: ACN
B 0% (0 min) → B 10% (10 min) UV at 260 nm Arbutin Kojic acid
Niacinamide
A: 20 mM Potassium phosphate / B: ACN
B 0% (0 min) → B 15% (15 min) UV at 220 nm Table 1. Conditions for HPLC Analysis
지용성 성분인 retinol, retinyl palmitate의 경우, pro- pylren glycol (Sigma, USA) : ethanol (DAEJUNG, Korea)
= 3 : 7의 비율로 한 용매를 만들어 사용하였고, 용출 액은 5% tween 80이 포함된 Phosphate Buffered Saline (PBS)를 이용하였다. 반면 ascorbyl glucoside, kojic acid, adenosine, vitamin C, niacinamide, arbutin과 같은 수용성 성분의 경우, propylren glycol : water = 5 : 5의 비율로 한 용매를 만들어 사용하였고, 용출액은 PBS 를 이용하였다.
시험물질에 따른 농도는 0.075% retinol, 0.3% retinyl palmitate, 2% ascorbyl glucoside, 1% kojic acid, 0.04 % adenosine, 2% vitamin C, 3% arbutin, 2% niacinamide 로 제조하였다.
2.2. In vitro 피부 흡수 실험
본 실험에서는 Microette Plus 자동피부 투과기 (Hanson Research, USA)를 이용했다. 피부 투과 실험 을 위해 6주령 수컷 쥐의 복부 부위를 피하조직까지 잘라 적출하고 -20 ℃에서 보관하였다. 수용성 성분 투과 실험의 경우 vertical-type diffusion cell에 PBS를 용출액으로 채웠고, 지용성 성분 투과 실험의 경우 5% tween 80이 포함된 PBS를 용출액으로 사용하였다.
적출된 피부조직은 세포의 수용기 부분에 얹고 공여 체 부분을 조립 후 시험물질을 1 mL 도포했다. 시험 물질 도포 직후를 0 h으로 하여 12, 24, 48, 72 h 경과 후 용출액을 채취하였으며 adenosine, vitamin C의 경 우 96 h, 120 h 경과 후, arbutin, niacinamide의 경우 36 h, 60 h 에 용출액을 추가로 채취하였다. 이때 용액의 온도는 피부 내 온도와 같은 32.5 ℃를 유지하였으며, 시간대별로 채취된 용출액은 high performance liquid
chromatography-ultraviolet (HPLC-UV) 분석을 통해 함 량 및 micrograms/sq.cm의 용출양을 계산하였다.
2.3. in vitro 분석조건
본 실험에 사용된 기기는 Agilent Technologies 1200 Series (Agilent technologies, USA)이다. 사용된 칼럼은 Shiseido Capcell pak C18 250 × 4.6 mm, 5 µm을 공통 으로 사용하였으나, 지용성 성분과 수용성 성분을 구 분해서 사용하였다. 칼럼의 온도는 40 ℃를 유지하였 고 10 µL 를 주입하였다. 시약 및 용매는 특급시약 및 HPLC grade를 사용하였고, 시료 분석을 위해 사용된 기기 조건은 다음과 같다(Table 1).
2.4. In vivo 시험액의 조제
지용성 성분인 retinol, retinyl palmitate의 경우, pro- pylren glycol : ethanol = 3 : 7로 섞은 것을 용매로 하 여 녹여 사용하였으며, ascorbyl glucoside, kojic acid, vitamin C, niacinamide, arbutin과 같은 수용성 성분의 경우, propylren glycol : water = 5 : 5로 섞은 것을 용매 로 하여 녹여 사용하였다. 모든 시험액은 0.1%로 조제 하여 사용하였다. Adenosine 은 고농도로 시험액을 만 들어도 라만 스펙트럼이 잡히지 않아 분석을 할 수 없 었기에 제외하였다. In vitro 평가 시험에서 시험액의 농도는 화장품기능성 허가 요건을 기준으로 현재 제 품에 상용되는 농도를 기준으로 하였고, in vivo 평가 에서는 라만 분광 피부 측정기를 이용한 보고된 자료 가 없어서 모두 0.1%로 통일하여 in vivo 흡수도를 상 대 비교하고자 하였다.
(A)
(B)
(C)
(D)
(E)
(F)
(G)
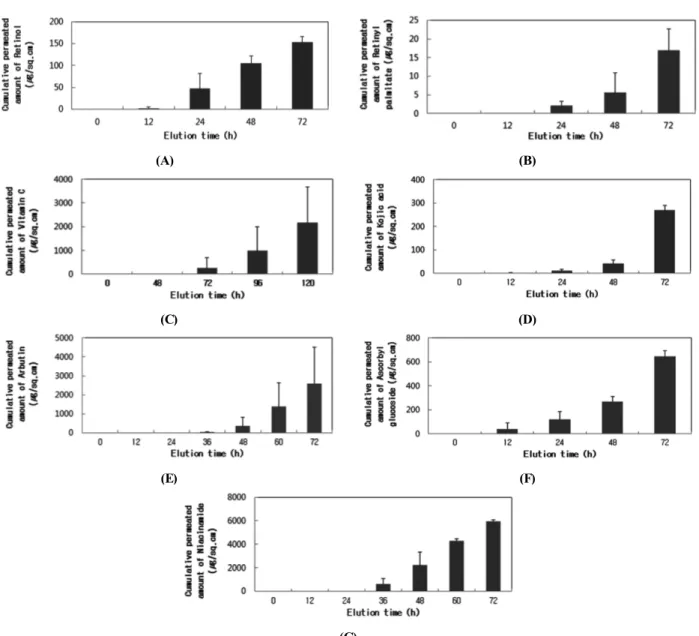
Figure 1. Cumulative permeated amount of 7 cosmeceutical ingredients with time. (A) retinol, (B) retinyl palmitate, (C) vitamin C, (D) kojic acid, (E) arbutin, (F) ascorbyl glucoside, (G) niacinamide.
2.5. 라만 분광 피부측정기
물질 투과율 측정 시 인간의 피부를 in vivo 상에서 비 침윤적으로 측정할 수 있는 Skin Composition Analyzer (model 3510 SCA, River Diagnostics, Netherlands)을 이 용하였다. 이것은 라만 스펙트럼의 high wavenumber region (2,400 - 4,000 cm-1)와 fingerprint region (400 - 2,400 cm-1)이라 불리는 영역을 각각 671 nm, 785 nm 레이저를 이용해 측정한다[5]. 피부에 대한 레이저 출 력값은 671 nm는 10 ~ 20 mW, 785 nm는 20 ~ 30 mW를 유지해야 하고, 피험자의 피부를 측정하기 전에
교정을 시행하여 상관 계수 값이 0.99, S/N fingerprint 값이 25 이상인지 확인한다. 물질의 피부 투과도는 피 부 구성요소인 keratin의 함량으로 상대적인 값으로 나 타낸다[7].
2.6. in vivo 시험방법
시험은 항온항습 조건(온도: 22 ± 2 ℃, 습도: 40 ~ 60%)에서 진행하였으며, 시험 시작 전 15분 이상 피험 자들을 항온항습 조건이 유지되는 공간에서 안정화시 켰다.
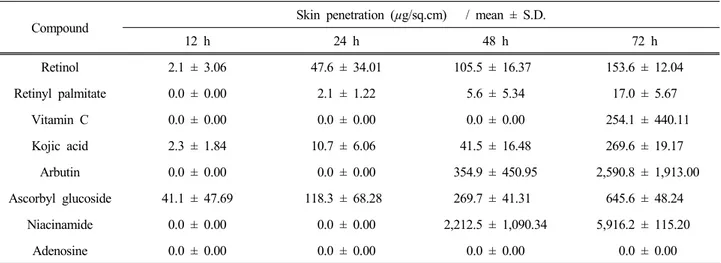
Compound Skin penetration (µg/sq.cm) / mean ± S.D.
12 h 24 h 48 h 72 h
Retinol 2.1 ± 3.06 47.6 ± 34.01 105.5 ± 16.37 153.6 ± 12.04
Retinyl palmitate 0.0 ± 0.00 2.1 ± 1.22 5.6 ± 5.34 17.0 ± 5.67
Vitamin C 0.0 ± 0.00 0.0 ± 0.00 0.0 ± 0.00 254.1 ± 440.11
Kojic acid 2.3 ± 1.84 10.7 ± 6.06 41.5 ± 16.48 269.6 ± 19.17
Arbutin 0.0 ± 0.00 0.0 ± 0.00 354.9 ± 450.95 2,590.8 ± 1,913.00
Ascorbyl glucoside 41.1 ± 47.69 118.3 ± 68.28 269.7 ± 41.31 645.6 ± 48.24 Niacinamide 0.0 ± 0.00 0.0 ± 0.00 2,212.5 ± 1,090.34 5,916.2 ± 115.20
Adenosine 0.0 ± 0.00 0.0 ± 0.00 0.0 ± 0.00 0.0 ± 0.00
Table 2. Cumulative Permeated Amount of 8 Cosmeceutical Ingredients with Time Measured by Franz Cell
Figure 2. The comparison of cumulative permeated amount of 8 cosmeceutical ingredients with time (12 h, 24 h, 48 h, 72 h).
피험자들은 알러지, 아토피 등 피부질환에 걸린 경 험이 없는 20 ~ 30대 여성으로 총 4명으로 구성되었으 며, 측정 당일 시험물질의 정확한 투과량을 조사하기 위해 스킨케어제품을 사용하지 않았다.
피험자의 하박부 내측에 4 × 5 cm2 측정부위를 표 시하고 초기 피부 상태를 라만 분광 피부 측정기를 사 용하여 측정한 후, 측정부위에 100 µL의 시험액을 흡 수시킨 4 × 5 cm2의 흡수지를 부착하고 30 min 동안 흡수시킨다. 측정은 시료 부착 후 30 min, 60 min 대에 실시하였으며, 라만 스펙트럼을 피부 깊이 4 µm 단위 로 40 µm까지 측정하고 분석하였다. 모든 측정 데이 터는 컴퓨터에 자동 저장되며 분석프로그램인 Skin Tools 2.0을 이용하여 각 시험물질의 피부 투과량을 arbitrary unit (AU)으로 계산하였다.
2.7. 통계처리
통계처리는 IBM SPSS statistics 20.0을 이용하였다.
3. 결과 및 고찰
3.1. In vitro 용출액의 함량 계산
실험에 사용된 8가지 표준품의 HPLC-UV 결과를 토대로 in vitro 피부 투과 실험을 통해 8가지 기능 물 질의 용출액을 0, 12, 24, 48, 72 h 경과 후 채취하였으 며 adenosine은 72 h에도 용출액이 검출되지 않았고, vitamin C의 경우 72 h 이후부터 용출액이 검출되었으 므로 96 h, 120 h까지 용출액을 채취해 장시간 경과 후
피부 투과 정도를 추가로 확인하였다.
Arbutin, niacinamide의 경우 48 h 이후부터 용출액 이 검출되었으므로 48 h 전, 후 12 h 간격으로 확인하 기 위해 36 h, 60 h에 용출액을 추가로 채취해 용출 간격이 짧을 때의 투과 정도를 확인하였다. In vitro 피부 투과 실험을 통해 기능성분의 피부 흡수 정도는 시간에 따라 모두 증가됨을 확인하였으나, adenosine 은 120 h까지 피부 투과가 이루어지지 않은 것으로 관찰되었다.
피부 투과 실험을 통해 시간대별로 채취된 용출액 을 µg/sq·cm로 나타낸 결과 adenosine을 제외하고 모 든 용출액이 시간이 지남에 따라 피부 흡수가 증가하 는 것으로 관찰되었고(Figure 1), 이 결과는 Table 2와
(A) 0.1% retinol
(B) 0.1% retinyl palmitate
(C) 0.1% vitamin C
(D) 0.1% kojic acid
(E) 0.1% arbutin
(F) 0.1% ascorbyl glucoside
(G) 0.1% niacinamide
Figure 3. Raman spectrum of 7 cosmeceutical ingredients. (A) 0.1% retinol, (B) 0.1% retinyl palmitate, (C) 0.1% vitamin C, (D) 0.1% kojic acid, (E) 0.1% arbutin, (F) 0.1% ascorbyl glucoside, (G) 0.1% niacinamide.
같았다. Table 2에서는 생략되었지만 vitamin C를 96 h, 120 h에 채취한 결과 각각 985.7 ± 1,012.28 (mean
(A)
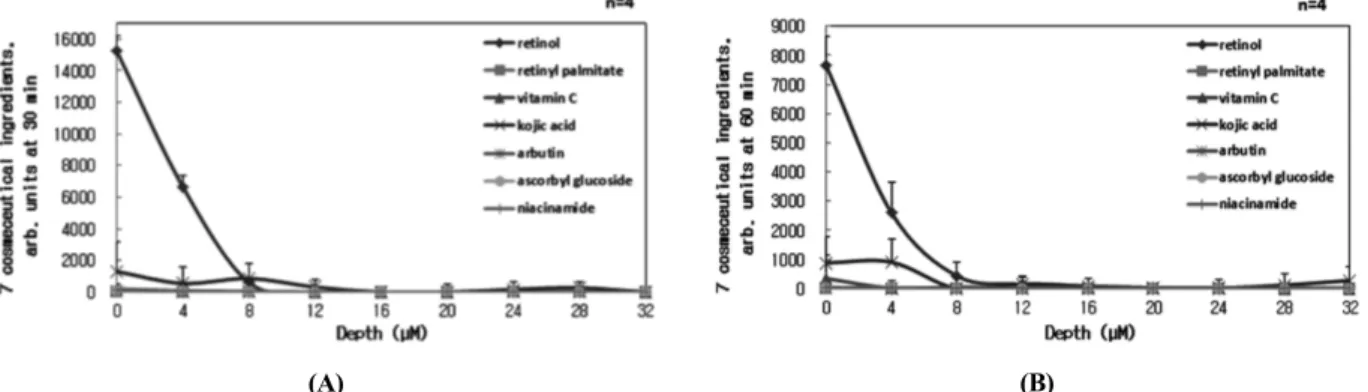
(B)
Figure 4. Skin penetration content (arbitrary unit) for 7 cosmeceutical ingredients with skin depth with time. (A) After 30 min, (B) After 60 min.
Depth (micron)
Compound
Retinol Retinyl palmitate Vitamin C Kojic acid Arbutin Ascorbyl glucoside Niacinamide 0 15265.77 ± 924.19 0.1467 ± 0.07 195.14 ± 331.01 1308.54 ± 1871.49 44.70 ± 64.28 45.49 ± 431.33 130.64 ± 166.14 4 6680.45 ± 701.80 0.0586 ± 0.02 82.84 ± 217.31 557.34 ± 1025.80 23.00 ± 35.36 32.40 ± 407.48 33.31 ± 44.65 8 615.74 ± 221.26 0.0090 ± 0.01 38.52 ± 67.18 866.52 ± 954.47 0.00 ± 18.13 13.91 ± 159.29 0.00 ± 0.00 12 0.00 0.0016 ± 0.00 3.64 ± 47.15 322.58 ± 440.52 0.77 ± 16.83 13.03 ± 210.99 0.71 ± 0.82 16 0.00 0.0005 ± 0.00 0.00 ±10.67 0.00 ± 202.51 0.00 ± 14.61 4.66 ± 79.71 8.47 ± 11.92 20 0.00 0.00 0.00 ± 10.83 0.00 ± 477.25 0.00 ± 3.94 4.18 ± 41.74 6.85 ± 19.97 24 0.00 0.00 35.38 ± 63.56 174.85 ± 470.57 0.00 ± 2.92 6.14 ± 66.01 4.66 ± 18.43 28 0.00 0.00 52.49 ± 90.21 275.60 ± 344.65 0.10 ± 4.69 4.17 ± 68.69 6.16 ± 11.68
32 0.00 0.00 9.90 ± 0.00 0.00 3.17 ± 8.40 5.24 ± 39.31 6.82 ± 10.78
Total content
(AU) 22561.96 ± 1404.73 0.22 ± 0.07 417.92 ± 814.85 3505.44 ± 2106.60 71.74 ± 147.29 129.22 ± 1184.95 197.62 ± 197.21 Table 3. Skin Penetration Content (AU) of 7 Cosmeceutical Ingredients After 30 min Measured by Raman Spectroscopy
± S.D.) µg/sq·cm, 2,173.2 ± 1,492.48 µg/sq·cm이었 고, arbutin의 경우 36 h, 60 h에서 각각 22.1 ± 16.37 µg/sq·cm, 1,372.4 ± 1,258.89 µg/sq·cm, niacinamide 은 36 h, 60 h에서 각각 610.4 ± 456.98 µg/sq·cm, 4,297.9 ± 161.01 µg/sq·cm이었다.
실험에 사용된 8가지 기능 물질에서 공통적으로 채 취한 12 h, 24 h, 48 h, 72 h에서의 용출양을 비교한 결 과, 8가지 기능성분 중 가장 높은 피부 투과도를 보인 성분은 12 h을 기준으로 ascorbyl glucoside, kojic acid, retinol 순으로 확인되었고, 24 h에서는 ascorbyl gluco- side, retinol, kojic acid, retinyl palmitate 순으로 확인되 었다(Figure 2). niacinamide, arbutin, vitamin C, ad- enosine은 24 h까지 피부 투과가 이루어지지 않은 것
으로 관찰되었다. 48 h 이후의 용출량을 비교했을 때 는 niacinamide, arbutin, vitamin C에서 상대적으로 많 은 투과도를 보이지만, 이는 용출 시간이 길어져 피부 가 손상되어 급격한 용출이 일어난 것으로 사료된다.
따라서 적출된 피부가 경피 제제와 용출액에 장시 간 접촉되었을 때 피부 손상 여부에 대한 연구가 추후 이루어질 필요가 있다고 생각된다. 물질에 따라 시간 별로 채취한 용출양의 오차범위가 큰 것은 in vitro 피 부 투과 실험의 특성상 적출된 피부의 컨디션 및 두께 차이로 인한 변동이 크기 때문인 것으로 생각된다. 따 라서 실험군의 수를 늘려 오차범위를 줄이는 것이 필 요할 것으로 생각된다.
Depth (micron)
Compound
Retinol Retinyl palmitate Vitamin C Kojic acid Arbutin Ascorbyl glucoside Niacinamide 0 7664.54 ± 999.70 0.1247 ± 0.06 350.87 ± 810.25 882.10 ± 890.91 25.03 ± 51.58 19.17 ± 345.26 47.02 ± 54.78 4 2601.47 ± 1034.48 0.0716 ± 0.04 17.79 ± 66.58 910.30 ± 776.79 5.72 ± 23.16 13.92 ± 249.92 22.04 ± 33.48 8 435.62 ± 480.54 0.0046 ± 0.01 57.55 ± 7.67 0.00 ± 186.33 0.00 ± 4.61 0.00 ± 65.11 0.00 12 144.31 ± 249.96 0.00 23.90 ± 30.15 165.15 ± 270.23 0.00 ± 7.62 0.00 ± 46.36 0.98 ± 1.96 16 0.00 0.0002 ± 0.00 10.75 ± 26.22 88.29 ± 269.89 0.00 ± 4.03 1.88 ± 43.82 0.00 ± 4.30 20 0.00 0.0002 ± 0.00 27.00 ± 16.21 30.82 ± 63.75 0.00 ± 2.51 3.84 ± 26.21 0.00
24 0.00 0.00 14.22 ± 21.09 18.51 ± 299.23 0.00 ± 0.70 6.15 ± 37.47 0.00
28 0.00 0.0001 ± 0.00 1.01 ± 31.43 123.71 ± 400.93 0.00 ± 2.14 4.77 ± 45.22 0.00 ± 5.57 32 0.00 0.0002 ± 0.00 0.00 ± 44.22 281.25 ± 444.19 0.00 ± 1.63 5.08 ± 28.62 0.98 ± 12.25 Total content
(AU) 10845.94 ± 1542.86 0.20 ± 0.11 503.09 ± 866.13 2500.14 ± 1000.50 30.76 ± 77.83 54.81 ± 714.92 71.01 ± 56.02 Table 4. Skin Penetration Content (AU) of 7 Cosmeceutical Ingredients After 60 min Measured by Raman Spectroscopy
Compound Content (AU)
30 min 60 min
Retinol 22561.96 ± 1404.73 10845.94 ± 1542.86 Retinyl palmitate 0.22 ± 0.07 0.20 ± 0.11
Vitamin C 417.92 ± 814.85 503.09 ± 866.13 Kojic acid 3505.44 ± 2106.60 2500.14 ± 1000.50
Arbutin 71.74 ± 147.29 30.76 ± 77.83 Asccorbyl glucoside 129.22 ± 1184.95 54.81 ± 714.92
Niacinamide 197.62 ± 197.21 71.01 ± 56.02 Table 5. Summary of Skin Penetration Content (AU) 3.2. 각 시험물질의 in vivo raman spectrum
각 시험물질의 라만 스펙트럼을 알아보기 위해 785 nm를 이용해서 fingerprint region (400 - 2,400 cm-1)을 4 µm 단위로 40 µm까지 측정하였다. 각 시험물질을 측정해서 얻은 peak들은 특정 부분(raman shift cm-1)에 서 확인할 수 있었다(Figure 3).
3.3. 각 시험물질의 in vivo 시간대별 피부 투과량 각 시험물질을 피부에 흡수시킨 30 min 후에 물질 의 피부 투과량을 측정한 결과 Figure 4와 같았다. 가 장 높은 피부 투과율을 보인 물질은 retinol이었고, koj- ic acid, vitamin C, niacinamide, ascorbyl glucoside, arbu- tin, retinyl palmitate 순으로 투과율이 높았다(Figure 4A). 이것을 표피 층별 피부 투과량으로 나타낸 결과 Table 3과 같다.
물질 도포 60 min 후 피부 투과량 측정결과는 30 min 후에 측정한 결과와 동일하게 retinol이 가장 높은 투과율을 보였으며, kojic acid, vitamin C, niacinamide, ascorbyl glucoside, arbutin, retinyl palmitate순이었다 (Figure 4B). 표피층별 피부 투과량으로 나타낸 결과 Table 4와 같다. Retinol이 30 min, 60 min에서 투과율 이 높지만 피부층 12 µm 이후 검출되지 않았는데, 이 것은 투과율이 빨라 표피의 각질층 상단부에서 물질 투과가 다 이루어진 것으로 추측된다. 그래프는 각 측 정 시간대에서 물질 도포하기 전 피부의 기본값을 뺀
값으로 그렸다.
3.4. 각 시험 물질의 in vivo 시간대별 피부 총 투과량 각 물질의 시간대별(30 min, 60 min) 피부 투과량의 AU는 Table 5와 같다. 측정 결과 retinol에서 투과량의 차이가 가장 많이 나며, kojic acid, niacinamide, ascorb- yl glucoside, arbutin, retinyl palmitate, vitamin C 순으로 투과량 차이가 크게 나타났다(Figure 5, Table 6). 이러 한 차이는 30분 간 투과된 물질의 양으로 해석될 수 있다. 또한, 대부분의 물질은 30 min에서 피부 투과량 이 높게 나타났지만, vitamin C의 경우는 60 min에서 피부 투과량이 더 높게 나타났으므로 측정 시간대를
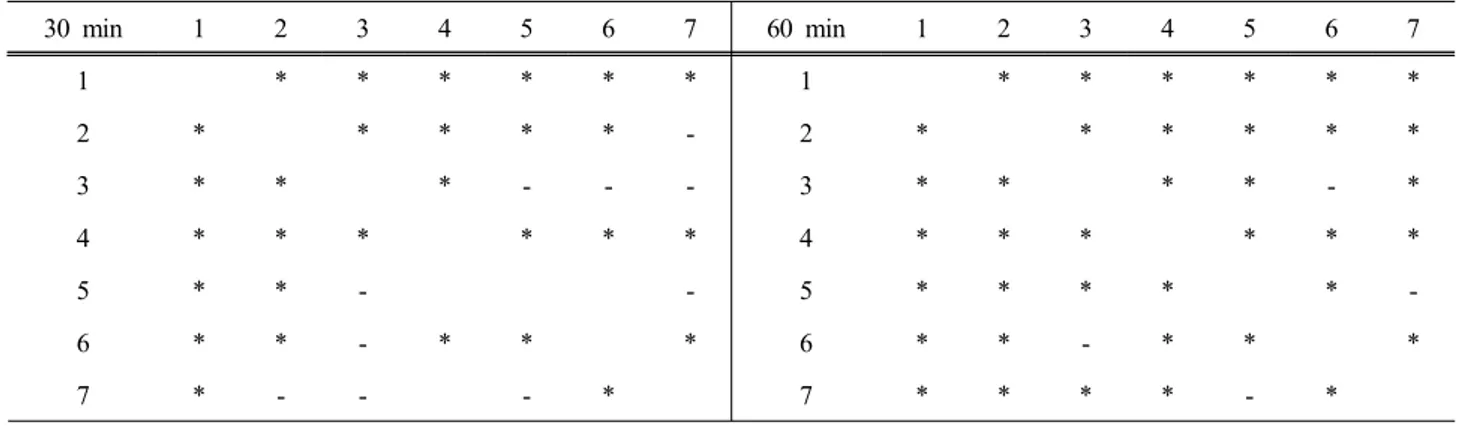
30 min 1 2 3 4 5 6 7 60 min 1 2 3 4 5 6 7
1 * * * * * * 1 * * * * * *
2 * * * * * - 2 * * * * * *
3 * * * - - - 3 * * * * - *
4 * * * * * * 4 * * * * * *
5 * * - - 5 * * * * * -
6 * * - * * * 6 * * - * * *
7 * - - - * 7 * * * * - *
( * P < 0.05, 1. Retinol, 2. Retinyl palmitate, 3. Vitamin C, 4. Kojic acid, 5. Arbutin, 6. Ascorbyl glucoside, 7. Niacinamide) Table 6. Statistical Analysis of in Vivo Skin Penetration of Test Compounds
Figure 5. The comparison of skin penetration content (arbitrary unit) for 7 cosmeceutical ingredients with time.
더 늘려서 확인을 하거나 농도를 달리 해봐야 할 필요 가 있을 것으로 생각된다.
4. 결 론
Franz cell을 이용한 평가와 라만 분광 피부 측정기 를 이용한 평가에서 유사성과 차이점을 볼 수 있었다.
우선 in vitro 평가에서 투과율이 우수한 물질은 as- corbyl glucoside, retinol, retinyl palmitate, kojic acid였으 며, in vivo 평가에서는 retinol, kojic acid이었다. 공히 두 가지의 시험에서 retinol은 투과율이 우수한 물질로 나타났다. Adenosine의 경우는 in vitro에서는 전혀 흡 수되지 않은 것으로 나타났고, in vivo에서는 라만 분 광을 볼 수 없어 측정이 불가하였다. In vitro 평가에서 는 ascorbyl-2-glucoside가 가장 우수한 투과율을 보였 고, 반면 in vivo 평가에서는 retinol이 가장 우수한 투 과율을 보였다.
두 가지 측정 결과 나타나는 차이점은 몇 가지의 원
인에서 비롯되는 것으로 보여진다. 첫째, in vitro 평가 는 모무생쥐 모델의 피부를 모두 관통하는 물질을 평 가하는 것이고, 라만은 표피의 각질층을 평가하는 것 이므로 물질의 특성에 따라서 표피 및 진피층의 영향 에 민감할 수 있다. 둘째, Franz cell을 이용한 in vitro 평가는 물질이 장시간에 걸쳐 서서히 용출되므로 측 정시간을 길게 한 반면, 라만을 이용한 평가는 초기 in vitro와 동일하게 12 h, 24 h 등으로 측정하려 했으나, 측정 결과 물질이 검출되지 않아, 도포 후 단시간(30 min, 60 min) 내에 측정을 해야 했는데, 이는 라만은 표피의 각질층을 대상으로 하기 때문에 물질이 이미 피부로 침투되어버린 경우는 측정이 안되기 때문으로 추측되며 in vitro와 in vivo 두 측정간에 차이가 발생 했을 가능성이 있다고 생각된다.
전반적으로 라만 분광 피부 측정기를 사용한 live in vivo 피부 흡수평가는 사용된 물질들의 자료를 살펴 볼 때 상당히 신뢰성 있고, 의미있는 결과를 보여주었 다(Table 4). 대부분 물질의 투과 장벽은 각질층이므로 각질층에서의 거동을 살펴보는 것이 의미있다고 생각 되며, 추후 tape striping법에 의한 in vitro 각질 투과도 를 평가하여 비교 분석해 보는 것도 필요할 것으로 생 각된다.
결론적으로 in vivo 라만 분광 피부 측정기를 통해 향후 고기능성 제형 개발 및 피부에 대상 전달을 위한 자료 활용, 화장품 소재, 의약품 소재, 단백질, 펩타이 드 등 다양한 물질의 경피 흡수 자료 확보, 피부흡수 개선제 연구, 개선된 피부 흡수도 평가 시험법 확립 및 흡수 가이드라인 자료로 활용, 화장품의 피부 흡수
도 평가를 위한 과학적 평가 기술 확립, 고기능성 소 재 및 화장품의 유효성 및 안정성 평가를 위한 기반 평가 기술 제공, 기능성 화장품소재 및 제품의 피부 흡수 자료를 확립하는데 활용할 수 있을 것으로 생각 된다.
감사의 글
이 논문은 한국보건산업진흥원 글로벌코스메틱연구 개발사업단(과제번호 A103017) 및 Basic Science Research Program through the National Research Foundation of Korea (NRF) funded by the Ministry of Education, Science and Technology (NRF-2013R1A1A2007330) 에 의하여 지원 되었습니다.
Reference
1. A. V. Rawlings and C. R. Harding, Moisturization and skin barrier function, Dermatologic therapy, 17, 43 (2004).
2. F. Gorouhi and H. I. Maibach, Role of topical pep- tides in preventing or treating aged skin, Internatio- nal Journal of Cosmetic Science, 31, 327 (2009).
3. T. Okamoto, Research on percutaneous absortion of cosmetics, Fragrance Journal, 36(5), 33 (2008).
4. P. J. Caspers, G. W. Lucassen, H. A. Bruining1, and G. J. Puppels, Automated depth-scanning confocal Raman microspectrometer for rapid in vivo determi- nation of water concentration profiles in human skin, JOURNAL OF RAMAN SPECTROSCOPY, 31, 813 (2000).
5. P. J. Caspers, G. W. Lucassen, E. A. Carter, H. A.
Bruining, and G. J. Puppels, In Vivo Confocal Raman Microspectroscopy of the Skin: Noninvasive Determination of Molecular Concentration Profiles, Journal of Investigative Dermatology, 116, 434 (2001).
6. E. Mariko, H. Tetsuji, and T. Motoji, In vivo Estimation of Stratum Corneum Thickness from Water Concentration Profiles Obtained with Raman Spectroscopy, Acta. Dermato-Venereologica, 87, 4 (2007).
7. P. J. Caspers, G. W. Lucassen, R. Wolthuis, H. A.
Bruining, and G. J. Puppels, In vitro and in vivo Raman spectroscopy of human skin, Biospectroscopy,