임상병리검사과학회지
:제 30권 제 3호
1998.자궁경부 상피내 종양에서 언체 유두종바이러스의 검출
아주대학교병원 해부병리과 서 기 춘
Detection of Human Papillomavirus in Cervical Intraepithelial Neoplasia.
Seo, Ki Chun
Dept. 01 Anatomical Pathology,
A.ψu
University Hospita1.cervi덩1
carcinoma of the uterus is the rmst comrmn cancer of theKOfl않n
woræn, but its않rly det:f왜on ~th띠
is notJX뼈ùarized
yet. Recent rep::>rtsin이caκrl
humanpapilloma찌rus(HPV)
as one of them퍼or
factors tot뾰 devel따ænt
of the ærvical canær.1bis study is
perfom빼
to find out whether the epithelia of the uterine ærvix werei파ectfrl
by HPV or not by using an in situ K:R~thod.
None of the chronic
nonsκ~ific i며larrnnation(CNI)
case was {X)Sitive for HPV, but 23.3%cases of
ærvi떠1
intraepithelial neoplasia(CIN) grade 1 were JX)sitive by immunohistochemi-S따.
But the JX)sitive rates by in situ PCR were different: 76.29-6 in CNI cases and fJj.7%in CIN grade 1 cases. The JX)sitive cases of
mαe
than one HPV subty}æs(rl1Ìxed subtypesJX)sitive cases) which
inc1ucX최
a high risk group was 40 armng the tota1 51 cases(OOO/O) by in situ PCR~thod.
1bis finding suggest that HPV JX)sitive cases have a JX)ssibility tom맹ress
to an얹rly 떠nc앉.
1be rmst significant finding in this study was that CNIca뚱S
showed a high JX)sitive rate for HPV by in situ PCR
~thod.
1bis JX)sitive finding was usually detectfrl in the koilocytes ofærvi떠1
epithelium, although in 4 cases non-koilocytes were also JX)sitive.1bis study suggests that the DNA
않st
for HPV should be carried for the earlyde~tion
of the high-risk group of HPV infection. And these patients빠처
follow-up studyandfl멸ular exænina디on:
andthe않
efforts would contribute to the reduction of the ærvical canærs.Key Words : Uterine cervix. HPV. Immunohistochemistry. In situ-PCR
-238 -
1. 서
료등‘-
한국 여성에서 발생하는 암(떠nær) 중에서 빈 도 1 위를 차지하는 것은 자궁경부암(uterine
cervixcanær) 이다. 1%년(1%.
1 - 1%. 12)보건복지부 한국인 암등록 분석보고서에 의하면 등록된 자궁경부암이 6,W6명으로 전체 ?i3,7껴건 의 여성암 발생의 21. 1%를 차지하고 있다1) 이는 선진국에 비하여 월등히 높은 수준이다.
자궁경부암의 원인에 관한 역학적, 실험적 연구 에 의하면 성관계 특히 낮은 연령부터 시작된 성 접촉, 여러명과의 성접촉, 저112형 단순포진 바이러 스(he~s
simplex type II)및 인체 유두종바이 러스(Human
papilloma virus ; HPV)등이 자궁 경부암의 발생에 원인이 된다는 많은 보고들이 있다8,14,18,19.때1.21.Z3.l3) 그 중에서도 자궁경부암은 성 접촉성 감염증(않X뻐lly transmitt어
diseaseSTD)과 관련성이 높은 것으로 알려져 있다~) 성접촉성 감염증중에 자궁경부암의 원인 인자로 서 인체 유두종바이러스가 자궁경부암 발생에서 중요한 요인으로 주목되면서 이에 대한 연구가 활발히 진행되고 있다~1l
인체 유두종바이러스와 자궁경부암과의 관련성 에 대하여 관심을 갖게 된 동기는 1ffi3년에
Dürst등이 자궁경부암 조직에서 매'v
type 8, 9, 10,11의 DNA를 검출함으로서 시작되었다~)
자궁경부암의 원인으로 알려진 인체 유두종바 이러스는 1잃4년 Serra에 의해 분류되어진 이래,
1æ8년에는
Ogilvie와 Dunn이 전자현미경으로 상피세포의 핵안에서
viral며rticles의 존재를 확 인하였다. 최근에는 DNA의 상동관계 (Homology) 연구를 통하여 약 70여종 이상의 아형 (sub ~) 이 발견되었으며 15) 이 중 약 20여종의 아형이 자 궁경부암 등에서 발현되고æ) 자궁경부암의 전구 병소(precancerous lesion) 에서 높은 빈도로 출현 하는 것이 밝혀져 인체 유두종바이러스가 암 발 생에 관여한다는 사실이 명확해지고 있다. 여러 가지 임상연구 및 분자생물학적 연구에 근거하여 볼 때 인체 유두종바이러스는 성적인 접촉으로
감염, 전파되는 인자(agent)로서 자궁경부암 발생 에 관여하는 가장 중요한 요인으로 인정되고 있
다31.32)
생식기계에서 주로 발견되는 인체 유두종바이 러스는 그 병변의 특이성에 따라 자궁경부 상피 내 종양(
ærvical intraepithelial neoplasia ; CIN )및 자궁경부암(
uterine ærvix canær)에 주로 연관되어 검출되는 고위험군
(high risk group )과 주로 여성생식기의 양성병변(
begnign lesion)인 첨규형 콘딜로매 condylo때
acuminata)에서 검출되는 저위험군(low
riskgroup)으로 분류하고 있다.
암 발생 빈도가 높은 고위험군에는
HPV-16,18, :I>, 31, 33, 35, 39, 45, 51, 52, æ, fß,
돼, 66이
있으며, 암 발생 빈도가 낮은 저위험군에는
HPV -6, 11, 40, 42,43, 44,
57이 있다13.낌.32.l).37.~) 실제로 인체 유두종바이러스와 연관된 암 발생 은 암의 전구병소(precanærous lesion)에서 암으 로 진행되는 잠재력 (p뼈ressive rnten디al)은 주 로 감염된 인체 유두종바이러스의 유형에 의하여 결정된다.
역학 연구조사 결과에 의하면 자궁경부 조직이 암 발생 빈도가 높은 고위험군인 인체 유두종바
이러스
type 16및 18에 감염된 경우가 암 발생
빈도가 낮은 저위험군인 인체 유두종바이러스
type 6
및 11 에 감염된 경우보다 자궁경부 상피
내 종양 및 자궁경부암으로 발전할 가능성이 높 은 것으로 보고되었다~.34) 인체 유두종바이러스가 자궁경부암의 원인일 것이라는 가능성을 갖게 해 주는 것은 자궁경부 상피내종양 및 자궁경부암에 서 인체 유두종바이러스
16형과 18형 같은 고위 험군의 인체 유두종바이러스가 주로 검출된다는 것이다7.16,찌.
최근 분자병리학의 발달과 함께
Southembl야,
In situ hybridization(ISH), Polyrærase chain
rea띠on(I{:R) 및
In situ-PCR등이 바이러스 검
출에 이용되고 있는데, 이 중
Southem비α 과
PCR은 조직에서 핵산을 추출하여 실험에 이용하
기 때문에 인공적인 변화가 일어날 수 있고 종양
세포에 비특이적인 염증세포들이 포함될 가능성 이 있다. 그러나 probe를 이용한
In situ hybrid-없다on이나 pruær를 이용한 PCR은 염색체나 세 포 그리고 조직의 DNA나 RNA의 염기서열 (sequenæ)을 검출하는 방법이다~,l1.l7) 특히 이들 의 임상적 응용은 감염성 질환 중에서도 바이러 스의 진단에 이용되고 있다. 최근에는 검출감도 가 높은
PCR법과 세포에서 유전자 해석을 할 수 있는
In situ hybridization법을 조합한
msitu PCR
법을 이용하여 세포나 조직의 형태학적
구조가 잘 보존된 상태에서 바이러스 감염을 확 인할 수 있어 유용한 검출방법으로 활용할 수가 있다.
따라서 본 연구는 자궁경부의 조직검사상 만성 염증과 상피내종양으로 확인된 51 개의 시료를 대 상으로 인체 유두종바이러스의 감염 유무를 확인 할 수 있는 면역조직화학적 염색(Irrnnunohistoc
hemi떼
stain)과
In situPCR을 시행하여 인체 유두종바이러스의 각 유형을 관찰하고 두 방법간 의 검출 정도를 비교하므로서 인체 유두종바이러 스의 고위험군에 노출된 시료를 조기발견하고 또 한 고위험군에 높은 발현도를 나타내는 방법을 확인하므로서 자궁경부암을 예방하는데 도움을 주고져 한다.
11 •
재료및 방법
1.연구재료
1ffi4년 6월 1 일부터 1937년 8월 31 일까지 아주 대학교병원에서 자궁경부상피의 생체검사 조직이
Hematoxylin & Eosin (H & E)
염 색상에서 만성 염증 (απonic
nonsp:x::ifici따1따nma디on
;CND과 자궁경 부상피 내 종양 등급
I( Cervical intraepithe- lialn∞plasia
grade 1 ; CIN grade1)으로 진단된
예 중에서
10%포르말린 고정액으로 처리된 파 라핀 블록중 보존상태가 양호한 51 예를 가지고 인체 유두종바이러스에 대한 면역조직화학적 염 색과
In situκR 법을 시행하였다.
이 중 CNI는 21 예이며
CIN grade1으로 진단 된 것은 30예였다.
2.
연구방법
1)
면역조직화학적 염색
(Immunohistochemical stain)10%
중성 포르말린에 고정하여 파라핀에 포매 된 조직 블록을 3μm로 절편을 만들어 슬라이드에 부착하였다. 5~rC oven에 1시간 동안 방치한 후 xylene으로 파라핀을 제거하였다 100%
ethanol에 2분씩 3번, 앉5% ethanol에 2분씩 2번 거 친 후 에 증류수로 세척하였다.
O.OlMs여iwn
citrate buffer(pH6.0)에 넣어 microwave(Shandon)로
5분간 처리하였다. 식힌 후 에 증류수로 세척하고
3%
I-破를 첨가한 ~단lanol어1 10분간 실온에서 처 리 하였다.
Tris buffered saline(pH 7.6. Tris base 1.4g, Tris Hcl 6.0g, NaCl8.7g)으로 세척한 후에 Labell어 stn야뼈vidine
biotineU.5AB, DaKO)피t에 들어 있는
blockingreagent로 10분간
처리하였다. 인체 유두종바이러스에 대한 일차 항 체 (Papillomavirus
JX)lychlonalantibc성y
Noboca-stra)로 처리한 후에 습윤상자를 이용하여 4
0C 에 서 18시간 동안 방치하였다.
TBS buffer(pH 7.6)로 충분히 씻어낸 후 이차 항체인 link용액 (DaKO)으로 æ분간 처리하였다.
TBS buffer(pH7.6)로 세척 한 후에
streptoavidineI=eroxidase로 æ분간 처리하였다. 다시
TBS buffer(pH7.6) 로 10분간 세척한 후에 발색은
AEC(3-amino-9-ethylca뼈zole) subs없te-chrorr맹en을 사용했고,
대조염색으로 뼈yer
hernatoxylin염색을 시행하 였다. 증류수로 세척한 후에
Univesalrmunt로 봉입한 후 검색하였다.
2)
조직내 중합효소 연쇄반응(In
situ Aolymerase O1ainReactiα1)
파라핀에 포매된 조직 블록올 3μm로 절편을 만 들어 슬라이드에 부착하였다. 5:~rC oven에 1 시 간 동안 방치한 후 xylene에서 파라핀을 제거하
-240 -
였다.
1000/0ethanol에 2분씩 3번,9)% eth뻐01에 서 2분씩 2번 거친 후에 머rdry시켰다.
Proteinase
K(a)μglm~; Bc양1fÎnger 뻐nnhe뼈 용액으로 '5rc 에서 10분간 처리하고 증류수로 세 척한 후에
9)%ethanol과
100%ethanol로 각각 처리하고 머rdry 시켰다. 처리가 끝난
slide표 본에
In situR::R용
slidesea1(T:라얼Ra
ox:le No.~-OO:B)올 붙인 후
In situTh앉ma1
Cyc1ers (M JResearch)어l 슬라이드를 장착하였다.
820C에서 7분간 처리하고, 55
0C 에서 조제된 ~R 반웅 액을 슬라이드 위에 얹었다.R::R 반응액은 다음 과 같이 조제하였다.
(Tag IX>lyrærase0.8,μ~.
10 x R::R buffer2.5μ~,
2.5mM dNTPs4μ~,
1mM DIG-11-dUfP1μ~, 2OpIID1/.μe 따JVpF 1μ~,
2OpIID1/.μ~
HPVpR1μ~,
DW up to2J뼈) 사용된 인체 유두종바이러스의 유형은 田JV
6,11, 16, 18, 31
및
33이었다. Prirær의 염기서열 은 다음과 같으며 Bioneer에서 주문 제작하였다.
HPV 6 <F5’-AAaXffifAACCGAAATCXXiT-3'’
R5’-1GfCACAAACXlrIG-3’), HPV 11 (F
5’ -j뾰nrGTAACCGAAA1αIT-3’,
R5’-1GfCACAACrCGI’IGfGIGA-3’), HPV 16
<F 5’-AAaXffifA와rGAMTCXXiT-3’,
R5’김~TA-3’),
.HPV 18 (F 5'’-AAaXffifAACCGAAATCXXiT-3’,
R5'’견IGI1’ ìπ CA(따:;r π ’m좌rcrr:;ACA-3'’'),
,f班iPV 3 퍼:1
<F5' 당당’(κ‘-감-
그리고
R5'’{좌VL1GIUffifAATπ "It:LlπC-3' 윈
’7 )HPV 33 (F
5’-AAaXffifAACCGAAA1αIT-3’,
R5’강TCTCCAA1αrn:rr:ACA-3').
시약이 마르지 않도록하기 위해서
In situ R::R용
slide sea1∞Iver film으로 밀폐하여 없℃에서 3분 처리 후 55
0C 에서 2분, g.rc 에서 1분씩
14cycles올 돌려 증폭시켰다.
In situR::R용
slide£머을 떼어낸 후
Tris Buffered Saline(pH7.6)으 로 세척하였다Ar띠-Digo:업g없m-.뾰(B:냥ninga-
h뀐mh많n)로 3TC 에서 $분간 반웅시켰다.
TBS(pH
7.6)로 세척하고
5’-bvonno-4-chlovo-3- indolyl-phosphate/nitnJbluetetI강olium
(BCIP/NBT ; Scy Tek)
발색제로 발색시킨 후에 증류 수로 세척하였다. 대조염색으로
l\t1ayer hematox-ylin을 사용했으며 세척 후에 unive:뼈 IIDunt로 봉입하였다.
川. 걸 과
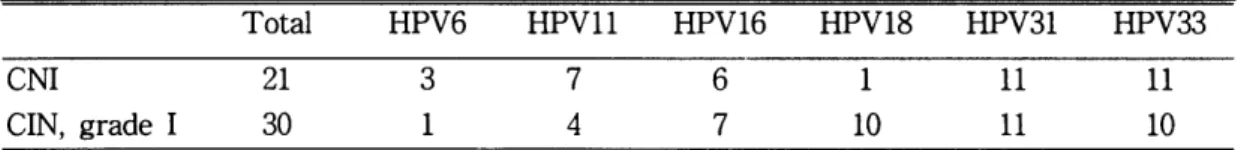
사용한 검체의 대상은 세포검사(Pap. srrear)에 서 Atypi ,떠 l 찍뻐IIDUS
ællsundeterrnir빼
signi-n떠nce(ASCUS) 또는 Iρw
grade squannous int-fa(행thelial lesion(LSIL)으로 진단된 환자의 자궁 경부 상피내세포(Fig. 1)이다. 통상적인 조직검사 의 Hematoxyline
& Eosin(H & E)염 색에서 만성 염증(ChnJnic nonspecific 따1mπm디on
CND (Fig. 3A,3C)으로 진단된 21 예와 자궁경부 상피 내종양 등급
1(않vi떠1 intr,뼈thelial n∞plasia 밍-ade
1 ; CIN grade 1 ) (Fig.4A)으로 진단된 30예를 합한 51 예를 대상으로 실험을 수행하였다.
면역조직화학켜 염색에서 인체 유두종바이러스 에 대한 양성반응은 핵이 적갈색의 과립상으로 염색되었다(Fig.
4B, 4D).인체 유두종바이러스에 대한 양성세포들은 주로 자궁경부상피의 표층 및 중간층에서 관찰되었으며 심층부에서는 관찰되지
Table 1.
Immunorea다ivity tìα
human맺다110-
Inavirus in CNI and CIN grade 1.
CNI CIN, grade 1
Number of case 21 2D
fb밍디ve
number 0 7 (23.3)*
(은
%Table 2. In situ R::R for human papillomavi- n1S in CNI and CIN grade 1.
C:NI CIN. grade 1
Number of
떠se
21 2DF>osi디ve
number 16 (76.2) 17 (ffi.7)*
(는
%Table 3. Number of HPV DNA IX>sitive lesion
associa때
with HPVsubty야s
in CNI and CIN gracle 1.Total HPV6 HPV11 HPV16 HPV18 HPV31 HPV33
CNI 21 3 7 6 1 11 11
CIN, grade 1 30 1 4 7 10 11 10
Table 4. Correlation
때th
IX>sitive HPV subtype in CNITotal
한종류만
11/33 11/31 16/31 31/33 11/16 16/31 6/11/ 6/11 11/16/18 /31 /33 16/33 /31/33 /31/3321 4 1 1 2 2 1 2
% 19 5 5 5 10 5 10 5 10 5
Table 5.
Correla디on 때th φsitive
HPV subtype in CIN grade 1 Total한종류만
18/33 31/33 18/3130 7 1 1 2
% 23 3 3 6
않았다. 이러한 양성반응 세포들은 대체로 비정형 스푼세포(atypi뎌1 koilocyte) 에서 관찰되었다. 면 역조직화학적 염색상에서
CNI병변에서는 양성반 응이 전혀 관찰되지 않았으며,
CIN grade1에서 는 23.3%의 양성률올 나타내었다(Table.
1).In situ
PCR은 검출감도가 높은
PCR법과 세 포에서 유전자 해석을 할 수 있는
In situ Hybridization법을 조합한 방법 이다 In
situK:R을 사용하면
1copy의 유전자배열을 갖는 세 포에서도 세포속에 존재하는 바이러스나 세포내 에 미량의 유전자발현 등을 확인할 수 있다.
In situ
PCR에서는 인체 유두종바이러스
DNA검색에 대한 양성반웅은 모두 핵이 흑갈색으로 진하게 염색되거나 과립상을 보였으며 핵 주변부 나 세포질에서는 관찰되지 않았다(Fig.
4C, 4E).양성반응은 면역조직화학적 염색에서와는 달리 심층부에서도 간혹 관찰되었다.
In situPCR상 에서는
CNI병변에서의 인체유두종바이러스의 양 성률은 76.ZO/o였고
CIN grade1에서는 ff3.7%로 관찰되었다(Table.
2).한편 많은 연구자들 13,낀짧,38) 에 의하면 인체 유두종바이러스의 아형
11/31/33 16/18/31/ 11/16 11/16/18 33 /31/33 /31/33
1 3 1
3 10 3 3
(sub-ψ~)들 중에서 암 발생빈도가 높은 고위 험 군으로는
16, 18, 3), 31, 33, 35, 39, 45, 51, 52, ff3, æ, 59, ffi이며, 암 발생빈도가 낮은 저위험 군으로는
6, 11, 40, 42, 43, 44, 57이 라고 보고하 였다.
본 연구에서
in situPCR을 위한 prirrer로 사 용한 인체 유두종바이러스의 sub-type으로 고위 험군에서
16, 18, 31,33형올 사용하였고, 저위험 군에서는 6과 11 형을 사용하였다.
In situ
PCR에 의한 실험결과(Table 3) 에서 사 용한 모든
prirær들에 대하여
CNI와
CINgradeI
예에서 모두 sub-띤야들이 검출되었다.
특히
CNI예에서는 저위험군인 11 형과 고위험군 인
31및 33형이 높게 관찰되었고,
CIN grade 1예에서는 저위험군인 6과 11 형은 낮게 관찰된 반 면 고위험군인
18, 31, 33형이 높게 관찰되었다.
또한 하나의 시료에서 인체 유두종바이러스의 여러 sub-ψ야들이
in situ K:R에서 동시에 관 찰이 되고 있다(Table
4).이중에
CNI예에서는 저위험군인 6과 11 형이 동시에 관찰된 경우는 없 었고 반면, 저위험군인 11 과 고위험군인 31 과
33- 242-
훌
•웰」
’‘ ,
·훌훌
,... ..
‘· ~
‘*‘혈.'"
‘’
-
-‘’
1ι
•
.. ...
..
--
-‘ • ’
i’
빼
--
* w.
·‘ ..
.. '
*
(B)
Fig 1.
Aty다떠1
SQuarmus ælls of tmdetennined significanæ (A)ar떠 koiloc뾰s
(B) inPa행ni∞J
aou
srm표 많p.
x ax>‘ (A)
(B)
Fig 2. Norrna1
따-vi떼
SQuarmus epithelium때단1
HPV앉pression
in superficia1 æll layer. (A H&E. x :ID. B ; In situ PCR. x :ID)(A)
었다. 반면 어느 한가지
sub-tyre형만이 존재하 는 경우도 4개의 예에서 관찰되었다.
한편
CIN grade 1의 예 (Table 5)에서는 저위 험군은 존재하지 않는 반면 고위험군인
16118131/33형이 동시에 존재하는 경우가 3개의 예에서 관 찰되었다. 또한
11/31/33, 11/16131/33및
11/16118/3ν33/형이 동시에 존재하는 경우는 각각 1개 형이 동시에 존재하는 경우는 각각 1개씩의 예에
서 관찰되었다. 또한 저위험군과 고위험군들이 동 시에 여러 sub-~ 들이 존재하는 경우는 611ν16/33형과 6111131/앓형으로 각각 1 개의 예 에서 관찰되었다. 더구나 고위험군들의 여러
sub-type
들이 동시에 존재하는 경우는 1ν16/31
및 11/16/18/31/33형으로서 2개의 예에서 관찰되
I . . . - : .‘ - -、a‘IIIIIIIIIII""~’-“'!. ~ ___ 4111ι1“。... ‘i“ ‘... ‘、 ι •
뜸=간 l
(A)
?활 쫓햄
영홉r 、·
(C)
(B)
(D)
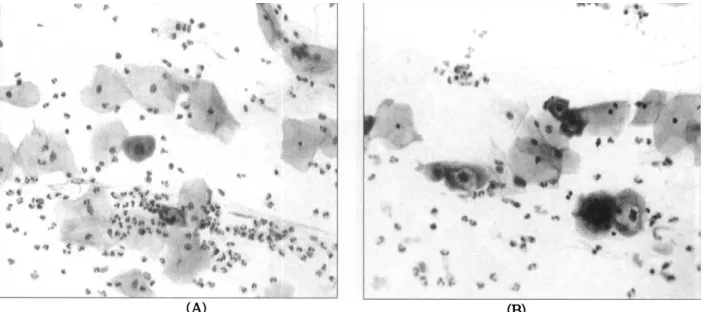
Fig 3.
αmmic nonsκrific i따l없nmation wi삼1
squarmus rretaplasiasho때ng
HPV앉pression.
(A, C ; H&E. x~.
B. D ; In situ PCR x~)
씩의 예에서 관찰되었으며, 한종류의 sub-ψR 만 존재하는 경우가 7예에서 관찰되었고, 2가지 형의 sub-type이 동시에 존재하는 경우는
1&'33, 31/33형으로 각각 1예, 18131형이 2예에서 관찰 되었다.
CIN grade
1으로 판독된 예에서 면역조직화학
적 염색에서도 양성반응이면서
in situPCR에서 양성반웅올 보인 경우는 6예이며, 면역조직화학적 염색에서 음성이면서
in situPCR이 양성인 경우
는 12예였다.
또한 면역조직화학적 염색에서 양성이면서
m빼 PCR이 음성인 경우도 1 개의 예가 있었다.
이것은 prirær로 사용한 6종류 sub-ψ야 이외의 것으로사료된다.
N. 고 찰
-244 -
(A) (B) (C)
(D) (E)
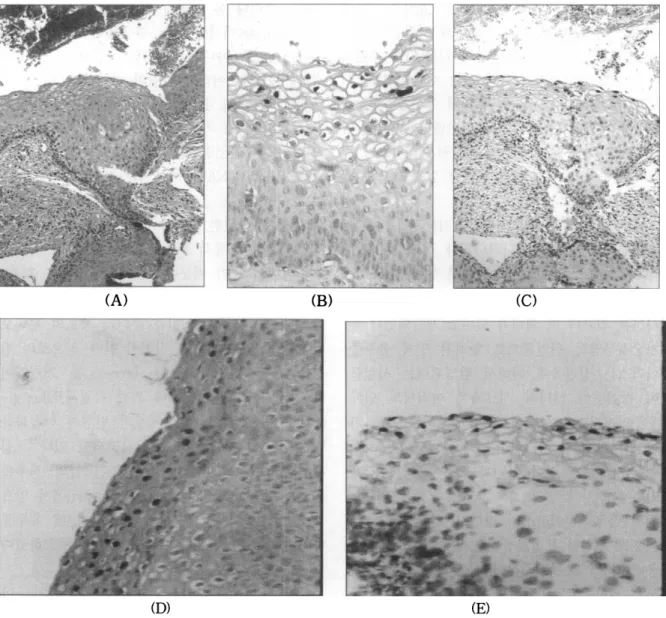
Fig 4.
않vi떠1
intraepithelial neoplasia grade 1 with HPVe짜Jression.
(A ; H&E, X ax>, D;Immunohistochemistry, X 400, B, C, E ; In situ PCR X 2C())
면역조직화학적 염색에서 인체 유두종바이러스 에 대한 양성반응은 핵이 적갈색으로 염색되었고,
In situ
PCR상에서 인체유두종바이러스 DNA에
대한 양성반웅은 핵이 흑갈색으로 진하게 염색되 거나 과립상을 보였으며 핵 주변부나 세포질에서 는 관찰되지 않았다.
In situPCR에 의한 인체 유두종바이러스 DNA에 대한 양성반응이 면역조 직화학적 염색에서 보다 더 많이 나타난 것은 세 포당 바이러스의 수가 적어도 증폭해서 검출할
수 있다는 장점을 가지고 있기 때문이다.
본 연구에서
drronicnonspecfic 따lamrr빼on
(CND으로 판독된 것과
cevical intraepithelialneo이a의a
(CIN) grade1으로 판독된 것을 대상으
로 면역조직화학적 염색상에서 CNI에서는 모두
음성인 반면에
CIN grade1에서는 23.3%가 양성
으로 발현되었다. 이는 국내의 연구결과인
21.7<>/0와 비슷한 수치이며 12) 만족할 만한 결과로 생각
되었다. 반면에
In situPCR상에서
CIN grade 1의 양성률은 fX)%였고 CNI에서는 76%로 높게 나타났는데, 이러한 결과는 기존의 조직검사 결과 에 의한 진단에 있어서 객관적이기보다는 주관적 인 관점이 개입되지 않았나 하는 생각을 갖게 되 었다. 즉 상피내세포 종양과 인체 유두종바이러스 감염에 대한 진단의 기준이 진단병리학 의사간에 일치하지 않은 것도 그 원인이 될 수 있으며 진 단의 기준이 과거에 비해 달라진 점에도 그 원인 이 있다고 하겠다.
연구결과에서 저위험군과 고위험군이 대체로 혼합해서 양성반응이 나타나거나 여러형이 같이 섞여서 나오는 것으로 보아 인체 유두종바이러스 를 검출하기 위해서는 최소한 몇가지를 동시에 검사를 수행하는 것이 한가지나 두가지의 형만을 검사하는 것보다 더 의미가 있다고 생각되었다.
자궁경부암의 원인균으로 알려진 인체 유두종 바이러스는 성접촉에 의해서 감염된다는 사실을 이미 밝혔듯이 하나의 시료에서 여러형의 인체 유두종바이러스가 동시에 각각 검색되는 것은 환 자나 환자와 성접촉을 한 배우자의 성 생활 방식 에 문제가 있는 것이 아닌가 하는 생각도 갖게 되었다.
있다. 그러나 본 연구에 의하면 반드시 스푼형세 포(koiloc뾰)에서만 인체 유두종바이러스가 검출 되는 것만은 아니다. CNI로 진단된 것 중 전혀 인체 유두종바이러스 감염의 변화가 없는(Fig.
2)4개의 예에서도
In situ PCR법에서 양성반응이 나타났다. 이는 기존의 사고방식과는 대치되는 것 으로 향후 자궁경부암 검사시 반드시 인체 유두 종바이러스 DNA에 대한 검사가 이루어져야함을 보여주고 있다. 조직검사에 스푼형세포화(koiloc
ytosis)가 확실한 상피내에서는 인체 유두종바이 러스 DNA의 증식 뿐만 아니라 바이러스 단백질 의 발현이 있기 때문에 이러한 세포에는 조직학 적인 검색과 면역조직화학적인 검색,
In situ hybridization및
In situ PCR등을 이용하여 감 염 여부를 확인할 수 있을 뿐더러 세포의 형태도 관찰할 수 있다는데 그 장점이 었다. 암으로의 진 행은 다단계과정 (m뻐S뼈 process)를 거칠것이 나 인체 유두종바이러스에 의한 각질세포(kera디
nocyte) 의
DNA변성이 세포의 변형과 악성화를 일으키는 첫 시작인 것으로 보고되고 있다~) 실 제 인체 유두종바이러스와 연관된 암의 경우를 볼 때, 암의 전구병변(precursor lesion)에서 암으 인체 유두종바이러스는 감염시 편평상피의 기 로 진행되는 잠재력은 주로 감염된 인체 유두종 저세포를 침범하여 잠복상태로 있으면서 인체 유 바이러스의 형에 의해서 결정된다고 보고하였다
두종바이러스 DNA는 땅so~ 상태로 세포에 존 떼.
재하게 된다째 인체 유두종바이러스의 잠복감 한편,
In situPCR같은 방법으로 극소량의 인 염은 특징적인 세포병리학적 변화를 동반하지 않 체 유두종바이러스 DNA를 검출하는 것이 의미 기 때문에 조직학적으로 검색하기가 힘들다. 세 있는 일인가에 대하여서는 논란이 있을 수 있다.
포내에서 바이러스의
DNA복제활동이 활발해지 잠복감염 Oatent infection} 의 경우 인체 유두종바 면서 감염된 세포들은 성숙해지고 표층으로 이동 이러스 DNA의 복제가 미약하여 매우 적은 양의 하면서 스푼형세포(koilocyte)가 표층부에 출현하 인체 유두종바이러스 DNA의
copy수를 지니고
게 된다. 있으며3)) 자궁경부 상피내종양 또는 암에서도 아
스푼형세포화(koilocytosis)는 편평상피의 표층 주 적은 양의 인체 유두종바이러스 DNA의 ∞py 세포에 나타나는 것으로 핵 주위가 밝게 탈락된 수를 지닐 수 있다. 그러므로 암을 일으키는데 이 것처럼 공동(vacuole) 이 형성되고 핵의 농축 등이 렇게 아주 적은 양의 인체 유두종바이러스
DNA보이는 형태학적인 현상으로(Fig.
1 B)일반적으 의
copy수라 하더라도 중요한 역할을 하기 때문 로 인체 유두종바이러스 감염의 특징적인 변화로 에:!B)
In situPCR로 극소량의 인체 유두종바이러 생각된다. 세포나 조직검사에서 인체 유두종바이 스 DNA를 검출하는 것은 의미가 있다. 본 연구 러스 감염의 지표로서 이러한 특징들이 이용되고 에서도 CNI인 경우 면역조직화학적 염색에서는
- 246-
양성반응을 보인 것이 하나도 없었지만
In situ human immunocleficiency virus typ:! 1 K:R법 에서는 76.2%라는 아주 높은 양성 반응을
provirus inrmnonucl않r
ælls by in situ나타내었다{X)lyrrerase
chainre<뼈on
N과19l.
J Med인체 유두종바이러스는
invitro와
invivo에서 3aJ:1표-1391,
1002감염된 숙주의 편평상피세포를 암세포화 시킨다는
4. Be::ker 1M, Stone KM,Ale때nder
ER것은 이미 잘 알려진 ^~실이래6,10,짧짧æ,뼈 특 히 고위험군의 인체 유두종바이러스 형들이 사람 성기의 각질세포를 변성 시킬 수 있다잉
본 연구에서 CNI나
CIN grade1을 대상으로 인체 유두종바이러스를 검출함에 있어서 면역조 직화학적 염색보다
In situK:R에서 높은 양성률 을 보였고 인체 유두종바이러스 감염의 형태학적 변화가 없는 정상상피 핵에서도 발현되었다는 것 은 진단법으로
In situK:R이 매우 유용한 방법 이 될 수 있다는 것을 의미한다. 또한 CNI로 판 독된 대상에서도 인체 유두종바이러스가 높게 검 출되었다는 것은 본 연구의 중요한 의미로 생각 된다. 향후 CNI나
CIN grade1으로 의심되는 경 우
In situK:R로 인체 유두종바이러스
DNA검 사를 반드시 시행하여야 하며 연구결과에서와 같 이 최소한 4종류 이상의 sub-ψ¢을 대상으로 검 사를 실시하여야 할 것으로 사료된다. 이 검사에 서 양성으로 발현되면 자궁경부상피내 종양의 등 급에 따라 추적과 관찰 및 치료를 결정하는 지침 에 따라 환자를 진료함으로서 자궁경부암의 위험 군을 구분하여 암으로의 진행을 사전에 예방하고,
불필요한 과다 치료를 방지함으로서 궁극적으로 환자에게 양질의 서비스를 제공하고 경제적 발전 을 도모할 수 있을 것으로 사료된다.
참고문헌
1.
보건복지부, 한국인 암등록 조사자료 분석보고 서, 1~
Genital human
탱pilloma
virus infection: a growing concem.α:>stetrics
andGynecol땅y,
αïnics
cf North Amerim 14:3ffi-ÐJ, 19ff7 5.&뾰n
MA, Jones앉1,
Lamins lA The&-E7 region of human
맹pillomavirus
typ:!18 is sufficient for transforrnation of NIH 3T3 and rat-1 ælls. J Vrrol 61 3635-æ40, 1æ7
6.
않rlell
MA, Jones KH, Grossman SR ldentification of human맹pillomavirus
typ:!18 transforrning genes in
irnrmrtali갖녔
and primary ælls. ] Virol 63:1247-1짧, 1뾰
7.
Bosh따t
M, Gissman L, Ikenberg H, Kleinheinz A, Scheurlen W, zur Hausen H A new typ:! of papillomavirus DNA, its presence in genital떠ncer biopsi않
and in않n
lines따ived
fromc앉vi떼 때cer.
EMBO Jt 3 ; 1151-1157,
1않4
8. Buckley jD, llill R,
없rris
RWC. Case control study of the husbands of woræn with dysplasia or carcinoma of the앙vix.
Lα7Cer;
ii : 1010-1014. 1ffi19.
carr뼈on
M],1\κanæ
DJ,ωzick
J, SingerA
Pr땅-essive pa따ltia1
of mild따vi갱l
atypia prospective
cytologi떠1,
col{X)scopic, and virologica1stuφ. 1α7Cet
8!1)1장7-2때,
19aJ10. Ca!nIn MS, Jarrett WFH Papillomvirus infection incattle Vira1 and
ch얹1Ìca1
2. Arye ]E. The vagina1 sræar :
“pIi없ncer"
cofactors in natura11ycxχurring
and ællsstu이es
USlngrr뼈ified
techniques. Ame짜Jerirænta1ly indu때
turmrs.αiba R뼈u1
J
αIstet
Gynecol ;많
: 12<E-1219,1쨌 S까7ψ
1al: 117-135,1쨌
3. Bagasra, 0., S.P.Hauptman, H
W.Lis따ler,
11. Carun, R W., j.F.Siles, L.MLi,MM&표n뀐n
MSachs and Rj.Pomerantz.
~tection
of and GJNuovo.~따:tion
ofher빼디s
C찌rus
infection inh뼈tectomy
speciIrens using irmrunohistochmistIy with reversetran따따ase
(RT) in situ JX)lyrærase chainM, Ræves WC, Rawls WE.
~s
simplex virusψpe
2: a JX)Ssible interaction with human맹pillomvirus
types 16118 in theI얹ction(PCR) co따’innation.
Cellvisiα1,
1:84, developrrent of invasive cervica1 cancer. In1004 ] Cancer, 49: 335-40, 1991
12. Chang
S∞ 뻐rk,
Jong Hee Nam, Jæ Hyuk 21. Howley PM The role of papillornavirus in뇨~,
JongS∞n
Kim, seung Jin Oh. human cancer. In ImI:nrtant Advaæs in~tection
of HumanPa다llorr뀐.virus
inα떼,10gy. I농vi떠1
VT Jr, Hellrnan S and Lesion of Uterine다πvix.
The KoreanRosen밟y
SA,어itors,
j.B. Lippincott Co.]ol1TTr11 q
Pat빼ogy.
31:289-297, 1997Philadelp비a
; ffi-73, 1ffi713. Crum CP, Mitao M, Levine RU,
Silverst잉n 낌. 없때a
T, Furuno A, Yoshiike K Human S. Cervica1papillorna까ruses 뚱훌I멍ate
papillornavirus type 16 open1없이ng
frame withinrm따101<핑i덩lly
distinctpri웠ncerous
E7없codes
a transforrning gene for rat 3Y1 lesion. ] Virol ; 54 :675행1, 1됐
ælls. ] Virology없:610-613,
19æa14.
~vesa
SS.않앙iαive epi뼈미01명y
of 23.Kessll하
II,Vener얹1
factors in human떠ncer
of the uterine cervix. Obstetαηe∞ cervica1 떠ncer
; 39 : 1912 -1919,1인7
; 63 : 003-612,
1~
24.없i따
jW, Bartlett GL. The Shope PipiU- 15.~
Villers EM. HumanPathogenic-탱pillo
rr빼rus
type ; An따雄.In 겐r Hau않n
H(edJ : "Human
path명많ic 탱pillorna띠rus."
Berlin ;
S띠nger-
Verlag ; W1-12, 1004orna-carcinorna complex of rabbits A mrlel
sys뼈n
of neoplasticpr멍ression
and sJX)ntaneousr멸ression.
Advαπ'er Re,아
35:81-100, 1931
16.
다irst
M, Gissrnann L,&안lberg
H, zur 25.터ncaster
WD, Olson j. Anirnal Pipillornav- Hausen H A맹pillornavirus
DNA from a iruses. Microbiol Rev. 46: 191-2fJ7,H없 ævi떼
biopsy samples from differentgec용- 26.1ρifincz
AT,뎌ncast앉
WD, Kurrnan RJ, CF raphicIi멍ions.
Proc NatlAαld
sci USA ; Temple. Cloning하펴 characteriza디on
of the 00 : 3812-3815,1~
DNA of a new human며pillornavirus
from 17. Gall 1F,많ùue
:ML.Bαmltion
and detectionof RNA-DNA hybrid rmlecules in cytolo-
gi뎌1 prl밑g때ons.
Proc NatlAα띠
sci USA 63:킨8-&3,
100318. Gram IT, l\1aca1uso M, Sta1sberg H Cigar- ette srmking and the
inci따læ
ofcerv때l intr뼈,ithelia1
neoplasia Am ] Obstet야fT1-
erol ; 167 : 40-44,
1앉
19.
뻐rris
WC, Brinton A, Cowdell RHαlara
cteristic of women with dysplasia or
a
worr뀐n
with dysplasia of the uterine따vix.
] Virol. ; 58 :장)-229, H쨌
27.
1ρrincz
AT, Terrple GF, Kurrrnn RJ, Jebson AB,터n떠ster
WD :Oncog 얹ic
l association of specific human Pipillornavirusψpes
withcervi떠1 neo미asia ./1뻐nχ11
q theNatiαχj
Cancer Institute
79:671판76.
1ffi728.
뼈rk
JA, Yvonne KD,많ward
D. HPV inf띠1
thickness cervica1 biopsies High preva1enæ in CIN 2 and CIN 3detect어
bycar디noræ
in situ of the uterine cervix. Br ] a옆lsitive
PCRrreth따 ]Rαhol.
165:301- Cancer ; 42 :꿨~웠 1쨌
300, 1991æ. Hildesheim A,
뼈nn
V, Brinton IA,Si때0 정.
Nasseri M, Gage ]R,1ρrincz
A Human -248 -없pi110mavirus ~
16 irmmrtalizes~얹a디n-
'51. Srmtkin D.Vrrol<핑y
of Human çøpillomavi- ocytes containtran앙따senα성ings
&, E7, rus.αin
ObstetGyne∞1/.
32(1) ; 117 : 125, and E2ini떠i1:f최
at단le
lW prormter and 19Ðexpress high levels of E7. Virology
잃'.
Syrjanen KEpi뼈띠이(핑y
of human맹pill-
184: 131-140, 1931
oma띠rusCHPV)
infections andth려r
aSSOCIa-3). Phelps WC, Yee CL, Munger K The tions with
gl뻐떠1 sq뻐rmus
æll떠ncer.
human papillomavirus ty}æ 17 E7 gene AMPIS ; CJ7 : ffi7-CJ70, 19Ð
encα농s
transactivation and transfonnation 39. Tanaka A, NOOa T,Y;해lllTB
Y.I따1뼈ca디m
functions
앙mil강
to those ofadeno찌rus
EIA Cell. ; 53 :
댔-547. 1쨌
31. Reeves. New
Ð핑
] Med ; 320 :1낌7-1441,
1앉B
32.
R앙d
and1ρrincz.
] Family Pract. 32 183-188, 1931of a transforming gene of human
탱pilloma
virus ty}æ 16. I Virol. 63:
14ffi-1뼈, 1쨌
40. Vousden
따f,
lliniger ], Diçøolo ]A The E7 openre:퍼ing
fraræ of human며pilloma
virus ty}æ 16enαrles
a transforming gene.Oncogene Res. 3:167-175, 1988
33.
Ro뼈n
DACorr뼈risα1
review of key 41. Watanabe S, Yoshiike K Transfonnation of멸Jidemiol<핑i떠1
studiers inær찌떠l 떠ncer
rat 3Y1 ælls byhur떠n papillorr뀐virus
ty}ærelat외
to current searchs for transmissible 18 DNA Int ]aπeπ
; 41 :æJ-~,
1988 agents. Cancer Res. ; 33 : 1353 -1367,1엔3
42. Woodworth CD, lliniger ], Dipaolo ]A 34.Schn잉엎.
A, Schuhmann R, de Villiers EM.Imrrn때iza디on
of human foreskinkera디no-
Kli띠sche &:빼ltung
von human빼llom-
cytes by varlous human맹때lorr빼rus
avirus-infection in unteren
Ger뼈ltract.
D-NAs corresJX)nds to their associationGeb띠tsdzFrCJ1.JE에æill.;
6 :m1-~웠"
1æ6 with따vi떠1
carcinoma.. ] Vìrol. 63:159-1없,
35. Schneider A
La따lt
and subclinica1gl없i떠 1~힘
HPV
inf때ons.
Papillorr:IVirus Rep. 1:2-5, 43. Zur없usen
HPa다llomaviruses
in human1930
뎌ncer.
Cancer 59: 1002--6, 1æ736. Sdmeider A Natural History of genita1
papilloma까rus
infectionInteroirolo.양 원:
a)l-214, 1934
44. 2m- Hausen H Human Papillomavirus in the pathogenesis of
anogeni떼 뎌nc앉.
Virology 184:9-13, 1931