Abstract : Background : Anti-neoplastic agents act by killing cells that divide rapidly, one of the main properties of most cancer cells. Chemotherapy can also harms cells that divide rapidly under normal circumstances, leading to various side effects such as anemia, leukopenia, alopecia, and mucositis. This pattern of side effects depends on the type and dosage regimen of the anti- neoplastic agents. However there is a paucity of such research in Korea. We analyzed the status of anti-neoplastic agent-related adverse events reported in a single hospital in Korea.
Methods : Adverse drug reaction data was collected prospectively from the Seoul National University Hospital Pharmacovigilance Center, from February 2010 to June 2012. One-thousand,
회원학술보고
단일 의료기관에서의 항암제 유해사례 보고 분석
송지예
�, 송수정, 서성연, 김향숙, 이혜숙, 이주연
a서울대학교병원 약제부, 한양대학교 약학대학 a
Analysis of Anti-neoplastic Agent-Related Adverse Events in a Single Hospital
Ji-ye Song
�, Su-jeong Song, Seong-yeon Seo, Hyang-suk Kim, Hye-suk Lee, Ju-yeun Lee
aDepartment of Pharmacy, Seoul National University Hospital, 101 Daehak-ro, Jongno-gu, Seoul, 110-744, Korea College of Pharmacy, Hanyang University, 55 Hanyangdaehak-ro, Sangnok-gu, Ansan Kyeonggi-do, 426-791, Korea
a투고일자 2014.8.4; 심사완료일자 2014.8.29; 게재확정일자 2014.9.12
�교신저자 송지예 Tel:02-2072-2328 E-mail:30487@snuh.org
연구 배경 및 목적
항암제는 암세포뿐 아니라 분열이 활발한 정상세포 에도 손상을 주기 때문에 부작용이 필연적이다. 항암 제 유해사례는 항암제의 종류뿐 아니라 암의 종류, regimen, 그리고 투여용량과 경로에 따라 발현 양상 이 달라진다.
1)실제 항암제 유해사례가 발생할 경우 심각도에 따라 용량 조절이 이루어지게 되는데, 그 기 준은 NCI-CTCAE grade에 따라 권고된다.
현재 서울대학교병원을 포함한 국내 유해사례는 보고 표준 용어인 WHO Adverse Reactions Terminology (WHO-ART)를 사용해 보고되고 있다.
2)WHO-ART
는 최대강도, 위중도 정보를 포함하지만 심각도에 대 한 정보는 포함하지 않는다.
3)반면, 항암제 임상시험 에서 사용되는 항암제 특이적인 유해사례 분류체계인 NCI-Common Terminology Criteria for Adverse Events(NCI-CTCAE)는 심각도 분류에 정확한 guideline을 제시하며,
4)CTCAE의 심각도에 따라 용 량 조절이 권고되기 때문에 항암제 유해사례 보고에 더 적합하다고 생각되어, 본 연구에서는 WHO-ART 기준으로 보고된 국내 항암제 유해사례를 NCI- CTCAE 기준으로 재분류하고, 분석하고자 하였다.
연구대상 및 방법
one-hundred and seventy-six anti-neoplastic agent-related cases (14.5%) were analyzed from a total of 8102 cases. We retrospectively analyzed patient information, cause drug, regimen, clinical symptoms, serious adverse events, and un-reported adverse events. We evaluated by Common Terminology Criteria for Adverse Events(CTCAE), the severity based on the report by WHO Adverse Reactions Terminology(WHO-ART).
Results : Patients with adverse events(AEs) had a median age of 57.7 years, between 51-60 years of age was most common. The most common causative anti-neoplastic agent was oxali- platin (24.2%), followed by irinotecan (12.2%), docetaxel (6.9%) and the highest proportion com- pared to the total AEs was sunitinib. The most common clinical manifestation of AEs was skin and appendage disorders (32.6%), and hypersensitivity (10.4%) was the most common clinical symptom, followed by nausea (6.9%), and pruritus (5.3%). A total of 265 cases were reported as serious AEs.
Conclusions : Unreported AEs may be expressed, hence more active AE reporting is required.
Anti neoplastic agents-specific adverse events reporting system, based on. the toxicity ratings and the chemotherapy protocol, is needed.
[Key words] Anti-neoplastic agent, WHO-ART, CTCAE, ADR(Adverse Drug Reaction)
1. 연구 대상 및 기간
2010년 2월 1일부터 2012년 6월 1일까지 서울대학 교병원 약물유해반응 관리센터에 보고된 유해사례를 대상으로, 원인약물이 항암제가 아닌 사례는 제외하 였다. 이 때, 항암제의 기준은 ATC 분류 코드 L(L : Anti-neoplastic and immunomodulating agent) 에 포함된 약물 중 항암목적으로 사용된 약물로 정의 하였다.
5)보고된 유해사례 한 건 중 여러 종류의 부작용과 여 러 원인 약물이 있는 경우 모두 각각의 유해사례로 처 리하였고, 가능성 희박 이하의 인과성을 가진 유해사 례는 분석 대상에서 제외하였다.
2. 연구 방법
서울대학교병원 약물유해반응 관리센터에 자발적으 로 보고된 항암제 유해사례를 바탕으로, 부족한 정보 는 전자의무기록을 통해 보완하였다. 연구는 기술적 방법으로 수행되었으며, 연구 대상을 바탕으로 환자 군의 기본 특성, 원인약물, 임상증상, regimen과 cycle 등에 대해 분석하였다. 유해사례의 인과성 평가 는 WHO-Uppsala Monitoring center(WHO- UMC)의 criteria를 사용하였으며, 유해 사례의 원인 약물은 ATC 코드를 사용해 분류하였다. 항암제 유해 사례의 보고 비율은 환자수와 처방건수, 2가지 기준을 사용해 분석하였다. 처방건수 기준의 항암제 유해사 례 보고 비율은 항암제 유해사례 보고건수를 연구 기 간 동안 항암제의 처방건수로 나눈 것을 의미한다. 이 때, 경구 항암제의 경우 복용일수를 처방 건수로 계산 하였고, WHO-ART 기준으로 보고된 항암제 유해사 례 재분류에는 NCI-CTCAE guideline을 사용하였 다.
연구결과
1. 보고 건수 및 환자군의 특성
2010년 2월 1일부터 2012년 6월 1일까지 보고된 유 해사례 8,102건 중 항암제에 의한 유해사례 보고 건수
는 1,176건으로 14.5%를 차지하였다.
중복 데이터 처리 후, 연구 대상 환자는 총 969명으 로, 1인당 부작용 보고 건수는 평균 1.69건으로 1인당 최대 6건까지 보고되었다. 평균연령은 57.7세로, 51- 60세의 환자군에서 보고 빈도가 가장 높았다. 남성이 505명(52.1%)으로, 여성(464명, 47.9%)보다 더 많은 비율을 차지하였다. 환자군을 진단명으로 분류한 결 과 대장암(32.9%), 유방암(11.8%), 위암(10.3%)의 순 서로 빈도가 높았다.
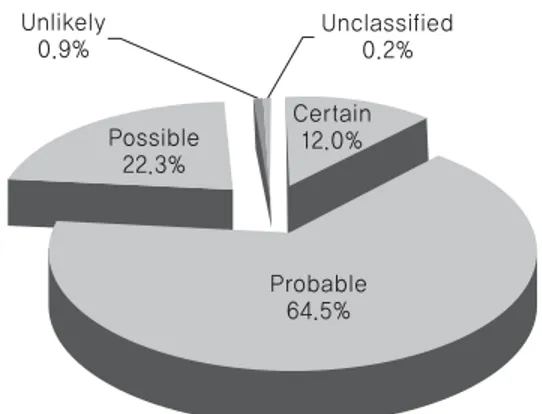
유해사례 보고 건수는 1,638건으로, WHO-UMC 기준으로 유해사례의 인과성을 평과한 결과‘가능성 높음(probable)’ 의 보고 건수가 1,057건(64.5%) 으로 가장 많았다. ‘가능성 희박(unlikely)’이하의 인과성 이 평가된 보고 건수는 19건으로, 이는 향후 분석에서 제외되어 총 분석 유해사례 건수는 1,619건이었다 (Fig. 1).
2. 유해 사례의 원인 약물
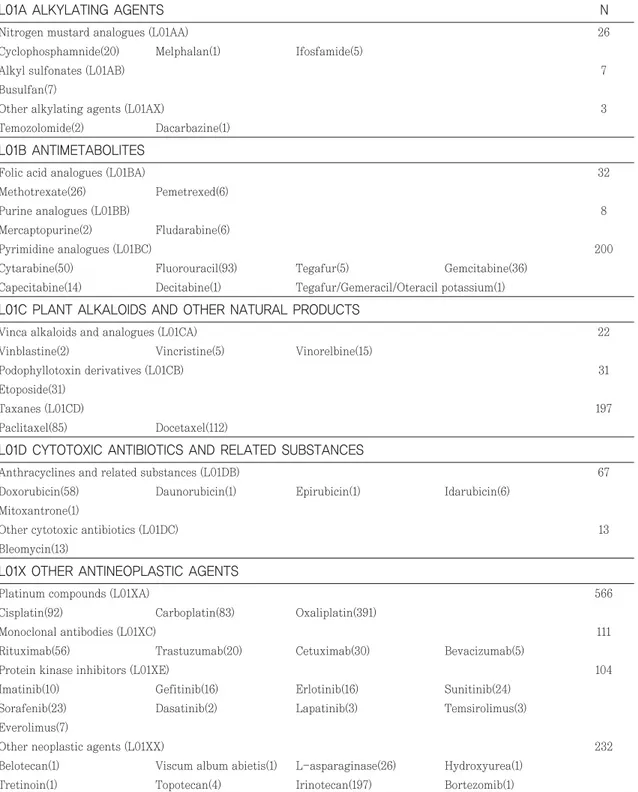
유해사례의 원인 약물을 ATC 코드 계열별로 분류한 결과 백금 화합물이 566건(35.0%)으로 가장 높은 빈 도로 보고되었고, irinotecan 등이 속해 있는 기타 군 (other neoplastic agents, 14.3%), 피리미딘 유도체 (12.4%)와 탁센 계열(12.2%)의 빈도가 높았다. 약품별 로 분류하였을 때는 oxaliplatin(24.2%), irinote- can(12.2%), docetaxel(6.9%)의 순서로 보고 빈도가 높았다(Table 1).
Fig. 1 Causality assessment by WHO-UMC category
Table 1. Causative antineoplastic drugs of adverse events
N L01A ALKYLATING AGENTS
L01B ANTIMETABOLITES
L01C PLANT ALKALOIDS AND OTHER NATURAL PRODUCTS
L01D CYTOTOXIC ANTIBIOTICS AND RELATED SUBSTANCES
L01X OTHER ANTINEOPLASTIC AGENTS
Nitrogen mustard analogues (L01AA) 26
Cyclophosphamnide(20) Melphalan(1) Ifosfamide(5)
Alkyl sulfonates (L01AB) 7
Busulfan(7)
Other alkylating agents (L01AX) 3
Temozolomide(2) Dacarbazine(1)
Folic acid analogues (L01BA) 32
Methotrexate(26) Pemetrexed(6)
Purine analogues (L01BB) 8
Mercaptopurine(2) Fludarabine(6)
Pyrimidine analogues (L01BC) 200
Cytarabine(50) Fluorouracil(93) Tegafur(5) Gemcitabine(36)
Capecitabine(14) Decitabine(1) Tegafur/Gemeracil/Oteracil potassium(1)
Vinca alkaloids and analogues (L01CA) 22
Vinblastine(2) Vincristine(5) Vinorelbine(15)
Podophyllotoxin derivatives (L01CB) 31
Etoposide(31)
Taxanes (L01CD) 197
Paclitaxel(85) Docetaxel(112)
Anthracyclines and related substances (L01DB) 67
Doxorubicin(58) Daunorubicin(1) Epirubicin(1) Idarubicin(6)
Mitoxantrone(1)
Other cytotoxic antibiotics (L01DC) 13
Bleomycin(13)
Platinum compounds (L01XA) 566
Cisplatin(92) Carboplatin(83) Oxaliplatin(391)
Monoclonal antibodies (L01XC) 111
Rituximab(56) Trastuzumab(20) Cetuximab(30) Bevacizumab(5)
Protein kinase inhibitors (L01XE) 104
Imatinib(10) Gefitinib(16) Erlotinib(16) Sunitinib(24)
Sorafenib(23) Dasatinib(2) Lapatinib(3) Temsirolimus(3)
Everolimus(7)
Other neoplastic agents (L01XX) 232
Belotecan(1) Viscum album abietis(1) L-asparaginase(26) Hydroxyurea(1)
Tretinoin(1) Topotecan(4) Irinotecan(197) Bortezomib(1)
3. 항암제 유해 사례 보고 비율
처방 건수 기준, 약물계열별 항암제 유해사례의 보 고 비율은 taxane 계열에서 1.6%로 가장 높았으며 platinum compounds(1.4%), monoclonal anti- bodies (1.2%), alkyl sulfonates(1.1%)의 순서로 빈 도가 높았다. 보고 빈도가 가장 낮은 약물 계열은 protein kinase inhibitor(0.4%)였다.
환자 수 기준, 약물 계열별 항암제 유해사례 보고 빈 도가 가장 높은 약물계열은 protein kinase inhi- botor로 14.3%였다. 다음은 other neoplastic agents가 8.3%, taxane 계열이 6.1%로 나타났다 (Table 2).
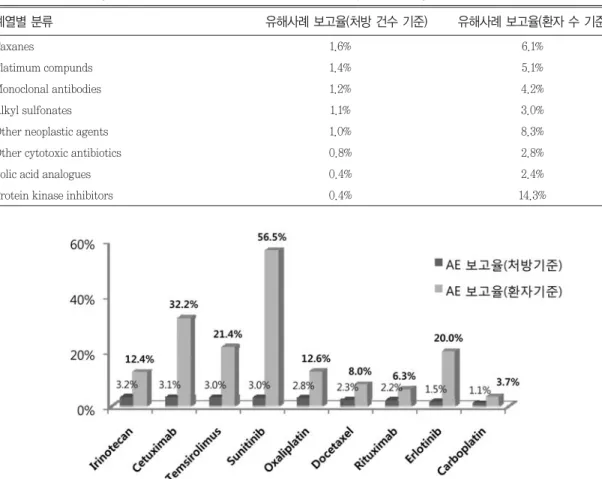
항암제 유해사례를 약물별로 분류한 결과, 처방 건
수 기준으로는 irinotecan이 3.2%, 환자 수 기준으로 는 sunitinib이 56.5%로 가장 높은 비율로 보고되었 다(Fig. 2).
4. 유해 사례의 임상 증상
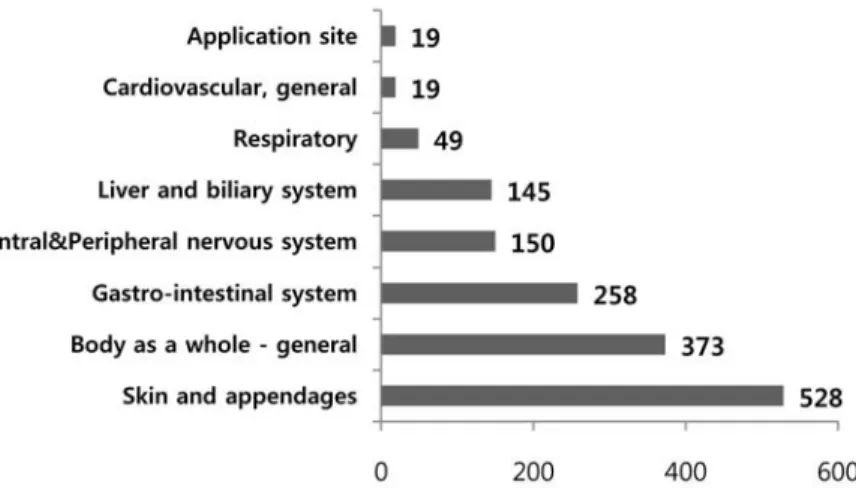
유해사례의 임상 증상을 WHO-ART 기준으로 분류 한 결과, 피부 부속기계 계열에서 528건(32.6%)으로 가장 많은 부작용이 보고되었다. 그 뒤로 전신 부작용 (23.0%), 위장관계 부작용(15.9%)이 높은 빈도로 보 고되었다(Fig. 3).
임상 증상별로 분류한 결과 과민증상이 169건 (10.4%)으로 가장 많았고, 오심(6.9%), 가려움증 (5.6%)의 순서였다(Fig. 4).
Table 2. Percentage of adverse events classified by antineoplastic drugs classes
계열별 분류 유해사례 보고율(처방 건수 기준) 유해사례 보고율(환자 수 기준)
Taxanes 1.6% 6.1%
Platimum compunds 1.4% 5.1%
Monoclonal antibodies 1.2% 4.2%
Alkyl sulfonates 1.1% 3.0%
Other neoplastic agents 1.0% 8.3%
Other cytotoxic antibiotics 0.8% 2.8%
Folic acid analogues 0.4% 2.4%
Protein kinase inhibitors 0.4% 14.3%
Fig. 2 Percentage of adverse events classified by antineoplastic drugs classes
5. 유해 사례의 임상 증상과 원인 약물
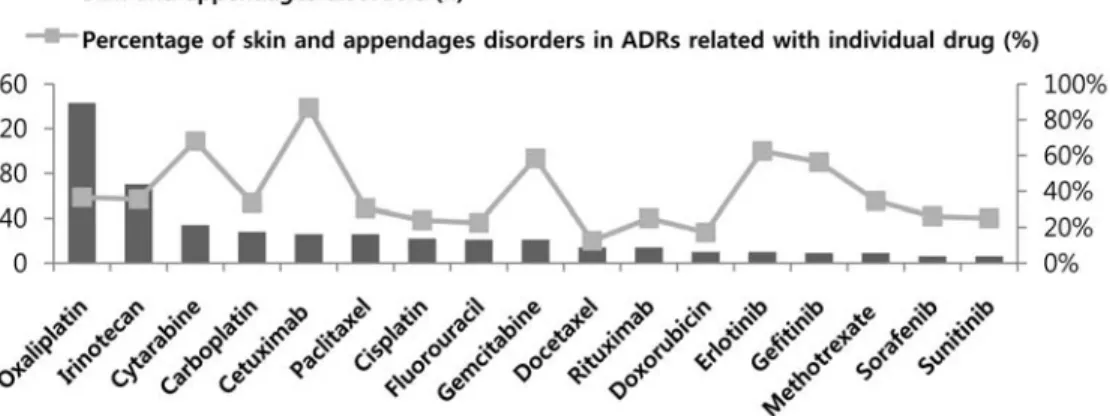
유해 사례의 보고 빈도가 가장 높은 3개의 임상증상 계열에 대하여 원인 약물별 부작용 보고 빈도(막대그 래프)와 해당 약물의 전체 유해사례 중 그 계열에 해 당하는 유해사례가 보고된 비율(꺾은선그래프)을 나 타내었다.
① 피부 부속기계 계열 부작용(Skin and appendages disorders, n=528)
피부 부속기계 계열에서는 oxaliplatin(143건)과
irinotecan(70건)의 보고 빈도가 가장 높았다.
Cetuximab의 경우 피부 부속기계 계열에서 보고 된 경우는 26건으로 보고 빈도는 낮지만, 전체 유 해사례 중 피부 부속기계 유해사례 보고 비율이 86%로 매우 높았다(Fig. 5).
② 일반적인 전신 부작용(Body as a whole - gen- eral disorders, n=373)
일반적인 전신 부작용에서는 Oxaliplatin(145건) 과 Docetaxel(73건)의 보고 빈도가 높았다.
Trastuzumab의 경우 전체 유해사례 중 일반적 전 Fig. 3 Clinical manifestation of adverse events classified by system-organ classes (WHO-ART)
Fig. 4 Clinical manifestation of adverse events classified by main symptoms (WHO-ART)
Fig. 5 Number and percentage of specific drug-induced skin and appendages disorders
Fig. 6 Number and percentage of specific drug-induced body as a whole-general disorders
Fig. 7 Number and percentage of specific drug-induced gastro-intestinal system disorder
신 부작용 보고 비율이 85%로 가장 높았고, Docetaxel (65%), Rituximab (46.4%)의 순서였 다(Fig. 6).
③ 위장관계 부작용(Gastro-intestinal system dis- orders, n=258)
위장관계 부작용에서는 irinotecan이 54건으로 가장 높은 빈도로 보고되었고, fluorouracil(44건), oxaliplatin(34건)의 빈도가 그 다음으로 높았다.
Fluorouracil의 경우 보고 빈도는 2번째로 높고, 전체 유해사례 중 해당 계열의 유해사례는 47%로 가장 높았다(Fig. 7).
6. Regimen, cycle별 분류
대부분의 항암제 유해사례는 cycle 1에서 보고되었 고(38.7%), cycle 횟수가 증가할수록 유해사례 보고 빈도는 줄어들었다. 가장 많은 유해사례가 보고된 regimen은 FOLFOX(folinic acid, 5-FU, oxali- platin)로 총 380건(23.5%)이 보고되었고, FOLFIRI (folinic acid, 5-FU, irinotecan, 11.4%), Taxol- Carboplatin(6.1%)의 순서였다.
① FOLFOX
FOLFOX에서 가장 많이 보고된 유해사례는 과
민성(20.3%), 가려움(19.7%), 두드러기(8.4%)의 순 서였고, 계열별로 분류하였을 때는 피부 및 부속기 계 부작용, 일반적인 전신 부작용의 보고 빈도가 높 았다. Cycle 횟수로 분석하였을 때는 전체적인 경 향성과는 다르게 #7 이상부터 유해사례 보고 빈도 가 증가하였다.
② FOLFIRI
FOLFIRI에서는 피부부속기계 부작용(37.8%), 위장관계 부작용 계열(29.2%)의 유해사례가 많이 보고되었고, 그 중에서도 발한(29.2%)의 빈도가 가 장 높았다.
③ Taxol-Carboplatin (TC)
TC에서는 피부부속기계(29.6%), 간 담도계 (22.4%) 부작용이 높은 빈도로 보고되었다. 유해사 례의 임상증상은 간독성(16.3%), 가슴 통증(8.2%), 두드러기(8.2%)의 순서로 많이 보고되었다.
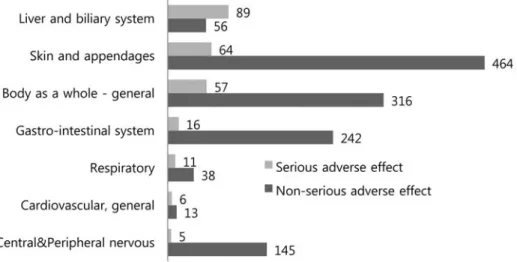
7. 중대한 유해사례
중대한 유해사례는 142명의 환자에서 265건이 보고 되었다. 51-70세의 연령에서 가장 많이 보고되었으 며, 계열별로 분류한 결과 간담도계 질환에서 61%로 높은 비율의 중대한 유해사례가 보고되었다(Fig. 8).
Fig. 8 Clinical manifestation of adverse events classified by system-organ classes and seriousness
8. 유해 사례의 임상 증상(NCI-CTCAE 기준)
보고된 유해 사례의 임상 증상을 CTCAE 기준에 따 라 재분류한 결과, WHO-ART에서의 분류와 같이 피 부 및 피하조직에서의 유해사례가 가장 높은 빈도로 보고되었고 위장관계, 면역기계 부작용이 높은 빈도 로 보고되었다(Table 3).
9. CTCAE에 따른 심각도 평가
CTCAE 기준으로 심각도를 평가한 결과 Grade 3 이상의 유해반응은 408건(25.2%)이 보고되었다.
Grade3 이상의 유해사례를 계열별로 분류한 결과 피 부부속기계 부작용의 빈도가 가장 높았고, 면역기 계 열에서는 보고된 유해사례 중 grade 3 이상의 비율이 46.9%로 가장 높았다.
Grade 3 이상 유해사례의 원인약물로는 oxalplatin (33.8%), docetaxel(8.3%), carboplatin (6.4%)의 빈 도가 높았다.
고찰 및 결론
본 연구는 단일 의료기관에서 자발적으로 보고된 항 암제 유해사례에 대한 분석으로, 전자의무기록 검토 를 통해 정보를 보완할 수 있었다.
연구 결과, 1,176건의 항암제 유해사례가 총 969명
의 환자에서 보고되었으며, 환자의 평균 연령은 57.7 세였다. 임상 증상으로 분류하였을 때는 과민증상, 오 심, 가려움증의 순서로 보고 빈도가 높았고, regimen 별로는 FOLFOX, FOLFIRI, TC의 순서였다. 원인 약물은 oxaliplatin, irinotecan, docetaxel의 순서 로 빈도가 높았다.
WHO-ART 기준으로 보고된 유해사례를 CTCAE 기준으로 심각도를 재분류한 결과 grade 3 이상의 유 해사례는 408건으로, 원인약물은 oxaliplatin, doc- etaxel, carboplatin의 순서로 빈도가 높았다.
이번 연구를 통해, 항암제 유해사례에 대한 포괄적 인 국내 연구가 미비한 실정에서, WHO-ART 기준으 로 보고된 유해사례를 항암제 임상시험에서 사용하고 있고, 심각도 정보가 포함된 CTCAE 기준으로 접목시 켜 분석을 함으로써 국내 항암제의 부작용에 관한 임 상 정보를 제공할 수 있었다.
이 연구는 자발적으로 보고된 부작용을 기반으로 하 여, 실제 부작용 발현과는 차이가 있을 수 있으며, 후 향적 연구이기 때문에 WHO-ART 형식으로 보고된 유해사례를 CTCAE로 재평가 할 때에 의무기록 확인 에 어려움이 있어, 현재 항암제 유해사례 보고 시스템 의 한계점을 알 수 있었다.
따라서, 앞으로는 항암제 유해사례의 보고가 더욱 활성화 되어야 하며, 심각도와 regimen 등을 포함한 보다 체계적인, 항암제에 맞춘 유해사례 보고 시스템 이 필요하겠다.
참고문헌
1) Jose J. and Rao P.G. : Pattern of adverse drug reactions notified by spontaneous reporting in an Indian tertiary care teach- ing hospital, Pharmacol Res, 54(3), 226-233 (2006)
2) Lim K.H., Shin H.T., Sohn H.S. : Com- parison of WHO-ART versus MedDRA, internationally standardized terminology of adverse drug reaction classification.
Korean, J Clin Pharm, 17, 46-51 (2007) 3) World Health Organization Uppsala Table 3. Clinical manifestation of adverse events
classified by classes(NCI-CTCAE)
유해사례 계열별 분류 n (건)
Skin and subcutaneous tissue disorder 524
Gastrointestinal disorders 249
Immune system disorders 249
Investigations 166
General and administration site 147
Nervous system disorders 92
Vascular disorders 87
Respiratory, thoracic and mediastinal disorders 58