경피경관 혈관성형술이 혈관협착의 비수술적 치료방법으로 발전되어 왔으나 탄성반도(elastic recoil), 내막 박리 등에 의 한 재협착이 다발하여 이를 극복하기 위해서 금속 스텐트가 고안되었다. 그러나 스텐트들도 급성혈전증과 내피 증식에 따 른 만성 재협착이 발생하는 문제점이 노출되었다(1-5). 이러 한 재협착을 줄이기 위한 노력 중 하나가 덱사메타손(DM이 라 약함)을 피복한 스텐트의 사용이다. 그러나 보고자에 따라 DM이 신생내막형성에 미치는 영향을 다르게 보고하고 있다 (6-16). 이에 저자들은 장기간에 걸쳐 안정적으로 DM을 방 출시킬 수 있는 스텐트를 제작하고 이를 개의 대혈관에 삽입 한 후 신생내막의 변화를 관찰하여 이 스텐트의 신생내막 억 제 가능성을 알아보고자 하였다.
대상과 방법
실험동물
체중 21-32 kg (평균 26 kg)의 잡견 6마리를 3개월 추적 군(3마리), 6개월 추적군(3마리)으로 구분하여 실험하였다.
스텐트의 제작
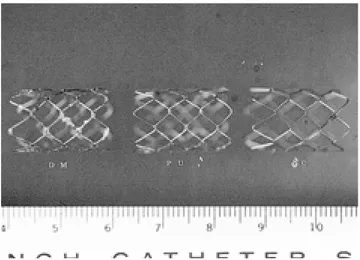
스텐트는 0.2 mm 굵기의 니티놀 세선(Nitinol wire, Euroflex, Germany)을 스테인레스강 재질의 틀에 꼬아서 다이아몬드 형 태의 격자를 갖도록 제작하였으며 완성된 스텐트의 길이는 20 mm, 직경은 12 mm 이었다. 총 36개를 제작하여 12개씩 3군 으로 나누어 사용하였다. 1군은 스텐트를 피복 시키지 않은 형 태(NC스텐트), 2군은 폴리우레탄(Polyurethane, Polymer Technology Group, Emmerville, CA, U.S.A.; 이하 PU라 약 함)을 피복한 형태(PU스텐트), 그리고 3군은 폴리우레탄과 DM(Sigma, St.Louis, MO, U.S.A.)을 피복한 형태(DM스텐트) 이었다 (Fig. 1). DM스텐트의 피복방법은 다음과 같았다. DM 96 mg을 Dimethylacetamide(DMAc) 8 ml에 넣고 상온에서
잡견 대혈관 모델에서 Dexamethasone 피복 니티놀 스텐트가 신생내막형성에 미치는 영향
1윤현기・박길선2・강성권3・박상수4・김태형5・성규보・송호영
목적: 덱사메타손(DM)과 폴리우레탄(PU)으로 피복된 니티놀 스텐트를 개의 대혈관에 삽입하 여 신생내막형성에 미치는 영향을 보고자 하였다.
대상과 방법: 니티놀 스텐트 36개를 6마리의 개의 하대정맥 및 대동맥에 설치하였다. 스텐트
는 덱사메타손이 함유된 폴리우레탄으로 코팅한 것(DM스텐트), 폴리우레탄만으로 코팅한 것 (PU스텐트), 코팅하지 않은 것(NC 스텐트) 3가지 종류를 사용하였다. 신동맥 혹은 신정맥기 시부 하방에 3종류의 스텐트를 그 순서를 달리하여 각각 설치하였다. 덱사메타손을 입힌 스텐 트에서 약물이 안정적으로 방출되는지 여부를 알기 위하여 체외 약물방출실험을 실시하였다.
스텐트설치 후 3개월(n=3)과 6개월(n=3)에 대동맥에서는 내막과 중막의 두께를 하대정맥에 서는 내막의 두께를 스텐트의 세선부위와 세선간격부위에서 측정하였다.
결과: DM스텐트의 약물방출실험 결과 스텐트 내의 DM중 25%가 처음 일주일 간에 방출된 후 3 μg/day의 비율로 6개월까지 방출되었다. 세선 부위의 대동맥 내막/중막비는 DM스텐트가 다 른 두 스텐트들에 비해 적은 수치이었으며(p<0.05), 대정맥 내막 두께도 DM스텐트가 PU스 텐트보다 적은 수치이었다(p<0.05). 그러나 이러한 차이는 세선 간격 부위에서는 감소되는 경 향이었고, 3개월 및 6개월 군간에 유의한 차이는 없었다(p>0.05).
결론: 잡견의 대혈관 모델에서 새로 고안된 DM 피복 니티놀 스텐트가 NC스텐트나 PU피복 스 텐트들에 비해 신생내막형성을 감소시켰다.
1울산대학교 의과대학 서울중앙병원 방사선과학교실
2충북대학교 의과대학 진단방사선과학교실
3조선대학교 의과대학 진단방사선과학교실
4서울보건대학 의공학과학교실
5울산대학교 의과대학 의공학과
이 논문은 2000년 2월 3일 접수하여 2001년 3월 2일에 채택되었음.
24시간동안 천천히 흔들며 녹여서 DM/ DMAc 용액을 만든 후 동량의 24% PU(in DMAc soln.)와 섞어 PU의 최종농도 12%, DM의 질량은 PU의 질량의 5%인 용액을 만들었다. 니 티놀 스텐트를 이 용액에 담근 후 꺼내어 40°C 오븐 속에서 건조 시킨 후 진공상태에서 DMAc성분을 완전히 증발시켰다.
이상의 과정을 4회 반복하여 스텐트의 표면이 DM과 PU의 중 합체로 균일하게 피복되도록 하였다. PU스텐트의 피복은 12%
PU 용액만을 사용하여 같은 방법으로 피복하였다.
체외 약물방출실험
분광측광기(Beckman Instruments Inc., Fullerton, CA, U.S.A.)를 이용하여 0.001-0.02 g/dL 농도범위에서 DM의 최 대흡수율인 265 nm에서 보정곡선을 그렸다. DM stent를 원 추형 관(Falcon tube, SA, France)에 넣고 0.1M 중성 인산염 완충액 4 ml를 가한 다음 37°C 항온기 내에서 천천히 회전 하도록 장치하였다. 일정 시간마다 원추형 관에서 용액을 빼 내어 265 nm에서의 흡수율을 구한 다음 미리 작성된 보정곡 선을 이용하여 방출된 DM의 농도를 구하였다. 일단 측정된 시점에서 새로운 중성 인산염 완충액으로 바꾸어주고 다음 시 점에서의 측정을 계속하였다. 측정은 초기 2일간은 3시간마다, 다음 5일간은 12시간마다, 그리고 그 이후에는 매일 측정을 하였고 어느 정도 곡선의 기울기가 정해진 다음에는 1주일에 1회씩, 6개월까지 측정을 하였다.
동물실험준비
실험동물은 실험 직전 케타민(20 mg/kg, 유한양행, 서울, 대 한민국)과 아트로핀(40mg/kg, 제일제약, 서울, 대한민국) 근 육주사로 진정시켰으며 실험 중의 마취는 펜토탈소디움(30 mg/kg, 중외제약, 서울, 대한민국) 정맥주사로 유도하였다.
스텐트 설치전 혈관조영술
실험동물을 수술대에 고정시킨 후 대퇴부위를 절개하였고, 대퇴동맥과 대퇴정맥을 각각 분리한 후 셀딩거씨법으로 대퇴 동맥 및 대퇴정맥을 각각 천자하여 5 French 굵기의 multi- purpose 카테터(COOK Inc, Bloomington, IN, U.S.A.)를 삽입 하였다. 조영제(Telebrix, Guerbet, France) 10 ml를 사용하 여 대동맥 조영술 및 하대정맥 조영술을 각각 시행하여 혈관 의 구조이상 및 신장동맥 및 신장정맥의 위치를 확인하였다.
하대정맥의 직경은 평균 9 mm (8-11 mm)였고, 복부 대동 맥의 직경은 평균 11 mm (10-12 mm)였다.
스텐트 설치
스텐트의 설치는 8.5 French굵기의 피포(COOK Inc, Bloomington, IN, U.S.A.)와 0.035인치 안내철사(Terumo, Tokyo, Japan)를 사용하였으며 스텐트 설치 전 헤파린 2,000 단위를 피포를 통해 주입하였다. 스텐트는 니티놀이 갖고 있 는 형상기억의 성질을 이용하여 얼음물 속에 담가 부피를 줄 여서 피포내로 삽입하였으며, 밀대로 스텐트를 밀면서 피포를 잡아 당겨 신장동맥 하방에 3개의 각기 다른 군의 스텐트를
설치하였으며, 신장정맥의 하방에도 3개의 각기 다른 군의 스 텐트를 장치하였다. 각 군의 스텐트의 위치는 혈관의 위치에 따른 굵기의 차이에 영향을 받지 않도록 상, 중, 하의 위치에 고루 배치하여 중복을 피했고(NC - PU - DM; NC - DM - PU; DM - NC - PU; DM - PU - NC; PU - DM - NC; PU - NC - DM), 각 스텐트 간에는 약 7 mm의 간격 을 두고 장착하였다. 스텐트-하대정맥비(stent to IVC diam- eter ratio)는 평균 1.32±0.14, 스텐트-복부대동맥비(stent to aorta diameter ratio)는 평균 1.1±0.08이었다.
스텐트 설치 후 혈관조영술
시술 직후 대동맥 및 대정맥 조영술을 실시하여 급성혈전 형성 등의 이상유무를 보았으며 시술 후 항응고제는 사용하지 않았다. 1주간격으로 복부 X-선 사진을 촬영하여 스텐트의 이 동 여부와 크기변화를 보았으며 실험동물을 희생하기 직전에 혈관조영술을 한번 더 시행하여 스텐트 내부와 주위의 협착의 유무 여부를 보았다 (Fig. 2).
병리표본 제작
다량의 펜토탈소디움 정맥주사를 이용하여 3개월 및 6개월 에 각각 3마리씩 실험동물을 희생시켰다. 사망 후 개복하여 대 동맥 및 하대정맥의 스텐트가 설치된 부위를 육안 관찰한 다 음 조심스럽게 적출하였다. 적출된 대동맥 및 하대정맥의 내 강을 10% 중성포르말린으로 10분간 씻은 다음, 같은 용액으 로 3일간 고정하였다. 고정 후 각 스텐트의 최상단, 최하단 및 중앙 부위 등의 3군데를 잘라서 스텐트의 세선을 조심스레 제 거한 다음 파라핀 포매시켜 헤마톡실린-에오신 염색을 하였 다. 단 스텐트가 이동되어 두개의 스텐트가 중첩되어 있었던 경우에는 중첩된 부분에서 약 5-7 mm 부위에서 절단하였다.
Fig. 1. Three stent types used. There are a NC-, a PU-, and a DM stent (from left to right). Each stent has diamond-shaped meshes, 2cm in length, and 12mm in diameter. DM stent was the thickest one.
병리조직 관찰 및 분석
광학현미경 하에서 대동맥 표본의 원위부, 중위부, 근위부에 형성된 신생내막 및 중막의 두께를 세선 바로 위에서는 세선 의 정점부위 즉 내강쪽으로 가장 돌출된 부위에서, 세선과 세 선 사이에서는 세선과 세선사이의 가장 가운데에서 microm- eter (Olympus,Osaka, Japan)를 이용하여 미크론 단위까지 측 정하였다. 하대정맥의 경우, 중막의 두께는 무시될 정도이므로 내막의 두께만을 같은 방법으로 측정하였다. 각 스텐트 별로 대동맥의 내막/중막비, 하대정맥의 내막의 두께를 비교하였다.
통계는 student t-test를 이용하였으며 5%의 유의수준에서 검 정하였다.
결 과 체외 약물방출실험
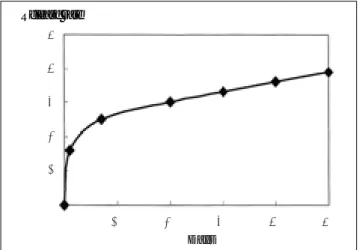
DM stent에 피복된 DM/PU의 질량은 평균 27 mg이었으며 DM의 평균함량은 스텐트 당 1.35 mg이었다. DM의 유리는 초기에는 매우 빨라서 24시간 동안 전체 함유 DM의 16%가 유리되었으며, 7일 동안에 25% 가 유리되었다. 이후 유리되 는 양은 6개월까지 측정 하였는데 하루 3 μg으로 일정하게 유 리되었다 (Fig. 3).
스텐트 설치
DM 피복에 의한 부피증가로 인하여 DM stent의 설치 시 에 피포와의 마찰력이 다른 두 스텐트들 보다 더 컸으나, 스 텐트 장착은 모두 성공하였다. SVR(stent to vessel ratio)은 대동맥에서 1.14-1.47 (평균 1.32), 하대정맥에서 1.0-1.25 (평균 1.1)이었다. 추적기간동안 하대정맥에서 3개, 대동맥에 서2개의 스텐트가 하방으로 이동하였으나 직하방의 스텐트와 겹쳐질 정도의 이동은 없었다. 희생 직전 혈관조영검사상 3개 월군은 모두 심한 혈관 협착은 없었으나 6개월군에서 대동맥 및 하대정맥의 PU stent 각각 1개에서 혈관벽에 치우친 내강 내 충만결손을 발견하였다.
육안조직 소견
혈관을 종축으로 절개하여 혈관내부를 육안관찰하였을 때, 모든 스텐트는 100% 내막으로 덮혀 있었으며 DM stent의 세 선이 다른 두 스텐트들보다 훨씬 선명하게 관찰되었다 (Fig.
4). 혈관조영검사상 내강내 충만결손을 보였던 PU 스텐트 2 개 중 한 예는 대정맥의 혈관벽이 세선에 의해 찢어지면서 두 꺼운 내막이 형성되어 있었다. 다른 한 예는 스텐트가 완전히 Fig. 2. The result of in vitro drug release test. 25% of DM in
DM stent was released within 7 days and then, the release rate was stabilized to 3μg/day.
A B
Fig. 3. Angiograms six months after stent placement.
A. Aortogram shows eccentric luminal narrowing at PU stent(arrow) which turned out to be folding of stent with thrombus formation. Otherwise, other stents shows no gross abnormalities.
B. Vena cavogram shows eccentric lu- minal narrowing at PU stent(arrow) which turned out to be excessive inti- mal huperplasia.
Release rate 0.5 0.4 0.3 0.2 0.1
0
0 10 20 30 40 50 Days
펴지지 않은 채 대동맥의 혈관벽과 스텐트의 간격에 혈전이 형성되어 있었고 SVR이 1.47로 가장 높았던 경우였다. 상기 의 문제가 발생한 PU stent들에서도 내막 및 중막의 측정을 하였으나 너무 오차가 커서 Smirnov의 기각검정법을 적용하
여 통계처리에서 제외하였다.
광학현미경 소견
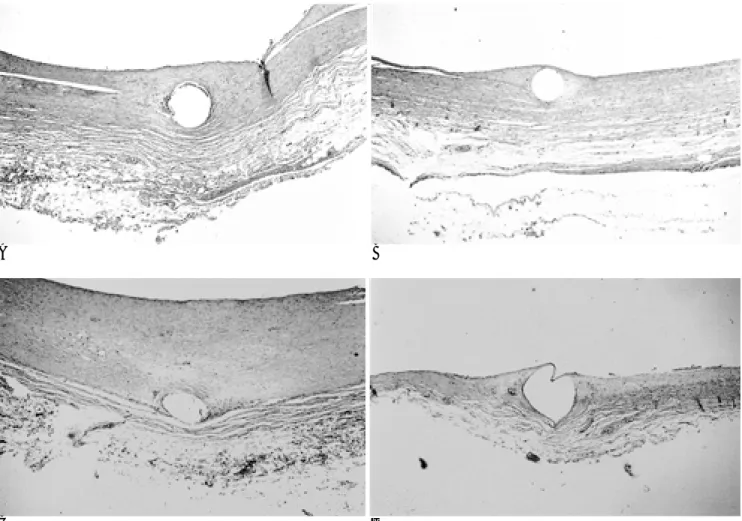
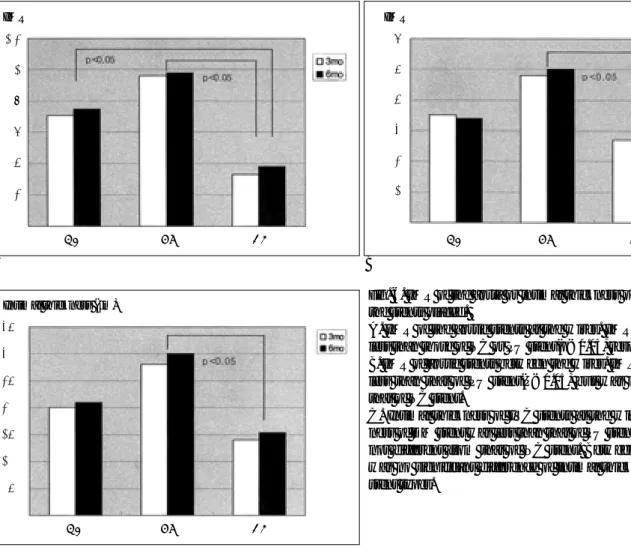
스텐트는 단면상 12개의 세선으로 이루어져 있으므로 한 스 텐트 당 세선 상부에서 36번의 측정값과 세선과 세선 사이에 서 36개의 측정값이 얻어져 총 72개의 측정값이 나올 수 있 으나, 조직 준비 과정 중에 불가피하게 손실되는 부위들이 있 어 한 스텐트 당 대동맥의 경우 평균 56개, 하대정맥의 경우 평균 52개의 측정값을 구할 수 있었다. 3개월군과 6개월군 사 이의 내막 및 중막의 측정치는 통계학적으로 유의한 차이가 없었다(p>0.05) (Table 1). 대동맥에서 중막의 두께는 각 군 에 따른 유의한 차이는 없었다(p>0.05). 반면 내막의 두께는 각 군에 따라 큰 차이를 보여 PU stent군, NC stent군, DM stent군 순으로 얇았다 (Fig. 5A, B). 하대정맥의 경우에도, 내 막의 두께는 PU stent군, NC stent군, DM stent군 순으로 얇 았다 (Fig. 5C, D). 대동맥의 내막/중막비는 세선 부위에서는 DM stent군이 다른 두 스텐트 군보다 유의하게 작았으며 (p<0.05) (Table 2), 세선과 세선사이 부위에서는 DM stent 가 PU stent보다 작았으나 (p<0.05) NC stent와는 유의한 차 이가 없었다 (p>0.05) (Fig. 6A, B). 대정맥의 내막 두께는 세선 부위에서만 DM stent군이 PU stent군보다 얇았고 통계 학적 유의성이 있었다 (p<0.05) (Fig. 6C).
고 찰
스텐트의 재협착은 40-50%까지 발생하며 대부분 시술 후 3-4 개월 이내에 시작되어 6개월에 완성된다 (1). 재협착은
Table 1. Tintima, Tmedia, at Various Portions of Three Types of Stent
Location Parameters Timing Intimal thickeness at the wires Intimal thickeness between wires NC(mm) PU(mm) DM(mm) NC(mm) PU(mm) DM(mm) Aorta Tintima (μm) 3 month 102±92 138±76* 050±54* 087±77 119±77 069±44 6 month 110±84 142±82* 048±39* 093±85 134±71 075±56
Tmedia (μm) 3 month 143±77 143±70 165±71 260±87 251±82 260±70
6 month 147±69 143±59 155±65 272±69 269±78 298±82 IVC Tintima (μm) 3 month 201±45 280±98$ 142±59$ 153±68 201±103 112±62 6 month 211±37 299±110$ 154±65$ 139±47 218±108 136±68 Tintima: intimal thickness, Tmedia : medial thickness, IMR : intima-to-media ratio
NC: Non-coated stent, PU: PU-coated stent, DM: DM/PU-coated stent
*; p<0.05, DM vs PU at the wires, ; p<0.05, DM vs NC at the wires,
; p<0.05, DM vs PU between the wires, $; p<0.05, DM vs PU at the wires Note. Data are the mean±SD
Table 2. IMR at Various Portions of Three Types of Stent
Location Parameters Timing Intimal thickeness at the wires Intimal thickeness between wires NC(mm) PU(mm) DM(mm) NC(mm) PU(mm) DM(mm) IMR 3month 0.71±0.23 0.96±0.41* 0.33±0.12* 0.35±0.12 0.48±0.27 0.27±0.09
6month 0.75±0.30 0.98±0.32* 0.38±0.09* 0.34±0.14 0.5±0.360 0.25±0.17 NC: Non-coated stent, PU: PU-coated stent, DM: DM/PU-coated stent
*; p<0.05, DM vs PU at the wires, ; p<0.05, DM vs NC at the wires,
; p<0.05, DM vs PU between the wires
Fig. 4. Opened view of abdominal aortic lumen. DM stent wires(middle one) were more clearly seen compared with that of NC stent(upper one) or PU stent(lower one).
혈관이 받게 되는 물리적 손상에 대하여 탄성반도, 내벽혈전 의 형성과 조직화, 신생내막 증식의 다단계반응을 거치며 혈 관의 만성적 기하학적 스트레스도 영향을 미친다. 탄성반도는 혈관이 심하지 않게 손상을 받는 경우 재협착의 중요한 원인 이 된다. 반면 손상이 심한 경우에는 내벽혈전이 급성으로 형 성되는 경향이 있으며 이러한 내벽혈전은 혈관 평활근세포 (smooth muscle cells: SMC라 약함)의 이동 및 증식에 필요 한 기질의 역할을 한다. 스텐트 삽입에 의한 기하학적 스트레 스로 인한 자양맥관의 손상과 저산소증, 중막의 압박으로 인 한 SMC의 손상 및 DNA합성의 증가 등이 동시에 발생하여 재협착이 진행되는 것으로 이해되고 있다. 이상의 반응을 차 단하기 위한 노력의 주된 목표는 SMC의 증식을 차단하는데 있다. 방사선요법, 유전자요법 등과 함께 약물을 사용하여 SMC 의 증식을 억제하고자 하는 실험들이 많이 진행되어 왔고 그 중 하나가 DM의 사용이다 (6-16). DM은 전술된 혈소판유 발성장인자 중 A-사슬의 형성을 차단, SMC 성장의 다른 자 극 원인인 interlukin-1 β유전자의 전사를 방해, mRNA의 안 정성을 저하, 세포의 성장에 중요한 c-jun/AP-1와 같은 핵 단백질의 작용을 억제할 뿐 만 아니라, 세포외간질의 침착을
방해하여 혈관재형성을 감소시킨다 (15).
Muller(7) 등은 돼지 경동맥의 스텐트 과신장 손상 모델에 서 DM을 20% 함유한 실리콘 중합체와 DM을 함유하지 않은 중합체를 손상된 경동맥의 외막에 각각 장치하였을 때 DM함 유 중합체가 혈관주위 섬유화는 현저히 감소시켰으나 내막의 증식을 억제하지는 못하였다고 하였다. Stone (8)등은 관상동 맥 풍선성형술 후 재협착이 발생한 102명의 환자를 대상으로 풍선성형술을 재시술하기 전날밤 및 당일아침에 methylpred- nisolone 125 mg의 근육주사와 시술 후 1주일간 매일 pred- nisolone 60 mg을 경구투여 하였을 때 재협착 예방효과가 없 었다고 하였다. 또한 Pepine(9) 등도 관상동맥 풍선성형술 시 술 전 methylprednisolone 1.0 g을 1회 정맥주사한 군이 대 조군에 비해 재협착 발생을 감소시키지는 못하였다고 하였다.
Lincoff(10) 등은 돼지 경동맥의 스텐트 과신장 손상 모델에 서 poly-L-lactic acid에 용해된 DM을 피복한 탄탈(tanta- lum) 재질의 스텐트를 설치하였을 때 28일간의 실험기간 동 안 DM이 지속적으로 잘 방출되었으나, 피복이 안 된 스텐트 를 설치한 대조군과 비교하여 신생내막의 증식을 억제하지 못 하였다고 하였다.
A B
C D
Fig. 5. Light microscopic findings of the abdominal aorta (A, B) and IVC (C, D) (H & E, ×40). The intima of the aorta at NC stent (A) was thicker than that at DM stent (B). The intima of the IVC at PU stent (C) was thicker than that of DM stent (D). These reactions were more prominent at the wires than between the wires.
반면 Colburn(11) 등은 토끼 경동맥의 풍선카테터 손상 모 델에서 DM 근육주사가 근내막 과증식 반응을 줄일 수 있다 고 하였다. Chervu(12) 등은 토끼 경동맥의 풍선카테타 손상 모델에서 DM근육주사군, cyclophosphamide근육주사군, aza- thioprine근육주사군, 대조군의 네 군으로 나누어 3개월 개통 율을 보았을 때, DM군과 cyclophosphamide군에서 각각 83.3% 및 100%의 개통율을 보인 반면 대조군과 azathioprine 군은 각각 62.5% 및 33.3%의 개통율(폐색의 원인은 혈전생 성에 의함)을 보여 DM이 효과가 있다고 하였다. Van Put(13) 등은 토끼의 정상 경동맥의 외막 주위에 실리콘 칼라를 2주 동안 장치하였을 때 신생내막의 증식이 일어나나 DM을 경구 로 혹은 피하펌프로 주입하였을 때 대조군보다 신생내막증식 이 억제됨을 보고하였다. Villa(14) 등은 쥐 경동맥의 풍선 카 테터 손상 모델에서 외막주위에 5% 및 0.5% DM 중합체로 감싼 군에서 대조군에 비해 각각 76% 및 75% 의 내막 대 중 막 두께비(intima to media ratio: IMR이라 약함)의 감소효과 가 있다고 하였다. Guzman(15) 등은 쥐 경동맥의 풍선 카테 터 모델에서 polylactic-polyglycolic acid 공중합체를 이용하 여 생체분해성 중합체를 만들고 여기에 형광물질을 붙여 손상 된 경동맥의 내강에 3분 동안 주입한 후 혈관벽을 성공적으 로 침투해 들어가며 2주후에도 고농도로 집적되어 있음을 증
명하였으며 또한 이 물질에 DM을 첨가하여 주입하였을 경우 대조군에 비해 31%의 IMR 감소 효과를 나타내었다고 보고하 였다.
이상의 문헌고찰에서 DM이 신생내막증식의 억제효과가 있 다고 추정은 되나 단발성 혹은 단기간의 투여만으로는 충분하 지가 않다고 생각되며 신생내막의 증식이 지속되는 3-6개월 의 장기간에 걸쳐 안정적으로 DM을 방출시킬 수 있는 스텐 트의 제작 및 사용이 가능하다면 재협착의 방지에 도움이 되 리라고 사료되어 본 연구를 하게 되었다.
DM이 피복된 스텐트의 제작은 여러 차례의 예비실험 끝에 본 실험과 같은 방법을 결정하였다. 피복의 중합체로서 폴리 우레탄을 선택하였는데 이는 생체적합성이 뛰어나 이미 각종 의료재료로 사용되고 있을 뿐 만 아니라 일정시간이 지나면서 함유하고 있는 DM을 서서히 방출할 수 있는 구조를 갖고있 기 때문이었다.
본 실험에서는 21-32 kg의 잡견을 대상으로 하였다. 개는 혈액응고체계가 사람보다 활발한 것으로 알려져 있어 스텐트 에 대한 혈전형성의 가능성이 사람보다 더 높다고도 볼 수 있 다. 개의 대퇴동맥 및 대퇴정맥을 박리하여 절개하는 데에 큰 어려움은 없었으며 스텐트 설치용 피포의 두께가 8.5 French 여서 다소 두꺼웠으나 삽입에 큰 어려움은 없었다.
A B
Fig. 6. IMR of the aorta or intimal thickness of IVC according to the stents placed.
A. IMR of the aortic stents at the wires. IMR of DM stent was less than those of NC or PU stent(p<0.05, respectively).
B. IMR of aortic stents between the wires. IMR of DM stent was less than that of PU stent(P<0.05) but was not different from that of NC stent.
C. Intimal thickness of IVC stents at the wires. Intimal thick- ness of DM stent was less than that of PU stent(P<0.05) but was not different from that of NC stent. Between the wires, there was no significant difference of intimal thickness among three stent types.
C IMR
1.2 1 0.8 0.6 0.4 0.2 0
NC PU DM
Intimal thickness (μm) 350
300 250 200 150 100 50 0
NC PU DM
IMR 0.6 0.5 0.4 0.3 0.2 0.1 0
NC PU DM
스텐트의 SVR은 예비실험에서 개의 대동맥의 직경이 약 10 mm로 측정되어 1.2의 SVR를 만들기 위해 12 mm로 제작하 였으며 하대정맥의 경우에는 SVR이 1.1로 다소 낮았으며 이 에 따라 3개의 하대정맥 스텐트의 하방 이동이 발생하게 되 었다. 대동맥의 SVR은 평균 1.3으로서 다소 과신장된 양상이 어서 내막의 증식을 좀 더 유발할 수 있는 조건을 갖추었으나 하대정맥의 경우에는 내막증식의 효과가 감소될 수 있었다. 본 실험에서 스텐트의 지름이 12 mm인 한 종류만 만들었기 때 문에 SVR을 일정하게 유지하기 위해서 체중이 비슷한 잡견을 사용했어야 하나 그렇지 못했던 점이 본 실험의 하나의 제한 점이었다. 그러나 이렇게 낮은 SVR에서도 대정맥이 심한 내 막 증식을 보인 점은 시사하는 바가 크다고 할 수 있다.
조직반응의 측정은 내막 및 중막의 부위별 두께 측정을 하 여 합산을 하였으며 내막과 중막의 면적이나 면적비를 구하지 는 않았다. 본실험의 측정횟수가 충분히 많아 면적을 굳이 산 출하지 않더라도 통계학적 유의성을 가질 수 있다는 판단에서 IMR을 비교하였으며 특히 세선 부위와 세선과 세선 사이에서 의 조직반응의 차이를 나누어 분석하기 위한 목적도 있었다.
본 연구의 결과는 DM stent가 개의 대동맥과 하대정맥에서 신생내막의 증식을 억제하는 효과가 있음을 보여주고 있다. 그 러나 이러한 억제의 효과는 세선 부위에서보다 세선과 세선 사이 부위에서 감소하는 경향을 나타내었는데 이는 세선 주위 에서 약물의 조직농도가 세선에서 멀리 떨어진 조직에서 보다 높기 때문일 것으로 생각된다. 본 실험의 제한점은 스텐트 설 치후 혈중 농도와 희생후 조직의 약물 농도를 측정하지 않았 으므로 약물의 조직농도와 신생내막 증식의 억제정도의 상관 관계를 확인하지 못한 점이다.
현재까지 DM의 국소 전달을 위해 중합체를 사용한 연구보 고 중 Linchoff(10) 등은 돼지의 경동맥의 스텐트 과신장 손 상 모델에서 poly-L-lactic acid를 스텐트를 장치하였으며, Muller(7) 등은 역시 돼지의 정상 경동맥의 외막 주위에 실리 콘 칼라를 장치하였으나, 모두 신생내막증식의 억제에 미치는 영향이 부정적이었음을 보고하고 있다. 그러나 Linchoff(10) 등의 실험은 28일간의 단기 성적이었으며 Muller(7) 등은 내 막보다는 외막에 약물의 영향을 더 줄 수 있다는 점에서 한계 가 있을 수 있는 실험이었다고 생각된다. 그러나 본 실험은 내 막에 최장 6개월까지 영향을 주면서 장기성적을 얻은 점에서 앞의 두 실험과 차이가 있으며 원형 팽창력과 같은 스텐트 자 체의 물리적 성질, 이물반응, 실험동물의 종이 다른 점 등에 의해서도 상이한 결과가 도출될 수 있을 것이다.
동맥에 대하여 많은 연구들이 있었던 이유는 주로 폐색성 동맥질환에 대한 경피경관 혈관성형술이나 스텐트 삽입이 이 루어져왔기 때문이다. 그러나 최근에는 이러한 치료가 정맥의 폐쇄성 질환에 있어서도 활발하게 이루어지고 있으나 이에 대 한 조직학적 연구는 많지 않다. 따라서 본 연구에서 하대정맥 에서 조직반응을 연구한 것은 의미가 있다고 사료되며 특히 SVR이 낮았음에도 대동맥보다 하대정맥의 내막증식이 현저하 다는 점을 확인할 수 있었다.
이상적인 스텐트란 협착 부위에 장착되어 원활한 혈류를 회
복시키고 혈전 등의 급성조직반응이 적을 뿐 만 아니라 만성 적으로 재협착을 적게 가져오는 스텐트라 할 수 있다. DM stent가 개의 대동맥 및 하대정맥에서 내막증식의 억제를 가 져온다고 해서 인간에서도 같은 반응이 일어날 지는 의문이 며, 내경이 작은 관상동맥이나 말초혈관에서도 같은 결과를 가 져올지 여부는 더욱 의문시된다. 따라서 궁극적으로 이러한 스 텐트가 인체에 사용되기 위해서는 본 연구를 보완하는 많은 실험이 있어야 한다고 사료된다. 우선 보다 고농도의 DM을 함유할 수 있는 안정적인 구조를 갖는 피막을 개발할 필요가 있으며 대퇴동맥 등의 좀 더 작은 혈관구조에서의 유용성도 입증하는 것이 바람직하다. 세선과 세선 사이의 내막증식 억 제효과를 높이기 위해 현재의 모형을 수정한 스텐트의 개발도 또한 요망된다. 현재 이와 유사하게 헤파린 피복 스텐트의 연 구도 활발히 진행되고 있듯이 여러 약제가 혼합된 스텐트의 개발도 기대되나 이는 각 약물간의 상호작용 등 보다 복잡한 연구가 되리라고 보인다.
결론적으로 새로운 DM피복 니티놀 스텐트가 잡견의 대혈 관에 장착되었을 때 대조군 스텐트들에 비해 신생내막의 형성 을 현저히 감소시켰다.
참 고 문 헌
1. Dangas G, Fuster V. Management of Restenosis after Coronary Intervention. Am Heart J 1996;132:428-436
2. Carter AJ, Laird JR, Farb A, Kufs W, Wortham DC, Virmani R.
Morphologic Characteristics of Lesion Formation and Time Course of Smooth Muscle Cell Proliferation in a Porcine Proliferative Restenosis Model. J Am Coll Cardiol 1994;24:1398-1405
3. Schwartz RS, Edwards WD, Bailey KR, Camrud AR, Jorgenson MA, Holmes DR. Differential Neointimal Response to Coronary Artery Injury in Pigs and Dogs. Implications for Restenosis Models. Arterioscler Thromb 1994;14:395-400
4. Fontaine AB, Spigos DG, Eaton G, et al. Stent-Induced Intimal Hyperplasia: Are There Fundamental Differences Between Flexible and Rigid Stent Designs? J Vasc Interv Radiol 1994;5:739- 744
5. Kornowski R, Hong MK, Tio FO, Bramwell O, Wu H, Leon MB.
In-Stent Restenosis: Contributions of Inflammatory Responses and Arterial Injury to Neointimal Hyperplasia. J Am Coll Cardiol 1998;
31:224-230
6. Prescott MF, McBride CK, Venturini CM, Gerhardt SC. Leukocyte Stimulation of Intimal Lesion Formation is Inhibited by Treatment with Diclofenac Sodium and Dexamethasone. J Cardiovasc Pharmacol 1989;14:76-81
7. Muller DW, Golomb G, Gordon D, Levy RJ. Site-Specific Dexamethasone Delivery for the Prevention of Neointimal Thickening after Vascular Stent Implantation. Coron Artery Dis 1994;5:435-442
8. Stone GW, Rutherford BD, McConahay DR, et al. A Randomized Trial of Corticosteroids for the Prevention of Restenosis in 102 Patients Undergoing Repeat Coronary Angioplasty. Cathet Cardiovasc Diagn 1989;18: 227-231
9. Pepine CJ, Hirshfeld JW, Macdonald RG, et al. A Controlled Trial of Corticosteroids to Prevent Restenosis after Coronary Angioplasty. Circulation 1990;81: 1753-1761
10. Lincoff AM, Furst JG, Ellis SG, Tuch RJ, Topol EJ. Sustained Local
Delivery of Dexamethasone by a Novel Intravascular Eluting Stent to Prevent Restenosis in the Porcine Coronary Injury Model. J Am Coll Cardiol 1997;29:808-816
11. Colburn MD, Moore WS, Gelabert HA, Quinones-Baldrich WJ.
Dose Responsive Suppression of Myointimal Hyperplasia by Dexamethasone. J Vasc Surg 1992;15:510-518
12. Chervu A, Moore WS, Quinones-Baldrich WJ, Henderson T.
Efficacy of Corticosteroids in Suppression of Intimal Hyperplasia. J Vasc Surg 1989;10:129-134
13. Van Put DJ, Van Hove CE, De Meyer GR, Wuyts F, Herman AG, Bult H. Dexamethasone Influences Intimal Thickening and Vascular Reactivity in the Rabbit Collared Carotid Artery. Eur J Pharmacol 1995;294:753-761
14. Villa AE, Guzman LA, Chen W, Golomb G, Levy RJ, Topol EJ.
Local Delivery of Dexamethasone for Prevention of Neointimal Proliferation in a Rat Model of Balloon Angioplasty. J Clin Invest 1994;93:1243-1249
15. Guzman LA, Labhasetwar V, Song C, et al. Local Intraluminal Infusion of Biodegradable Polymeric Nanoparticles. A Novel Approach for Prolonged Drug Delivery after Balloon Angioplasty.
Circulation 1996;94:1441-1448
16. Strecker EP, Gabelmann A, Boos I, et al. Effect on Intimal Hyperplasia of Dexamethasone Released from Coated Metal Stents Compared with Non-Coated Stents in Canine Femoral Arteries. Cardiovasc Intervent Radiol 1998;21:487-496
J Korean Radiol Soc 2001;44:433-440
Address reprint requests to : Hyun-Ki Yoon, M.D., Departments of Radiology, University of Ulsan College of Medicine, 138-736 서울시 송파구 풍납동 388-1
Tel. 82-2-3010-4379 Fax. 82-2-476-4719 E-mail: hkyoon@www.amc.seoul.kr
Influence of Dexamethasone-Coated Nitinol Stent on Neointimal Formation in the Canine Great Vessel Model
1Hyun-Ki Yoon, M.D., Kil-Sun Park, M.D.2, Sung-Gwon Kang, M.D.3, Sangsoo Park, Ph.D.4, Tae-Hyung Kim, BS.5, Kyu-Bo Sung, M.D., Ho-Young Song, M.D.
1Departments of Radiology and 5Biomedical Engineering Asan Medical Center, University of Ulsan College of Medicine
2Department of Diagnostic Radiology, Chungbuk National University College of Medicine
3Department of Diagnostic Radiology, Chosun University College of Medicine
4Department of Biomedical Engineering, Seoul Health College
Purpose: To evaluate the effect of dexamethasone(DM) and polyurethane(PU)-coated nitinol stent on neointi- mal formation in the canine great vessels.
Materials and Methods: Thirty-six nitinol wire stents were implanted in the abdominal aorta and inferior vena cava(IVC) of six dogs. In each animal, six different types of stent (NC, non-coated; PU, polyurethane coated;
DM, DM and polyurethane coated) were serially positioned in permutationally possible order in the aorta be- low the renal arteries and in the IVC below the renal veins. For DM stent an in-vitro drug release test was per- formed to determine the stability of DM release. The thickness of the intima and media of the aorta and of the intima of the IVC were measured three (n=3) or six months (n=3) after stent placement at and between the wires.
Results: In the in-vitro study, 25% of DM was released during the first week, and the subsequent release rate was 3 μg/day for 6 months. The intima-to-media ratio of DM-stented aorta was less than in aortas where PU or NC stents were used (p<0.05). The neointima thickness of DM stent in the IVC was less than that of PU stent (p<0.05). These differences were less prominent between the wires than at them, and there was no significant difference between the three-and six-month groups (p>0.05).
Conclusion: In this canine great vessel model, newly designed DM-coated nitinol stent decreased neointimal formation.
Index words :Stents and prostheses Drugs
Aorta, graft and prosthesis Venae carae, graft and prosthesis