Kortan J. Appl. Microóiol. Bioeng.
Vol. 5. No. 2.
89~98.1977
抗生勳質과 代謝括抗
---그 作用機序률 中心으로---
朴 富 +. 仁l
江康大學 農化學科
Antibiotics and Antimetabolite
Boo
Kil Park
Dept. of Agr. Chemistry. Gang Weon University. Chun Cheon.
(Received J uly 8. 1977)
用機序를 細뼈의 代謝와 관련지워 해명하려고하는 머 릿 말 연구가 진행되어왔고 또 長足의 進前을 보이고 있 抗生物質 (antibiotics) 이 란 微生物 기 타 細뼈의 發 다.
育을 限害하는 微生動의 生塵勳을 말한다. 세포는 이 러 한 抗生物質의 作用機序가 分子生物學에
71
그 생명을 유지하기 위하여 여러가지의 代謝를 영 초를 두고 연구됨에 따라 抗生動質이 代謝홈抗횡 위하고 있다고 한다연 抗生動質은 微生物퉁 細뼈의 質로써 作用하고있는 것이 정정 밝혀지게되고 따 말육증식에 필요한 必須代짧에 作用하는 것으로 라서 生物옮抗動質 (antibiotics, 抗生빼質)과 代짧 생각되여진다. 그러나 抗生物質은 처음부터 代謝
옮抗勳質 (antimetab이ites) 처 럼 , 必須代謝勳質(esse.
ntial metabolites)
과 化學構造가 유사한 물질 을 합성 하여 그것을 가지고 必須代謝物質의 作用을 E且害 하기위한 의도로 연구가 시작된것은 아니다.자연계에 널리 존재하는 抗生物質은 19세기경부 터 흩§察되 여 온 微生物 상호간의 *솜抗現훌을 일으키 는 物質로서 分離되여 그 연구가 시작된 역사적 배 경 을 보더 라도 抗生物質과 代謝括抗物質과는 상관 없이 각각 발견되고 또한 그 연구도 무관계하게 진 전되 었다고 말할 수 있겠다. 1930年代에
para amino
安息香數의 代謝홈抗物質로서 슬폰아미드륨I가 화 려하게 그 연구를 전개한 관계로혜서 Fleming 의penicillin
發見 (1929年)이 빛 을 옷보고 抗生뺑質의 연구는 약 10년간 암혹시대플 거쳤다. 그뒤Florey
둥에 의 한pencillin
의 再開짧 (1939"-'1없O年) 및 Wak뾰umn 둥에 의 혜streptomycin
이 發見 (1944年) 된 후에야 비로서 그 연구가 활발하게 되었다는 사실을 생각혜볼때 代짧옳抗物質의 연구가 抗生행 質의 연구를 지연시켰다고 하는 견해도 있게 된다.그러나 최금 分子生物學의 진보에 힘업어, 微生 物둥 세포의 發育增植을 R且害하는 抗生物質의 作
*농抗~質 (antimetabolites) 과의 개 념 이 점 점 융합되 여 가는 경 향이 있다. 그러 나 抗生秘質과 代謝옮抗
~質과는 그 역사적 배경과 발전경과가 다르며 다 만 그 作用機序에 있어셔 抗生빼質윤 代謝括抗~
質的인 연에서 해연되여가고 있다고 볼수있겠다.
그러나 抗生動質의 作用擬序는 아직 그 일부밖에 밝혀지지않고 있으며 抗生物質 전반에 걸친 作用 機序의 해영이 代짧옮抗의 헤벨에서 이혜되여가야 한다고 생각되여지냐 현재까지 불가능한 상태에 놓여있다.
여기서는 다만 지금까지 알려져있는 사실을
7T
반A로, 일부의 抗生빼質에 관한 그 作用農序를 代 謝옮抗의 觀點에셔 간단히 서솔하고져 한다.
1. 뼈홉의 뼈뼈훌
glycopeptide
슴成系와 抗호빼 톨의 作用細홉이 細R힘훌의 基本흙造인 gly∞'peptide
(pep-
tidoglycan.
mlκopep다de,murein
둥£로도 풀리 운 다)의 生合成系에 作用하는 抗生빼質이 몇개 알려 져있다 Glyco야ptide 는N
.acetylmurax띠C 앙미d(MNAc) , N-acetylglucosamine(GNAc)
및 J홈빼de 흘 • 成單位로하는polymer
로써 細홉꿇률 둘러 싹는M
GNAc-MNAc-acceptor
pentapeptide
l
’
transpeptidatiün - Penicill in
, CephalosporinC
’
cell
wall glycopeptide(murein
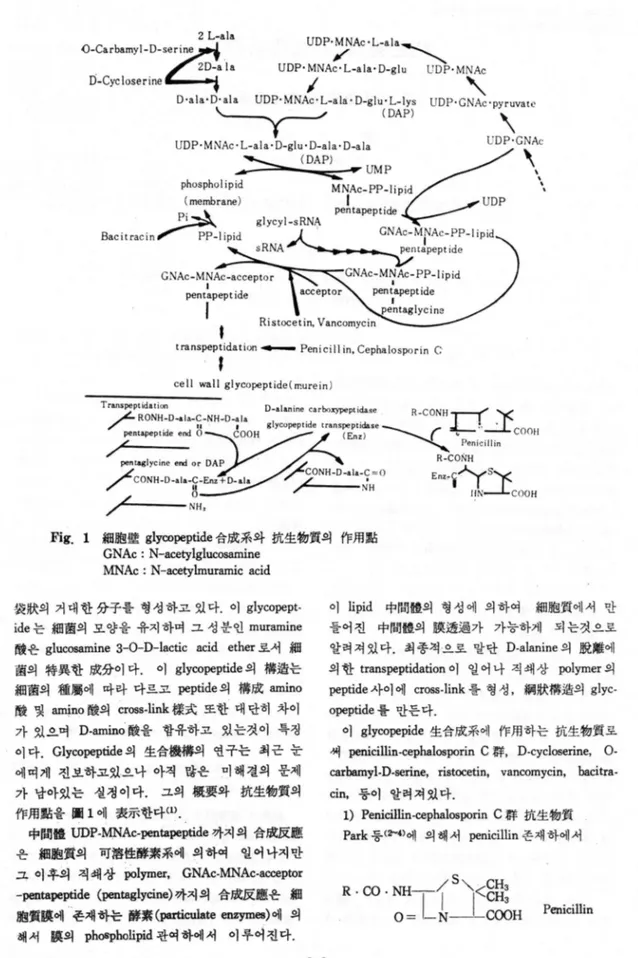
)Fig. 1
細뼈慶 gly,∞peptide 合成系와 抗生物質의 作用點GNAc : N-acetylglucosamine
MNAc : N-acetylrnurarnic acid
짧狀의 거 대 한 分子를 형 성 하고 있 다. 이
glycopept.
이 1ipid 中間體의 형 성 에 의 하여 細뼈質에 서 만 ide 는 細홈의 모양을 유지하며 그 성분인muramine
을어진 中間體의 題透過가 가능하게 되는것으로 했윤glucosamine 3-0-D-lactic acid
ether 로셔 細 알려져있다. 최종척£로 말단 D-alanine 의 脫離에 園의 特異한 成分이 다. 이glycopeptide
의 構造는 의 한transpeptidation
이 일 어 나 직 쇄 상polymer
의 細園의 種屬에 따라 다르고 peptide 의 構成amino
peptide 사이에 cross-link 흘 형성, 網狀構造의glyc-
嚴 및arnino
醒의 cross-li빼 樣式 또한 대 단히 차이opeptide
흘 만든다.가 있£며 D-arnino 嚴을 함유하고 있는것이 특정 이
glycopepide
生合成系에 作用하는 抗生物質로 이 다.Glycopeptide
의 生合機構의 연구는 최 근 눈 써penicillin-cephalosporin C
群,D-cycloserine, 0-
에띠게 진보하고있으나 아직 많은 미해결의 운제 @뼈rnyl-D-serine,ristocetin
,vancomycin
,bacitra-
가 낭아있는 실갱이다. 그의 樓要와 抗生勳質의cin ,
둥이 알려져있다.作用點을 뼈 1 에 表示한다(1) 1) Penicillin-∞phalosporin C 群 抗生행質 中間體
UDP
-MNAc-pentapeptide 까지의 슴成反應 Park 동(~예에 의해서 penicillin 존채하에서 은 細臨質의 可홈性홉¥素系에 의 하여 얼어 나지만그 이 후의 직 쇄 상
polymer , GNAc-MNAc-acceptor
-따ltapeptide (뼈ltaglycine) 까지 의 合成反廳온 細 뼈質題에 촌채 하는 篇素(particulate
웬zymes) 에 의 해서 題의 phospholipid 관여하에셔 이루어진다.R . CO . NH-1- { S 'ì<짧
0= 1-N_LCOOH
- 9 0 -
Penicil1in
/ 5\
R. CO. NH---
,I
-CH
2 . R'0=
----"' \.;/ CephalosporinC 群cboH
햄養한 細園에
UDP.MNAc-pentapeptide
가 축적 되 는것이 관찰되 고 이 것이 細R잉현좋glycopeptide
合成 의 며1 間體인것이 확인된 후 penicillin 의 作用點이 細뼈밸glycopeptide
깜成系에 있다는것이 定說로 되 여 있 다. 이 그룹의 抗生物質은 細뼈慶glycope.
ptide
合成系의 최 종 단계 인glycopeptide transpepti.
dase 反應및 D.alanine carboxypeptidase 反應을 租害 하는것으로 알려져있다. 이들 抗生檢質은 그 化學 構造가 細服훨
glycopeptide
合成의 中間體와 類似 하기 때문에 꿇質과 疑合해서 基質대신에 上記의 解素活性 中心과 삶合함으로써 §¥素í'F用을 E且害하 는것으로 推定되고 있다(圖 1 참조) . 이 U且害作用의 원인으로써 앞서 말한 構造類似性이 제창되고 있는 데Collins , Richmond
둥 (5) 은N.acetylmuramic acid
와,
Wise
,Park
둥 (6)은 L.ala.D.glu 와 Tipper,5tro.
minger둥(7)은
D.ala.D.ala
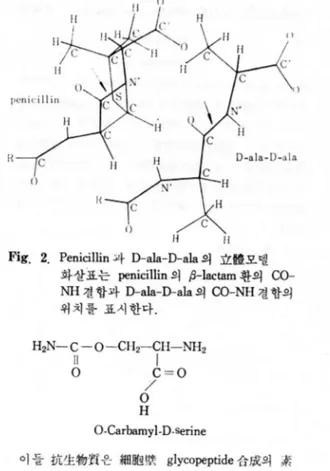
과 그 構造가 닮아있다고 주장하고있 다. 그중 Tipper,5trominger
동은glyc.
opeptide transpeptidase
가 中間엠의 D.ala.D.ala 부 분에 작용해 맏단의D-ala
을 遊離시 켜 (圖2
의 오 른쪽 화살표) ð흥素와 中間體의 結合物을 만든다고 하면penicillin
存在 F에 서 이 解素는 역 시penicillin
의 ß-lactam 짧을 U덤짧해서 (圖 2 의 왼쪽 화잘표)penicilloyl enzyme conjugate
플 만든다고 말하고 있 다([웰 1 의 우하 참조)이 假,;Q의 論않는
penicllin
의 éE物活性의 中心 이 되 는 反뻗:性높은 ß-lactom 環의co-r ‘ H
結合과D-ala.D.ala
의 CO-NH結삼이 分子模型에 서 같은 위치를 차지하고 있다는 짐이다(圖 2 참조) .中問샘의 직 쇄 상
poymer
와penicillin
및cephal.
osporin
C
가 이 §¥素에 대해서 魔合的으로 作用하는지 ~W鏡合ú'~으로 ('F用하는지 는 확션한
data
가 없!3...며 또한
D.ala.D.ala
과 이 들抗生物質의 構造類似 性도 약간의 論點은 있으나 現在로써는 定說로 되 여있다.2) D.Cycloserine;
O.carbamyl.D.serine
CH
2-CH-NH
2o c=o
\ N/
H
D.Cycloserine
CH
3-CH-NH
2C=O O /
H D.Alanine
{)
냈l!
H
/"
l! IC
\1)
l!
R
기6D-ala-D-ala
/ε l‘ ~H
I~ C
1)
서 H
Fig. 2. Penicillin
과D-ala-D-ala
의 立體모텔 화살표는penicillin
의 껴-lactam 환의CO- NH
결 합과 D-ala-D-ala 의CO-NH
결 함의 위치를 표시한다.H
2N-C - 0
-CH
2-CH- NH
2o C
=O
O /
H
O.Carbamyl.D.serine
이 들 抗生物첩은 細뼈l!.t;
glycopeptide
合成의 素 材인 uridine nucleotide precursor 合成의 初期단계플~Jl.害한다 즉
D-cycloserine
은 D.alanine 과 그 化學 構造가 닮아있 어D.alanine
의 옮抗4'kJ質로써alanine racemase
및 D.ala.D-ala synthetase 에 대 해 基質과 鏡合的으로 作用한다(圖 1 참조) . 이들 醒素의 훌1;質생용度에 대한
Michaelis
定數는 Km=5XlO-3M인 대 비 하여D-cycloserine
은K
i=5
XlO-5M
이 다 즉 이들효소는 기칠보다 D-cycloserine 과 100 倍나 강 하게 結合하기 때운에 결국 D-cycloserine 은 이을 효소反應을 姐뽑해 서 細뼈雙glycopeptide
의 f1成을 저해한다(8- 10)
O--Carbamyl-D-serine 도
D-cycloserine
과 마찬가 지 로 D-alanine 과 유사한 樞造를 하고있 으며D- alanine
과 鏡合的으로alanine racemase
反應을 저 해 한다K
i=5
XlO-4M
이 다1J) O--Carbamyl-D-serine 과 D-cycloserine 간에는 현저한 相乘的 抗園作用을 보이는데 이것은 연속적으로 일어나는 뚫素反應에 대 한 限害, 즉 sequentialinhibition
에 의 한 相乘í'r' 用 때 문이 바고 한다(12)3)
Ristocetins , vancomycin
이 들 抗生빼質은 細뼈堅
glycopeptide
合成中에 셔lipid 中間體,
GNAc-MNAc-p- p-lipid
에 서 칙 쇄 상pentapeptide
(p야en따lαtaglycine)
의 polymer 흘 만드는
polymerization
反應을 뼈害한 다(13) 이 뚫素는 細8힘體에particulate enzymes
의 形 으토 存在하고 있다. lU$tocetins A
,B
및vancomy-
cin 은 모두 多觸體抗生物質로lipid
中間體 部分 (-G NAc~~,mAc-)과 構造類似性에의 한 括抗作用으로 생각되여지나 이들 抗生物質의 化學構造가 아직 決定되어었지 않기 때문에 定 ,ilt이마고는 볼 수가 었다.t) Bacitracirt
H I:l • S -CH
,
/ 0
디 I , C I1,-C - C - (:. ν
、,,- C - - C• L- Lf'!t
CII, NH
, ’
,’ H
/ ’
/
/ / I)-A 시r→ N fI, 0• Gll1
/
/ • |
!)-p!w --* t.-llìs-+1.""" 서 .1.
• ε↓
r.-lIellL-lI ν" • IJ- Orn • L- Ly-" ~
Haeitl"í.lcin !\
Bacitracin
완 peptide 抗生物줬로써 細8생현좋glyco-
合成系의
P-P-1ipid
•P-lipid+Pi
反應에 관여 하는 옳素 反應을 저 해 한다. 이 것은 Micrococcus Iyso.deikticus 의
particulate
enzyme 을 사용해 서 밝혀 진 사실 이 기 때 문에 (14) ll4.icrococcus lysodeikticus 의 細 R빙뿔glycopeptide
의 構造및 그 生合成系가 포도상 球園및 大題園의 그것과 달라(圖 3 창조) 일율적 으로 말할수 없£나 편의상 bacitracin 의 l'FfH짧i 을 圖 1 에 표시했다.2. Nucleotide
生슴成系와 흉호物質의 作用Nucleotide
의 生合成및 그의polymerization
응-뻐 害하는 抗生物質이 몇 가지 있다. 이들의 大짧分응 뼈j癡作用을 나타내 며 動物의 移植性 睡짧에 대해 넓은tumor
spectrum 을 나타내는것이 특정이다.그려나 싣제 임상척으로 사용되고 있는 것은 거의 없다.
이 들 抗生₩質은 그 作깨機序에 있어 f\;;謝括:j/L의 樣式이 비 교척 확실하으로 몇 가지 소개 한다 Purinè
nucleotide
生合成系의 陽要를 圖4
에 表示한다. 이 生合成系는 初期段階서 부터ribose-5-phosphate
가 反應에 관여 하므로nucleoside monophosphate
가 양e novo 合成의 主經路가 되 여 있 다.Pyrimidine
生合成 系에 서 도orotidine monophosphate
이 후의 反應系가 同-하다고 볼 수 있다./싫
/시 미//ι
시L
/
A
ι
-
(/써 새 /써’써!ι’야!싸 M/써
C
M/
빠
l“ /N
A
ω
폐쉰 이l 펀
/ i
…
/
-
//
/
빠
내 싸/“ l
싸/M /
J
M/ν 애
/
y
싸
4
//
mlJ
/뼈 싸
/
G
/f 펀’써 l 람써
μl써
/써/J
랜
” “
/써
…
싸
y
싸
M/
μ‘
J
빠
/빠l
채L폐l
바 μ낀/빼|싸써빠 γμl 꽤
MιιγLM
/싸
l
Fig. 3.
細服뿔Peptidoglycan
의 춰훌造樣式圖 (1) 포도상 구균 (Staphylococcus aureus) (2) Micrococcus lySl.짜eikticus(3)
대 장균 (Escherichia coli)- 9 2 -
\
ιvlH 、
1{jnp
ln
/
남’
H
뺏
H
α
|니 l / ι1“ 、。Pι
-
슨14
ll.
,
우 -씨 -a
-pe
개‘
짜(願 빠
pl
J 때
M
T-
때C F -- u“
시4애 우 ι 「
얘 g·
H 낸O
F P-
glycine
NH
,
?H2 GAR
c=o
NH R
..s’
-p@
차THFQ
fi @110-여rH
,
N .Jl...-"
NN‘
,~ νν2 ‘ U μ ‘ ::-;-!IJ H,
N-CHC-N 、11 - N:C’ ~ H.나 ?r Á.C C.. ‘ N、C)
HO -f7추←←← g:lUL•‘
mlne l &-5 -P R-5’ _p NH’ ‘ HC-AIR
I
aspa때 AIR R-5' -PI
aspartate FGAMf웠끄fE:〉
• HNJfE > 騙::f[3‘
R-5' l' AICAR R-5‘ _P H R-5~P
꾸
)
FR잉 때
mR
、、
Ju‘
、f‘
/
\
””
Ol l C
ν
· ‘ 2
;
rl
R
σ
SAICAR F-AICAR
uH
시 씨r N \ _ t f
i
“
tl / ~.Iutarninp Hσ 、.;~.... 、N' 0R-5’-P
6MP ι(
XMP 、 N1'"γN
<D
glutamine al)lagol)istlfrr
bON. rluazomyein)
l U
(2)f이 ic acid &ra뼈 」---A ‘N 、?
dump•d1:MP CH
,
-COO’
! ,,~ R-5’
-PL
, . / IMPNH
,
NH-CH-C∞ H~/ ' aspartate
?\ιNλ 7\,-,N、
N 1T' 、 N' γ 、
~NJlN ) - ~ N J. N ì A-5
’ -PAMP 이MP-S
1"'1&
4, P\1rine Nucleotide 生合成系와 抗生物質의 作用點PRPP : 5--Phosphoribosyl-l-pyrophosphate R-5-P: Ri뼈~5-,l?hosphate
PRA : 5-Phosphoribosyl-l-amine GAR : Glvcinamide ribotide
FGAR: N-formylglycinamide ribotide FGAM : N-Formylglycinamidine ribo벼e
C-AIR : 5-Amin
0-
4-earboxvimidazole ribotide F-AICAR : 5-Formamid←4갑rboxy-imidazole ribotide AIR : 5--Aminoimidazole ribotideAICAR : 5-Amino-4-carboxamidoimidazole ribo뼈e
SAICAR: 5-Aminoimidazole-4-N-succinylo carboxamide ribotide IMP : Inosine-5' -phosphate
XMP : Xanthosine-5
’
-phosphate GMP': Gilanosi.ne-5’-phosphate AMP:,
Adenosine-5' -phosphate AMP-S : Adenylosuccinate ribotide1)
Cordycepin( = 3 ’ -Deoxyadenosine) , formycin.
HN2
NH
2'" H
/\\ /i~ 、
/ \ / N \
N N N
l'\
>.r/ 、/!
、
...
, / i~N \ /
HOH2~
.~_ NOH2C 1 / 0 "-1
1/0-이 \_/
\_~
11
1 Cordycepin
OH OH
OH Formycin
이들
adenosine
analog 의 抗生物質은 生體內에서5'-OH
가 인 산화反應을 거 쳐mon
o-,di-
,triphos- phate
가 되 여, nucleotide
生合成系종의5-phospho- ribosyl-1-pyrophosphate
生成反應(R-5-P+ATP•
PRPP+ AMP)
을 限害한다(15-17)이 姐害는 抗生物質 自體보다in
vivo 에서 인산화된것이 더욱 강하다.(圖 4 참조) 또한 cordycepin 은
in
vivo 에서 인산 화되 여RNA
또는DNA
중에 직접 들어 감으로써 異常核짧을 生成해서 核醒 또는 蛋白質 生合成을 姐춤한다(18-19)Adenosine
은cordycepin
의 인산화 反應에 홈抗的£로 作用한다.2)
Azaserine( =O-
Diazoacetyl-serine) , DON (=6- diaz
o-5-ox
o-L-norleucine)
,duazomycin A (= N- acetyl OON) , alazopeptin (L-alanyl- (6-diazo-5- ox
o-)-L-norleucyl- (6-diazo-5-oxo) - L-norleucine)
이을 抗生빼質윤 대개 통일한 作用을 나타내며 그중에서도 azaserine 과 OON 이 잘 알려져있다.
이 들윤
glutamine
과 그化學構造가 類似하기 때 문 에glutamine
括抗物質로써nucleotide
生合成을 U且 t융한다.%cH-co-0-CH2-CH-∞OH
N/
NH
2N\
11
)CH-CO-CH2-CHz-CH-COOH
Azaserine
N/
‘OON: R=H
NHR
DuazomycinA: R=CH
3CO H2N-CO-CH2-CH2-CH-COOH
NH
2Glutamine
Purine nucleotide
生合成系에 는glutamine
이 관 여되는 3 種의 홉素反應이 있는데 이들 反應을 천 부 眼훔하나 특히N-formylglycinamide
(FGAR) 에 서N-formylglycinamidine (FGAM)
으로 되 는 反應 을 캉하게 姐害한다Azaserine 은 이 蘇素와 훌抗 的으로 結合하는것요로 알려져있다(圖 4 창조)(20-잉)또한
pyrimidine nucleotide
合成系에 있 어 서 는 따idine nucleotide
에 셔cytidine nucleotide
의 合成강)-(23)
, shikimic acid-5-phosphate
에 서p- aminobenzoic acid
및anthranilic acid
의 合成 (24) ,deamide-NAD
에서NAD
의 合成等의 여 러 反應에 도glutamine
이 관여 하는 관계 로azaserine
과OON
에 의 해 서 g且 害된 다고 보고 되 여 있 다Azase띠.e,DON
等은glutamine
옮抗빼質로써 이 들옳素反應을 E且뽑하는 외에 alkyl 化홉j로써도 作用한다는것을 염두에 두어 야한다.3) Hadacidin(=N-Formyl hydroxyamino acid)
acetlc
OHC- N -CH2-COOH OH
Hadacidin
은asparagine
嚴과 鏡合的으로 t.1iÐt해 서adenine nucleotide
生合成을 R且害한다. 즉aden- ylosuccinate synthetase (IMP + ASP
•AMP-S)
의f 'f
用을 강하게 限害한다(圓 4 참조) (엉)
4) Angustmycin A
및C
Angustmycin A (= Decoyinine)
와angustmycin C ( =
Psicofuranine) 는nucleoside
抗生動質로써adeno- sine
,inosine
,xanthosine
,guanosine
等의nucleosides
에 의 해 홈抗된다. 이 들 抗生物質은adenosine ana- log
로서GMP synthetase
反應(XMP aminase; XMP +ATP+Glu(NH2)
또는NH
3•GMP+AMP
+PPi)
융 姐害한다. Angustmycin 의 作用은 基質과 非鏡 산的이 며allosteric inhibition
으로 얄려 져 있 다NH
2/ \ -N 、
N
、、 /-N/
N
CH2=ι O y
\ - ( CH.OH
1 1 χOH OH
Angustmycin ANH
2/\
,- N 、 N 1 LN /
、/
N
HOCH. 21/ , /0 , \ | ,
l \ -( ICH.OH
1 1 ιOH OH Angustmycin C
Angustmycin
존재 에서 細홉(抽草홉) 을 培養할 경 우 培地中에xanthosine
의 훌積이 나타난다(26-29)이 사실은 上記의 作用點을 支持하는 것으로 생치 된다.
Angustmycin A , C
는 둘다adenosine
anat빼 로써cordycepin , formcin
둥과 같이PRPP
의 生)反應에도 영향을 미치나
in
viνo 에서 인산화 反뺑 은 일으키지 않는다.- 9 4 -
3.
核훌슴成과 抗生物質의 作用Nucleotide
가polymerization
을 거 쳐 核嚴이 되 는 反應을 짧훔하는 抗生動質이 몇가지 었 다. 그중의 대 부분이DNA
와 結合해서DNA
를 주형 으로하는RNA
혹은DNA polymerase
反應을 限害한다. 이 경우 抗生物質의 活性은 DNA 에의해 씀抗되서Lineweaver-Burl ‘
曲線을 그려 보연 抗生物質과pri-
mer-DNA
간에 는polymerase
反應에 鏡合的인 括抗 을 나타낸다. 그러나 이것은 外觀上의 문제이고RNA
혹은DNA polymerase
反應은 다른 §¥素反應 과 달라 基質外에 주형을 필요로 하기때문에 보통 의 代짧浩抗과는 그 내용이 다르나 여기서는 간단 히 소개한다.Actinomycin ,
(30)chromomycin
A3(31l동은 주로DN
A의 guanine 부분과 결합해서RNA
p이ymerase 와DNA polymerase
反應을 姐害하며 전자의 反應을 더 욱 강하게 뼈害한다 chromomycinA3
와DNA
와의 結合에는 Mg++ 가 관련되있다.Streptoni맑in(32) ,
pluramycin(33) , echinomycin , dau-
L-valine- N -CH3 CH3- N -L-valine
i
gL-proline fne 쐐 m L-proline
。 D-valine
D• valine 0
1- L-thr~nine L-Ithreoninel
CO co
/ l \ /
N 、/1、_NH 2
1 _ "
、/\ 0 /、/-v
CH3 CH3
Actinomycin D
‘ Q
이 샤
OH
OMe
Chromomycin A3
o
11CH ‘
3o
\ / \ / 、” ” l
NCOOH
HoN/ \/ \ / \ / \ /
"" N
o H~N/、 /\CH 3 HO, )
\ / \
/、/
CH
30
1OCH
3Streptonigrin
nomycin
,nogalamycin
,Cinerubin
등도DNA
와 結 合해 서DNA
및RNA polymerase
反應을 租좁한다.그외
mitomycin C , phleomycin , bleomycin , sarko
-mycin
등도DNA
合成을 限害하는 抗生物質에 속 한다.4.
훌白슴成과 抗生物質의 作用훌蛋白合成은
ribosome
이 다 불리 우는 細B힌顆원(上CH
3 CH3\ /
/]/N 、
객C
젠3 CH3 CH 0
、 /\N./'\ c -N-CH-c -N-dH- c -야
-CH-C-N-CH-Co 0
H0 0
CH2
~H\0
| ζ
\ SCH
3d o c&
‘JO
Oc닙2/ H
11
./'C-CH-N-C-CH- N-C-CH-N-C-CH-N-C "T
./' H
\./'''\/、o
,CH3 CH3 / CH CH3 \ CH3 CH3
、N/\/Echin~~며흥
O
-s
chloramphenicol erythromycin mikamvcin B bottromycìn fusidic acid puromycm blasticidin S sparsomycm
GA G A .\익 mRNλ
5
•3'/
streptomycin, kanamycin.
kasngamycin. tetracycline.
mikamyc i n A. 1 incomyc in, cnomvcin. edeine. phenomycin
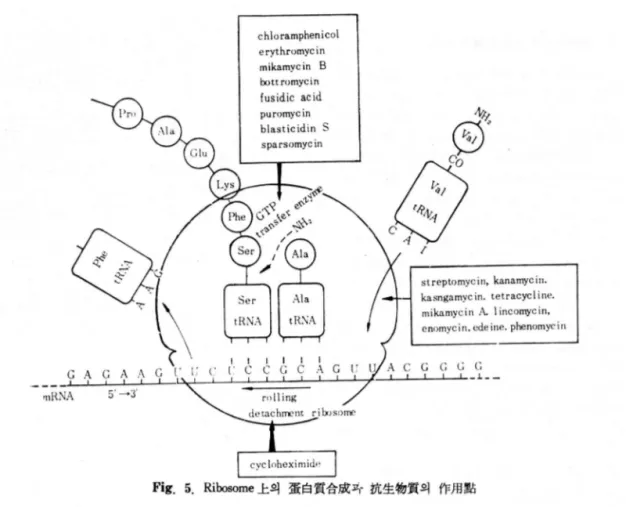
Fig. 5. Ribosome 上의 蛋白質合成곽 抗生행質의 作用點
·에 서 mRNA 의 관여 하에 서 peptidyl-tRNA 의 pep- tide 의 C 末端에 aminoacyl-tRNA 가 轉移하므로써 進行된다(뼈 5 참초) .
즉 각각의 amino 嚴운 ATP 존재 하에 서 각각의 特 異떠인 活性化뚫素에 의해셔 活性化되어 aminoacyl -AMP 가 되 여 §¥素와 結合한 中間體를 형 성 한다.
다음에 이것이 tRNA 의 末端의 adenosine 의 3'-OH 와 結合하므로써 aminoacyl-tRNA 가 된다. 各 am- ino 1짧은 1개 以上의 特異的인 tRNA 가 있 으며 ribo.
"Some 上에서 mRNA 의 特異的인 3 개의 훌基配列 triplet(c여on) 에 對應하는 tRNA 의 triplet 부분 (an
ticodon) 에 의혜 mRNA 의 codon 과 結合한다. 이 러 한 蛋白質 合成파갱 중에 amin얘cyl tRNA 형 성 까지 의 반웅에 作用하는 抗生物質은 없고 주로 rib∞0- me 上에서 때inoacyl-tRNA 에서부터 蛋白質이 合 成되 는 여 러 過뚫을 姐害하는 抗生:1ØJJ質이 여 러 가 지 알려져있다. 이충 aminoacyl tRNA 와 ribosome RNA 複合짧와의 結合을 P且害하는 抗生행質로써 :streptomycin
,
kanamycin,
kasugamycin,
tetracycline,
mikamycin A
,
lincomycin,
enomycin,
phenomycin,
edein 等이 있으며 ribosome 上에 서 amin<영cytRNA 부터 蛋白質형성 과갱 의 ammo 嚴 뼈移反應을 組害 하는 抗生物質로써 chloramphenicol
,
erythromycin,
mikamycin
B ,
bottromycin,
fusidic acid,
puromycin,
blasticidin
S,
sparsomycin,
cycloheximide 둥이 알려 져 있다.그중 cycloheximide 는 mRNA 와 ribosome 파의 운동 (rol뻐g) 및 mRNA 와 ribosome 의 解離흘 @且 害하는 抗生物質로서 그作用機序가 注 目되 고 있다 (뼈 5 창조).
이 러한 蛋白合成系에 作用하는 抗生횡質들운 蛋 白合成系가 대 단히 복잡한 관계로 아칙 分子레 벨 에서 그 作用옳序가 확실히 밝혀진 것은 드물며 또한 代짧結抗의 홉念에셔 그 作用農序률 셜명하 기 도 현재 로써 는 매 우 곤란하다. 그러 나 puromycin 에 관해서는 그 作用홉序가 代짧홈抗이 라는 측연 에서 解明되 있기때문에 여기 간단히 소개한다.
Puromycin 의 껴훌造는 蛋白質合成의 中間體인
aminoa양ItRNA 의 amino 짧 末端과 類似하기 혜 문 에 (構造式 창초) ribosome 위 에서 때in∞cyl tRNA
- 9 6 -
와 括抗해서 야ptide 쇄와 結合한다. 따라서 때1-
noacyl tRNA
가ribosome
과 結合하지 못하고ribo-
some 에서 유리된다. 그 結果 蛋白質合成이 中途 에서 끝내 완전한 蛋白質合成이 이루어지지 않는 다. 이 따應을puromycin
反應이 다고도 하며 다음 다과 같이 나타낼 수 있다34)Peptidyl-tRNA-ribosome+puromycin
•peptidyl- puromycin
+tRNA+ribosome_N(CH3
h
f' N\/
、 N\ N / \ /
HOCH
2 ,.N
\ / \l
\ _ / I I
NHOHo=
d-CH-CH?/-、-∞H3
' ... - " ' 1 . . 1 .2\==/-VV
J..I.3
NH2Puromycin
NH2
f' N\/
、N\ 1"
N / \ /
R'OCH2,, '
N\/V\|
\ _ /
1 1 OHO O=C-CH-R
R; Amino
산 잔기의 나 머지 부분R'; tRNA의 나머지 부 NH2
Aminocyl-tRNA
그외의 蛋白質合成을 姐害하는 抗生狗質에 대해 서 도 將來에 는 代謝옮抗的인 面에서 그 作用擬序 가 밝혀지리라고 생각되나 현재로써는 확실치가 않다.
Blasticidin S
와같은aminoacyl nucleoside
抗生物 質 또는 chloramphe띠col 둥에 대 해 서 도 그 化學構 造와 蛋白質合成 姐홈作用과의 관련성을 여러가지 로갤명한 說이 있으나 假짧에 지나지 않으며 여기 서는 생략하기로 한다.5. Vitamin
代빼에 作用하는 抗生物톨合成化學 癡法륙tl로써 는
sulfonamides
및PAS
(p- amiriosalicylic acid)
퉁이 葉嚴生合成系에 홈抗的으 로 作用하는 것으로 알려져 있으나 抗生物質에는 vitamin 生合成에 fF用하는것이 드플다. 현재 알려져 있는 것으로는
actithiazic acid
(=thiazolidone
antibiotics) 가 있£며biotin
生合成系의desthiobiotin
→biotin 合成反應을 P且害하는것으로 알려져있다.
그 作用은
biotin
에 의해서 鏡合的ξL록 浩抗된다.O
11
/\NH
S \
(CH2)sCOOH
Actitl넌azic
acid
맺 음 말
抗生物쩔의 f'F用樓序에 관하여 그 作用을 代謝 浩抗이 략는 面에 셔 살펴 보았다. 細뼈뿔;
glycopeptide
合成系에 作用하는 抗生物質에 관해 셔 는Strominger
일파의 lff究흘 中心A로 최근 그 내용이 현저하게 진보했으며 代謝홈抗의 面에셔 그 의 作用繼序가 정정 밝혀지고 있다.또한
nucleotide
및 核앓合成系에 관여 하는 抗生 物質의 作用도 代짧홈抗의 觀點에셔 어느정도 밝 혀지고 있다.그러 나 蛋白質合成系에 作用하는 抗生빼質온 그 選揮毒性이 뛰 어 나는 중요한 抗生物質이 많음에도 불구하고 蛋白質合成이 複雜하고,
ribosome
이 라는 細뼈顆함에서 蛋白質合成이 이 루어 지 며 , 遺傳情報 의홉達形式이 밝혀져있는蛋白質合成뚫素일지라도 그 정제가 곤란하며 따라서 뚫素의 性質도 밝혀져 있지앉은 現狀이다. 蛋白質 合成系에 관여하는 항 생 물질의 ff'用點을 代謝옮抗의 面에서 論하는것은 우리라고 생각된다. 그러나 蛋白質 合成系의 문제 흘 分子生행學의 中心課題의 하나로 많윤 lff究者 들이 빠究하고 있는실정이고보연 열지않은 장례에 이들 抗生빼質의 作用이 分子레벨에서 理解되리라 고 사려되는 바이다. 그것은 순학문적인 연에서 뿐만아니라 새로운 化學薦法빼의 開發둥의 實用面 에서도 큰 意義를 갖는것으로 생각되는 바이다.文
1) J _ L Strominger:
and D_ J _ Tipper ,
(1967)_
K.
* Izaki ,
M_Matsuhasi
Federa.tion Proc .•26 , 9
2)
J. T. Park: J .
Biol. Chem., 194, 877 (1952)_3) J. T. Park
andJ. L Strominger
: Sciena,
125,
99 (1957)_4) J. L Strominger , J. T. Park and
R.E.
Thomson:
J.Biol. Chem. ,
앓4,3263 (1959).
5)
J. F.
Collins and M. H. Richmond:Nature, 195 , 142
(1962).6) E. M. Wise and]. T. Park: Proc. Natl.
Acad. Sci.
, 54..75
(1965).7)
D. J. Tipper and J. L. Strominger: ibid. ,
54, 1133 (1965).
8)
J.
L.Strominger , E. 1to and
R.H. Threnn:
J.
Am. Chem. Soc. , 82 , 998 (1960).
9)
F. C. Neuhaus and J. L. Lynch:
Biochemistrν,3 , 471
(1964).10) U. Rose and J.
L.Strominger: Mol. Phar.
11I
acol. , 2 , 92
(1966).11) N. Tanaka: Biochem. Biophys. Research Co- mmun. , 12 , 179 (1963).
12) N. Tanaka and H. Umezawa ,
J.Antibiotics, 17 , 8
(1964).13) J. S. Anderson , M.
Matsuhasi, M. Haskin and J.
L.Stromìnger: Proc. Natl. Acad.
Sci. , 53 , 881 (1965).
14) G. Siewert and J.
L.Strominger: ibid. , 57, 767(1967) .
15) F. Rothman and A. J. Guarino: Biochim. et Biophys. Acta, 80 , 632 , 640 (1964).
16)
K. Overgaad-Hansen:ibid. , 80 , 504 (1964).
17) T.
Sawa, Y. Fukagawa , Y. Shimauchi ,
K.It
o , M. Hamada , T. Takeuchi , and H. Umez- awa: J. Antibiotics , 18 , 259 (1965).
18) M. A. Rich , P. Meyers , G. Weinbaum , J.
G.
Cory and R. ].Suhiadolnik: Biochim. et Biophys. Acta , 95 , 194 (1965).
19) J. G.
Cory,
R.J. Suhadolnik , B. Resnick and M. A. Rich: ibid. , 103 , 646 (1965).
20) J. M. Jr. Clark and J. K. Gunther: ibid. , 76 , 636 (1963).
21) S. C.
Hartman, B.
1ιevenburgand J. M.
Buchanan: J.
Am.Chem. Soc. , 77 , 501 (1954) ,
J.Biol. Chem. , 1221 , 1057 (1956).
22) H. O.
Kammen
뻐d R.B. Hur1bert: Biochim.
Biophys. Acta ,
30, 195 (1958).
23)
R. B.Hur1bert and H. O.
Kammen: J.Biol.
Chem. , 235 , 443 (1960).
24) P.
R.Srinivasan and B. Weiss: Biochim.
Biophys. Acta , 51 ,
597(1961).
25) H. T. Shigeura and C. N. Gordon:
J.Biol.
Chem. , 237 , 1932 , 1937 (1962).
26)
L.Slechta: Biochem. Biophys. Research Com.
mun. , 3 , 96
(1960).27) T. T. Fukuyama and
H.S. Moyed: Bioche- mistry, 3 ,
1얘8(1964).
28) H. Kuramitsu and H. S. Moyed:
Biochem.
et Biophys. Acta , 85 , 504 (1964).
29) N. Tanaka:
J. Aηtibiotics,16 , 163 (1963).
30)
J. Hurwitz , J. J. Furth , M. Ma1amyand M.
Alexander: Proc. Natl. Acad. Sci. U. S. , 48 , 1222 (1962).
1. H. Goldberg and M.
Rabinowitz: Science , 136 ,
315 (1962).E. Reich ,
1.H. Goldberg and M. Rabinowitz:
Nature, 196 , 743
(1962).G. Hartmann , U.
Coy and G. Kniese: Z.Physio
l.Chem. , 330 , 227
(1962).31)
H.Hartmann , H. Goller ,
K.Koschel , W.
Kersten and
H.Kersten: Biochem. Z. , 341 , 126 (1964).
D. C. Ward , E. Reich and
1.H. Goldberg:
Science, 149 , 1259 (1965).
Y. Kaziro and M. Kamiyama: Biochem. Bio- phys. Research. , Commun 19 , 433
(1965).32) N. S. Mizuno: Biochim etal Biophys. Acta, 108 , 394 (1965)
.33) N. Tanaka ,
K.Nagai , H. Yamaguchi and H. Umezawa: Biochem. Biophys. Research Commun. , 21 , 328
(1965).34) M. B. Yarmo
\insky and G.
L.de 1a Haba:
Proc. Natl. Acad. Sci. U. S. , 45 , 1721
(1858).A. Morris and
R. Scweet:Biochim. et Biop- hys. Acta , 47 , 415 (1961).
D. W. Allen and P. C. Zamecnik: ibid. , 55 , 865 (1962).
D.