ARTICLE Vol. 3, No. 1, May 2010
논문접수일: 2010년 4월 5일 / 심사완료일: 2010년 5월 7일
교신저자: 정준기, 서울시 종로구 연건동 28번지, 110-744, 서울대학교병원 핵의학과 Tel: 02-2072-2530, Fax: 02-745-7690, E-mail: jkchung@snu.ac.kr 이 종설은 2009년 범산학술상 기념 종설논문입니다.
갑상선암에서 핵의학 진료 연구
서울대학교 의과대학 핵의학교실
정준기
Research on the Management of Thyroid Carcinoma Using Nuclear Medicine Technique
June-Key Chung, MD, PhD
Department of Nuclear Medicine, Seoul National University College of Medicine, Seoul, Korea
After specific accumulation of iodide in the thyroid gland was found, nuclear medicine techniques including radioactive iodine have been important roles in the management of differentiated thyroid cancer. For the detection of cancer recurrence/metastasis after thyroidectomy, serum Tg measurement is the most sensitive modality. However, it is affected in the presence of anti-Tg antibody. Persistently elevated anti-Tg antibody levels appear to serve as a useful marker for residual cancer. A significant number of differentiated thyroid cancer patients had negative Tg level with negative anti-Tg antibody despite a positive radioiodine scan finding. Diffuse liver uptake on whole-body scan without thyroid remnant or metastasis suggests hidden metastases. FDG PET scan localizes metastatic sites in radioiodine scan-negative carcinoma patients with high accuracy. We found that lung metastases were completely resolved in 35%, and partially resolved in 40% after I-131 therapy. The treatment to bone metastasis needed combination therapy with surgical resection or external radiation therapy. When patients are refractory to the conventional fixed dose of I-131 therapy, the administration dose could be increased within maximal safe dose based on radiation dose to the bone marrow.
The other could be using retinoic acid to induce re-differentiation and to restore the accumulation of radioiodine in cancer cells. NIS activity is the molecular basis of radioiodine therapy in thyroid cancer. Several medications have been investigated to enhance the expression of NIS gene and protein. The recent cloning and characterization of the NIS gene has paved the way for the development of novel radionuclide gene therapy. This novel therapy is being improved by several modified approaches, and can be applied in the near future.
Key Words: Thyroid cancer, Radioiodine, Nuclear medicine, Treatment, Gene therapy
필자는 1977년 전공의 시절 범산 고창순 교수님을 대학원 지도 교수로 모시고 인연을 맺은 후 지난 33년 동안 선생님의 지도를 받아왔다. 선생님은 학문뿐만 아니라 인생살이 모든 분야에서 지침을 주시고 어려울 때 헌신적으로 도와 주셨다. 이런 필자에게는 범산학 술상 수상이 무엇보다도 영예롭고 감회가 크다. 이 자 리를 빌려 대한갑상선학회 회원 여러분께 감사드리고, 선생님의 만수무강을 축원 드린다.
1915년 갑상선에 요오드가 선택적으로 흡수된다는
것이 밝혀지고, 그 후 방사성요오드를 인공적으로 만 들게 되면서 갑상선질환의 진단과 치료에 이용하기 시 작하였다. 1940년에 미국 Harvard 대학의 Joseph Hamilton이 갑상선암 조직에 방사성요오드가 섭취되 는 것을 관찰하였고, 1943년 New York Montefore병원 의 Samuel Seidlin이 갑상선 전이암 환자에서 방사성요 오드치료를 성공적으로 시행하였다.1) 우리나라에서는 1959년 이문호, 고창순 교수가 방사성요오드를 처음 사 용하였고, 1980년 조보연 교수가 갑상선암 환자에서 대
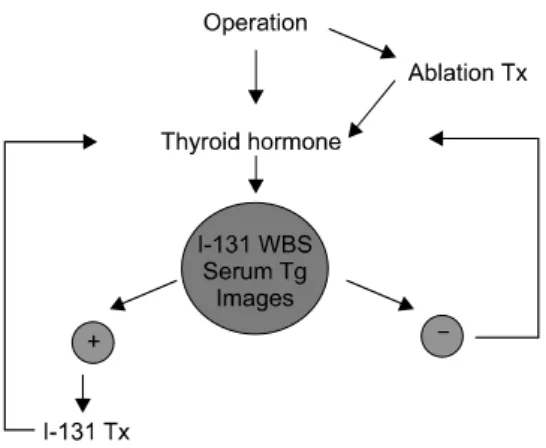
Fig. 1. Scheme of management in patients with differentiated thyroid carcinoma.
량의 방사성요오드 치료를 시작하였다.2)
갑상선암의 진료에 아직도 핵의학적 방법은 유용하 게 사용되고 있다. 분화성 갑상선암의 경우 2∼3병기 이상이면 갑상선 전절제술 후 I-131로 잔여조직을 제거 하고 갑상선 호르몬으로 TSH 억제 치료를 계속한다.
정기적으로 혈중 갑상선글로불린(thyroglobulin, Tg)을 측정하고, 방사성요오드로 전신촬영과 초음파, CT 등 으로 영상촬영을 시행한다. 재발/전이암이 발견되면 다량의 I-131로 치료한다(Fig. 1). 이 논문에서 필자는 핵의학교실에서 그동안 갑상선암 환자에서 핵의학적 방법으로 진료하고 연구하였던 내용을 소개하겠다.
핵의학적 진단법
혈청 Tg 측정
갑상선암 환자에서 수술 후 혈중 Tg 농도는 재발/전 이암을 조기에 발견하는데 아주 유용하게 쓰인다. 특 히 TSH가 자극된 상태에서 혈중 Tg 농도는 예민하게 암의 유무를 반영한다고 알려져 있다. 실제 대한내분 비학회에서는 저위험군 환자에서 혈중 Tg 농도와 경부 초음파검사만으로 추적 관찰하도록 권고하고 있다.3)
그러나 Tg 측정에는 몇 가지 문제점이 있다. 우선 660 kDa의 큰 분자량인 Tg는 수십 개의 항체를 만드는 항원결정인자(epitope)를 가지고 있다. 제조사마다 다 른 항체를 이용하므로 Tg 측정키트는 서로 다른 결과 를 보일 수 있다. 또, TSH 자극 상태에서 Tg 농도의 기준치도 실험실마다 다르다. 갑상선 잔여조직을 수술 과 방사성요오드로 제거시켜도 일부 조직은 남아있게 된다. 수술자에 따라 또 병원에 따라 이러한 잔여조직 의 양이 서로 다르기 때문에 혈중 Tg의 절대 값이 다르 게 된다. 이외에도, 혈청에 항-Tg 항체가 있으면 면역
측정법 원리 상 Tg가 위음성으로 나타난다. 항-Tg 항 체는 갑상선암 환자의 10∼25%에서 존재하고 있어 문 제가 된다.4) 림프절에 작은 병소가 있거나 분화도가 낮 은 경우 혈청 Tg의 진단 예민도는 떨어진다는 보고도 있다.5)
항-Tg 항체의 의미
그러나 혈청 항-Tg의 항체 농도를 추적하면 재발암 의 진단에 도움이 되기도 한다. 혈중에 노출된 Tg의 자 극에 의하여 항-Tg 항체가 기억세포에서 만들어지므 로 최근에 항체가 높은 농도로 증가하면 암의 재발을 의미할 수 있다.
저자는 412명의 분화성갑상선암 수술환자에서 혈청 Tg (TSH 자극), 항Tg 항체의 농도를 측정하고 추적관 찰 소견과 비교하여 보았다.6) 220명에서 TSH 상승 시 에도 혈중 Tg가 측정되지 않았고, 항-Tg 항체가 175명 은 음성이며 51명(22.6%)은 양성이었다. 항-Tg 항체가 양성인 환자 중 반수인 25명에서 나중에 재발암이나 전이암이 발견되었다. 즉 적지 않은 재발/전이암에서 항-Tg 항체에 의하여 Tg가 위음성으로 나타난다. 이 연구에서는 혈청 Tg가 음성인 환자 중 11%에서 항-Tg 항체로 재발/전이암을 의심할 수 있었다. 재발/전이암 의 경우 혈중 항-Tg 항체 농도가 1,124±1,879 U/ml으 로 완전관해 환자 520±724 U/ml보다 높았다. 완전관 해 환자에서는 수술 후 혈중 항-Tg 항체농도가 75%에 서 점차 감소하였다. 즉, 재발/전이암이 있는 경우 항 -Tg 항체의 혈중 농도가 관해 환자보다 더 높고, 또한 항체의 농도가 지속적으로 증가하면 재발/전이를 의심 하여야 한다.
항-Tg 항체의 음성이면서 Tg 위음성
이러한 몇 예가 이태리에서 보고된 바 있다. 저자는 824명에서 4년 동안 방사성요오드 제거술(ablation) 후 얻은 전신스캔을 분석하였다.7) 이중 255명에서 혈중 항-Tg 항체가 음성이면서 Tg도 음성이었다. 이들의 전 신스캔에서 203명은 잔여 갑상선 조직만 스캔에서 발 견되었으나, 52명(6.3%)에서 스캔에 재발/전이암에 방 사성요오드 섭취가 있었다. 즉 적지 않은 경우에 항-Tg 항체가 없으면서도 Tg가 위음성인 것이다. 혈중 Tg가 양성인 경우와 비교하여, 경부나 종격동 림프절에 재 발/전이암이 있는 경우에 혈중 Tg 위음성이 많았다. 이 러한 경우 전신 방사성요오드스캔이 도움이 된다.
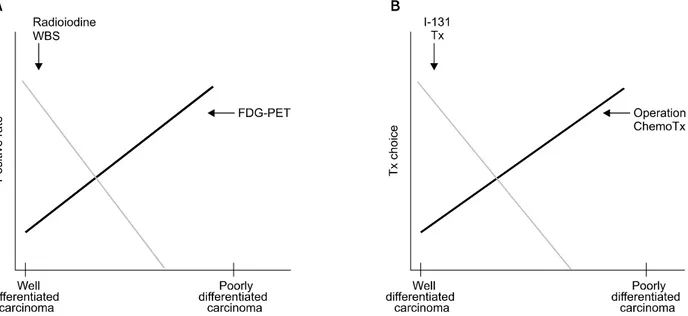
Fig. 2. (A) Detectability of radioiodine whole-body scan and FDG PET according to the differentiation spectrum of differentiated thyroid carcinoma. (B) Treatment of choice in the management of recurrent/metastatic cancer according to the differentiation spectrum of differentiated thyroid carcinoma.
전신 방사성요오드 스캔
방사성요오드 전신스캔은 잘 알려진 바와 같이 투여 한 양에 따라 암을 찾는 예민도가 달라진다. I-131 1∼
10 mCi를 투여하는 진단적 스캔보다 방사성요오드 치 료 후 스캔에서 재발/전이암을 20∼50% 더 찾아내고, 치료양이 많을수록 진단적 예민도도 증가한다.8) 또 3 mCi 이상의 I-131로 촬영한 경우 바로 치료용량의 I-131을 투여하면 암조직의 섭취가 감소되는 갑상선 기 절(stunning) 현상이 나타난다.
이를 해결할 수 있는 방법이 I-123으로 대체하는 것 이다. I-123은 I-131보다 광선의 방출이 많아 예민도가 20배 향상되고, I-131과 달리 감마선만 방출하고 베타 선은 방출하지 않기 때문에 암 조직의 방사선 피폭량 이 적어 갑상선 기절현상이 나타나지 않는다. 따라서 I-123스캔 후 바로 방사성요오드 치료를 시행할 수 있 다.
방사성요오드 전신스캔에서 방사능이 잔여 갑상선 조직이나 암조직에 섭취되면서, 동시에 간에 미만성 섭취가 보일 수 있다. 이는 잔여 갑상선 세포나 암세포 에 들어간 I-131이 세포내 Tg와 결합되어 혈중에 배출 되어 간세포에 집적되기 때문이다. 간혹 갑상선 조직 이나 암조직의 섭취 없이, 간에만 미만성 섭취가 보이 는 경우가 있다. 저자는 이러한 소견을 보이는 15명의 환자를 추적하여 7명에서 나중에 재발/전이암이 나타 나는 것을 확인하였고, 이런 환자의 혈중에 I-131 표지
Tg의 농도가 증가하는 것을 크로마토그래피법으로 확 인하였다. 즉, 전신스캔에서 잔여 갑상선조직이나 암 부위가 보이지 않고 미만성 간섭취만 관찰되면 숨어있 는 재발/전이암을 의심하여야 한다.9)
F-18 fluorodeoxyglucose (FDG) PET의 적응증
F-18 FDG PET이 최근 각종 암환자에서 유용하게 사용되고 있다. 우리 교실에서는 25명의 갑상선 유두암 조직에서 RT-PCR법으로 나트륨옥소 공동수송체(sodi- um iodide symporter, NIS)와 포도당 수송체(glucose transporter-1, Glut-1)의 유전자 발현을 측정하고, 병리 학적 분화도와 비교하여 보았다. 암세포의 분화 정도, 호산성변화(oxyphilic change), 역형성전환(anaplastic transformation)을 평가하여 두 군으로 나누었다. 분화 가 좋은 암에서 상대적으로 분화가 나쁜 암보다 NIS발 현은 증가하고, Glut-1발현은 감소하였다.10) 이 현상을 유추하면 Fig. 2A를 얻을 수 있다. 따라서 FDG PET은 상대적으로 분화가 나빠진 갑상선암에서 요오드스캔 이 음성인 재발/전이암을 발견하는데 유용하다. 우리 병원에서 갑상선암 환자 추적검사에서 요오드 전신스 캔이 음성인 환자에서 재발/전이암을 FDG PET이 92
∼94% 예민도로 찾아내었다.11)
이러한 유전자발현의 차이는 각 환자와 병소에 따라 치료방침을 정하는데 중요하다. 즉, NIS 발현이 높은 암일수록 I-131 치료 효과가 높고, Glut-1 발현이 높을 수록 I-131 치료 효과가 낮아 재수술, 항암약물치료를
Table 1. Response to I-131 treatment according to I-131 whole body scan findings
Response to RIT
Patterns of I-131 whole body scan Diffuse Diffuse+Nodular Nodular
Complete remission 23 12 3
Partial remission 20 16 8
No change 1 6 9
Progression 1 1 9
선택하여야 한다(Fig. 2B).
방사성요오드 치료법
고정 용량법
일반적으로 I-131 치료 용량은 재발/전이암의 위치 에 따라 다르다. 경험적으로 림프절 전이의 경우 100 내지 150 mCi, 폐전이와 뼈전이의 경우 150 내지 200 mCi를 투여한다.
서울대학교병원에서 지난 20년간(1984∼2004년) 2,036 명의 수술한 분화성 갑상선암 환자를 분석하여 보았 다.12) 방사성요오드 제거술 후 시행한 전신스캔상 313 명(15.4%)에서 림프절 전이, 109명(5.4%)에서 폐전이, 29명(1.4%)에서 뼈전이를 발견하였다. 갑상선 유두암 이 1873명(92%), 여포암이 165명(8%)이었고, 유두암중 92명(4.9%), 12명(0.7%)이 각각 폐와 뼈에 전이가 있었 다. 여포성암의 경우 원격전이가 많아, 10.4%에서 폐전 이, 7.4%에서 뼈전이가 있었다.
폐전이의 경우 방사성요오드에 잘 반응하여 35%에 서 완전관해, 40%에서 부분관해에 도달하였다. 특히 미만성 폐전이의 경우 예후가 아주 좋았다. 전신스캔 에서 미만성 병변인 경우 완전관해 51%, 부분관해 44%
에 비하여 결절성 병변인 경우 안전관해는 10%, 부분 관해는 28%에 불과하였다(Table 1). 뼈전이는 방사성 요오드 치료만으로는 완전관해에 도달하지 못하고, 수 술, 외부 방사선치료 등을 적절히 병용하여야 한다. 병 소 별로 계산하여 9%에서 완전관해, 61%에서 부분관 해를 관찰하였다.
최대안전 용량법(maximal safe dose, MSD)
기존의 I-131 치료에 반응이 없는 분화성 갑상선 재 발/전이암은 두 가지의 변형치료를 시도할 수 있다. 투 여한 I-131이 여러 인자에 의하여 병소에 충분량이 도 달하지 못하는 경우가 있기 때문에 더 많은 용량의 I-131을 투여하는 방법이다. 특히 우리나라 환자들은
분화도가 나쁜 유두암이 대부분이고, 평소에 음식으로 요오드를 다량으로 섭취하므로 투여한 I-131이 암부위 에 적게 들어갈 가능성이 많다. 원칙적으로는 암 병소 의 방사성요오드 섭취를 방사선량측정법(dosimetry)으 로 계산할 수 있으나 실용화하기에는 너무 복잡하다.
MSD를 차선책으로 사용할 수 있다. MSD에서는 골수 가 방사선피폭에 제일 예민하므로, 골수에 200 rad (2 Gy) 미만이 피폭되도록 용량을 계산한다.
본격적인 방사성요오드 치료 전에 소량인 2 mCi의 I-131을 경구투여 한 후 3일까지 하루에 한번 혈액을 채취한다. 표준 시료와 함께 in vitro에서 방사능 양을 측정하고 혈액 중 동태를 컴퓨터로 모델링 하여 혈액 및 골수의 방사선 피폭량을 계산한다. 혈액 및 골수에 2 Gy의 피폭을 줄 수 있는 최대안전 용량을 역으로 산 출한다. 이 계산법은 미국 Memorial Sloan-Kettering Cancer Center에서 소프트웨어로 개발하였다.
저자는 갑상선암 환자에서 수술 후 기존의 고정용량 법으로 두 번 이상 치료하여 효과가 없었던 47명의 환 자에서 MSD 치료를 시도하였다.13) 용량을 계산하여 평균 340±57 mCi을 투약할 수 있었고, 기존의 고정 용 량보다 평균 170±60 mCi를 더 투여하였다. 7명(17%) 에서 완전관해, 15명(32%)에서 부분관해의 효과가 있 었다. 그러나 혈액 중 혈구의 숫자가 감소되는 부작용 이 62%에서 있었고 이중 4명에서는 영구적인 혈구 감 소가 관찰되었다.
레티노이드산(retinoic acid, RA) 병용요법
기존의 I-131 치료에 반응이 없는 갑상선 재발암에 서 또 다른 방법은 갑상선암의 분화 촉진제인 RA 병용 요법이다. 암세포의 핵에는 RA와 반응하는 DNA 결합 장소가 있다. 투여된 RA는 세포내에서 RA 수용체와 결 합하고, 이 결합체가 핵내의 특정 DNA 장소에 작용하 여 세포의 분화, 성장, 자연사 등을 관여하는 유전자를 조절하게 된다. 이미 in vitro 실험에서 RA는 갑상선암 에서 NIS 유전자 발현을 증가시키고 NIS 단백질로의 발현을 항진시키는 것이 밝혀졌다.14) 또 RA 자체가 갑 상선 암세포의 증식을 억제시킨다는 보고도 있다.
저자는 기존의 방사성요오드 치료에 듣지 않는 44명 의 전이암 환자에서 이 병용치료를 시도하였다.12) 첫 2주는 13-cis-retinoic acid (isotretinion)를 1.0 mg/kg를 경구투여 하고 관찰하여 간 기능이나 혈중지방농도의 변화가 없고 피부병변이 심하지 않으면 1.5 mg/kg로 증 량한다. 23%의 환자에서 RA 투여 후 재 시행한 치료에 서 전이암 부위에 방사성 요오드 섭취가 증가되는 것
Table 2. Medications to enhance the NIS expression - Retinoids
- Peroximal Proliferator Activated Receptor-gamma agonists - Aromatic fatty acids
- Histone deacetylase inhibitors - DNA methylation inhibitors - Hsp90 inhibitors
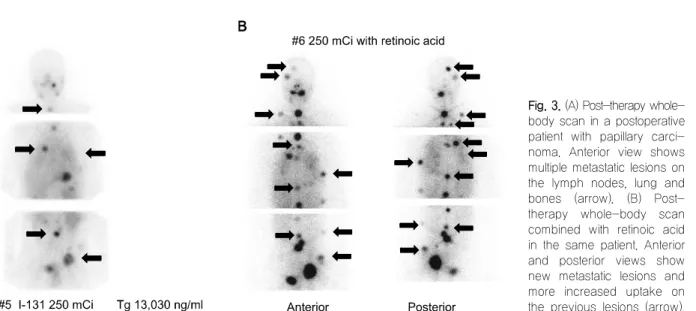
Fig. 3. (A) Post-therapy whole- body scan in a postoperative patient with papillary carci- noma. Anterior view shows multiple metastatic lesions on the lymph nodes, lung and bones (arrow). (B) Post- therapy whole-body scan combined with retinoic acid in the same patient. Anterior and posterior views show new metastatic lesions and more increased uptake on the previous lesions (arrow).
을 관찰하였다(Fig. 3). 또한 25%에서 I-131과 RA 병용 치료가 효과를 보았다. 특히, 나이가 젊고, 병리학적으 로 분화가 잘되어 있고, 요오드스캔에서 미약하나마 병소에 다소 섭취가 있을 때 효과가 있었다.
갑상선암에서 NIS 발현 증진 기초연구
갑상선 재발/전이암의 치료 효과는 결국에는 암세포 의 NIS 발현과 관계가 있다.15) NIS 발현 증진을 위하 여 많은 약제와 화합물을 시도하고 있다(Table 2). 이중 RA와 PPAR-감마 작용제인 로지글리타존(rosiglitazone) 은 현재 임상시도 중에 있다. 우리 교실에서는 HSP-90 억제제인 타네스티마이신(tanestimycin)이 펜드린(pen- drin) 발현도 억제하여 세포내에 들어간 요오드의 배출 을 지연시키는 현상을 발견하였다. 갑상선 세포에 이 약제를 처리하면 요오드 섭취가 3∼4배 증가한다.
이런 실험을 용이하게 하기 위하여 NIS를 적색 형광 유전자인 tdTomato과 융합시켜 동일초점현미경(con- focal microscope)으로 NIS 발현양과 세포막으로의 이 동정도를 동시에 평가하고 있다.
방사성핵종 유전자치료법(radionuclide gene the- rapy)
암세포에 NIS 유전자를 이입하면, NIS 단백질이 합 성되고 세포막에 이동하면, I-131을 섭취하게 되어 치 료가 가능하다. 이러한 개념을 방사성핵종 유전자치료 법이라고 한다. 이 치료법은 갑상선암 뿐 아니라 다른 암종에서도 가능하다. 우리 실험실에서는 이에 대한 일련의 기초연구를 진행 중이다.16,17)
사람의 미분화성 갑상선암 세포주(ARO)에 NIS 유 전자를 삽입시키면 방사성요오드의 섭취가 증가하게 된다(Fig. 4). I-131보다 치료효과가 더 강력한 Re-188도 NIS에 의하여 암세포로 들어갈 수 있기 때문에 치료효 과를 높일 수 있다.18) 갑상선 암 뿐만 아니라 다른 종류 의 암에서도 이 방사성 핵종 유전자 치료법을 시도할 수 있다.
그러나 문제점은 세포내로 들어간 방사성요오드가 쉽게 세포 밖으로 배출되는 데에 있다. 이 경우 잔존 방사성요오드의 양이 적어 치료효과를 기대하기 어려 운 경우가 있다. 치료효과를 높이기 위하여 여러 방법 을 모색하고 있는데, 세포내 요오드의 잔류를 촉진하 기 위하여 갑상선과산화효소(thyroperoxidase) 유전자 이입, 방사선 감수성을 높이기 위한 p53 유전자 이입, 유전자 표적이입(targeted gene transfer) 등을 시도하고 있다.
RA를 병용하여 사용하면 또한 이 치료법을 향상시 킬 수 있다. 우리 연구실 경험에 의하면 이 병용치료법 으로 ARO-NIS 세포의 경우 5배의 섭취증가가 나타난 다. 표적 유전자 치료법도 새로운 방법으로 치료되고 있다. 간암세포를 표적화 하기 위해서 NIS 유전자의
Fig. 4. Photographic and scintigraphic images of nude mice bearing ARO and NIS transfected ARO (ARO-NIS) tumors. Both I-131 and Re-188 scintigraphies show increased uptake in ARO- NIS tumor, and just back- ground uptake in ARO tumor.
In addition, physiologic up- takes are found in the thyroid, stomach and urinary bladder.
Fig. 5. Response of ARO, ARO-NIS, ARO-p53, ARO-NIS- p53 tumors after Re-188 treatment. Compared to other tumors, ARO-NIS-p53 tumor only shows the shrinkage of the mass.
프로모터(promoter)에 AFP 결합 장소를 만들어주면 치 료유전자를 함유한 바이러스 전신투여 후에도 간암 조 직에만 선택적으로 방사성핵종이 모여드는 것을 확인 할 수 있었다.19) 텔로미어효소(telomerase)와 결합하는 프로모터를 이용하면 거의 모든 암세포를 표적할 수 있다. 암세포의 계속적인 분열을 위하여서는 세포분열 시 소모되는 텔로미어(telomere)를 계속 생산하는 효소 가 있어야 하기 때문이다. 실제 사람 전체 암의 85%에 서 이 효소가 존재하고 있다. 따라서 이 방법은 다른 암의 방사성핵종 치료법에 쉽게 응용할 수 있다.20)
p53 유전자는 암세포의 방사선치료 예민도를 결정 하는 중요한 인자이다. 기능을 하는 p53 유전자가 없는 암세포는 방사성핵종 유전자치료법에 반응하지 않으 나 p53 유전자를 함유한 바이러스를 투여하면 방사성 핵종 치료로 종양이 감소된다(Fig. 5).21)
방사성핵종 유전자치료법은 아직까지는 연구 단계
이고 임상에 이용되고 있지 않으나, 여러 새로운 방법 이 제안되고 유전자 함유물질의 안전성이 좋아지면 앞 으로 환자에게 큰 도움을 줄 것으로 기대한다.
중심 단어: 갑상선암, 방사성요오드, 핵의학, 치료, 유전자 치료.
References
1) Siegel E. The beginning of radioiodine therapy of metastatic thyroid carcinoma: A memoir of Samuel M. Seidlin, MD (1895-1955) and his celebrated patient. Cancer Biother Radio- pharm 1999;14(2):71-9.
2) Lee MH, Kang SS, Koh CS, Lee JK, Nam KY, Jin BH, et al. Investigation and treatment of disease of the thyroid gland with radioactive iodine. Korean J Inter Med 1961;4(3):29-47.
3) Kim WB, Kim TY, Kwon HS, Moon W-J, Lee JB, Choi YS, et al. Management guidelines for patients with thyroid nodules and thyroid cancer. J Korean Soc Endocrinol 2007;22(3):157-87.
4) Spencer CA, LoPresti JS, Fatemi S, Nicoloff JT. Detection of residual and recurrent differentiated thyroid carcinoma by serum thyroglobulin measurement. Thyroid 1999;9(5):435-41.
5) David A, Blotta A, Rossi R, Zatelli MC, Bondanelli M, Rotti E, et al. Clinical value of different response of serum thyro- globulin to recombinant human thyrotropin in the follow-up of patients with differentiated thyroid carcinoma. Thyroid 2005;
15(3):267-73.
6) Chung JK, Park YJ, Kim TY, So Y, Kim S-K, Park DJ, et al. Clinical significance of elevated level of serum antithyro- globulin antibody in patients with differentiated thyroid cancer after thyroid ablation. Clin Endocrinol (Oxf) 2002;57(2):215-21.
7) Park EK, Chung JK, Lim IH, Park DJ, Lee DS, Lee MC, et al. Recurrent/metastatic thyroid carcinoma false negative for serum thryoglobulin but positive by posttherapy I-131 whole body scans. Eur J Nucl Med Mol Imaging 2009;36(2):172-9.
8) Lee BW, Lee DS, Moon DH, Chung JK, Lee MC, Cho BY, et al. Comparison of I-131 diagnostic scan and therapeutic scan in thyroid carcinoma. Korean J Nucl Med 1990;24:80-6.
9) Chung JK, Lee YJ, Jeong JM, Lee DS, Lee MC, Cho BY, et al. Clinical significance of hepatic visualization on Iodine-131 whole-body scan in patients with thyroid carcinoma. J Nucl Med 1997;38(8):1191-5.
10) Chung JK, Youn HW, Kang JH, Lee HY, Kang KW. Sodium iodide symporter and the radioiodine treatment of thyroid carcinoma. Nucl Med Mol Imaging 2010;44(1):4-14.
11) Chung JK, So Y, Lee JS, Choi CW, Lim SM, Lee DS, et al. Value of FDG PET in papillary thyroid carcinoma with negative 131I whole-body scan. J Nucl Med 1999;40(6):986-92.
12) Lee HY, Chung J-K, Lee JJ, Oh SW, Kang KW, Park DJ, et al. Radioiodine treatment of differentiated thyroid carcinoma:
The experience at Seoul National University Hospital. Current Med Imaging Rev 2010;6(1):2-7.
13) Lee JJ, Chung JK, Kim SE, Kang WJ, Park DJ, Lee DS, et al. Maximal safe dose of I-131 after failure of a standard fixed dose therapy in patients with differentiated thyroid carcinoma.
Ann Nucl Med 2008;22(9):727-34.
14) Schmutzler C, Winxer R, Meissner-Weigl J, Kohler J. Retinoic acid increases sodium iodide symporter mRNA levels in human thyroid cancer cell lines and suppresses expression of functional symporter in nontransformed FRTL-5 rat thyroid cells. Biochem Biophys Res Commun 1997;240(3):832-8.
15) Min JJ, Chung JK, Lee YJ, Jeong JM, Lee DS, Jang JJ, et al. Relationship between expression of the sodium/iodide symp-
orter and I-131 uptake in recurrent lesions of differentiated thyroid carcinoma. Eur J Nucl Med 2001;28(5):639-45.
16) Chung JK. Sodium iodide symporter: Its role in nuclear medicine. J Nucl Med 2002;43(9):1188-200.
17) Chung JK, Kang JH. Translational research using the sodium/iodide symporter in imaging and therapy. Eur J Nucl Med Mol Imaging 2004;31(6):799-802.
18) Lee YJ, Chung JK, Shin JH, Kang JH, Jeong JM, Lee DS, et al. In vitro and in vivo properties of a human anaplastic thyroid cancer cell line transfected with the sodium iodide symporter gene. Thyroid 2004;14(11):889-95.
19) Jin YN, Chung HK, Kang JH, Lee YJ, Kimm KI, Kim YJ, et al. Radioiodine gene therapy of hepatocellular carcinoma targeted human alpha fetoprotein. Cancer Biother Radiopharm 2008;23(5):551-60.
20) Kim SH, Chung HK, Kang JH, Kim KI, Jeon YH, Jin YN, et al. Tumor targeted radionuclide imaging and therapy using human sodium iodide symporter gene driven by a modified telomerase reverse transcriptase promoter. Hum Gene Ther 2008;19(9):951-7.
21) Lee YJ, Chung JK, Kang JH, Jeong JM, Lee DS, Lee MC.
Wild-type p53 enhances the cytotoxic effect of radionuclide gene therapy using sodium iodide symporter in a murine anaplastic thyroid cancer model. Eur J Nucl Med Mol Imaging 2010;37(2):235-41.