Abstract :
Background : Recent guidelines recommend that vancomycin trough concentrations should be maintained above 10mg/L and 15-20mg/L for complicated infections. Several studies have sug- gested that higher trough values are associated with higher risk of nephrotoxicity. The aim of this study was to determine the incidence and risk factors for vancomycin associated nephrotoxi- city, among patients managed through therapeutic drug monitoring (TDM).
Method : A retrospective study was conducted among adult patients who received vancomycin TDM service more than twice, at Seoul National University Hospital between July, 2009 and December, 2009. Patients were excluded, if they had a baseline serum creatinine level of 〉 1.4mg/dl, were in ICU when they initiated vancomycin therapy, or received vancomycin with nephrotoxic agents during therapy. Vancomycin associated nephrotoxicity was defined as an increase in serum creatinine of 0.5mg/dl from the baseline, on at least two consecutive days. Risk factors for nephrotoxicity are classified into patient-related factors, underlying disease-related factors, drug-related factors, and TDM-related factors. Univariate and multivariate analyses were performed for comparison of the patients.
Vancomycin의 TDM을 의뢰한 환자에서 신기능 변화에 대한 위험인자 분석
서울대학교병원 약제부
Risk Factors for Vancomycin Associated Nephrotoxicity in Patients Managed Through Therapeutic Drug Monitoring
Su Jeong Song, Min Jung Kim, Yoon Sook Cho, Hyang Sook Kim, Hye Suk Lee
Department of Pharmacy, Seoul National University Hospital, 101 Daehak-ro, Jongno-gu, Seoul, 110-744, Korea
회원학술보고
연구배경
Vancomycin은 1956년 페 니 실 린 내 성 Staphylococcus aureus에 대한 치료제로 사용되 기 시작한 glycopeptides 항생제이다. 개발 초기 vancomycin은 infusion-related toxicity, 신독 성, 이독성 등의 부작용이 빈번하게 나타났고, 상대 적으로 독성이 적은 반합성 페니실린이 개발되면서 널리 사용되지 않았다. 하지만 1980년대 초부터 methicillin에 내성을 나타내는 균에 의한 감염이 증가하면서 vancomycin의 사용이 증가하여, 현재 는 페니실린에 알러지가 있거나 methicillin- resistant S. aureus(MRSA), coagulase-nega- tive staphylococci(MRCNS) 감염에 1차 선택약물 로 사용되고 있다1).
주로 사구체 여과에 의해 배설되는 vancomycin은 약동학적 변수의 개체 차가 커서 경험적 용량조절만
으로는 적절한 치료효과를 거두기가 어렵다. 따라서 독성을 최소화하고 적정 사용을 유도하기 위해 ther- apeutic monitoring(이하 TDM)이 권고되고 있다.
최근 vancomycin의 치료 실패2)와 내성균 발생의 위 험성에 대한 문제들이 제기되면서, 미국병원약사회에 서는 vancomycin TDM 가이드라인3)을 발표하였다.
이 가이드라인에서는 vancomycin의 적정 trough 농 도를 10mg/L 이상으로 상향조정하고, bacteremia, meningitis 등 일부 감염은 15-20mg/L의 높은 trough 농도를 유지할 것을 권장하고 있다. 하지만 trough 농도가 높을수록 신독성 발현의 위험성이 커 진다는 연구들4, 5)이 지속적으로 발표되고 있어 van- comycin에 의한 신독성이 재조명되고 있다.
Vancomycin을 비롯한 많은 약물은 신독성의 위 험성을 가지고 있다고 알려졌다. 이러한 신독성은 다른 부작용에 비해 혈중 크레아티닌 농도 등의 평 가지표로 모니터링이 용이한 편이다. 이에 신독성 Results : The incidence of vancomycin associated nephrotoxicity is 21/173 (12.1%) in patients managed through vancomycin therapeutic monitoring. Patients with nephrotoxicity had higher average and 1st trough concentration (19.9mg/L vs. 12.2mg/L, p=0.005; 20.6mg/L vs. 19.9mg/L, p=0.015), than patients without nephrotoxicity. Vancomycin duration therapy of ≥14days (76.2%
vs. 50%, p=0.024) were associated with increasing nephrotoxicity. Presence of underlying dis- eases (diabetes, heart failure, hepatic disease) was likely to be associated with development of nephrotoxicity, though this was not statistically significant.
Conclusions : Vancomycin trough concentration (≥15mg/L) and duration of therapy (≥14days) are identified to be significant predictors of nephrotoxicity. It is necessary to carry out more studies, focusing in particular on the association between vancomycin nephrotoxicity and under- lying disease.
[Key words] vancomycin, TDM, nephrotoxicity, trough, underlying disease 투고일자 2012. 4. 4; 심사완료일자 2012. 5. 2; 게재확정일자 2012. 7. 6
위험인자에 대한 연구는 이미 많이 진행되었다. 단 독요법 시 vancomycin의 신독성 발현빈도는 0- 17%로 알려졌으나, aminoglycosides계 항생제와 같은 신독성 약물을 병용할 경우 7-35%로 나타나 신독성의 위험성이 증가한다6)고 보고된 바 있다. 또 한 고령일수록7), 투여기간이 길수록5,8), 투여량이 많 을수록(≥4g/day)9), 기존의 신기능이 나쁠수록9) 신 독성이 발생할 가능성이 높아진다는 연구들도 발표 되었다. 이처럼 vancomycin에 의한 신기능 변화에 영향을 미치는 요인들은 매우 다양하다. 하지만 기 저질환과의 상관관계에 대한 자료는 아직 미흡하다.
또한 연구마다 신기능 변화에 유의한 영향을 미치는 요인에 다소 차이가 있고, 다른 신독성 약물에 비해 밝혀진 위험인자가 확실치 않아 구체적인 위험인자 분석이 필요하다.
TDM은 약사의 중요한 업무 중 하나로, 약물의 혈 중농도를 파악하여 용량의 적절성을 평가하고 부작 용 발생을 감소시킬 수 있는 업무이다. 이는 안전역 이 좁은 약물을 대상으로 하고 있어 그 중요성이 더 크다. 따라서 약물의 부작용 발생과 여러 위험인자들 의 상관관계를 잘 파악하고 모니터링 한다면 더욱 효 과적인 업무가 될 것이다. 본 연구에서는 서울대학교 병원에서 vancomycin에 대한 모니터링이 이루어지 고 있는 환자의 신독성 발현 빈도를 알아보고 신독성 에 영향을 미치는 요인을 분석하여 vancomycin의 안전하고 효과적인 사용을 돕고자 한다.
연구방법
1. 연구대상
2009년 7월 1일부터 2009년 12월 31일까지 서울 대병원에서 vancomycin의 TDM 자문을 2번 이상 의뢰한 만 18세 이상의 환자들을 연구대상으로 하였 다. 미국병원약사회에서 발표한 가이드라인이 성인 환자를 대상으로 하고 있으므로 만 18세 미만의 환 자들은 연구대상에서 제외하였으며, vancomycin에 대한 면밀한 모니터링이 이루어진 환자들을 대상으 로 하기 위해 TDM 자문을 적어도 2번 이상 의뢰한
환자로 제한하였다.
기존의 연구에서 vancomycin에 의한 신기능 변화 에 영향을 미친다고 알려진 환자의 기저 신기능9), 중 환자실 재원10), sepsis4) 등의 영향을 배제하기 위해 기저 혈중 크레아티닌이 정상범위(≤1.4mg/dl)를 넘 는 환자, 첫 TDM 발행처가 중환자실인 환자, 적응 증이 sepsis 또는 endocarditis인 환자는 제외하였 다. 또한 vancomycin 투여기간 중 amphotericin B, calcineurin inhibitor와 같이 신독성 발현빈도 가 25% 이상으로 알려진 약물을 병용한 경우도 배제 하였다. 한편, 첫 TDM 의뢰시점이 투여 후 2주를 초 과한 환자는 vancomycin에 대한 적절한 모니터링 이 되었다고 보기 어려우므로 제외하였다.
2. 연구방법
2009년 7월 1일부터 2009년 12월 31일까지 van- comycin을 투여한 환자를 대상으로 하여 임상자료 를 후향적으로 분석하였다. 환자의 기본정보인 성별, 나이, 체중, 기저질환(diabetes, heart failure, hepatic disease), 기저 혈중 크레아티닌, 기저 알 부민, 혈중 크레아티닌 변화에 대한 자료를 수집하 고, vancomycin의 적응증, 총 투여량, 총 투여기 간, 총 투여일수, 병용약물 수를 조사하였다. 또한 TDM 측면에서 의뢰횟수, 의뢰주기, TDM 시 trough 농도, TDM 의뢰시점을 수집하였다.
기저 혈중 크레아티닌은 vancomycin 투여시작일 또는 이를 기준으로 가장 최근의 혈중 크레아티닌 농 도로 정의하였다. 이는 vancomycin 치료 개시 24 시간 이내에 측정한 값을 기저 혈중 크레아티닌 값으 로 정한 기존의 연구방법11)과 TDM 자문 시 고려하는 크레아티닌 농도를 바탕으로 본 연구에 맞게 수정한 것이다. 크레아티닌 클리어런스는 나이를 고려하기 위한 Cockcroft-Gault equation과 알부민 수치를 보정하기 위한 Sanaka equation을 통해 GFR을 산 출하였다. 또한 환자의 기저질환은 다른 약물들의 신 독성에 영향을 미친다고 알려진 diabetes, heart failure, hepatic disease 유무로 구분하였으며12,13), 병용약물은 신기능에 따라 용량조절을 하는 약물로 한정하여 그 수를 알아보았다.
Vancomycin에 의한 신독성은 미국병원약사회에 서 발표한 가이드라인12)에 따라 적어도 이틀 연속으 로 혈중 크레아티닌이 기저 혈중 크레아티닌에서 0.5mg/dl 이상 상승한 경우로 정의하였다. 이를 기 준으로 신독성이 나타난 환자와 신독성이 나타나지 않은 환자로 나누어 비교해봄으로써 위험인자를 분 석하였다.
3. 통계분석
신독성 유무를 종속변수로 한 후, Mann- Whitney U-검정을 하여 연속변수의 유의성을 검정 하였다. 불연속변수의 비교를 위해서 카이제곱 검정 을 이용하였으며, 5보다 작은 기대빈도를 가지는 칸 이 있는 경우 Fisher의 직접 확률계산법을 사용하였 다. 모두 P값이 0.05 미만일 때 통계적으로 유의한 것으로 판단하였다.
이상의 분석은 SPSS 17.0V 프로그램을 이용하였다.
연구결과
1. 연구대상자의 일반적 특성
연구기간 중 vancomycin을 투여한 환자는 1453 명이었고, 만 18세 미만인 274명과 TDM 의뢰건수 가 1번 이하인 750명을 제외한 429명의 전자의무기 록을 분석하였다. 이 중 선정기준에 해당하는 환자는 총 173명이었다.
남성과 여성은 각각 97명(56.1%)과 76명(43.9%) 으로 남성이 약간 많았다. 평균 연령은 59.5±15.8 세이었고, 만 60세 이상의 환자가 90명(52.0%)으로 절반 이상을 차지하였다. 기저 혈중 크레아티닌은 0.8±0.2mg/dl로 정상이었고, 기저 혈중 알부민은 3.2±0.6g/dl로 다소 낮았다. 크레아티닌 클리어런 스는 Cockcroft-Gault equation에 따르면 24.5±
18.2%, Sanaka equation에 따르면 17.4±19.0%
의 감소율을 보였다(Table 1). 기저질환으로 dia- betes, heart failure, hepatic disease가 하나라 도 있는 환자는 82명(47.4%)이었고, 이 중 diabetes
성별 나이
ABW Baseline SCr Initial albumin Baseline CLcr
CLcr의 감소율
SCr의 최대 변화량 최대 SCr 시점 SCr cut off까지의 일수 Vancomycin 총 투여량 Vancomycin 총 투여일수
Vancomycin 초기 투여량
TDM 의뢰횟수 TDM 의뢰주기 첫 TDM 의뢰시점 Trough 농도
적응증
Target trough ≥15mg/L
Table 1. Demographics and Characteristics for Patients
특성
남 : 여 [세]
≥60 [kg]
[mg/dl]
[g/dl]
[ml/min]
Cockcroft-Gault Sanaka [%]
Cockcroft-Gault Sanaka [mg/dl]
[일]
[일]
[mg/kg]
[일]
≥14
<14 [mg/kg/day]
>30
≤30 [회]
[일]
[일]
[mg/L]
평균 1st
HAP CNS infection, Meningitis MRSA bacteremia
97 : 76 58.0 ± 15.8 90 (52.0%) 59.5 ± 11.4 0.8 ± 0.2 3.2 ± 0.6
79.8 ± 36.4 63.9 ± 22.9
24.5 ± 18.2 17.4 ± 19.0 0.2 ± 0.5 (0.0 - 5.2) 5.5 ± 7.4 (0 - 41) 9.9 ± 5.4 (2 - 20) 412.8 ±330.1 (9 -2487) 18.0 ± 12.9 (3 - 82) 92
81
30.7 ± 12.9 (4 - 119) 83
90
3.7 ± 2.1 (2 -12) 4.9 ± 2.0 (2 -14) 3.6 ± 2.0 (1 -13)
13.1 ± 6.3 (4.4 - 53.4) 11.9 ± 8.9 (2.3 - 57.3)
63 (36.4%) 14 36
6
n=173
환자가 가장 많았다.
Vancomycin의 총 투여량은 412.8±330.1 mg/kg, 총 투여기간은 18.0±12.9일이었다.
Vancomycin 투여시작일로부터 첫 TDM 의뢰시점 까지 평균 30.7±12.9mg/kg/day를 투여하였다.
또한 target trough 농도를 15mg/L 이상으로 하는 적응증을 가진 환자는 63명(36.4%)이었고, 이 중에 는 CNS 감염이 가장 많았다.
Vancomycin의 TDM 측면에서 보면, 한 명당 3.7
±2.1회 자문을 의뢰하였고 주기는 4.9±2.0일이었 다. 평균적으로 vancomycin 투여시작 3.6±2.0일 후에 처음으로 TDM을 의뢰하였으며, 이 때 측정한 trough 농도는 13.1±6.3mg/L이었다.
2. 신기능에 영향을 미치는 요인 분석
총 173명 중 21명(12.1%)에서 vancomycin에 의 한 신독성이 의심되었다.
Vancomycin에 의한 신독성 유무에 따라 특성을 비교해보았다. 크레아티닌 클리어런스는 신독성이 나타난 환자군에서 55.3±14.0% (Cockcroft- Galut), 51.3±15.1% (Sanaka), 신독성이 나타나지 않은 환자군에서 20.2±14.2%, 12.8±14.1%의 감 소율을 보였다(Table 2).
두 군간의 성별, 나이, 기저 혈중 크레아티닌, 기저 알부민, 기저 크레아티닌 클리어런스, 병용약물 수는 유의적인 차이를 보이지 않았다. 60세 이상의 환자 는 61.9% vs. 50.7%로 신독성이 나타난 환자군에서
많았으나 유의성은 없었다(Table 2). 몸무게(ABW) 에는 유의한 차이를 보였으나, ABW/IBW 값은 차이 가 없었다.
환자가 기저질환으로 diabetes, heart failure, hepatic disease가 하나라도 있는 경우는 66.7%
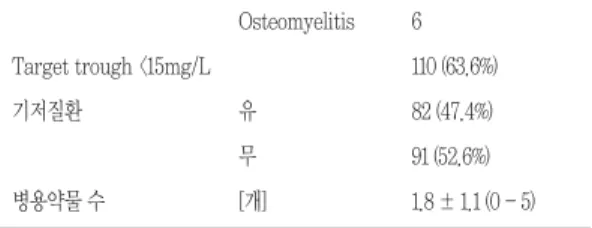
vs. 44.7%으로 신독성이 나타난 환자군에서 많았 다. 각 기저질환으로 나누어 비교해 보았을 때 역시 신독성이 나타난 환자군이 기저질환을 가진 환자가 많은 것을 볼 수 있었으나 모두 통계적 유의성은 없 었다(Table 3, 6). 하지만 diabetes는 신독성이 나 Target trough <15mg/L
기저질환
병용약물 수
Osteomyelitis
유 무 [개]
6 110 (63.6%) 82 (47.4%) 91 (52.6%) 1.8 ± 1.1 (0 - 5) SCr cutoff는 SCr이 baseline SCr에서 0.5mg/dl 상승한 경우를 말한다.
적응증(target trough ≥15mg/L인 경우)은 CNS infection과 MRSA bac- teremia 중복 1건을 포함한다.
성별, 남 : 여 나이(세)
≥60세 ABW(kg) ABW/IBW Baseline SCr(mg/dl) Initial Alb(g/dl) Baseline CLcr(ml/min)
Cockcroft-Gault Sanaka CLcr의감소율(%)
Cockcroft-Gault Sanaka SCr의 최대 변화량 (mg/dl) 최대 SCr 시점(일) SCr cutoff까지의일수(일)
P value
0.716b 0.776a 0.334b 0.015* a 0.077a 0.212a 0.632a
0.158a 0.744a
<0.001* a
<0.001* a
<0.001* a
<0.001* a Patients without nephrotoxicity (n=152)
86 : 66 57.8 ± 15.3
77 (50.7%) 58.6 ± 11.2
1.1 ± 0.5 0.8 ± 0.2 3.2 ± 0.6
81.0 ± 37.3 64.1 ± 23.4
20.2 ± 14.2 12.8 ± 14.1 0.1 ±0.2 (0.0 -1.7)
4.6 ± 7.3 (0 -41) Patients with
nephrotoxicity (n=21)
11 : 10 59.1 ± 19.2
13 (61.9%) 65.5 ± 11.4
1.2 ± 0.2 0.9 ± 0.3 3.2 ± 0.7
71.0 ± 28.6 62.6 ± 18.9
55.3 ± 14.0 51.3 ± 15.1 1.1 ±1.0 (0.5 -5.2)
12.0 ±5.0 (4 -22) 9.9 ± 5.4 (2 -20)
Table 2. Comparison of Patients-related Factors between Patients with and without Nephrotoxicity
*P 값이 <0.05으로 통계적으로 유의하다.
a는 Mann-Whitney U-검정, b는 카이제곱 검정으로 구한 값이다.
타난 군의 42.9%, 신독성이 나타나지 않은 군의 25.7%, hepatic disease는 각각 33.3%, 14.5%로 90% 신뢰구간에서는 유의적 차이가 있어 기저질환 이 신독성에 영향을 끼치는 경향을 보였다.
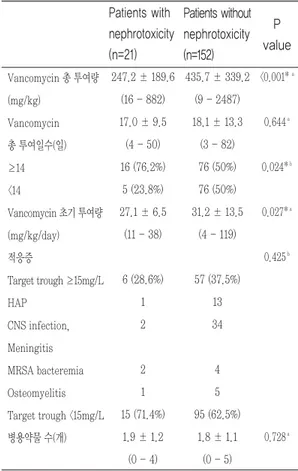
Vancomycin의 총 투여량은 신독성이 나타난 환 자군이 247.2±189.6mg/kg, 신독성이 나타나지 않 은 환자군이 435.7±339.2mg/kg로 신독성이 나타 나지 않은 환자군이 유의하게 많았다. 초기 투여량도 마찬가지로 신독성이 나타나지 않은 환자군이 더 많 았다. 반면 vancomycin의 총 투여기간은 각각 17.0
±9.5일 vs. 18.1±13.3일로 비슷하였으나 투여기간 이 14일 이상인 환자 수와 14일 미만인 환자 수는 두 군간의 유의한 차이가 있었다(Table 4, 6).
신독성이 나타난 환자군의 vancomycin TDM 의 뢰횟수는 4.3±2.5회로 신독성이 나타나지 않은 환
자군의 3.6±2.1회보다 다소 많으나 유의하지 않았 다. 의뢰주기는 4.2±1.5일 vs. 5.0±2.0일로 신독 성이 나타난 환자군이 유의하게 짧았다. 즉, 신독성 이 나타난 군에서 TDM을 더 빈번하게 의뢰하는 것 을 볼 수 있었다. 신독성이 나타난 환자군과 나타나 지 않은 환자군은 vancomycin 투여시작 후 각각 3.9±2.5일, 3.5±1.9일만에 TDM을 의뢰하여, 신 독성이 나타나지 않은 환자군이 늦게 의뢰하는 편이 었으나 유의성은 없었다(Table 5). Target trough
14 (66.7%) 7 (33.3%)
9 (42.9%) 12 (57.1%)
6 (28.6%) 15 (71.4%)
7 (33.3%) 14 (66.7%) Total (n=82)
유 무
Diabetes (n=48) 유
무
Heart failure (n=28) 유
무
Hepatic disease (n=29) 유
무
Table 3. Comparison of Underlying Disease- related Factors between Patients with and without Nephrotoxicity
Patients with nephrotoxicity (n=21)
68 (44.7%) 84 (55.3%)
39 (25.7%) 113 (74.3%)
22 (14.5%) 130 (85.5%)
22 (14.5%) 130 (85.5%) Patients without nephrotoxicity (n=152)
0.059c
0.099b
0.116c
0.055c P value
b는 카이제곱 검정, c는 Fisher의 정확한 검정으로 구한 값이다.
Heart failure는 CHF, atrial fibrillation, atrial flutter, angina 등을 포 함한다.
Hepatic disease는 liver cirrhosis, hepatocellular carcinoma, hepati- tis 등을 포함한다.
247.2 ± 189.6 (16 - 882) 17.0 ± 9.5
(4 - 50) 16 (76.2%)
5 (23.8%) 27.1 ± 6.5
(11 - 38)
6 (28.6%) 1 2
2 1 15 (71.4%) 1.9 ± 1.2 (0 - 4) Vancomycin 총 투여량
(mg/kg) Vancomycin 총 투여일수(일)
≥14
<14
Vancomycin 초기 투여량 (mg/kg/day) 적응증
Target trough ≥15mg/L HAP
CNS infection, Meningitis MRSA bacteremia Osteomyelitis Target trough <15mg/L 병용약물 수(개)
Table 4. Comparison of Drug-related Factors between Patients with and without Nephrotoxicity
Patients with nephrotoxicity (n=21)
435.7 ± 339.2 (9 - 2487) 18.1 ± 13.3
(3 - 82) 76 (50%) 76 (50%) 31.2 ± 13.5
(4 - 119)
57 (37.5%) 13 34
4 5 95 (62.5%)
1.8 ± 1.1 (0 - 5) Patients without nephrotoxicity (n=152)
<0.001* a
0.644a
0.024*b
0.027*a
0.425b
0.728a P value
*P 값이 <0.05으로 통계적으로 유의하다.
a는 Mann-Whitney U-검정, b는 카이제곱 검정으로 구한 값이다.
Patients without nephrotoxicity의 적응증(target trough ≥15mg/L)은 CNS infection, MRSA bacteremia 중복 1건을 포함한다.
를 15mg/L 이상 유지할 것이 권장되는 적응증을 가 진 환자수 역시 두 군 사이에 유의한 차이가 없었다 (Table 4).
두 군에서 vancomycin의 trough 농도는 전반적 으로 신독성이 나타난 환자군이 높은 것으로 나타났 다. 평균 trough 농도는 각각 19.9±11.4mg/L, 12.2±4.5mg/L (p=0.005), 첫 번째 TDM에서의 trough 농도는 20.6±17.5mg/L, 10.8±6.3mg/L (p=0.015)로 신독성이 나타난 환자군이 신독성이 나 타나지 않은 환자군보다 유의적으로 높았다. 또한 평 균 trough 농도가 15mg/L 이상인 환자는 71.4%
vs. 23.0%로 신독성이 나타난 환자군에서 확연히 많았다(Table 5, 6).
고찰
개발 초기 vancomycin은 갈색을 띄고 있어
"Mississippi Mud”라고 불렸으며, 불순물을 포함하
고 있어 여러 부작용을 일으켰다14). 하지만 정제기술 이 개선되면서 vancomycin의 순도가 높아졌고, 부 작용에 대한 보고도 줄어들었다. 그 후 vancomycin 과 신독성에 대한 여러 논문들이 발표되었으나, 다른 신독성 약물의 병용여부와 vancomycin에 의한 신 독성 정의가 다양하여 그 인과관계가 뚜렷하지 않았 다3). 따라서 본 연구에서는 최근 미국병원약사회에 서 발표한 vancomycin TDM 가이드라인3)의 신독 성 정의를 기준으로 하여, 혈중 크레아티닌이 적어도 이틀 연속으로 기저 혈중 크레아티닌에서 0.5mg/dl 상승한 경우를 신독성이 나타났다고 판단하였다.
Vancomycin에 의한 신독성은 0-17%로 다양하게 보고되고 있지만, 일반적으로 5-7%정도로 알려져 있다8). 하지만 다른 신독성 약물을 병용하는 경우 vancomycin에 의한 신독성의 위험성이 증가한다
6,15)고 한다. 기저 신기능이 나쁜 환자 역시 신독성이
발생할 가능성이 높아진다는 연구결과2,6)가 있었다.
또한 Lodies TP, et al.10)의 연구에서는 중환자실 재 원환자가 그렇지 않은 환자보다 더 낮은 trough 농 도 역치에서 신독성 위험성이 크게 나타났다. 따라서 본 연구에서는 신독성 발현빈도가 25% 이상으로 알
4.3 ± 2.5 (2 - 12) 4.2 ± 1.5 (2 - 8) 3.9 ± 2.5 (2 - 13)
19.9 ± 11.4 (7.7 - 53.4) 15 (71.4%) 6 (28.6%) 20.6 ± 17.5 (2.3 - 57.3) Intervention 횟수(회)
Intervention 주기(일) 첫 TDM 의뢰시점(일) Trough 농도(mg/L) 평균
≥15
<15 1st
Table 5. Comparison of TDM-related Factors between Patients with and without Nephrotoxicity
Patients with nephrotoxicity (n=21)
3.6 ± 2.1 (2 - 12) 5.0 ± 2.0 (2 - 14) 3.5 ± 1.9 (1 - 12)
12.2 ± 4.5 (4.4 - 29.1) 35 (23.0%) 117 (77.0%) 10.8 ± 6.3 (2.5 - 31.1) Patients without nephrotoxicity (n=152)
0.233a 0.034*a
0.570a
0.005*a
<0.001*b
0.015*a P value
*P 값이 <0.05으로 통계적으로 유의하다.
a는 Mann-Whitney U-검정, b는 카이제곱 검정으로 구한 값이다.
Odds ratio 1.583 3.200 0.667
8.357
2.545
2.471 2.173 2.364 2.955 특성
나이(세; ≥60 vs. <60) 총 투여기간(일; ≥14 vs. <14) 적응증(target trough, mg/L;
≥15 vs. <15) 평균 trough 농도(mg/L;
≥15 vs. <15) 1st trough 농도(mg/L;
≥15 vs. <15) 기저질환(유무) Diabetes(유무) Heart failure(유무) Hepatic disease(유무)
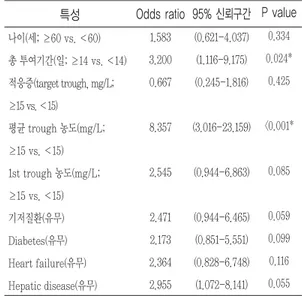
Table 6. Predictive Risk Factors for Nephrotoxicity 95% 신뢰구간
(0.621-4.037) (1.116-9.175) (0.245-1.816)
(3.016-23.159)
(0.944-6.863)
(0.944-6.465) (0.851-5.551) (0.828-6.748) (1.072-8.141)
P value 0.334 0.024*
0.425
<0.001*
0.085
0.059 0.099 0.116 0.055
*P 값이 <0.05으로 통계적으로 유의하다.
려진 amphotericin B와 calcineurin inhibitor를 병용한 환자, 기저 혈중 크레아티닌이 정상범위(≤
1.4mg/dl)를 넘는 환자, TDM 첫 발행처가 중환자 실인 환자는 배제하였다. 이와 같은 선정기준을 만족 하는 vancomycin의 TDM을 의뢰한 환자를 대상으 로 하여 신독성 발현여부를 확인해보았다. 연구결과, 연구대상자 중 약 12%에서 vancomycin에 의한 신 독성이 의심되었다. 이는 vancomycin에 대한 면밀 한 모니터링이 이루어지고 있는 환자임에도 신독성 발현빈도가 높다는 점을 시사한다. 따라서 van- comycin에 의한 신독성에 대한 구체적인 위험인자 를 규명할 필요가 있겠다.
Jeffres MN, et al.5)의 연구는 MRSA pneumo- nia 환자 중 vancomycin을 투여받은 94명을 대상 으로 하였는데, 이 중 42.6%에서 신독성이 발생했고 평균 trough 농도가 15mg/L 이상인 경우(40.7%
vs. 67.5%, p=0.010)나 투여기간이 14일 이상인 경 우(19.6% vs. 62.1%, p=0.007) 그 위험성이 증가했 다. 또한 Lodies TP, et al.2)의 연구에서는 3일 이상 vancomycin을 투여받은 성인 환자 166명 중 21명 에서 신독성이 발생하였으며, vancomycin의 첫 번 째 trough 농도가 높을수록(14.6mg/L vs.
9.6mg/L, p=0.014) 신독성 발현이 증가하는 것을 볼 수 있었다. 그 외의 해외논문들4,7,8)에서도 trough 농도가 높은 군이 trough 농도가 낮은 군보다 신독 성의 위험성이 큰 것으로 나타났다. Vancomycin의 TDM 자문을 의뢰한 환자를 대상으로 한 본 연구에 서도 신독성이 나타난 군에서 투여기간이 14일 이상 인 경우가 많았고, 평균 trough 농도와 첫 번째 trough 농도가 유의하게 높은 것을 알 수 있었다 (Table 4-6). 최근 vancomycin의 치료실패와 내성 균 증가로 target trough 농도가 전반적으로 상향 조정된 점을 고려해보면 TDM 자문 시 신독성 발생 의 위험성을 인지하고 환자의 신기능 변화를 유심히 관찰해야 할 것이다.
하지만 vancomycin의 target trough 농도는 적 응증에 따라 다르다. Vancomycin TDM 가이드라 인에서 제시한 적정 trough 농도는 10mg/L 이상이 지만, MRSA pneumonia, MRSA bacteremia, meningitis, osteomyelitis, endocarditis와 같은
일부 적응증은 15mg/L 이상으로 더 높은 trough를 요구한다. 즉, 적응증에 따라 trough 농도는 높거나 낮게 조절할 수 있다. 하지만 신독성이 나타난 환자 군과 나타나지 않은 환자군의 적응증을 비교해본 결 과, target trough가 높은 적응증을 가진 환자는 유 의한 차이가 없었고 오히려 신독성이 나타나지 않은 환자군에서 더 많았다(Table 4, 6). 또한 target trough가 높은 적응증을 가진 63명 중 첫 번째 trough 농도가 15mg/L 이상에 도달한 경우는 11명 (17%)에 그쳤다. 이는 target trough가 높은 군일 지라도 실제 평균 trough 농도를 target trough가 낮은 군과 비슷하게 유지했기 때문으로 보인다(13.2
±4.2mg/L vs. 13.1±7.2mg/L, p=0.870). 또한 2009년 초 새로운 TDM 가이드라인이 발표되었는 데, 2009년 후반기에 TDM 자문을 의뢰한 환자를 대상으로 연구자료를 수집했기 때문에 상향된 tar- get trough 농도를 실제 임상에 적용하기 조심스러 웠다고 생각해볼 수도 있겠다.
Lodies TP, et al.9)의 연구에서는 vancomycin의 투여량이 4g/day 이상인 환자가 4g/day 미만일 환 자보다 신독성이 나타날 위험성이 크게 나타났다 (34.6% vs. 10.9%, p=0.001). 그러나 이는 환자의 체중당 용량을 고려하지 않는 결과로 본 연구에서는 가이드라인에서 제시하고 있는 용량(mg/kg)을 기준 으로 하여 분석하였다. Vancomycin의 투여량은 일 반적으로 8-12시간마다 15-20mg/kg이고, target trough 농도까지 조기에 도달하기 위해서 25- 30mg/kg를 투여할 수 있다3). 총 투여량을 총 투여 기간으로 나눈 평균 투여량(mg/kg/day)은 임상경과 나 신기능 변화에 따라 매우 다르게 조절할 수 있으 므로, 본 연구에서는 총 투여량과 초기 투여량을 기 준으로 비교해보았다. 그 결과, 기존의 연구와 달리 vancomycin의 투여량은 신독성이 나타나지 않은 환자군이 유의하게 많았다(Table 4). 총 투여량은 신 기능 변화가 적은 군에서 적극적인 증상조절을 위한 aggressive dosing이 가능했기 때문으로 보인다.
Pritchard L, et al.11)의 연구에서도 신독성이 나타 나지 않은 환자군의 투여량(mg/kg/day)이 신독성이 나타난 환자군보다 유의하게 많았는데, 이 역시 같은 이치로 생각할 수 있을 것이다. Vancomycin의 초기
투여량은 신독성이 나타나지 않은 환자군의 나이가 적었다는 점, target trough 농도가 높은 적응증을 가진 환자들이 많았다는 점 등의 다중요인이 복합적 으로 작용한 것으로 보인다. 하지만 본 연구에서 각 요인들이 두 군사이의 유의적 차이가 있는 것은 아니 므로 명확한 인과관계를 밝히긴 어렵다.
앞서 기술한 vancomycin의 trough 농도, 투여기 간, 투여량은 임상경과에 따라 변경될 수 있는 항목 들이다. 다시 말해 약물관련인자는 적절한 임상효과 를 얻기 위해 필요한 부분으로 신독성 예방을 위해 조절하는데 한계가 있다는 것이다. 한편, van- comycin의 투여량이 적음에도 불구하고 신독성 위 험성이 크게 나타난 점은 투여량 외에 강력한 위험인 자가 있을 것이라고 생각해 볼 수 있다. 따라서 본 연 구에서는 환자관련인자들, 특히 기저질환과의 상관 관계를 알아봄으로써 신독성 위험인자를 파악하고자 하였다.
약물에 의한 신독성은 환자의 기저질환, 특히 dia- betes, heart failure, hepatic disease가 그 위험 인자로 알려진 바 있다12,13). 하지만 vancomycin에 의한 신독성과 기저질환 사이의 관계는 아직 밝혀지 지 않았다. 본 연구에서는 diabetes, heart failure, hepatic disease 유무에 따라 vancomycin에 의한 신독성에 영향을 미치는지 알아보고자 하였다. 신독 성이 나타난 환자군에서 세 가지 질환 중 하나라도 있는 환자(%)가 많았으나 유의한 차이가 없었다 (Table 3). Diabetes, heart failure, hepatic dis- ease 각각으로 나누어 비교해 보았을 때 역시 신독성 이 나타난 환자군에서 기저질환을 가진 환자들이 더 많았다. 특히 hepatic disease의 경우 p값이 0.055 로 90% 신뢰구간에서 유의성을 보였는데, 이는 hepatic disease가 vancomycin에 의한 신독성에 영향을 미치는 경향을 보인다고 해석할 수 있다. 다 수의 환자를 대상으로 한 추가적인 연구가 진행된다 면 보다 의미 있는 결과를 기대해볼 수 있을 것이다.
또한 신독성이 나타난 환자군의 ABW는 신독성이 나타나지 않은 환자군보다 유의하게 크게 나타나 (Table 2), 비만인 환자가 신독성 위험이 크다는 기 존의 연구9, 10)와 일치하는 듯 보인다. 하지만 기존의 연구들은 외국인들을 대상으로 한 연구9)이므로 본
연구에 그대로 적용하기 무리가 있다. 기존 연구와 본 연구의 평균 ABW를 비교해보면 신독성이 나타 난 군에서 87.5kg vs. 65.5kg, 나타나지 않은 군에 서 78.3kg vs. 58.6kg으로 한국인을 대상으로 한 본 연구대상과는 차이가 컸다. 또한 101kg을 기준으 로 몸무게가 이보다 많이 나가는 환자들이 신독성이 나타난 환자군에서 많다는 결과를 도출하였는데, 이 번 연구대상 중 101kg 이상의 환자는 한 명도 없었 다. 이러한 점을 고려하여 본 연구에서는 ABW를 IBW로 나눈 값으로써 두 군을 비교해보았고, 그 결 과 유의한 차이는 없었다.
본 연구에서는 vancomycin의 TDM 자문을 의뢰 한 환자들의 혈중 크레아티닌 변화를 관찰하면서 신 독성에 영향을 미치는 요인을 알아보고자 하였다. 기 존의 국내논문은 vancomycin TDM의 유용성 중심 의 연구가 주를 이루고 있고, 아직 한국인을 대상으 로 한 vancomycin에 의한 신독성 위험요인에 대한 연구는 미비하다. 반면 해외에서는 MRSA pneu- monia와 같이 특정 적응증을 가진 환자, 만 18세 미 만의 소아 등 다양한 집단을 대상으로 신독성 위험인 자 분석이 이루어지고 있다. 그러나 각 논문마다 유 의한 위험인자가 다소 차이가 있어 아직까지 그 인과 관계가 명확하게 밝혀지지는 않았다. 따라서 본 연구 에서는 vancomycin에 대한 모니터링이 이루어지고 있는 성인 환자를 연구대상자로 선정하여 신독성에 영향을 미치는 요인에 대해 분석해보았다.
TDM이란 약동학과 약력학적 원리에 의해 약물의 혈중농도를 파악하고 환자의 상태를 확인한 후 개별 적인 약물의 투여량과 투여간격을 자문하고 그 결과 를 관찰하는 업무이다16). 이는 안전역이 좁은 약물을 대상으로 하여 용량의 적절성을 평가하고 부작용 발 생을 감소시킬 수 있는 업무라는 점에서 약사의 중요 한 업무 중 하나라 할 수 있다. 즉, 약사의 TDM 업무 는 환자 중심의 필수적인 임상 업무이다. 따라서 연구 를 통해 vancomycin의 신독성에 대한 구체적인 위 험인자들을 잘 알고 모니터링 한다면 더욱 효과적인 업무가 될 것이라 기대된다. 특히 본 연구에서 hepatic disease가 있는 환자의 경우 vancomycin 에 의한 신독성 발현의 위험성이 큰 경향을 보였다는 점을 고려할 때, 간 기능이 떨어지는 환자들은 모니터
링에 세심한 주의를 기울여야 할 것이다. 또한 환자가 위험인자를 가지고 있다고 생각되는 경우, van- comycin 투여 후 첫 TDM이 늦어지지 않도록 그 시 점을 앞당기거나 의뢰주기를 짧게 하는 등 보다 적극 적인 모니터링이 될 수 있도록 하는 것이 좋겠다.
하지만 본 연구는 몇 가지 제한점이 있다. 첫째, single center에서 vancomycin TDM 환자를 대 상으로 후향적으로 분석했다. 따라서 약물 투여 방 법과 수액 사용에 따른 반응의 차이를 고려할 수 없 었다. 둘째, 표본수가 작아 검증력이 약했다. 이에 적응증 또는 기저질환에 따른 환자군의 비교에 제한 이 있었다. 셋째, 실제 trough 농도가 아닌 첫 번째 TDM 시 측정한 vancomycin의 농도를 trough 농 도로 정했다. 환자에 따라 채혈시간이 다르므로 vancomycin의 농도가 더 높거나 낮게 측정되어 결 과에 영향을 줄 수 있다. 넷째, 혈중 크레아티닌 농 도가 모든 신기능 변화를 반영하기 힘들다. 일례로 혈중 크레아티닌 농도의 유의한 차이가 없음에도 반 감기가 길어지는 양상을 보여 vancomycin의 용량 을 감량해야 하는 사례가 있었다. 다섯째, 신기능에 따라 용량 조절하는 약물로 하여 일부 vasopressor 의 영향을 고려하지 못했다. 따라서 향후 대규모 집 단을 대상으로 한 전향적인 연구가 요구된다. 또한 trough 농도가 높을수록 신독성 위험이 증가하는 만큼 실제로 높은 trough 농도가 치료에 긍정적인 효과가 미치는지 그 유익성에 대해 고찰해 볼 필요 가 있을 것이다.
결론
본 연구는 서울대학교병원에서 연구기간 동안 vancomycin의 TDM 자문을 의뢰한 환자를 대상으 로 하여 신독성의 발현빈도와 신독성에 영향을 미치 는 요인을 알아보았다. 연구결과, vancomycin에 대 한 모니터링이 이루어지고 있는 환자 총 173명 중 21명 (12.1%)에 서 신 독 성 이 의 심 되 었 다 . Vancomycin에 의한 신독성이 나타난 환자군은 신 독성이 나타나지 않은 환자군보다 평균 trough 농 도와 첫 번째 trough 농도가 유의적으로 높았고, 투
여기간이 14일 이상인 환자가 유의하게 많았다. 하 지만 trough 농도와 투여기간은 임상경과에 따라 변경될 수 있는 항목이므로 신독성 예방을 위해 약물 관련인자를 조절하는 한계가 있다. 한편, van- comycin의 초기 투여량이 적었음에도 불구하고 신 독성의 위험성이 크게 나타났다. 이는 투여량 외의 다른 위험인자가 있을 것이라 사료되며, 본 연구에서 는 유의적이지는 않았으나 기저질환이 신독성에 영 향을 미치는 경향을 보이고 있었다. 이를 바탕으로 연구대상을 넓혀 환자관련인자에 대한 추가적인 연 구가 필요하다고 사료된다. 보다 구체적인 신독성 위 험인자가 밝혀져 TDM 자문 시 이에 대한 사전검토 가 이루어진다면, 치료의 유익성을 위한 trough 농 도 상향을 고려함과 동시에 부작용 발생을 감소시키 는데 기여할 수 있을 것이다.
참고문헌
1) Stevens D.L. : The role of vancomycin in the treatment paradigm, Clinical infec- tious diseases, 42, 51-7 (2006)
2) Lodise T.P., Graves J., Evans A., Graffunder E., Helmecke M., Lomaestro B.M., and Stellrecht K. : Relationship between vancomycin MIC and failure among patients with methicillin-resistant Staphylococcus aureus bacteremia treated with vancomycin, Antimicrob Agents Chemother, 52, 3315-3320 (2008)
3) Rybak M., Lomaestro B., Rotschafer J.C., Moellering R. Jr, Craig W., Billeter M., Dalovisio J.R., and Levine D.P. : Therapeutic monitoring of vancomycin in adult patients:
A consensus review of the American society of health-system pharmacists, the infec- tious disease society of America, and the society of infectious disease pharmacists, American journal of health-system phar- macists, 66, 82-98 (2009)
4) Hermsen E.D., Hanson M., Sankara narayanan J., Stoner J.A., Florescu M.C., and Rupp M.E. : Clinical outcomes and nephrotoxicity associated with van- comycin trough concentrations during treatment of deep-seated infection, Expert opinion, 9, 9-14 (2010)
5) Jeffres M.N., Isakow W., Doherty J.A., Micek S.T., and Kollef M.H. : A retro- spective analysis of possible renal toxicity associated with vancomycin in patients with health care-associated methicillin- resistant Stapylococcus aureus pneumo- nia, Clinical therapeutics, 29, 1107-1115 (2007)
6) Hazlewood K.A., Brouse S.D., Pither W.D., and Hall R.G., Vancomycin-associ- ated nephrotoxicity: Grave concern or death by character assassination?, the American journal of medicine, 123, 182.e1-182.e7 (2010)
7) Elting L.S., Rubenstein EB, Kurtin D., Rolston K.V., Fangtang J., Martin C.G., Raad I.I., Whimbey E.E., Manzullo E., and Bodey G.P. : Mississippi mud in the 1990s- risks and outcomes of van- comycin-associated toxicity in general oncology practice, Cancer, 83(12), 2597- 2607 (1998)
8) Farber B.F. and Moellering R.C. Jr : Retrospective study of the toxicity of preparations of vancomycin from 1974 to 1981, Antibicrob Agents Chemother, 23, 138-41 (1983)
9) Lodise T.P., Lomaestro B., Graves J., and Drusano G.L. : Larger vancomycin doses (at least four grams per day) are associ- ated with an increased incidence of nephrotoxicity, Antimicob Agents Chemother, 52, 1330-1336 (2008)
10) Lodies T.P., Patel N., Lomaestro B.M., Rodvold K.A., and Drusano G.L. : Relationship between initial vancomycin concentration-time profile and nephro- toxicity among hospitalized pateints, Clinical infectious diseases, 49, 507-14 (2009)
11) Pritchard L., Baker C., Leggett J., Sehdev P., Brown A., and Bayley K.B. : Increasing vancomycin serum trough concentrations and incidence of nephro- toxicity, the American journal of medi- cine, 123(12), 1143-1149 (2010)
12) Naughton C.A. : Drug induced nephro- toxicity, American academy of family physicians, 78, 6, 743-750 (2008)
13) Tisdale J.E. and Miller D.A., drug- induced diseases : prevention, detection, and management, second edition, American society of health-system pharmacists, SectionⅨ, Chapter43 14) Moellering RCJr, Vancomycin : A 50-
year reassessment, Clinical infectious diseases, 42, 3-4 (2006)
15) Hidayat L.K., Hsu D.I., Quist R, Shriner K.A. and Wong-Beringer A. : High dose vancomycin therapy for methicillin resistant Staphylococcus aureus infec- tions - efficacy and toxicity, Arch Intern Med, 166, 2138-44 (2006)
16) 김해숙, 이숙향 : Vancomycin Therapeutic Drug Monitoring 운영 실태 조사와 업무 개 선 방안, 한국임상약학회지, 19, 2, 120-130 (2009)
![Table 1. Demographics and Characteristics for Patients 특성 남 : 여 [세] ≥60 [kg] [mg/dl] [g/dl] [ml/min] Cockcroft-Gault Sanaka [%] Cockcroft-Gault Sanaka [mg/dl] [일] [일] [mg/kg] [일] ≥14 <14 [mg/kg/day] >30 ≤30 [회] [일] [일] [mg/L] 평균 1st HAP CNS infect](https://thumb-ap.123doks.com/thumbv2/123dokinfo/4717473.262822/4.798.420.719.187.989/table-demographics-characteristics-patients-cockcroft-sanaka-cockcroft-sanaka.webp)