책임저자:김병창, 부산시 중구 대청동 4-12 메리놀병원 진단검사의학과, 600-730 Tel: 051-4612-279, Fax: 051-441-6950 E-mail: [email protected]
접수일 : 2009년 5월 4일, 게재승인일 : 2009년 6월 30일
비장적출을 하지 않은 ABO 혈액형 부적합 생체 신장이식 경험
메리놀병원 신장내과
1, 외과
2, 비뇨기과
3, 이식코디네이터
4, 진단검사의학과
5공진민1ㆍ이동렬1ㆍ정준헌2ㆍ최재호2ㆍ이정오3ㆍ이화림4ㆍ김병창5
ABO Blood Group Incompatible Living Donor Kidney Transplantation without Splenectomy
Jin Min Kong, M.D.
1, Dong Ryul Lee, M.D.
1, Joon Heun Jeong, M.D.
2, Jae Ho Choi, M.D.
2, Jung Oh Lee, M.D.
3, Wha Rhim Lee, R.N.
4and Byung Chang Kim, M.D.
5Division of Nephrology
1, Departments of Surgery
2, Urology
3and Transplant Coordinator
4, Laboratory Medicine
5, Maryknoll Medical Center, Busan, Korea
Background: Serious organ shortage necessitates ABO incompatible (ABOi) kidney transplantation (KT). Recent reports utiliz- ing rituximab instead of splenectomy and tacrolimus (FK)-based triple immunosuppressants showed excellent graft outcome.
Methods and Results: Thirteen cases of ABOi living donor KT have been performed since Feb. 2007 in our center. Donor and recipient blood group was B to O (n=5), A1 to O (2), AB to B (2), AB to A1 (1), A1 to B (2) and B to A1 (1). Rituximab was given at 4 weeks before transplantation. Plasmapheresis (PP) was initiated at 7∼14 days before transplantation with concurrent immunosuppressants. The number of pretransplant PP was 5.7±1.4. Posttransplant PP was also performed in 6 patients with higher initial titer of ABO antibody (IgG ≥256; n=2), rapidly rising antibody titer during the critical period of 2 weeks posttransplantation (n=2), or increase in serum creatinine during the critical period while awaiting pathology report of graft biopsy (n=2). Mean number of posttransplant PP in these 6 patients was 2.2±1.3. Median IgG anti-ABO anti- body titer before precondition, at transplantation, at 2 weeks and at 6 months was 64 (8∼512), 2 (1∼8), 2 (1∼16) and 6 (1∼16), respectively. IgM titer at corresponding time point was 16 (2∼128). 1 (1∼1), 1 (1∼2) and 1.5 (1∼4), respectively.
Median follow up was 8 (5∼27) months. No patient or graft was lost. No patient developed acute humoral rejection. Graft function remained stable with latest serum creatinine 1.2±0.3 mg/dl.
Conclusions: ABOi living donor KT without splenectomy can be safely performed with the use of current preconditioning and immunosuppressive regimen, and is therefore a valuable option for expanding donor pool and should be actively per- formed in Korea.
Key Words: ABO incompatible kidney transplantation, Antibody mediated rejection, Rituximab 중심 단어: 혈액형 부적합 신장 이식, rituximab, 항체 매개 거부반응
서 론
신장이식은 말기신부전의 최선의 치료법임에도 불구하 고 말기신부전 환자들 중 일부만 신장이식을 받을 수 있 다. 2007년 한 해 동안 국내에서 말기신부전으로 진단 받고 신대체요법을 새로 시작한 환자의 수는 약 9,200명 인 반면 신장이식을 받은 환자의 수는 928명에 불과하여 투석환자의 수 및 뇌사 장기 대기자의 수가 매년 빠르게
증가하고 있다.(1) 혈액형 부적합(ABOi) 이식은 생체 신 장 이식의 기회를 높여 장기 부족 상태를 완화시킬 수 있는 유용한 수단의 하나이다.
ABO 혈액형 항원은 적혈구 표면뿐 아니라 혈관 내피 세포 등 인체의 조직에 광범위하게 표현된다. 따라서 ABOi 공여자의 장기를 이식하는 경우, 적절한 술 전 또 는 술 후 처치를 하지 않는다면 수여자의 혈액에 있는 ABO 항체에 의해 체액 면역 기전의 혈관성 거부 반응이 일어날 수 있다. Alexandre 등은(2,3) 1985년 혈장 교환 및 비장 적출 등의 술 전 처치후의 성공적인 ABOi 신이 식을 처음 보고하였으나, 서구에서는 뇌사자 장기 공급이 비교적 용이하고, 또한 ABOi 생체 이식 생존율이 뇌사 장기 이식 생존율에 비해 낮으면서도 비장적출 등의 번
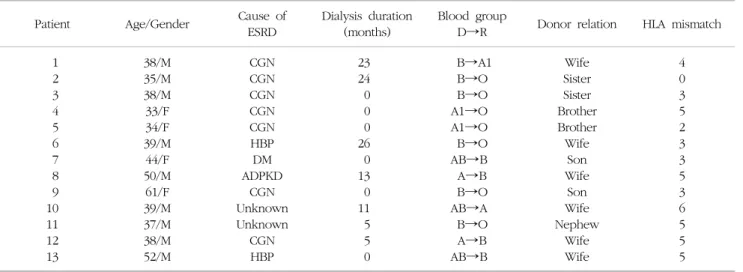
Table 1. Patient characteristics and follow up data
Patient Age/Gender Cause of ESRD
Dialysis duration (months)
Blood group
D→R Donor relation HLA mismatch 1
2 3 4 5 6 7 8 9 10 11 12 13
38/M 35/M 38/M 33/F 34/F 39/M 44/F 50/M 61/F 39/M 37/M 38/M 52/M
CGN CGN CGN CGN CGN HBP DM ADPKD
CGN Unknown Unknown CGN HBP
23 24 0 0 0 26 0 13 0 11 5 5 0
B→A1 B→O B→O A1→O A1→O B→O AB→B A→B B→O AB→A B→O A→B AB→B
Wife Sister Sister Brother Brother Wife
Son Wife Son Wife Nephew
Wife Wife
4 0 3 5 2 3 3 5 3 6 5 5 5 (Continued)
거롭고 비용이 드는 술전 처치가 필요한 등의 이유로, ABOi 이식은 서구에서는 1990년대 말까지 거의 시행되 지 않았다. 그러나 일본에서는 뇌사자 장기 공급이 되지 않아 장기 부족 때문에 ABOi 이식을 할 수 밖에 없었는 데, 90년대 중반까지의 이식신 생존율은 혈액형 적합 이 식에 비해 좋지 않았으나 90년대 후반 tacrolimus 및 mycophenolate가 도입되면서 혈액형 적합 이식과 차이 없는 좋은 성적이 보고 되었고,(4) 이에 고무 받아 2000 년대 초반부터 북미 및 유럽의 이식기관에서 ABOi 신장 이식이 시작되었다.(5-7) 특히 Tyden 등은 2003년 비장 적출 대신 rituximab을 사용 후 좋은 성적을 보고하여, 비장 적출과 관련된 단기적 및 장기적 부작용 없이 ABOi 이식이 가능하게 되었다.(6)
저자들은 2007년 2월 비장적출을 하지 않고 ABOi 생 체 신장 이식을 시행한 이후 현재까지 13예의 부적합 이 식을 하여 보고하는 바이다.
대상 및 방법 1) 대상 환자
2007년 2월부터 2009년 4월까지 14명의 ABOi 신장 이 식 희망자가 있었으며 이중 혈액형 항체 역가가 매우 높 은 1명(IgG 항체가 4,096)을 제외한 13명에서 ABOi 이식 이 시도되었다. 공여자와 수여자의 혈액형 조합은 B형에 서 O형 5명, A1형에서 O형 2명, AB형에서 B형 2명, AB 형에서 A1형 1명, A1형에서 B형 2명, B형에서 A1형 1명 이었다. 수여자의 평균연령은 41±8 (33∼61)세, 남자 9
명 이었으며 모두 초회 이식이었다. 6명은 투석 시작 전 이식이었고, 4명은 복막투석, 3명은 혈액투석을 하였으며 투석 환자의 평균 투석기간은 15±9개월이었다. 말기신 부전의 원인은 만성 사구체신염 7명, 고혈압 2명, 당뇨성 신증 1명, 다낭신 1명, 원인불명 2명이었다. 공여자의 평 균연령 36±7 (25∼49)세, 남자 4명이었고 수여자와의 관계는 부인 6명, 형제자매 4명, 아들 2명, 조카 1명이었 다. HLA 불일치 수는 3.8±1.6 (0∼6)이었다(Table 1).
2) 방법
신장이식 1개월 전에 rituximab을 투여하였는데 2008 년 9월 이전에는 375 mg/m2, 이후에는 187 mg/m2를 1 회 정맥 주사 하였다. 신장이식 7∼14일 전에 혈장교환 을 시작하였는데 1 혈장량을 5% albumin으로 치환하였 고 수술 직전 혹은 신생검 전후의 혈장교환은 혈액응고 인자 보충을 위해 치환량의 반은 albumin 용액, 반은 신 선냉동혈장을 사용하였다. 또 매 혈장교환 직후에 IVIG 100 mg/kg을 정주하였다. 이식 전 혈장교환은 IgG 또는 IgM ABO 혈액형 항체의 역가가 수술 당일에 8 이하가 될 때까지 격일 또는 매일 시행하였고, 이식 후 혈장교환 은 술 후 2주 동안에 다음의 경우 선택적으로 하였는데, 1) IgG 혹은 IgM 항체 역가의 rituximab 투여 전의 초회 측정치가 256 이상인 경우, 2) 술 후 2주간 혈액형 항체 가 최저측정치에 비해 3단계 이상 상승하는 경우, 3) 술 후 2주 동안 혈청 creatinine이 15∼20% 이상 증가하여 신생검을 한 환자에서, 본원의 경우 신생검 조직 결과가 나오기까지 2∼3일이 소요되므로, 그 기간 동안에 em-
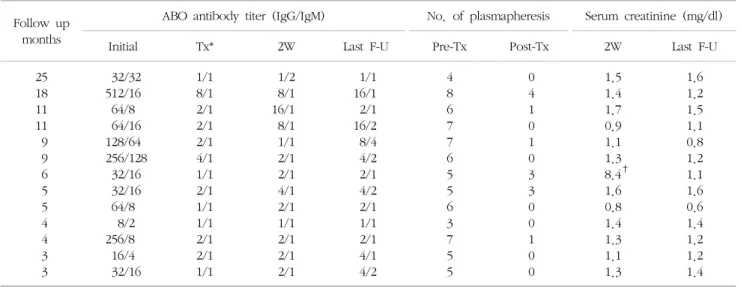
Table 1. Continued
Follow up months
ABO antibody titer (IgG/IgM) No. of plasmapheresis Serum creatinine (mg/dl)
Initial Tx* 2W Last F-U Pre-Tx Post-Tx 2W Last F-U
25 18 11 11 9 9 6 5 5 4 4 3 3
32/32 512/16 64/8 64/16 128/64 256/128
32/16 32/16 64/8 8/2 256/8 16/4 32/16
1/1 8/1 2/1 2/1 2/1 4/1 1/1 2/1 1/1 1/1 2/1 2/1 1/1
1/2 8/1 16/1
8/1 1/1 2/1 2/1 4/1 2/1 1/1 2/1 2/1 2/1
1/1 16/1 2/1 16/2 8/4 4/2 2/1 4/2 2/1 1/1 2/1 4/1 4/2
4 8 6 7 7 6 5 5 6 3 7 5 5
0 4 1 0 1 0 3 3 0 0 1 0 0
1.5 1.4 1.7 0.9 1.1 1.3 8.4
†1.6 0.8 1.4 1.3 1.1 1.3
1.6 1.2 1.5 1.1 0.8 1.2 1.1 1.6 0.6 1.4 1.2 1.2 1.4 Abbreviations: CGN, chronic glomerulonephritis; HBP, hypertension; ADPKD, autosomal dominant polycystic kidney disease.
*on transplantation day;
†DGF secondary to bleeding at operation room.
piric하게 혈장교환을 하였다.
첫 혈장교환 시점부터 tacrolimus, mycophenolate mofetil, prednisolone 투여를 시작하였는데 tacrolimus는 술 후 1개월까지 혈중농도 8∼12 ng/ml, 이후 4∼8 ng/
ml 되도록 용량 조절하였고, mycophenolate는 술 후 첫 3개월까지 750 mg bid, 이후 500 mg bid 투여하였으며 steroid는 술 전 0.3 mg/kg/day 경구 투여, 수술 당일 5 mg/kg bid IV, 2일에 4 mg/kg qd IV, 3일에 2 mg/kg qd IV, 4일에 0.3 mg/kg/day 경구 투여 후 점차 감량하 여 술 후 3개월에 5 mg/day의 유지용량이 되게 하였다.
급성거부반응의 진단은 혈청 creatinine의 상승이 있으 면서 신생검상 거부반응의 조직 소견이 보이는 조직적 진단, 또는 임상적으로 다른 신기능 저하의 원인이 배제 되고 임상 경과가 급성거부에 합당한 경우의 임상적 진 단에 의하였는데, 이식 초기 3주 이내에는 항체 매개 거 부반응(AMR)의 위험이 큰 시기이므로 혈청 크레아티닌 이 15∼20% 이상 증가하는 경우 모두 신생검을 하는 것 을 원칙으로 하였다. 프로토콜 생검은 하지 않았다.
IgM 항ABO 혈액형 항체는 immediate spin 방법(식염 수 방법)으로 측정하였는데, 3% 신장 공여자 혈구 부유 액 200 μml에 동량의 식염수를 순차적으로 첨가하여 2 배씩 희석한 시험관들을 3,400 RPM으로 15초간 원심분 리 후 1+응집도를 보인 최대 희석배수를 IgM 역가로 하 였다. IgG ABO항체는 gel card(DiaMed AG, Cressier sur Morat, Switzerland)를 이용하여 측정하였는데, 공여 자 혈구 부유액 50 μml을 gel card에 올려 15분 배양 후 gel card 용 원심분리기로 1,175 RPM 10분간 원심분
리 후 1+응집도를 보인 역가를 IgG 역가로 하였다.
결 과
추적 기간 중간값은 8 (5∼27)개월이었고 환자 및 이 식신 손실은 없었으며 급성 AMR도 관찰할 수 없었다.
이식 전 혈장교환 회수는 5.7±1.4(평균±표준편차)회 이었으며, 이식 후 혈장교환은 6명에서 2.2±1.3회 하였 는데 IgG 항체 초기 역가가 256 이상이거나(2명), 술 후 2주 동안 혈액형 항체가 최저 측정치에 비해 3단계 이상 상승하였거나(2명), 술 후 2주 동안 혈청 creatinine이 15
∼20% 이상 증가한 환자에서 신생검을 한 뒤 병리진단 결과가 나오기까지 empiric하게 한 경우(2명)였다.
IgG ABO 항체의 중간값은 rituximab 투여 전의 초기 값, 이식 당일, 2주, 1개월 및 6개월에 각각 64 (8∼512), 2 (1∼8), 2 (1∼16), 2 (1∼8) 및 6 (1∼16)이었고 같은 시점에서의 IgM 값은 각각 16 (2∼128). 1 (1∼1), 1 (1
∼2), 1 (1∼4) 및 1.5 (1∼4)이었다(Table 1).
혈청 creatinine의 상승으로 술 후 2주 이내에 3명의 환자에서 4회 신생검을 하였는데, 이 중 1예(#7)는 수술 중 실혈로 인한 이식신 기능 지연(DGF)으로 tacrolimus 의 용량을 줄이고 2주간 혈액투석을 받은 환자로서 술 후 14일에 시행한 생검에서 급성 세포성 거부반응 IA의 조직소견을 보였고 이때 ABO 항체 역가는 2로 낮았으 며, steroid 충격 등의 치료 후 회복되었다. 나머지 2명의 환자에서는 면혁형광염색에서 C4d의 국소성 염색을 보 였으나 ABO 항체 역가는 1∼2로 낮았으며 광학현미경
소견 정상이었던 환자로, 특별한 치료 없이 저절로 crea- tinine이 감소되었다. 또 다른 1명의 환자에서(#1) 술 후 2개월에 creatinine이 1.4에서 2.2 mg/dl로 증가하여 신 생검 한 결과 C4d의 미만성 염색이 보였으나 생검 당시 ABO 항체 역가가 1로 낮았고, 광학현미경 상 특이 소견 이 없었으며 tacrolimus 혈중농도 10.5 ng/ml로, CNI 신 독성의 진단 하에 tacrolimus 용량 감소 후 creatinine 1.6 mg/dl으로 신기능이 호전되었다.
술 후 2주의 혈청 creatinine은 DGF 1예를 제외한 환 자들에서 1.3±0.3 (0.8∼1.6) mg/dl이었고, 마지막 추적 시의 모든 환자의 creatinine은 1.2±0.3 (0.6∼1.6) mg/dl이었다. 술 후 2주 및 3개월의 혈청 tacrolimus 농 도는 각각 8.7±4.3 ng/ml 및 7.9±3.4 ng/ml이었다. 입 원 치료를 요하는 감염, CMV 감염 또는 질환, BK 바이 러스 신병증 등은 없었다.
고 찰
저자들은 2007년 2월 이후 13예의 ABOi 생체 신장이 식을 하였고, 8 (5∼27)개월 추적한 현재까지 환자 및 이 식신 손실은 없었으며, 급성 AMR도 없었다. 또한 비장적 출을 하지 않고 대신 rituximab을 사용함으로써 비장적출 에 의한 단기간의 수술 합병증 및 평생 동안의 감염위험 의 증가 등의 부작용을 피할 수 있었으며, rituximab을 사용함에도 불구하고 감염 빈도의 증가는 관찰할 수 없 었다. 신장 공여 희망자의 약 35%는 혈액형이 부적합하 므로(8) ABOi 이식이 활발히 시행된다면 생체 신장이식 이 큰 폭으로 증가할 수 있을 것으로 기대할 수 있는데, 실제로 ABOi 신장이식이 활발히 이루어지고 있는 일본 에서는 생체신장이식의 20% 이상을 ABOi 이식이 차지하 고 있다.(4) 또한 국내에서 비교적 활성화된 교환이식과 ABOi 이식이 병행된다면 생체 신장이식의 기회는 더욱 커질 수 있을 것이다. 가령 O형의 수여 희망자와 AB형 공여 희망자는 교환 이식의 대상자를 찾기가 힘들며, 따 라서 다중 교환 이식의 장애가 되고 있는데 이들을 ABOi 이식으로 해결을 한다면 다중 교환 이식이 더 활발히 이 루어질 수 있을 것이다.
Alexandre 등은 1985년 비장적출과 cyclosporin을 포 함한 면역억제제, 이식 전 혈장 교환 등의 현대적 프로토 콜을 처음 사용하여 성공적인 ABOi 생체신장이식을 보 고하였으나 1년 이식신 생존율 70%로 혈액형 적합 이식 에 비해 낮은 성적이었고,(2,3) 1990년대 후반까지 주로 일본에서 행해진 ABOi 이식의 성적도 적합 이식에 비해 좋지 않았으나, tacrolimus 및 mycophenolate를 사용하
기 시작하면서 2000년 이후의 환자 및 이식신 생존율은 혈액형 적합 이식과 차이 없는 좋은 성적이 보고 되고 있다. 일본의 ABOi 생체 신장이식의 보고를 보면 1989 년부터 2006년까지 1,012명의 이식 환자가 있었는데, 1989∼1994년에 이식한 환자의 1년 및 5년 이식신 생존 율은 각각 80%, 68%였고, 1995∼2000년의 1년 및 5년 이식신 생존율은 84%, 79%였던 반면, 2000∼2006년에 이식한 환자 567명의 1년 및 5년 생존율은 96% 및 90%
로 매우 좋은 성적이 보고 되었다.(4) Tanabe 등은 단일 기관 연구에서 cyclosporine과 azathioprine 등을 사용하 여 1989∼1999년에 이식한 ABOi 환자 105명의 1년 및 5 년 이식신 생존율은 각각 78% 및 73%인 반면 tacrolimus 와 mycophenolate mofetil을 사용한 2000∼2004년 이식 환자 117명의 1년 및 5년 이식신 생존율은 94% 및 90%
로 현저한 향상이 있었음을 보고하였다.(9) 또한 Tyden 등은 비장적출 대신 rituximab을 사용하고 수술 전과 수 술 후에 면역흡착방법으로 혈액형 항체를 제거하는 프로 토콜을 사용하여 2001년 이후 60예의 ABOi 신장이식을 하여 평균 17개월의 추적기간 동안 AMR은 관찰할 수 없 었으며, 면역억제제 복용을 중단한 1예와 환자 사망 1예 를 제외한 모든 예의 이식신 생존을 보고하였다.(10)
혈액형 항체에 의한 급성 AMR은 이식 초기 1∼3주의 소위 위험시기(critical period)에 집중적으로 일어나며 그 이후에는 혈장 교환 등으로 감소하였던 혈액형 항체의 역가가 다시 상승하는 한편 이식신에 혈액형 항원의 표 현이 지속됨에도 불구하고 accommodation에 의해 이식 신은 생존하게 된다. Takahashi 등은 441예의 ABOi 신 이식 환자 중에서 관찰된 20예의 급성 AMR이 모두 이식 3주 이내에 발생하였고, 이 중 17 (85%)예는 1주 이내에, 나머지 3예는 2∼3주에 발생함을 보고하였는데(11) 이는 ABOi에 의한 이식신 손실의 위험이 이식 초기에 국한됨 을 의미한다. 실제로 일본의 ABOi 신장이식 등록 자료를 보면 이식신 손실이 이식 직후에 집중적으로 일어나고 그 이후의 이식신 탈락율은 혈액형 적합 이식과 차이가 없었다.(12) 따라서 ABOi 이식의 성공의 관건은 이식 첫 2∼3주 동안 혈액형 항체를 안전한 수준으로 낮게 유지 하는 것이라 할 수 있으며 이식 후 첫 수 주 동안 적절한 치료로 AMR을 방지한다면 그 이후는 혈액형 적합 이식 과 차이가 없는 좋은 장기간의 경과를 기대할 수 있다.
수술 당일의 혈액형 항체를 어느 수준까지 감소시켜야 하는가에 대해서는 논란이 있으며 지역과 이식 센터에 따라 항체의 목표 역가가 다른데, 일반적으로 유럽에서는 4 이하,(10) 미국은 8 또는 16 이하,(10,13) 일본은 32 이 하를(9) 목표 역가로 하여 수술 전 혈장 교환 등에 의해
항체를 낮추고 있다. Tanabe 등은 수술일의 항체 목표치 를 32 이하로 하는 프로토콜을 사용한 환자에 관한 최근 의 분석 보고에서,(14) 전체 환자 57명 중 7명이 수술일 의 항체 역가가 32이었는데, 이 중 5명에서 creatinine 상 승을 동반한 임상적 급성 AMR이 발생하였고 4명(57%)에 서 급성 및 만성 AMR에 의한 이식신 손실이 일어난 반 면, 수술일의 항체가 16 이하인 나머지 50명의 환자에서 는 14명에서 급성 AMR이 발생하여 3명(6%)에서만 급성 및 만성 AMR에 이한 이식신 손실이 있었다 하였으며, 다중 회귀 분석에서 수술 당일의 항체 역가 32가 급성 AMR 발생의 독립적 위험인자라고 보고하여 항체를 16 이하로 낮추는 것이 안전함을 시사하였다. 한편 수술일 의 항체 목표를 4 이하로 낮게 하는 경우, 물론 낮을수록 안전하기는 하나, 기저치가 높은 환자의 일부는 수술 전 에 많은 회수의 항체 제거에도 불구하고 수술일에 목표 역가에 도달하지 못하여 수술에서 제외될 수 있는데, 실 제로 이와 같은 프로토콜을 사용하는 센터에서 21%의 환 자가 수술의 기회를 잃었다고 보고 되었다.(15) 따라서 수술 당일의 항체 역가 8 또는 16이 현재로서는 적절한 것으로 생각되며, 저자들의 경우 8을 목표로 하였고, 현 재까지 초기 항체 역가가 4096으로 매우 높아 처음부터 전처치를 시작하지 않은 1예를 제외한 나머지 13예는 모 두 수술일까지 목표 역가 이하로 낮추어 성공적으로 수 술할 수 있었고 AMR도 현재까지 발생하지 않았다.
수술 후 혈장교환을 해야 하는가에 관해서도 논란이 있는데, 일본의 대다수의 센터에서는 이식 후 혈장교환을 하지 않는 반면,(4) 대부분의 유럽과 미국의 센터에서는 routine하게 이식 후 첫 2주간 면역흡착 또는 혈장교환을 한다.(5-7) 이식 후 항체 제거를 하는 센터의 환자에 비 해 하지 않은 환자들의 급성 AMR의 빈도가 높으나, 이 들 센터들의 프로토콜 간에는 이식 후 항체 제거 여부 이외에도 목표 항체 역가, IVIG 사용 여부, 면역억제제의 용량 등의 차이들이 있어 AMR 발생에 술 후 혈장교환이 어느 정도 영향을 주었는지 정확히 알기 어려우나, 수술 후 첫 2주 동안의 위험시기에 낮은 농도의 항체를 유지 하는데 술 후 혈장교환이 어느 정도 기여했을 가능성이 있다. 그러나 이식 후의 혈장교환은 비용을 증가시키므 로 비용 대비 효과 측면을 고려하여 적정한 조정이 필요 할 것으로 생각되며, 저자들의 경우 이식 후 혈장교환을 routine 하게 하지는 않고 AMR의 위험이 높을 것으로 생 각되는 일부 환자들에서만 선택적으로 하였으며, Wilpert 등도 이식 후 첫 2주간 혈액형 항체가 일정 수준 이상 상 승하는 환자들에서만 선택적으로 면역흡착을 하는 프로 토콜을 사용하여 좋은 결과를 보고한 바 있다.(15)
C4d의 염색은 혈액형 적합 이식 환자에서 AMR의 소 견 중 하나로 불량한 예후의 지표이나, ABOi 신장 이식 에서는 이식신 기능이 안정된 환자의 프로토콜 생검의 80%∼94%에서 C4d의 염색을 볼 수 있어,(13,16) ABOi 신장 이식에서는 AMR 보다는 accommodation을 가리키 는 소견이라는 견해가 많다. 실제로 ABOi 환자의 이식 초기의 프로토콜 생검에서 C4d의 염색 정도가 심할수록, 추적 프로토콜 생검의 세뇨관 위축, 간질 섬유화 등의 만 성 이식신의 조직 변화가 오히려 적다는 보고도 있 다.(17) 저자들의 경우 5예의 임상 적응 신생검 중 4예에 서 미만성 혹은 국소성 C4d 염색을 관찰하였으나, 생검 당시 혈액형 항체의 역가가 낮았고 광학 현미경 소견이 정상이어서 AMR은 아닌 것으로 생각된다.
혈액형 항체의 정확한 측정은 ABOi 이식 수술의 성공 의 기본 요건이나, 일반적으로 많이 사용하고 있는 tube 방법은 검사 기법의 표준화가 되어있지 않아 결과치의 기관간의 차이가 커서, 일본의 이식센터들을 대상으로 한 조사를 보면 기관간의 차이가 최고 8배까지 난다고 하였 다.(18) 저자들의 경우 IgG 항체는 비교적 재현성이 좋은 것으로 알려진 gel card 방법을 사용하였다. 향후 검사기 법의 국제적인 표준화가 필요하며, 또한 더 객관적이고 재현성이 좋은 것으로 알려진 flow cytometry를 이용하 는 것도 고려해야 할 것으로 생각된다.(18)
ABOi 이식은 현재의 항체 제거 및 면역억제 프로토콜 을 사용하는 경우 안전하게 시행될 수 있으며, 혈액형 적 합 이식과 차이가 없는 단기간 그리고 장기간의 좋은 성 적을 기대할 수 있다. 혈액형의 장벽을 제거함으로써 생 체신장이식을 의미 있게 증가시킬 수 있으며, 또한 교환 이식과 병행한다면 말기신부전 환자들의 이식 기회를 더 욱 높일 수 있을 것이므로 국내에서도 활발히 시행되어 야 할 것으로 생각된다.
REFERENCES