GaN 기반 광전극을 이용한 광전기화학적 물분해 수소 생산
허지원1·배효정2·하준석1,2,†
1전남대학교 화학공학부, 2전남대학교 광전자융합기술연구소
Photoelectrochemical (PEC) Water Splitting using GaN-based Photoelectrode
Jiwon Heo1, Hyojung Bae1,2, and Jun-Seok Ha1,2,†
1Department of Advanced Chemicals & Engineering, Chonnam National University, 77 Yong-bong-ro, Buk-gu, Gwangju 61186, Korea 2Optoelectronics Convergence Research Center, Chonnam National University, 77 Yong-bong-ro, Buk-gu, Gwangju 61186, Korea
(Received March 7, 2021: Corrected March 26, 2021: Accepted March 30, 2021)
초 록: GaN은 III-V족 화합물 반도체로 밴드갭을 조절하는 것이 가능하고 화학적으로 안정하기 때문에 다른 물질에 비해 산성, 염기성 용액에서 부식이 적다. 또한 GaN의 밴드갭이 물의 산화·환원 준위를 포함하고 있어 외부전압 없이 물 분해가 가능하다는 장점이 있다. 하지만 GaN 자체만으로는 태양광-수소 변환 효율(solar-to-hydrogen conversion efficiency, STH)이 낮아 이를 개선하기 위해 최근 활발한 연구가 이루어지고 있다. 본 총설에서는 GaN을 PEC 물분해의 광전극으로 사용하기 위한 방법들과 연구에 대해 정리하였다.
Abstract: GaN has shown good potential owing to its better chemical stability than other materials and tunable bandgap with materials such as InN and AlN. Tunable bandgap allows GaN to make the maximum utilization of the solar spectrum, thus improves the solar-to-hydrogen (STH) efficiency. In addition, GaN band gap contains the oxidation and reduction level of water, so it can split water without external voltage. However, STH efficiency using GaN itself is low and has been actively studied recently to improve it. In this thesis, we have summarized the studies related to the use of GaN as a photoelectrode for photoelectrochemical water splitting.
Keywords: Gallium Nitride, Photoelectrode, Photoelectrochemical Water splitting
1. 서
론
현대 문명은 화석연료로 인해 이룩되었다고 해도 과언 이 아니다. 18세기 중엽, 영국에서 일어난 산업혁명으로 부터 시작되어 전 세계로 이어진 공업화에는 석탄을 이 용한 기술혁신이 있었으며 19세기 중후반에서 20세기 초, 2차 산업혁명을 거치면서 석유와 전기가 대중화되었 다. 이후 200여년이 지난 지금까지도 인류가 사용하는 에너지원의 근간은 석탄과 석유, 천연가스 등의 화석연 료이며 세계 1차 에너지 소비량의 80% 이상을 차지하고 있다.1) 화석연료를 기반으로 한 에너지 시스템은 온실가 스인 이산화탄소를 배출하기 때문에 지속적인 화석연료 사용으로 인한 기후 변화가 이미 세계 곳곳에서 일어나 고 있다. 이를 잘 알 수 있는 한 지표로서 지구 평균 기온 의 상승을 들 수 있다. 2006년부터 2015년까지 10년 동안 관측된 전 지구 평균 표면 온도는 1850-1900년의 평균보 다 0.87oC 상승했는데 이는 지구 표면 온도를 관측한 이 래 가장 급격한 변화이다.2,3) 화석연료에 대한 의존도를 줄일 필요성이 대두됨에 따 라 청정에너지인 수소에 대한 관심이 집중되고 있다. 수 소는 연소될 때 온실가스나 대기오염 물질을 배출하지 않 아 친환경적이지만 석유나 태양열처럼 채굴하거나 채집 하는 것이 불가능한 2차 에너지이기 때문에 1차 에너지 원을 통해서만 얻을 수 있다. 굉장히 역설적으로 현재 생 산되고 있는 수소의 대부분은 석탄이나 천연가스 등 화 석연료를 연소시켜 생산되는데 이 과정에서도 온실가스 나 대기오염 물질이 배출된다. 때문에 수소를 환경오염 이 없는 차세대 에너지원으로서 지속적으로 이용하기 위 해서는 화석연료를 사용하지 않는 수소 생산 방법을 연 구하는 것이 필요하다. †Corresponding author E-mail: [email protected]© 2021, The Korean Microelectronics and Packaging Society
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License(http://creativecommons.org/ licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
태양광은 태양으로부터 무한히 제공받는 에너지이고 물은 지구 상에 가장 많이 존재하는 물질이기 때문에 그 양이 한정되어 존재하는 화석연료와는 달리 에너지원 고 갈의 우려가 없다. 이런 관점에서 볼 때 태양 에너지로 물 을 분해하여 수소를 생산하는 것은 가장 이상적인 수소 생산방법이다. 태양에너지를 이용하여 수소를 생산하는 방법에는 크게 태양 전지 물분해(Photovoltaic Electrolysis; PV-E), 광화학 (Photochemical; PC) 물분해, 광전기화학(Photoelectrochemic-al; PEC) 물분해, 세 가지 종류가 있다. PV-E는 태양 전 지를 물이 담긴 전해조에 연결, 태양 전지로 생성된 전 류를 이용하여 물을 분해하는 방법이다. 이 방법은 10% 이상의 높은 태양광-수소 전환 효율(solar-to-hydrogen conversion efficiency, STH)을 갖지만 다른 방법에 비해 많 은 비용이 든다는 단점이 있다. PC 물분해는 광촉매를 이 용하여 수소를 생산하는 방법으로 간단하고 저렴하지만 STH가 1% 미만으로 매우 낮다. PEC 물분해는 PEC 셀을 이용하여 물을 분해하는 방법으로 태양전지와 물분해 전 해조를 사용하지 않아도 되기 때문에 최근 가장 많은 관 심을 받고 있는 분야이다. PEC 물분해는 다른 물분해 방 법에 비해 저렴한 비용으로 상당히 높은 STH를 나타내 며 양극과 음극에서 산소와 수소가 따로 분리되기 때문 에 별도로 분리 공정을 추가할 필요가 없어 비용을 절감 할 수 있다는 장점이 있다. 1972년 Fujishima와 Honda가 TiO2전극에 태양광을 조사하면 광전효과로 인해 전류가 흐르면서 물이 분해되어 수소가 발생한다는 것을 처음으 로 보고한 이후 현재까지도 활발한 연구가 이루어지고 있 다.4) 하지만 음극으로 사용되는 Pt가 매우 비싼 귀금속이 라는 점과 광전극인 TiO2의 밴드갭이 3.2 eV로 크기 때문 에 자외선 영역의 빛만 흡수할 수 있다는 단점이 존재한 다. 따라서 다양한 반도체 물질을 이용하여 PEC 물분해 연구가 진행되어왔다. 반도체 물질 중 GaN가 가장 처음 으로 PEC 물분해의 광전극으로 사용된 것은 1995년 Shyam S. Kocha와 John A. Turner에 의해서이다.5) GaN은
밴드갭이 물의 산화·환원 전위를 포함하고 있어 외부 전 압 없이도 물을 분해할 수 있다. 또한 GaN은 다른 산화 물 광전극에 비해 산·염기 환경에서도 화학적으로 매우 안정적이다. 하지만 여전히 광부식으로 인하여 PEC 물분 해 시스템의 안정성이 저하되는 문제를 가지고 있다. 뿐 만 아니라 GaN 자체의 밴드갭이 3.4 eV로 크기 때문에 태양 스펙트럼 중 자외선 영역 밖에 사용할 수 없다는 단 점이 존재한다. 따라서 수소 생산 효율을 증가시키기 위 해 태양 스펙트럼 흡수 효율을 향상시키고 광생성 캐리 어를 보다 빠르고 효과적으로 분리하고 수송하는 방법 등 의 연구 및 GaN의 광부식을 줄이는 연구가 주로 진행되 고 있다. 본고에서는 이러한 GaN의 PEC 물분해를 통한 수소생 산의 연구동향과 전망에 대해 다루어 보고자 한다.
2. 본
론
2.1. 태양광을 이용한 광전기화학 (PEC) 물분해의 구동 원리 PEC 물분해는 PEC 셀을 이용하여 물의 환원 반응을 통해 수소 기체를 생성하는 방법이다. PEC 셀은 광전효 과에 의해 태양에너지를 전기에너지로 변환시키며 반도 체 물질인 작업전극과 금속 물질인 상대전극, 그리고 전 해질로 이루어진다. 전해질과 접촉하고 있는 광전극에 빛이 입사되면 광전 효과에 의해 전극 물질의 밴드갭보다 큰 에너지를 갖는 파장의 빛을 흡수하여 전자-정공쌍을 생성한다. 광전효 과에 의해 생성된 전자-정공쌍은 광전극과 전해질 계면 에 생성된 band bending에 의해 전자와 정공으로 분리된 다. 분리된 정공은 양극과 전해질 계면에서 물(H2O)을 산 화시켜 양성자 이온(H+)을 생성하고 산소기체(O 2)를 발 생시킨다. 2OH− + 2h+ → ½O2(g) + H2O 분리된 전자(e−)는 외부회로를 따라 음극으로 이동, 전 해질을 통해 이동한 양성자 이온(H+)을 음극과 전해질 계 면에서 환원시켜 수소기체(H2)를 발생시킨다. 2H2O + 2e− → H2(g) + 2OH− 따라서 광전극의 효율은 광전극에서 생성되는 광전류 와 밀접한 관련이 있다. 광생성 캐리어의 수는 반도체의 광흡수효율에 의해 결정된다. 자연상태에서 물을 수소와 산소로 분해하는데 필요한 에너지는 4.0-6.5 eV로 지표면에서 얻을 수 있는 태양에 너지 1.1-3.5 eV 보다 크기 때문에 태양에너지를 이용하 여 물을 직접 분해하는 것은 불가능하지만 PEC 셀을 이 용하면 물을 분해하는데 필요한 최소 에너지는 1.23 eV 이다.6) H2O → H2 + ½O2 ΔG0 = 237.2 kJ/mol, E0 = 1.23 eV 외부 전압 없이 물을 분해하기 위해서는 광전극의 전 도대 전위가 수소 환원 전위인 0 V보다 낮아야 하고, 가 전자대 전위는 물의 산화 전위인 1.23 V보다 높은 값을 가져야 하기 때문이다. 다시 말하면, 반도체 광전극의 밴 드갭이 물과 수소의 산화·환원 전위를 포함하고 있어야 추가로 전압을 걸어주지 않아도 물을 분해할 수 있다는 것이다. 여기에 전자가 이동하면서 받는 저항이나 금속 과의 접촉에서 발생하는 전압강하 등 실제 조건을 고려 하더라도 1.6-1.7 eV 이상의 에너지면 물을 분해하여 수 소를 얻는 것이 가능하다.7)때문에 광전극으로 사용할 물 질은 밴드갭이 최소 1.7 eV 이상이어야 한다. 밴드갭이 이보다 작으면 전자-정공쌍이 갖는 에너지가 작아져 물분자를 분해할 수 없고 수소가 생성되지 않는다. 하지만 밴드갭이 너무 크면 자외선 영역의 빛밖에 사용할 수 없 게 되므로 광전극으로 사용할 물질의 밴드갭은 물을 분 해하기 위한 최소한의 에너지 레벨 이상이어야 하며 동 시에 가시광선 영역의 빛을 흡수할 수 있어야 한다. 이렇게 생성된 전자-정공쌍은 광전극과 전해질 계면으 로 이동하여 전자와 정공으로 분리되는데 이 과정에서 일 부는 이동하는 도중 재결합으로 인해 손실된다. 재결합 은 광전극에서 생성된 광전류를 100% 활용하지 못하게 되는 가장 큰 원인이다. 따라서 재결합을 줄이기 위해 광 생성 캐리어를 빠르게 전송하고 분리해야 한다. STH은 다음 수식 ⑴에 의해 정의된다.8) ηSTH = ⑴ 여기서 JSC는 short-circuit 광전류, ηF는 패러데이 효율, 1.23 V는 수소 생성 깁스 자유에너지, PSolar은 광원의 세 기이다. 2.2. GaN의 밴드갭 조절 GaN은 다양한 방법으로 밴드갭을 조절하는 것이 가능 하다. 도핑은 재료의 성능을 개선하기 위해 일반적으로 사용되는 방법 중 하나로 GaN의 밴드갭을 조절하여 가 시광선 영역의 태양광 스펙트럼을 이용할 수 있도록 한 다. Shu-Yen Liu 등은 양쪽 면이 광택처리 된 사파이어 기 판 위에 유기금속화학기상 에피택시를 통해 성장시킨 GaN 템플릿을 2개 준비하고 Mn이 도핑된 GaN 층(PEC-I)과 도핑되지 않은 GaN 층(PEC-II)을 각각 성장시켜 광 전류밀도를 비교하였는데 PEC-I의 광전류밀도는 PEC-II 에 비해 10배가량 더 높게 나타났다9). 두 PEC 셀의 응답
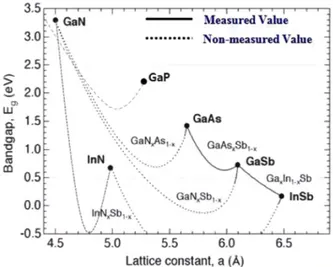
스펙트럼을 나타낸 Fig. 1(a)를 보면 PEC-II의 경우 GaN 의 밴드갭 에너지에 해당하는 365 nm 부근에서 응답이 차단되는 전형적인 특성을 보이지만 PEC-I은 UV 영역 흡수 외에도 380-600 nm사이에서 높은 응답을 보여주었 는데 이는 GaN의 밴드갭보다 낮은 에너지를 가진 파장 의 빛을 흡수하여 광전류를 생성했다는 것이다. Fig. 1(b) 에서 또한 어떠한 응답도 보이지 않은 PEC-II에 반해 PEC-I은 가시광선 범위인 400 nm<λ<600 nm에서 상당한 반응을 보여 Mn 도핑을 통해 GaN가 흡수할 수 있는 태 양 스펙트럼 영역을 늘릴 수 있음을 알 수 있다. Mg, Zn 등의 금속을 GaN에 도핑하여 광촉매 활성을 비교한 연구도 보고되었다. N Arai, N Saito 등의 연구에 서 도핑되지 않은 GaN의 경우 아주 소량의 수소를 생산 하는데 그쳤지만 Mg, Zn, Be가 도핑된 GaN은 더 많은 H2 와 O2를 생성하며 매우 안정적인 광촉매 활성을 나타냈 다10). GaN의 밴드갭을 조정하는 방법에는 도핑 이외에도 밴 드갭이 낮은 이원계 반도체와 GaN의 합금을 형성하는 방 법이 있다. Fig. 2에서 볼 수 있듯이, GaN보다 낮은 밴드 갭을 갖는 이원계 반도체는 GaP, GaAs, GaSb, InSb 등이 있지만 그 중에서도 InN은 밴드갭이 0.7 eV 정도로 매우 낮아 GaN과 합금을 형성하는데 가장 많이 사용되는 물 질이다.
K Aryal, HX Jiang 등은 p-InGaN 광전극을 이용하여 In
함량에 따른 PEC 물분해 효율을 비교 분석하였다11). 작
JSC[mA cm⁄ 2] 1.23 V× [ ]×ηF
PSolar[mW cm⁄ 2]
---Fig. 1. Typical spectral responses of PEC-I and PEC-II (a) without a 400 nm long-pass filter and (b) with a 400 nm long-pass filter. Reproduced from Ref. 9.
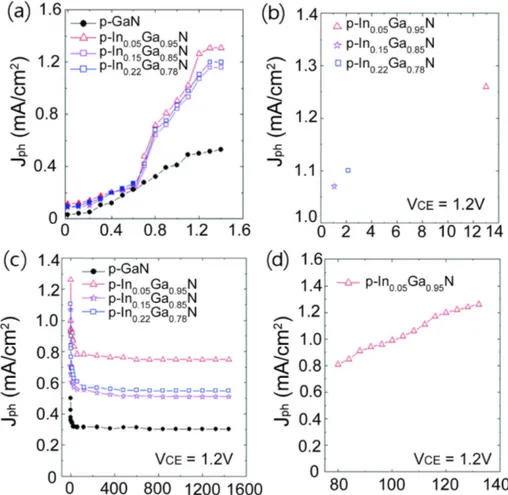
동 전극(p-InχGa1-χN)과 상대전극(Pt), 기준전극(Ag/AgCl/ NaCl)로 PEC 셀을 구성하였으며 전해질로는 1 M의 HBr 용액을 사용하였고 광원은 표준 AM 1.5 태양광 시뮬레 이터를 이용하였다. Fig. 3(a)는 빛을 조사했을 때의 전류 밀도를 나타낸 것이다. 측정 초반에는 광전류밀도에 거 의 차이가 없었지만 전압이 0.6 V를 넘어가면서부터 전 압이 높아질수록 점점 격차가 벌어졌다. 특히 1.2-1.4 V 에서 p-In0.05Ga0.95N 광전극의 광전류밀도가 약 1.3 mA/ cm2로 같은 조건에서 p-GaN 광전극의 0.5 mA/cm2보다 2 배 이상 증가한 것을 알 수 있다. Fig. 3(b)는 광전류밀도 를 p-InχGa1-χN 전극의 전공 이동도에 따라 나타낸 것이 다. 광전류밀도가 정공 이동도에 따라 거의 선형적으로 증가하는 것을 볼 수 있는데 이는 광생성 캐리어가 더 빨리 이동할수록 광전류 값이 커진다는 것을 의미한다. Fig. 3(c)는 전해질 내에서 p-InχGa1-χN 전극의 안정성을 평가하기 위한 것으로 광전류밀도의 변화를 24시간 동 안 측정한 것이다. 광전류밀도는 측정 시작 후 얼마 지 나지 않아 급격하게 떨어졌다가 약 10분 후부터는 매우 안정적으로 유지되었다. Fig. 3(d)는 빛의 세기에 따른 In0.05Ga0.95N 전극의 광전류밀도를 나타냈는데 빛의 세기 가 증가할수록 광전류밀도 또한 증가하는 것을 볼 수 있 다. 이는 빛의 세기가 증가하면 더 많은 전자-정공쌍이 생 성되기 때문이다. 이처럼 InGaN은 GaN의 밴드갭을 조절하여 광흡수효 율을 향상시키고 전해질 내에서도 매우 안정하지만 사파 이어나 실리콘 기판과의 격자 불일치(lattice mismatch)로 인해 In의 함량이 큰 경우에는 두꺼운 InGaN 층을 성장 하면 threading dislocation 등의 결함이 생기고 급격한 효 율 저하가 발생한다.12-14) 이런 결함들은 재결합 site로 작 용하여 광생성 캐리어가 전극으로 이동하여 물의 산화· 환원 반응에 참여하는 것을 방해하기 때문에 물분해 효 율을 떨어뜨린다. 따라서 InGaN 광전극의 효율을 높이기 위해서는 In 조성이 큰 박막을 성장시킬 때 결함을 최소 화하는 방법의 개발이 필요하다. 이에 대한 연구의 일환 으로 안소연, 라용호 교수 팀은 Mg가 도핑된 p-GaN 나 노와이어 위에 p-InGaN 나노와이어를 증착하는 2단계 나 노구조를 도입하여 발광 파장 특성을 조사하였다.14)
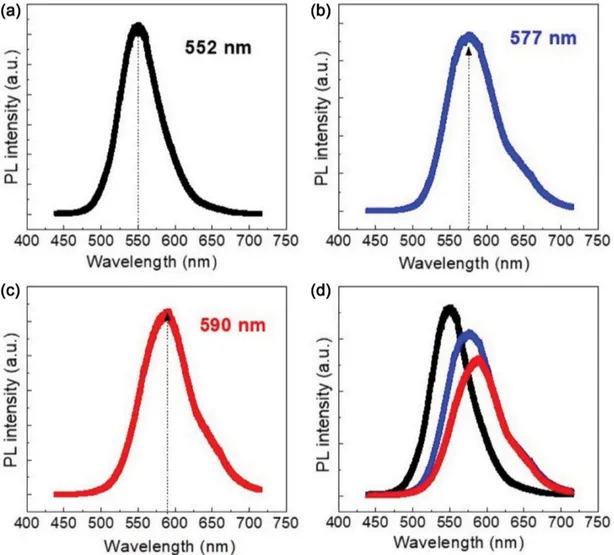
샘플 A는 p-InGaN 나노와이어, 샘플 B는 샘플 A보다 In 조성을 증가시킨 p-InGaN 나노와이어 광전극이다. 샘 플 C는 p-GaN 나노와이어 위에 p-InGaN 나노와이어를 성장시킨 것이다. Fig. 4(a)는 샘플 A, Fig. 4(b)는 샘플 B 의 Photoluminescence (PL) 측정 결과로 In의 조성이 증가
Fig. 3. (a) Photocurrent densities (Jph) as a function of VCE, (b) Jph as a function of hole mobility of p-InxGa1−xN electrodes at VCE=1.2 V,
(c) Jph of p-InxGa1−xN electrodes at VCE=1.2 V as a function of the measurement time (t), (d) Jph of p-In0.05Ga0.95N as a function
함에 따라 발광 파장이 552 nm에서 577 nm로 증가하였 음을 알 수 있다. Fig. 4(c)는 샘플 C의 발광 파장 스펙트 럼으로 약 590 nm의 발광 파장을 보이는데 이는 앞의 두 샘플보다 더 높은 In 함량을 가졌다는 것을 나타낸다. Fig. 4(d)는 세 샘플의 PL 분석 결과를 비교한 것으로 In의 조 성이 증가할수록 발광 강도가 낮아지는 것을 볼 수 있는 데 이는 In의 조성이 증가하면서 결정질이 저하되었기 때 문이다. 위의 결과를 기반으로 기판의 온도를 줄이고 p-GaN과 p-InGaN의 성장 시간을 조절하여 기존보다 더 길이가 긴 p-InGaN/p-GaN 나노와이어를 성장시켰다. 그 결과 기존 에 비해 약 2배 이상 광특성이 향상되었는데 이는 나노 와이어의 길이가 길어짐에 따라 결함 발생률이 감소하여 결정성이 향상된 결과이다. 2.3. 나노구조 도입 광전극에 나노구조를 도입하여 물분해 효율을 높이는 방법은 주로 산화물 광전극에서 주로 이루어졌으나 최근 에는 GaN 광전극에도 나노구조를 도입하여 수소 생성 효 율을 높이고자 하는 연구가 많이 진행되고 있다. 나노와 이어나 나노튜브 같은 나노구조에서는 전극 표면에서 빛 의 산란을 일으켜 빛의 흡수를 증가시키고 광생성 캐리 어가 반도체와 전해질 계면으로 이동하는 거리가 줄어들 기 때문에 전자와 정공의 재결합이 줄어들고 전하 분리 효율이 향상된다.14-16)
Junjie Kang, Zhiqiang Liu 팀은 나노-임프린트 리소그 래피와 2차 스퍼터링 공정을 통한 InGaN/GaN 나노튜브
기반 광전극을 제작하고 PEC 특성을 평가하였다.15)
먼저 세 개의 c-평면(0001) 패턴 사파이어(Al2O3) 기판
에 금속 유기 화학 기상 증착(Metal-organic chemical vapor deposition; MOCVD)법을 이용하여 InGaN/GaN 박막을 성 장시키고 그 중 2개에 각각 600 nm와 900 nm의 깊이를 가진 InGaN/GaN 나노튜브를 제작하였다. 600 nm의 나노튜브를 성장시킨 경우와 900 nm의 나노 튜브를 성장시킨 경우 모두 나노튜브없이 InGaN/GaN 박 막 만을 성장시킨 전극보다 높은 광전류밀도가 측정되었 다. 특히 600 nm의 나노튜브를 성장시킨 샘플의 경우 나 노튜브가 없는 전극과 대조하여 0.004 mA/cm2에서 0.068 mA/cm2로 15배 가까이 증가했다. 이는 InGaN/GaN 나노 튜브의 광 분산 효과에서 기인한 것으로 광전극과 전해
Fig. 4. (a), (b), (c) Photoluminescence (PL) spectrum of p-InGaN nanowires grown under different conditions, (d) Comparison of PL of three p-InGaN nanowires. Reproduced from Ref. 14.
질의 접촉면적이 넓어져 광자 대 전류 효율이 증가했기 때문이다. 또 모든 광전극이 지속적으로 빛에 노출된 상 황에서도 긴 시간동안 좋은 안정성을 보였다.
J. Benton, T. Wang 등의 연구에서도 평면형 GaN 광전 극과 높이 700 nm, 직경 220 nm의 GaN 나노로드 기반 광전극을 제작하여 0.5 M HCl 전해질 내에서 광전류밀 도를 측정하였다16). 평면 구조 GaN 광전극과 비교하여 GaN 나노로드 광전극은 4배가량 표면적이 증가하였다. 따라서 광흡수효율이 크게 향상되어 광전극과 전해질의 계면에서 더 많은 캐리어가 생성되고, 캐리어의 이동 거 리가 줄어들기 때문에 전자와 정공의 재결합 확률이 줄 어들어 더 많은 캐리어들이 물분해에 참여할 수 있게 된 다. 그 결과로 GaN 나노로드 광전극이 평면 GaN 광전극 에 비해 최대 5배 높은 광전류밀도를 보였다. 같은 나노구조 전극이라도 기판의 종류에 따라 그 성 능이 달라질 수 있다는 보고도 존재한다. Loganathan Ravi 등은 사파이어(Al2O3)(002)와 실리콘(Si)(111) 기판 위에 GaN 나노와이어를 성장시키고 광전류밀도를 측정하였 다.17) 그 결과 GaN/Al 2O3 나노와이어보다 GaN/Si 나노와 이어에서 광 전류 밀도가 0.15 mA/cm2으로 더 높게 측정 되었다. 또한 Si 기판 위에 성장된 GaN 나노와이어의 경 우, 가시광선 영역에서 수소 발생 효율이 크게 향상되었 다. 이는 광생성 전자와 정공이 GaN/Si 광전극에서 더 효 율적으로 분리되어 물분해에 참여하기 때문이다.
2.4. co-catalyst 및 protection layer 도입
앞에서 언급한 밴드갭 엔지니어링과 나노구조 형성은 전하 분리 및 전하 이동 촉진으로 인하여 물분해의 효율 을 향상시키는데 효과적이다. 하지만 여전히 광부식으 로 인한 효율 저하 및 낮은 수소 산소 반응으로 인한 효 율 한계가 존재한다. 이를 해결할 수 있는 방법으로 co-catalyst 혹은 protection layer를 광전극과 결합시키는 방 법이 있다. 광생성 전자와 캐리어는 반도체 광전극 표면 에서 흡착되어 물 분자를 산화·환원시키는데 반도체 광 전극 표면에 금속 또는 산화금속 등의 co-catalyst를 증착 하면 광생성 정공과 전자의 표면흡착을 증가시켜 전자와 정공의 재결합률을 줄이고 물을 산화·환원시키는데 필요 한 에너지를 감소시켜 물분해 효율이 증가한다.18,19)
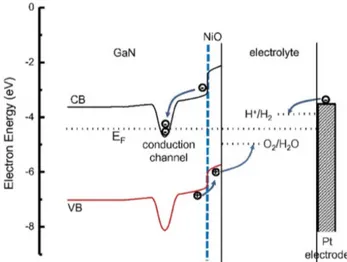
강진호, 류상완 교수 팀은 GaN 광전극 표면에 NiO co-catalyst를 결합시킨 여러 개의 샘플을 제작하여 광전류밀 도를 측정하였다.18) NiO co-catalyst는 GaN 전극에서 생
성된 정공을 빠르게 포착하여 광전류밀도를 증가시키고 광전극-전해질 계면의 정공 밀집을 줄여 전극의 부식을 억제하였다. 6시간 동안 NiO 코팅된 광전극을 작동시킨 결과 광전류밀도의 감소가 23%에 불과하였는데, 이는 NiO가 코팅되지 않은 광전극의 경우에 광전류밀도 70% 가 감소한 것에 비하면 안정성이 크게 향상된 결과이다. 이처럼 NiO 코팅으로 전자와 정공의 재결합을 방지하여 광전류밀도를 증가시키고 광전극의 안정성을 크게 향상 시킨 결과 기준보다 약 3.5배 높은 물분해 효율을 얻었다. 또한 최근 크게 주목받은 촉매로 Co-Pi가 있다. Jumpei Kamimura, Lutz Geelhaar 팀은 도핑되지 않은 GaN 템플 릿 위에 약 18 nm 두께로 Co-Pi를 증착하고 Co-Pi를 증 착하지 않은 GaN 템플릿과 함께 광전류밀도를 측정하였 다20). Co-Pi이 증착된 경우 표면에서의 정공-전자쌍의 재 결합이 억제되고 특히 낮은 전압에서 광전류가 증가하였 다. 그러나 안정성 테스트에서는 Co-Pi를 증착한 경우와 그렇지 않은 경우에 큰 차이는 보이지 않았다. 이는 Co-Pi가 다공성 구조를 가지기 대문에 GaN 표면이 전해질에 노출되는 것이 원인으로 보인다. 위의 결과에서 광부식을 억제하기 위해서는 전해질로 부터 GaN 표면을 보호해야 한다는 것을 알 수 있다. 본 연구그룹에서는 산화 알루미늄(Al2O3) 박막을 광전극의 표면 보호층으로 사용하여 GaN 광전극의 안정성을 테스 트하였다.21) 먼저 3개의 c면 사파이어 기판 위에 도핑되지 않은 GaN 을 2 µm 두께로 성장시키고 그 중 2개에 Atomic layer deposition (ALD)를 사용하여 Al2O3을 각각 1 nm와 2 nm 로 코팅하였다. 이후 샘플의 안정성을 측정하기 위해 외 부 전압이 없는 상태에서 240분 동안 광전류밀도의 변화 를 측정하였다. 초기 광전류밀도의 값은 Al2O3가 코팅되 지 않은 GaN(샘플 A), Al2O3가 1 nm로 코팅된 전극(샘플 B), Al2O3가 2 nm로 코팅된 전극(샘플 C) 순서로 각각 0.49
mA/cm2, 0.408 mA/cm2, 0.415 mA/cm2이었다. 약 30분 후, 샘플 A에서 빠른 속도로 광전류밀도의 감소가 관찰되었 으나 Al2O3가 코팅된 샘플 B와 샘플 C의 경우에는 240분 동안 거의 일정한 광전류밀도를 나타냈다. 이는 Al2O3가 GaN 표면의 광부식을 방지하기 때문이며 이는 GaN 표 면에 Al2O3 박막을 형성함으로써 GaN 광전극의 화학적 안정성을 향상시킬 수 있음을 나타낸다. 하지만 여전히 낮은 효율과 장기간 안정성 측면에서 여전히 상용화되기
Fig. 5. Schematic band diagram of unu-GaN coated with NiO cocatalyst. The Fermi level (EF) and redox potentials for water splitting are displayed for comparison. Reproduced from Ref. 18.
에는 어렵다는 한계점을 보인다. 이러한 점은 낮은 밴드 갭을 가지는 물질을 이용한 Tandem 구조를 도입하거나 태양전지 소재를 이용함으로써 해결해야할 추가적인 과 제이다.
3. 결
론
PEC 물분해는 무한히 제공되는 태양에너지와 지구에 서 가장 풍부한 물질인 물로부터 연료를 얻는 친환경적 이고 미래지향적인 에너지 기술이다. PEC 물분해의 원리는 간단하지만 상용화 단계에 이르 기에는 아직 해결해야 할 문제들이 많이 존재한다. 앞에 서 알아본 GaN 광전극의 연구 동향으로 볼 때, GaN의 밴 드갭을 조절하여 가시광선 영역의 광흡수율을 향상시키 고, 나노구조의 도입과 co-catalyst의 활용으로 전자와 정 공의 재결합률을 줄이고 높은 신뢰성과 안정성이 확보된 광전극을 얻는 등 셀 구동에 핵심인 전극 제조 기술이 많 이 연구되어 왔으며 기술 수준도 어느정도 확보된 것으 로 보인다. 물론 여전히 다른 반도체 물질에 비하여 낮은 효율 등 문제점들이 존재하긴 하지만 이를 해결하기 위 한 연구가 여러 분야에서 이루어지고 있고 신뢰성 부분 에서 GaN 재료 자체가 가진 강점이 큰 만큼 PEC 물분해 연구에 있어 GaN 광전극의 활용이 기대된다. 이러한 기 술을 바탕으로 향후 tandem 셀 제조기술, 셀의 scale up 등의 연구를 통해 고성능화와 상용화를 위한 실용성을 갖 춘다면 원천기술로서 선진국 수준의 기술 확보에 도움이 될 것으로 기대된다.감사의 글
이 논문은 한국산업기술진흥원의 국제공동기술개발 사업 (P0006851) 과제와 한국 기초과학지원연구원 국 가연구시설 장비 진흥센터의 지원을 받은 기초과학 연 구역량강화사업 핵심연구지원센터 조성지원 과제에서 에너지 융복합 전문핵심 연구지원센터를 조성하여 (2019R1A6C1010024) 수행된 연구임.References
1. N. Abas, A. Kalair, and N. Khan, “Review of fossil fuels and future energy technologies”, Futures, 69, 31 (2015). 2. J. Hansen, R. Ruedy, M. Sato, and K. Lo, “Global surface
temperature change”, Rev. Geophys., 48, RG4004 (2010). 3. M. E. Mann, Z. Zhang, M. K. Hughes, R. S. Bradley, S. K.
Miller, S. Rutherford, and F. Ni, “Proxy-based reconstructions of hemispheric and global surface temperature variations over the past two millennia”, PNAS, 105(36), 13252 (2008). 4. A. Fujishima, K. Honda, “Electrochemical photolysis of water
at a semiconductor electrode”, Nature, 238(5358), 37 (1972). 5. S. S. Kocha, M. W. Peterson, D. J. Arent, J. M. Redwing, M. A. Tischler, and J. A. Turner, “Electrochemical investigation
of the gallium nitride-aqueous electrolyte interface”, J. Elec-trochem. Soc., 142(12), L238 (1995).
6. T. Hisatomi, J. Kubota, and K. Domen, “Recent advances in semiconductors for photocatalytic and photoelectrochemical water splitting”, Chem. Soc. Rev., 43(22), 7520 (2014). 7. H. j. Choi, S. H. Seo, and S. H. Lee, “Recent Research Trend
in Organometal Halide Perovskite-Based Photoelectrodes for Efficient Solar Hydrogen Production (in Kor.)”. Korean Ind. Chem. News, 24(1), 14 (2021).
8. B.K. Min, “Hydrogen Production by Photoelectrochemical Cells (in Kor.)”, Polymer Science and Technology, 19(3), 228 (2008).
9. S. Y. Liu, J. K. Sheu, Y. C. Lin, S. J. Tu, F. W. Huang, M. L. Lee, and W. C. Lai, “Mn-doped GaN as photoelectrodes for the photoelectrolysis of water under visible light”, Opt. Express, 20(S5), A678 (2012).
10. N. Arai, N. Saito, H. Nishiyama, K. Domen, H. Kobayashi, K. Sato, and Y. Inoue, “Effects of divalent metal ion (Mg2+, Zn2+ and Be2+) doping on photocatalytic activity of ruthenium oxide-loaded gallium nitride for water splitting”, Catalysis Today, 129(3-4), 407 (2007).
11. K. Aryal, B. N. Pantha, J. Li, J. Y. Lin, and H. X. Jiang, “Hydrogen generation by solar water splitting using p-InGaN photoelectrochemical cells”, Appl. Phys. Lett., 96(5), 052110 (2010).
12. M. Shimizu, Y. Kawaguchi, K. Hiramatsu, and N. Sawaki, “Metalorganic vapor phase epitaxy of thick InGaN on sap-phire substrate”, Jpn. J. Appl. Phys., 36(6R), 3381 (1997). 13. G. B. Stringfellow, “Microstructures produced during the
epi-taxial growth of InGaN alloys”, Journal of Crystal Growth, 312(6), 735 (2010).
14. S. An, D. W. Jeon, J. Hwang, and Y. H. Ra, “High aspect-ratio InGaN nanowire photocatalyst grown by molecular beam epitaxy (in Kor.)”, Journal of the Korean Crystal Growth and Crystal Technology, 29(4), 143 (2019). 15. J. Kang, H. J. Choi, F. Ren, J. Ao, H. Li, Y. Li, & Liu, Z,
“Fabrication of an InGaN/GaN nanotube-based photoanode using nano-imprint lithography and a secondary sputtering process for water splitting”, Jpn. J. Appl. Phys., 58(8), 081001 (2019).
16. J. Benton, J. Bai, and T. Wang, “Enhancement in solar hydro-gen hydro-generation efficiency using a GaN-based nanorod struc-ture”, Appl. Phys. Lett., 102(17), 173905 (2013).
17. L. Ravi, K. Boopathi, P. Panigrahi, and B. Krishnan, “Growth of gallium nitride nanowires on sapphire and silicon by chem-ical vapor deposition for water splitting applications”, Applied Surface Science, 449, 213 (2018).
18. J. H. Kang, S. H. Kim, M. Ebaid, J. K. Lee, and S. W. Ryu, “Efficient photoelectrochemical water splitting by a doping-controlled GaN photoanode coated with NiO cocatalyst”, Acta materialia, 79, 188 (2014).
19. S. H. Kim, M. Ebaid, J. H. Kang, and S. W. Ryu, “Improved efficiency and stability of GaN photoanode in photoelectro-chemical water splitting by NiO cocatalyst”, Applied surface science, 305, 638 (2014).
20. J. Kamimura, P. Bogdanoff, F. F. Abdi, J. Lahnemann, R. van de Krol, H. Riechert, and L. Geelhaar, “Photoelectrochemical properties of GaN photoanodes with cobalt phosphate catalyst for solar water splitting in neutral electrolyte”, J. Phys. Chem. C, 121(23), 12540 (2017).
21. H. Kim, H. Bae, S. W. Bang, S. Kim, S. H. Lee, S. W. Ryu, and J. S. Ha, “Enhanced photoelectrochemical stability of GaN photoelectrodes by Al2O3 surface passivation layer”, Opt. Express, 27(4), A206 (2019).
• 허지원 • 전남대학교 신화학소재공학과 • 전자재료 • E-mail: [email protected] • 배효정 • 전남대학교 광전자융합기술연구소 • 전자재료 • E-mail: [email protected] • 하준석 • 전남대학교 화학공학부 • Compound Semiconductors /패키징, 화공소재 • E-mail: [email protected]