= 증례보고 =
근육-눈-뇌병 1예
이은지1⋅김재형2⋅황정민1
서울대학교 의과대학 안과학교실 분당서울대학교병원 안과1, 서울대학교 의과대학 영상의학교실 분당서울대학교병원 영상의학과2
목적: 근육-눈-뇌(Muscle-eye-brain)병의 증례를 국내에서 처음으로 보고하고자 한다.
증례요약: 35개월 여아가 내사시와 눈떨림을 주소로 내원하였다. 환아는 3.45 kg, 39주로 태어났고, 성장발달지연과 발달성고관절탈 구의 병력이 있었다. 환아의 부모는 이상이 없으나, 언니가 발달지연이 있었다. 혈액검사에서 creatinine phosphokinase와 lactate dehydrogenase가 높았다. 조절마비굴절검사에서 양안의 심한 근시난시가 있었다. 눈떨림이 관찰되었고, 근거리에서 교대프리즘가림 검사로 20프리즘디옵터의 내사시가 있었다. 세극등 검사에서 하안검의 부안검과 경도의 후낭하백내장, 안저검사에서 양안 일차유리체 의 잔여줄기, 망막변성, 비정상적인 혈관가지를 동반한 시신경이형성을 보였다. 시유발전위도는 정상이었고, 망막전위도의 진폭은 현저 히 감소되었다. 뇌 자기공명영상에서 대뇌백질의 광범위한 T2신호 증가, 대뇌피질의 광범위한 경뇌회, 뇌교의 형성부전, 소뇌의 많은 낭종이 관찰되었다.
결론: 발달지연과 동반된 심한 근시, 백내장, 사시, 망막이상이 있을 때 전신질환의 동반 여부를 확인해야 할 것이며 근육-눈-뇌병의 진단에는 혈액검사와 뇌 자기공명촬영이 도움이 되었다.
<대한안과학회지 2009;50(2):318-323>
■ 접 수 일: 2007년 10월 22일 ■ 심사통과일: 2008년 9월 11일
■ 통 신 저 자: 황 정 민
경기도 성남시 분당구 구미동 300 분당서울대학교병원 안과
Tel: 031-787-7372, Fax: 031-787-4057 E-mail: hjm@snu.ac.kr
* 본 연구는 한국과학재단 특정기초연구(R01-2005-000-10875-0)의 지원을 일부 받았음.
근육-눈-뇌(Muscle-eye-brain)병은 선천성 근이영양증, 중 추신경계와 눈 이상이 특징인 상염색체 열성 유전질환 으로 출생시부터 저하된 근긴장도, 시력 저하, 심한 발달 지연과 지능저하를 보인다.1 1977년 Santavuori et al2의 보고 이후 핀란드를 중심으로 보고되며, 최근 관련된 유 전자(O-mannose beta-1, 2-N-acetylglucosaminyltransferase 1, POMGNT1)가 밝혀졌다.3,4 가장 많이 증례를 보고한 핀란 드에서도 그 발생률은 약 0.002% 정도로 매우 드물고,2,5,6 국내에서는 발표된 바 없다.
증례보고
35개월 여아가 눈떨림과 눈이 안으로 몰림을 주소로 내 원하였다. 환아는 성장발달지연으로 재활의학과에서 물리 치료를 받고 있으나 목을 가누고 혼자 뒤집는 정도가 가능 하고, 1시간 이상 앉거나 혼자 일어서지는 못하였다. 양측 의 발달성고관절탈구로 정형외과에서 3회 수술을 받았으나 수술 후에도 걷거나 서지는 못하였다.
산전진찰은 정상이었고, 태생 39주에 3.45 kg으로 제왕 절개로 분만하였다. 출생시 부모의 연령은 각각 39세, 37세 였다. 가족력상 부모는 근친관계는 아니었고, 특이병력 없 었으며, 9세 된 언니가 성장발달장애로 정신지체 1급이었다.
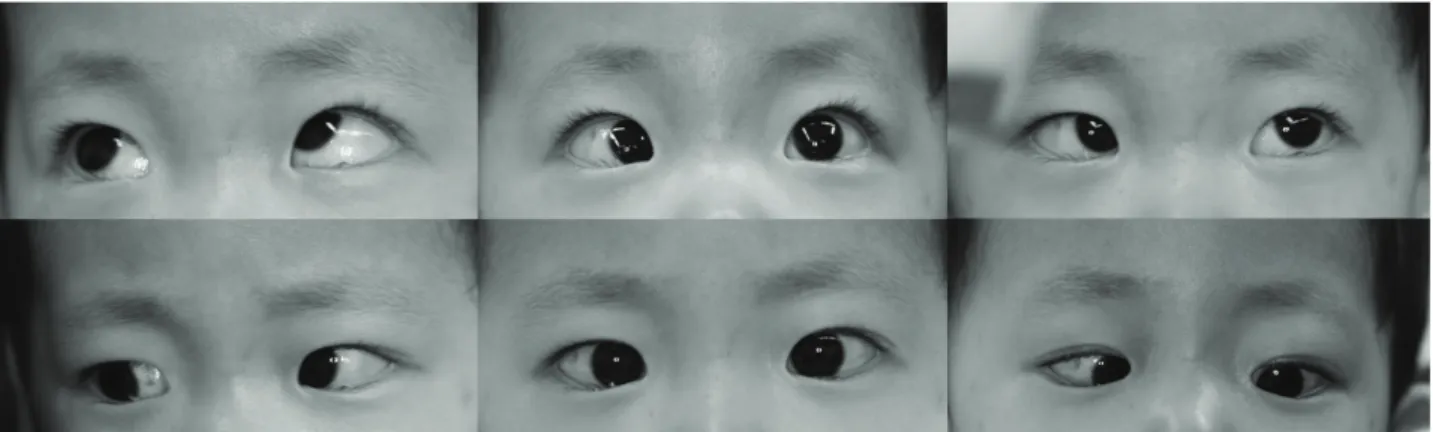
외관상 환아의 이마가 돌출되어 있었고, 측두부 앞뒤길 이가 짧아 전반적으로 앞뒤로 납작한 두상을 보였다. 안과 검사에서 양안 주시와 따라보기가 불량하였고, 눈떨림이 있 었으며, 근거리에서 교대프리즘가림검사로 20프리즘디옵 터의 내사시가 있었다(Fig. 1). TonoPen® XL (Medtronic Solan, Jacksonville, FL)으로 측정한 안압은 우안 평균 12 mmHg, 좌안 평균 11 mmHg였다. 전안부검사에서 양안 하 안검의 부안검과 경도의 후낭하백내장이 관찰되었으며, 조절 마비굴절검사에서 우안 -18.50 Dsph -2.50 Dcyl×180 A, 좌안 -19.50 Dsph-3.00 Dcyl×180 A의 심한 근시난시가 있었다. 안저검사에서 양안 일차유리체의 잔여줄기와 함께 전반적인 망막변성이 관찰되었다. 시신경은 비정상적인 혈 관가지를 동반한 이형성증을 보였다(Fig. 2). 표준망막전위 도에서 전체적인 기능저하를 보였으나(Fig. 3), 시유발전위 검사에서 p100 잠복기는 우안 91.0 ms, 좌안 93.5 ms, 진 폭은 우안 15.0 µV, 좌안 13.2 µV로 정상이었다(Fig. 4).
혈액검사에서 serum glutamic oxaloacetic transaminase가 48 U/L, serum glutamic pyruvate transaminase가 32 U/L 로 간수치가 경미하게 상승되었고, creatinine phosphokinase 가948 U/L, lactate dehydrogenase가 370 U/L로 근육효 소치가현격히 상승되었다.
Figure 1. Photographs showing esotropia and inferior oblique overaction in the left eye.
Figure 2.Fundus photograph showing diffuse retinal degeneration and optic disc dysplasia accompanied by abnormal vascular branching pattern.
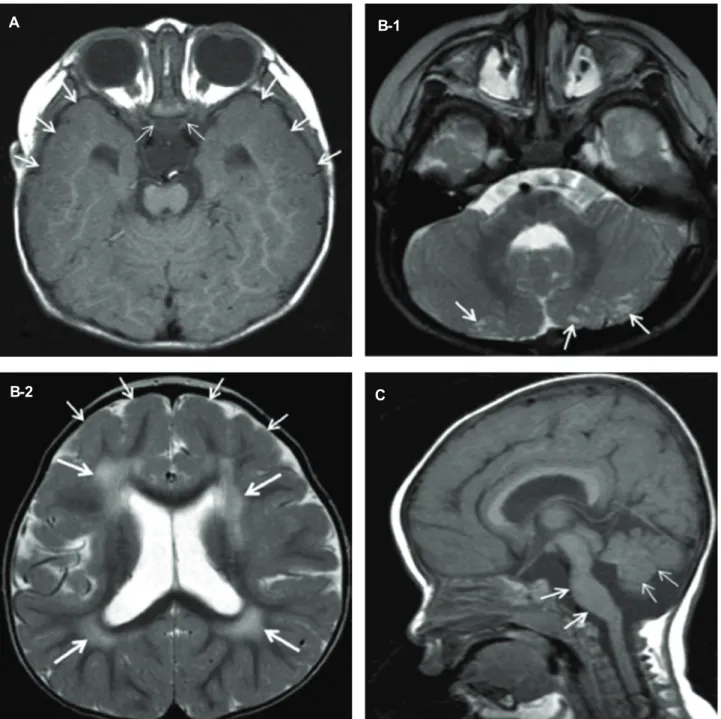
생후 19개월째 촬영하였던 뇌 자기공명영상에서 뇌실주 변백질의 광범위한 T2 고신호 병변, 전두엽과 측두엽의 광 범위한 경뇌회(pachygyria), 양측 시신경의 위축과 뇌교 및 소뇌 충부의 형성부전이 관찰되었으며, 소뇌에 많은 낭종이 관찰되었다(Fig. 5).
고 찰
선천성 근이영양증과 중추신경계의 신경원이행이상(migration disorder)을 동반하는 질환군으로 근육-눈-뇌(Muscle- eye-brain)병, Walker-Warburg syndrome, Fukuyama congenital muscular dystrophy가 있다.6이 질환군은 알파 -디스트로글리칸(alpha dystroglycan, α-DG)의 당화장애 로 인한 근이영양증이 공통적이다. α-DG는 디스트로핀 (dystrophin) 단백과 기저막에 간접적으로 결합함으로써 근원섬유의 세포골격의 결합을 이루도록 하는 고당화(high
glycosylated) 막단백질이며,7최근 연구에서는 이 단백의 당화 부족으로 인해 발생하는 이 질환군을 “dystroglycanopathy”라 통칭하였다.8,9
Walker-Warburg syndrome과 관련된 유전자는 O-manno- syltransferase 1, 2 (POMT1 and POMT2)10,11이고, 이는 근육-눈-뇌병과 신경병리학적으로는 유사하나 보다 심한 임상양상과 뇌자기공명영상 이상을 보인다.6 구순열 등의 얼굴기형을 비롯하여 눈 이상으로 소안구증, 전방유착, 백 내장, 망막기형, 시신경형성부전 등이 있다. 뇌 자기공명영 상에서 심한 뇌이랑없음증, 교뇌와 소뇌의 기형과 심한 백 질의 변성이 관찰되고, 후구가 낭성으로 확장되거나 뇌량이 관찰되지 않는 경우도 있다.1 예후가 불량하여 종종 시력 상실과 정신지능발달 지체를 동반하고, 생후 약 10개월에 사망한다.1
Fukuyama congenital muscular dystrophy와 관련된 유 전자는염색체 9q31~q33 위치에 있는 fukutin과 fukutin-
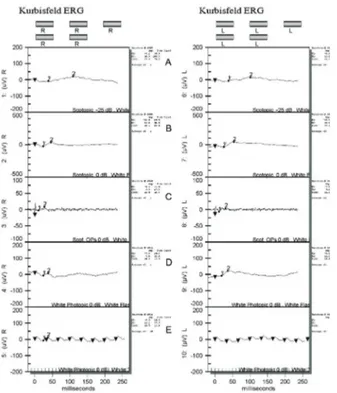
Figure 3. Standard electroretinogram at 35 months of age showing generalized decreased function of retinal ganglion cells in both eyes (A=rod response; B=
maximal combined response; C=oscillatory potentials;
D=cone response; E=30 Hz flicker).
Figure 4. Flash visual evoked potential at 35 months of age showing normal to decreased latencies and normal amplitudes in both eyes (A=right eye; B=left eye).
related protein (FKRP)13,14으로 알려져 있다. 일본에서 주 로 보고되고, 눈 이상이 매우 드물며 근시, 경도의 시신경창 백, 맥락망막변성 등이 알려져 있다.15 결국 이 질환군 내 감별진단은 분자유전검사가 도움이 되지만, 임상적으로는 눈 소견의 유무와 그 정도가 매우 중요하겠다.
이 환아는 특징적인 근육병 소견과 눈 소견, 그리고 뇌 자기공명영상을 바탕으로 근육-눈-뇌병으로 진단되었다.
근육-눈-뇌병에 이환된 환아는 영아기에는 주로 근육 긴 장도의 저하가 나타나고, 이후 점차 성장발달, 지능장애와 함께 근력이 점차 약화된다. 골격근 퇴행은 시간이 지나면 서 진행하여, 경우에 따라서는 호흡근 마비로 20세 이전에 사망하거나, 성인기까지 생존하더라도 심각한 기능적 장애 가 남는다. 혈청 근육효소수치 상승이나 침근전도 검사나 근생검에서 이상을 보일 수 있다.12 이 환아에서는 침근전 도검사나 근생검은 못했지만, 성장발달과 지능 장애, 근긴 장도 저하와 혈청 근육효소수치 상승 등 특징적인 근육병 의 소견을 보였다.
근육-눈-뇌병의 눈 이상은 양안의 진행성 고도근시, 시 신경위축, 망막변성 등이 주된 소견이며, 그 외 사시, 선천 녹내장, 선천백내장 등이 알려져 있다.1,6,12,17 망막전위도는 대개정상이지만, 시유발전위검사에서 50 µV 이상의 비정
상적으로 큰 파형과 잠복기 지연을 보일 수 있어 이를
“giant VEP(visual evoked potential)”라고 한다.1,16 이 증 례에서 현저히 감소된 망막전위도의 진폭은 전반적인 망막 기능 감소를 반영하겠다. 반면 시유발전위검사에서 p100 잠복기가 정상 또는 약간 단축되었고, 진폭은 정상범위였으 며, giant VEP는 관찰되지 않아 Fahnehjelm et al1의 증례 와 비슷하였다.
근육-눈-뇌병의 뇌 자기공명영상 소견은 전반적으로 피질이 비후되면서 조약돌 모양의 거친 표면과 얕은 고랑 을 동반한 경뇌회를 보이는 것이 전형적이고, T2 강조영상 에서 대뇌 백질이 고신호강도로 나타난다. 시신경 위축, 교 뇌와 충부 소뇌의 형성 부전, 다소뇌회 등도 동반될 수 있 다. 그 외 뇌실 확장, 소뇌의 다발성 낭종 등이 보이는데, 이 는 중추신경계 신경원이행이상을 증명하는 소견이다.1,6,12 이 환아의 전두엽과 측두엽의 경뇌회, 뇌실주위 백질의 T2 고신호 병변, 뇌교 및 소뇌 충부의 형성부전, 소뇌 내 작 은 낭종들과 양안 시신경형성부전 등은 모두 근육-눈- 뇌병에 부합되며, 일반적인 선천성 발달 장애 때 이 모든 소견이 함께 나타날 가능성은 매우 적다. 특히 pontine hypoplasia 와 multiple small cerebellar cysts 는 다른 종 류의 발달 장애(neuronal migration disorder, congenital leukodystrophy 등)에서는 관찰하기 힘든 소견으로 근육- 눈-뇌병, Fukuyama congenital muscular dystrophy 계열 의 질환을 강력히 시사한다.1,6,18-22
근육-눈-뇌병의 염색체 손상은 1p32-p34에 위치하는 22개의 엑손(exon)으로 이루어진 POMGNT1 유전자의 돌 연변이로 알려져 있다.3,4 POMGNT1 유전자의 점돌연변이 로 α-DG의 당화가 억제되어 골격근의 이영양이 생기고 근
A B-1
B-2 C
Figure 5. Brain MRI. (A) T1-weighted axial image. Thick cortices (arrows) are found in the anterior portion of the temporal lobes bilaterally, suggesting diffuse pachygyria. The optic nerves (thin arrows) are atrophic. (B) T2-weighted axial images. (B-1), Multiple small cysts (arrows) are found in the cerebellar hemispheres bilaterally. (B-2), Multiple patch T2 high signal lesions (thick arrows) are shown bilaterally in the periventricular white matter of the frontal and parietal lobes. Mild pachygria (arrows) are also noted in the frontal cortices bilaterally. (C) T1-weighted sagittal image. The pons is severely hypoplastic (arrows) with absence of normal anterior bulge. The inferior cerebellar vermis is also hypoplastic (thin arrows).
육-눈-뇌병에서 보이는 근육병의 임상양상을 나타난다.3,4 Michele et al23은 α-DG의 당화 부족이 laminin, argin, neurexin 등의 단백질의 리간드 결합능력의 저하와 관련있 으며, 이는 골격근 형성과 뇌의 신경이행 발달을 저해하여 근이영양증 뿐 아니라 뇌의 기형에도 영향을 끼칠 것이라
고 하였다. 최근 융모막융모생검(chorionic villi sampling) 과 연관분석을 통한 유전자검사로 태아에서 진단한 보고가 있어 추후 산전진단이 가능할 수 있을 것이다.17이 환아 보 호자는 유전자검사에 동의하지 않아 검사하지 못했지만, 특 징적인 MRI 소견과 눈 이상, 근이영양증과 그에 수반된
효소치의 변화로 근육-눈-뇌병을 확진할 수 있었다.
결론으로 발달지연과 심한 근시, 백내장, 사시, 망막이상 이 동반될 때 전신질환 여부를 확인해야 하며, 근육-눈-뇌 병의 진단에 혈액검사와 뇌 자기공명촬영이 도움이 되었다.
참고문헌
1) Fahnehjelm KT, Ygge J, Engman ML, et al. A child with Muscle-eye-brain disease. Ophthalmological and neurological characteristics. Acta Ophthalmol Scand 2001;79:72-5.
2) Santavuori P, Leisti J, Kruus S. Muscle, eye and brain disease:
a new syndrome. Neuropädiatrie 1977;8:553-8.
3) Cormand B, Avela K, Pihko H, et al. Assignment of the Muscle-eye-brain disease gene to 1p32-p34 by linkage analysis and homozygosity mapping. Am J Hum Genet 1999;64:
126-35.
4) Yoshida A, Kobayashi K, Manya H, et al. Muscular dystrophy and neuronal migration disorder caused by mutations in a glycosyltransferase, POMGNT1. Dev Cell 2001;1:717-24.
5) Diesen C, Saarinen A, Pihko H, et al. POMGnT1 mutation and phenotypic spectrum in Muscle-eye-brain disease. J Med Genet 2004;41:115.
6) Valanne L, Pihko H, Katevuo K, et al. MRI of the brain in Muscle-eye-brain disease. Neuroradiology 1994;36:473-6.
7) Henry MD, Campbell KP. Dystroglycan inside and out. Curr Opin Cell Biol 1999;11:602-7.
8) Michele DE, Campbell KP. Dystrophin-glycoprotein complex:
post-translational processing and dystroglycan function. J Biol Chem 2003;278:457-60.
9) Haliloglu G, Topaloglu H. Glycosylation defects in muscular dystrophies. Curr Opin Neurol 2004;17:521-7.
10) Beltran-Valero de Bernabe D, Currier S, Steinbrecher A, et al.
Mutations in the O-mannosyltransferase gene POMT1 give rise to the severe neuronal migration disorder Walker-Warburg syndrome. Am J Hum Genet 2002;71:1033-43.
11) Van Reeuwijk J, Janssen M, van den Elzen C, et al. POMT2
mutations cause alpha-dystroglycan hypoglycosylation and Walker-Warburg syndrome. J Med Genet 2005;71:907-12.
12) Yu HJ, Oh JY, Jung JH, et al. A case of Fukuyama type congenital muscular dystrophy. J Korean Assoc EMG- Electro- diagnostic Med 1999;1:226-9.
13) de Bernabe D, Van Bokhoven H, van Beusekom E, et al. A homozygous nonsense mutation in the fukutin gene causes a Walker-Warburg syndrome phenotype. J Med Genet 2003;40:
845-8.
14) Beltran-Valero de Bernabe D, Voit T, Longman C, et al.
Mutations in the FKRP gene can cause Muscle-eye-brain disease and Walker-Warburg syndrome. J Med Genet 2004;41:61.
15) Tsutsumi A, Uchida Y, Osawa M, Fukuyama Y. Ocular findings in Fukuyama type congenital muscular dystrophy.
Brain Dev 1989;11:413-9.
16) Pihko H, Lappi M, Raitta C, et al. Ocular findings in Muscle- eye-brain disease: a follow-up study. Brain Dev 1995;17:57-61.
17) Balci B, Morris-Rosendahl DJ, Celebi A, et al. Prenatal diagnosis of Muscle-eye-brain disease. Prenat Diagn 2007;27:51-4.
18) Widjaja E, Nilsson D, Blaser S, Raybaud C. White matter abnormalities in children with idiopathic developmental delay.
Acta Radiol 2008;49:589-95.
19) Ertl-Wagner B, Rummeny C, von Voss H, Reiser M. MR imaging in congenital disorders of the brain. Nervenarzt 2006;77:1521-35.
20) Schiffmann R, van der Knaap MS. The latest on leukody- strophies. Curr Opin Neurol 2004;17:187-92.
21) Lamer S, Carlier RY, Pinard JM, et al. Congenital muscular dystrophy: use of brain MR imaging findings to predict merosin deficiency. Radiology 1998;206:811-6.
22) Mackay MT, Kornberg AJ, Shield L, et al. Congenital muscular dystrophy, white-matter abnormalities, and neuronal migration disorders: the expanding concept. J Child Neurol 1998;13:
481-7.
23) Michele DE, Barresi R, Kanagawa M, et al. Post-translational disruption of dystroglycan-ligand interactions in congenital muscular dystrophies. Nature 2002;418:417-22.
=ABSTRACT=
A Child With Muscle-eye-brain Disease
Eunji Lee, MD1, Jae Hyoung Kim, MD2, Jeong-Min Hwang, MD1
Department of Ophthalmology, Seoul National University College of Medicine, Seoul National University Bundang Hospital1, Seongnam, Korea Department of Radiology, Seoul National University College of Medicine,
Seoul National University Bundang Hospital2 Seongnam, Korea
Purpose: To describe a child with muscle‐eye‐brain disease as the first case report in Korea.
Case Summary: A 35‐month‐old girl presented with esotropia and nystagmus since birth. She was born with a birth weight of 3.45 Kg at the gestational age of 39 weeks. She had a history of developmental delay and developmental dislocation of the hip.
Her elder sister also had generalized weakness and mental retardation. The patient’s creatinine kinase and lactate dehydrogenase serum levels were high. Cycloplegic refraction showed a significant myopic astigmatism in both eyes. She showed nystagmus and 20 prism diopters of esotropia in the primary position with the alternative prism cover test. Slit lamp examination revealed a mild posterior subcapsular cataract and lower lid epiblepharon in both eyes. Funduscopic examination showed diffuse retinal degeneration with remnant hyaloids membranes in both eyes. Both optic nerves were dysplastic with abnormal vascular branching pattern. Flash visual evoked potential was normal and standard electroretinography showed decreased amplitude in both eyes. Brain magnetic resonance imaging (MRI) revealed diffuse T2 high signal lesions of the cerebral white matter, diffuse pachygyria of the cerebral cortices, pontine hypoplasia, and multiple small cerebellar cysts.
Conclusions: When a child with developmental delay has ophthalmologic problems including severe myopia, cataract, strabismus and retinal degeneration, the systemic condition should be examined. In this case, in addition to the ophthalmologic findings, blood test and brain MRI were helpful for the diagnosis of muscle‐eye‐brain disease.
J Korean Ophthalmol Soc 2009;50(2):318-323
Key Words: Congenital muscular dystrophy, Muscle‐eye‐brain disease
Address reprint requests to Jeong-Min Hwang, MD
Department of Ophthalmology, Seoul National University Bundang Hospital
#300 Gumi‐dong, Bundang‐gu, Seongnam, Gyeonggi‐do 463‐707, Korea Tel: 82-31‐787‐7372, Fax: 82-31‐787‐4057, E-mail: hjm@snu.ac.kr