베타-사이클로 덱스트린 중합체/신남산 복합체의 제조 및 특성 연구
목은영⋅차현주⋅김진철†
강원대학교 의생명과학대학
(2012년 6월 29일 접수, 2012년 8월 3일 심사, 2012년 8월 16일 채택)
Preparation and Characterizations of Complex Composed of β-Cyclodextrin Polymer/Cinnamic Acid
Eun Young Mok, Hyun Ju Cha, and Jin-Chul Kim
†College of Biomedical Science and Institute of Bioscience and Biotechnology, Kangwon National University, Chunchon 200-701, Korea (Received June 29 , 2012; Revised August 3, 2012; Accepted August 16, 2012)
베타-사이클로덱스트린(β-cyclodextrin, β-CD) 중합체(polymer)는 가교제인 epichlorohydrin (EPI)과 β-CD의 몰 비가 10 : 1으로, 강한 염기조건에서 합성하였다. 합성한 β-CD 중합체 내의 β-CD contents는 52%였다. 광, pH반응성 복합체 를 제조하기 위해 신남산을 첨가하였고 첨가된 신남산은 소수성 상호작용에 의해 β-CD 공동에 포접되었다. 형성된 β-CD 중합체와 신남산 복합체를 투과전자현미경을 이용하여 관찰하였을 때 복합체의 형상을 관찰하였다. 광 조사에 따른 이량화도는 λ = 365 nm의 UV조사 시 증가하였으며 λ = 254 nm의 UV조사 시 감소하였다. 또한 동적 광 산란 (dynamic light scattering) 장치를 이용하여 측정한 복합체의 크기는 광 조사 유무에 따라 큰 변화가 측정 되지 않았고, pH 반응성을 관찰한 실험에서도 복합체의 크기와 제타 전위(zeta potential) 모두 pH에 따른 변화가 나타나지 않았다.
β-cyclodextrin (β-CD) polymers were prepared in a strong alkali condition solution (NaOH solution 30% (w/v)) using epi- chlorohydrin (EPI) as a cross-linker, and the molar ratio of EPI to β-CD was 10 : 1. The β-CD content in β-CD polymers is about 52%. In order to get the photo-responsible and pH-responsible, cinnamic acid was added to be inserted into the cav- ities of β-CD due to the hydrophobic interaction. The complex formation was confirmed using transmission electron microscope. The dimerization degree of complexes increased under UV irradiation at λ = 365 nm but decreased under the UV irradiation at λ = 254 nm. Dynamic light scattering analysis of particle sizes showed that the sizes of complexes did not change with different UV wavelength. Moreover, the complexes were pH-responsible because of the carboxyl group of cinnamic acid, but the size and zeta potential of the complex did not change in strong acid and alkali conditions.
Keywords: β-cyclodextrin, cinnamic acid, hydrophobic interaction, UV responsive
1. 서 론
1)
자극 반응성 복합체는 원하는 시간과 부위에서 주위 환경에 따라 능동적으로 약물을 방출을 할 수 있고 이러한 자극 반응성 복합체 중 pH 반응성 마이크로겔에 관한 연구가 가장 활발하게 이루어져 있다.
대부분의 pH반응성 복합체는 카복실기(-COOH)나 아미노기(-NH
2)와 같은 이온 그룹을 가지는 고분자를 이용해 제조한다[1,2]. 예를 들면, Poly( γ-glutamic)acid를 1,4-butanediol diglycidyl ether와 화학적으로 결합시켜 pH의 변화에 따라 팽윤도(swelling ratio) 양상이 변화하는 하이드로겔 복합체를 제조한 연구가 보고되어 있다[3].
자극 반응성을 부여하는 요인으로써 pH 외에도 광 조사에 반응하는
† Corresponding Author: Kangwon National Univesity
College of Biomedical Science And Institute of Bioscience and Biotechnology 192-1, Hyoja2-dong, Chunchon, Kangwon-do 200-701, Korea
Tel: 033-250-6561 e-mail: jinkim@kangwon.ac.kr
pISSN: 1225-0112 @ 2012 The Korean Society of Industrial and Engineering Chemistry.
All rights reserved.
복합체 또한 많은 연구가 되어있다. 광 반응성 복합체 중 광 반응성
마이크로겔은 주파수, 조사 시간, 광의 세기와 같은 조절 요인에 의해
빠르고, 효과적인 약물의 방출 조절이 가능하다[4,5]. 일반적으로 광
민감성을 나타내기 위한 photochromic group으로 azide groups, diazo
groups, cinnamate groups 등이 이용된다[6]. 이 중 cinnamate group을
가지는 신남산(cinnamic acid)은 천연에서 얻을 수 있는 물질로 카복
실기와 이중결합을 포함하고 있어 UV 조사 시, 이중결합의 첨가 환화
(cycloaddition) 에 의해 광 반응성을 관찰 할 수 있으며 카복실기에 의
해 pH반응성 또한 나타낼 수 있다[7]. 하지만 페닐기의 소수성에 의해
낮은 용해도를 나타내기 때문에 신남산 자체의 수용액상에서의 이용은
제한적이다. 본 연구에서 이용한 베타 사이클로덱스트린(beta-cyclo-
dextrin, β-CD) 중합체는 글루코스 분자가 연결된 환형 올리고당으로
그 외부 표면은 친수성이고 내부는 소수성인 공동이 원통형 구조를
가지고 있어 난용성 약물의 용해성 개선 및 흡수성의 개선 등 약물의
물리화학적인 성질을 개선시키는 것으로 알려져 있다[8]. 기존에 연구
된 β-CD와 신남산에 관한 연구에서는 자극반응성에 관한 연구가 충
분히 이루어지지 않았기 때문에 본 연구에서는 β-CD 중합체와 신남
121.14) 은 Sigma (St. Louis, MO, USA)로부터 구입하였다. Glycine (M.W. 75.37) 는 BIO BASIC INC. (markham, ON, CANADA)에서 구 입하였고, [2-(N-Morpholino)-ethanesulfonic Acid] (MES, M.W.2B.25) 는 BIO PURE (Cambridge, MA, USA)에서 구입하였다.
2.2. β-CD 중합체의 합성
5 g 의 β-CD 를 8 mL의 NaOH (30%, w/v)수용액에 넣고 하루 동안 실온에서 녹인다. 반응액을 30 ℃로 유지하고 400 rpm으로 교반 하면서 EPI 3.44 mL를 천천히 한 방울씩 떨어뜨린다. 겔이 되기 전에 20 mL의 아세톤을 넣고 5 h 지난 후 아세톤을 제거한다. 반응을 정지시키기 위해 6M HCl 을 소량 넣은 후 남은 아세톤을 제거하기 위해 3 h 동안 교반 한다. 반응액에 6 M HCl을 넣어주며 pH를 12로 조절한 후에 50 ℃ 진공 오븐에서 24 h 방치한다. 반응액을 상온에서 식힌 후 6 M HCl을 넣어 pH 6 ∼7로 맞춘다. 그 후에 dialysis membrane (MWCO 1000, Spectra/Por
Ⓡ Biotech Cellulose Ester (CE) membrane)을 이용해 48 h 동안 투석 하여 반응 부산물을 제거한다. 투석이 완료된 용액을 1 L의 아세톤에 넣어 침전 시킨 후 거름종이(Whatman, No. 2)를 이용하여 합성된 β-CD 중합체를 걸러낸 후 진공오븐에서 건조한다[11].
2.3. β-CD 중합체의 합성 확인
건조된 β-CD 중합체는 D
2O 에 용해시킨 후
13C NMR 을 이용하여 확인하였다.
13C NMR spectrum (Karlsruhe, Germany, in the Central Laboratory Center of Kangwon National University) 은 Bruker Advance 600spectrometer (600 MHz) 를 사용하여 측정하였다. β-CD 중합체 내의 β-CD 함유량은 페놀프탈레인(phenolphthalein)을 이용한 발색법 (colorimetry) 으로 측정 하였으며 측정 결과 52% (w/w)의 β-CD이 함 유되어 있음을 확인 하였다[12].
2.4 β-CD의 농도에 따른 신남산의 용해도 측정
β-CD 수용액에서 신남산의 용해도는 β-CD 중합체에 포함되는 신남산의 최대 농도에 의해 결정된다. β-CD 중합체가 신남산의 포화도 에 영향을 미치는지 알아보기 위해 단량체(monomer)인 HP-β-CD와 비교하였다. 3 mL의 MES buffer (2-morpholinoethanesulfonic acid, pH 5.0, 30 mM) 에 β-CD와 HP-CD를 동일한 농도(0, 0.0084, 0.0169, 0.0338, 0.0675, 0.135 M) 가 되도록 용해시킨 후, 신남산 0.2 g을 첨가하였다.
24 h 동안 roller mixer에서 회전 시킨 후, 반응액을 syringe filter (pore size 0.45 µm)를 이용하여 필터 한다. 필터한 용액을 동일한 buffer로 1000 배 희석시켜 UV/vis spectrometer (6505 UV/Vis. Spectrophotometer, JENWAY, U.K.) 를 이용해 273 nm에서 흡광도를 측정하였다.
2.5. β-CD 중합체-신남산 복합체의 제조
합성된 β-CD 중합체에 신남산을 포접시키기 위하여 MES버퍼 3 mL
의 파장에서 흡광도를 측정한다. 그 후 같은 용액에 10 min간 λ = 254 nm의 UV (6 W)를 조사 하여 전과 같은 조건에서 흡광도를 측정한다. 같은 과정을 5회 반복하여 파장의 변화에 따른 신남산의 이 량화도를 측정한다[13].
2.7. β-CD 중합체/신남산 복합체의 형상관찰 및 광, pH반응성 관찰 β-CD 중합체와 신남산의 상호작용에 의한 복합체의 형상 관찰을 위하여 투과전자현미경(JEM-2010, JEOL Ltd., Japan, in the Central Laboratory of Kangwon National University) 을 이용하였고, 동적 광산란 (dynamic light scattering, DLS) 측정 장치(Plus 90, Brookhaven, USA) 를 이용하여 UV 조사 유무, 용액의 농도변화에 따른 크기 변화를 측정 하였으며, 제타 전위(zeta potential) 측정 장치(ZetaPlus 90, Brookhaven Instrument Co., USA ) 를 이용해 pH에 따른 제타 전위의 경향성을 살 펴보았다.
β-CD 중합체와 신남산 복합체의 pH에 의한 영향을 보기 위하여 pH별 DLS샘플을 준비하였다. DLS샘플은 pH 3.0 (glycine, 30 mM), pH 5.0 (MES, 30 mM), pH 7.0 (trizma base, 30 mM), pH 9.0 (trizma base, 30 mM) 버퍼 용액 3 mL에 과량의 신남산을 첨가해 24 h 동안 roller mixer 에 회전 시켜 버퍼 용액에 용해되는 신남산의 영향을 배제 시키기 위해 pH별 신남산 포화용액을 제조 한다. 각 pH별 신남산 포 화용액 5 mL에 0.6 g의 β-CD 중합체를 첨가한 후 신남산의 포화용 해도의 80% (w/w)에 해당하는 신남산을 넣어주고 pH를 측정하여 각 pH별 복합체 용액을 제조하였다. 제조한 용액을 각 pH별 버퍼를 이용 하여 30, 10, 3.3, 1.1%로 희석시키며 크기와 제타 전위를 측정하였다.
투과전자현미경(transmission electron microscope, TEM, JEOL-JEM- 2010, JEOL Ltd., Japan) 시료는 Phosphotungstic acid (PTA)용액으로 염색한 UV조사 전/후의 30% β-CD/신남산 복합체 용액을 구리 격자에 한 방울 떨어뜨려 상온에서 24 h 건조 시켜 제조 되었고, TEM이미지 분석을 통해 형태를 관찰하였다.
3. 결과 및 고찰
3.1. β-CD수용액에서 신남산의 용해도
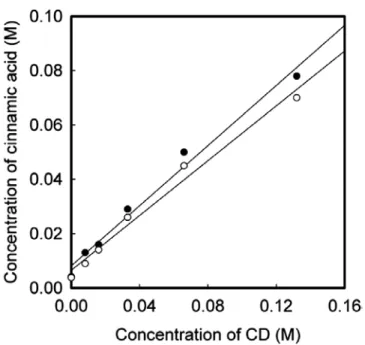
Figure 1 은 수용액상에서 β-CD의 농도에 따른 신남산의 용해도이다.
β-CD가 가용화제로 작용하여 β-CD가 존재하지 않는 신남산보다
용해도가 증가하였다. 또한, 신남산의 용해도 곡선 식은 단량체
(monomer)인 HP-β-CD을 사용하였을 때 Y = 0.5049X + 0.0065
(R
2= 0.9828), β-CD 중합체를 사용하였을 때 Y = 0.5532X + 0.0082
(R
2= 0.9838) 였다. 용해도가 낮은 나프탈렌 아세트산(Naphthalene
acetic acid), 쿠마린(coumarin), 페닐알라닌(L-phenylalanine) 등과 같은
물질이 β-CD 와의 소수성 상호작용에 의해 용해도가 증가한 이전의
연구결과를 바탕으로 하여 신남산의 페닐기(phenyl group)가 β-CD의
Figure 1. Effect of β-CD polymer ( ● ), HP-β-CD ( ○ )on the
cinnamic acid solubility in buffer solution (pH 5). (a)
(b)
Figure 2. Dimerization and dedimerization of complexes composed of HP- β-CD/cinnamic acid (a), and β-CD polymer/cinnamic acid (b) under the altering irradiation, which is the UV irradiation with λ = 365 nm (400 W) for 10min and then with λ = 254 nm (6 W) for 5 min.
소수성 공동에 포접되기 때문에 β-CD의 농도에 비례하여 신남산의 용해도가 선형적으로 증가하는 경향이 나타난다고 사료된다[14,15, 16].
3.2. β-CD 중합체/신남산 복합체의 이량화도(Dimerization Degree) 측정
Figure 2 는 UV의 파장에 따른 신남산의 이량화도를 측정한 결과이다.
β-CD의 형태에 따른 신남산의 이량화도를 비교하기 위해 HP-β-CD/
신남산 복합체와 β-CD 중합체/신남산 복합체의 이량화도를 측정하 였다. λ = 365 nm의 UV를 30 min 조사했을 때, 단량체인 HP-β-CD/
신남산 복합체의 초기 이량화도는 53%이었으며, β-CD 중합체/신남 산 복합체의 초기 이량화도는 59%였다. 이후 λ = 254 nm의 UV를 10 min 간 조사했을 때, 단량체인 HP-β-CD/신남산 복합체와 β-CD 중합체/신남산 복합체의 이량화도는 각각 33%, 34%로 감소하여 신남 산의 탈이량화(dedimerization) 현상을 확인하였다. 이와 같은 실험을 5 회 반복했을 때, 전반적으로 β-CD 중합체/신남산 복합체는HP-β -CD/ 신남산 복합체에 비해 이량화도와 탈이량화도가 일정하게 유지 되는 것이 확인되었다.
3.3. β-CD 중합체/신남산 복합체의 형상관찰 및 광, pH반응성 관찰 UV조사에 따른 복합체의 형성 유무를 확인하기 위하여 UV조사 전, 후에 입자의 크기 변화를 DLS를 통하여 확인하였다. 신남산, β-CD 중합체, β-CD 중합체/신남산 복합체를 각각 UV 조사 전과 UV조사 ( λ = 365 nm, 400 W, 30 min) 후 입도 분석기를 이용하여 분석한 결과, 신남산은 UV조사 전/후 모두 입자의 크기가 측정되지 않았고, β-CD 중합체의 크기는 6회 측정 평균값이 UV 조사 전 210 nm이었으며, UV 조사 후 평균 218 nm로 측정되었다. 또한 β-CD 중합체/신남산 복 합체의 크기는 UV조사 전 평균 245 nm, UV조사 후에도 평균 241 nm 로 측정되었다. β-CD 중합체와 β-CD 중합체/신남산 복합체의 입자 크기는 큰 차이가 나지 않았고 UV조사 전/후의 두 샘플 모두에서 크기 변화가 측정되지 않았다(Tables 1, 2). 3.2에서 나타나는 β-CD 중합체
/ 신남산 복합체의 이량화도에 변화가 나타났지만 크기 변화가 일어나 지 않은 사실과 결부시켜 보아 UV에 의해 신남산 이량체가 형성되어 이량화도가 변화하는 것은 β-CD 중합체/신남산의 복합체 내부에서 일어나는 현상이지만 복합체 간에 일어나는 현상이 아니기 때문에 관 찰할 수 없었던 것으로 사료된다.
β-CD 중합체/신남산 복합체에 함유된 카복실기는 각기 다른 pH에서
이온화 정도의 차이를 나타내므로 복합체의 전위 변화가 나타나고,
입자에 존재하는 신남산의 전위 변화로 입자 내 반발력이 생겨 입자
의 크기변화가 일어날 수 있기 때문에 pH변화에 따른 입자의 크기와
Pβ-CD/CA
30% Zeta potential
(mV) 1.93
± 0.92 -4.88
± 1.22 -2.89
± 3.18 -3.21
± 0.79
1) CA : Cinnamic acid
2) Pβ-CD; Polymeric β-cyclodextrin
3) Pβ-CD/CA: The complex composed of polymeric β-cyclodextrin and cinnamic acid
4) Not detected.
Table 2. The Size and Zeta Potential of Cinnamic Acid, Polymeric β -cyclodextrin (30%, w/v), and the Complex (30%, w/v) Composed of P β-CD and Cinnamic Acid After UV Irradiation (λ = 365 nm, 400 W, 30 min)
pH 3 pH 5 pH 7 pH 9 CA
Size (nm) - - - -
Zeta potential (mV) -3.16
± 1.42 -6.59
± 0.61 -9.67
± 4.24 -6.34
± 3.54 Pβ-CD
30%
Size (nm) 227.7 162.1 237.4 248.6 Zeta potential
(mV) -0.33
± 0.33 -0.57
± 1.03 -0.72
± 0.25 -3.91
± 0.00 Pβ-CD/CA
30%
Size (nm) 241.0 249.0 201.8 276.1 Zeta potential
(mV) -11.08
± 1.27 -3.29
± 0.21 -5.31
± 1.64 -2.51
± 0.69
1) CA : Cinnamic acid,
2) Pβ-CD; Polymeric β-cyclodextrin,
3) Pβ-CD/CA: The complex composed of polymeric β-cyclodextrin and cinnamic acid
1) Pβ-CD; Polymeric β-cyclodextrin
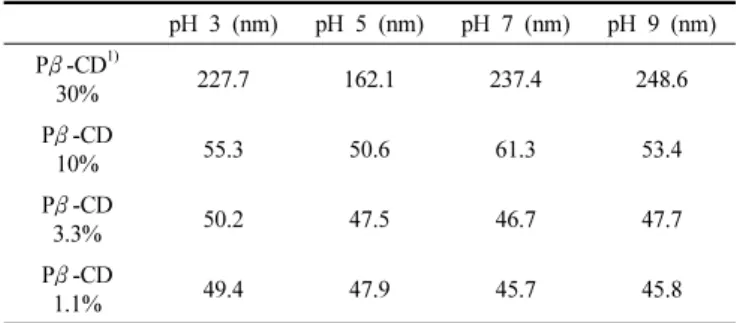
Table 4. The Size of the Complexes (30%, w/v), (10%, w/v), (3.3%, w/v), and (1.1%, w/v) which are Composed of P β-CD and CA after UV Irradiation ( λ = 365 nm, 400 W, 30 min)
pH 3 pH 5 pH 7 pH 9
Pβ-CD/CA
1)30% 241.0 249.0 201.8 276.1
Pβ-CD/CA
10% 73.5 78.6 70.8 73.6
Pβ-CD/CA
3.3% 50.2 54.3 51.9 52.8
Pβ-CD/CA
1.1% 54.1 55.6 51.6 51.2
1) Pβ-CD/CA: The composed of polymeric β-cyclodextrin and cinnamic acid
제타 전위 값을 측정하였다. 각각의 pH (pH 3.0, pH 5.0, pH 7.0, pH 9.0) 에서 제타 전위 값은 음전하(negative charge)값을 나타냈고, pH 변화에 따른 뚜렷한 경향성이 관찰되지 않아 전위 차이에 따른 크기 변화에서도 큰 차이를 보이지 않았다. pH에 따른 영향이 관찰되지 않는 것 또한 UV조사 시와 동일하게 β-CD 중합체/신남산 복합체에 존재 하는 신남산이 분자량이 매우 큰 β-CD 중합체간의 반발력에 영향이 있을 만큼 충분하지 않고 β-CD 중합체에 존재하는 수산기의 영향에 의해 복합체 제타전위 측정시 경향성이 보이지 않는 것으로 사료된다.
Tables 3, 4 에서는 UV가 조사된 β-CD 중합체와 β-CD 중합체/신 남산 복합체의 농도를 30% (w/v), 10% (w/v), 3.3% (w/v), 1.1% (w/v)로 감소시키며 DLS을 이용하여 입자의 크기를 측정하였다. β-CD 중합 체와 β-CD 중합체/신남산 복합체는 pH 변화에 관계없이 30% (w/v) 에서 각각 평균 218 nm, 241 nm이었으나 농도가 감소할수록 크기가 감소하였고 1.1% (w/v)에서 평균 53 nm, 47 nm까지 감소하였다. 이러 한 농도의 감소에 따른 입자의 크기 변화는 Table 2의 β-CD 중합체/
신남산 복합체의 DLS결과가 용액 속에 존재하는 β-CD 중합체의 광 산란 결과라고 여겨진다.
Figure 3 은 β-CD 중합체/신남산 복합체의 UV 조사 전과 후의
TEM이미지이다. TEM이미지를 살펴보면 UV 전/후에 뚜렷한 형상이 관찰되지 않았고 이미지에 서 보이는 형상은 앞서 언급했던 β-CD 중 합체/신남산 복합체에 포함된 β-CD 중합체로 보인다. Figure 3(a)와 (b) 에서 보이는 차이는 고분자의 분포 차이와 TEM시료 준비 과정 중 PTA 시료 염색 정도의 차이라고 보인다.
4. 결 론
본 연구에서는 β-CD 중합체와 신남산의 상호작용과 그 상호작용에
의한 복합체의 형성을 확인하였다. UV spectrometer를 이용해 β-CD
중합체의 농도에 따른 신남산의 용해도를 측정하였을 때, β-CD 중합
체의 농도가 증가 할수록 신남산의 용해도가 UV조사 유무에 따라 크
기에 큰 차이를 보이지 않았지만 대체적으로 증가하였다. TEM을 통
해 마이크로겔의 형성 여부를 확인 했을 때, 뚜렷한 형상이 관찰되지
않은 것으로 보아 마이크로겔이 형성 되었다고 볼 수 없고 복합체의
농도를 감소시킬수록 크기가 감소하는 것으로 보아 측정된 DLS에 의해
측정된 크기는 중합체 복합체의 광 산란에 의해 측정된 것이라고 생각
된다. 또한 pH의 변화에 따른 복합체의 크기 변화나 제타 전위의 차
이가 측정되지 않았다. 하지만 β-CD 중합체와 신남산의 복합체의
이량화도가 측정되었으며 단량체인 HP-β-CD/신남산의 복합체와
이량화 정도를 비교했을 때 차이를 확인할 수 있었다. 이 사실로 보아
β-CD 중합체와 신남산의 상호작용에 의한 복합체가 형성되었으며,
이 복합체는 광 반응성을 가지는 것으로 보여진다.
(a) (b)
Figure 3. TEM photos of complexes composed of β-CD polymer/ cinnamic acid before UV irradiation (a), and after UV irradiation for 30 min ( λ = 365 nm, 400 W) (b).
감 사
본 과제(결과물)는 교육과학기술부의 재원으로 한국연구재단의 지 원을 받아 수행된 산학협력 선도대학 육성사업의 연구결과입니다.
참 고 문 헌