약학회지 제42권 제 1 호 31~38(1998)
Yakhak Hoeji
Vol. 42. No. 15-아미노살리실산의 블Bi될 프 로 드 럭 :
텍스트란-5-(4-에톡시카르보날페 날아조)살리설산 에스테르
정연진 • 이정수 ■ 김윤텍 ■ 김영미* ■ 김대덕 ■ 한석규
부산대학교약학대학 (Received October 17. 1997)
D e x t r a n - 5 - ( 4 - e t h o x y c a r b o n y l p h e n y l a z o ) s a l i c y l i c A c i d E s t e r a s a C o l o n - s p e c i f i c P r o d r u g o f 5 - A m i n o s a l i c y l i c A c i d
Y u n J i n J u n g . J e o u n g S o o Lee. Y u n T a e k K im , Y o u n g M i K i n / , D a e D u k K im a n d S u k K y u H a n
College o f pharm acy, P usan N ational University, P usan Korea 609-735
Abstract—— Dextran-5-{4-ethoxycarbonylphenylazo)salicylic acid ester (Dextran-5-ESA) was synthesized as a potential colon-specific prodrug of 5-aminosalicylic acid (5-ASA). No free 5-(4-ethoxycar- bonylphenylazo) salicylic acid (5-ESA) was detected when the chemical stability of dextran-5-ESA was tested at pH 1.2, or pH 6.8 bath solution. Effects of the degree of substitution (DS) and molecular weight of dextran on the depolymerization by dextranase was investigated. Depolymerization
{%)
decreased with increasing DS. and was not affected by M.W. of dextran. The extent of prodrug conv
ersion after incubation in the contents of various G.I. tract segments of rats was evaluated. 5rASA was released in the cecal contents, but not in the contents of proximal small intestine (PSD or distal small intestine (DSI). No significant prodrug conversion was observed in the cecal contents of rats pretreated with kanamycin sulfate, which indicated that microbial enzymes were responsible for the cleavage of the prodrug.
Keywords □ Colon-specific delivery. 5-aminosalicylic acid prodrug, dextran, inflammatory bowel disease.
SSI
에선택적으로^ 을iS t
하고자하는 연구가 최근많은연구자둘에의해활발하게진행되고있다.
경 구투여한^ 을 선택적으로131
에is a
하고자하는 목적은크 게 두가지로구분된다.
첫째.
의작용부 위가^81
인 경우(feSi
내에 발생한 질환.
예컨대Crohn's disease.
궤양성 과민성8
틀증후군.
등
).
인^^»에 ^ 을 선택적으로 함으 로서전신적인부작용을줄이고치료효과를높이기위 함이다. ^^
둘째.
이^ 외 부위인의약품을개 발하고자하는경우이다.
이러한경우는신를에서Oftij
웃가여외치못한 외 를
test
에서일어나도록하"■본 논문에 관한 문외는 이 저자에게로 (전화) 051-510-2807 (팩스) 051-513-6753
는경우와경구투여한^ 의 보시간대를지연시킬 필요가있는경우를돌수있다
.^^
경구투여된^ 의 대사는 외효소와 의효소에의해일 어난다.
사람의GI tract
는호기성및혐기성^^^%둘 이 복잠한ecosystem
을 이루고있어서 영양물질이나^ 의 대사에중요한역할을하고었다
."*
^■외 가장 득톡한톡성은 함량이매우높다는점이며ycgi
내용물의약30%
정도) .
에서소화되지않는여러 종류의 기질들이bacteria
에외해서 대사된다.
내 외bacteria
은세포기능을위한에너지원으로서J
틀에서소화되지않는여러유형외기질을이용하는데,
내인성mucopolysaccharide
이외에도소위식이성섬 유로알려진cellulose, hemicellulose. pectin
그러고dextran
같은nonstarch polysaccharide
둘이대표적32 정연진• 이정수• 김윤텍• 김영미• 김대덕• 한석규
인둘질이다
."^
이둘은보통소화효소의작용을받지않지만
ISii
^의 둘에외해분해될수있기때문에고분자성
colorrspecific drug carrier
로활용할수 있다68>
Nonstarch polysaccharide
인dextran
은 약간의ot-1.3-
걸합의 가있는(x-1.6-glucopyranose
결합 으로이루어진직선형polysaccharide
로서득성,
면역 성이없고생체적함성이뛰어나서혈장확장제로서널리 사용되어 왔으며,
비경구용고분자 텔로서연 구되었다.® Dextran
분해효소인dextranase
는SSi
(청에서살고있는bacteriods
에의해서생산되며 이들 의 이나효소활성은개체PbI
또는개체^의 차이 가적은것으로알려져 있다."'®
이러한특성은colon- specific drug delivery system
으로서메우중요한성 질이라하겠다. Dextran prodrug
는matrix
외입체장 애로인해서상부소화관에서는결합된^ 이 가수분 해되지않고bacterial count
가높은호J i
이나158
룹에 서dextranase
에의해dextran matrix
가먼저 빠른 속도로분해되어분자크기가작아진후약물이가수분 해되어유러되는것으로알려져있다.®
5-Aminosalicylic acid
는Crohn's disease
같은염 중성8
^■질환치료에유효하지만상부소화관에서P
표i
|효 되거나대사불활성화되기때문에그자체로는환부인말단또는걸장에잘도달하지못하며
.
흡수된5- aminosalicylic acid
는nephrotic syndrome
을일으키 는 것으로 알려져 었으므로inflammatory bowel disease
의치료에적함하지못하다/ "
오'
따라서5-am- inosalicylic acid
의azo prodrug
인sulfasalazine, ol
salazine
등이개발되어사용되고있는데,
이 돌은 위나/H i
을그대로통과한후 ■에서 ^의m
토에 의해
azo
결합이 환원되어5-aminosalicylic acid
가유리되어작용하는것으로알려져있다/^
최근 에는5-aminosalicylic acid
외 고분자prodrug.**
내누brush-border enzyme-mediated amino acid pro~
d r u g s
또는glycoside
유도체*^^가개발되어 보고된 바있다.
본연구에서는
Crohn's disease,
궤양성 에사 용하는5-aminosalicylic acid
의 새로운 스rtt prodrug
외개발을목적으로dextran-5-ESA
틀합성하 고 이의 상부 소화관에서의 화학적 안정성. dextra- nase
에의한depolymeiization
에영향을미처는요인,
관부위별내용물에의한^ 의 유러정도를조사하
고자한다
. Dextran-5-ESA
는I
콤S
틀에서dextranase
에의하여matrix
가분해되면서5-ESA
가유리되고a- zoreductase
에 의하여azo group
이 환원되면서5- aminosalicylic acid
가유리될것으로예상된다.
실 험
시 약 및 기 기
Dextran. dextranase(Pe/iidZ/iMm sp.). carbony- Idiimidazole, salicylic acid, ethyl-p-aminobenzo- ate, sulfamic acid, kanamycin sulfate
및2.4-din- itrosalicylic acid(DNS
)는Sigma
제품을, HPLC
용 시약은Merck
제품을. Sephadex LH-20
은Phar- macia
제품을. sodium nitrite,
용매 및기타시약은 룩급을사용하였다.
IR spectra
는Bomem MB100 FT-IR spec- trophotometer
를사용하였다.
약물의 정량및분석은Shimadzu UV 2101-PC UV/VIS spectrophoto- meter
와Gilson HPLC
로 하였다. pH
는Orion 320 pH meter#.
시료는OHAUSE Analytical Plus
를사 용하여 평량하였다.
시료의 원심분리는Hanil Supra K-22 centriflige
를사용하였다. TLC
는Kieselgel 60 1^254
를사용하였다.
완 층 액
- USP
외규정에따라조제하여사용하였다.
완충액
A
:염산완충액(pH 1.2)
완층액B
:.1 M
초산완충액(pH 5.4)
완충액
C
:등장성 인산완충액은0.1 M sod. phos
phate dibasic
용액과0.15 M sod. phosphate mono
basic
용액을pH 6.8
이되도록흔합하여조제하였다.
완중액D
:5.0 mM
인산완중액은5 mM sod. phos
phate dibasic
용액과phosphoric acid
를pH 6
이되 도록흔합하여조제하였다.
HPLC
룹이용한5-ASA
의정량HPLC
는2 pump system (model 305, 306). vari
able UV detector(model 117). autoinjector(model 234). manometric module (model 805), dynamic mixer(model 811C)
로구성된Gilson
사의제품을사용 하였다. Column
은Gilson
사의Synchropac ODS(250
X 4 . 6 .
5^1111
)를사용하였고.
약물은254nm. AUFS
0.01
에서검출하였으며.
자료의처러는Gilson
사의712
software
로하였다.
이동상은0.5 mM tetrabutylam-
5-아미노살러실산의 I3 IS W 14 프로드럭 개발 33
monium chloride
가포함된 완충액D
외10% MeOH
용액을0.45 Mm membrane filter
로여과하여 사용하 였고,
유속은1.5m//min
으로2000 psi
정도외압력에 서사용하였다.
시료액중의
5-ASA
의측정은Chungi
등외®•방법을 참고하여행하였으며,
자세한내용은투고중인논문에 있다.*®'
UV spectrophotometer룹 이 용 한 약 울 의 정 랑
0.1N NaOH 100 m
/에약물100 mg
을넣고60°C
에 서1
시간반응시킨후반응액중외5-ESA
의농도가1 Ug/m/-20 ng/m/
되도록0.1N NaOH
로 희석하고358nm
에서흡광도를측정하여 검량선을작성하고미 지시료의흡광도를측정하여검량선으로부터약물외농 도를측정하였다.
DNS 법에 의 한 환 원 당 의 정 량
DNS
시액은dinitrosalicylic acid 5g
에2N NaOH 100 m
/와증류수250 m
;를가하여 완전히녹 인 후. sodium potassium tartrate tetrahydrate 150
담을용해시키고증류수를넣어500m
;가되게조 제하고차광용기에보관하였다.
Maltose
표준액(0.093 mg/m/~0.75 mg/m/) 200 ti
/를DNS
시액600 H
/와섞은후5
분간수욕상에서끓 이고얼음에서10
분간냉각후540 nm
에서흡광도를측 정하여검량선을작성하고미지시료의흡광도를측정하 여검량선으로부터환원당외농도를측정하였다.
5-(4-Ethoxycarbonylphenylazo)salicylic acid (4, 5- ESA)의합성
Ethyl p-aminobenzoate(
1, 4.13 g, 25 mmole
)을18%
염산13 m
/에 현탁시키고4°C
로 냉각시킨 후, sodium nitrite(1.9 g, 27.5 mmole) 3.5 m
/에용해시 킨용액을가하여30
분간반응시켰다.
과량의nitrous acid
는sulfamic add(0.25g, 2.5 mmole
)를 가하여 분해시키고,
냉각한후salicylic acidO, 3.45g, 27.5 mmole
)을20% sodium carbonate
용액에용해시킨 용액을가하여pH 9~10
을유지시키면서4°C
에서1
시 간 교반하면서 반응시켰다.
생성된 화합물 4외 S0-dium
염을여과하고Et0H/H20(l
:7)
용액으로재결 정시켜분리하고진한염산으로중화하여5.5g(69%)
외결정을얻었다. mp 216~217°C, IR(nujol) cm
'':1690(C = O. acid), 1720(C = O, ester).
Dextran-5-(4-ethoxycarbonylphenylazo)salicylic acid ester(7, Dextran-5-ESA)의 합 성
화합물(4,
0.5 g, 1.6 mmole
)을DMF 3.5 m
/에녹여benzene 17 m
;를 가하고carbonyldiimidazole(5.
0.52 g, 3.2mmole
)을가한후한시간반응시켰다.
여 기에benzene 18 m
/를가하고Sephadex LH-20 550 mg
을 가하여1
시간 반웅시켜 과량의carbonyl- diimidazole
를제거한후Sephadex LH-20
은 여과하 고benzene
을증발시킨 후, dextran(MW 70,000) 3
담을DMSO 60
m H 녹인 용액을 적가하고triethy- lamine 5.25 m
/틀가하여55°C
에서3
시간반응시켰다.
반응물을과량의Et0H/Et20(l
:5)
용액에가하여생성 된침전을 분리한후다시DMSO
에용해하고과량의Et0H/Et20(l
:5)
용액에가하여침전시키는조작을몇번반복하여분말상외침전을얻었다
. TLC
에서유리상태외화합물4는검출되지않았다
.
약 물 의 치 환 도(Degree of substitution : D S)의 측 정
Dextran-5-ESA 100 mg
을O.IN NaOH
용액100 m
;와60°C
에서1
시간반응시켜 유리되는sodium 5- (4-carboxylphenylazo) salicylate
를358 nm
에서UV
로정량하고이값(mg
)을DS
로하였다.
즉DS
는Dextran-5-ESA 100 mg
에결합된화합물4의mg
수 로정외하였다.
Dextran-5-ESA의 화 학 적 안 정 성
Dextran-5-ESA 1 g
을 완충액A 50 m
/와완충액C 50m
/에각각넣고3TC
에서6
시간반응시켰다.
반 응액0.1m
/에MeOH 0.9 m
/을가하여2
분간흔합하 고lO.OOOxg
에서5
분간원심분러한상등액에서dex- tran-5-ESA
로부터 유러된 화합물 4룰358nm
에서UV
로정량하였다.
Dextranase에 의 한 depolymerization에 미 치 는 dex- tran 분 자 량 의 영 향
분자량이
9,000
및70,000
인dextran
을사용하여합 성한DS 10
인dextran-5-ESA
를dextran
양으로2.52 mg/m/
되도록완충액B
에녹이고, dextranase
틀15 dextranase unit(DU)/m
/가 되도록 가하여,
37°C
에서 일정시간 반응시킨 후,
생성된 환원당을34 정연진• 이정수• 김윤텍• 김영머• 김대덕• 한석규
DNS
법으로즉정하여 분자량이depolymerization
에 미치는영향을조사하였다.
Dextranase에의한depolymerization에머처는DS
의영향
분자량
70,000
인Dextran
을 사용하여DS
가 각각43, 20. 15, 10. 9, 6
인dextran-5-ESA
를 합성하고depolymerization
에 미치는DS
의 영향을 조사하였 다. Dextran-5-ESA
를dextran
량으로2.52 mg/m/
가되도록각각완충액
B
에녹이고dextranase
틀15 DU/m
/가되도록가하여37°C
에서일정시간반응시킨 후 생성된 환원당을DNS
범으로 정량하여depoly
merization
정도틀측정하였다.
쥐행장내용물의dextranase 활성측정
Dextran
을완중액C
에녹인용액(25 mg/m/) 1
m l를일정량외
dextranase(Pe«ici7/iM; n sp
.)와37T
)에서30
분간배양시킨후,
즉시끓는물에1
분간넣어효소를 불활성화시키고 생성된환원당을DNS
법으로측정하 였다. Dextranase
사용량0.5 DU/mZ
에서4.5 DU/
m/
범위에서 검량선을 얻었다. it t t Sprague-Daw
ley rat
를EtsO
로마취하여개복한후맹장부위의양 쪽을봉합사로묶고그바깥쪽을절단한후질소로처 환되어있는장처내에서절개하여그내용돌을0.1 g
씩 평량하여마이크로튜브에넣고여기에dextran
을녹인 완충액C(25 mg/m/) 1 m
;룰가한후37°C
에서30
분 간배양하고즉시끓는물에1
분간넣고,
배양액내의환 원당을DNS
법으로측정하여검량선으로부터 맹장내 용물1 g
당dextranase
활성을측정하였다.
취하여유리된약물의양을
HPLC
로분석하였다.
쥐의맹장내용물과배양한dextran-5-ESA로부터유
리되는5-ASA의측정
tttt Sprague-Dawley rat
를EtaO
로마취하여 개 복한후맹장부위의앙쪽을봉합사로묶고그바깥쪽 을절단한후질소로치환되어있는장처내늬1
서절개하 여그내용물을0.1 g
썩평량하여마이크로튜브에넣고 여기에Dextran-5-ESA(DS 10
:5-ESA
로서110 Hg/0.5 m
/)를완층액(그에녹인용액0.5 m
/를각각가 하여6
시간동안37°C
에서 배양하였다.
그후적절한 시간간격에서시료를5.000rpm
에서3
분간원심분리 하여 얻은상등액0.1m
/에MeOH 0.9 m
/을가하여2
분간흔합하고lO.OOOxg
에서5
분간원심분리하여상 등액20H
/를취하여유리된5-ASA
의앙을HPLC
로 분석하였다.
Kanamycin sulfate(5x 200 mg/rat
)를2
일 동안 하루2
회그러고실험을시작하기4
시간전에경구투여 한 쥐 외 맹장내용물을사용하여위와같은방법으로dextran-5-ESA
부터 유리되는5-ASA
의 앙을HPLC
로분석하였다.
결과 및고찰
Dextran-5-ESA (7)의합성
Dextran
과5-ASA
의결합은Scheme I
에나타낸것C O O C ] H |
쥐의 소장상부 및소장하부 내용물과 배양한 dex-
tran-5-ESA로부터유리되는5-ASA의측정
쥐룰개복후위외말단과회장의 말단부위를절단하 고그중간을기준으로상부를소장상
.
부(PSI),
하부를 소장하부(DSI
)라하였다. PSI
및DSI
내용물을완충액C
로두배희석한용액0.2 m
/롤취하여마이크로튜브에 넣고여기에dextran-5-ESA(DS 10
:5-ESA
로서110 Hg/0.4m
/)를 완충액E
에녹인용액0.4 m
/를가하여6
시간동안37°C
에서배양하였다.
그후적절한시간간 격에서시료를5,000 rpm
에서3
분간원심분리하여얻은 상등액0.1 m
/에MeOH 0.9 m
/을가하여2
분간흔합하 고lO.OOOxg
에서5
분간원심분리하여 상등액20H
/를-COOCiHs
Scheme I -- Synthesis of 5-ESA and dextran-5-ESA.
5-아미노살러실산의 함14 프로드럭 개발 35
과같이 먼저
5-ASA
의아미노기롤봉쇄하기 위하여ethoxycarbonylphenylazo
기틀도입하여화합물4를 합성하고 이것을dextran
과 반응시켰다.
화합물 4외 합성은화합물1
를디아조화시켜화합물2
를얻은후화 합물3
과반응시켜얻었으며,융점과IR data
가문헌처 와 일치하였다.^^^
화합물4
와dextran
외 결합반응은Scheme I
에나타낸바와같이carbonyldiimidazole
(5)를 사용하여 이들을 화합물 6로한 후
triethy- lamine
를촉매로하여dextran
과반응시켰다.
화합물6
의생성반응을촉진시키기위하여두배과량의화합 물5를사용하였으며.
이때반응액중에존재하는과잉 의화합물5에외해dextran
의cross-linking
이일어 나는것을방지하기위하여Sephadex LH-20
을가하 여과잉의화합물5
를제거한후dextran
과반응시켰 다.
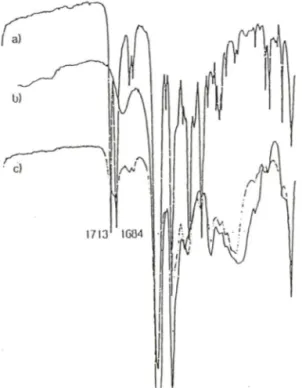
으오^ Fig. 1
에dextran-5-ESA
의IR spectrum
을나 타내었으며.
반응물질인 화합물4 및dextran
에기인 하는peak
둘이관찰되며약물과dextran
의결합에의 해생긴ester carbonyl
기의peak
가1690 cm'^
견푸에 서나타남을관찰할수있었다.
Dextran
일정량에대하여화합물4
의사용앙을달러 하여DS
가다른생성물을얻을수있었으며.
그결과를Table I — Weight of 5-(4-ethoxycarbonyllphenylazo) sal
icylic acid (5-ESA) per gram of dextran used for the coupling of 5-ESA to dextran to pre
pare dextran-5-ESA and the DS* of the resul- ting product
5-EAS 1.8 0.6 0.35 0.25 0.17
DS 43 21 15 10 6
* DS ; mg of 5^ESA bound per 100 mg of dextran-ESA.
Table I
에 나타내었다. DS
값은dextran-5-ESA
틀O.IN NaOH
용액에서1
시간반응시켜유리되는약물 을UV
로측정하여dextran-5-ESA 100 mg
당결합된 약물의mg
수로정하였다.
Dextran-5-ESA의화 학 적 안 정 성
결장표적성
prodrug
는경구투여한투상부소화관을 거치는동안물리화학적으로안정해야하므로 이를검 점하기 위하여dextran-5-ESA
를37T
:에서,
위또는 소장외pH
[틀고려하여pH 1.2
또는pH 6.8
수용액에 서6
시간동안반응시켰으나DS
값에관계없이화합물4는검출되지않았으므로위또는소장에서화학적으로 는안정한것으로생각되었다
.
Dextran-5-ESA의 dextranase에 의 한 depolyitieri- zation
Depolymerization
정도는dextran
이dextrana- se
에의하여분해되어생성되는isomaltose
를DNS
법 에 따라 정량하여 측정하였다.
분자량이 다른dex- tran
을사용하여얻은dextran-5-ESA(DS 10
)의de- polymerization
결과를Table II
에 나타내었으며.
dextran
의 분자량에 따른 영향은 나타나지 않았다.
DS
가다른시료둘외depolymerization
정도를 시간Table I I — Influence of variation in molecular weight (MW) of dextran on the depolymerization
{%)
of dextran-5-ESA by dextranase^^ \ T im e
M W ^ \ 0.5 min 0.5 hr 1 hr 3 hr
9000 42 60 94 100
70000 38 58 94 100
Fig. 1 — IR spectra of a) 5-ESA, b) Dextran, c) Dextran- 5ESA.
* The amount of sample (DS 10) containing 2.52 mg e- quivalent of dextran was incubated w ith dextra
nase (15 DU/m/) at 37"C and the degree of de
polymerization was determined by DNS method at specified time interval.
00 0.4 0.8 1.2 1.6 2 Absorbance
Fig. 2 — Calibration of dextranase activity (DA) and de
termination of DA in rat cecum contents. Dex
tran (25 mg in 1
m l
of phosphate buffer) was incubated with dextranase at 37°C for 30 min and the degree of depolymerization was determined by measuring the absorbance at 540 nm. Cali
bration curve was constructed at a range of 0.5^
4.5 DU/m/ of DA. DA of cecum contents was deduced from the calibration after incubation of dextran and cecum contents (0.1 g wet weight) by the same procedure.
10)
로측정되었다.
맹장내에는많은종류의효소가존재하고그중에는
dextranase
에의해생성된환원당을분해시키는것도 있는것으로알려져있다는점을고려하면.""^
실제쥐의 맹장내의dextranase activity
는본실험에서DNS
법 으로측정한값보다클것으로생각된다.
Dextran-5-ESA(DS 10)
를 쥐의 맹장 내용물과3TC
에서 배양한 결과를Fig. 3
에 나타내었다. Dex- tran-5-ESA
는8
시간경과했을때약50% (26.45
나g)
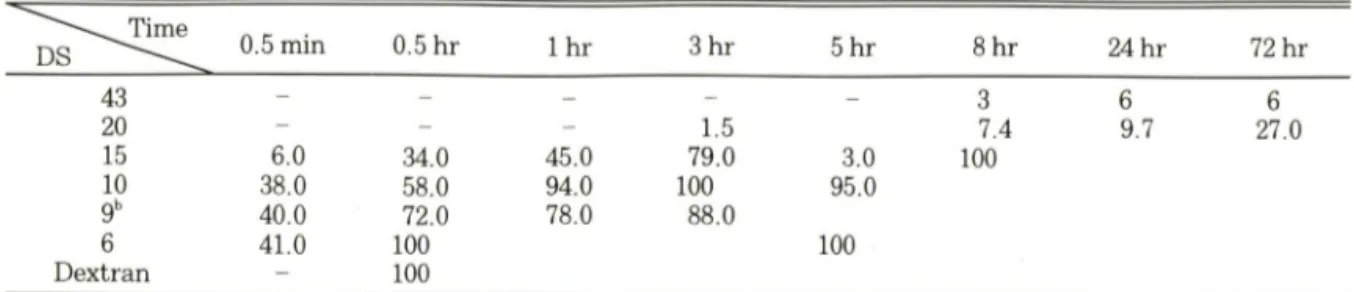
의 별로 즉정하여 그 걸과를Table III
에 나타내었다.
Dextran
은30
분 이내에 완전히 분해되었으며DS
가 클수록분해가잘일어나지않았고DS
가20
이상이되 면분해가거의일어나지않아서화합물4
의유러나아 가서는5-aminosalicylic acid
및benzocaine (1)
의 방출이제한적일것으로생각된다.
쥐의장관내용몰에의한
dextran-5-ESA
의활성화Dextran-5-ESA
외 활성화 과정은 상부소화관에서 는dextran
의업체장에로인하여esterase
의작용을 받지않아결합된 약물이가수분해대지않고bacterial count
가높은colon
에서 미생물에 의해 유래된en- dodextranase
에 의해dextran matrix
가먼저 빠른 속도로분해되어분자크기가작아진후소화관어디에 나존재하는esterase
에의해약물이가수분해되어유 러된다고 보고되어 있다.
따라서, dextran-5-ESA
를 경구투여하면,
결장에서 미생물의 작용으로dextran
골격이먼저분해되고ester
결함의가수분해와azo
기 의환원으로활성약물인5-ASA
가유러될것으로예상 하며.
이때보호기로이용한benzocaine
이어느정도 안정하게 남아서 작용한다면통증외 완화에도도움이 될것으로기대하였다.
쥐의장내dextran
분해효소외 개체간의 활성 차이를 조사하기 위하여 일정 과량의dextran
을dextranase(Pem'cfZ/fwrn sp.)
와배양한후depolymerization
되는정도를dextranase
의양을변 화시키면서DNS
법으로조사하여검량선을만들고.
같 은앙의dextran
을쥐의맹장내용물일정량과배양하 여depolymerization
정도틀측정한결과로부터검량 선을이용하여맹장내용물의dextranase
외활성을측 정하였고그결과를Fig. 2
에나타내었다.
쥐외맹장내 의평균dextranase activity(DA)
는7.4±0.11. (n =
6 Dextran
The am ount of sample containing 2.52 mg equivalent of dextran was incubated with dextranase (15 DU/m/) at 37T! and the degree of depolymerization was determined by DNS method at specified time interval.
^ Sephadex LH-20 non-treated product.
36 정연진 • 이정수 • 김윤택 • 김영미 • 김대덕 • 한석규
Table III — Influence of DS on the depolymerization (%) of dextran-5-ESA by dextranase determined by DNS m e t h o d ^ __________________________________________________________________
DS 0.5 min 0.5 hr 1 hr 3 hr 5 hr 8 hr 24 hr 72 hr
43 20 15 10 9"
7.- 27.
00 95.
00
- 9 0 8 7
o
00
45.
94.
78.
o o o
^ 0^ 0^ 5 7
어 어
V A IX ,
pcp
- 0 0
1 3 4 4
—# ~ 5-ESA 0.11 m g eqvJIOO m g cecal contents
— o ~ 5-ESA 0.11 m g »qv.MOO m g PSI or DSI conlente
10 - k >
15 20 25 30
Time(hr)
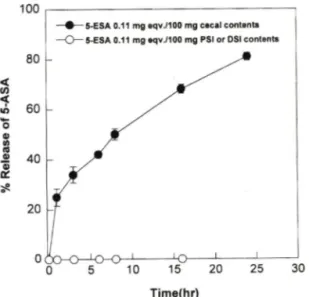
Fig. 3 — Release of 5-ASA in contents of 0.6 ml of six-fold dilution in isotonic phosphate buffer (pH 6.8) of cecum (w/v). PSI (v/v) and DSI (v/v) during in
cubation of dextran-5-ESA (DS 10, 110 |ag equiv.
of 5-ESA). Data are m eaniS.E . (n=5).
5-ASA가 유리되었고
.
24시간이 지나서는 80%(42.3^ig) 이상이유러되었다
.
소장내용물(PSI 와D S I)을사 용하여동일한방식으로행한실험에서는5-ASA가유 리되지않았다(Fig. 3).K a n a m y c in sulfate를전처러한실험동물의맹장내 용물에서는pro drug의활성화가거외관찰되지않았는 데(5-ASA농도가0.1 u g / m;이하
)
이는prodrug외활 성화가대장내미생물의효소에기인됨을보여준다.
본 실험결과로 5-am inosalicylic acid외 고분자성
prodrug인dextran-5-ESA는상부소화관에서롭수가 억제되고
.
화학적생물학적으로안정하며.
대장에도달 하면미생물유래외효소에의해분해되어결장표적성 을가지리라예상된다.
문 헌
1) Mcleod. A. D. and Tozer. N. T. ; Kinetic per
spectives in colonic drug delivery, in
Oral Colon Specific D rug Delivery, Friend,
D. R.. Ed.. CRC press. Boca Raton, F L.. 85 (1992).2) Mrsny, R. J . . Drug absorption in the colon
'■ A
critical review, inOral Colon Specific Drug D e livery,
Friend. D. R.. Ed., C R C press, Boca R a ton. FL., 45 (1992)3) Saffran. M ., O ral colon-specific d ru g delivery w ith emphasis on in s u lin: A critical review, in
Oral Colon Specific D rug D elivery,
Friend. D. R ..Ed.. C R C press, Boca Raton. F L ., 45 (1992).
4) S ham at, M . A.
'■
The role of the gastrointestinal microflora in the m etabolism of drugs.Int. J.
Pharm.
97. 1 (1993).5) Englysth. N.. Hay. s.. and Mcfarlane. G. T. ■ Po
lysaccharide breakdown by mixed populations of hu m an faecal bacteria,
FEMS Microbiol Ecol.
45,163 (1987).
6) Andrew D. M . : Dextran prodrugs for colonic- specific drug delivery, in
O ral Colon Specific D rug Delivery,
Friend. D .R ., E d .. C R C press.Boca Raton. F L.. 213 (1992).
7) Rubinstein. A.. Nakar. D. an d Sintov. A .. Chon- droitin sulfate : a potential biodegradable car
rier for conlon-specific d ru g delivery.
In t. J.
Pharm.
84, 141 (1992).8) Ashore. M. Fell, J., Astwood, D .. S harm a, H.
an d Woodhead. P.. A n evaluation of pectin as a carrier for drug targeting to the colon,
J. Control.
Rel. 26,
213 (1993).9) Larsen. C.. Johansen, M ., Dextrans as carriers for drug compounds-realized an d potential a p plications,
Arch. Pharm. Chemi.
92, 809 (1985).10) McLeod. A. D., Friend. D. R ., Tozer, T. N. : Glucocorticoid-dextran conjugate as potential prodrugs for colon-specific delivery: Hydrolysis in rat gastrointestinal tract contents.
J. Pharm.
Sci.
83, 1284(1994).11) Crotty. B. and Jewel, J . P. - D ru g therapy of u l
cerative colitis,
Br. J. Clin. Pharmacol.
34, 189 (1992).12) Novis. B. H., Korzets, J.. Chen. P. and Bem - heim . J .. Nephrotic syndrome after treatm ent w ith 5-aminosalicylic acid.
Br. Med. J.
296. 1442 (1988).13) Ryde, E. M . ■ Low-molecular-weight azo com
pounds. in
Oral Colon Specific D ru g D elivery
. Friend. D. R., Ed.. C R C press, Boca Raton, FL..143 (1992).
14) Brown. J. P., M cGarraugh, G. V., Parkinson. T.
M .. W ingard. R. K , Onderdonk. A. B. A poly Omeric d ru g for tre a tm e n t o f in fla m m a to r y
5•아미노살리실산의 해양14 프로드럭 개발 37
0
0
0 6
4
2
<
w
<
. w i o
%
38 정연진• 이정수• 김윤텍• 김영미• 김대덕• 한석규
bowel disease. I Med. Chem, 26. 1300 (1983).
15) Kopeckova. P. and Kopecek. J. ■ Release of 5- aminosalicylic acid from bioadhesive N-(2-hy- droxypropyOmethacrylamide copolymers by a- zoreductases in vitro, Makromol Chem. 191. 2037 (1990).
16) Pellicciari. R.. Garzon-Aburbeh. N athalini, B..
M a rin o zzi. M . : Brush-border-enzyme-medi- ated intestine-specific drug delivery. A m ino acid prodrugs of 5-aminosalicylic acid. J. Med.
Chem. 36. 4201 (1993).
17) Istran. C.. Gabor, S. and Ferene. S. '■ Glycosides of 5-AminosalicyIic acid. Magy Kent. FOLY. 97, 143 (1991).
18) Chungi, V. S.. Rekhi. G. S. and Shargel, L. : A simple and rapid liquid chromatographic method for the determination of major metabolites of sul
fasalazine in biological fluids. I Pharm. Sci. 78(3).
235 (1989).
19) 정연진. 이정수. 김학현. 김영미. 한석규: ■머노살 리실산의 결장표적성 prodrug '■ 5■아미노살리설-Lr 글루타민산과 5■아미노살리실-L~아스파틸산의 합성 과성상. 약학회지 . submitted for publication.
20) Yam aguchi. T.. Sasaki. K.. Nakayam a. T.. and K im u ra. T. : Biopharm aceutical evaluation of salicylazosulfanilic acid as a novel colon-targe
ted prodrug of 5-aminosalicylic acid, 2, 123 (1994).
21) Robert. C. M . and Gerhard. E. G ■ A novel m ethod of complete activation by carbonyldi
imidazole ; application to ester synthesis. Can. J.
Chem. 66 1701 (1988).
22) Mortensen, P. B.. Hove. H ., Clausen. M. R.
and Holtug, K. '■ Ferm entation to short-chain fatty acids and lactate in h u m an faecal batch cultures. Scand, J. Gastroenterol. 26. 1285 (1991).