그 동안 우리 방사선과 의사의 관심 영역에서 조금 떨어져 있던 뇌혈관 질환(cerebrovascular disease) 특히 허혈성 뇌 졸중(ischemic brain stroke)에 대한 관심이 최근 고조되고 있 다. 그 이유는 이 질환이 여러 질병군 사이에서 차지하는 비중 과 사회적 관심이 높아진 원인도 있겠으나 무엇보다도 에코평 면영상(echo-planar imaging, EPI) 기법을 이용한 확산강조 영상(diffusion-weighted imaging, DWI)의 성공적인 임상 무 대로의 데뷔가 큰 역할을 하지 않았나 생각된다. 이는 임상의 에게 있어서도 뇌경색의 진단과 치료 패턴에 큰 변화를 가져 온 가히 혁명적이라고 할 수 있는 것으로 평가된다(1).
뇌혈관 질환에 의한 사망은 우리 나라의 경우 인구 10만 명 당 73.2명으로 악성 신생물에 이어 두 번째의 사망 원인으로 알려져 있다(2). 뇌졸중을 크게 출혈성과 허혈성 원인으로 나 눌 때, 과거 우리나라는 출혈성 뇌졸중의 비율이 높았으나, 최 근 허혈성 원인이 50%이상을 상회하면서 그 비율이 서구화되 어 가고 있다(3). 이와 같이 허혈성 뇌졸중이 증가하고 있는 것은 관상동맥 질환의 증가와 그 맥을 같이 한다고 볼 때, 식 습관의 서구화와 생활 패턴의 변화가 큰 원인일 것으로 생각 된다.
뇌질환에 대한 관심은 국내외적이며 이미 미국의 경우‘뇌 연구 10년(decade of the brain)’을 주창하고 뇌질환에 관한 연구에 매진하고 있고, 늦은 감이 있지만 우리 나라에서도 같 은 움직임이 있는 상황이라 우리 방사선과 의사들의 적극적인 관심이 요구되는 때라고 생각된다. 이를 계기로 뇌졸중 환자의 진료에 적극적으로 참여하는 계기가 되었으면 하는 바램이다.
아직 여건상 초급성기에 MR을 적용할 정도로 여유 있는 기관 이 많지는 않으나 향후 더 보편적으로 적용할 여지가 많다고 생각되며 그런 맥락에서 이 종설을 통하여 급성 허혈성 뇌경
색 특히, 증상 발현 6시간 이내의 초급성기(hyperacute stage) 환자의 진단과 치료에 있어서 MR 영상의 방법과 역할을 자세 히 살펴볼 기회를 가져보고자 한다.
허혈성 뇌경색의 치료
90년대 초까지만 해도 허혈성 뇌경색의 치료는 허혈 경과 시간에 관계없이 내과적 지지요법 또는 항응고요법이 주를 이 루었으나, 90년대 중반 이후 tissue plasminogen activator (tPA)를 이용한 정맥내 혈전용해술(intravenous thromboly- sis, IV-tPA)과 다양한 혈전용해제를 이용한 국소적 동맥내 혈전용해술(local intraarterial thrombolysis, LIT)이 각광을 받 으면서 초급성기에 적극적인 치료를 하고자 다양하게 시도되 었다(4-8). 그 결과 증상 발현 3시간 이내에는 IV-tPA가, 6 시간 이내에는 LIT가 환자의 예후의 호전에 많은 도움이 될 수 있다는 사실이 비교적 널리 인정 받게 되었으며, 초급성기 에 응급실로 내원한 허혈성 뇌경색 환자의 상당수가 적극적인 치료를 받을 수 있게 되었다.
초급성기 허혈성 뇌경색의 치료 목표
초급성기의 혈전용해술은 허혈 상태의 뇌조직의 상당 부분 이 조직 재관류(tissue reperfusion)에 의해 가역적인 허혈 반 영대(ischemic penumbra)가 존재할 것이라는 믿음에서 시행 되고 있다(9). 이 부위는 시간이 경과하면서 급속히 감소하며, 반대로 비가역적인 변화를 겪게 되는 허혈 중심부(ischemic core)가 증가 되어 재관류 시 오히려 출혈성 전환(hemorrhagic transformation)을 초래할 수도 있다. 실제로 앞에서 언급한 일 련의 연구들의 결과를 봐도 통계적으로 유의한 치료 성적의 향 상뿐만 아니라 원하지 않는 합병증으로 뇌출혈의 빈도가 유의 하게 증가되어 전체적인 기능적 예후 향상 효과가 반감되는 것 을 알 수 있다. 그러므로 혈전용해술을 시행하기 전에 허혈의
급성기 허혈성 뇌경색의 자기공명영상 1
이 덕 희・이 정 현
최근 뇌혈관 질환 특히 허혈성 뇌졸중에 대한 관심이 고조되고 있고, 확산강조영상의 성공적 인 임상 적용은 방사선과, 신경과 의사들의 진단과 치료 패턴에 큰 변화를 몰고 온 계기가 되 었다. 이러한 뇌질환에 대한 관심은 국내외적인 상황이라 우리 방사선과 의사들의 적극적인 관 심이 요구되는 때라고 생각된다. 이를 계기로 급성 허혈성 뇌경색 특히 증상 발현 6시간 이내 의 초급성기 환자의 진단과 치료에 있어서 MR의 역할을 살펴보고자 한다.
1울산대학교 의과대학 서울아산병원 방사선과
이 논문은 2004년 1월 7일 접수하여 2004년 1월 26일에 채택되었음.
진행 정도를 평가하는 것이 무엇보다도 중요하다고 할 수 있 으며 바로 이것이 초급성기 영상 진단 작업의 가장 중요한 목 표인 것이다.
허혈성 뇌경색 환자의 영상에 있어서 필수적인 요소를 4P로 요약할 수 있다(10). 4P란 뇌조직의 손상 정도를 말하는 parenchyma, 혈관 폐색 상태를 뜻하는 pipe, 뇌조직의 관류상 태를 말하는 perfusion, 마지막으로 penumbra의 머리 글자이 다. 이 네 가지 요소를 동시에 평가할 수 있는 검사법이 바로 MR인 것이다.
허혈에 의한 급성기 뇌손상
갑작스런 뇌혈관 폐색으로 뇌조직이 겪게 되는 일련의 과정 을 살펴보자(11). 먼저 관류 이상(perfusion abnormality)이 나타난다. 이 단계는 혈관이 폐색되어 뇌조직으로의 혈류의 차 단이 일어난 과정으로 MR 혈관조영술(MR angiography, MRA)과 MR 관류영상(MR perfusion image, perfusion- weighted image, PWI)를 이용해서 영상화할 수 있다.
관류 이상의 결과, 에너지 공급이 차단되면 기능 이상(func- tional impairment)이 뒤따르며 환자의 신경학적 증상 발생의 원인이 된다. 이 경우도 뇌혈류 감소의 정도에 따라 크게 두 가지 상황으로 나누어 볼 수 있다. 뇌혈류 감소가 심하여 뇌세 포의 모양을 유지할 수 없을 정도인 경우는 기능 이상과 더불 어 세포독성부종(cytotoxic edema)이 초래되어 뇌세포 손상 이 비가역적인 단계를 밟게 되며, 이 경우가 바로 DWI가 진가 를 발휘하는 단계이다. 또 한 경우는 뇌혈류의 감소 정도가 심 하지 않아 비록 기능 이상은 초래된 상황이지만 세포가 기본 적인 대사를 할 수 있을 정도는 되어 세포가 살아있는 상태를 말하며 소위 허혈성 반영대에 해당되는 부위이다. 이를 MRI를 이용하여 영상화할 수는 없는데, DWI에서의 세포독성부종이 발생한 부위 주변의 PWI에서 보이는 관류 이상 부위가 이러 한 변화를 겪고 있는 영역이라는 가정하에 DWI-PWI 불일치 (mismatch) 부분으로 잠정적으로 규정하고 있다.
마지막으로 지속적인 허혈의 결과 형태적 변화(morpholog- ical change)가 초래된다. 심한 허혈상태가 지속되면 세포독성 부종에 빠진 세포에 심한 부종 등의 형태적 변화가 일어나고 뇌조직의 모세혈관 내막의 기저막이 파괴되면서 소위 혈관성 부종(vasogenic edema)가 초래되면 고식적인 MR로도 그 변 화를 볼 수 있는 상태가 된다.
MR은 조직 시계(tissue clock)이다
앞에서 언급한 소견들은 허혈에 빠진 뇌조직이 겪게 되는 일 련의 변화로 볼 수도 있고 국소적으로 한 구역 내에서도 각 조 직의 상황에 따라 다양하게 일어나는 현상으로 볼 수도 있다.
다시 말해서 같은 초급성기라는 일정한 시간 안에서도 허혈에 빠진 뇌조직이 다양한 변화를 겪게 된다는 것이다. 더구나 실 제 환자에서는 다양한 인자들의 영향으로 더 복잡한 경과를 취 할 것이라는 것은 자명한 것이다. 예를 들어 같은 중뇌동맥 폐 색 시에도 환자의 전신상태, 혈관 폐색의 원인, 측부혈행의 발 달 정도 등에 따라 다양한 영상 소견을 나타내는 것을 관찰할
수 있다.
그러므로 허혈시간(time to treatment)의 중요성을 매우 강 조하여 3시간 이내에 혈전용해제 투여를 원칙으로 하고 있고 90분 이내에 투약을 받은 그룹의 예후가 더 좋다는 보고를 하 고 있는 NINDS의 IV tPA 요법에 관한 연구(5)는 제한점이 있다고 할 수 있겠다. 이러한 역동적인 뇌조직의 허혈에 대한 반응의 다양성을 고려하기 위해 단순한 허혈시간 (ischemic duration measured by a ticking clock)뿐 만 아니라 조직 자 체의 허혈 손상 정도를 평가하는 것이 중요하다는 관점에서 조 직 시계를 적용하는 것도 의미 있는 주장이라고 할 수 있다.
CT를 이용하여 조기 뇌경색 소견(early infarct sign)의 범위 를 확인하고자 하는 것 등이 바로 이러한 조직 시계를 읽기 위 한 노력의 하나라고 생각되며, 현재로서는 MR이 가장 손쉽고 정확한 조직 시계의 역할을 할 수 있는 검사법으로 생각된다.
수 년 전부터 급성기 허혈성 뇌경색 환자의 일차적 영상 검사 법으로 MR을 이용하는 경우가 증가하고 있으며 서울아산병원 도 그 중 하나이다(12, 13).
서울아산병원의‘Acute Stroke MR’프로토콜
구체적인 펄스 연쇄의 소개와 그 역할에 대한 설명에 들어 가기 전에 먼저 저자가 근무하고 있는 병원의 프로토콜을 보 자. 2003년 12월 30일 현재 5대의 장비가 오전 7시부터 저녁 10시까지 가동되고 있으며 그 중 한 장비(GE CVi 1.5T)를 주 로 이용하고 있다. 장비가 가동되지 않는 시간에는 부득이 CT 를 이용하고 있다.
환자가 응급실에서 도착하여, 간단한 신경학적 검사 결과 뇌 경색으로 생각되고 증상 발현 6시간 이내인 경우, 바로 MR실 에 연락하고 검사를 시작할 수 있도록 하는데, 영상이 얻어지 기 시작할 때까지 가능한 한 연락 후 20분 이상 경과되지 않 도록 하였다. 신경과 의사와 방사선과 의사는 영상 획득이 이 루어지고 있는 사이에 환자에 대한 정보를 교환하고 향후 치 료에 대한 대강의 계획을 세운다. 영상 획득이 완료된 후 즉시 방사선과 의사는 얻어진 자료들의 후처리(post-processing) 를 시행하며, 그 동안 신경과 의사는 정확한 신경학적 검사로 환자를 다시 평가하고 종합적인 임상 소견과 MR검사 소견을 참고하여 구체적인 치료 방침을 토의/결정한다.
영상 획득에 있어서 일반적인 MR검사 시와는 달리 좋은 영 상을 얻는 것보다는 영상 획득의 신속성에 더 중점을 두어 신 호 대 잡음비나 해상도를 희생하고 영상 획득 시간을 줄이기 위해 노력하였다. 2001년 3월 처음 시작한 이후 프로토콜과 펄스 연쇄에 다소의 변화가 있었는데 가장 최근의 프로토콜을 기준으로 기술한다(Table 1).
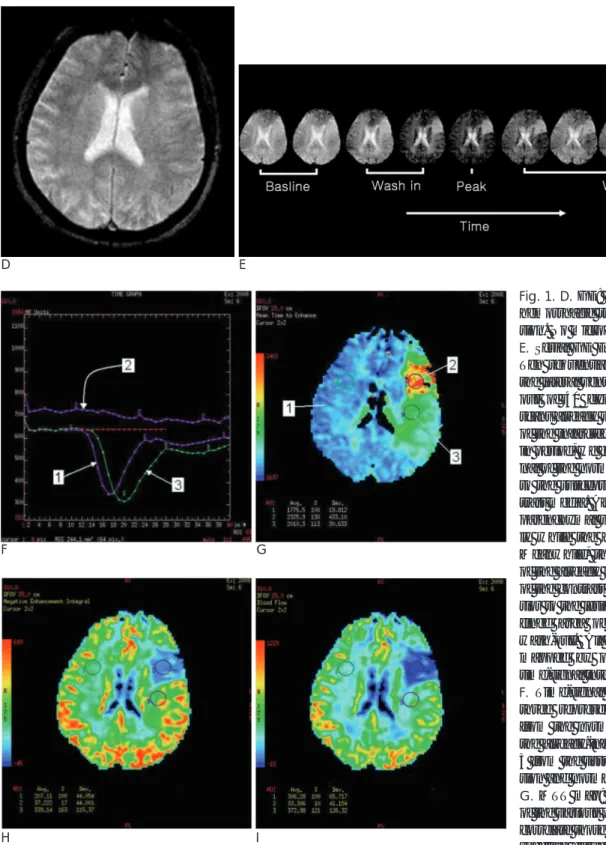
먼저 T2 강조영상(T2-weighted imaging, T2WI)을 얻어 과거 병변 유무와 현재 병변의 T2 신호 변화 여부를 확인한 다. 고속 스핀에코 기법을 사용하여 1분 이내에 영상을 얻을 수 있다(Fig. 1A).
이어서 b값(b factor)을 2000 sec/mm2(이하 단위 생략)으 로 한 DWI를 얻어 급성기의 뇌경색 소견 여부와 위치, 범위를 평가한다. 뇌경색 여부를 어느 정도 알 수 있는 단계이며, 병
변이 있다면 열공성 뇌경색(lacunar infarction)인지, 구역성 뇌 경색(territorial infarction)인지 대개는 파악된다(Fig. 1B).
바로 3차원 유체속도강조 혈관조영술(3D time-of-flight MR angiography, TOF-MRA)를 윌리스 환을 중심으로 시행 하며, 영상 획득 시간을 줄이기 위해 2개의 판(slab)만 얻는다 (Fig. 1C). 그래도 4분 이상이 소요되는 가장 시간이 많이 걸 리는 검사이다. 또한 환자의 협조가 불량하여 두부의 움직임으 로 인해 좋은 영상을 얻기 힘든 경우가 많다. 그러나 동맥의 폐색이 있는 경우 중뇌동맥의 원위부까지는 정확히 확인할 수 있으므로 진단적 정보를 얻는 데는 손색이 없고 혈관 폐색의 위치를 바로 알 수 있다는 큰 장점이 있으므로 꼭 필요한 검 사라고 생각된다.
이어서 경사에코 영상(Gradient echo imaging, GRE)을 얻 는데 역시 2분 이상의 시간이 걸리지만 미량의 출혈도 민감하 게 검출해주므로 특히 혈전용해술을 받을 환자에서는 시간의
경과도 문제이지만 미세한 출혈을 간과하는 경우 매우 위험할 수 있으므로 꼭 확인할 필요가 있다고 생각한다(Fig. 1D).
구역성 뇌경색인 경우 추가적으로 PWI를 시행한다(Fig. 1E).
민감한 자화율 효과를 가진 GRE EPI기법을 이용하여 역동적 영상을 얻어 옆에 있는 작업대(workstation, GE advantage windows ver. 4.1)로 자료를 전송한 뒤 바로 후처리 한다(Fig.
1F-I). 만약 후뇌순환 병변(posterior circulation lesion)이 있 는 경우에는 PWI를 시행하지 않고 추골 동맥의 상태를 보기 위해 조영증강 MRA(Contrast-enhanced MRA, CE-MRA) 를 시행한다.
최근 FLAIR(fluid-attenuated inversion recovery) 기법을 적용하기 위한 시도를 하고 있는 중인데, 그 이유는 T2WI보 다 훨씬 병변의 명료성이 뛰어난 등의 장점이 있기 때문인데, 영상 획득에 소요되는 시간이 다소 길어 문제이다(Fig. 1B).
병변의 추적 검사는 증상 발현 3-5일 후에 MR로 시행하였
Table 1. Imaging Protocol of
‘Acute Stroke MR’in Asan Medical Center
Pulse sequence Imaging parameters Acquisition time
Common parameters Neurovascular coil, axial scan, FOV: 250mm, slice thickness: 5mm, interslice gap: 2mm, number of slices: 20, reconstruction matrix size: 256×256
FSE T2WI ETL: 16, TR: 4000 ms, TE: 118 ms, 1 NEX 48 sec
DWI SE EPI, b factor: 2000, TR: 7500 ms, TE: 80 ms, 2 NEX 1 min
3D TOF MRA SPGR, TR: 25 ms, TE:3.1ms, 1 NEX, FOV: 200mm, 2 axial slabs 4 min 36 sec
T2*WI GE, TR: 500, TE:30, Flip angle: 20o, 1 NEX 2 min 32 sec
PWI GE EPI, TR: 2000 ms, TE: 60 ms, number of slices: 10 1 min 22 sec
CE-MRA TR: 6.9 ms, TE:2.2ms, 1 coronal slab, 0.5 NEX 46 sec
FLAIR TR: 8000 ms, TE:80ms, TI: 2000ms, 1 NEX 2 min 20 sec
A B C
Fig. 1. MR images of
‘Acute Stroke MR’protocol obtained in a 72-year-old female. She revealed global aphasia and right side weakness three hours before the imaging.
A. FLAIR image: An obvious signal change is noted at the frontal portion of the left middle cerebral artery (MCA) vascular territo-
ry. The T2 change of the lesion may suggest longer duration of ischemia more than three hours.
B. DWI b(2000): densely high signal intensity is noted at the area with the T2 change. Rest of the left MCA territory is spared from
the DWI abnormality.
C. TOF MRA of intracranial vessels: The MCA is occluded at its mid M1 segment. Although the quality of the MRA is not good, we
can clearly see the level of the occlusion without difficulty.
F G
H I
Fig. 1. D. GE: There is no evidence of
hemorrhagic transformation of the le- sion. No microbleed is noted.
E. Serial GE EPI images for the PWI:
Ten sequential images of the slice at the lateral ventricle level were selected out of 40 dynamic images. Baseline scans already show an increased signal of the infarcted area. During the wash- in period, we can see the decreased sig- nal of the normally perfused tissue due to the susceptibility effect of the con- trast media. After the peak, the normal parenchymal signal decreases gradual- ly while the contrast is washing-out.
Meanwhile, there is no signal change of the already infarcted area regardless of the contrast filling status. Just poste- rior to the lesion, we can see an ill-de- fined area of delayed wash-in and wash-out. All these findings can be mapped by obtaining pixel-by-pixel time-signal intensity curves.
F. Time-signal intensity curves of the
three representative areas (curve 1 from the normal tissue, curve 2 from the already-infarcted tissue, and curve 3 from the tissue with decreased perfu- sion and normal DWI).
G. MTT map: The most sensitive one
of the various parameter maps. We can correlate those three areas with the re- spective curves of (E) in different col- ors. (H) CBV map: The area 3 of the MTT map seems to have normal CBV suggesting good collaterals. (I) CBF map: We can see slightly decreased CBF at the central area of the area 3 just posterior to the area 2.
D E
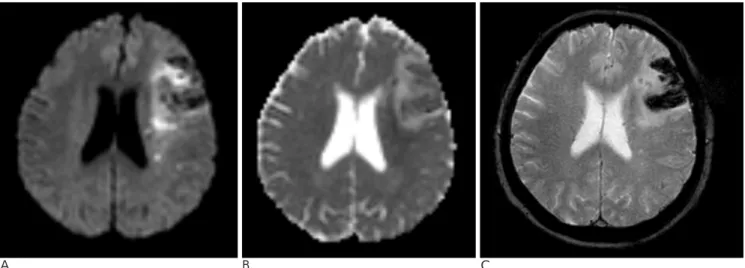
으며 환자의 상태가 안정화된 경우에는 일반적인 MR과 같은 해상도로 얻는다(Fig. 2). 포함된 펄스 연쇄는 T2WI, DWI, GRE, TOF-MRA, CE-MRA이다. 병변의 진행 정도의 파악, 혈관 협착/폐색의 정도와 원인 규명에 초점을 맞춘다.
급성 허혈성 뇌경색의 고식적 MR 소견
DWI가 임상적용이 가능하기 이전에는 초급성 뇌경색의 진 단에 있어서 MR의 역할은 아주 제한적이었다. 그 이유는 세포 독성부종에 의한 뇌실질의 변화는 T1WI 또는 T2WI 등의 고 식적 MR영상에서는 나타나지 않았기 때문이다. 다음은 Yuh 등이 정리한 발병 24시간내의 MR소견이다(14).
MR로 관찰할 수 있는 가장 초기 소견은, 혈류의 차단에 의 해 혈관 신호 소실(vascular signal void)이 보이지 않거나 느 린 혈류로 오히려 혈관 신호가 증가될 수 있다. 특히 조영증강 시 매우 느려져 있는 피질 혈관의 조영 증강 현상이 보이는 경 우가 많으며 이는 연질막 측부혈행을 대변하는 소견으로 이해 되고 있다.
가장 초기에 관찰할 수 있는 형태적 변화는 T1WI에서 뇌고 랑이 잘 보이지 않는 소견(obliteration of the cortical sulci) 인데, 이는 CT에서 보이는 초기 뇌경색 소견과 같은 기전으로 설명할 수 있다. 미미하지만 세포독성 부종으로 인해 뇌조직의 전체적인 수분의 증가에 기인 하는 것으로 생각된다.
T2WI상 병변의 신호의 증가를 관찰할 수 있는 것은 8시간 이후라야 분명해지며, 최소한 4-6시간은 지나야 육안으로 구 분할 수 있는데, 이는 혈관성부종이 시작되었음을 시사하는 소 견이다. 이때 양자밀도 강조영상이 좀 더 병변을 잘 보여주는 것으로 알려져 있다(15). Fig. 1B의 경우 3시간 전에 최초 증 상이 발현되었다고 하지만 이미 분명한 병변이 보인다는 것은 그 이상의 시간이 경과되었을 가능성을 염두에 두어야 한다.
물론 이 환자의 조직 시계가 보통의 경우보다 빨리 돌아갔을
가능성도 있는 것이다. 이와 같이 MR은 증상 발현 시간이 불 분명하거나 의심스러운 경우뿐만 아니라 이와 같이 병력이 분 명한 경우에도 병변의 진행 정도를 단순히 경과 시간으로만 판 단하는 차원을 지나 상당히 객관적인 정보를 제공할 수 있다.
T1WI에서 낮은 신호 강도로 나타나기까지는 24시간은 경과 해야 한다.
최근 FLAIR 기법이 초급성기에 도움을 줄 수 있다는 보고 가 있는데, 뇌척수액의 신호를 완전히 억제함으로써, 앞에서 언 급한 뇌 피질 혈관의 느려진 혈류에 의한 증가된 혈관내 신호 의 증가(intravascular signal)가 매우 뚜렷하게 보이며, T2WI 에서 놓치기 쉬운 피질부의 신호변화도 매우 민감하게 보여줄 수 있기 때문으로 주장하고 있다(16, 17). 그러나 뇌간의 작 은 병변에 대한 발견율이 떨어지며 특히 환자의 미세한 움직 임에도 민감해서 좋은 영상을 얻지 못하는 경우가 있다 (17).
새로운 국면에 들어선 MR 영상
이와 같이 CT와 비교할 때 고식적 MR은 별 장점을 발휘하 지 못하고 있었으며, 1990년대 초 실험실에서는 급성기 뇌경 색에 대한 다양한 연구들이 쏟아져 나왔음에도 불구하고, 검사 환경의 특수성, 긴 검사 소요 시간, 출혈에 대한 낮은 민감도, EPI 기법의 비상용화 등의 이유로 급성기에 MR을 이용하여 허혈성 뇌경색 환자의 영상을 얻는 경우는 거의 없었다. 그러 나 1990년대 중반에 접어들면서 EPI 기술을 손쉽게 구현할 수 있는 MR 장비의 진보와 함께 급성기 뇌경색에 관한 MR 영상 은 새로운 국면에 접어들게 되었다(18).
SE T2WI 기법을 기반으로 확산자계(diffusion gradient)를 이용하여 처음으로 스핀의 확산 현상을 측정한 것은 1965년 도였다(19). 그러나 조직 내에서 일어나는 미세한 분자 운동 현상인‘확산(diffusion)’을 영상으로 얻어내기 위해서는 초고 속 영상 기법인 EPI가 상용화되는 90년대 중반이 이르기까지
A B C
Fig. 2. Follow-up MR images were obtained three days after the initial MR.
A. DWI: The area 2 revealed hemorrhagic transformation. Part of the area 3 shows progression of the DWI abnormality at the very
region where the initial CBF abnormality was.
B. ADC map (C) GE (The T2WI, TOF MRA, and CE MRA are not shown here).
거의 임상에 적용할 수 없었다. 아무리 머리가 장기 중에서 움 직임이 적다 해도 FSE 기법도 아닌 고식적 SE 기법으로 영상 을 얻는 것은 그 전까지는 거의 불가능했기 때문이다. 그러나 MR 장비가 발전하면서 강력한 경사자계를 이용한 EPI 기법이 가능해지면서 DWI가 임상적으로 폭 넓게 사용될 수 있게 된 것이다(20).
확산 강조영상
‘확산’이란 열에 의해서 가장 민감하게 반응하는 물 분자의 자유로운 움직임을 말한다. 물잔에 잉크를 한 방울 떨어뜨린 후 관찰할 수 있는 자유로운 움직임 즉, 브라운 운동(Brownian motion)을 생각하면 된다. 그런데 왜 갑자기‘확산’인가? 문제 는 이 현상의 주인공인 물 분자의 움직임은 여러 가지 조건에 영향을 받아 다양한 정도로 나타난다는 것이다. 예를 들어 뇌 농양은 DWI에서 강한 신호를 내는데 그 이유는 정상적인 뇌 조직에 있는 물 분자보다 농양을 이루는 농액 내에 있는 물 분 자의 확산이 심하게 제한되기 때문이며, 그로 인해 MR 신호강 도가 증가되는 이유를 다음과 같이 설명할 수 있다.
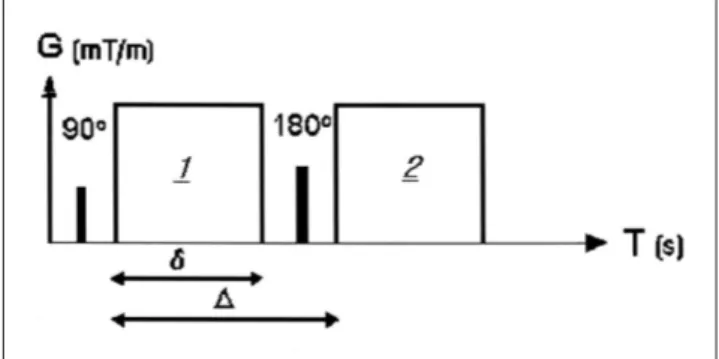
DWI 펄스연쇄(pulse sequence)를 들여다보면 Fig. 3과 같 이 T2WI SE EPI 기법을 근간으로 하고 있음을 알 수 있다.
여기에 확산 현상을 감작(sensitization)하기 위해서 추가적으 로 180도 펄스의 앞과 뒤에 방향이 반대인 확산자계를 걸어준 다(Fig. 3). 확산 현상은 3차원적인 현상이므로 x, y, z의 3방 향으로 같은 확산자계를 걸어서 영상을 얻은 것이 바로 우리 가 보고 있는 등방성(isotropic) DWI이다(20). 만약 인체 내 에서 물 분자의 움직임이 전혀 없는 상태라면, 90도 펄스 후 탈위상(dephasing)되는 스핀들이 이 추가적인 확산자계(Fig.
3에서 1로 표시한 경사자계)에 의해서 더 탈위상 현상이 촉진 되어 다른 위상 값을 가져도, 180도 펄스 후 재위상(rephas- ing)될 때 가해지는 반대 방향의 경사자계(Fig. 3에서 2로 표 시한 경사자계)에 의해서 원래의 위상 값으로 환원되어 확산 자계의 존재에 관계없이 원래의 T2WI의 신호 특성을 유지할 수 있게 된다. 그러나 인체 내에 있는 대부분의 자유 물 분자 (free water molecule)는 정도의 차이는 있을 지라도 확산이 일어나므로, 두 번의 경사자계를 겪고 다시 같은 위상을 유지 한다는 것은 기대하기 어렵다. 다시 말해 그만큼 T2 신호 강 도가 떨어지게 된다. 뇌농양이나 세포독성 부종 등과 같이 확 산 현상이 제한되는 상황에서는 병변의 신호 강도는 큰 변화 가 없는 반면 주변 정상 뇌조직의 심한 T2 신호 감소 때문에 상대적으로 매우 밝게 보이는 것이다.
DWI에서 얻어진 영상 신호의 크기 S와 확산자계를 걸기 전 의 신호 S0와의 관계는 어떤 조직내의 물 분자의 확산 계수를 D, 확산자계의 특정 값 즉, b값을 b라고 할 때 ln(S/S0)=-bD 로 나타낼 수 있다. 물 분자의 확산 계수는 고정된 값이라고 가정할 때, 경사자계의 크기나 경사자계를 사용하는 기간 등 의해서 확산강조의 정도를 조절할 수 있는데 이를 b값으로 나 타내며, b값은 γ를 gyromagnetic ratio, G를 확산자계의 크기, δ를 확산자계를 걸어준 기간, Δ를 두 개의 대칭적인 확산자계 를 걸어주는 시간적 간격으로 표시할 때 γ2G2δ2(Δ-δ/3)에 의
하여 결정된다(Fig. 3). 그러므로 b값은 확산자계의 크기가 클 수록, 기간이 길수록, 두 자계의 시간 간격이 길수록 커진다.
조직의 확산 계수(D)를 알 수는 없으므로, 그 대신 DWI에 서 얻어진 확산 정도를 정량화한 수치를 이용하여 현성확산계 수(apparent diffusion coefficient, ADC)로 표시할 수 있다.
ln(S/S0)=-b(ADC)와의 관계에서 DWI에서의 S와 S0의 관계 를 이용하면 ADC를 계산할 수 있다. 연구에 의하면 물 팬톰 으로 얻은 ADC값이 2013×10-8cm2/s 정도라고 하며 정상 뇌 는 회색질이 760×10-8cm2/s, 백색질은 770×10-8cm2/s정도 라고 한다. 일반적으로 DWI를 시행하면 세 가지 형태의 영상 을 볼 수 있으며, b값이 0인 영상(b=0), 일정한 b값 하에서 얻어진 영상(b=1000, b=2000 등)과 두 영상에서의 값들로 각 화소 별로 구해진 ADC값을 회색조 표시로 나타낸 영상 (ADC map)이다. 각각 b(0) DWI, b(1000) DWI, ADC map 라고 줄여 부른다(20).
대부분의 병변은 DWI에서의 신호 강도만 보고 확산 정도를 평가해도 무리가 없는데, 드물게 T2WI에서 신호강도가 매우 높은 경우에는 확산자계를 경험한 후에도 상당한 T2 신호 강 도가 남아 있어 DWI에서 강한 신호를 보이는 경우가 있다. 이 를 T2 비침(T2-shine through) 효과라고 하며 ADC map을 보기 전에는 정확히 구분하기 어렵다.
초급성기의 경색부의 ADC값을 관찰해보면 병변의 중심부의 경우 대개 300×10-8 cm2/s 내지 500×10-8cm2/s 정도의 값 을 보이는데, 이 ADC값은 많은 요인에 의한 영향을 받기 때 문에 이러한 절대값을 일반화하여 임상에 바로 적용할 수 없 다. 대신 병변의 ADC값을 대칭된 정상 부위의 ADC값으로 나 눈 상대 ADC비(relative ADC, rADC)로 표시하는 것이 일반 적이다.
확산강조영상과 급성 허혈성 뇌경색
DWI는 뇌 허혈에 의해 유발된 세포의 변화를 아주 극적으 로 보여준다. 아직 완전히 밝혀지지는 않았지만 세포독성 부종 으로 그 신호 증가를 설명하고 있다(21). 세포독성 부종은 허 혈에 빠진 뇌 조직이 기능을 상실하면서 신경학적 증상을 유 발함과 동시에, 세포막의 평형을 유지하는데 필수적인 Na+/K+ 펌프의 기능도 멈추게 되며, 그 결과 세포막을 중심으로 이온
Fig. 3. Pulse sequence diagram of DWI. Diffusion-sensitive
gradients are shown as a pair of rectangle located before and
after the 180°refocusing pulse.
경사가 없어져 물이 세포외구역(extracellular compartment) 에서 세포내구역(intracellular compartment)으로 이동하여 발 생한다.
세포독성부종이 자유 물 분자의 확산을 제한하는 기전에 대 해서도 아직 의견이 다양한데, 일차적으로 비교적 물 분자의 운동이 자유롭던 세포외구역 내의 물 분자가 미세구조물들 (microstructures)이 많은 세포내구역으로 이동하여 제한되고, 이차적으로 세포가 부풀면서 세포 사이 사이의 세포외구역을 조밀하게 만들어 세포 내외의 자유 물 분자들의 확산이 더욱 제한되는 것으로 설명하고 있다. 그 외에도 허혈로 인한 국소 적인 조직 온도의 감소, 혈관 폐쇄에 의한 거시적인 움직임 (macroscopic motion)의 제한, 막 투과성의 변화 등도 기여할 것으로 추측하고 있다(22). 동물 실험 결과에 의하면 빠르면 뇌혈관 폐쇄 10분에서 30분 이내에도 조직의 rADC값이 감소 하여 신호 강도의 증가를 보인다. 사람에게서도 빠르면 30분 에서 1시간이면 병변을 관찰할 수 있는 것으로 보고되어 있다.
그렇다면 과연 DWI의 뇌경색 진단율은 얼마나 될까? 보고 자들에 따라 다소 차이가 있기는 하지만 진단정확도를 95%이 상으로 볼 수 있을 것으로 생각된다. 증상 발현 6시간 이내의 환자들을 대상으로 한 연구들을 보면, 놀랍게도 뇌경색 진단의 민감도는 95-100%, 특이도를 100%로 보고하고 있다(23, 24). 또한 DWI는 이러한 높은 진단율과 함께 초기에도 상당 히 명료한 병변을 보여줄 수 있다는 큰 장점이 있다. 그러나 심심치 않게 위음성에 대한 보고도 있으며, 한 연구에서는 5.8%
까지 보고하고 있는데 주로는 뇌간의 작은 병변들이었다. 매우 드물게는 구역성 병변도 위음성을 보이는 경우가 있는데, 이는 DWI변화가 오지 않을 정도의 관류 이상, 또는 -뒤에서 설명 하겠지만- 조기 재개통의 영향으로 검사 전에 이미 ADC 변 화가 있었다가 촬영 시 이미 위정상화(pseudo-normalization) 가 되었기 때문으로 설명하며 대개는 추적 검사 시에는 병변 이 보인다(25). 또한 대표적인 위양성 병변들로는 다음과 같 은 경우가 있다. 급성기 혈종, 뇌농양, 일부의 다발성 경화증 병변, 세포가 조밀하게 구성된 임파종 등과 같은 종양, 헤르페 스성 뇌염과 변형 Creutzfeldt-Jacob병과 같은 감염성 병변 등 이다. 다행히 이러한 병변들은 대개 그 모양이나 양상이 뇌경 색과는 쉽게 구분될 수 있어 크게 진단에 어려움을 초래하지 는 않는다(18, 26, 27).
문제는 임상적으로 급성 뇌경색으로 생각되는 환자가 DWI 상 음성을 보이는 경우인데, 이 때는 반드시 임상적인 소견을 고려하여 판단하여야 한다. 실제 임상증상이 뇌경색과 유사한 질환(예, 편두통, 간질 등)일수도 있겠고, 실제 병변이 존재하 는데도 위음성인 경우도 있을 것이기 때문이다. 특히 뇌간의 작은 병변을 인공물과 혼동하거나 간과하는 경우가 있는데 주 의를 요하며, 매우 초기이거나 허혈의 정도가 경미해서 세포독 성부종을 일으키지 않은 경우도 생각할 수 있겠다. 이 경우 PWI나 MRA 소견을 참고하면 쉽게 진단할 수 있을 것으로 생 각되며, 대개 추적 검사를 해보면 병변이 쉽게 발견된다(22).
b값의 영향
언급하였듯이 b값이란 확산자계의 크기, 부과 시간, 한 쌍의 확산자계를 180도 펄스를 중심으로 걸어주는 시간적 간격 등 에 의해서 결정되는 값으로 그 값이 클수록 전체적으로 T2효 과에 의한 신호들이 감소하여 신호 대 잡음비는 감소하지만 확 산강조 효과는 더 증대되어 뇌경색 진단의 민감도를 증가시킬 수 있다. 일반적으로 b값을 500-700 정도를 기준으로 높고 낮음을 구분(low and high b factors)하는데, 낮은 b값인 b(500)과 높은 b값인 b(1000)으로 각각 같은 환자에서 영상 을 얻어보면 높은 b값으로 얻은 DWI에서 뇌의 정상 회색질/
백색질의 구분이 없어지고 병변이 더 명료하게 나타나는 것을 확인할 수 있다. 그러나 기계적인 제한 때문에 무조건 높은 b 값을 적용할 수는 없으며, 최근 3T MR을 이용할 경우 5000- 7000정도까지 높게 적용할 수 있어 확산텐서영상(diffusion tensor imaging, DTI)를 얻는 데는 큰 장점이 있겠지만 DWI 의 입장에서는 높은 경사자계로 인한 인공물의 영향이 크게 나 타나서 뇌경색 진단에서는 큰 이점이 없지 않을까 생각된다.
그러나 b값 1000과 2000으로 얻은 DWI를 비교한 연구에서 는 높은 b값을 적용했을 때 우려했던 뇌간의 작은 병변의 진 단에도 어려움이 없었으며, 병변의 명료성이 증가되어 실제 병 변을 더 잘 보여주었다고 보고하였다(28). 저자들의 경험에 의 하면 b(1000) 이상이라면 진단에 큰 문제가 없을 것으로 생 각된다.
시간 경과에 따른 DWI 병변의 변화
앞에서도 언급하였지만 허혈에 의한 뇌경색의 진행 과정은 허혈 시간의 경과에 따라서 심화된다. 또한 일단 뇌경색에 빠 진 부위는 허혈성 뇌경색의 자연 경과를 거치게 되며, 허혈로 인한 세포독성 부종의 진행에 의한 세포의 손상과 모세 혈관 기저막의 손상에 따른 혈관성 부종이 발생하면 T2 신호의 증 가가 분명해지며 2-3일에 걸쳐서 점차 부종이 심해지면서 3- 5일에 극에 달한다. 그 이후 점차 부종이 감소하게 된다(Fig.
4A) (29).
이와 같은 시간적 변화는 세포독성부종의 정도의 변화를 반 영하는 ADC값에서도 관찰된다(Fig. 4B). 시간에 따른 ADC값 의 변화가 DWI의 신호 강도의 변화와 거의 대칭적으로 보인 다(이 그림에서는 초급성기의 ADC값의 변화 양상이 생략되 었음). 이러한 시간적 변화의 양상은 뇌경색 패턴에 따라서 다 소의 차이가 있다는 주장(30)도 있지만 일반적으로 초급성기 에 급격하게 ADC가 감소하였다가 점차 완만하게 정상 ADC 로 환원된 이후 다시 정상보다 증가되는 양상을 보인다. 그 과 정을 좀 더 구체적으로 살펴보면, 허혈 시간이 90분 정도 경 과하면서 아주 급속하게 ADC가 감소하는데 그 이후에도 완만 하지만 계속 감소하여 약 18시간 정도 경과할 때 가장 낮아진 다(31). 그 이후는 다시 완만하게 감소되었던 ADC가 증가되 는데 원래의 값으로 환원되어 마치 ADC가 정상처럼 보이는 현상이 발견되며, 바로 앞에서 언급한 ADC의 위정상화 현상 이다. 그 시기는 다양하게 보고되고 있는데 7-10일 정도라고 보면 될 것으로 생각되며 약 2주까지 거의 정상 ADC값을 보 일 수 있다. Fig. 4B에서 rADC값이 1주와 2주 사이에 기준선
을 지나가고 있는 것을 확인할 수 있다. 그러나 3주 이상 지속 적으로 ADC감소가 있는 경우도 있어 다변적일 수 있다는 것 을 염두에 두는 것이 좋겠다. 이 시기를 지나면 ADC는 점차 증가되어 만성 병변의 경우는 뇌척수액과 거의 비슷한 ADC를 보인다.
이러한 병변의 ADC의 시간적 변화는 여러 가지 요인에 의 해서 영향을 받는데, 병변의 크기가 작은 열공성 경색이나 분 수계성 뇌경색(watershed infarction)인 경우, 환자의 나이가 젊은 경우 조금 느리게 진행되는 경향을 보이며, 허혈 시간이 짧은 경우(폐색 혈관의 조기 재개통)는 ADC값이 빨리 정상치 로 회복되는 경향을 보인다(30, 32, 33). 이와 같은 시간적인 변화를 잘 관찰함으로써 발견된 병변의 발생 시기를 추측할 수 있는데 DWI에서의 ADC값을 확인함으로써 급성기 병변도 그 발생 시기를 상당히 정확히 평가할 수 있게 되었다.
DWI의 병변의 크기는 어떤 변화의 과정을 밟을까? 앞에서 언급하였지만 DWI의 신호 강도에는 ADC의 감소와 증가된 T2 신호가 같이 작용한다. 그러므로 혈관성 부종이 진행되는 시기 에는 당연히 DWI에서 증가된 신호를 보이는 영역이 실제 경 색부위보다도 크게 나타날 것이며 반대로 이러한 혈관성 부종 이 서서히 감소하는 경우에는 다시 작아질 것이다. 대개 1주까 지는 넓게 나타나다가 1개월 경까지 서서히 감소하는 양상을 보인다. 그러므로 급성기 DWI 영상에서 관찰할 수 있는 고신 호 강도 영역은 최종경색부위(final infarct area)보다 넓게 나 타난다고 이해하는 것이 좋겠으며, 초급성기의 병변보다 3-5 일 경과하여 얻은 DWI 병변의 범위가 넓다고 그것을 병변이 진행했다고 보는 것은 혈관성부종에 의한 영향을 감안하지 않 은 해석이 될 것이다(34).
DWI상에서의 병변의 가역성(reversibility)
이 의문은 혈전용해술 등 재개통 치료의 대상을 선택함에 있 어 매우 중요한 것이다. 동물실험을 통하여 이에 대한 해답을 얻기 위해 허혈 시간과 ADC값이라는 두 개의 역치에 따른 병 변의 가역성에 관한 연구를 하였다(35-39). 이들 연구를 보 면 30분 이내의 허혈 시간에서 일부가 가역성을 보였고(37), 45분 허혈시간 경과 시에는 혈관 폐색 전 정상 상태에서의 ADC값보다 250×10-8 cm2/s 이상 떨어지면 비가역적이라고 보거나(38), 2시간 허혈 시간에서 550×10-8cm2/s 이하인 경 우는 가역적인 부분이 없었다는 보고를 하고 있다(39). 다시 말해서 이들 일련의 연구의 결과는 허혈에 의한 모든 DWI 이 상은 ADC값이 어떤 역치 이하로 떨어진 상태가 아니라면 조 기 재관류 시에 가역적일 수 있다는 결론을 내릴 수 있게 해 준다.
그러나 이러한 DWI상에서 보이는 ADC 변화가 정상화 되었 다는 것이 과연 신경 손상에서 회복되었다는 것을 의미하는가 는 회의적이다. 최근의 한 연구를 보면 초급성기에 발견된 ADC 변화 부위를 추적 관찰하면 지속적으로 감소되어 있는 경우, 일시적으로 정상화되었다가 다시 감소되는 경우(transient normalization), 일시적으로 감소되었다가 정상화된 후 그대로 지속되는 경우(permanent normalization)를 볼 수 있다고 하 였다(35). 즉, ADC가 일시적으로 정상화되었다 해도 다시 떨 어질 수 있다는 것이다. 더욱이 ADC값이 떨어졌다가 정상화 된 군에서도 조직학적 검사상 정도의 차이는 있었지만 신경손 상을 의미하는 신경세포의 위축과 성상세포(astrocyte)의 부 종이 그래도 관찰되었다고 한다. 이 실험은 30분 허혈 시간 모 델을 대상으로 한 것이기 때문에 그보다 짧은 허혈시간에서는 또 어떤 결과를 보여줄지는 의문이다. 그러나 최소한 우리가 임상적으로 만날 수 있는 초급성기 DWI병변이 세포독성부종 에 의한 신경손상을 의미하는 것이라면 대부분의 병변은 비가
A B
Fig. 4. Chronological changes of the MR signal intensities after an ischemic insult.
A. The change of T2 signals.
B. The change of DWI. The initial rise DWI signal is omitted in this graph. The DWI signal gradually increases for 3-5 days and
then rapidly decreases while the initially decreased ADC gradually increases.
역적이라는 결론을 얻을 수 있다.
여기에서 한 가지 문제가 되는 것은 어느 정도의 신호 강도 의 변화를 유의한 변화로 볼 것이냐는 것이다. 실제 구역성 뇌 경색의 경우 구분이 되지 않거나 아주 미미한 정도의 신호 강 도의 증가만 보이는 경우도 있으며, 적용한 b값의 크기에 따라 서도 그 명료함이 달라질 수 있어 정확히 병변을 구분하는 것 이 매우 어려운 경우도 종종 있다. 그래도 조금은 실용적인 결 론을 내려본다면‘DWI상 명료하게 변화를 보인 병변은 비가 역적이다’라고 할 수 있겠다.
DWI 소견과 임상적 결과
DWI 소견으로 임상적인 결과와 예후를 예측하는데 많은 도 움을 받을 수 있다(18). 그러나 병변의 크기가 임상 증상의 경 중을 그대로 반영하는 것은 아니다. 예를 들어 작은 병변이라 도 병변의 위치에 따라 때로는 심한 증상을 유발할 수도 있기 때문이다. 일반적으로 구역성 뇌경색의 경우 병변이 클수록 임 상 증상도 심하고, 병변 자체에 의한 이차적인 변화도 심하게 나타나므로 예후가 나쁘다고 할 수 있다. ADC값이 낮을수록 최종 기능적 결과가 더 나쁘다는 보고도 있는데 이에 대해서 는 이견이 많다(40, 41).
일과성 허혈 발작의 개념의 변화
전통적으로 일과성 허혈성 발작(transient ischemic attack, TIA)이라 함은‘갑자기 생긴 혈관성 기원의 증상으로 24시간 이내에 뇌신경학적 증상이 회복되는 것’으로 정의하고 있다.
그러나 임상적으로는 분명히 TIA의 기준에 맞는 환자임에도 불구하고, CT로 그 일시적이었던 증상을 설명할 수 있는 병변 이 있는 경우가 15-20%정도에서 볼 수 있어 이를‘cerebral infarction with transient signs’라고 정의하기도 하였다(42).
이런 현상은 DWI 시대에는 훨씬 더 그 빈도가 증가하였다.
Kidwell등의 보고에 의하면 TIA환자의 48%에서 증상을 설명 할 수 있는 분명한 병변을 발견할 수 있었다고 한다(43).
TIA는 최종 뇌경색의 위험성을 경고하는 임상적 개념의 중 요성도 있지만, 이와 같이 영상 검사에서 병변이 있을 수 있다 는 것은, 일과성의 허혈 상태로 끝난 것이 아니라 이미 뇌경색 이 온 상태임을 의미하므로 더욱 적극적인 대처가 필요함을 뜻 한다고 하겠다. 최근 한 그룹에서는 TIA의 정의를 더 좁혀서 1시간 이내로 지속된 국소적 뇌 또는 망막 증상으로 급성 뇌 경색의 증거가 없는 상태로 정의하자고 제안하였다(44). 새로 운 영상 기법의 발전이 마치 확고부동할 것처럼 보였던 개념 을 뒤흔들 수도 있다는 것을 잘 보여주는 예라고 할 수 있겠 다.
MR 관류영상
4P 중에서도 가장 중요하게 생각되는 허혈 반영대의 의미를 앞 부분에서 잠시 살펴보았었는데, 현재의 검사 방법 중 가장 정확하게 이 영역의 존재와 크기를 알 수 있는 것은 PET(positron emission tomography)이다. 그러나 이 방법은 현실적으로 초급성기에 시행한다는 것은 거의 불가능한 상황
이며, 그 외에도 교과서에는 Xe-CT 관류영상이 언급되어 있 고 SPECT도 매우 정확한 정보를 제공할 수 있다고 하지만 역 시 급성기에 실시하기는 제약이 많다(45). 그런데 다행히 DWI 가 이미 막강한 역할을 하고 있는 MR로도 관류영상이 가능하 다. MR PWI는 핵의학 검사보다 더 해상도와 대조도가 높고, CT를 이용한 방법보다 다면 영상 획득(multi-slice image acquisition)이 가능하여 전체 뇌관류 상태를 한꺼번에 볼 수 있고, 동시에 DWI-PWI를 얻음으로써 매우 유용한 정보를 제 공할 수 있다는 큰 장점이 있다.
DWI-PWI를 동시에 얻을 수 있다는 것은, 많은 가정이 필 요하긴 하지만, 우리가 재개통 치료의 대상으로 삼고 있는 허 혈 반영대 즉 허혈 위험 조직(tissue at risk)를 보여줄 수 있 다는 뜻을 내포한다(9, 46). 많은 연구에서 PWI에서 보이는 관류 이상 부위가 DWI 병변보다 넓은 경우 추적 시에 DWI 이 상 부위가 더 넓어지며, 만약 관류 이상 부위가 DWI 이상 부 위와 비슷하거나 좁은 경우에는 병변이 진행하지 않는다는 것 을 발견했다는 것이 이론적 근거를 떠나 이러한 가정을 잘 뒷 받침해주고 있다. 즉, 앞에서 충분히 설명하였듯이 허혈 반영 대 속의 허혈 중심부는 임상적으로는 DWI에서 보이는 영역으 로 간주해도 크게 틀리지 않을 것이며, 앞으로 설명할 PWI는 허혈 중심부 외에도 그 주변의 허혈 반영대를 포함하는 유의 한 관류 이상 영역을 보여 줄 수 있을 것이라는 것이다.
MR을 이용하여 조직의 관류를 영상화하는 방법은 여러 가 지가 있다(47). 가장 대표적인 방법이 역동적 조영증강 자화 율 강조 관류 영상(dynamic contrast-enhanced susceptibil- ity-weighted perfusion imaging)이라고 해서 가돌리늄 (gadolinium)과 같은 상자성 MR 조영제가 농도에 따라 자화 율에 변화를 주어 T2이완시간 단축의 효과를 가지는 성질을 이용하여 역동적 영상을 얻는 방법이다. 가돌리늄 외에 추적자 (tracer)로 사용할 수 있는 조영제는 SPIO등 다양하며, van Zijl 등은 fMRI에서와 같이 헤모글로빈을 추적자로 사용한 방법을 제시했고(48), 최근에 관심을 받고 있는 연속적 동맥내 스핀 표지법(continuous arterial spin labeling, CASL)도 혈액 내에 있는 스핀을 특수한 RF 펄스로 변형시켜 하나의 추적자로 사 용하는 방법이다(47). 그러나 CASL은 표지를 하는 부위와 영 상을 얻는 부위 사이의 통과 시간이 길어 스핀 표지의 감쇄가 일어나는 현상과 낮은 SNR, 긴 영상 획득 시간 등으로 인한 제약 때문에 아직 보편적인 방법으로 사용되고 있지는 못하다.
역사적으로 보면 뇌혈류를 측정하기 위한 시도는 1948년 Kety 등이 확산성 추적자인 산화질소(nitrous oxide, NO)를 이용한 NO 법이 최초였는데, NO의 경동맥 혈액내 농도와 경 정맥 혈액내 농도를 통해서 국소 뇌혈류량을 측정하였다. 그 이후 임상 및 연구 목적으로 비교적 많이 사용되었던 방법이 xenon-133을 추적자로 이용하여 방사능을 외부에서 방사능 을 측정하는 방법이었다. Xenon도 역시 확산성 추적자 중의 하나이며 기체의 농도와 CT영상밀도의 감소가 비례적이라는 데 착안한 Xenon CT법은 안정적 xenon(stable xenon)을 이 용해서도 할 수 있는 방법으로 아주 정확한 비침습적인 검사 법으로 인정되나 기체를 흡입하는 특수한 장치가 필요하고 불
편한 단점이 있어 역시 초급성기에 적용하기에는 어려움이 있 다 (45). 이와 같이 뇌혈류를 측정하는 데는 크게 확산성 추적 자 (diffusible tracer: 조직 내로 확산할 수 있는 추적자로 조 직의 관류 상태를 더 잘 반영한다)와 비확산성 추적자(non- diffusible tracer: 조직 내로 확산해서 들어가지 못하고 혈관 내에만 존재하는 추적자로 혈관내 추적자라고도 부른다)를 이 용한 방법이 있다.
주지하다시피 가돌리늄은 혈액-뇌 장벽(blood-brain bar- rier, BBB)을 통과하지 못하는 비확산성 추적자여서 조직의 관 류 상태를 정확히 반영할 수 없다는 문제점이 있는데, 다행히 혈관 내에 존재하는 이 조영제에 의한 자화율 증가 효과는 인 접한 조직의 이완 정도에 충분히 영향을 미칠 수 있어 유용한 추적자로 사용할 수 있다. 그럼에도 불구하고 여전히 중요한 시간-농도 곡선(time-concentration curve)을 바로 얻을 수 없다는 것이 큰 단점으로 남는다(47). BBB가 파괴된 상태에 서는 얻어진 시간-농도 곡선이 부정확할 수 있다는 단점도 지 적되었는데 이는 다행히 급성 뇌경색의 경우 대개는 BBB 파 괴가 발생하기 전이므로 큰 문제가 되지는 않을 것으로 생각 된다(46).
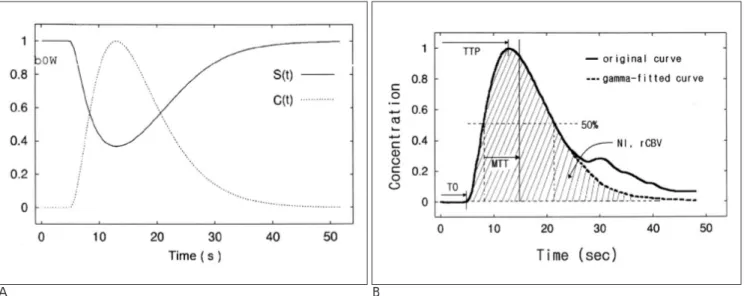
조영제를 주입하면서 역동적으로 얻은 영상에서 얻어진 시 간-신호 강도 곡선에서 시간-농도 곡선을 얻기 위해서는 많 은 가정하에서 이루어진 실험과 수학적 계산이 필요하였는데, Fig. 5A로 그 두 곡선의 관계를 결론지을 수 있으며 구체적인 과정은 생략하기로 한다(47). 요점은 관심 영역의 뇌조직에 ROI를 두고 역동적으로 얻은 일련의 GRE EPI영상의 신호강 도는 그 조직을 지나가는 조영제의 농도를 반영한다는 것이다 (49). 여기서는 가돌리늄이 소위 음성 조영(negative contrast) 효과를 내므로 신호강도와 조영제의 농도는 역비례하는 관계 를 취한다(Fig. 1F, 5A).
MR 관류 영상 획득의 실제 방법
앞에서 언급한 바와 같이 기본적으로 가돌리늄 조영제의 자 화율 효과(susceptibility)를 가장 민감하게 영상화하려면 T2*
강조가 매우 중요하다. 당연히 여기에는 SE보다는 GRE가 훨 씬 유리하다. SPGR(short SPoiled GRadient Acquisition in a Steady State)이나 FLASH(Fast Low Angle SHot)와 같은 고 속 GRE를 이용하여 하나의 단면만을 선택할 수 밖에 없는 제 한이 있지만 1-3초 간격으로 역동적 영상 획득이 가능하다 (49). 여기서 EPI가 또 한 번의 위력을 발휘하는데, 단발(sin- gle-shot) GRE EPI를 이용하면 7-10개 정도의 단면을 2초 간격(TR=2000 ms)으로 한 번 스캔 할 때 마다 동시에 얻을 수 있어 병변 부위를 충분히 포함하여 넓은 범위를 동시에 검 사할 수 있다.
이와 같이 스캔이 반복적으로 이루어지고 있는 동안 전주정 맥으로 18-16G의 큰 바늘을 이용하여 가돌리늄 조영제를 0.1 mmol/kg의 용량으로 초당 3-5 ml의 속도로 주입한다. 이때 일시 주사(bolus injection)가 잘 되는 것이 매우 중요하므로 바로 10-20 ml의 식염수를 급속히 주입하여 조영제 덩어리 (bolus)를 밀어주어야 한다. 조영제 주입 전, 주입 중, 주입 후 전 과정을 80초에 걸쳐서 역동적 영상을 얻는데 만약 10단면 을 선택하여 스캔 하였다면 총 400장의 영상을 얻을 수 있다.
Fig. 1E는 그 400장의 영상 중에서 대표적인 10장을 뽑아 서 시간별 조영 효과를 보여주고 있다. 조영제의 농도가 최고 에 달하는 지점(peak)에서 영상의 신호강도가 매우 떨어지는 것이 잘 나타난다. 좌중뇌동맥의 폐색이 있는 환자인데 우뇌 반구가 시간이 지나면서 조영제의 농도 증가와 함께 검게 되 었다가 빠져나가는 동안 다시 원래의 뇌조직 신호를 회복하는 정상적인 과정을 보여주는 반면(Fig. 1G의 1 지역에 해당), 좌 뇌 반구는 이미 경색이 분명하게 와 있는 부분은 전 과정 동 안 거의 조영제의 유입이 없어 신호 강도의 변화를 보이지 않
A B
Fig. 5. A. The relationship of a time-signal intensity curve and a time-concentration curve.
B. The dotted-line was obtained after gamma-variate fitting of the original time-concentration curve which was drawn in a solid
line. T0: arrival time, TTP: time to peak, MTT: mean transit time, NI: negative integral, rCBV: relative cerebral blood volume.
고 있으며(2 지역에 해당), 그 바로 뒤 부분에는 DWI 변화는 없지만 허혈 상태인 곳으로 조영제가 유입되어 최고점에 이르 렀다가 다시 유출되는 과정이 매우 느리게 지연되어 일어나는 것을 보여주고 있다(3 지역에 해당). 그래프를 보면 그 정도 를 한 눈에 확인할 수 있다(Fig. 1F).
이와 같이 눈으로 어느 정도 관류 이상 부위를 짐작할 수 있 겠으나 개관적인 평가를 위해서는 후처리 과정이 필요하다. 후 처리는 각 화소별 시간-신호강도 곡선(time-signal intensity curve)을 얻는 것에서부터 시작된다. 언급하였듯이 신호강도 의 감소 정도가 조영제의 농도와 비례한다는 것을 상기하면 Fig. 5B와 같은 의미임을 알 수 있으며 이때는 시간-농도 곡 선이 된다. 그림에서 굵은 색으로 표시된 곡선의 뒤 부분이 첫 번째 통과(first pass) 후 재순환된(recirculated) 조영제를 의 미하는 부분이며 점선부분은 이를 gamma variate fitting이라 는 수학적인 방법으로 보정한 것이다. 각 EPI 영상은 128×
128 매트릭스 크기로 얻으며 각 화소별로 상기의 그래프를 얻 어서 각종 파라미터들에 따른 다양한 지도(map)를 얻을 수 있 다(Fig. 1G-I) (45).
시간-신호강도(농도) 곡선의 해석과 관류 관련 파라미터들 Fig. 5B에서 보는 곡선의 꼭지점은 조영제의 최고 농도 도 달점을 의미하며, 그 진폭이 클수록, 곡선의 폭이 좁을수록 조 영제의 덩어리 주입이 아주 이상적으로 되었음을 의미한다.
뇌조직의 입장에서 보았을 때 조영제가 들어오고(wash in) 최고 농도에 이르렀다가(peak) 다시 빠져나가는(wash out) 과정(transit)을 밟는다고 보았을 때(Fig. 1E), 조영제 주입 후 일정한 시간이 지나 곡선에서의 꼭지점(peak)에 도달하는 시 간까지를 유입 부분(wash-in component)으로 표현할 수 있 으며 이는 혈관의 폐색에 매우 민감하게 변화를 보인다. 다시 말해 혈관이 막히거나, 측부혈행 등으로 느려져 있는 경우 그 꼭지점까지의 도달 시간이 길어져 곡선이 완만하게 그려진다.
아래 그림에서 T0(time to arrival)과 TTP(time to peak)가 이를 반영한 값들이며 정상보다 길어지면 허혈 상태를 시사하 는 것으로 되어 있다(Fig. 5B). 그러나 얼마나 길어지면 유의 한 허혈인지에 관한 연구는 아직 해답을 내고 있지 못하다.
언급하였듯이 정맥 주입된 조영제를 아무리 덩어리로 주었 다고 해도 주입하는 동안 지연되는 3-5초 가량의 시간과 조 영제가 혈관과 폐, 심장 순환을 돌면서 분산(dispersion)되는 것은 MR 관류 영상의 또 하나의 한계이기는 하지만 이러한 효 과를 감안하고 그래프를 보면 나름대로 의미 있는 평균통과시 간(mean transit time, MTT)을 얻을 수 있다. 잘 알고 있는 FWHM(full width half maximum)방법을 적용하면 왜 MTT 를 측정하는데 꼭지점까지의 시간이 아니라 그 보다 조금 지 난 시간까지 표시되는지 알 수 있다. 그래프의 유입 부분과 유 출 부분을 잘 비교해보면 서로 대칭되지 않고 유출 부분이 조 금 더 완만해서 50%농도로 내려가는데 걸리는 시간이 조금 더 걸림을 알 수 있다. 그러므로 Fig. 5B를 보면 점선으로 표시된 사각형의 반을 나누는 선까지의 시간이 바로 MTT에 해당된 다. 그 평균 시간을 얻으면 농도의 꼭지점에 이르는 시간보다
약간 늦다는 것을 이해할 수 있다.
또한 이 그래프를 보면 기준선(baseline)과 곡선 사이에 일 정한 면적(빗금 친 영역 전체)이 발생되는 것을 알 수 있다.
이는 곡선의 기울기를 적분한 값으로 한 복셀을 일정한 시간 동안 지나가는 조영제의 총량이라고 볼 때 그 복셀의 뇌혈용 적(cerebral blood volume, CBV)에 비례한다고 볼 수 있다. 동 맥투입함수를 알지 못하는 상태에서는 비례 상수를 구할 수 없 으므로 상대뇌혈용적(relative CBV, rCBV)이라고 한다. 후처 리 프로그램 (GE; Functool ver. 4.1)에 따라 negative enhancement integral이라고 부르는 경우도 있는데 설명한 내 용이 함축적으로 잘 표현된 용어라고 생각된다.
동맥투입함수(arterial input function, AIF)
앞에서 언급한 각종 파라미터들을 잘 이해하고 분석함으로 써 초급성기의 허혈의 상태를 평가하는데 큰 도움을 받을 수 있다. 그러나 앞에서 우리가 얻은 곡선으로 얻은 몇 개의 파라 미터들은 현실적으로 불가능한 조영제의 일시 주입이 완벽하 게 잘 되었다는 가정하에서 구한 것들이다. 이 문제를 해결하 기 위한 한 방편이 바로 AIF를 구하는 것이다. AIF란 대상 뇌 조직의 영양동맥의 시간-농도 곡선에 해당되는 값이다. 이 방 법을 잘 적용하면 MR 관류 영상의 객관성을 상당히 높일 수 있다.
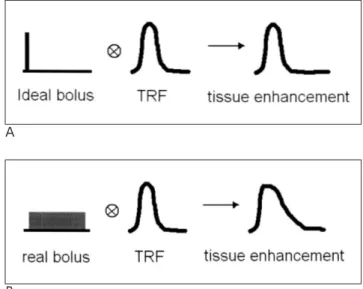
먼저 생소한 수학적 용어인 convolution과 deconvolution을 이해할 필요가 있다. Convolution을 의미하는 연산기호는 ⓧ 이다. Fig. 6A를 보면 아주 이상적인 조영제 bolus의 함수를
A
B
Fig. 6. A schema explaining the concept of convolution and de-
convolution of the contrast bolus and tissue reserve function for obtaining the tissue residue function.
A. Convolution of the ideal bolus and tissue reserve function
results in a tissue enhancement curve.
B. The same is true for the real bolus, which means arterial in-
put function (AIF). AIF is a time-concentration curve of a cer-
tain feeding artery. We can get a tissue reserve function by the
deconvolution of the tissue enhancement curve with the AIF.
대상 뇌조직 자체가 가진 잔여 함수(tissue residue function, TRF)와 convolution하는 과정을 보여주는데, 그 결과가 바로 우리가 MR을 이용하여 얻은 대상 조직의 시간-농도 곡선(그 림에서는 tissue enhancement curve)이 된다. 이를 거꾸로 말 하면 시간-농도 곡선을 조영제 주입 함수(contrast bolus function)로 다시 deconvolution하면 조직 잔여 함수를 알 수 있다는 뜻이다. 이들 값들을 우리가 얻을 수 있는 값들과 비교 하면 Fig. 6B에서와 같이 조직의 시간-농도 곡선(그림에서는 tissue enhancement curve)에 해당되는 것이 MR을 통해 얻 은 시간-신호 강도 곡선에 해당하며, 조영제 주입 함수(그림 에서는 real bolus)가 AIF에 해당하므로 이 시간-신호강도 곡 선 함수를 AIF로 deconvolution하면 우리가 알고자 하는 대상 뇌조직의 잔여 함수를 얻을 수 있다. 이 조직 잔여 함수를 아 는 것이 중요한 이유는 이 함수 곡선의 first moment를 통해 MTT를 추출할 수 있기 때문이다. rCBV는 곡선 아래 면적을 적분하는 방법(area under the curve)을 통해 쉽게 구할 수 있으므로 MTT를 정확히 알 수 있다면, 소위 중심체적정리 (central volume theorem: CBF=CBV/ MTT)을 이용하여 뇌 혈류량(cerebral blood flow, CBF)를 정확히 구할 수 있다.
그러나 이를 임상 적용하는 데에는 다소 문제가 있다. 왜냐 하면 아직 어느 혈관을 대상으로 AIF를 구하는 것이 가장 정 확한가에 대한 해답이 없고, 가장 유용하게 사용할 수 있는 중 뇌동맥 근위부의 경우 혈관을 잘 확인하기 어렵다거나 ROI를 정확히 둘 수 없는 점과 MR의 이완율과 조영제 농도간의 관 계가 비선형적인 점 등 실용적으로 여러 가지 제약이 있어 제 한적으로 사용되고 있는 실정이며, 실용적인 방법을 찾기 위한 많은 노력이 행해지고 있다(47, 50, 51).
PWI를 본격적으로 시행하고 있는 기관 중에도 AIF를 구해 서 이용하는 곳이 있고 그렇지 않은 곳이 있는데, 어떤 방법을 사용하든 MR PWI를 통해 얻어진 각종 map의 의미를 해석할 때는 비록 이러한 값들이 정량적인 자료를 얻기 위한 노력을 통해서 얻어졌지만, 아직까지는 어떤 절대적인 값에 의미를 둘 것이 아니라 정상 부위와 비교한 상대적인 값으로 해석에 임 하는 것이 오류를 줄이는 길이라고 생각된다.
MR관류영상의 임상 적용과 다양한 파라미터 지도의 해석 초급성기 허혈성 뇌경색 환자의 치료 방침 결정의 중요한 도 구로서의 MR이 진가를 발휘하기 위해서는 신속히 유용한 정 보를 제공할 수 있어야 할 것이다. 그러므로 복잡한 방법보다 는 손쉽게 바로 얻을 수 있는 정보가 훨씬 도움이 될 수 있겠 으며 검사와 동시에 바로 후처리 과정을 거쳐 관류 상태를 평 가할 수 있어야겠다. 경색부위는 이미 DWI를 이용하여 알았 고, MR 혈관조영술로 폐색 혈관도 확인 가능하며, 남은 것은 허혈 부위의 범위가 얼마나 되는지 측부혈행은 얼마나 발달되 어 있는지, 허혈의 정도가 얼마나 심한지 등을 알 수 있는 관 류 상태에 관한 정보를 얻는 것이다.
MTT map은 매우 예민하게 관류 이상을 보여줄 수 있다 (Fig. 1G). 실제 임상적으로 매우 폭 넓게 사용되고 있고 연구 목적으로도 가장 널리 사용되는 지표인데, 그 이유는 map의
특성상 관류 이상 영역을 아주 명확하게 보여주기 때문에 측 정이 용이하여 객관성이 높다는 큰 장점이 있기 때문이다. 그 러나 측부혈행에 의한 지연된 조영증강이 있는 경우에도 map 의 특성상 비정상적으로 나타나므로 병변의 범위를 과장하는 경향이 있음을 명심하여야 한다. 대개는 최종 병변과 비교할 때 MTT map에서의 병변의 크기가 크다. 또한 근위부 경동맥 이나 중뇌동맥 등에 현재의 병변과 관련 없이 만성적인 폐색 이나 협착이 있는 경우에는 증상이 없는 쪽의 MTT도 협착 때 문에 동시에 지연되어 마치 MTT의 차이가 없는 것으로 오인 할 수 있으며, 증상이 있는 쪽에 이러한 병변이 있는 경우에는 실제보다 과장되어 MTT 지연 소견이 보일 수 있으므로 이 map을 분석할 때는 미리 이러한 상황을 염두에 두고 있어야 한다.
Fig. 1G의 정확한 해석을 위해서는 전체를 세 부분으로 나 누어서 보아야 할 것이다. 좌중뇌동맥 영역 외의 파란색 계열 로 표시된 부분(1 지역)이 정상적인 관류 상태를 보여준다.
Fig. 1F의 시간-신호강도 곡선들 중에서 곡선 1에 해당된다.
좌중뇌동맥 영역 중에서도 뒤 쪽의 초록색 계열로 나타난 부 분 (3 지역)이 관류 시간이 다소 느려진 부분이며 측부혈행의 존재를 시사한다. 시간-신호강도 곡선에서 곡선 3에 해당하는 부분이며 앞의 곡선 1과 비교할 때 약 3-4초 정도 지연된 형 태를 보여준다. 반면 전두부 쪽에는 붉은 색 계통으로 표시된 지역 (2 지역)이 있으며, 이 부분은 정상적인 관류뿐만 아니라 측부혈행도 거의 없는 부위이다. 시간-신호강도 곡선에서 시 간 경과에 따라 거의 신호강도의 변화가 없는 곡선 2에 해당 하는 병변이며 DWI에서 매우 밝은 신호강도를 보이는 부분과 거의 일치하는 것을 알 수 있다. DWI 병변과 비교할 때 초록 색으로 표시된 부분이 허혈 반영대에 해당되는 것으로 생각할 수 있으며 실제보다는 다소 넓게 표시된 상태라고 이해하면 될 것으로 생각된다.
CBV map은 측부혈행을 아주 잘 반영하며, 최종경색범위와 상당히 일치율이 높은 것으로 알려져 있다(Fig. 1H) (51). 특 히 MTT map과 거의 일치하여 CBV map의 이상이 보인다면 그 부위(2 지역에 해당)는 유의한 측부혈행이 없는 상태로 볼 수 있으며 모두 최종경색을 초래할 것을 예측할 수 있다. 반대 로, MTT map에서의 병변 부위가 CBV map에서는 관류가 정 상 또는 오히려 증가된 것으로 나타난다면 그것은 측부혈행이 잘 발달되어 있다는 것을 의미하며, 때로는 이미 재개통 된 경 우를 의미하기도 한다. MRA 소견이 이 두 경우의 감별에 이 용될 수 있다. 이 환자의 경우는 3 지역이 그럴 가능성이 매우 높은 부분이다. 만약 MRA에서 혈관의 폐색이 보인다면, 재관 류 시에 구제가 가능한 허혈 반영대로 생각되며 만약 재관류 에 실패하였다고 해도 뇌경색은 국소적으로 발생할 가능성이 높은 경우로 생각할 수 있다(52).
CBF map(Fig. 1I)은 만약 절대값을 정확히 구할 수만 있다 면 가장 유용한 파라미터가 되겠지만, 현실적으로 각 복셀의 CBV값을 MTT값으로 나눈 값에 불과하기 때문에 큰 의미를 두기 어렵다. AIF를 통해서 CBF를 구한 경우에는 최종경색부 위를 가장 잘 반영한다고 알려져 있다(53, 54). 이 환자의 경
우는 3 지역 중에서도 중심 부분의 2 지역 근처가 관류 상태 가 더 감소되어 있는 것으로 보여 재관류에 실패한다면 그 부 분이 경색이 진행될 가능성이 높을 것으로 보이며, 실제 추적 검사에서 DWI 이상이 발견되었다(Fig. 2A).
이와 같이 상대적인 map의 형태를 보고 조직 생존력(tis- sue viability)이나 최종경색부위를 예측하고자 하는 시도와 함 께 어떤 한계치(threshold)를 구해서 관류 이상부위의 운명을 예측하기 위한 노력도 이루어져 왔다. SPECT를 이용한 한 연 구는 rCBF=0.70를 주장했고(55), CT관류 영상을 이용한 연 구는 rCBF=0.48, rCBV=0.60를 제시했으며(56), MR관류 영 상을 이용한 연구는 rCBF=0.48, rCBV=0.87을 주장하였다 (57).
이러한 문제점에다가 최근 한 연구에서 DWI-PWI 불일치 정도 평가의 신뢰성을 검토하여 보았더니 시각적으로 어림해 서 계산하였을 때(visual assessment)는 물론이고 손으로 그 려서 계산했을 때(hand-drawn assessment)도 검사자간의 차 이가 심하여 신뢰성에 큰 의문을 제시하였다(58).
이와 같이 현재까지 많은 연구가 이루어지고 있음에도 불구 하고 아직 가장 신뢰할 만한 방법이 제시되고 있지 못하고 기 관별로 자체적으로 나름대로의 기준을 적용하고 있는 것은 MR PWI를 정확히 얻고, 그 소견을 정확히 해석하는 것이 어렵다 는 것을 의미할 뿐만 아니라 기관별로 영상을 얻는 방법, 얻어 진 자료를 후처리 하고 해석하는 방법이 제각각 이기도 한 데 원인이 있다고 생각된다. 핵의학적 여러 검사, CT 관류 검사, MR PWI 등의 표준의 필요성 때문에 최근 미국심장협회 (American Heart Association, AHA)에서는 이에 대한 지침 을 만들었다(59).
MR 혈관조영술
MR을 이용한 혈관조영술은 이미 널리 임상에 이용되어 왔 다. 초급성 뇌경색의 경우에도 어느 혈관에 협착/폐색이 왔는 지 매우 신속하게 알 수 있어 매우 유용한 검사라고 생각된다.
두개내 동맥은 3D TOF 기법을 이용하며, 검사 시간의 단축을 위해 윌리스 환을 중심으로 근위부 혈관만 확인하는 정도로 펄 스연쇄를 구성하는 것이 좋으며, 좋은 영상을 얻기 위해 검사 시간을 길게 해도 많은 경우 환자가 협조적이지 않아 좋은 영 상을 얻기 힘들다. 대신 신속하게 영상을 얻을 수 있는 CE- MRA를 시행할 수도 있다. 이 방법은 경부의 큰 혈관들에 대 한 검사를 신속하게 할 수 있다는 장점도 있어 TOF 기법에 부 가적으로 시행하면 도움이 될 것으로 생각된다.
T2 WI 또는 FLAIR 영상
이 둘 중의 하나는 반드시 검사에 포함시키는 것이 좋다. 왜 냐하면 과거 병변 여부를 알 수 있고, DWI에서 발견된 급성 병변의 진행 여부에 대한 추가적인 정보를 제공해줄 수 있기 때문이다. 허혈 반영대가 존재하여 재개통 요법을 결정한 환자 라 할지라도 허혈 중심부가 이미 혈관성 부종을 의미하는 T2 신호의 변화를 보인다면 재개통으로 인한 손상(reperfusion injury)이 심각할 수 있기 때문이다.
FLAIR 영상은 앞에서도 언급하였지만 T2 신호 변화를 좀 더 명확하게 보여줄 수 있는 장점이 있으므로 많은 기관에서 프로토콜에 포함시키고 있다(16, 60, 61). Toyoda 등은 그 외 에도 느려진 피질 혈관 신호가 상황에 따라 다양하게 보이는 것에 대해 착안하여, 혈관 폐색이 있으면서도 이러한 혈관 신 호가 보이지 않는 경우는 측부혈행이 잘 발달되지 않은 것으 로 의미하며 경색으로 진행된다고 하였고, 혈관 신호가 보이는 경우는 최종경색영역은 DWI병변 영역과 혈관 신호를 보이는 영역의 중간 정도가 된다고 하였다(61). 그러한 FLAIR 영사 의 단점으로 지적할 수 있는 것은 영상획득 시간이 FSE기법 으로 얻는 T2WI보다 상당히 길다는 것인데, 최근의 감도 부 호화 기법(sensitivity-encoding method, SENSE)과 같은 병 렬 영상 기법을 추가로 적용하면 어느 정도 보완될 수 있을 것 이다 (62).
경사에코영상과 미세출혈(microbleeds)
초기에 MR을 이용한 허혈성 뇌경색 환자의 평가가 문제가 있다고 지적된 이유 중의 하나가 MR은 CT보다 출혈을 잘 보 여주지 못한다는 것이었다(63). 실제 뇌경색 환자의 치료 방 침을 결정함에 있어 출혈 여부는 매우 중요한 문제이므로 충 분히 타당성이 있는 주장이라고 생각할 수 있다. 특히 혈전용 해술을 시행할 환자의 경우 출혈이 동반되어 있다면 그 결과 는 혈전용해술을 하지 않은 것보다 훨씬 나쁠 수 있으므로 출 혈의 진단은 무엇보다고 중요하다.
급성 혈종은 MR상, T1WI에서는 뇌실질과 등강도로 보이고, T2WI에서는 고신호 강도로 보이는데 변연부의 탈산소헤모글 로빈(deoxyhemoglobin, deoxyHb)의 높은 자화율에 의한 영 향으로 테두리에 검은 띠를 보인다(64). 그러나 이러한 소견 들이 불분명한 경우가 많고 혈종의 크기에 따라 다양하게 보 일 수 있어 CT와 비교할 때 진단율이 현저히 낮다. 그러나 자 화율에 대한 감수성이 높은 GRE에서는 그 검은 띠가 더 분명 하게 보여 쉽게 출혈을 진단할 수 있다. 실제 일부 보고에서는 CT보다도 더 예민하게 출혈을 찾아내는 것으로 되어 있다 (65).
최근에 관심사로 떠오르고 있는 미세출혈은 CT상에서는 대 부분 보이지 않으며 GRE에서는 아주 민감하게 관찰된다. 최 근의 일련의 보고에 의하면 이러한 미세출혈이 있는 경우 무 증상의 과거병변일지라도 혈전용해술에 의한 출혈성 합병증 발 생의 빈도가 높아진다고 하므로 GRE의 중요성은 매우 크다고 볼 수 있으며, von Kummer도 GRE를 포함한 MR이 혈전용해 술을 계획하는 경우에는 최적검사(modality of choice)라고 주 장하고 있다(66-68). 문제는 이러한 미세출혈의 빈도가 낮지 않고, 환자에 따라서는 수효의 차이가 크기 때문에 모든 미세 출혈 동반 환자를 혈전용해술의 비적응으로 해야 할 지에 대 해서는 의문이 제기되고 있으며, 향후 이에 대한 연구가 필요 할 것으로 생각된다.
문제는 GRE영상을 얻기 위해서는 추가적으로 2-3분간의 영상 획득 시간이 소요된다는 것인데 분 초를 다투는 상황에 서는 단점이 될 수 있다. 이를 해결하기 위해 DWI가 SE이기