원고 접수일 2012년 8월 28일, 원고 수정일 2012년 10월 4일, 게재 확정일 2012년 11월 27일
책임저자 지영덕
(435-805) 군포시 산본로 321, 원광대학교 산본치과병원 구강악안면외과 Tel: 031-390-2875, Fax: 031-390-2777, E-mail: [email protected]
RECEIVED August 28, 2012, REVISED October 4, 2012, ACCEPTED November 27, 2012
Correspondence to Young-Deok Chee
Department of Oral and Maxillofacial Surgery, Wonkwang University Sanbon Hospital
321, Sanbon-ro, Gunpo 435-805, Korea
Tel: 82-31-390-2875, Fax: 82-31-390-2777, E-mail: [email protected]
CC This is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/
by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
골유도재생술과 동시에 식립한 임플란트의 변연골 흡수량에 대한 후향적 고찰
박슬지ㆍ선화경ㆍ고세욱ㆍ지영덕
원광대학교 치과대학 구강악안면외과학교실
Abstract
Retrospective Clinical Study on Marginal Bone Loss of Implants with Guided Bone Regeneration
Seul-Ji Park, Hwa-Gyeong Seon, Se-Wook Koh, Young-Deok Chee
Department of Oral and Maxillofacial Surgery, College of Dentistry, Wonkwang UniversityPurpose: The purpose of this study was to evaluate marginal bone loss of the alveolar crest on implants with or without guided bone regeneration and variables that have influenced.
Methods: The clinical evaluation were performed for survival rate and marginal bone loss of 161 endosseous implants installed with guided bone regeneration (GBR) in 83 patients from September 2009 to October 2010 in relation to sex and age of patients, position of implant, implant system, length and diameter of implant. Study group (n=42) implant with GBR procedure, control group (n=41) implant without GBR technique. Simultaneous GBR approach using resorbable membranes combined with autogenous bone graft or freeze-dried bone allograft or combination. Radiographic examinations were conducted at healing abutment connection and latest visit. Marginal bone level was measured.
Results: Mean marginal bone loss was 0.73 mm in study group, 0.63 mm in control group. Implants in maxillary anterior area (1.21 mm) were statistically significant in study group (P<0.05), maxillary posterior area (0.81 mm) in control group (P<0.05). Mean marginal bone loss 1.47 mm for implants with diameter 3.4 mm, 0.83 mm for implants of control group with diameter 4.0 mm (P<0.05). Some graft materials showed an increased marginal bone loss but no statistically significant influence of sex, implant type or length.
Conclusion: According to these findings, this study demonstrated the amount of marginal bone loss around implant has maintained a relative stable during follow-up periods. We conclude that implants with GBR had similar survival rate and crestal bone level compared with implants in native bone.
Key words: Dental implant, Guided bone regeneration, Bone resorption
Table 1. Gender, number and mean age of samples Gender Study group Control group
N (n) Mean age (yr)
N (n) N (n)
Male Female Total
18 (27) 24 (49) 42 (76)
18 (44) 23 (41) 41 (85)
36 (71) 47 (90) 83 (161)
51.2 56.3 54 N, number of patients; n, number of implants.
서 론
치과 임플란트에서 골유착(osseointegration)을 얻기 위해서 는 주변의 적절한 골량이 중요한 요소 중의 하나일 것이다[1-4].
1986년 Lekholm 등[5]은 임플란트의 성공을 위해서 임플란트 표면으로부터 최소한 1 mm 이상의 협, 설측의 골이 필요하다고 하였다. 하지만 임플란트를 식립하기에 충분하지 못한 수직적 혹은 수평적 잔존 치조제를 가진 환자들을 임상에서 흔하게 접하 게 된다. 이러한 조건에서는 임플란트의 표면이 완전히 골에 덮이 지 않게 되며, 치은의 퇴축, 비심미적인 외형과 구강 위생 유지의 어려움 및 임플란트 주위염과 같은 감염의 위험성을 증가시킨다.
이와 같은 상황을 예방하기 위하여 Nyman 등[6]은 치주 결손부 치료에 차단막 사용을 언급하면서 조직유도재생술의 개념을 제창 하여 임플란트 식립 시 위축된 무치악 치조제의 증대술을 위한 수술적 방법을 제시하였다.
골유도재생술(guided bone regeneration)은 치과 임플란트 영역에 있어서 다양하게 시행되고 발전되어 왔다. 1989년 Dahlin 등[7]은 티타늄 임프란트 주변의 열개성 결손부(dehiscence de- fect)에 차단막을 사용한 후 골형성에 대한 동물실험을 진행한 결과 임플란트 주변 열개성 결손부에 expanded polytetra- fluoroethylene (e-PTFE)을 사용한 경우가 사용하지 않은 경우 에 비해 유의성 있는 골재생이 이루어졌다고 보고하였다. 이후에 도 골유도재생술은 수평적으로 위축된 무치악 치조제 폭의 증강을 위하여 사용되었고[8-12], 열개 또는 천공이 있는 잔존 치조제 [13-15], 그리고 잔존 골성 결함 부위나 크기가 넓은 구치부 발치와 같은 부위에서도 사용되었다[16-18].
골유도재생술을 이용하여 수직 또는 수평적으로 증대시킬 수 있는 양은 일부 연구에서 수평적으로 약 2∼4.5 mm, 수직적으로 약 2∼7 mm라고 하였다[19-21]. 그러나 지금까지 수행되어 왔던 수많은 연구들은 매우 다양한 골이식 재료들이 사용되었고 표준화 된 전향적 연구가 부족하여 골이식재의 선택과 골유도재생술의 결과와 관련성에 대한 확실한 결론을 내릴 수 없으며 임상가들은 재료의 선택을 경험에 의존하고 있다.
이에 따라 본 연구에서는 골유도재생술과 동시에 식립된 임플 란트에 대하여 임플란트 생존률과 변연골 흡수량을 조사하고자 하였으며, 환자의 성별, 임플란트 식립위치, 임플란트의 길이와 직경, 골이식재의 종류와 양에 따라 분류하여 향후 임플란트 환자 의 치료 시 최소한의 변연골 흡수량을 얻기 위한 지표를 만들고자 함에 목적을 두었다.
연구방법
1. 연구 대상 및 재료
2009년 9월부터 2010년 10월까지 원광대학교 치과대학 산본 치과병원 구강악안면외과에서 부분 또는 완전 무치악 부위에 임플 란트 식립술을 시행 받은 83명의 전신적으로 건강한 환자를 대상 으로 하였다. 조절되지 않는 당뇨병, 방사선 치료, 심장질환, 지혈 문제, 혈액질환 등의 전신 병력을 가진 환자는 대상에서 제외하였 다. 이 연구에 포함된 83명의 환자는 남자 36명, 여자 47명으로 23세부터 75세까지 분포하였으며 평균 연령은 54세였다. 총 161 개의 임플란트가 식립되었고, 1차 수술 시 골유도재생술 술식을 시행 받은 환자군을 실험군(n=42), 골이식술 없이 임플란트 식립 술만 시행 받은 환자군을 대조군(n=41)으로 하였다(Table 1).
2. 연구방법 1) 외과적 술식
모든 수술 과정은 83명의 환자 모두 정주 진정요법(midazolam 0.2 mg/kg)을 병행한 국소 마취하에 진행되었고, 골이식술 없이 임플란트를 식립하거나 또는 임플란트 식립과 동시에 골유도재생 술이 시행되었다. 절개는 무치악 치조정에서부터 인접한 치아의 치은 열구내 절개까지 확장하였다. 근심과 원심부의 수직이완 절개를 시행하고 협, 순측 및 설, 구개측 전층판막 거상을 하였다.
4-0 VicrylⓇ을 이용한 태깅 봉합(tagging suture)으로 수술 시야 확보 및 견인을 수월하게 하였다. 수술용 스텐트를 이용하여 최적 의 임플란트 식립 위치를 결정하였다. Adell 등[2]에 의한 통법에 따라 골흡수에 의해서 변연골의 경계부위에서 식립체의 머리와 thread 부분이 치조정 상방으로 돌출되어 노출이 되었더라도 임 플란트는 이상적인 위치로 식립하였다. 최적의 초기 안정성을 얻기 위해 주의를 기울였으며 마지막으로 피개나사를 체결하였다.
총 161개의 임플란트(XiveⓇ [DENTSPLY Friadent, Mannheim, Germany], Nobel Speedy groobyTM [Nobel Biocare, Gothenburg, Sweden], ImplantiumⓇ [Dentium, Seoul, South Korea], GSIIⓇ [Osstem, Seoul, South Korea])가 식립되었다. 결손부위는 다양 한 골이식재들을 사용하여 치조능 증대술을 시행하였다. 골이식재 는 동결 건조 동종골(freezed dried bone allograft)인 OragraftⓇ
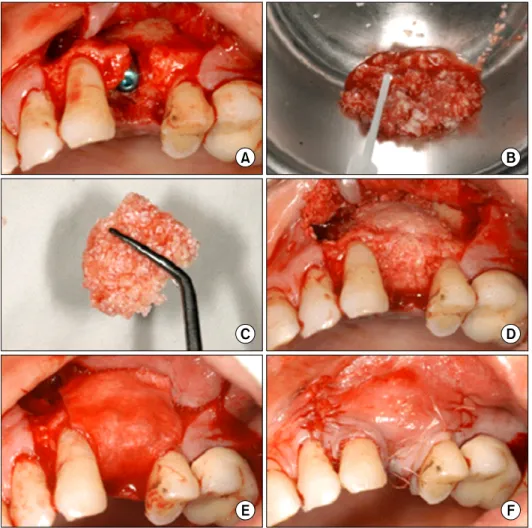
Fig. 1. An example of the basic pro- cedures for implant installation with guided bone regeneration. (A) Implant installment: a large de- hiscence at buccal aspects of the implant at site 24. (B) Combine par- ticular bone graft materials with tis- sue glue. (C) Molded bone graft mixture for defect shape. (D) Same dehiscence covered with graft materials. (E) Resorbable membrane covering the bone grafts and the bone defect. (F) Complete tension free suture.
(Lifenet Health, Virginia Beach, VA, USA), Puros (Zimmer Dental Inc., Carlsbad, CA, USA), ICBⓇ (Rocky Mountain Tissue Bank, Denver, CO, USA) CTS Bone powderⓇ (Community Tisseu Service, Dayton, OH, USA), 이종골인 Bio-ossⓇ (Geistlichpharma AG, Wolhusen, Switzerland), 자 가골은 본 스크래퍼(bone scraper)를 이용하여 수술장 내에서 입자형 골편을 채득하였다. 입자형의 골이식재를 조직 접착제인 TisseelⓇ (Baxter Healthcare, Deerfield, IL, USA)과 혼합하여 결손부 외형에 맞게 주조하였다. 흡수성 차폐막인 LyoplantⓇ (B. Braun Surgical GmbH, Stuttgart, Germany)을 외형에 맞게 잘라내고 피개한 후 완전한 장력 해소를 위하여 조심스럽게 골막 이완 절개를 시행하였다. 피판은 4-0 VicrylⓇ을 사용하여 수평 매트리스 봉합법, 단순 봉합법, 연속단속 봉합법을 적용하였 다(Fig. 1). 환자에게 수술 1시간 전 감염 예방과 부종의 억제를 위한 아미노글리코사이드 계열의 항생제(amikacin 2.0 mL)와 스테로이드 약물(dexamethasone 1.0 mL)을 근주하였고, 술 후 약 5일간 Amoxilciln 325 mg을 매일 3회씩 경구 복용하도록 하였다. 임플란트 식립 후 상악 5∼6개월, 하악 3∼4개월 경과하 여 치유 지대주를 연결하였고, 골유도재생술식을 시행한 경우
상악에서는 최소 6개월 이상, 하악에서는 최소 3개월 이상 경과 기간 후 치유 지대주를 연결하였다. 2주간의 연조직 치유기간을 거친 뒤 보철 지대주를 연결하고 임시 보철물을 2주간 장착하여 점진적인 부하를 가한 후 보철물을 장착하였으며 이 때 부하 시점은 2차 수술을 시행한 날짜로 하였다. 1회법 수술(one stag- ed type surgery)은 본 연구에서 제외하였다.
2) 진료 기록부를 이용한 임상적 검사
의무기록지를 후향적으로 분석하였으며, 골유도재생술과 동시 에 임플란트 식립술을 시행 받은 환자(실험군)와 골이식술 없이 임플란트 식립술만 받은 환자(대조군) 두 군으로 나누어 분류하였 다. 매식체의 동요가 있거나, 치유 지대주 연결 시 매식체가 같이 돌아가 골유착이 실패했다고 판단되는 경우, 그리고 조절되지 않는 임플란트 주위 염증이 존재하거나 주위 골 소실이 50%
이상 관찰되는 이유로 임플란트를 제거한 경우를 실패로 분류하여 임플란트의 생존율을 분석하였다. 또한 골이식 방법, 골이식재의 종류와 적용된 양, 차단막 사용 여부, 식립된 임프란트의 유형, 합병증, 치유기간 등을 조사하였다. 골이식 후 지연식립법과 상악 동 거상술식은 포함하지 않았다.
Fig. 2. Measurement of marginal bone loss. Reference point used for the radiographic readings & baseline of marginal bone loss.
Digital processing of a radiographic image using UTHSCSA Image Tool (For windows version 3.0, The University of Texas Health Science Center in San Antonio).
Table 2. Distribution of implant system of study group
Implant system N (%)
XiveⓇ GSIIⓇ ImplantiumⓇ
Nobel Speedy GroobyTM Total
7 (9.2) 13 (17.2) 48 (63.1) 8 (10.5) 76 (100)
XiveⓇ: DENTSPLY Friadent, Mannheim, Germany, GSIIⓇ: Osstem, Seoul, South Korea, ImplantiumⓇ: Dentium, Seoul, South Korea, Nobel Speedy groobyTM: Nobel Biocare, Gothenburg, Sweden.
N, number of implants.
Table 3. Distribution of implant system of control group
Implant system N (%)
XiveⓇ GSIIⓇ ImplantiumⓇ
Nobel Speedy GroobyTM Total
11 (12.9) 8 (9.4) 49 (57.6) 17 (20.1) 85 (100) XiveⓇ: DENTSPLY Friadent, Mannheim, Germany, GSIIⓇ: Osstem, Seoul, South Korea, ImplantiumⓇ: Dentium, Seoul, South Korea, Nobel Speedy groobyTM: Nobel Biocare, Gothenburg, Sweden.
N, number of implants.
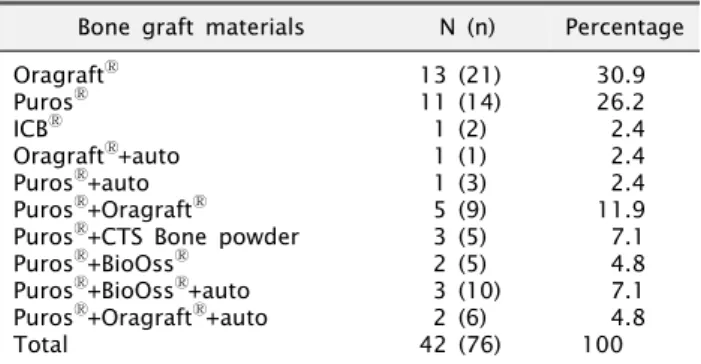
Table 4. Distribution of graft materials of study group Bone graft materials N (n) Percentage OragraftⓇ
PurosⓇ ICBⓇ
OragraftⓇ+auto PurosⓇ+auto PurosⓇ+OragraftⓇ PurosⓇ+CTS Bone powder PurosⓇ+BioOssⓇ
PurosⓇ+BioOssⓇ+auto PurosⓇ+OragraftⓇ+auto Total
13 (21) 11 (14) 1 (2) 1 (1) 1 (3) 5 (9) 3 (5) 2 (5) 3 (10) 2 (6) 42 (76)
30.9 26.2 2.4 2.4 2.4 11.9 7.1 4.8 7.1 4.8 100 OragraftⓇ: Lifenet Health, Virginia Beach, VA, USA, PurosⓇ: Zimmer Dental Inc., Carlsbad, CA, USA, ICBⓇ: Rocky Mountain Tissue Bank, Denver, CO, USA, CTS Bone powder: Community Tisseu Service, Dayton, OH, USA.
N, number of patients; n, number of implants; auto, autogenous bone.
3) 방사선학적 분석
임플란트 식립 시 방사선 사진을 촬영한 후 이차수술 후 파노라마 방사선 사진과 최종 경과 관찰 시점에서 촬영한 파노라마 방사선 사진을 비교하였다. 방사선 사진은 구외촬영기인 Orthopantomograph OP100Ⓡ (Instrumentarium Corp. Imaging Division, Tuusula, Finland)로 파노라마를 촬영하여 영상정보를 얻었다. 단, 왜곡이 심하게 나타나는 영상의 경우 추가적인 치근단 방사선 사진을 촬영하였다.
4) 컴퓨터 프로그램을 이용한 측정
임플란트 매식체 치관부의 기시 부위를 기준점으로 하고 변연 골의 높이는 임플란트-변연골 경계 부위의 흡수된 변연골 양상 중 최하방 기저부로 정하여 그 거리를 UTHSCSA Image Tool (For windows version 3.0, The university of Texas Health Science Center in San Antonio)을 이용하여 측정하였다. 정확 한 임플란트 주변의 골흡수량을 측정하기 위하여 방사선 사진의 확대율을 보정하는 작업을 시행하였으며, 임플란트 매식체의 근 원심에서 각각 골높이를 2회 측정 후 그 평균값을 골흡수량으로 이용하였다(Fig. 2).
5) 통계학적 분석
환자의 나이, 연령, 식립한 임플란트의 종류, 직경, 길이, 식립 위치, 골유도재생술에 사용된 골이식재의 종류와 량을 독립변인 으로 설정하고 임프란트 보철 기능 최소 6개월(6∼24개월) 이상 의 최근 내원 시의 측정된 변연골 흡수량을 종속변인으로 설정하 였다(Table 1∼4). SPSS 통계 프로그램 version 12.0 (SPSS Inc., Chicago, IL, USA)을 이용하여 one-way ANOVA test를 시행하였고, 분석결과 얻어진
P
값이 0.05 이하일 경우 통계학적 으로 유의한 차이를 보인다고 판정하였다.결 과
2009년 9월에서 2010년 10월까지 총 83명의 환자에서 161개 의 임플란트가 식립되었다. 골유도재생술과 동시에 식립한 군(실 험군)의 환자가 42명이었으며, 76개의 임플란트가 식립되었고, 임플란트만 식립한 군(대조군)의 환자는 41명이었으며 85개의 임플란트가 식립되었다.
Table 6. Mean marginal bone loss according to age in both groups
Age Study group N Control group N
30∼39 40∼49 50∼59 60∼69
>70 Total
0.31±0.26 0.74±0.52 0.77±0.50 0.83±0.72 0.67±0.66 0.73±0.59
7 15 20 24 10 76
0.32±0.28 0.59±0.35 0.67±0.32 0.80±0.55 0.81±0.62 0.62±0.40
14 24 28 12 7 85 Values are presented as mean±standard deviation (mm).
N, number of implants.
*P <0.05.
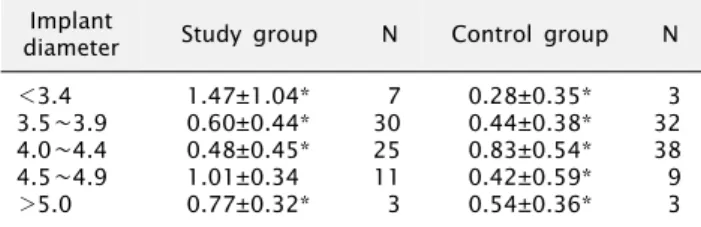
Table 8. Marginal bone loss according to implant diameter Implant
diameter Study group N Control group N
<3.4 3.5∼3.9 4.0∼4.4 4.5∼4.9
>5.0
1.47±1.04*
0.60±0.44*
0.48±0.45*
1.01±0.34 0.77±0.32*
7 30 25 11 3
0.28±0.35*
0.44±0.38*
0.83±0.54*
0.42±0.59*
0.54±0.36*
3 32 38 9 3 Values are presented as mean±standard deviation (mm).
N, number of implants.
*P <0.05.
Table 5. Mean marginal bone loss according to gender in both groups
Gender Study group Control group N
Male
Female 0.63±0.43
0.78±0.66 0.64±0.41
0.62±0.36 71
90 Values are presented as mean±standard deviation (mm).
N, number of implants.
*P <0.05.
Table 7. Marginal bone loss according to position
Position Study group N Control group N Mx. ant
Mx. post Mn. ant Mn. post
1.21±0.95*
0.55±0.42*
1.02±0.38 0.62±0.48*
11 13 6 46
0.28±0.35*
0.81±0.55*
0.37±0.25*
0.29±0.29*
9 22 6 48 Values are presented as mean±standard deviation (mm).
N, number of implants; Mx., maxilla; Mn., mandible; ant, anterior area; post, posterior area.
*P <0.05.
1. 성별 및 연령에 따른 변연골 흡수량
모든 임플란트에 대한 기능적 부하 후 평균 15.8개월에 관찰한 변연골 흡수량의 평균은 실험군에서 남자 0.63±0.43 mm (n=18), 여자 0.78±0.66 mm (n=24), 대조군에서 남자 0.64±0.41 mm (n=18), 여자 0.62±0.36 mm (n=23)를 보였으나 통계학적 유 의한 차를 보이지 않았다(
P
<0.05)(Table 5).피실험자의 평균 연령은 54세(범위: 23∼75세)였으며 두 군 모두 연령에 따른 변연골 흡수량의 통계학적 유의한 차이는 없었 다(
P
<0.05)(Table 6). 단, 대조군의 23세 여환 1명은 집단 간 통계학적 분석을 위해 30대 집단에 포함시켰음을 밝힌다.2. 임플란트 식립 위치 및 분포에 따른 변연골 흡수량
총 161개의 임플란트가 식립되었으며 실험군에서 상악전치부 11개(14.5%), 상악구치부 13개(17.1%), 하악전치부 6개(7.9%), 하악구치부 46개(60.5%)였으며, 대조군에서는 상악전치부 9개 (10.6%), 상악구치부 22개(25.9%), 하악전치부 6개(5.8%), 하 악구치부 48개(56.2%)로 하악구치부에 가장 많이 식립되었다 (Table 7).각 부위별로 변연골 흡수량을 살펴보면 평균 기능 부하 15.8개 월 후 실험군에서 전치부에서는 상악 1.21±0.95 mm, 하악 1.02±0.38 mm, 구치부에서는 상악 0.55±0.42 mm, 하악 0.62±0.48 mm로 나타났으며 상악전치부에서 가장 많은 골흡수 를 보였으며 통계적으로 유의성 있는 차이를 보였다(
P
<0.05).대조군에서 전치부에서는 상악 0.28±0.35 mm, 하악 0.37±0.25 mm, 구치부에서는 상악 0.81±0.55 mm, 하악 0.29±0.29 mm
로 나타났으며 상악구치부에서 가장 많은 골흡수를 보였으며 이는 통계적으로 유의성 있는 차이를 보였다(
P
<0.05).3. 임플란트 종류, 직경 및 길이에 따른 변연골 흡수량
직경에 따른 분포를 보면 실험군에서는 3.4 mm 이하 1개(9.2%), 3.5∼3.9 mm 30개(39.4%), 4.0∼4.4 mm 25개(33.8%), 4.5∼4.9 mm 11개(14.4%), 5.0 mm 이상 3개(3.9%)로 3.5∼3.9 mm 직경의 임플란트가 가장 많이 식립되었다. 대조군에서는 3.4 mm 이하 3개(3.5%), 3.5∼3.9 mm 32개(37.6%), 4.0∼4.4 mm 38개(41.2%), 4.5∼4.9 mm 9개(10.5%), 5.0 mm 이상 3개 (3.2%)로 4.0∼4.4 mm 직경의 임플란트가 가장 많이 식립되었 다. 그리고 길이에 따른 분포를 보면 실험군에서는 8.0 mm 1개 (1.3%), 9.5 mm 1개(1.3%), 10 mm 26개(34.2%), 11 mm 4개(5.4%), 11.5 mm 8개(10.5%), 12 mm 27개(35.5%), 13 mm 8개(11.8%), 15 mm 1개(1.3%)로 12 mm가 가장 많이 식립되었다. 대조군에서는 8.5 mm 3개(2.4%), 10 mm 19개 (15.3%), 11.5 mm 31개(43.5%), 12 mm 28개(34.1%), 15 mm 4개(4.7%)로 11.5 mm가 가장 많이 식립되었다. 변연골 흡수량을 살펴보면 평균 기능부하 15.8개월 후 실험군에서는 직 경 3.4 mm 이하 임플란트에서 1.47±1.04 mm로 가장 많은 골 흡수량을 보였으며 이는 다른 직경의 임플란트의 변연골 흡수 량과 통계적으로 유의한 차이를 보였다(
P
<0.05). 대조군에서는 직경 4.0 mm 임플란트에서 0.83±0.54 mm로 골흡수량이 나타 났으며 다른 직경의 임플란트와 비교했을 때 통계적으로 유의한 차이를 나타내었다(P
<0.05)(Table 8).Table 11. Marginal bone loss according to graft materials in study groups
Combination of graft materials Marginal bone loss N OragraftⓇ
PurosⓇ ICBⓇ PurosⓇ+auto PurosⓇ+OragraftⓇ PurosⓇ+CTS Bone powder PurosⓇ+BioOssⓇ
PurosⓇ+BioOssⓇ+auto PurosⓇ+OragraftⓇ+auto
1.07±0.64*
0.73±0.60 0.90±0.00 0.67±0.35 0.39±0.35*
1.16±0.45*
0.30±0.22*
0.36±0.50*
0.30±0.33*
21 14 2 3 9 5 5 10 6 Values are presented as mean±standard deviation (mm). OragraftⓇ: Lifenet Health, Virginia Beach, VA, USA, PurosⓇ: Zimmer Dental Inc., Carlsbad, CA, USA, ICBⓇ: Rocky Mountain Tissue Bank, Denver, CO, USA, CTS Bone powder: Community Tisseu Service, Dayton, OH, USA.
N, number of implants.
*P <0.05.
Table 9. Marginal bone loss according to implant length Implant
length Study group N Control group N
<9.9 10∼10.9 11∼11.9 12∼12.9
>13
0.45±0.07 0.53±0.44 0.81±0.43 0.80±0.76 0.98±0.48
2 26 12 27 9
0.59±0.40 0.47±0.38 0.52±0.46 0.81±0.62 0.67±0.32
3 19 31 28 4 Values are presented as mean±standard deviation (mm).
N, number of implants.
*P <0.05.
Table 10. Marginal bone loss according to implant system Implant system Study group N Control group N XiveⓇ
GSIIⓇ ImplantiumⓇ
Nobel Speedy GroobyTM
0.89±0.34 0.72±0.46 0.68±0.66 0.88±0.60
7 13 48 8
0.76±0.49 0.80±0.81 0.70±0.65 0.59±0.58
11 8 49 17 Values are presented as mean±standard deviation (mm). XiveⓇ: DENTSPLY Friadent, Mannheim, Germany, GSIIⓇ: Osstem, Seoul, South Korea, ImplantiumⓇ: Dentium, Seoul, South Korea, Nobel Speedy groobyTM: Nobel Biocare, Gothenburg, Sweden.
N, number of implants.
*P <0.05.
하지만 임플란트 시스템의 종류와 임플란트 길이에 따른 골 흡수량의 차이에 대한 통계학적 유의한 차이가 관찰되지 않았다 (
P
<0.05)(Table 9, 10).4. 골유도재생술에 사용된 골이식재에 따른 변연골 흡수량
실험군에서는 임플란트 식립과 동시에 골유도재생술이 시행되 었으며, 골이식재의 종류와 이식량에 따른 변연골 흡수량 차이를 분석하였다. 각 이식재료에 따른 변연골 흡수량은 OragraftⓇ 1.07±0.64 mm (n=21, 30.9%), PurosⓇ 0.73±0.60 mm (n=14, 26.2%), ICBⓇ 0.90±0.00 mm (n=2, 2.4%), PurosⓇ와 자가골 혼합 사용 시 0.67±0.35 mm (n=3, 2.4%), PurosⓇ와 OragraftⓇ 혼합 사용 시 0.39±0.35 mm (n=9, 11.9%), PurosⓇ 와 CTS Bone powder 혼합 사용 시 1.16±0.45 mm (n=5, 7.1%), PurosⓇ와 Bio-OssⓇ 혼합 사용 시 0.30±0.22 mm (n=5, 4.8%), PurosⓇ, Bio-OssⓇ와 자가골 혼합 사용 시 0.36±0.50 mm (n=10, 7.1%), PurosⓇ, OragraftⓇ와 자가골 혼합 사용 시 0.30±0.33 mm (n=6, 4.8%)로 OragraftⓇ 단독 사용했을 때와 PurosⓇ와 CTSⓇ 혼합 사용했을 때가 변연골 흡수 량이 많았다. 임플란트 식립과 동시에 골유도재생술을 시행 받은 42명의 환자에게서 이식량에 따른 변연골 흡수량은 통계학적인 유의한 차이를 나타내지 않았다(Table 11).고 찰
Esposito 등[22]은 임플란트의 실패를 보철물을 장착한 시점을 기준으로 초기 실패와 후기 실패로 나누었을 때 Bränemark 임플 란트에서 초기실패가 전체 실패의 47% 가량을 차지한다고 보고하 였다. Adell 등[3]은 임플란트 식립 이후 초기 2년 동안에 가장 높은 실패율을 보이다가 그 이후에 점진적인 안정화가 진행되어 임플란트의 실패율이 감소한다고 하였다. 또한 골유착과 관련된 Zarb과 Schmitt[23]의 연구에서는 임플란트의 실패는 매식 후 1년 사이에 나타나기 쉽다고 하였다. 따라서 이번 연구에서 초기 에 실패율이 높은 것을 참고로 하여 임플란트 최종 보철물 장착 후 최소 6개월 이상 지난 환자를 대상으로 하였고, 최대 관찰 기간은 22개월이었으며 평균 기능적 부하 기간은 약 9개월이었다.
최종 내원 시기의 변연골 흡수량을 측정하여, 임플란트 식립 수술 시기와 이차 수술 시 치유 지대주 연결 시기의 방사선 사진과 비교하였다. Hollender와 Rockler[24]는 Bränemark 임플란트 의 변연골 흡수량 변화를 관찰하기 위해 평행 촬영법에 의해 치근단 촬영을 실시하였으며 정확한 기준점을 잡기 위해 임플란트 축에 수직촬영이 이루어져야 한다고 하였다. Molander 등[25]은 구내방사선 사진과 파노라마 사진으로부터 변연골을 측정한 결과 그 결과는 동일하였으며, 따라서 파노라마 사진만으로도 변연골 측정이 가능하다고 하였다. 단, 파노라마 사진의 상의 질이 충분하 지 못한 경우에는 추가적인 치근단 사진을 촬영할 것을 추천하였 다. 본 연구에서도 기본적으로 파노라마 사진을 이용하여 변연골 흡수량을 측정하였지만 하악전치부와 같이 왜곡이 심한 부위는 치근단 사진을 촬영하여 부분적으로 이용하였다.
골유도재생술은 발치와의 골흡수 보존 및 골재생, 위축된 치조 능에 대한 증강술, 상악동골이식술, 임플란트 주변 결손부 수복 등을 목적으로 시행되는 경우가 많으며 예측 가능하고 비교적 안전한 술식으로 평가 받고 있다[13]. 골유도재생술의 성공에 영
향을 미치는 요소는 차단막의 세포 차단성, 공간 확보 및 유지, 물리적 강도가 우수해야 하며 골이식 혹은 티타늄 나사나 핀 등을 이용한 tenting을 통해 공간을 확보하는 것이 중요하다.
또한 차단막의 고정성, 엄격한 무균적 수술, 하방의 혈병을 안전하 게 보호할 수 있는 능력, 창상의 안정, 골이식재의 유동성 방지 등을 들 수 있다[26-28]. 일부 학자들은 입자형 골이식재를 사용할 때 조직접착제를 사용함으로써 입자들의 유동성을 방지하고 결국 골치유를 촉진한다고 하였으며[29], 본 연구에서도 실험군의 모든 증례에서 TisseelⓇ을 복합 적용하였다.
Becktor 등[30]과 Fugazzotto[31]은 골이식에 대하여 골유도 재생술에 의해 적절한 골이 형성되고 기능적 부하 초기에 실패한 임플란트를 제외한다면, 임플란트의 생존율은 골이식이나 골유도 재생술의 유무에 따라 크게 영향을 받지 않을 것이라고 하였다.
임플란트 치조골 소실에 관한 많은 연구가 보고되었고 이에 영향 을 줄 수 있는 식립 위치, 수술 방법, 치주지수, 교합면의 재료, 환자의 기능 이상 등과 같은 여러 인자에 대하여 보고된 바 있다.
이에 본 연구에서도 평균 16개월의 관찰 기간 동안 골흡수량을 측정하여 골유도재생술식이 시행된 부위에 식립된 임플란트와 골유도재생술 없이 식립된 임플란트 간의 변연골 흡수량의 차이를 알아보고자 하였다. 실험군과 대조군 간의 변연골 흡수량은 각각 0.73±0.44 mm와 0.63±0.42 mm로 골유도재생술을 사용한 부위의 골흡수량이 0.10 mm 더 많았으나 그 차이는 유의미하지 않다고 생각한다.
Wyatt와 Zarb[32]은 전치부와 구치부 사이에 골흡수량의 차이 는 없다고 하였으나, 본 연구에서의 식립 부위에 따른 변연골 흡수량은 실험군에서는 상악전치부에서 대조군에서는 상악구치 부에서 더 많은 골흡수량을 나타내었다. Peñarrocha[33]는 108 개의 임플란트에서 상악에서 보다 많은 골 소실이 있음을 보고하 였고, 본 연구 또한 같은 결과를 얻었다. 이는 골량과 골질에 따른 임플란트 주위의 응력분산이 다르며 밀도가 낮은 해면골에서 더 많은 응력의 집중이 보고된 바 있다[34].
임플란트의 직경과 길이에 따른 흡수량을 살펴보면 길이에 따른 통계적 유의 차는 없었다(
P
<0.05). 직경의 경우 실험군에 서는 3.4 mm 이하 직경의 임플란트에서 1.47±1.04 mm로 가장 많은 골흡수량을 보였으며 이는 통계적으로 유의한 차이를 보였다. 대조군에서는 4.0 mm 직경의 임플란트에서 0.83±0.54 mm로 골흡수량이 나타났으며 통계적으로 유의한 차이를 나타내 었다(P
<0.05). 실험군의 경우 상대적으로 잔존 치조제의 폭이 좁은 상악전치부에서 대체적으로 지름이 작은 임플란트가 식립된 환경적인 요인과 연관성이 있을 것으로 생각해 볼 수도 있을 것이다. 대조군의 경우 4.0 mm 직경의 임플란트 변연골흡수량이 0.83±0.54 mm로 가장 많이 나타났는데, 다른 직경의 임플란트 의 수가 상대적은 통계 처리의 한계점과 대조군의 식립 위치에 따른 골흡수량이 가장 많았던 상악 대구치 부위에 4.0 mm 직경의임플란트가 다수 식립된 관계도 생각해 볼 수 있다. 그러나 다른 요인을 통제하고 측정된 연구 결과는 아니므로 추가적인 연구가 필요하다. 임플란트의 직경이 증가되면 치조정 부위의 응력이 감소되며 길이의 증가는 응력 감소를 보고된 바 있다[35]. Hertel 과 Kalk[36]는 임플란트 설계 시 응력분산을 위해 가능한 골과 넓은 접촉면적을 가져야 하며 치조정에서 골흡수를 일으킬 수 있는 임플란트 부분은 과도한 응력 집중을 막을 수 있어야 한다고 하였고, 작은 직경의 임플란트는 골에 전달하는 응력을 증가시키 므로 가능한 크기를 증가시켜야 한다고 하였다. 반면 Friberg 등[37]은 임플란트의 직경이 임플란트의 실패와는 연관성이 없다 는 결과를 보고한 바 있다.
본 연구의 실험군에서는 골유도재생술을 시행하였으며, 골이 식재로는 자가골, 동종골, 합성골 등이 다양하게 단독 또는 혼합되 어 사용되었다. 입자형 골이식재를 골결손부위에 적용하고 그 상방에 흡수성의 콜라겐막으로 피개하였다. Jovanovic 등[14]은 12개 임플란트 주변 골열개부위를 e-PTFE막을 사용하여 처치하 였으며 방사선 사진을 통해 분석한 결과 6∼12개월에 평균 1.73 mm의 흡수를 보였다고 발표하였다. Zitzmann 등[38]은 골유도 재생술 여부에 상관없이 5년 후 유사한 임플란트 생존율을 보였으 나 골흡수는 골유도재생술이 시행된 군에서 좀 더 현저하게 나타 났다고 하였다. Jensen 등[20]은 차단막과 자가골이식을 동시에 사용한 경우 이식 골편의 약 70%가 보존되었다고 하였으며 이 때 차단막은 연조직 침투를 방지하는 장벽 역할을 하며 골편과 혈병을 안정시켜 이식 골편을 보존하는 역할을 수행한다고 하였 다. 또한 Hämmerle 등[39]은 골대체 재료만을 단독 사용한 경우 보다 골대체 재료를 차단막과 함께 사용했을 때 골재생이 더 많이 일어났음을 증명하였다.
본 연구는 후향적으로 시행되어 변수들이 매우 많고 여러 가지 임플란트 시스템과 다양한 골이식재들이 사용되었으며 각각의 개체 수가 적어 의미 있는 결과를 도출하기에는 다소 미흡하다.
따라서 임플란트 시스템, 골이식재와 차단막의 사용 등을 표준화 한 상태에서 골유도재생술이 동반된 경우의 중장기적인 예후를 평가하기 위한 전향적인 연구가 필요할 것이라 생각한다.
결 론
2009년 9월부터 2010년 10월까지 원광대학교 치과대학 산본 치과병원 구강악안면외과에 내원하여 임플란트 식립술을 시행한 환자 83명, 161개의 임플란트를 대상으로 골유도재생술과 동시에 식립한 집단을 실험군(n=42명, 76개)으로, 골이식술 없이 임플란 트만 식립한 집단을 대조군(n=41명, 85개)으로 하여 이차수술 시와 부하가 가해진 후 최소 6개월 이상 최대 22개월(평균 15.8개 월) 내원 시 촬영한 방사선 사진을 이용하여 변연골의 변화를 측정하였으며 다음의 결과를 얻었다.
1. 기능적 부하 후 평균 변연골 흡수량은 평균 15.8개월 후 실험군에서는 0.73±0.44 mm, 대조군에서는 0.63±0.42 mm 로 통계적인 유의한 차이는 없었다(
P
<0.05).2. 성별 및 연령에 따른 변연골 흡수량에서 두 집단 간의 통계적 유의한 차이가 없었다(
P
<0.05).3. 식립 위치에 따른 골흡수량을 살펴보면 실험군에서는 상악 구치부(0.55±0.42 mm)와 하악구치부(0.62±0.48 mm)에 비 해 상악전치부(1.21±0.95 mm)에서 가장 많은 골흡수량을 보여 유의한 차이를 나타내었고(
P
<0.05), 대조군에서는 상악구치부 (0.81±0.55 mm)에서 가장 많은 골흡수량을 보였다(P
<0.05).4. 임플란트의 종류와 길이는 두 집단에서 골흡수량에 통계학적 유의한 차이가 없었으나, 임플란트의 직경은 실험군에서 3.4 mm 이하(1.47±1.04 mm), 대조군에서 4.0∼4.4 mm (0.83±0.54 mm)에서 다른 직경의 임플란트보다 많은 골흡수량을 보였다 (
P
<0.05).5. 골유도재생술에 사용된 이식재 종류에 따른 골흡수량은 대 체적으로 골이식재들을 혼합하여 사용했을 때가 동종골 단독 사용 시 더 많은 골흡수량을 보였는데, OragraftⓇ 단독 사용 시 가장 많은 변연골 흡수량(1.07±0.64 mm)을 보였다.
6. 본 연구에서 식립된 임플란트는 실험군과 대조군에서 합병 증이나 실패 없이 모두 생존하였다.
이상의 결과로 임플란트 식립 후에 임플란트 주변골의 흡수량 은 두 집단 모두 안정적으로 유지되는 것이 관찰되었으며, 치조골 증대술이 필요한 무치악 부위에서 골유도재생술이 임상적으로 선택할 만한 술식이라 생각한다.
References
1. Adell R, Lekholm U, Rockler B, Brånemark PI. A 15-year study of osseointegrated implants in the treatment of the edentulous jaw. Int J Oral Surg 1981;10:387-416.
2. Branemark PI. Introduction to osseointegration. In: Branemark PI, Zarb GA, Albrektsson T, editors. Tissue-integrated prosthese.
Osseointegration in clinical dentistry. Chicago: Quintessence Publishing Co, Inc.; 1985.
3. Adell R, Eriksson B, Lekholm U, Brånemark PI, Jemt T.
Long-term follow-up study of osseointegrated implants in the treatment of totally edentulous jaws. Int J Oral Maxillofac Implants 1990;5:347-59.
4. Friberg B, Jemt T, Lekholm U. Early failures in 4,641 con- secutively placed Brånemark dental implants: a study from stage 1 surgery to the connection of completed prostheses.
Int J Oral Maxillofac Implants 1991;6:142-6.
5. Lekholm U, Adell R, Lindhe J, et al. Marginal tissue re- actions at osseointegrated titanium fixtures. (II) A cross-sec- tional retrospective study. Int J Oral Maxillofac Surg 1986;15:53-61.
6. Nyman S, Lang NP, Buser D, Bragger U. Bone regeneration adjacent to titanium dental implants using guided tissue re-
generation: a report of two cases. Int J Oral Maxillofac Implants 1990;5:9-14.
7. Dahlin C, Sennerby L, Lekholm U, Linde A, Nyman S.
Generation of new bone around titanium implants using a membrane technique: an experimental study in rabbits. Int J Oral Maxillofac Implants 1989;4:19-25.
8. Buser D, Weber HP, Bragger U, Balsiger C. Tissue in- tegration of one-stage ITI implants: 3-year results of a longi- tudinal study with Hollow-Cylinder and Hollow-Screw implants. Int J Oral Maxillofac Implants 1991;6:405-12.
9. Buser D, Dula K, Belser U, Hirt HP, Berthold H. Localized ridge augmentation using guided bone regeneration. 1.
Surgical procedure in the maxilla. Int J Periodontics Restorative Dent 1993;13:29-45.
10. Buser D, Dula K, Belser UC, Hirt HP, Berthold H. Localized ridge augmentation using guided bone regeneration. II.
Surgical procedure in the mandible. Int J Periodontics Restorative Dent 1995;15:10-29.
11. Buser D, Dula K, Lang NP, Nyman S. Long-term stability of osseointegrated implants in bone regenerated with the mem- brane technique. 5-year results of a prospective study with 12 implants. Clin Oral Implants Res 1996;7:175-83.
12. Buser D, Dula K, Hirt HP, Schenk RK. Lateral ridge aug- mentation using autografts and barrier membranes: a clinical study with 40 partially edentulous patients. J Oral Maxillofac Surg 1996;54:420-32.
13. Nevins M, Mellonig JT, Clem DS 3rd, Reiser GM, Buser DA.
Implants in regenerated bone: long-term survival. Int J Periodontics Restorative Dent 1998;18:34-45.
14. Jovanovic SA, Schenk RK, Orsini M, Kenney EB. Supracrestal bone formation around dental implants: an experimental dog study. Int J Oral Maxillofac Implants 1995;10:23-31.
15. Simion M, Misitano U, Gionso L, Salvato A. Treatment of dehiscences and fenestrations around dental implants using resorbable and nonresorbable membranes associated with bone autografts: a comparative clinical study. Int J Oral Maxillofac Implants 1997;12:159-67.
16. Palmer RM, Smith BJ, Palmer PJ, Floyd PD, Johannson CB, Albrektsson T. Effect of loading on bone regenerated at im- plant dehiscence sites in humans. Clin Oral Implants Res 1998;9:283-91.
17. Becker W, Becker BE. Guided tissue regeneration for im- plants placed into extraction sockets and for implant de- hiscences: surgical techniques and case report. Int J Periodontics Restorative Dent 1990;10:376-91.
18. Simion M, Scarano A, Gionso L, Piattelli A. Guided bone re- generation using resorbable and nonresorbable membranes:
a comparative histologic study in humans. Int J Oral Maxillofac Implants 1996;11:735-42.
19. Gotfredsen K, Nimb L, Buser D, Hjørting-Hansen E.
Evaluation of guided bone generation around implants placed into fresh extraction sockets: an experimental study in dogs. J Oral Maxillofac Surg 1993;51:879-84.
20. Jensen OT, Greer RO Jr, Johnson L, Kassebaum D. Vertical guided bone-graft augmentation in a new canine mandibular model. Int J Oral Maxillofac Implants 1995;10:335-44.
21. Kassolis JD, Bowers GM. Supracrestal bone regeneration: a pilot study. Int J Periodontics Restorative Dent 1999;19:131-9.
22. Esposito M, Hirsch JM, Lekholm U, Thomsen P. Biological
factors contributing to failures of osseointegrated oral implants. (I). Success criteria and epidemiology. Eur J Oral Sci 1998;106:527-51.
23. Zarb GA, Schmitt A. The longitudinal clinical effectiveness of osseointegrated dental implants: the Toronto study. Part III: problems and complications encountered. J Prosthet Dent 1990;64:185-94.
24. Hollender L, Rockler B. Radiographic evaluation of osseoin- tegrated implants of the jaws. Experimental study of the in- fluence of radiographic techniques on the measurement of the relation between the implant and bone. Dentomaxillofac Radiol 1980;9:91-5.
25. Molander B, Ahlqwist M, Gröndahl HG, Hollender L.
Agreement between panoramic and intra-oral radiography in the assessment of marginal bone height. Dentomaxillofac Radiol 1991;20:155-60.
26. Hockers T, Abensur D, Valentini P, Legrand R, Hammerle CH. The combined use of bioresorbable membranes and xenografts or autografts in the treatment of bone defects around implants. A study in beagle dogs. Clin Oral Implants Res 1999;10:487-98.
27. Iasella JM, Greenwell H, Miller RL, et al. Ridge preservation with freeze-dried bone allograft and a collagen membrane compared to extraction alone for implant site development:
a clinical and histologic study in humans. J Periodontol 2003;74:990-9.
28. Dahlin C, Lekholm U, Becker W, et al. Treatment of fenes- tration and dehiscence bone defects around oral implants using the guided tissue regeneration technique: a pro- spective multicenter study. Int J Oral Maxillofac Implants 1995;10:312-8.
29. Graziani F, Ducci F, Tonelli M, El Askary AS, Monier M, Gabriele M. Maxillary sinus augmentation with platelet-rich plasma and fibrinogen cryoprecipitate: a tomographic pilot study. Implant Dent 2005;14:63-9.
30. Becktor JP, Isaksson S, Sennerby L. Survival analysis of en-
dosseous implants in grafted and nongrafted edentulous maxillae. Int J Oral Maxillofac Implants 2004;19:107-15.
31. Fugazzotto PA. Success and failure rates of osseointegrated implants in function in regenerated bone for 72 to 133 months. Int J Oral Maxillofac Implants 2005;20:77-83.
32. Wyatt CC, Zarb GA. Treatment outcomes of patients with im- plant-supported fixed partial prostheses. Int J Oral Maxillofac Implants 1998;13:204-11.
33. Peñarrocha M, Palomar M, Sanchis JM, Guarinos J, Balaguer J. Radiologic study of marginal bone loss around 108 dental implants and its relationship to smoking, implant location, and morphology. Int J Oral Maxillofac Implants 2004;19:
861-7.
34. Tada S, Stegaroiu R, Kitamura E, Miyakawa O, Kusakari H.
Influence of implant design and bone quality on stress/strain distribution in bone around implants: a 3-dimensional finite element analysis. Int J Oral Maxillofac Implants 2003;18:
357-68.
35. Petrie CS, Williams JL. Comparative evaluation of implant designs: influence of diameter, length, and taper on strains in the alveolar crest. A three-dimensional finite-element analysis. Clin Oral Implants Res 2005;16:486-94.
36. Hertel RC, Kalk W. Influence of the dimensions of implant superstructure on peri-implant bone loss. Int J Prosthodont 1993;6:18-24.
37. Friberg B, Ekestubbe A, Sennerby L. Clinical outcome of Brånemark System implants of various diameters: a retro- spective study. Int J Oral Maxillofac Implants 2002;17:671-7.
38. Zitzmann NU, Schärer P, Marinello CP. Long-term results of implants treated with guided bone regeneration: a 5-year pro- spective study. Int J Oral Maxillofac Implants 2001;16:355-66.
39. Hämmerle CH, Jung RE, Feloutzis A. A systematic review of the survival of implants in bone sites augmented with barrier membranes (guided bone regeneration) in partially edentu- lous patients. J Clin Periodontol 2002;29 Suppl 3:226-31.