대한소화기학회지 2009;53:98-105
접수: 2008년 5월 28일, 승인: 2008년 11월 10일 연락처: 김명환, 138-736, 서울시 송파구 풍납 2동 388-1
서울아산병원 소화기내과
Tel: (02) 3010-3183, Fax: (02) 476-0824 E-mail: mhkim@amc.seoul.kr
Correspondence to: Myung-Hwan Kim, M.D.
Division of Gastroenterology, Department of Internal Medi- cine, Asan Medical Center, 388-1, Pungnap 2-dong, Songpa- gu, Seoul 138-736, Korea
Tel: +82-2-3010-3183, Fax: +82-2-476-0824 E-mail: mhkim@amc.seoul.kr
췌장의 신경내분비 종양 122예의 임상양상 및 악성 예측인자
울산대학교 의과대학 서울아산병원 내과학교실, 외과학교실*
한정혜ㆍ김명환ㆍ문성훈ㆍ박수정ㆍ박도현ㆍ이상수ㆍ서동완ㆍ이성구ㆍ김송철*ㆍ한덕종*
Clinical Characteristics and Malignant Predictive Factors of Pancreatic Neuroendocrine Tumors
Jeung Hye Han, M.D., Myung-Hwan Kim, M.D., Sung Hoon Moon, M.D.,
Soo Jung Park, M.D., Do Hyun Park, M.D., Sang Soo Lee, M.D., Dong Wan Seo, M.D., Sung Koo Lee, M.D., Song Cheol Kim, M.D.*, and Duck Jong Han, M.D.*
Departments of Internal Medicine and Surgery*, Asan Medical Center, University of Ulsan College of Medicine, Seoul, Korea
Background/Aims: Neuroendocrine tumors (NET) of the pancreas are rare. Its prognosis is better than pancreas adenocarcinoma due to the slow growth, however, malignant NET of the pancreas are observed. The purposes of this study were to evaluate the clinical characteristics and to find the predictive factors of NET which are asso- ciated with malignancy and survival. Methods: We retrospectively evaluated the clinical outcomes of 122 patients with NET of the pancreas who were pathologically diagnosed at Asan Medical Center between 1990 and 2006.
Results: Mean age of the patients was 48.9±14.0 years and there was no gender predilection. The major clinical manifestations were abdominal pain (44.0%) in non-functional tumor, neuroglycopenic symptoms (100%) in in- sulinoma and diarrhea (60%) in gastrinoma. Tumor size ranged from 4 to 140 mm (average 29.8±23.22). Ninety cases (73.8%) were classified as benign tumors and 32 cases (26.2%) as malignant. In multivariate analysis of clinical characteristics, large sized tumor (>20 mm, p=0.001) was confirmed as sole independent factor to predict malignant NET. Surgical resection was performed in 114 patients. All patients with benign NET are still alive without recurrence. Six out of 32 patients with malignant NET died at an average 40.3 months after diagnosis.
The factors indicating favorable outcome were small size of tumors (p=0.046), resection of primary tumor (p=0.000), absence of lymph node invasion (p=0.0116) and distant metastasis (p=0.0005). Conclusions: Large NET of the pancreas, regardless of their functioning status, were more likely to be associated with malignancy and predictor of worse survival. (Korean J Gastroenterol 2009;53:98-105)
Key Words: Pancreas; Neuroendocrine tumor
서 론
췌장의 신경내분비 종양은 인구 10만 명당 0.4-1명의 빈도
로 발생하는 매우 드문 질환으로1 전체 췌장 종양의 0.4- 1.6%를 차지한다.2,3 췌장의 신경내분비 종양은 호르몬 과다 분비에 의한 임상 증상의 유무에 따라 기능 종양 및 비기능
한정혜 외 9인. 췌장의 신경내분비 종양 122예의 임상양상 및 악성 예측인자 99
Table 1. Characteristics of the Patients (n=122) Characteristics
Age (Mean±SD, year) 48.9±14.0
Male (%) 50 (41)
Symptoms (%)
Incidental 31 (25.4) Hypoglycemia 42 (34.4) Abdominal pain 35 (28.7) Indigestion 2 (1.6)
Fatigue 3 (2.5)
Jaundice 3 (2.5)
Back pain 2 (1.6) Abdominal mass 1 (0.8)
Diarrhea 3 (2.5)
Size (mm) 29.8±23.2
Location (%)
Head 59 (48.4)
Body 25 (20.5)
Tail 32 (26.2)
Diffuse 6 (4.9)
Malignant tumor (%) 32 (26.2) Nonfunctional tumor (%) 75 (61.5) Metastasis of tumor (%) 22 (18.0) Multiplicity (%) 10 (8.2) Follow up duration (Mean±SD, month) 45.0±38.0 SD, standard deviation.
종양으로 구분되며 이 중 기능 종양은 과다 분비되는 호르 몬의 종류에 따라 인슐린종, 가스트린종, 소마토스타틴종, 혈관활성 장 폴리펩티드 분비종(vasoactive intestinal polypep- tidoma, VIPoma)으로 세분화된다.
췌장의 신경내분비 종양의 악성화 빈도는 인슐린종의 경 우 10%, 가스트린종은 60% 그리고 췌장의 비기능 신경내분 비 종양은 50% 이상으로 알려져 있으며,4 악성 종양의 경우 대부분 종양의 진행에 의한 간부전으로 사망한다.5 영상진 단법의 발전으로 췌장 신경내분비 종양의 진단빈도는 증가 하였으나 수술 전에 악성 종양을 감별하는 것은 어려운 문 제이다. 만약 수술 전에 종양의 악성 가능성이 배제된다면 덜 침습적인 수술을 시행함으로써 수술로 인한 이환율을 최 소화하며, 환자의 삶의 질에 긍정적인 영향을 미칠 수 있을 것으로 생각한다. 이에 저자들은 췌장의 신경내분비 종양의 임상 특징 및 악성 예측인자와 생존율에 영향을 주는 인자 에 대해 조사하였다.
대상 및 방법
1. 대상
1990년 11월부터 2006년 12월까지 서울아산병원에서 조 직학적으로 췌장 신경내분비 종양으로 확진된 환자 중 췌장 에 기타 악성 종양이 합병되지 않은 122명의 환자를 대상으 로 하였다.
2. 방법
각 환자의 임상기록, 방사선 소견, 수술 기록, 병리 기록 등을 검토하여 후향 분석하여 췌장 신경내분비 종양 환자의 임상 특징, 종양의 크기, 위치, 악성 빈도, 영상 소견과 이에 따른 악성 예측 인자 및 생존에 미치는 인자 등에 대해 분 석하였다.
췌장 신경내분비 종양의 악성 여부는 주변 장기로의 침 윤, 혈관으로의 침윤, 림프절 혹은 타장기로의 전이가 있는 경우로 정의하였다.
이번 연구는 임상시험심사위원회의 승인을 받은 시험계 획서에 따라 진행되었다.
3. 통계 분석
환자의 나이, 종양의 크기와 악성과의 연관성 분석에는 student t-test를 이용하였고, 환자의 성별, 종양의 위치와 임상 증상, 종양의 기능성 여부, 영상진단 소견과의 연관성 분석에 는 χ2 test를 이용하였다. 악성 예측인자에 대한 다변량 분석 이 필요한 경우 이분형 로지스틱 회귀 분석을 시행하였으며 생존율 분석에 대해서는 Kaplan-Meier method를 이용하였다.
또한 p값이 0.05 미만일 경우 의미 있는 것으로 판정하였다.
결 과
1. 종양의 특성
췌장 신경내분비 종양 중에 비기능 종양은 전체 122예 중 75예로(61.5%) 가장 많았고, 인슐린종 42예(34.4%), 가스트 린종 5예(4.1%)였다. 제1형 다발 내분비 종양이 동반된 경우 는 6예가 있었고, 이 중 인슐린종 4예, 가스트린종 2예였다.
Von Hippel-Lindau 증후군이 동반된 예는 총 2예로 모두 비 기능 종양이었다.
췌장의 신경내분비 종양은 2000년도 이후 그 진단 예가 급격히 증가하는 양상을 보여 1990년부터 2000년까지 11년 간 진단된 췌장 신경내분비 종양은 총 39예(비기능 종양 14 예, 기능 종양 25예)에 비해 2001년부터 2006년까지 6년간 진단된 예는 총 83예(비기능 종양 61예, 기능 종양 22예)였 다.
2. 임상적 특성(Table 1)
환자의 연령 분포는 17세에서 74세로 평균 48.9±14.0세였
100 The Korean Journal of Gastroenterology: Vol. 53, No. 2, 2009
Table 2. Clinical Factors which Predict Malignant Neuroendocrine Tumor of the Pancreas
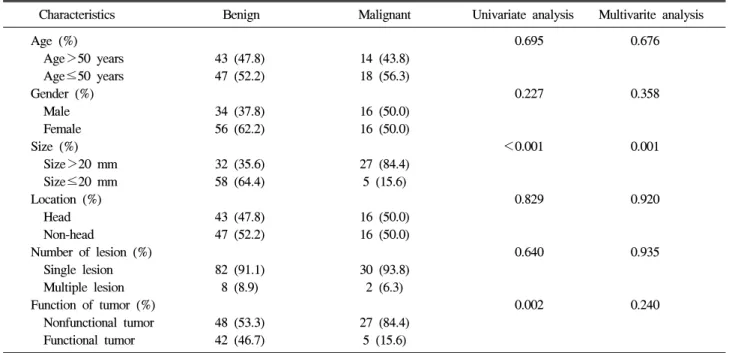
Characteristics Benign Malignant Univariate analysis Multivarite analysis
Age (%) 0.695 0.676
Age>50 years 43 (47.8) 14 (43.8) Age≤50 years 47 (52.2) 18 (56.3)
Gender (%) 0.227 0.358
Male 34 (37.8) 16 (50.0) Female 56 (62.2) 16 (50.0)
Size (%) <0.001 0.001
Size>20 mm 32 (35.6) 27 (84.4) Size≤20 mm 58 (64.4) 5 (15.6)
Location (%) 0.829 0.920
Head 43 (47.8) 16 (50.0) Non-head 47 (52.2) 16 (50.0)
Number of lesion (%) 0.640 0.935
Single lesion 82 (91.1) 30 (93.8) Multiple lesion 8 (8.9) 2 (6.3)
Function of tumor (%) 0.002 0.240
Nonfunctional tumor 48 (53.3) 27 (84.4) Functional tumor 42 (46.7) 5 (15.6) 고, 40대와 50대에 호발하며 환자수는 각각 33명, 31명이었
다. 비기능 종양을 따로 분석해 보았을 때 평균 연령이 51.4±13.2세로 기능 종양 환자의 평균 연령 45.0±14.6세보다 유의하게 높았다(p=0.016). 기능 종양의 경우 인슐린종은 저 혈당 신경계 증상이 42예 모두에서 나타났고, 가스트린종은 5예 중 3예에서 설사가 있었으며, 2예에서 공복 시 상복부 통증이 있었다. 75예의 비기능 종양 중 44예에서 주 증상이 있었으며 복부 통증이 33예(44.0%)로 가장 흔하게 나타났 고, 피로감 및 황달이 각각 3예(4.0%)로 그 다음을 차지하고 있었다. 증상이 없던 31예(41.3%)는 건강 검진 등을 통하여 우연히 발견되었다.
종양의 위치는 비기능 종양의 경우 췌두부 42예, 체부 16 예, 미부 16예, 미만형 1예였다. 기능 종양의 경우는 췌두부 17예, 체부 9예, 미부 16예, 미만 5예였다. 비기능 종양의 경 우 췌두부에 호발하였고, 기능 종양일 경우 췌두부 및 미부 에 호발하였으며 이는 의미가 있었다(p=0.026). 두 군 간의 종양 크기를 비교하여 보았을 때, 기능 종양의 평균 크기는 17.0±6.3 mm, 비기능 종양의 평균 크기는 37.7±26.1 mm로서 비기능 종양의 크기가 기능 종양에 비해 유의하게 큰 것으 로 나타났다(p<0.001).
3. 악성 예측인자
1) 임상 소견(Table 2)
양성 환자군의 평균 연령은 49.3±14.6세, 악성 환자군은 47.8±12.5세로 양 군 간 유의한 차이는 없었고, 성별에 대해 서도 유의한 차이는 없었다. 양성 종양의 평균 크기는 23.5±
18.7 mm, 악성 종양의 평균 크기는 48.5±25.4 mm로 악성 종 양의 크기가 유의하게 큰 것으로 나타났다(p<0.001). 종양 의 위치에서 양성 종양 환자군은 두부 43예, 체부 20예, 미 부 23예, 미만부 4예였고, 악성 종양 환자군은 두부 16예, 체 부 5예, 미부 9예, 미만부 2예로 종양 위치에 따른 통계학적 인 차이는 없었다. 종양의 기능면에서 보았을 때, 양성 종양 중 비기능성 종양은 48예(53.3%), 기능 종양은 42예(46.7%), 악성 종양 중 비기능 종양 27예(84.4%), 기능성 종양 5예 (15.6%)로 악성 종양군에서 비기능 종양이 유의하게 많았다 (p=0.002). 전체 대상 환자 122명 중 79예에서 혈청 CA 19-9 이 측정되었고, 68예에서 CEA가 측정되었다. CEA는 모두 정상 범위였고, CA 19-9가 증가된 경우는 4예로 75.8 U/mL, 125 U/mL로 측정된 2예에서는 악성으로 나왔으나 42.3 U/mL, 190 U/mL로 측정된 2예에서는 양성으로 나타나 종양 표지자가 악성 예측인자가 되지 못하였다. 연령, 성별, 종양 의 크기 숫자, 위치 및 기능 여부에 대해 다변량 분석을 시 행한 결과 종양의 크기만이 악성도와 연관이 있는 것으로 나타났다.
2) 영상 소견(Table 3)
복부 전산화단층촬영에서 악성 환자 21예(67.7%), 양성 환자 57예(62.1%)가 췌장 종괴의 조영증강 소견을 보였다.
종양 내부에 석회화를 동반한 경우는 8예로 그 중 악성은 5 예, 양성은 3예였다. 종괴 내 저음영 소견을 보이는 9예 중 2예가 악성, 7예가 양성이었다. 종양에서 석회화가 관찰될 경우 악성 종양을 의심할 수 있으나(p=0.015), 종괴 내 저음
Han JH, et al. Clinical Characteristics and Malignant Predictive Factors of Pancreatic Neuroendocrine Tumors 101
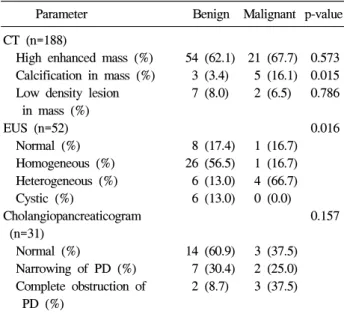
Table 3. Imaging Features that Predict Malignant Neuro- endocrine Tumor of the Pancreas
Parameter Benign Malignant p-value CT (n=188)
High enhanced mass (%) 54 (62.1) 21 (67.7) 0.573 Calcification in mass (%) 3 (3.4) 5 (16.1) 0.015 Low density lesion 7 (8.0) 2 (6.5) 0.786 in mass (%)
EUS (n=52) 0.016
Normal (%) 8 (17.4) 1 (16.7) Homogeneous (%) 26 (56.5) 1 (16.7) Heterogeneous (%) 6 (13.0) 4 (66.7) Cystic (%) 6 (13.0) 0 (0.0) Cholangiopancreaticogram 0.157 (n=31)
Normal (%) 14 (60.9) 3 (37.5) Narrowing of PD (%) 7 (30.4) 2 (25.0) Complete obstruction of 2 (8.7) 3 (37.5) PD (%)
CT, computed tomogram; EUS, endoscopic ultrasonography;
PD, pancreatic duct.
Table 4. Univariate Analysis of Factors Impacting on Median Disease-Specific 5 Year Survival
Median 5-year No of
Factors survival surviva p-value patients
(Mo) (%) Age
>50 years 57 89 0.1018
≤50 years 65 95
Gender (%)
Male 50 89 0.5070
Female 72 94
Location of tumor
Head of pancreas 59 87 0.8953 Non-head of pancreas 63 95
Tumor functional status
Functional tumor 75 100 0.0745 Nonfunctional tumor 47 84
Distant metastasis 0.0005
No 114 94
Yes 8 74 67
Size
>20 mm 59 82 0.0046
≤20 mm 63 100
Treatment of primary tumor
Resection 114 95 <0.001 No resection 8 24
Lymph node
Positive 7 68 0.0116
Negative 115 96
Surgical margin
RM (+) 7 67 0.1207
RM (−) 107 97
LVTE status
LVTE (+) 8 83 0.524
LVTE (−) 106 96
RM, resection margin; LVTE, lymphovascular tumor embolus.
영 소견은 종양의 악성화와 통계적인 유의성을 찾지 못했 다. 내시경 초음파를 시행한 경우는 총 52예로 이 중 췌장에 종괴가 보였던 경우가 43예로, 양성 종양일수록 균질한 에코 소견을 보였고, 악성 종양일수록 비균질한 에코소견을 보였 다(p=0.016). 췌담관 조영술을 시행한 경우는 31예로 주췌관 이 부분적인 협착을 보인 경우는 악성 2예, 양성 7예였고, 완 전 협착을 보인 경우는 악성 3예, 양성 2예였다. 주췌관의 완 전 협착과 악성 여부는 유의한 연관성은 없었다.
4. 치료 및 추적관찰 결과
122예 중 114예에서 근치 절제를 시행하였고, 원위부 췌 절제술 37예, 유문부 보존 췌두십이지장절제술 22예, 단순 종양 절제술이 19예, 고식적 췌두십이지장 절제술 16예, 부 분 췌절제술 16예, 췌전절제술 4예가 시행되었다. 근치 절제 후 방사선 치료를 시행한 5예로 그 중 1예에서는 항암 화학 요법도 같이 시행하였다. 근치 절제 후 항암 화학요법만 시 행한 경우는 2예였고, 수술 절제를 시행하지 않고 인터페론 의 면역 요법이나 간동맥 화학 색전술 또는 항암 화학 요법 을 시행한 예는 6예였다. 보존 치료만 시행한 예는 2예였다.
평균 45.0개월의 추적관찰 기간 동안, 근치 절제를 시행한 양성 종양 환자는 재발 없이 모두 생존하였다. 근치 절제를 시행한 후 재발한 예는 총 9예로 모두 악성 종양이었고, 종 양의 기능 측면에서 보았을 때 비기능 종양이 8예, 기능 종 양이 1예로 가스트린종이었다. 재발의 장소로는 간이 6예, 위가 1예, 복막전이가 2예로 간에 재발한 경우가 가장 많았
다. 간에서 재발한 경우 3예에서 수술 절제를 시행하였고 이후 고주파 열치료 또는 방사선 치료를 동반한 경우가 각 각 1예씩 있었다. 간에서의 재발에 대해 간동맥 화학 색전 술만 시행한 경우는 2예, 색전술 및 고주파 열치료를 한 경 우가 1예 있었다. 위에서 재발한 경우 수술 절제를 시행한 반면 복막전이로 재발한 경우는 보존 치료만 하였다. 추적 관찰 기간 동안, 질환과 연관되어 사망한 경우는 총 6예로 모두 악성 종양 환자였고, 수술 후 또는 진단 후 평균 40.3 개월 만에 사망하였다. 근치 절제 이후 재발하여 사망한 4 명을 분석해 보면, 간에 재발한 비기능 종양환자는 간 절제 를 시행하였음에도 불구하고 재발 9개월 만에 사망하였고, 간에 재발한 가스트린종 환자는 간동맥 화학 색전술를 시행 하였으나 재발한 지 29개월 만에 사망하였다. 위에 재발한
102 대한소화기학회지: 제53권 제2호, 2009
Fig. 1. Diease-specific survival comparing patients with large sized tumors (>20 mm) and small sized tumors (≤20 mm).
Fig. 2. Diease-specific survival comparing patients who under- went definitive resection of the primary tumor and those who did not.
Fig. 3. Diease-specific survival comparing patients with lymph node metastases and those without lymph node metastases.
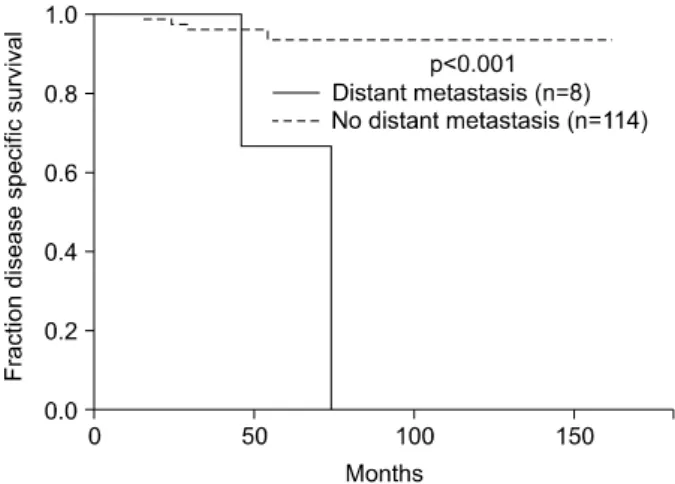
Fig. 4. Diease-specific survival comparing patients with distant metastases and those without distant metastases.
비기능 종양환자는 전위 절제술 시행 후 22개월 만에, 복막 전이로 재발한 비기능 종양환자 1명은 재발 27개월 만에 사 망하였다.
5. 생존에 영향을 미치는 인자
1개월부터 162개월까지 평균 45.0개월의 추적관찰 기간 동안 11명(9.0%)이 사망하였고, 이 중 질환과 연관이 있는 사망이 6예, 질환과 연관이 없는 사망이 5예였다. 111명 (91.0%)의 생존자 중 10명은 질환을 가지고 있는 채 생존하 고 있고, 101명은 질환 없이 생존 중이다. 122명의 췌장 신 경내분비 종양 환자의 질병특이 5년 생존율은 92%였다. 일 변량 분석을 시행했을 때 생존에 영향을 미치는 인자로는 종 양의 크기, 원발 병소의 수술 절제 유무, 림프절 침윤 여부, 원격 전이가 통계학적인 의미가 있었으나 나이, 성별, 종양 의 위치, 기능성의 여부, 절제 변연의 상태, 림프 맥관 종양
색전의 유무 등과는 의미 있는 연관성이 없었다(Table 4). 원 발 병소의 크기가 20 mm 이하인 경우는 평균 50개월의 추적 관찰 기간 동안(1-139개월) 모두 생존하였으나, 20 mm가 넘 는 경우 질병특이 5년 생존율은 82%였고(p=0.0046), 두 군 모두 중앙 생존기간에 도달하지 못했다(Fig. 1). 원발 병소를 수술 절제한 경우 중앙 생존기간에 도달하지 못했고, 질병 특이 5년 생존율은 95%였으나 수술 절제를 시행하지 않은 경우 중앙 생존기간은 24개월로 5년 내에 모두 사망하였다 (p=0.000)(Fig. 2). 림프절 침윤에 대해 분석하였을 때 림프절 침윤이 없는 경우 질병특이 5년 생존율은 96%, 림프절 침윤 이 있는 경우는 질병특이 5년 생존율이 68%였고(p=0.0116), 두 군 모두 중앙 생존기간에는 도달하지 못했다(Fig. 3). 원 격전이가 없는 경우 질병 특이 5년 생존율은 94%로 중앙 생존기간에 도달하지 못한 반면, 원격전이가 있는 경우는 질병특이 5년 생존율이 67%로 중앙 생존기간이 74개월이었
한정혜 외 9인. 췌장의 신경내분비 종양 122예의 임상양상 및 악성 예측인자 103
다(p=0.0005)(Fig. 4).
고 찰
췌장의 신경내분비 종양은 전형 발육능 줄기세포나 분화 된 성숙 내분비 세포에서 기원하며 호르몬 분비로 인한 임 상 증후군 유발 여부에 따라 기능 및 비기능 신경내분비 종 양으로 구분된다.6 기능 신경내분비 종양은 이소 호르몬을 분비함으로써 임상 증후군을 야기하는 반면 비기능 신경내 분비 종양은 종괴가 크거나 전이가 진행되었을 때 증상이 나타나게 된다. 따라서 비기능 신경내분비 종양은 복부 영 상 촬영 시 우연히 발견되는 경우가 많다.7 비기능 종양은 형태학적으로 기능 종양과 구분하기 힘들지만 기능 종양과 는 달리 불충분한 양의 호르몬을 생산하거나, 비활성형태의 호르몬을 분비하거나, 또는 충분한 양의 호르몬을 생산하지 만 분비 과정에서 부족한 양으로 분비하기 때문에 임상 증 상이 없는 것으로 여겨진다.8,9
여러 보고에 의하면 췌장 신경내분비 종양 환자의 평균 연령은 48-57세이며,10-14 기능 종양의 경우 평균 연령이 40 세로 비기능 종양보다 낮은 연령에서 발생하였다.13 이번 연 구에서도 췌장 신경내분비 종양 환자의 평균 연령은 49세였 으나 기능 종양의 평균 연령이 45세, 비기능 종양의 평균 연 령이 51세로 기능 종양의 평균 연령이 유의하게 낮았다 (p=0.015).
비기능 종양의 평균 크기는 36 mm, 기능 종양의 평균 크 기는 17 mm로 비기능 종양의 크기가 기능 종양보다 의미 있게 큰 것으로 나타났다(p<0.001). 이는 비기능 종양이 내 분비 호르몬에 의한 임상증상이 없기 때문에 주로 진행된 상태에서 발견되는 경우가 많고,15 평균 발견까지의 기간이 기능 신경내분비 종양에 비해 5개월에서 2-7년까지 길게 보 고되는 것과 연관이 있다.15,16
췌장의 신경 내분비 종양의 악성 진단은 일반적으로 주변 장기로의 침윤, 혈관으로의 침윤, 림프절 혹은 타 장기로의 전이가 있을 때 가능하다.10,11,17-20
췌장의 신경내분비 종양은 그 종류에 따라서 악성도가 다른데 일반적으로 비기능 종양 이 기능성 종양에 비해 악성도가 높아 50-90%이며15,21 진단 시 약 50% 정도에서는 이미 전이가 존재하며, 전이가 가장 잘 일어나는 부위는 간으로 알려져 있다.9,15,16 이번 연구에 서도 악성 비율은 기능 종양이 10.6%, 비기능성 종양이 36.0%로 비기능 종양일수록 악성빈도가 유의하게 높았으나 (p=0.015), 이전의 보고와 비교했을 때4,9,22 비기능 종양의 전 반적인 악성빈도는 낮았다. 이번 연구에서 진단 당시 전이 가 있던 경우는 비기능 종양이 25.3%, 기능 종양이 6.4%로 나타났다. 비기능 종양의 진단 당시 원격전이 소견이 보인 경우가 50-59%, 기능 종양의 진단 당시 원격전이 소견이 보
인 경우가 50-57%라는 이전의 보고와 비교할 때9,10 이번 연 구에서 진단 당시 원격전이가 있던 경우는 비기능 종양과 기능 종양 모두 이전보다 낮은 빈도를 보였다. 이는 이전의 연구에서는 기능 및 비기능 췌장의 신경내분비 종양의 크기 가 평균 60 mm (4-150 mm)였던데 반해 이번 연구에서의 종 양 크기는 기능 종양의 경우 평균 17.0 mm (4-35 mm), 비기 능 종양의 경우도 평균 37.7 mm (5-140 mm)로 비교적 작은 크기에서 진단되었기 때문에 전반적인 악성 빈도나, 진단 당시 전이 빈도가 낮았을 가능성이 있다. 이번 연구에서는 2000년 이후 총 췌장 신경내분비 종양의 진단 빈도가 급증 하였는데, 본원의 병상 규모 확장과 더불어 건강 검진 수검 률이 증가함으로써, 특히 전형적인 증상이 동반되지 않는 비기능 종양의 진단 빈도가 뚜렷이 증가하였기에 타 연구에 비해 종양의 크기가 작은 상태에서도 진단될 수 있었던 것 으로 생각한다.
만약 수술 전에 악성과 양성 종양을 감별할 수 있다면 수 술 범위를 종양의 국소 절제 또는 십이지장 보존 췌두부절 제술 등의 비교적 덜 침습적인 방법을 선택할 수 있어 임상 적인 의의가 있다고 생각하여 췌장 신경내분비 종양의 악성 예측 인자를 검토하였다. 연령, 성별, 종양의 위치는 양성과 악성 환자군 사이에 유의한 차이가 없었다. 또한 CEA, CA 19-9와 같은 종양표지자 측정도 악성 예측에 도움이 되지 못하였다. 일변량 분석을 시행하였을 때 종양의 크기가 20 mm 이상인 경우, 종양이 비기능성일 경우 악성 종양일 가 능성이 높았다. 그러나 다변량 분석을 시행한 결과 악성 예 측인자로서는 종양의 크기만이 유일한 인자로 나타났다. 이 는 종양의 크기가 클수록 국소 침윤, 혈관 침윤, 간 혹은 원 격 전이와의 연관성이 높다는 이전의 보고와도 연관 있는 결과라 하겠다.23
췌장 신경내분비 종양은 양성과 악성의 구별 없이 복부 전산화단층촬영 소견에서 일부 혹은 전체가 조영 증강되는 성향을 가진다. 이번 연구에서도 종양은 비교적 조영 증강 이 잘 되는 양상을 보였으며 일부에서는 출혈, 괴사, 낭성 변화로 인해 종양 내부에 저음영 소견을 보였지만 악성 여 부와는 연관성이 없었다. 종양 내부에 석회화를 보인 8예 중 5예에서 악성으로 나타났고, 의미가 있었다(p=0.015). 이 는 석회화를 동반한 10명의 췌장 신경내분비 종양 환자 중 에서 7명이 악성을 보였던 외국의 성적과 일치한다.24 또한 종양의 크기가 클수록 종괴 내부에 석회화와 괴사가 잘 일 어나는 것으로 알려져 있는데23 이번 연구에서는 석회화가 종양의 크기에는 연관관계가 있으며(p=0.016), 악성 종양을 예측할 수 있는 것으로 나타났으나, 종괴 내부의 저음영 소 견은 종양의 크기 및 악성 종양과의 연관 관계가 없는 것으 로 나타났다. 이번 연구에서는 43명의 환자에게 내시경초음 파검사를 시행하였는데, 양성 종양일수록 균질한 에코를,
104 The Korean Journal of Gastroenterology: Vol. 53, No. 2, 2009
악성 종양일수록 비균질한 에코 소견을 나타내는 경향을 보 였다(p=0.016). 대부분 췌장의 신경 내분비종양은 췌장선암 종과는 달리 췌관을 침범하지 않으나, 만약 췌관 조영술에 서 주췌관의 완전폐쇄를 보이는 경우 악성을 의심해야 한다 는 보고가 있다.25-28 그러나 이번 연구에서는 췌담관 조영술 을 시행한 31명 중 주췌관의 외부 압박 소견을 보인 경우는 3예로 모두 양성 환자였고, 부분협착을 보인 경우는 양성과 악성 환자 각각 2예였다. 주췌관의 완전협착을 보인 3예는 모두 악성 소견을 보였으나 주췌관의 협착과 악성 종양 간 에는 통계적인 유의점을 찾지 못했다. 총 환자 중 췌담관 조 영술을 시행한 환자의 비율이 25.4%로 극히 적었고, 조직 침윤 여부를 확인하지 못하였기 때문에 이에 대해서는 추가 연구가 필요할 것으로 생각한다.
췌장의 신경내분비 종양은 외과 절제가 완치를 기대할 수 있는 유일한 방법으로 수술 절제 이후 장기간의 추적 성적 은 좋은 것으로 보고되고 있다.10,29-31 이번 연구에서도 수술 을 시행한 114예에서 수술 절제가 시행되었고 현재 105명 (92.1%)이 재발의 증거 없이 추적 관찰 중이다. 췌장의 신경 내분비 종양의 기능 여부, 환자의 연령과 성별, 위치 등은 질병특이 생존율과 통계학적인 유의성이 없는 것으로 나타 났으며, 원발 병소의 수술 절제와 림프절 침윤 및 원격전이는 질병특이 생존율과 의미 있는 유의성이 있는 것으로 나타나 이전의 연구와 비슷한 결과를 보였다.10,11 그러나 종양의 크 기가 생존율에 영향을 주지 못했다는 과거의 보고11와는 달 리 이번 연구에서는 종양의 크기 또한 질병특이 생존율과도 의미 있는 연관성이 있는 것으로 나타났다. 췌장 신경내분 비 종양의 크기와 악성도 및 생존율에 대한 연관 관계는 각 연구마다 상이한 결과가 도출되는 경향이 있었다. 국내 연 구 결과만 하더라도 종양의 크기가 악성도와 관련이 있다고 보고한 예32와 관련이 없다고 보고된 예33가 공존하였고, 종 양의 크기와 생존율을 비교한 외국의 예에서는 서로 연관관 계가 없다는 결과11가 나와 종양의 크기, 악성도, 생존율의 상관관계에 대해 그 결론이 혼선을 빚고 있었다. 그러나 이 번 연구에서는 종양의 크기가 악성도 및 생존율과도 연관관 계가 있다는 비교적 일관된 결과가 나왔다. 결론으로 췌장 의 기능 및 비기능 신경내분비 종양은 서로 다른 임상양상 과 방사선 특징을 가지고 있으나, 기능 여부와 관계 없이 종 양의 크기가 클수록 악성도와 독립적인 연관관계가 있을 뿐 만 아니라 질병특이 생존율과도 관련이 있어, 종양의 크기 가 악성 예측도 및 예후인자로 중요한 의미를 지닌다고 할 수 있다.
요 약
목적: 췌장의 신경내분비 종양은 매우 드문 종양이나, 진
행속도가 늦어 췌장선암종에 비해서는 예후가 좋다. 그러나 악성 신경내분비 종양은 양성에 비해 예후가 불량하다. 따 라서 이번 연구에서 췌장의 신경내분비 종양의 임상 특징과 악성 예측인자 및 생존율에 영향을 미치는 인자에 대해 조 사하였다. 대상 및 방법: 1990년 11월부터 2006년 12월까지 조직검사에서 췌장의 신경내분비 종양으로 진단받은 122명 의 환자를 대상으로 하여 임상기록, 방사선 소견, 수술기록, 병리기록 등을 후향 검토하였다. 결과: 122명의 췌장 신경 내분비 종양 환자 중 75명(61.5%)은 비기능 종양이었고 평 균 관측기간은 45.0±38.0개월이었다. 환자의 평균 연령은 48.9±14.0세였으며, 성별에 따른 차이는 없었다. 가장 흔한 임상증상은 비기능 종양에서는 복통(44.0%), 인슐린종에서 는 저혈당성 신경증상(100%), 가스트린종에서는 설사(60%) 였다. 종양의 크기는 4-140 mm로 평균 29.8±23.2 mm였다.
조직학적으로는 32명(26.2%)이 악성 소견을 보였다. 일변량 분석에서는 종양의 크기가 클수록(>20 mm), 비기능성 종양 일수록 악성 소견을 나타내었으나(p<0.001, p=0.002), 다변 량 분석에서는 종양의 크기만이 유일한 악성 예측인자였다 (p=0.001). 복부 전산화단층촬영에서 종괴 내에 석회화가 보 인 환자 8명 중 5명이 악성 소견을 보여 의미가 있었다 (p=0.015). 수술 절제는 114명에서 이루어졌고, 양성의 췌장 신경내분비 종양 환자는 수술 후 재발 없이 모두 생존하였 다. 32명의 악성 종양 환자 중 6명이 수술 후 또는 진단 후 평균 40.3개월 만에 사망하였다. 전체 환자의 질병특이 5년 생존율은 92%였고, 종양의 크기가 작을수록, 원발 병소를 수술 절제할수록, 림프절 침윤이나 원격 전이가 없을수록 생존율이 의미 있게 높았다. 결론: 췌장의 신경내분비 종양 은 기능 여부와 관련 없이 크기가 클수록 악성화의 가능성 이 높으며 또한 질병특이 생존율도 의미 있게 낮은 것으로 나타났다.
색인단어: 췌장, 신경내분비 종양
참고문헌
1. Wick MR, Graeme-Cook FM. pancreatic neuroendocrine neo- plasms; a current summary of diagnostic, prognostic, and dif- ferential diagnostic information. Am J Clin Pathol 2001;115:
S28-45.
2. Norton JA. Neuroendocrine tumors of the pancreas and duodenum. Curr Probl Surg 1994;31:77-156.
3. Furukawa H, Mukai K, Kosuge T, et al. Nonfunctioning islet cell tumors of the pancreas: clinical, imaging and pathological aspects in 16 patients. Jpn J Clin Oncol 1998;28:255-261.
4. Ectors N. Pancreatic endocrine tumors: diagnostic pitfalls.
Han JH, et al. Clinical Characteristics and Malignant Predictive Factors of Pancreatic Neuroendocrine Tumors 105
Hepatogastroenterology 1999;46:679-690.
5. Eriksson B, Oberg K. Neuroendocrine tumours of the pancreas. Br J Surg 2000;87:129-131.
6. Simon P, Spilcke-Liss E, Wallaschofski H. Endocrine tumors of the pancreas. Endocrinol Metab Clin North Am 2006;35:
431-447.
7. Yamada T, Alpers DH. Endocrine neoplasms of the pancreas.
Textbook of gastroenterolgoy. 2nd ed. Philadelphia:
Lippincott Williams & Wilkins, 2003.
8. Delcore R, Friesen SR. Gastrointestinal neuroendocrine tumors. J Am Coll Surg 1994;178:187-211.
9. Azimuddin K, Chamberlain RS. The surgical management of pancreatic neuroendocrine tumors. Surg Clin North Am 2001;
81:511-525.
10. Chu QD, Hill HC, Douglass HO Jr, et al. Predictive factors associated with long-term survival in patients with neuro- endocrine tumors of the pancreas. Ann Surg Oncol 2002;9:
855-862.
11. Jarufe NP, Coldham C, Orug T, et al. Neuroendocrine tu- mours of the pancreas: predictors of survival after surgical treatment. Dig Surg 2005;22:157-162.
12. Kang TW, Lee KT, Ryu MK, et al. Clinical features of neu- roendocrine tumor of the pancreas: single center study.
Korean J Gastroenterol 2006;48:112-118.
13. Kazanjian KK, Reber HA, Hines OJ. Resection of pancreatic neuroendocrine tumors: results of 70 cases. Arch Surg 2006;141:765-769.
14. Lo CY, van Heerden JA, Thompson GB, Grant CS, Soreide JA, Harmsen WS. Islet cell carcinoma of the pancreas. World J Surg 1996;20:878-883.
15. Broughan TA, Leslie JD, Soto JM, Hermann RE. Pancreatic islet cell tumors. Surgery 1986;99:671-678.
16. Kent RB 3rd, van Heerden JA, Weiland LH. Nonfunctioning islet cell tumors. Ann Surg 1981;193:185-190.
17. Evans DB, Skibber JM, Lee JE, et al. Nonfunctioning islet cell carcinoma of the pancreas. Surgery 1993;114:1175-1181.
18. Phan GQ, Yeo CJ, Hruban RH, Lillemoe KD, Pitt HA, Cameron JL. Surgical experience with pancreatic and peri- pancreatic neuroendocrine tumors: review of 125 patients. J Gastrointest Surg 1998;2:472-482.
19. Matthews BD, Heniford BT, Reardon PR, Brunicardi FC, Greene FL. Surgical experience with nonfunctioning neuro- endocrine tumors of the pancreas. Am Surg 2000;66:1116- 1122.
20. Dralle H, Krohn SL, Karges W, Boehm BO, Brauckhoff M,
Gimm O. Surgery of resectable nonfunctioning neuro- endocrine pancreatic tumors. World J Surg 2004;28:1248- 1260.
21. Eckhauser FE, Cheung PS, Vinik AI, Strodel WE, Lloyd RV, Thompson NW. Nonfunctioning malignant neuroendocrine tu- mors of the pancreas. Surgery 1986;100:978-988.
22. Oberg K, Eriksson B. Endocrine tumours of the pancreas.
Best Pract Res Clin Gastroenterol 2005;19:753-781.
23. Buetow PC, Parrino TV, Buck JL, et al. Islet cell tumors of the pancreas: pathologic-imaging correlation among size, ne- crosis and cysts, calcification, malignant behavior, and func- tional status. AJR Am J Roentgenol 1995;165:1175-1179.
24. Imhof H, Frank P. Pancreatic calcifications in malignant islet cell tumors. Radiology 1977;122:333-337.
25. Kaufman AR, Sivak MV Jr, Ferguson DR. Endoscopic retro- grade cholangiopancreatography in pancreatic islet cell tumors. Gastrointest Endosc 1988;34:47-52.
26. Mao C, Howard JM. Pancreatitis associated with neuro- endocrine (islet cell) tumors of the pancreas. Am J Surg 1996;171:562-564.
27. Obara T, Shudo R, Fujii T, et al. Pancreatic duct obstruction caused by malignant islet cell tumors of the pancreas.
Gastrointest Endosc 2000;51:604-607.
28. Sugiyama M, Abe N, Izumisato Y, et al. Differential diag- nosis of benign versus malignant nonfunctioning islet cell tu- mors of the pancreas: the roles of EUS and ERCP.
Gastrointest Endosc 2002;55:115-119.
29. Legaspi A, Brennan MF. Management of islet cell carcinoma.
Surgery 1988;104:1018-1023.
30. Grama D, Eriksson B, Martensson H, et al. Clinical charac- teristics, treatment and survival in patients with pancreatic tu- mors causing hormonal syndromes. World J Surg 1992;16:
632-639.
31. Madura JA, Cummings OW, Wiebke EA, Broadie TA, Goulet RL Jr, Howard TJ. Nonfunctioning islet cell tumors of the pancreas: a difficult diagnosis but one worth the effort. Am Surg 1997;63:573-577.
32. Jang HJ, Kim SC, Lee SG, Han DJ. Nonfunctioning islet cell tumors of the pancreas. Korean J Gastroenterol 1999;33:837- 844.
33. Kim HJ, Kim MH, Lee SK, et al. Clinical characteristics and malignant predictive factors in patients with nonfunctioning islet cell tumors of the pancreas. Korean J Gastroenterol 2003;42:57-62.