DOI 10.17480/psk.2018.62.2.77
Caffeic acid phenethyl ester의 cytochrome P450 저해 활성 평가
류창선 · 박지은 · 김상겸*
충남대학교 약학대학
(Received February 12, 2018; Revised March 28, 2018; Accepted April 4, 2018)
In vitro assessment of cytochrome P450 inhibition by caffeic acid phenethyl ester
Chang Seon Ryu, Ji-Eun Park, and Sang Kyum Kim*
College of Pharmacy, Chungnam National University, Daejeon, 305-763, Korea
Abstract — Caffeic acid phenethyl ester (CAPE) is one of the major active components of propolis showing inhibitory activ- ity against cytochrome P450 (CYP). The purpose of this study was to determine CYP inhibitory potential and metabolic sta- bility of CAPE using human liver microsomes (HLM) for characterization of its metabolic properties. Among CYP isoforms including CYP1A2, 2A6, 2B6, 2C8, 2C9, 2C19, 2D6, 2E1 and 3A4, CAPE exhibited strong inhibitory potential against CYP1A2 and 2C9, moderate against CYP2E1, 2B6, 2C8, 2C19 and 3A4, and weak against CYP 2D6 and 2A6, based on the IC50 values. The inhibition of CYP1A2 but not CYP2C9 was increased by preincubation with CAPE and NADPH, suggesting that the CAPE-induced CYP1A2 inhibition may be metabolism-dependent. In metabolic stability study using HLM, CAPE was rapidly hydrolyzed to caffeic acid in a NADPH-independent manner. Caffeic acid exhibited week CYP inhibitory activity, relative to CAPE. These results raise the possibility that CAPE plays a role in propolis-mediated CYP inhibition.
Keywords cytochrome p450, drug-drug interaction, caffeic acid phenethyl ester, propolis
벌집을 구성하고 유지하는 성분에서 유래한 프로폴리스(propolis) 는 꿀벌에 의해 침엽수, 식물의 새싹 등과 같은 물질로부터 만들 어진다. 프로폴리스는 가장 널리 사용되는 기능성 식품의 하나 로 2016년 건강 기능 식품의 품목 매출액 기준으로 103.1억원을 차지하고 있다.1)프로폴리스의 항산화 활성을 포함한 생리활성 은 플라보노이드, 페놀릭 산, 에스터, 알데하이드, 알코올 및 케 톤과 퀴논, 쿠마린, 세스퀴테르펜 등 유효성분과 관련이 있다.2) 프로폴리스의 구성성분과 구성비율은 벌의 종과 벌집을 만들 때 사용된 식물 등에 따라 달라진다.3,4)
카페익 산 페네칠 에스테르(caffeic acid phenethyl ester;
CAPE)는 프로폴리스의 가장 중요한 생리 활성 물질의 하나로 적 혈구의 지질 과산화, 세포 가닥 파손 및 단백질의 단편화 등에
대한 보호 기능5), 인슐린 저항성의 경감 기능 등이 보고 되었다.6) Cytochrome P450 (CYP)은 약물대사 효소 중 가장 중요한 효 소계로 인간에서 57개의 기능적 동형단백질(isoform)로 존재하 며 주로 간에 발현된다.7) CYP는 다양한 내인성 및 외인성 물질 에 의해 발현과 활성이 조절되며 약물의 병용 투여시 CYP 저해 와 유도는 임상약물치료에서 약물-약물 상호작용(drug-drug interaction)을 유발하는 대표 기전이다.8)
최근, 브라질산 녹색 프로폴리스 에탄올 추출물9), 프로폴리스 건조분말추출물10)등이 CYP 활성을 저해하는 것으로 보고되었 다. 또한 주요 구성성분인 폴리페놀11), apigenin과 genistein에 의한12) CYP 활성 변화에 대한 연구가 보고되었다. 본 연구에서 는 프로폴리스의 유효 성분인 CAPE에 의한 CYP의 직접적 억제 효과 및 기전을 연구하였다. 선행연구에서 확립된 실험계를13,14)바 탕으로 인간 간세포로부터 분리된 microsomes (HLM)을 활용하 여 9개 CYP isoform에 대한 저해효과를 10개의 기질을 이용하 여 액체 크로마토그래피-사중극자 질량분석기로 분석하는 방법 을 이용하였다. 또한 CAPE의 대사적 안정성과 대사체 분석을 수행하여 이 물질의 대사적 특성을 규명하였다.
#
Corresponding Author Sang Kyum Kim
College of Pharmacy, Chungnam National University, Daejeon, 305-763, Korea
Tel.: 042-821-5930 Fax.: 042-823-6566 E-mail: [email protected]
Short Report
종설재료 및 실험 방법 (Experimental Methods)
시약
Phenacetin, acetaminophen, bupropion, coumarin, 7- hydroxycoumarin, caffeic acid, tolbutamide, 4-hydroxytolbutamide, dextromethorphan, chlorzoxazone, 6-hydroxychlorzoxazone, testosterone, fluvoxamine, furafylline, ketoconazole, carbamazepine, CAPE및 환원된 β-nicotinamide adenine dinucleotide phosphate (NADPH) 는 Sigma-Aldrich (St. Louis, MO, USA)로부터 구입 하였다. Hydroxybupropion, 4'-hydroxymephenytoin, 1'- hydroxymidazolam 및 6β-hydroxytestosterone은 BD Gentest Co. (Woburn, MA, USA)로부터 구입하였다. Midazolam은 부 광약품(서울, 대한민국)에서 구입하였다. Pooled human liver microsomes (BD UltraPool™ HLM 150, lot 38289)은 BD Gentest Co. (Woburn, MA, USA)로부터 구입하였다. 모든 시약 은 분석용 또는 구입 가능한 가장 높은 등급을 사용하였다.
CYP 저해 평가
CAPE와 caffeic acid의 CYP 직접 저해와 대사 의존적 저해 방 법은 이미 보고된 실험방법을 바탕으로 수행되었다.13,14) CAPE 와 caffeic acid를 각각 DMSO에 100 mg/ml 그리고 3차 증류수 에 10 mg/ml 농도로 녹이고 3을 공비로하여 계열 희석하였다.
8× 12 rack (1.2 mL; VWR, Emeryville, CA, USA)에 8-well tube strips을 반응에 이용하여, 최종 농도 1 mg/mL 인간 마이 크로좀 단백질 분획, 0.1 M phosphate buffer (pH 7.4), 1 mM NADPH와 다양한 CYP isoform의 CYP isoform-specific 개별 기 질의 혼합액의 2개의 부분으로(A set: phenacetin, coumarin, amodiaquine, S-mephenytoin, dextromethorphan, and midazolam;
B set: bupropion, tolbutamide, chlorzoxazone, and testosterone) 나누어 의해 최종 부피 200 μL로 구성되었다. 기질은 각각의 Michaelis-Menten constant (Km) 값에 맞게 다음과 같이 농도를 설정하였다: phenacetin 50 μM, coumarin 5 μM, bupropion 50μM, tolbutamide 100 μM, S-mephenytoin 100 μM, dextromethorphan 5μM, chlorzoxazone 50 μM, midazolam 5μM, 및 testosterone 50 μM. 모든 실험에 사용된 기질은 acetonitrile 또는 DMSO에 녹여 희석하였다 유기 용매의 조성이 최종 부피의(v/v) 1.0% 이하가 되도록 설정하였다. 반응 시간은 37oC에서 5분간의 미리 가열한 반응액에, NADPH용액을 가하 여 10분간 37°C 진탕배양기를 이용하여 incubation하였다. 반응 종결은 200 μL 부피의 ice-cold acetonitrile(내부 표준물질로 50 nM carbamazepine을 포함)을 가하여 이루어졌다. 각 부분 반 응액(A, B set) 을 4oC, 3,000 rpm, 20분간 원심분리한 후, 각 부 분 반응액을 1:1로 96 well plate에서 희석하였다.
대사의존적 CYP 저해 평가는 대사체의 생성을 위하여 CYP의
기질 없이 HLM과 CAPE를 NADPH의 존재 유무에 따라 30분 간 반응시켜 진행하였다.13) 반응 후 7개의 농도 구간으로(최종 농 도 0에서 100 μg/ml) 전반응시킨 반응액을 희석시키고 1 mM NADPH와 CYP1A2 (phenacetin 50 μM)과 CYP2C9 (tolbutamide 100μM)의 기질을 가하고 5분간 추가로 반응하였다. NADPH를 가한 군과 가하지 않은 군의 IC50의 차이를 통하여 대사의존적 CYP 억제활성을 평가하였다.13)
반응액을 Shimadzu LC-20A prominence 고성능 액체 크로마 토 그래피(Shimadzu Corp. Tokyo, Japan)와 Turbo IonSpray™
source (Applied Biosystems, Foster City, CA, USA)가 장착된 API3200™ Q-trap LC-MS/MS (Applied Biosystems, Foster City, CA, USA)로 구성된 분석 시스템을 통해 미리 확립된 분석 조건을 이용하여 분석하였다.14)샘플의 분석은 positive와 negative (6-hydroxychlorzoxazone) multiple reaction monitoring (MRM) mode를 이용하여 각각 형성된 대사체와 내부 표준물질의 peak 넓이를 통해 계산하였다. 분석의 dwell 시간은 각 채널 별로 0.08 초로 설정하였다. 분석된 값들은 Analyst™ 소프트웨어(version 1.5.2, Applied Biosystems, Foster City, CA, USA)를 통해 처리 하였다.
마이크로좀 대사 안정성 평가 및 대사체 분석
CAPE과 caffeic acid의 인간 마이크로좀에서의 NADPH 의존 적 대사 안정성 평가를 위해 1 mg/mL 인간 마이크로좀 단백질 분획을 0.1 M phosphate buffer (pH 7.4)에서 4 mM MgCl2, 1 mM nicotinamide adenine dinucleotide phosphate, 5 mM glucose-6- phosphate와 1 unit/mL glucose-6-phosphate dehydrogenase를 포함 한 NADPH-generating system과 함께 진탕 배양 하였다. 5분간 의 예비 배양 후에 반응 NADPH-generating system를 가하여 반응을 시작하였고 내부표준물질인 200 nM 농도의 4-methyl umbelliferone를 포함하는 ice-cold acetonitrile 가하여 반응을 종 결시켰다. 반응액은 원심분리기에서 4oC에서 3000 × g로 20분간 원심분리하여 상등액을 질량분석기에 연결된 HPLC에 주입하였 다. 반응액은 CYP 저해 실험계와 동일한 질량분석 시스템을 활 용하여 Waters Xterra MS C18 column (2.1 mm × 50 mm, 입자 경 3.5 μm; Waters, Milford, MA, USA)과 SecurityGuard™ C18 guard column (2.0 mm× 4.0 mm; Phenomenex, Torrance, CA, USA)을 이용하여 분리하고 negative MRM mode에서 검출하였 다. CAPE와 caffeic acid의 MRM transition은 282.9>135.1과 178.9>135.1을 이용하였다.
자료 분석
CYP의 활성은 대조군의 백분율로 환산하였다. 대사안정성 평 가는 0시간을 대조군의 백분율로 환산하였다. 모든 결과는 평균
±표준편차로 나타내었다. 비선형 회귀분석은 GraphPad Prism,
version 5.0. (GraphPad Software Inc., San Diego, CA, USA) 을 이용하여, IC50과 95% 신뢰구간으로 나타내었다. 실험군 사 이의 차이는 Student’s t-test를 이용하여 검증하였다.
결과 및 고찰 (Results and Discussion)
특정 CYP isoform에 대한 inhibition 양상을 확인하고 실제 약물 의 투여 시 발생할 수 있는 약물상호작용을 평가하기 위해서 CYP probe 기질의 cocktail을 이용한 assay를 실시하였다. CYP3A4 저 해제인 ketoconazol을 양성 대조군으로 사용하여, 기존 문헌의 IC50값과 비교하여 본 실험계가 잘 구축되었음을 확인하였다 (data not shown).
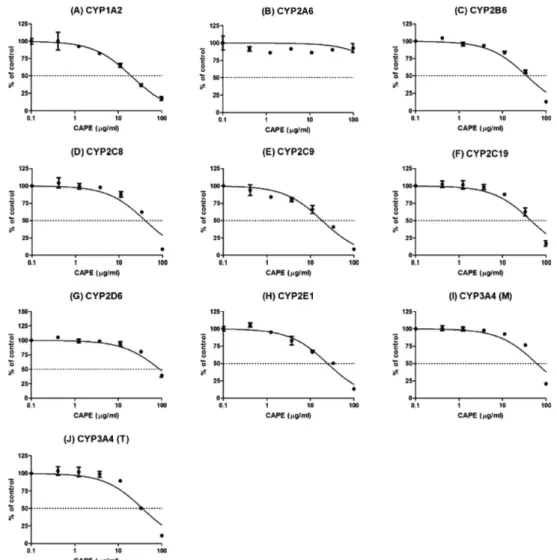
CAPE의 CYP 개별 isoform에 대한 IC50값 (95% 신뢰구간)은 CYP1A2에서 19.67 (6.87~22.94) μg/mL, CYP2B6에서 35.81 (28.80~44.54)μg/mL, CYP2C8에서40.49 (28.96~55.78) μg/mL,
CYP2C9에서 18.47 (15.05~22.66) μg/mL, CYP2C19에서 44.98 (34.58~58.51)μg/mL, CYP2D6에서 90.32 (73.46~111.1) μg/
mL, CYP2E1에서 24.70 (20.59~29.64) μg/mL, midazolam을 기질 로 할 때 CYP3A4에서 60.65 (44.87~81.97) μg/mL, testosterone 을 기질로 한 CYP3A4에서 33.76 (26.41~48.43) μg/mL으로 관찰 되었다. CYP2A6에서는 유의적 저해가 일어나지 않았다(Fig. 1).
계산된 IC50값에 근거하여 CAPE가 CYP1A2와 CYP2C9에 대 해 강한 억제, CYP2E1, 2B6, 2C8, 2C19와 3A4에 중간 정도 억 제 그리고 CYP2D6와 2A6에 약한 억제효과를 나타내었다. 이 결과는 CAPE가 프로폴리스의 CYP 억제에 기여함을 시사한다.
CAPE의 CYP 억제효과가 CAPE자체보다 CYP 매개성 대사 체에 기인할 가능성을 확인하기 위해 CAPE에 의해 가장 큰 억 제효과를 보인 CYP1A2와 CYP2C9를 대상으로 추가 실험을 수 행하였다. CAPE로부터 대사체가 생성될 수 있도록 HLM과 NADPH를 가하고 반응시킨 후 얻은 CYP의 IC50과 NADPH 없
Fig. 1 − Effect of caffeic acid phenethyl ester (CAPE) on activities of CYP1A2 (A), CYP2A6 (B), CYP2B6 (C), CYP2C8(D), CYP2C9 (E),
CYP2C19 (F), CYP2D6 (G), CYP2E1 (H), CYP3A4 (midazolam as a substrate) (I), and CYP3A4 (testosterone as a substrate) (J) in
pooled human liver microsomes (HLM). Each data point represents the mean±SD of three independent samples.
이 반응시킨 후 얻은 CYP의 IC50를 비교하였다. NADPH로 CAPE를 반응시켰을 때 얻은 IC50 값으로 반응시키지 않고 얻은 IC50값을 나누었을 때 CYP1A2는 2.0 그리고 CYP2C9에서 1.1 로 CAPE에 의한 CYP1A2의 저해가 대사 의존적일 가능성을 시 사한다(Fig. 2).
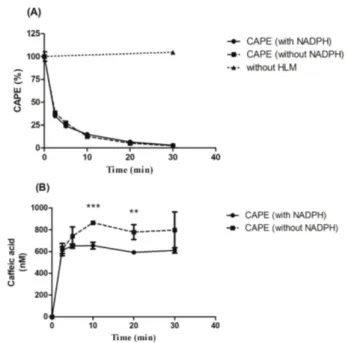
CAPE는 혈액 및 간을 포함한 다양한 esterase에 의해 caffeic acid로 대사된다.15) HLM에서 CAPE의 대사적인 특성을 분석하 기 위해 1 μM CAPE를 기질로 하여 대사적 안정성과 caffeic acid 의 생성을 조효소인 NADPH의 유무에 따라서 평가하였다. 안정 성 평가에서 CAPE는 NADPH의 유무와 관련 없이 반감기가 3 분 이내로 매우 신속하게 제거되었다(Fig. 3A). 반면 HLM이 없 이 반응시켰을 때에는 반응 30분까지 안정적으로 농도가 유지되 었다. 이 결과는 CAPE의 대사가 HLM에 존재하는 효소에 의존 적이나 NADPH에 비의존적인 반응에 의해 제거됨을 시사한다.
CAPE를 HLM과 반응시키고 caffeic acid의 생성을 측정하였다.
CAPE로부터 caffeic acid의 생성은 NADPH의 존재 유무와 무관 하게 매우 신속하게 생성되었다(Fig. 3B). HLM에 1 μM CAPE
를 가하고 반응 후 caffeic acid의 최대 생성량은 NADPH가 없 는 조건과 있는 조건에서 각각 864±11 μM과 655±31 μM로 대 부분이 caffeic acid로 전환되었다. Caffeic acid의 생성량은 NADPH가 있는 조건에 비하여 NADPH가 없는 조건에서 반응 후 10분과 20분에 유의적으로 증가하였다. 이 결과는 일부 CAPE 가 caffeic acid가 아닌 다른 물질로 CYP에 의존적인 대사를 받 았을 가능성을 시사한다.
Caffeic acid가 HLM에서 CAPE의 주대사체로 평가되었기 때 문에 caffeic acid가 CYP의 활성에 미치는 영향을 평가하였다.
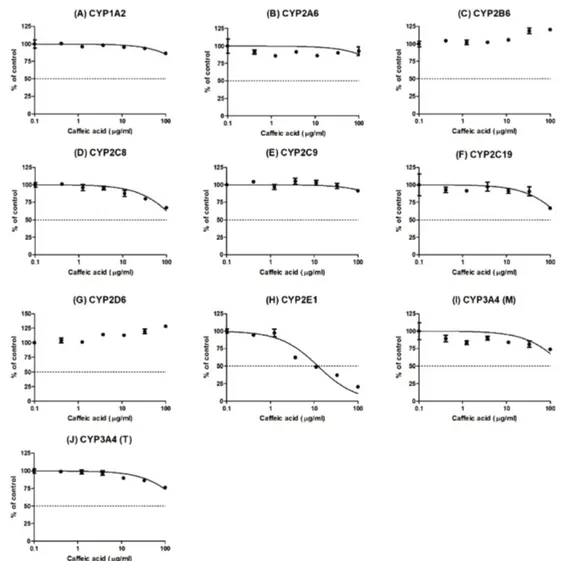
Caffeic acid의 CYP 개별 isoform에 대한 IC50값은 CYP2E1에 서 12.21 (9.078~16.41) μg/mL 이고 다른 isoform에서는 최고 농도에서 50% 미만의 저해가 관찰되어 IC50를 구할 수 없었다 (Fig. 4). 이 결과는 HLM에서 CYP의 억제가 대사체인 caffeic acid가 아닌 CAPE 자체나 다른 대사체에 기인할 가능성을 시사 한다.
CAPE의 대사적 안정성을 평가한 연구는 랫드 혈장에서 CAPE 는 빠른 속도로 분해되었으나16)인간 혈장에서는 상대적으로 안 정적인 것으로 보고 되었다.15)본 실험은 간 마이크로좀에서 CAPE가 NADPH에 비의존적으로 빠르게 분해되는 것으로 확인 하였다. 이는 간에 존재하는 esterase의 활성에 의해서 CAPE가 caffeic acid로 전환됨을 시사한다. Caffeic acid는 CAPE의 대사 체로서 CYP의 억제에 기여하지 않으나 CYP2E1의 경우 CAPE 에 비하여 caffeic acid의 억제효과가 우세하였다.
Fig. 2 − Evaluation of the metabolism dependence of the inhibitory effects of CAPE on CYP1A2 (A) and CYP2C9 (B) in HLM.
CAPE was pre-incubated in pooled human liver microsomes with (black circle) or without (white circle) NADPH for 30 min. Each data point represents the mean±SD of three independent samples. *,**,***Significantly different between two groups at P<0.05, P<0.01 or P<0.001, respectively (Student’s t-test).
Fig. 3 − Metabolic stability of CAPE (A) and its metabolite
identification (B) in HLM incubated with or without
NADPH. Each data point represents the mean±SD of three
independent samples. **,***Significantly different from the
control at P<0.01 or P<0.001 (Student’s t-test).
CAPE의 CYP1A2에 대한 저해는 이미 보고 된바 있다.17)또 한 CAPE는 랫드에서 CYP1A2와 CYP2B1/2의 발현을 감소 시 키는 것으로 보고 되었다.18)또한 CAPE는 hypoxia-inducible factor-1를 유도함으로써 3-methylcholanthrene에 의해 유도된 CYP1A1에 대해 저해 효과를 나타내었다.19)본 연구는 CAPE가 CYP1A2를 대사의존적으로 억제하여 CYP1A2의 억제에 CAPE 의 대사체가 관여함을 보이고 있다. 또한 CYP1A2 외에도 CYP2C9을 비롯하여 다양한 CYP가 CAPE에 의해 억제되었다.
결 론 (Conclusion)
본 연구에서 대표적인 건강기능식품인 프로폴리스의 지표 성 분 중 하나인 CAPE가 9개의 대표적인 CYP 동형 단백질의 활 성에 미치는 영향을 HLM 과 LC-MS/MS를 이용하여 평가하였 다. 실험결과 CAPE는 CYP1A2와 CYP2C9에 대해 강한 억제능
을 보였다. HLM에서 CAPE는 NADPH에 비의존적으로 매우 신 속하게 caffeic acid로 전환되어 esterase가 CAPE의 대사에 관 여할 가능성을 시사하였다. 결론적으로 CAPE는 프로폴리스의 CYP 억제에 기여할 가능성을 시사한다.
감사의 말씀 (Acknowledgment)
이 연구는 충남대학교 학술연구비에 의해 지원되었음
References
1) Korea Agency of HACCP Association and Services, 2016 Korean market analysis of functional foods (2017).
2) Sobocanec S., Sverko V., Balog T., Sarić A., Rusak G., Likić S., Kusić B., Katalinić V., Radić S. and Marotti T.: Oxidant/
Fig. 4 − Effect of caffeic acid on activities of CYP1A2 (A), CYP2A6 (B), CYP2B6 (C), CYP2C8(D), CYP2C9 (E), CYP2C19 (F), CYP2D6 (G),
CYP2E1 (H), CYP3A4 (midazolam as a substrate) (I), and CYP3A4 (testosterone as a substrate) (J) in pooled HLM. Each data point
represents the mean±SD of three independent samples.
antioxidant properties of Croatian native propolis. J. Agric.
Food Chem. 54, 8018 (2006).
3) Ahn M.R., Kumazawa S., Hamasaka T., Bang K.S., Nakayama T.: Antioxidant activity and constituents of propolis collected in various areas of China. Food Chem. 101, 1383 (2007).
4) Sibel S., Semiramis K.: Chemical composition and antibacterial activity of propolis collected by three different races of honeybees in the same region. J .Ethnopharmacol. 99, 69 (2005).
5) Wang, T., Chen, L., Wu, W., Long, Y. and Wang, R.: Potential cytoprotection: antioxidant defense by caffeic acid phenethyl ester against free radical-induced damage of lipids, DNA, and proteins. Can. J. Physiol. Pharmacol. 86, 279 (2008).
6) Nie J., Chang Y., Li Y., Zhou Y., Qin J., Sun Z., Li H.: Caffeic acid phenethyl ester (propolis extract) ameliorates insulin resistance by inhibiting JNK and NF-κB inflammatory pathways in diabetic mice and HepG2 cell models. J. Agric. Food Chem.
65, 9041 (2017).
7) Guengerich F.P.: Role of cytochrome P450 enzymes in drug_drug interactions. Adv. Pharmacol. 43, 7 (1997).
8) Zanger U.M., Schwab M.: Cytochrome P450 enzymes in drug metabolism: regulation of gene expression, enzyme activities, and impact of genetic variation. Pharmacol Ther. 138, 103 (2013).
9) Naramoto K., Kato M. and Ichihara K.: Effects of an ethanol extract of Brazilian green propolis on human cytochrome P450 enzyme activities in vitro. J. Agric. Food Chem., 62, 11296 (2014).
10) Ryu C.S., Oh S.J., Oh J.M., Lee J.Y., Lee S.Y., Chae J.W., Kwon K.I., Kim S.K.: Inhibition of cytochrome P450 by propolis in human liver microsomes. Toxicol. Res. 32, 207 (2016).
11) Kimura Y., Ito H., Ohnishi R., Hatano T.: Inhibitory effects of polyphenols on human cytochrome P450 3A4 and 2C9 activity.
Food Chem. Toxicol., 48, 429 (2010).
12) Shimada H., Eto M., Ohtaguro M., Ohtsubo M., Mizukami Y., Ide T., Imamura Y.: Differential mechanisms for the inhibition of human cytochrome P450 1A2 by apigenin and genistein. J.
Biochem. Mol. Toxicol., 24, 230 (2010).
13) Lee J.Y., Lee S.Y., Oh S.J., Lee K.H., Jung Y.S., Kim S.K.:
Assessment of drug-drug interactions caused by metabolism- dependent cytochrome P450 inhibition. Chem. Biol. Interact.
198, 49 (2012).
14) Lee K.S., Kim S.K.: Direct and metabolism-dependent cytochrome P450 inhibition assays for evaluating drug-drug interactions. J. Appl Toxicol. 33, 100 (2013).
15) Celli N., Dragani L.K., Murzilli S., Pagliani T., Poggi A.: In vitro and in vivo stability of caffeic acid phenethyl ester, a bioactive compound of propolis. J. Agric. Food Chem. 55, 3398 (2007).
16) Celli N., Mariani, B., Dragani L. K., Murzilli S., Rossi C., Rotilio D.: Development and validation of a liquid chromatographic- tandem mass spectrometric method for the determination of caffeic acid phenethyl ester in rat plasma and urine. J. Chromatogr., B, 810, 129 (2004).
17) Jaikang C., Chaiyasut C., Narongchai P., Niwatananun K., Narongchai S., Kusirisin W.: Inhibitory effects of caffeic acid ester analogues on free radicals and human liver microsome CYP1A2 activities. Med Chem 7, 99 (2011).
18) Beltrán-Ramírez O., Pérez R.M., Sierra-Santoyo A., Villa-Treviño S.: Cancer prevention mediated by caffeic acid phenethyl ester involves cyp2b1/2 modulation in hepatocarcinogenesis. Toxicol.
Pathol. 40, 466 (2012).
19) Kim H.G., Han E.H., Im J.H., Lee E.J., Jin S.W., Jeong H.G.:
Caffeic acid phenethyl ester inhibits 3-MC induced CYP1A1 expression through induction of hypoxiainducible factor-1α.
Biochem. Biophys. Res. Commun., 465, 562 (2015).