Journal of the Pharmaceutical Society of Korea 21, 70-80(1977)
核酸 代謝 技抗劑
張 日 武
서 울 *學 校 生藥硏究所
(Received April 5, 1977)-
Ilmoo Chang { N a tu r a l P roducts Research In s titu te ,Seoul N a tio n a l University, Seoul 110^)' Antimetabolites in Nucleic A cid Biosynthesis
代謝捨抗劑라는 뜻을 정확히 이해하기 위하여 도움이 되도록 J.A . Montgomery d a/.10이 定 義한 바를引用하면 “antimetabolite 는正常的인代謝物(metabolite) 과매우 비슷한化學構造를 갖 고 있으며 細胞내에서 metabolite 가 生合成되는 것을 방해하거나, 또는 이들 metabolite 가 세 포내에서 이용되는 것을 방해하는 물질이며 이러한 방해작용읍 첫째,代謝 捨抗劑가 효소(또는 효소들)와 결합하여 효소의 촉매작용 자체를 억제하거나 둘째,代謝 捨抗劑가 마치 정상적인 대사물로 효소들에 誤認되어 정상적인 대사물이 도입되어 들어가야 할 生化學的 高分子物質(단 백질 혹은 핵산 등)중의 어느 위치에 대신 도입되어 이들 高分子 物質의 生化學的 기능을 억제 내지는 파괴하는 것이다”라고 하였다. 첫째 경우에 해당하는 例로서는 近代 화학요법제 개발에 큰 공헌을 한 W ood and Fildes2~4)理論의 뒷받침이 된 sulfanilamide (代謝 捨抗齊IJ) 와 />-amino-
benzoic acid(대사물)과의 관계가 좋은 例이며,둘째 경우에 해당하는 것은 6-thioguanine(代謝
捨抗劑) 및 guanine(대사물)과의 관계로 6-thioguanine 이 마치 ganine 이 대사과정을 거치는 것 과 같은 경로를 세포내에서 거친 후 D N A에 guanine 이 들어갈 위치에 대신-들어가는 것이다. 앞에서 예를 든 첫째 및 둘째 경우에서 보듯이 대사 捨抗劑는 대사물의 화학구조중 一H 대신 F, - O 대신 S 나 ᅳC H 2,ᅳO H 대신 一N H2등을 치환한 정도이며 이들 치환된 部分은 分子 크기나 化學的 特性이 대사물이 치환되기 전의 原子나 分子의 것과 매우 비슷한 것이 특징인데
최근 B.R. Baker7)등은 대사물의 구조를 대단히 많이 變化시킨 대신에 이들 물질이 효소와는
매우 강하게 결합하는(예로써 covalent bond) 성질을 갖는 物質을 合成하여 소위 “irreversible inhibitors”說을 내놓았으며 실제로 xanthine oxidase 의 irreversible inhibitor 인 />-bromoacetᄋ-
amidophenyl guanine 등이 하나의 例에 속한다고 하겠으며 이와 같은 物質도 대사 捨抗劑의 범
주에 넣어도 좋겠으나 좀더 개발 및 연구하여야 할 필요가 있겠다. 그러나 어느 化學物質에 조
그마한 변화를 주건 또는 Baker 둥이 제안한 대로 커다란 구조변화를 준 化學物質이건실
제로 세포내에서 代謝捨抗作用을 하는지의 여부는,현재까지의 방법으로는 in vivo 실험을 통 해서 만이 확인 및 입증되어질 뿐이다. 그러므로 antimetabolite 의 개념은 生化學, 藥學, 효
소학 등 관련 분야의 발전과 더불어 특히 drug design 의 理論的 발전에 따라 조금씩 달라져서
이해되어져야 한다고 생각된다.
核酸 生合成에서는 많은 대사물이 生合成 및 利用되는데 현재 procaryotic cell 이나 eucaryotic
cell 을 모멜로 하여 거의 밝혀진 상태이며 本 表題에서는 주로 m am m alian cell 및 동물癌 세포 의 核酸 生合成을 억제하는 核酸 代謝捨抗劑를 다룰 것이며 그 이유중의 하나로써 대부분의 核 酸代謝捨抗劑는 암화학요법제, 즉抗癌劑 開發을 위하여 合成내지 發見되어졌다고 하여도 過言 이 아니기 때문이다.
核酸 生合成
核酸 生合成에 관하여는 여러 學者들이 종합적으로 펴낸 훌륭한 보문 및 저서5,6,卜해들이 많 으므로 이곳에서는 捨抗劑의 作用기전에 비추어 중요하다고 생각되는 핵산대사 및 생합성과정 을 간추려 저자의 주관에 따라 설명한다.
mammalian cell 에서는 핵산 生合成은 일반적으로 두개의 경로에 의해서 이루어진 다. 하나는
de novo purine 및 pyrimidine 生合成 경로이고 다른 하나는 salvalge pathw ay 또는 一名 pre
formed purine, pyrimidine utilization 이라는 것이다. 上記 두개의 生合成 경로는 同時에 존재
하면서 서로 補完的 作用의 성질을 띄면서 balance 룰 이루어 , 핵산생합성을 조 절 한 다. feed
back control 작용으로 이러한 조절작용올 하는 것은 모든 생체 및 세포의 일반특성에 속하기도
한다.
De novo purine 생합성 경로는 ribose-5'-phosphate 로 부터 시작하여 inosine-5'-monophos- phate ( I M P) 까지의 과정을 의미하나 다른學者들은좀더확장하여 IM P 이후즉 A M P 및 G M P 생합성 까지를 포함시키고 있는데 그 나름대로충분한이유가 있다. 첫째 이유로는, purine rin g 이최초로 完成되어지는 때가 IM P level 에서 이루어지기 때문이며,둘째 이유로는 전체 de
purine 생합성 과정을 조절하는 feedback control 작용이 A M P 나 G M P 에 의해서 end product inhibition 형태로 이루어지기 때문이다. 이것은 바로 A M P 나 G M P 가 w ow purine 생합성경로의 첫번째 allosteric 효소의 하나인 phosphoribosyl pyrophosphate amidotransferase (P R P P amidotransferase; E.C . 2,4,2,14)를 end-product inhibition 하여 total purine 생합성의 量을 조절한다는 意味를 갖기 때문이다.
그러므로 만약 어느 핵산대사 捨抗劑가 앞에서 말한 P R P P amidotransf erase 효소작용을 효과
적으로 억제시킬 수 있으면11,12),결과적으로 모든 de novo purine 생합성이 억제되고 더 나아
가서 R N A 나 D N A 生合成 역시 억제될 것이므로 세포기능이 파괴된다. 이런 이유 때문에 이
효소작용을 억제하기 위하여 合成된 洁抗劑 중의 하나가 현재도 抗癌劑로 쓰이는 6-mercapto-
purine 이 다. 論理的으로 볼 때 쇼 purine 생합성 경로중 아무 한 단계의 과정을 억제시켜
도 모두 同一한 洁抗作用 및 lethal effect 가 나타날 둣 보이는게 타당하나실제로 생체( k w V o)
에서는 어느 특정한 捨抗劑에 예민하게 반응하는 핵산생합성 단계 (예 ,P R P P amidotransferase) 가 많지는 않다.
Salvage Pathway (Preformed Purine U tilizatio n )
핵산 生合成경로중의 하나인 上記의 대사경로는 핵산대사 捨抗劑의 捨抗作用과 매우 밀접한 관계가 있다. 그 이유는 대부분의 핵산대사 捨抗劑는 捨抗作用을 나타내기 위하여 세포내세서 活性化 되어야 하는데 대부분의 活性化型(active fo rm )은 nucleotide level 이상이기 때문이며 ,
바로 salvage pathway 에 필요한 여러효소들에 의하여 桂抗劑들이 活性化型으로 되어지끼 때문
이다. 물론 정상적인 purine 또는 purine nucleoside 둘도 이 salvage pathway 를 통하여 nucle
otide 형태로 변환되며,Fig. 1에서 보듯이 base, nucleoside, nucleotide 의 상호 변환은 R N A 및 D N A 生合成에 필요한전구물질의 중 요한 source 가 되는 대사 경로이다 . 그러면
de 와 salvage 두 대사 경로가 서로 얼
마만큼 작용되고 있는가는 생체 조직 및세포 에서 이들 대사경로에 작용하는 여러 효소들 의 작용양 및 活性度를 측정하면 두 대사경로 가 작용되는 양을 비교할 수 있는데,골수13〉
나백혈구145와여러종류의 癌세포에는 salvage pathway 가de tzow 보다 더 활발이 작용된다 고 보고한 例들이 있다. 그러나 만약 salvage
pathway 를 적절한 捨抗劑로 차단시켰을경우
de 대사경로에 작용하는 여러 효소들의 量및活性度가증가(indu ction )하는 것으로보 아 이 두 대사경로는 서로 상호보완하는 조절 기능을 갖는다고 생각되어지며 실제로 정확한 양을 측정하여 두 경로를 비교하는 것은 바로 측정 당시의 주어진 조건에서 조직이나 세포가
De novo Pyrim idine Biosynthesis
D e novo pyrimidine 生合成 과정은 de novo purine 生合成의 경우와 같이 조그마한 化學物 質인 N H j3, C O2, 및 aspartic acid 로 부터 시작하여 pyrimidine ring 이 구성되어진다. 최초의 pyrim idine 이 生合成 되어지는 것은 uridine-57-monophosphate ( U M P) 이고 이것으로 부터 kinase 작용에 의하여 U D P ,U T P 둥이 생성되어 R N A 에 도입되는 동시에 C T P 는 U T P 로 부 터 T M P 는 d U M P 로 부터 생성되어 이 역시 kinase 에 의해 5'-triphosphate 로 바전 후 D N A 에 도입된다. pyrimidine diphosphate(즉 ,U D P , C D P ) level 에서 ribonucleotide reductase에 의해 deoxynucleotide 로 되는 것은 purine 의 경우에서와 같다. Z사加 pyrimidine 生合成 경 로에서 최초의 allosteric enzyme 은 aspartate carbamyltransferase 로 이 control enzyme 은 end- product inhibition 을 받는데 주르 cytidine nucleotide 에 의해 억제되어 전체 de 舶규? 生合成과 정을 조절하게 되는 것은 de novo purine 生合成 경로에서 P R P P amidotransferase 의 조절역 할과 유사한 점이다.
Salvage Pathw ay (Preformed Pyrim idine U tilization)
purine 및 purine nucleoside 경우에서와 같이 pyrimidine, pyrimidine nucleoside 역시 nucle- otide 형태로 상호 변환되며,이둘의 deoxynucleoside 역시 deoxynucleotide 형태로 상호 변환된 다(도표 참조) . 특히 cytidine, deoxycytidine, 및 thymine 및 thymidine 등은최소한 mammalian c e ll에서는 salvage pathway 를 거쳐 R N A 나 D N A로 도입되는 양은 de 加w?에서 생성되어
도입되는 양 이상으로 활발한 것이 중요한 점이다; 그,러므로 pyrim idine계열의 대사 捨抗혹!!들
Fig. 1—Interconversion of base, nucleoside and nucleotide
①: Nucleotide pyrophosphorylase
②: Nucleoside phosphorylase
③: 5'-nucleotidase
④: Kinase
PRPP: Y-phosphoribosyl pyrophosphate R-l-P: ribos-1-phosphate
P: inorganic phosphorus ATP: adenosine-Y-triphosphate ADP: adenosine-5'-diphosphate
나타내는 數値로 보아야 할 것이다.
■역시 nucleotide 형태로 쉽게 活性化되어捨抗作用을나타내며 ,이런이유때문에 pyrim idine 계열 의 대사捨抗劑가 특히 많이 개발되어진 이유중의 하나이다.
Purine Base 및 Purine Nucleoside 와 비슷한 構造를 가진 核酸 代謝 捨抗劑
6-M ercaptopurine (6-MP) ᅳ약 25년전에 개발되어 현재까지 백혈병 치료에 쓰이며,핵산대
사 捨抗作用을 발휘하기 위하여 일단 nucleotide 형태로 活性化되어져야만 한 다. 이때 작용하는 효소는 hypoxanthine-guanine pyrophosphorylase (E .C . 2,4,2,8) 이다16).
6-M P >6-MP-5/-1-phosphate, 이와같이 nucleotide 형태로 된 것은 feedback inhibitor 작용을 하여 P R P P amidotransferase 의 효소작용을 강력히 억제하여 de novo purine 生合成을 왼전히 차단시킨다. 이외에도 6-MP nucleotide 가 R N A 에 도입되며,또한 hypoxantine 및 guanine 이 nucleotide 형태로 변환되는 것을 방해한다고 하며 또한 inosinic acid 가 xanthylic acid 로 되는 과정 및 adenylosuccinate 로 부터 A M P 가 생성되는 것을 억제한다고 하나17~19) 主된 藥理作用 ..으로 보기는 어렵다.
A rabinofuranosyl-6-mercaptopurine (ara-6-MP) ᅳ化學구조는 6-MP 와 매우 비슷하나 전 혀 다른 捨抗作用을 나타낸다. 첫째 ara-6-MP 는 nucleotide 형태로 活性化되지 않으며 ara-6- M P 자체가 ribonucleotide reductase (cy tidy late reductase) 효소작용을억제한다. 둘째로 6-MP 에 저항을 띄고 있는 암세포는 ara-6-MP 에 cross-resistance 를 나타내지않고, 捨抗作用을 받는
점으로 보아 6-MP 와는 전혀 다른 挂抗作用을 갖고 있으리라고 생각된다2o~22\
A llo p u rin o l (6ᅳhydroxypyrazolo (3,4-d) p y rim id in e ) ᅳHypoxanthine 과비숫한화학구조를 갖고 있으며 nucleotide 형대로 변환되지 않고 puriae 生合成을 방해하는 역할은 못하지만 xan- thine oxidase 의 효소작용을 억제하므로만성 gout 에 사용되고 hyperuricemia 에 사용되는데 이 는 uric acid 의 생성을 저해시키는 성질 때문이다24).
9-M ethylthiopurine ribonucleoside (M M P R )ᅳ 6-methylthioinosine 이 라 고 도 하며 adenosine 'kinase 에 의해서 nucleotide 형태로 活性化된다. M M P R ^ ^ ^ e — MMPR-S'-phosphate, 이활성 화된 M M P Rᅳ5'-phosphate는 PRPP-amidotransferase 를 feedback inhibition 하게 된다. M M P R
를 活成化시키는 효소가 6-MP 를 活性化시키는 효소와 서로 다른것이므로 6-M P 에저항을 띤
세포에 사용하여도 結抗作用을 나타낸다25). 또한 6-MP 보다 세포내에서 안정한 화학구조를 갖
-고있다. 이 挂抗劑는 adenosine 계열의 대사洁抗劑로 취급된다.
T hioguanine (6-TG)— guanine 제 6위치의 “ᄋ”대신 “S”로 치환한 것으로 과거 20年동안 많 -은: 연구대상이 되온 核酸대사길항제이다. 처움 이 捨抗劑가 출현되었을 때는 6-M P 와 비숫한
■结抗作用을나타낸다고 여겨졌으나 현재 밝혀진 바에 의하면 6-MP 와는 매우 다른 작용기전을
보여준다. 물론 6-MP 와도 비숫한 生化學的 작용이 몇가지 있으나 6-TG 가 세포에 결정적인
lethal effect 를 주는 것은 6-TG 가 活性化 단계를 거친 후 세포의 D N A 에 guanine 대신 도입 괴는 量에 비례하여 桂抗作用 및 lethal effect 가 증가하는 점이 특징이다5,6,2
6-TG 가 活性化되는 과정은
6-TG + P R P P > 6- T G M P ~ '6-T dG M P
pyrophos- I
pnorylase I
6-T G T P 6-T dGT P
R.NA : D N A
S C H *
OH
(4) (5) (6)
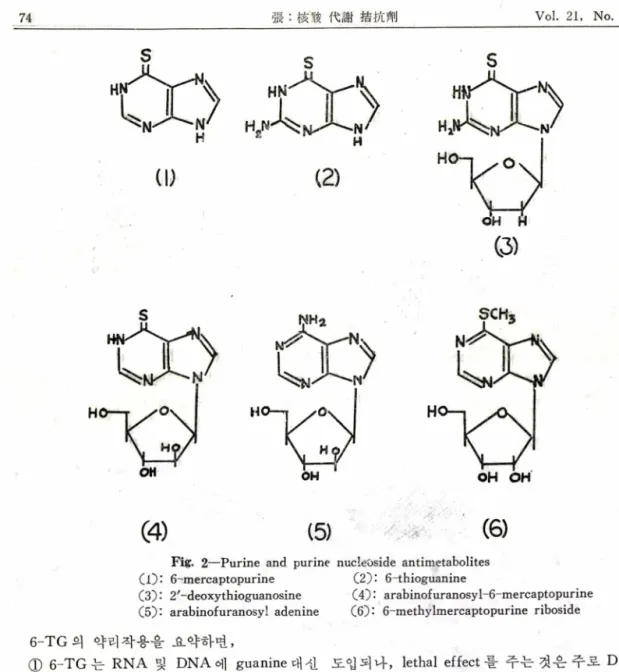
Fig. 2—Purine and purine nucleOside antimetabolites Cl)* 6-'mercaptopurine (2): 6-thioguanine
C3): 2,-deoxythioguanosine CO: arabinofuranosyl-6-mercaptopurine C5): arabinofuranosyl adenine C6): 6-methylmercaptopurine riboside 6-T G 의 약리작용을 요약하면 ,
① 6-T G 는 R N A 및 D N A 에 guanine 대신 도입되나, lethal effect 를 주는것은주로 D N A 에 도입되는 양에 따른다. 임상 결과에서도 약 5 일간 6-TG 를 투여하면 골수 D N A의 guanine 중 58〜 98%정도가 6-TG 로 치환된다撕는 점이 위의 사실을 뒷받침하며,
② 6-TG 에 저항을 띤 암세포가 아직 6-MP 에는 반응한다30). 이는 6-TG 와 6-MP 와의 结 抗作用의 차이점이다.
③ Salvage pathway 경로에서 guanine 이 G M P 로 되는 과정을 6-T G 가 방해한다-
④ De novo purine 生合成을 방해한다3 이는 6-M P 의 挂抗作用과 유사한 점이다.
⑤ Purine 이 purine nucleotide 로 서로 변환되는 것을 방해한다. 이는 6-M P 도 비슷한 作用 을 나타낸다.
⑥ A M P - G M P pyrophosphorylase 의 효소작용을 억제한다32(
⑦ D N A polymerase 의 competitive inhibitor 인 arabinofuranosyl cytosine (Ara-C) 와 6-TG
를 병용 투여했을 때 6-T G 가 D N A 에 도입되는 양이 대단히 줄어든다33). 아울러 挂抗作用도
감소된다.
s
C3) s
(2)
H
iS-2/-Deoxythioguanosine (6-TGdR)一 6-TG 가 여러 단계를거쳐 활성화되는 관계로 최종적 으로 D N A 에 도입되는 양은 줄어들게 된다. 6- T G dR 는 단지 kinase 에 의해 쉽게 活性化되어 ,6-T G M P 가 6-T G dM P 로 되는 과정을 생략할 수 있는 장점이 있으며 6-TG 보다 단위량당 6- T G d R 가휠_ 씬 lethal effect 가 높다34\ 또한 6-T G dR 는 6-TG 에 저항을 받어 hypoxanthine- guanine pyrophosphorylase 의 양이 저하된 암세포에도 洁抗作用을 나타낸다. 왜냐하면 kinase
는 6-TG 에 저항을 띤 암세포에도 아직 존재하기 때문이다35\
A ra b in o fu ra n o s y l a denine (A ra - A )— Adenosine 과 비슷한 구조를 갖으며 단지 furanose
H Cl)
(4)
H K r X -
人n k "
(7)
H
(2)
(5)
OH OH
(6)
NH
(8)
Fiff. 3—(Pyrimidine and pyrimidine nucleoside antimetabolites).
(1): 5-Fluorouracil (2): 5-Fluorocytosine (3): 5~Fluoro-2^deoxyuridine (FU dR) CO: Trifluorothymidine
(5): 5-Azacytidine (6): 6-Azauridine
(7): 5-Iodo~2/-deoxyuridineCIUdR5 ® ) : arabinofuranosyl cytosine Cara-C) (9): 2, 2/-Anhydro-l~jS-D-arabinofuranosyl cytosine (cyclo-ara-C)
제 2위치의 ᅳ O H 기의 입체구조만다를 뿐이다• Ara-A 역시 活性化되어야 結抗作用을 나타내 는데 그 과정은 Ara-A ^ ^ — A ra-A M P— Ara-ADP— Ara-ATP 이고 非活性化過程은 A ra-A
^minase ■"今Ara- hypoxanthine 이며, Ara-ATP 가 DNA-directed D N A polymerase 를 competitive 하게 억제한다. 그러므로 Ara-AT P 는 purine ribonucleotide 라기 보다 purine deoxyribonucleot- ide 의 結抗劑로 취급함이 타당하다3 이 結抗劑는 생체조직 및세포에 다량으로 분포되어 있 는 adenosine deaminase 에 의해 쉽게 arabinofuranosyl hypoxanthine 으로 되어 非活性化된다. 따라서 D N A polymerase 를 억제하는 작용도 상실하게 된다. 이와같은 이유 때문에 대신 arabi- nofuranosyl cytosine 을 오히려 임상에서는 抗癌劑로 많이 사용한다. Ara-A 는 D N A polymerase
의억제작용 이외에도 R N A 에 도입된다는 보고도 있으나,세포싸이클중 S phase 에 작용하는洁
抗劑인 점으로 보아 主된 桂抗作用은 D N A 合成을 방해하는 것으로 풀이된다. 자세한 것은 뒤 에 나오는 arabinofuranosyl cytosine 의 경우를 참조하기 바라며 近年 Ara-A 의 抗 바이러스
CD N A virus) 효과를높이는의도로 많은 유도체가 합성되어지고 있다72,73).
P y rim id in e 및 P y rim id in e N u cleo side오卜비슷한 화학구조를 갖는 核酸 代謝 捨抗劑 5-FluorouraciI (5 - F U )ᅳuracil 의 제 5 위치 수소를 불소로 치환한것이며 ,Heidelberger40,41〉
에 의해 최초로 합성된 후 현재까지 많이 쓰고 있는 抗癌劑중의 하나이다38, 불소원자의 V an der W aals radii 는 1. 35 A 이고 수소는 1.20 A 이다. 그러므로 5-FU 는 세포내에서거의 uracil
의 대사과정과 비슷한 과정을 밟는다. 5-FU 의 活性化 과정을 보면,
F d U M P 가 活性化型이며,이것은 d U M P 가 T M P 로 되는데 필요한 thymidylate synthetase 를 competitive 하게 억제한다43~45).
5-FU 는 5-FU T P 로 되어 R N A 에 도입되기도 하나 主된 捨抗作用은thymidylate synthetase 를 억제하여 T M P 의 생성을 억제하는 것이lethal effect 의 원인이라고 여겨진다. 만약 5-FU
와 thymidine 올 동시에 투여한 후 세포를 배양하면 b-FU 의 길항작용이 안나타나는점으로보
아 위의 사실을 뒷받침한다如고 하겠으나 만약 thymidine 의 투여를 5-FU 보다 늦게 투여할 시 는 thymidine 의 해독작용이 不完全한 것으로 보아서46,47),5-FU 가 thymidylate synthetase 의 효소작용을 억제하는 것 외에도 아직 알려지지 않은 洁抗作用이 5ᅳF U 의 lethal effect 에 중요 한 역할을 할지도 모른다고 짐작된다.
(5-fIuoro-2-Fdeoxyuridine) FUdR ᅳ5-FU 이후에 開發된 것으로현재 抗癌劑로도 사용되고
있다. 6-TG 와 요ᄂ크的표모出노四犯ᅵ예 의 경우와 견주어 볼 때 F U d R 역 시 5-FU 보다 活性化 과 정이 될씬 줄어든다. F U d R 는 thymidine kinase 에 의해 活性化型인 F d U M P 로 된 후 thym i
dylate synthetase 의 효소작용을 competitive 하게 억제하는 점은 5-FU 의 경우와 같으나 5-FU 보다 될씬 적은 양을 투여하여도 높은 捨抗作用을 얻게 되는 장점이 있다43
그러나 F U d R 活性化에 필요한 thymidine kinase 는 기왕에 만들어져서 공급되는 소위 pre
formed thymidine 역시 T M P 로 만들므로세포 D N A 합성 자체로 볼 때 d U M P ᅳ>TMP 로 되는 과정을 F U d R ( F d U M P )로 완전히 억제하여도 아직 salvage pathway 로 부터 T M P 를 공급받
사 j,
C 0 2+ N H s F U d R - |F dU M p|F U d R —
게 되므로 F U d R 의 洁抗作用은 줄어들게 된다.
그러므로 F U d R 를 活性化시키는 thymidine kinase 의 양과 F U d R 의 捨抗作用과는 역비례 관계가 성립된다48).
T rifluo roth y m idine (F 3T d R )—아래와 같은 活性化 경로를 거친 후 D N A 에 도입된다. F 3丁dR->F3T M P — F 3T D P —F 3T T P — D N A,措抗作用은 F 3T d R 이 D N A 에 도입되는 정도에 따라 비례한다. 例로써,HeLa 癌세포에 배양한 바이러스 배양액에 F 3T d R 을 첨가했을 때 F3
T d R 이 바이러스 D N A 에 도입된 것을 관찰할 수 있었으며 이 바이러스 입자는 전염성을 잃게 된다49\ 이 洁抗劑는 抗 바이러스劑로 사용되고 있으며,항암제로는 별 효과가 없다.
이와 관련하여 앞에서 말한 F U d R 은 in 에서는 抗바이러스 효과를 나타내나 in vivo
에서는 그렇지 못한 점50,51>이 F 3T d R 과 서로 다른 藥理作用중의 하나이다.
5-Fluorocytosine (5-FC )—동물세포에는 거의 독성이 없고 活性化 과정을 거치지도 않으며
5-FC 자체로 배설된다56). 5-FC 의 특징은 抗眞菌作用이 있는점이며,곰광이 (Candida albicans〉
에서는 동물세포와는 달리 5-FC 가 5-Fluorodeoxycytidine 으로 된후최종적으토는 D N A 에 도 입된다. 그러므로 抗眞菌作用을 나타내는 것으로 여겨진다.
5-A zacytidine ( k A z C R )ᅳ체코스로바키아에서 開發된 것으로 나중에는 미생물
ticillium ladakanus')로 부터도 분리된 항생물질이다52,53). 정확한 捨抗作用의 기전은 알려져 있지 않으나 아래와 같이 活性化되어진다.
5~AzCR—>5~AzCMP—>5~AzCDP—>5~AzCTP—>RNA, 活性化된 후 R N A,특히 m - R N A 에 도 입된다5 4 이 洁抗劑는 抗菌作用도 보여주며,미생물 배양액에 cytidine 과 함께 배양하면 抗菌
性이 저하되는 것으로 볼 때 cytidine 계 捨抗劑로 취급된다. R N A 에 도입되는 점으로 미루어
보아 단백질 함성 즉 translation level 에서 捨抗作用을 나타내는 것으로 믿어진다.
6-A zauridineᅳ정확한 捨抗作用의 기전은 잘 알려져 있지 않으나 6 - A zU M P 로活性化 된후 orotidylate decarboxylase 의 효소작용을 competitive 하게 억제하는 것은 확실하다57,58,71). 이 洁 抗劑는 거의 毒性이 없는게 특징이며 6-azauridine 의 ribose 의제 2',3',5'위치에 acetyl 기를 도 입한 triacetyl-6-azauridine (Azaribine®)이 psoriasis에 효과가 있는 것으로 알려져 있다. 이 triacetyl-6-azauridine 은 생체내에서 6-azauridine 으로 분해되며,抗癌劑로는 사용되고 있지
않다. ᅳ
5 lodo-2-deoxyuridine ( I U d R)ᅳIU d R 은 1959年 최초로 합성되었다59) . 이 洁抗劑의 作用 기전을 간추려 보면,① Uridine 의 제 5 위치 수소를 옥소로 바꾼것으로옥소의 V an der W a a ls radii 는 thymidine 의 제 5 위치의 一C H3의 크기 ( 2 . 15 A 및 2 . 10 A) 와매우비숫한관계로 IU d R 는 tyhmidine 과 유사한 대사경로를 밟는다 .
② IU d R 는 IU dR -T P 로 活性化 된 후 D N A 에 도입된 다. D N A 도입은 단지 하나의 세포싸 이클내에서만 가능하지 그 이상은 도입이 아니되며,D N A double helix 중 한쪽편에만도입된 다61,62).
③ IU d R 가 억제하는 효소들은 thymidine kinase, thymidylate kinase, 및 D N A polymerase 들이다6o,63). 以上의 洁抗作用중 主된 藥理作用은 IU d R 이 D N A 에 도입되는 것으로 보여진다. IU d R 는 세포내에서 분해되어 IU 로 되고 결국 무기 I ,uracil 등으로배출된다. 抗癌劑보다 抗 바이러스제로 사용 가능성 많으며,IU d R 가 D N A 에 도입되는 점에 착안하여 X-ray sensitizing
agent 로이용 가능성 있으나 임상에서는 아직 별효과가 없다.
l-/3-D-arbinofuranosyl cytosine (A ra- C )_ 앞에서 설명한 purine 계 대사捨抗劑인 1-/3-D-