이
이
이학
학
학 석
석
석사
사
사학
학
학위
위
위 논
논
논문
문
문
신
신
신경
경
경섬
섬
섬유
유종
유
종
종증
증
증 제
제
제1
1
1형
형의
형
의
의 악
악
악성
성
성화
화
화에
에
에 관
관
관여
여
여하
하
하는
는
는
유
유
유전
전
전자
자
자의
의
의 발
발
발굴
굴
굴과
과
과 기
기
기능
능
능 규
규
규명
명
명
아
아
아 주
주
주 대
대
대 학
학
학 교
교
교 대
대
대 학
학
학 원
원
원
의
의
의 학
학
학 과
과
과
신
신
신경
경
경섬
섬
섬유
유종
유
종
종증
증
증 제
제
제1
1
1형
형의
형
의
의 악
악
악성
성
성화
화
화에
에
에 관
관
관여
여
여하
하
하는
는
는
유
유
유전
전
전자
자
자의
의
의 발
발
발굴
굴
굴과
과
과 기
기
기능
능
능 규
규
규명
명
명
지
지
지도
도
도교
교
교수
수
수 김
김
김 현
현 주
현
주
주,
,
,정
정
정 선
선
선 용
용
용
이
이
이 논
논
논문
문
문을
을
을 이
이학
이
학
학 석
석
석사
사
사학
학
학위
위
위 논
논
논문
문
문으
으
으로
로 제
로
제
제출
출
출함
함
함.
.
.
2
2
20
0
00
0
07
7
7년
년
년 2
2
2월
월
월
아
아
아 주
주
주 대
대
대 학
학
학 교
교
교 대
대
대 학
학
학 원
원
원
의
의
의 학
학
학 과
과
과
박
박
박용
용
용예
예
예의
의 이
의
이
이학
학
학 석
석
석사
사
사학
학
학위
위
위 논
논
논문
문
문을
을 인
을
인
인준
준
준함
함
함.
.
.
심
심
심사
사위
사
위
위원
원
원장
장
장
김 현
김
김
현
현 주
주
주
인
인
인
심
심 사
심
사
사 위
위
위 원
원
원
정 선
정
정
선
선 용
용
용
인
인
인
심
심
심 사
사
사 위
위
위 원
원
원
강
강
강
엽
엽
엽
인
인
인
아
아
아 주
주
주 대
대
대 학
학
학 교
교
교 대
대
대 학
학
학 원
원
원
-국문요약-신
신
신경
경
경섬
섬
섬유
유
유종
종
종증
증
증 제
제
제1
1
1형
형
형의
의
의 악
악
악성
성
성화
화
화에
에 관
에
관
관여
여
여하
하
하는
는
는
유
유
유전
전
전자
자
자의
의
의 발
발
발굴
굴
굴과
과
과 기
기
기능
능
능 규
규
규명
명
명
신경섬유종증 제1형(neurofibromatosistype1,NF1)은 다기관의 신경계에 종양을 형성하는 우성 유전질환으로 높은 발병률,예측이 불가능한 합병증의 동반과 악성 화,임상적 증상의 다양성과 심각성,외과적 수술이외의 치료방법의 부재 등으로 효 과적이고 근본적인 치료법에 대한 기초적 연구가 절실히 요구되고 있으나 현재 국 내에는 NF1에 대한 연구가 매우 미비한 실정이다.NF1은 NF1유전자의 돌연변이 가 원인이 되어 그 산물인 neurofibromin의 결핍에 의한 Ras단백질의 과잉활성에 의해 발병한다는 기전이 밝혀져 있다.동일한 NF1 환자의 동일한 유전형을 가진 같은 종류의 세포에서도 정상,양성,악성으로 다르게 변화하기 때문에 조직의 악성 화에 관여하는 유전자가 존재할 것이라 생각된다. 본 연구에서는,발현량 또는 발현양상의 차이에 의해 조직 및 세포 특이적으로 다양한 임상증상에 관여하는 특정의 유전자를 동정하고,그 유전자의 NF1악성화 에 관여하는 기전을 규명하는 것을 연구의 목표로 하였다.한명의 NF1환자 유래 의 정상세포,양성종양세포,악성종양세포를 실험재료로 사용하여,ACP(annealing controlprimer) based PCR method,GeneFishing DEG(differentially expressed gene)screening을 사용하여 각 세포간의 발현양상을 체계적으로 비교․분석하여, NF1의 악성화에 관여하는 유전자를 발굴․동정하였다.DEG screening 결과에서 64개의 DEGs를 발굴하였으며,발굴된 유전자중에서 8개의 유전자를 선정하여
RT-PCR과 Western blotting을 통해 mRNA 및 단백질 수준에서 발현량의 차이를 확인하였다.그 결과 최종적으로 악성화 된 NF1세포에서 발현량이 증가하는 2개 의 유전자 TAGLN과 SERPINE1을,감소하는 1개의 유전자 IFITM1을 NF1의 악 성화에 관여하는 candidategene으로 선정하였다.DEG screening의 정확성을 제고 하기 위하여 comparative genomic hybridization(CGH) array 방법을 사용하여 wholegenome상에서 특정 유전자의 증폭과 소실 유무 등의 유전적 변이(genetic alteration)가 있는지 비교․분석한 결과,NF1환자 유래의 정상세포,양성종양세포, 악성종양세포 모두에서 로 특정 유전자의 소실이나 변이를 발견할 수 없었다.
RNA 간섭(RNA interference,RNAi)에 의한 TAGLN과 SERPINE1 유전자의 발현억제와,과발현(over-expression)에 의한 IFITM1유전자의 발현증가의 인위적 발현조절방법을 악성화 된 NF1세포에 적용하여, NF1의 악성화에 이들 유전자들 이 어떻게 관여하는지 기능규명(functional study)을 실시하였다. TAGLN과 SERPINE1에 대한 RNAi적용과 IFITM1의 over-expression의 모든 경우에서, NF1 malignantcell의 증식률(proliferation rate)이 감소되었다.특히,IFITM1의 over-expression의 경우 양성 및 악성 NF1 cell 모두에서 mitochondria의 fragmentation을 유도 하였으나,악성세포 특이적인 celldeath를 확인 하였다.본 연구결과가 NF1의 악성화 기전규명에 도움이 되기를 기대한다.
차
차
차
례
례
례
국문요약 ···ⅰ 차례 ···ⅲ 그림차례 ···ⅳ Ⅰ.서론 ···1 Ⅱ.재료 및 방법 ···9A.A.Tissuesample···9
B.Cellculture···9
C.DNA extractionandwholegenomeCGH array···10
D.Differentiallyexpressedgene(DEG)screening···10
E.TotalRNA extractionandcDNA synthesis···11
F.RT-PCR···12
G.Westernblotting···13
H.유전자의 과발현을 위한 construct구축 ···13
I.RNAiconstruct구축 ···15
J.Transfection···15
K.Cellproliferationtest···16
L.Confocalmicroscopy···17
Ⅲ.결과 A.CGH array를 이용한 유전적 이상 분석 ···21
B.NF1의 악성화에 관여하는 DEG 발굴 및 동정 ···21
E.Westernblotting을 이용한 DEG 단백질 발현량 평가 ···24
F.악성세포에서 up-regulation된 유전자(TAGLN)에 대한 RNAi적용 ···33
G.악성세포에서 up-regulation된 유전자(SERPINE1)에 대한 RNAi적용 ····38
H.악성세포에서 down-regulation된 유전자의 over-expression시행 ···42
I.IFITM1over-expression에 의한 세포형태 변화 ···46
Ⅳ.고찰 ···48
Ⅴ.결론 ···52
참고문헌 ···53
그
그
그림
림
림 차
차
차례
례
례
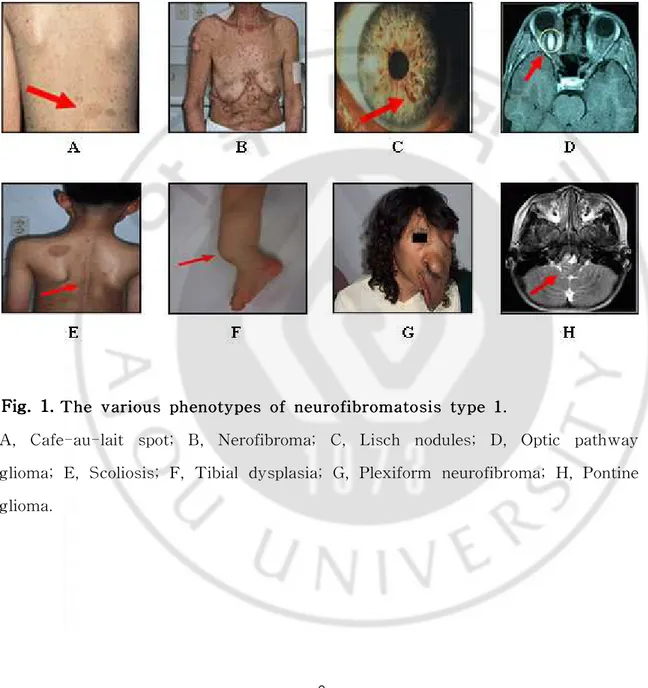
Fig.1.Thevariousphenotypesofneurofibromatosistype1···6
Fig.2.Thestructureandfunctionofneurofibromin···7
Fig.3.A diagram ofmalignantdegenerationpathwayofNF1···8
Fig.4.NF1tissueandcelltype···18
Fig.5.Diagram ofwholegenomeCGH array···19
Fig.6.IFITM1geneengineering ···20
Fig.7.BAC-mediatedarrayCGH microarray···25
Fig.8.ExpectedexpressionpatternsinDEG screening ···26
Fig.9.Detectedexpressionpatternsin20DEGs ···27
Fig.10.Expressionpatternsoftheidentified8DEGs ···29
Fig.11.Validationoftheidentified8DEGsbyRT-PCR···31
Fig.12.Validationoftheidentified4DEGsbyWesternblotting···32
Fig.13.TheRNAitargetsequenceforhumanTAGLN···35
Fig.14.EvaluationofRNAiconstructsforTAGLN inHeLacells···36
Fig.15.EffectofTAGLN knockdowninNF1cells···37
Fig.16.TheRNAitargetsequenceforhumanSERPINE1···39
Fig.17.EvaluationofRNAiconstructsforSERPINE1inHT1080cells···40
Fig.18.EffectofSERPINE1KnockdowninNF1cells···41
Fig.19.A sequenceofhumanIFITM1···43
Fig.20.Over-expressionofIFITM1inHT1080andT24celllines···44
표
표
표 차
차
차례
례
례
Table1.Identificationof20DEGs ···28 Table2.Descriptionoftheidentified20DEGs···30
Ⅰ
Ⅰ
Ⅰ.
.
.서
서
서론
론
론
신경섬유종증 제1형(Neurofibromatosistype1,NF1)은 전 세계적으로 3500명중 1 명꼴로 발병되는 매우 흔한 유전질환중 하나로,말초 신경계에 종양을 형성하는 상 염색체 우성 유전질환이며,성별,나이,민족의 차이가 없으며(Huson 등,1989),환 자의 약 50% 가까이는 새로운 돌연변이에 의해서 발생된 것으로 밝혀졌다(Wright 등, 2003). 주요 임상증상으로는 밀크커피색반점(cafe-au-lait spot)과 피부주름 (skin-fold),주근깨(freckling),홍채결절(lischnodules)과 같은 색소이상,신경섬유종 증(nerofibroma),시신경교종(optic pathway glioma),척추측만(scoliosis),경골형성 이상(tibial dysplasia), 총상신경섬유종(plexiform neurofibroma), 교뇌신경교종 (pontineglioma)등 이다(Huson,1989;Riccardi,1992;North,1993)(Fig.1).신경섬 유종(neurofibroma)은 피부나 피부 바로 아래에 발생하는 양성종양으로 몸의 심부에 서 발생하기도 하며,신경조직과 섬유조직이 섞여 있는 형태로 주로 사춘기 전후에 생기며,환자에 따라 수 개에서 수천 개 까지 나타날 수 있다.신경섬유종증의 아형 인 plexiform neurofibroma는 뼈와 주위 조직의 성장을 자극하여 거대한 크기로 자 라나 추형의 외모를 나타내기도 하며,이 환자의 약 10%는 malignantperipheral nervesheathtumors(MPNSTs)로 변형된다(Evans등,2002;Rasmussen등,2001; Zoller등,1997).MPNST는 고도로 악성화 된 전이 암으로 높은 사망률과 화학요법 과 방사능에 낮은 반응을 보이는 것으로 알려져 있다.이와 같이 높은 발병률과 우 성유전,추형의 외모로 인한 사회적 스트레스가 심하며,다양한 합병증과 악성화에 대한 불확실성을 나타낸다.또한,유전성 질환으로 근본치료가 불가능하고,수술적 절제 후에도 가끔 재발하기도 하며,뇌 심부 발생시 수술의 어려움으로 치료 상에 큰 문제가 있다.
NF1은 NF1유전자의 돌연변이로 인한 그 유전자 산물인 neurofibromin의 양적 결핍으로 발병한다(Gutmann등,1991;Huynh등,1992;Eisenbarth등,2000;Serra 등,2001).NF1은 17번 염색체의 장완(17q11.2)에 위치하며,350 kb의 genomic DNA,60개의 exon으로 구성되어 있고,mRNA는 11~13Kb정도이다.NF1은 종양 억제유전자로 ~320kDa의 세포질(cytosol)에 존재하는 neurofibromin 단백질을 암 호화하고 있다(Cawthon 등, 1990; Wallace 등, 1990; Legius 등, 1993). Neurofibromin은 신경세포(neuron),희소돌기아교세포(oligodendrocyte)와 슈반세포 (schwann cell),백혈구,부신속질(adrenalmedulla)을 포함해 많은 세포와 조직에서 발현되며,뇌에서는 신경세포 가지돌기(neuronaldendrite)와 축삭(axon),신경세포 골격(neuronalcytoskeleton)과 관련된 조직에서 발현된다(DeClue등,1991;Daston 등, 1992; Golubic 등, 1992; Datson과 Ratner, 1993; Gutmann 등, 1995). Neurofibromin의 염기서열 분석 결과,작은 중심영역(smallcentralregion)이 존재 하는 것으로 알려졌는데,원발암(primary cancer)유전자인 p21-Ras의 조절에 관여 하는 catalyticdomain(p120-GAP,GTPase-activating proteins)과 상동성을 가진다 (Ballester등,1990;Xu 등,1990a,b)(Fig.2A).Neurofibromin에 암호화된 GAP related domain(GRD)은 p21-Ras를 GTP와 결합된 활성화 상태에서 GDP 결합의 불활성화 상태로,GTP를 가수분해하여 많은 유형의 세포에서 증식과 분화를 자극 하며(Bollag와 McCormick,1991),원발암유전자 Ras의 과잉 발현을 억제하도록 조 절한다(Fig.2).그러나 NF1에 돌연변이가 발생하고,GTP-Ras가 과잉발현되어 세 포내에 축적됨으로,종양이 형성되고 NF1이 발병하게된다.
현재 NF1에 대한 국내․외에서 진행되는 주된 연구는 환자의 DNA로부터 NF1 유전자의 돌연변이 부위와 염기배열을 밝히는 것이 주류를 이루고 있고,질환치료를 궁극적인 목표로 하는 연구는 거의 진행되고 있지 않으며,환자에서 유전형과 임상
증상에 상호관계가 없다는 사실로부터 NF1 유전자 이외의 신경섬유종증 제1형의 유발 관련유전자의 존재를 밝히는 연구 등이 진행되고 있다.최근 수식유전자의 존 재가능성에대한 보고는 있으나(Wiest등,2003;Holtkamp등,2004),NF1의 임상적 표현형의 다양성과 악성화 과정에 대한 정확한 기전은 여전히 밝혀지지 않았다.현 재 유전형이 다른 여러 환자들로부터 검체를 채취하여 양성의 neurofibroma가 악성 MPNST로 진행되는 연구가 진행되고 있으나,그 위험성 평가에 있어 이미 알려진 악성화로의 진행과 관련된 유전자를 분석하는 것 등의 대안적 접근법만을 적용하는 실정이다.신경섬유종증 제1형에서 양성종양 발생에 있어서는 NF1유전자의 돌연 변이가 필수적이나,양성종양의 악성섬유육종(neurofibrosarcoma)으로의 변화 등,계 속되는 이차적 악성변화에는 충분하지가 않다.또한,신경섬유종이 악성화 되는 데 에는 다른 유전자의 이상 혹은 유전적 변화가 일어 날 것으로 생각되어지는데,악성 신경섬유육종의 형성은 사람의 다른 악성종양과 같이 다양한 종양형성기전이 관여 할 것으로 사료된다.이와 관련해서는 chromosome17p와 p53돌연변이가 악성섬유 육종의 형성에 관련이 있다고 보고 된 바 있다(Menon등,1990).한편,암 억제유전 자인 NF1과 TP53유전자를 조작하여 human malignanttumors인 MPNSTs모델 마우스가 개발되었고(Vogel등,1999;Reily등,2000;Zhu등,2005),모델 마우스를 이용한 NF1질환 연구가 활발히 진행되고 있다.또한 손실,전좌,역위,증폭의 염 색체 수적 이상 등 genetic alteration을 확인하기 위한 방법으로 comparative genomic hybridization(CGH) 및 특정 유전자의 증폭 및 손실을 확인하기 위한 CGH array를 이용하여 신경섬유종증 제1형과 관련된 MPNST에서 17,19번 22q염 색체의 손실과 증폭이 보고 된바 있다(Mechtersheimer등,1999;Koga 등,2002a, b;Bridge등,2004;Mantripragada등,2006).
양한 임상증상에 관여하는 특정의 유전자를 동정하고,그 유전자의 NF1 악성화에 관여하는 기전을 규명하는 것을 연구의 목표로 하였다.NF1에서는 동일한 유전형을 가지는 한 명의 환자 내에서 신경섬유세포의 표현형이 정상(normal),양성(benign), 악성(malignant)으로 다양하게 나타나는 경우가 많다.이러한 현상에는 NF1유전자 의 germ cellmutation외에 특정 유전자의 somaticcellmutation또는 특정 단백질 발현양의 차이가 관여 할 것으로 예상되어,neurofibroma와 MPNSTs의 조직을 이 용하여 TP53/p53,CDKN2A/p16,CDKN1B/p27,TGB1/TGF-β1,HGF/HGFα,그 리고 수용체 MET,MMP13등의 유전자/단백질에 대한 비교,분석의 연구가 진행 되고 있다(Rao등,1997;Kourea등,1999;Nielsen등,1999)(Fig.3).하지만,아직 까지 정확한 NF1의 악성화 기전이 밝혀지지 않고 있다.본 연구에서는,상기의 유 전자 외에 NF1의 악성화에 관여하는 특정 유전자를 발굴(screening)하여 그 기능을 규명하기 위하여,한명의 NF1환자에게서 수술에 의해 획득한 정상 조직,양성종양 조직,악성종양 조직에서 각각 primarycell을 순수 배양하여,각 조직 세포 간에 발 현량에 차이가 나는 유전자를 screening 하였다.우선 CGH array를 통해 정상,양 성종양,악성종양 간에 특정유전자의 증폭 및 손실 등의 wholegenome상에서 유 전적 변이(geneticalteration)가 있는지를 확인 하였으며,그 다음단계로 annealing controlbased PCR(ACP)법을 이용한 mRNA differentialdisplay(DD)를 통하여 유 전자 발현량의 차이를 분석하여 의미 있는 유전자를 발굴․동정 하고,발굴․동정된 유전자에 대한 RT-PCR,Westernblotting을 통한 평가를 통하여 candidategene을 선정하고자 하였다.특히,선정된 유전자에 대해서는 발현조절 시스템을 통하여 NF1악성화에 관여하는 기능을 규명(functionalstudy)하였다.즉,정상세포가 양성 및 악성종양 세포로 진행됨에 있어 점차 발현량이 증가되는 유전자에 대해서는 인 위적으로 유전자의 발현량을 감소시키는 방법인 RNA 간섭(RNA interference,
RNAi)을 적용하고,발현량이 점차 감소되는 유전자에 대하여서는 그 유전자를 과발 현(over-expression)시킴으로써 각각의 유전자의 NF1의 악성화에 미치는 역할 및 기능을 규명 하였고.본 연구의 결과가 NF1의 악성화 기전의 규명과 치료법 개발에 도움이 되기를 기대한다.
Fig. Fig. Fig.
Fig. 1. 1. 1. 1. TTThhheeevvvaaarrriiiooouuusssppphhheeennnoootttyyypppeeesssoooffnfnneeeuuurrroooffifiibbbrrrooommmaaatttooosssiiissstttyyypppeee111...
A,Cafe-au-lait spot; B,Nerofibroma; C,Lisch nodules; D,Optic pathway glioma;E,Scoliosis;F,Tibialdysplasia;G,Plexiform neurofibroma;H,Pontine glioma.
F
FFiiiggg...222..T.TThhheeessstttrruruuccctttuuurrreeeaaannndddfffuuunnnccctttiiiooonnonoofffnnneeeuuurrrooofffiiibbbrroroommmiiinnn...
A,Structure ofNF1 (Dasgupta et al., 2003); B,Neurofibromain and Ras regulation (Reed et al., 2001). Neurofibromin contains a central region of sequence homology shared with a family of proteins that accelerate the conversion of Ras from its active GTP-bound conformation to its inactive GDP-bound form.Theinactivation ofRasby neurofibromin GAP activity leads to regulated cellgrowth.Loss ofneurofibromin in tumors as a resultofNF1 geneinactivationleadstoincreasedRasactivityandincreasedcellgrowth.
F
FFiiiggg...333...AAA dddiiiaaagggrrraaammm oofoffmmmaaallliiigggnnnaaannntttdddeeegggeenenneeerrraaatttiiioononn pppaaattthhhwwwaaayyy ooofffNNNFFF111 (((DDaDaasssggguuuppptttaaa e
eetttaaalll...,2,,22000000333)))...
NF1 loss in Schwann cellprecursors during development-in cooperation with NF1+/- fibroblasts, perineural cells, and mast cells result in plexiform
neurofibromaformation.Theaccumulation ofothergeneticchange(e.g.p53,p16, orp27loss)promotestransformation intoMPNSTs.NF1lossin Schwann cells incooperationwithNF1+/-cellsresultsindermalneurofibromaformation.
Ⅱ
Ⅱ
Ⅱ.
.
.재
재
재료
료
료 및
및
및 방
방
방법
법
법
A AA...TTTiiissssssuuueeesssaaammmpppllleee 2004년 12월 아주대학교병원을 내원하여 신경섬유종증 제1형(Neurofibromatosis type1,NF1)으로 외과수술을 받은 24세 남자 환자의 종양 적출물로부터 3가지 종 류의 조직을 획득하였으며,각 조직은 포르말린 고정 후,파라핀으로 포매하여 조직 절편슬라이드를 제작,Hematoxylin & Eosin 염색하여 현미경(400×)으로 관찰하여, 정상,양성,악성조직임을 확인하였다(Fig.4).B
BB...CCCeeellllllccucuullltttuuurrreee
환자의 조직으로부터 정상(normal skin), 양성종양(benign tumor), 악성종양 (malignanttumor)조직으로부터 explant방법을 이용하여 fibroblasts를 분리하여,1% antibiotics(GibcoBRL,U.S.A.),15% FBS(HycloneLaboratoriesINC.,U.S.A.)를 첨 가한 Dulbecco's modified Eagle's medium(Hyclone Laboratories INC.,U.S.A.)에 배양하였다.또한 cellline으로는 HeLa cells(human epithelialadenocarcinomas origin by cervix and uterine),HT1080 cells(human N-Ras activated epithelial fibrosarcoma),T24 cells(human H-Ras activated epithelialcarcinomas),A549 cells(humanepithelialcarcinomaoriginbylung)를 사용하였으며,A549,HeLacell lines은 1% antibiotics(Gibco BRL,U.S.A.),10% FBS(HycloneLaboratoriesINC., U.S.A.)가 포함된 DMEM(HycloneLaboratoriesINC.,U.S.A.)에서,HT1080과 T24 는 1% antibiotics(Gibco BRL,U.S.A.),10% FBS(Hyclone Laboratories INC., U.S.A.)가 포함된 RPMImedium(HycloneLaboratoriesINC.,U.S.A.)에서 배양하였 다.
C
CC...DDDNNNAA eA eexxxtttrrraaaccctttiiioononnaaannndddwwhwhhooollleegeggeeennnooommemeeCCCGGGHHH aaarrrrrraaayyy
Normalskin,benign tumor,malignanttumortissue에서 분리․배양한 세포에서 DNA를 추출(QiagenInc,CA,U.S.A.)하였으며,(주)MacrogenwholegenomeCGH array service를 이용하였다.본 연구에 이용한 BAC chip은 BAC library의 제작과 end-sequencing을 통해 확보된 sequence-mapped BAC clone중 발암관련 유전자 나 염색체,band그리고 breakpointmarker를 포함하는 BAC clone은 FISH 과정을 통해 염색체상의 특정 위치에 특이적으로 결합하는지를 확인한다.FISH까지 확인이 된 BAC clone은 그대로 BAC chip위에서 염색체상의 특정 위치를 대표하게 되고, test를 CY3로 reference를 CY5로 표지한 후 두 형광염료의 상대적인 강도를 측정함 으로써 test염색체의 어느 부위가 증폭 혹은 결실되었는지를 알아낸다.BAC Chip 위에 올라가는 모든 BAC clone은 scanning과 analysis과정을 통해 결과가 수치화되 므로 BAC chip은 genome-widescreening이 가능하다.BAC chip은 glassslide위에 전체 염색체를 올려놓고 형광 강도 차이를 구하는 CGH와 달리 절편화되고 mapping이 된 BAC clone을 올려놓아 CGH에 비해 해상력이 월등히 높다.BAC chip의 해상력은 BAC clone의 개수에 비례하며 전체 염색체상에서 일어나는 최소 변화인 microdeletion이 1Mb내외로 3000clone이면 전체 염색체의 수적인 변화를 감지 할 수 있다(humangenome30억 bp/3000clones=1Mb/clones)(Fig.6).
D
DD...DDDiiiffffffeeerrreeennnttitiiaaallllllyyeyeexxxppprrreeesssssseeedddgggeeennneee(((DDDEEEGGG)))ssscccrrreeeeeennniiinnnggg
3가지 종류의 조직에서 추출한 RNA를 First-strand cDNA Synthesis를 통하여, ACP-basedGeneFishingTM PCR을 이용하여 유전자를 증폭한 후 directsequencing 을 통해 염기서열 분석을 실시하였다(Seegene,Inc.,Korea).DEG screening을 위하 여 사용한 ACP-based GeneFishingTM PCR 기술은 (주)Seegene에서 개발한
annealing controlbasedprimer(ACP)를 사용하여 annealing 온도를 높여 줌으로써, 주형과의 특이성과 정확성을 높여 두 가지 이상의 시료에서 다르게 발현하는 유전 자를 찾을 수 있도록 개발된 방법으로,microarray와 비교하여 novelgene발굴 가 능성이 높으며,적은 transcript의 확인이 가능하고,위양성(false positive)이 없고, 재현성이 높아 모든 eukaryoticcells에 적용이 가능하며 확인이 용이한 강점이 있 다.유사 염기서열(sequence homology)조사는 NCBI(http://www.ncbi.nlm.nih.gov /BLAST)에서 Blastn프로그램을 사용하여 GenBankdatabase에서 시행하였다.
E
EE...TTTooottataalllRRRNNNAAA eeexxxtttrraraaccctttiiiooonnnaaannnddcdccDDDNNNAAA sssyyynnnttthhheeesssiiisss
Normalskin,benign,malignanttissue에서 배양한 세포에서 TizolTM reagent (InvitrogenCo,U.S.A.)를 이용하여 RNA를 추출하고,그 중 RNA 1 μg을 이용하여 DNase I(Invitrogen Co,U.S.A.)1 U를 처리하여 남아있는 gDNA를 제거하였다. gDNA의 잔존여부를 확인하기 위하여 DNaseI을 처리한 RNA를 주형으로 gDNA 특이 GAPDH primer set(F, 5´-GAAGCTGACTCAGCCCTGCAAAG-3'; R, 5'-AGACCACCTGGTGCTCAGTGTAG-3´)를 이용하여 PCR로 증폭하여 확인하였 다.사용한 primer는 RNA가 PCR의 주형이 될 수 없으며,intron영역은 gDNA에만 존재하는 특성을 이용하여 제작하였다.PCR 결과 gDNA가 완전히 제거된 것으로 확인이 된 RNA를 TrueScriptII Reverse Transcriptase PCR Kit (SAWADY Technology,Japan)를 이용하여 cDNA를 합성하였으며,cDNA 합성 여부를 확인하 기 위하여 cDNA에서 두개의 exon이 만나는 부분에 cDNA 특이 GAPDH primer set(F,5´-GCCTCAAGATCATCAGCAATGCCT-3´;R,5´-AGACCACCTGGTGCT CAGTGTAG-3´)를 제작하였고,cDNA주형으로 하여 PCR로 증폭하여 확인하였다.
F
FF...RRRTTT---PPPCCCRRR
DEG screening을 통하여 발굴된 유전자 중 8가지를 선정하여,동정된 유전자임을 평가하기 위하여 각 조직(normalskin,benign,malignanttissue)에서 배양한 세포 에서 totalRNA를 추출하여,합성한 cDNA를 주형으로 하여 유전자 특이 primer를 사용하여 PCR로 증폭하였다.사용한 primer는 다음과 같다. 1.DYNLL1: F,5´-ATGCGGACATGTCGGAAGAGATGC-3´ R,5´-ACATCGAGATGTTCCCTTAGCAAGG-3´ 2.ENC1: F,5´-GTACCAGTGTCAGTCATGACAAGCT-3´ R,5´-CGTCTAATGTTGGATCGTAGCAGT CC-3´ 3.RADIXIN: F,5´-CCTGGCCTACTGTGAAGACAGAGTC-3´ R,5´-GATGGACTTGATCAATGCCGGACA-3´ 4.TAGLN: F,5´-CAGCTTGGCAGTGACCAAGAATG-3´ R,5´-GTGCAGTTACCATTGCTCAGTGACAG-3´ 5.SERPINE1:F,5´-ATCCACAGCTGTCATAGTCTCAGC-3´ R,5´-GCCAAGGTCTTGGAGACAGATCTG-3´ 6.IFITM1: F,5´-GCATTCGCCTACTCCGTGAAGTCT-3´ R,5´-CAGCATTGCACAGTGGAGTGCA-3´ 7.DHRS3: F,5´-GACAGTGGAAGCTGTGCAGCTCA-3´ R,5´-CATCAGTCCTGTGCAAAGGT CCTG-3´ 8.ATP2A2: F,5´-AGAGTGTCCTTCTACCAGCTGAGTC-3´ R,5´-CACGTTCAGCGGTGTGATCTGGA-3´
TotalRNA로 합성한 cDNA를 주형으로,유전자 특이 primer를 이용하여 95℃ 20초,60℃ 30초,72℃ 30초에서 TAGLN, SERPINE1은 24 cycle,DYNLL1, IFITM1은 26cycle,ATP2A2는 28cycle,ENC1,RDX,DHRS3는 30cycle반복
하여 PCR(BioRad,MJResearch,U.S.A.)로 증폭된 산물을 1.5% agarosegel에 전 기 영동하여 EtBr로 염색하여 transiluminator로 확인하였다.
G
GG...WWWeeesssttteeerrrnnnbbblllooottttttiiinnnggg
3가지 종류(Normalskin,benign,malignanttissue)의 조직에서 배양한 세포를 lysisbuffer(20mM TrispH 7.5,150mM NaCl,1% TritonX,2mM EDTA,50 μ g/mlPMSF,Proteaseinhibitorcocktail)와 혼합하여 단백질을 추출한 뒤 여기서 얻 어진 시료를 Brafordproteinassay(Bio-radlaboratories,Hercules,CA,U.S.A.)방법 으로 정량 분석하여 samplebuffer(5×)와 섞은 후,95℃에서 5분간 가열하였다.이를 각각 40 μg씩 loading 한 후 8~15% SDS PAGE로 전기영동하여 분리하고, nitrocellulose membrane(Sheicher&SchuellBio Science GmbH,Dassel,Germany) 에 흡착 이동시켜,동정된 4개의 단백질에 대하여 다음과 같이 각각의 특이항체로 Western blotting방법으로 분석하였다. 사용한 1차 항체는 Transgelin (1:1000, Abcam, U.K.), PAI-1(1:1000, Calbiochem, Germany), IFITM1(1:100, Boster, China), SERCA2(atpase2; 1:1000, Bethyl, U.S.A.)를 사용하였고, peroxidase가 conjugation된 goatanti-rabbitantibody(SantacruzBiotechnology,INC,U.S.A.)를 이용하여 반응시킨 뒤,ECL(enhanced chemilluninescence,Amersham biosciences, England)에 반응시켜 현상하였다.
H
HH...유유유전전전자자자의의 과의 과과발발발현현현을을을 위위위한한 c한 ccooonnnssstttrrruuucccttt구구구축축축
악성종양조직세포에서 발현량이 점차적으로 감소하는 유전자인 IFITM1을 세포 내에 과발현(over-expression)시키는 시스템을 구축하기 위하여 유전자를 cloning하 였다.해당 유전자의 cDNA에 사용하고자 하는 제한효소 부분을 포함한 primer를
다음과 같이 제작하였다.F,5´-TTCTCGAGCTATGCACAAGGAGGAACATGAGG TGG-3´;R,5´-CTGGATCCAGCATTGCACAGTGGAGTGCA-3´(Fig.5).
pEYFP-C1(Clontech Laboratories,INC,Japan),pREP4(Invitrogen Co,U.S.A.) vector를 이용하여,NF1에 돌연변이가 없는 cDNA를 주형으로 하여 LA Taq polymerase(TAKARA,Japan)를 사용하여 95℃ 20초,60℃ 30초,72℃ 30초를 30 cycle반복하여 PCR로 증폭하였다.증폭된 산물은 1.5% agarosegel에서 전기영동 하여 EtBr로 염색 후,transiluminator로 확인하여 해당 유전자의 증폭된 부분을 잘 라내고 gelextraction(Geneallbiotechology,Korea)을 통해 DNA를 추출한 뒤,제한 효소 XhoI,BamHI(Roche Diagnostics Corporation,Germany)를 사용하여 PCR로 증폭된 DNA와 vector에 제한효소를 처리하여, vector와 IFITM1유전자를 T4 ligase(Invotrogen Co, U.S.A.)를 이용하여 16℃에서 12시간 이상 반응하였다. Ligation된 산물을 E.coliDH5α strain competentcell에 transformation하고,37℃ 에서 배양하였다.배양 후 형성된 집락에 대하여 다음의 primer를 이용하여 colony screeningPCR을 시행하였다.
pE3FP-C,F,5´-GATCACCTCGGCATGGACGAGCTGTA-3´
R,5´-GTATGGCTGATTATGATCAGTTATCTAGAT-3´ pREP4, F,5´-CCACTGATTCCGCATTGCAGAGAT-3´
R,5´-CAACTGAAGGGATTACATGCACTGC-3´
Colony screening PCR은 pREP4 vector를 사용하여 cloning한 유전자는 3 step (98℃ 30초,60℃ 30초,72℃ 1분,35cycle반복)으로 시행하였고,pEYFP-C1vector 를 이용하여 cloning한 유전자는 2 Step(98℃ 10초,68℃ 1분,35cycle 반복)으로 PCR하여 증폭시키고,확인하였다.그리고 colony screening PCR을 통해 해당 유전 자가 cloning되었다고 확인이 된 집락은 antibiotics를 포함한 LB broth에 배양하여
plasmid minikit(Axygen,U.S.A.)를 이용하여 plasmid DNA를 추출한 뒤,cloning 에 사용한 두 제한효소로 반응시켜 vector와 insert를 다시 한번 확인한 뒤 sequencing하여 construct를 구축하였다.
I
II...RRRNNNAAAiiicccooonnsnsstttrrruucuccttt구구구축축축
TAGLN,SERPINE1 유전자를 인위적으로 knockdown하기 위하여 RNA 간섭 (RNA interference,RNAi)시스템을 구축하였다.human U6promotor를 사용하고, HindIII를 이용하여 hairpin 구조를 가진 유전자 특이 염기서열을 3가지 제한효소 XbaI,BglII,SalI(RocheDiagnosticsCorporation,Germany)를 이용하여 TAGLN, SERPINE1에 대하여 각각 5개씩,두 유전자에 대하여 모두 10가지의 shorthairpin RNA(shRNA)를 제작하고 episomalvector인 pREP4에 cloning하였으며,control RNAi로는 human에 존재하지 않는 green fluorescenceprotein(GFP)에 대한 RNAi 를 제작하여 사용하였다.
J
JJ...TTTrrraaannnsssfffeeeccctttiiiooonnn
TAGLN, SERPINE1에 대한 RNAi construct와 IFITM1 유전자를 세포에 transfection하기 위하여 TAGLN과 SERPINE1의 각 5개의 RNAiconstruct는 각각 HeLa(TAGLN),HT1080(SERPINE1; Lipofectamin LTX,Invitrogen)celllines에 transfection하였고,IFITM1의 over-expression을 위해 HT1080 (Lipofectamin LTX,Invitrogen)과 T24(FuGENE HD,RocheDiagnosticsCorporation,Germany) celllines에 transfection 하였다.그리고 transfection된 cell만 선택배양하기 위하여 Hygromycin B1(A.G.Scientific,INC,U.S.A.)을 사용하였고,HeLa,HT1080 cell lines은 각각 300 μg/ml,100 μg/ml에서 선택배양한 뒤,30 μg/ml,20 μg/ml에서 각
각 증식 배양하였다.또한 NF1 cells(Microporator-miniTM,Digitalbiotechology)에 transfection하여 5일간 배양하였다.
K
KK...CCCeeelllllplpprrrooollliiifffeeerrraaatttiiiooonnnttteeesssttt
TAGLN과 SERPINE1에 대한 RNAiconstructs및 IFITM1유전자를 세포내에 발현시킨 후에 세포특성을 확인하기 위하여 세포 proliferation rate(증식량)을 정량 분석하였다.세포증식실험을 위하여 AlamarBlueassay(Biosource,U.S.A.)를 사용하 였으며, resazurin과 resorufin은 fluorometric-colorimetirc oxidation-reduction (redox)indicator로서 환원된 세포 대사산물에 대하여 형광을 나타내어,색을 변화 시킨다(Page등,1993;Larson 등,1997).NF1cells는 96wellplate에 NF1세포를 well당 250 μl내에 8×103cells/ml의 세포를 준비하여,5% CO
2incubator에서 12시
간 배양 후,AlamarBluereagent를 각 well에 25 μl씩 떨어뜨리고,incubator에서 9 시간 반응시키고,HT1080과 T24celllines는 1× 104cells/ml5% CO2incubator에
서 24시간 배양 후,AlamarBluereagent를 각 well에 25 μl씩 떨어뜨리고,incubator 에서 4시간 반응시킨 후에,spectrophotometer(Bio-Tek Instruments,Italy)를 사용 하여 570nm,600nm에서 흡광도를 측정하였다.증식율은 아래의 계산식을 이용하 였으며,εred값은 570nm에서 155677,600nm에서 14652이며,εox값은 570nm에서 80596,600nm에서 117516으로 계산하였다.각 용어와 계산식은 다음과 같다.Cred, concentration of reduced form AlamarBlue(RED); Cox, oxidized form of AlamarBlue(BLUE); εox,molar extinction coefficient of AlamarBlue oxidized form(BLUE); εred, molar extinction coefficient of AlamarBlue reduced form(RED);A,absorbance of test wells;A´,absorbance of negative control well(negativecontrol=media+AlamarBlue/nocell);A°,absorbanceofpositive
growthcontrolwell;λ1,570nm;λ2,600nm
% Reduced= Credtestwell ×100 Coxnegativecontrolwell
= (εox)λ2.Aλ1-(εox)λ1.Aλ2 (εred)λ1.A'λ2-(εred)λ2.A'λ1
L
LL...CCCooonnnfffooocccaaalllmmmiiicccrrrooossscccooopppyyy
IFITM1의 세포내 기능을 규명하기 위하여,pEYFP-C1과 cloning한 IFITM1을 NF1 cell에 transfection하여 over-expression시킨 후,confocal현미경(CarlZeiss LSM 510,Germany)으로 세포의 형태변화를 관찰하였다.Mitochondria의 염색을 위 하여 mitotracker(MitoTrackerRed,Invitrogen)를 사용하였으며,핵 염색을 위하여 DAPI(Pierce,U.S.A.)를 사용하였다.
F
FFiiiggg...444...NNFNFF111tttiiissssssuuueeeaaannndddccceeelllllltttyyypppeee...
Mass of Neurofibromatosis type 1 containing Normal,Benign and Malignant tissue regions(A,B,C) and paraffin-embeded tissue sections were counter stained with Hematoxylin & Eosin stain(viewed at400×)(D,E,F).A,Normal skin tissue region;B,Benign tissue region;C,Malignant tissue region;D, Normaltypeoftissue;E,Benigntypeoftissue;F,Malignanttypeoftissue
F
A
AA... BBB...
F
FFiiiggg...666...IFIIFFIIITTTMMM111gggeeennneeeeeennngggiiinnneeeeeerrriiinnnggg...
IFITM1 gene engineering using 2 restriction enzymes,XhoI,BamHIwith 2 types ofvector.A is a fluorescence expressing vector,pEYFP-C1.B is an expressionvectorcontainingresistancegeneagainstHygromycinB1,pREP4.
Ⅲ
Ⅲ
Ⅲ.
.
.결
결
결과
과
과
A
AA...CCCGGGHHH aaarrrrrraaayyy를를 이를 이이용용용한한한 유유유전전적전적적 이이이상상상 분분분석석석
신경섬유종증 제1형(Neurofibromatosistype1,NF1)환자의 종양 적출물에서 분 리한 normalskin,benign,malignanttissue에서 배양한 세포로부터 추출한 DNA를 이용하여 comparativegenomichybridization(CGH)array를 시행하여 손실,전좌,역 위,증폭의 whole genome 상의 유전적 이상(genetic alteration)을 확인하고,특정 유전자의 증폭 및 손실을 발견하고자 하였다. 현재 NF1과 관련된 malignant peripheralnervesheath tumors(MPNSTs)에서 17,19번 22q염색체의 손실과 증폭 이 이미 보고 된 바 있다(Mechtersheimer등,1999;Koga등,2002a.b;Bridge등, 2004;Mantripragada등,2006).Normal,benign,malignanttissue에서 DNA를 추출 하여 normal과 benign,normal과 malignant,benign과 malignanttissue를 test와 reference로 하여 CGH array를 실시하였으며,본 연구에서 사용한 (주)마크로젠의 BAC-mediatedarrayCGH microarray는 gain/loss를 확인할 때,최소한 3개의 연속 된 spot이 threshold를 넘어갔을 때를 chromosome aberration을 반영할 가능성이 높다고 할 수 있다.그러나 본 실험 결과 의미 있는 변화는 관찰되지 않았다(Fig. 7).
B
BB...NNNFFF111의의 악의 악악성성성화화화에에에 관관관여여여하하하는는는 DDDEEEGG 발G 발발굴굴굴 및및및 동동동정정정
Normalskin,benign,malignanttissue에서 배양한 세포에서 추출한 RNA로부터 합성한 cDNA를 이용하여 (주)Seegene의 ACP-based GeneFishingTM PCR 방법을 이용하여 정상,양성,악성 세포에서 발현량에 차이가 있는 유전자(differentially expressed gene,DEG)를 screening하였다.먼저 발현양의 차이를 예상한 결과 8가
지 패턴으로 분류하였다. 정상에서 악성세포로 발현량이 up-regulation, down-regulation의 경우를 각각 4가지로 다음과 같이 분류하였다. 발현량이 up-regulation되는 경우는 정상에서 악성으로 갈수록 발현량이 점차적으로 증가하는 경우,정상만을 제외하고 양성과 악성에서만 발현량이 증가하는 경우,정상과 양성 에서는 차이가 없으나 악성에서만 발현량이 증가하는 경우,정상과 악성은 차이가 없으나 양성에서만 발현량이 증가하는 경우로 총 4가지이다. 그리고 발현량이 down-regulation되는 경우는 정상에서 악성으로 갈수록 발현량이 점차적으로 감소 한 경우,정상에 비해 양성과 악성의 발현량이 감소한 경우,정상과 양성은 차이가 없으나 악성에서만 발현량이 감소한 경우,정상과 악성은 같으나 양성에서만 발현량 이 감소한 4가지 경우이다(Fig.8).
DEG screening 결과 발현량의 차이를 보이는 총 64개의 DEGs를 발견하였고,그 중에서 발현량이 up-regulation되는 경우 35개,down-regulation되는 경우는 26개였 다.그리고 확인된 64개의 DEGs중에서 발현량의 차이가 뚜렷한 20개의 DEGs를 선정하여 먼저 발현 패턴을 분석한 결과,up-regulation의 경우 4가지 패턴이 모두 나타났고,down-regulation 경우는 첫 번째와 두 번째 패턴만 나타났다(Fig.9).20 DEGs에 대하여 염기서열을 분석하고,유전자를 동정한 결과 종양세포에서 up-regulation되는 경우 4가지 경우 중,점차적으로 증가되는 4가지의 유전자,HLC5, COL4A1,KRT18,DYNLL1를 동정하였으며,정상을 제외하고 양성,악성에서 모두 증가되는 TAGLN,unknowngene2개를 포함하는 3가지 유전자,악성에서만 증가 되는 ENC1,SERPINE1,weaklysimilarRDX의 3가지 유전자,양성에서만 증가되 는 CLU, TNXA의 2가지의 유전자가 동정되었다. 한편,종양세포에서 down-regulation되는 경우는,점차적으로 감소되는 CIS,DHRS3,Lamininbeta-2similar gene,unknowngene1종류의 4가지 유전자와 정상에서는 발현이 되나,양성,악성
에서는 발현량이 모두 감소되는 IFITM1,ATP2A2,ASS,unknown gene1개의 4 가지의 유전자가 동정되었다(Table.1). C CC...NNNFFF111의의의 악악악성성성화화화에에에 관관관여여여하하하는는는 ccacaannndddiiidddaaatteteegggeeennneee선선선정정정 발굴된 DEG 중에서 발현량의 차이가 뚜렷한 20개의 유전자를 선별하여 cloning, 염기서열 분석을 통하여 유전자를 동정하였다.Un-knowngene4개를 제외한 16가 지의 유전자 중 NF1의 악성화에 의미가 있는 8개의 유전자를 연구대상으로 선정 하였다(Fig. 10). 유전자의 선정은, 이미 알려져 있는 유전자에 한해서 tumorigenesis와 관련이 있고,양성세포에서보다 악성세포에서 발현량이 증가 또는 감소한 유전자를 고려하였으며,세포가 악성화 되어 2차적 변화로서 당연히 발현량 이 변화하는 유전자는 배제하였다.이렇게 선정된 8가지 유전자로는,종양세포에서 발현량이 점차 증가하는 유전자,DYNLL1,양성과 악성 모두에서 발현량이 증가하 는 유전자,TAGNL,악성에서만 증가하는 유전자,ENC1,weakly similarRDX, SERPINE1,악성세포에서 발현량이 점차 감소하는 유전자는 IFITM1과 ATP2A2 이다(Table.2).
D
DD...RRRTTT---PPPCCCRRR을을을 이이이용용용한한한 DDDEEEGGG mmmRRRNNNAAA 발발발현현현량량량 평평평가가가
Screening통해 발굴된 64개의 DEGs중에서,선별된 8개의 DEGs에 대하여 해당하 는 유전자와 그 발현량의 차이가 일치하는지를 확인하기 위하여 normalskin, benign,malignanttissue로부터 배양한 fibroblasts에서 추출한 mRNA를 RT-PCR 로 합성한 cDNA를 주형으로 유전자 특이적 primer를 사용하여,상기 8개의 유전자 를 PCR로 증폭하였다. 그 결과 ENC1, weakly similar RDX, TAGLN, SERPINE1의 4개의 유전자에 대해서는 정상,양성,악성에 따라 발현량이 증가하
는 양상이 DEG screening결과와 일치하였으나,DYNLL1은 RT-PCR 결과 악성에 서보다 양성에서 발현량이 증가된 것으로 나타나,DEG screening 결과와 일치하지 않았다.또한 IFITM1과 DHRS3,ATP2A2의 3가지 유전자는 정상,양성,악성으로 발현량이 점차 감소하여 DEG screening결과와 일치하였다(Fig.11).
E
EE...WWWeeesssttteeerrrnnnbbblllooottttttiiinnnggg을을을 이이이용용용한한한 DDDEEEGGG 단단단백백백질질질 발발발현현현량량량 평평평가가가
DEG screening test와 mRNA 수준에서 해당 유전자의 발현량 차이를 단백질 수 준에서 확인하고자 normalskin,benign,malignanttissue에서 배양한 세포에서 단 백질을 추출하여 총 단백질 40 μg으로 Westernblotting을 통해 발현량을 확인하였 다. 8개의 candidated gene 중에서 transgelin(TAGLN), plasminogen activator inhibitor1(PAI-1, SERPINE1), interferone induced transmembrane protein1 (IFITM1),atpase2(ATP2A2)의 4개의 단백질에 대하여 발현량을 비교하였다.그 결과 transgelin과 PAI-1은 정상에서 양성,악성으로 갈수록 점차적으로 증가하는 것으로 나타났다.그리고 3가지의 celllines,HT1080,T24,A549를 각 40μg으로 Western blotting으로 endogenous한 발현량을 확인하였다.그 결과 transgelin은 HeLacells에서 상대적으로 발현량이 많은 것으로 나타났고,PAI-1은 HT1080cells 에서만 발현된 것을 확인하였다.IFITM1과 atpase2는 악성세포에서 발현량이 감소 한 것으로 나타났고,cellline에서 endogeneous한 발현량을 확인한 결과 IFITM1은 T24에서 발현되고,atpase2는 HT1080,T24celllines에서도 발현하나 HeLacells에 서 가장 많이 발현하였다.Westernblotting에 의한 단백질 수준에서 4가지의 DEGs 를 평가한 결과 DEG screening및 RT-PCR의 결과와 정확하게 일치하지는 않았으 나,정상과 악성에서 발현량이 증가 또는 감소하는 패턴은 일치하였다(Fig.12).
A AA... B BB... C CC... F FFiiiggg...77.7..BBBAAACCC---mmmeeedddiiaiaattteeedddaararrrrraaayyyCCGCGHGHH mmmiiicrccrroooaaarrrrrraaayyy...
Nogeneticalteration among the3typesofNF1cells.A,normalvsbenign;B, normalvsmalignant;C,benignvsmalignant.
F
FFiiiggg...888...EEExxxpppeeecccttteeedddeeexxxppprrreeessssssiiiooonnnpppaaatttttteeerrrnnnsssiiinnnDDDEEGEGG ssscccrrreeeeenenniiinnnggg...
8patternsofDEGsforconsideration,Thereareeach 4casesforup-regulation anddown-regulationinmalignantcells.
F
FFiiiggg...999...DDDeeettteeecccttteeedddeeexxxppprrreeesssssisiiooonnnpppaatattttteeerrrnnnsssiiinnn222000DDDEEEGGGsss...
4 patterns(11 DEGs) of Up-regulation and 2 patterns of Down-regulation(9 DEGs).(1)up-regulation from normalto malignantgradually;(2)Expression in benign and malignant; (3)Expression in malignant; (4)Expression in benign; (5)Down-regulation from normalto malignant gradually;(5)No expression in benign,malignant;N,normal;B,benign;M,malignant.
T
F
FFiiiggg...11100.0..EEExxxppprrreesesssssiiiooonnnpppaaatttttteeerrrnnsnssooofffttthhheeeiiidddeeennnttitiifffiiieeeddd888DDDEEEGGGsss...
A,Up-regulation 5 DEGs in the malignantcells.DEG 2,DYNLL1;DEG 18, ENC1;DEG 20,similar RDX; DEG 26,TAGLN;DEG 28,SERPINE1;B, Down-regulation 3 DEGs in the malignantcells.DEG 6,IFITM1;DEG 22, DHRS3,DEG 30,ATP2A2;N,normal;B,benign;M,malignant.
F
FFiiiggg...111111..V.VVaaallliiidddaatattiiiooonnnoofoffttthhheeeiiideddeennntttiiifffiiieeeddd888DDDEEGEGGsssbbbyyyRRRTTT---PPPCCCRRR...
cDNA was synthesized from NF1 cells'using reverse transcriptase.RT-PCR wasperformed using thecDNA with thegenespecificprimersfor8DEGs.C, control;N,normal;B,benign;M,malignant.
F
FFiiiggg...111222...VVVaaallliiidddaaatttiiiooonnnooofffttthheheeiiidddeeennntttiififfiiieeeddd444DDDEEEGGGsssbbbyyyWWWeeesssttteeerrrnnnbbblllooottttttiiinnnggg...
Forty μg ofprotein extractsfrom NF1cellsorcelllineswereloadedonto8~ 15% SDS-PAGE geland blotted ontonitrocellulosemembrane.Western blotting was performed using the specific antibody indicated.C,control;N,normal;B, benign;M,malignant;S,established cellline;S1,HT1080 cells(human N-Ras activatedepithelialfibrosarcoma);S2,T24cells(humanH-Rasactivatedepithelial carcinomas);S3,HeLa cells(human epithelialadenocarcinomas origin by cervix anduterine);S4,A549cells(humanepithelialcarcinomaoriginbylung).
F
FF...악악악성성성세세세포포포에에에서서서 uuuppp---rrreeeggguuulllaaatttiiiooonn된n된된 유유유전전전자자자(((TTTAAAGGGLLLNN)N))에에에 대대대한한한 RRNRNNAAAiii적적적용용용
TAGLN은 DEG screening,mRNA,단백질수준에서의 평가 결과 악성세포에서 발현이 증가되는 유전자로서 인위적으로 유전자를 knockdown하기 위하여 RNA간 섭(RNA interference,RNAi)법을 구축하였다.TAGLN에 대한 RNAiconstruct를 5 가지 제작하였다(Fig. 13). Control로는 human에게 존재하지 않는 green fluorescenceprotein(GFP)에 대한 RNAi를 사용하였다.pREP4 vector에 cloning한 RNAiconstructs는 먼저 endogenous한 transgelin 발현량이 많았던 HeLa cells에 transfection하여 추출한 단백질 40 μg을 이용하여 Westernblotting으로 발현량 감 소를 확인하였다.그 결과 RNAiconstruct5개 중에서 T#1,T#2,T#5가 효과적으로 발현량을 감소시켰고,T#4는 control에 비하여서는 감소가 되었으나 다른 construct 와 비교하였을 때 가장 효과적이지 않은 것으로 확인되었다.확인된 construct중에 서 가장 효과적인 T#2,5와 효과적이지 않은 T#4를 NF1 normalfibroblasts와 malignantcells에 각각 transfection하여 총 단백질을 추출하고,각각 40 μg의 단백 질을 이용하여 Western blotting을 통해 발현량을 확인하였다.먼저 NF1 normal fibroblasts에서는,T#2,T#4,T#5모두 control에 비하여 효과적으로 발현량이 감소 된 것을 확인하였고,그 중 T#4가 발현량의 차이가 가장 적어 비교적 효과적이지 않는 것으로 나타났다.이는 HeLa cells에 적용한 것과 일치하는 결과이다.또한 malignantcells에 동일한 constructs를 적용한 결과 3개의 constructs의 발현량 감 소 차이가 크지 않았으나,control에 비해서는 발현량이 감소된 것을 확인할 수 있 었다.또한 RNAi를 적용한 NF1 cells의 증식률(proliferation rate)을 비교한 결과 transfection하지 않은 NF1 normalfibroblasts는 56.8%,malignantcells은 72.67% 였고,TAGLN에 RNAi를 적용한 normalfibroblasts에서 control은 62.05%,T#2는 71.56%,T#4는 64.1%,T#5는 69.15%로 나타났으며,malignantcells에서 control은
62.86%,T#2는 65.11%,T#4는 66.88%,T#5는 69.17%로 나타났다.또한 RNAi를 적용한 normalfibroblasts에서는 Westernblotting 결과 발현량이 감소된 construct 와 증식율의 감소가 정확하게 일치하지 않았으나,malignant cells에서 Western blotting한 결과 발현량이 가장 많이 감소했던 T#2가 T#4,T#5와 비교하여 증식율 또한 가장 많이 감소한 것으로 나타났다.
F
FFiiiggg...111333...TTThhheeeRRNRNNAAAiiitttaararrgggeeetttssseeeqqquuueeennnccceeefffooorrrhhhuuummmaaannnTTTAAAGGGLLLNNN...
F
FFiiiggg...111444..E.EEvvvaaallluuuaaattitiiooonnnooofffRRRNNNAAAiiicccooonnnssstttrrruuuccctttsssfffooorrrTTTAAAGGGLLLNNN iiinnnHHHeeeLLLaaaccceeellllllsss...
Western blotting were performed using 40 μg ofprotein extracts from HeLa cells transfected with RNAi constructs forTAGLN(T#1, 2, 3, 4, 5) and GFP(control).T#1,2and 5areeffectiveconstructsto knockdown forTAGLN. C,controlRNAidesignedforGFP.
AAA...
BBB...
F
FFiiiggg...111555...EEEffffffeeeccctttooofffTATTAAGGGLLLNNN kknknnoooccckkkddodoowwwnnniiinnNnNNFFF111ccceelelllllsss...
A,Forty μgofproteinextractsfrom NF1cells'transfectedwithRNAiconstructs forTAGLN(T#2,4,5)andcontrolloadedonto15% SDS-PAGE gelsandblotted onto nitrocellulose membrane.Western blotting was performed with specific antibody indicated;B,NF1 cells'were seeded in 96wellplate(8 × 103cells/ml perwell)incubated at37℃ CO2incubatorfor12hours.Absorbanceat570nm
and 600nm weredetectedby spectrophotometerafterreaction with AlamarBlue for9 hours.N,normal;M,malignant;C,controlRNAidesignedforGFP.
G
GG...악악악성성성세세세포포에포에에서서서 uuuppp---rrreeeggguuulllaaatttiiiooonnn된된된 유유유전전전자자자(((SSSEERERRPPPIIINNNEEE111)))에에에 대대대한한한 RRRNNNAAAiii적적적용용용 악성세포에서 발현이 증가되는 SERPINE1에 대하여 발현량을 인위적으로 knockdown하기 위하여 RNAi를 구축․적용하였다.SERPINE1에 대하여 5개의 construct를 구축하였고,제작하였다(Fig.17).controlRNAiTAGLN의 경우와 같이 사용하였다.제작된 RNAi를 먼저 cellline에 적용하여 그 효율을 확인 하기위해, endogenous한 PAI-1의 발현량이 많았던 HT1080에 transfection하여 단백질을 추출 하고 Westernblotting으로 발현량의 변화를 확인하였다.그 결과 RNAiconstruct5 개중에서 P#2가 가장 효과적으로 발현량이 감소되었으며,P#5는 효과적이지 않은 것으로 나타났다(Fig. 18). 확인된 2개의 construct를 NF1 normal fibroblasts, malignantcells에 각각 transfection하여 총 단백질을 추출하고,40 μg으로 Western blotting을 통해 확인 한 결과,NF1cells모두에서 P#2가 발현량에 있어 가장 많은 감소 차이를 나타내었고,normalcells에서는 그 차이가 크게 나타났으나,malignant cells에서는 발현량 감소의 차이가 크지 않았다.또한 SERPINE1에 대한 RNAi constructs를 transfection한 NF1cells의 증식률을 비교한 결과 transfection하지 않 은 NF1의 normalcells 56.8%,malignantcells 72.67%였고,SERPINE1에 대한 RNAi를 처리한 NF1normalfibroblasts의 control은 62.05%,P#2는 68.68%,P#5는 66.42%로 나타났고, malignant cells에서 control 62.86%, P#2는 63.6%, P#5는 64.61%로 나타났다.Normalfibroblasts에서는 construct간의 발현량 감소와 증식율 의 변화가 일치하지 않았으나,malignantcells에서는 Westernblotting결과 가장 효 과적이었던 P#2가 그렇지 않은 P#5보다 증식률이 감소되었다.
F
FFiiiggg...111666...TTThhheeeRRRNNNAAAiiitttaaarrrgggeeetttssseeeqqquuueeennnccceeeffofoorrrhhhuuummmaaannnSSSEEERRRPPIPIINNNEEE111...
A cDNA sequenceandaminoacidsequenceofhumanSERPINE1wereshown. RNAiconstructsaredesignedat3sites.
F
FFiiiggg...111777...EEEvvvaaallluuuaaatttiiiooonnnooofffRRRNNNAAiAiicccooonnnssstttrrruuuccctttsssfffooorrrSSESEERRRPPPIIINNNEEE111iiinnnHHHTTT111000888000ccceeellllllsss... Western blotting performed using 40 μg ofprotein extractsfrom HT1080 cells transfected RNAiconstructs forSERPINE1(P#1,2,3,4,5)and GFP(control). P#2 is an effective constructto knockdown forSERPINE1.C,controlRNAi designedforGFP.
A A A... B B B... F FFiiiggg...111888...EEEffffffeececctttooofffSESSEERRRPPPIIINNNEE1E11KKKnnnooocckckkdddooowwwnnniininnNNNFFF111ccceeellllllsss...
A,Forty μgofproteinextractsfrom NF1cells'transfectedwithRNAiconstructs forSERPINE1(P#2,5)andcontrolloadedonto12% SDS-PAGE gelsandblotted onto nitrocellulose membrane.Western blotting was performed with specific antibody indicated;B,NF1 cells'were seeded in 96wellplate(8 × 103cells/ml
perwell)incubated at37℃ CO2incubatorfor12hours.Absorbanceat570nm
and 600nm weredetectedby spectrophotometerafterreaction with AlamarBlue for9 hours.N,normal;M,malignant;C,controlRNAidesignedforGFP.
H
HH...악악악성성성세세세포포에포에에서서서 dddooowwwnnn---rrreeeggguuulllaaatttiiiooonnn된된된 유유유전전전자자자의의의 ooovvveeerrr---eeexxxppprrreeessssssiiiooonnn시시시행행행
악성에서 down-regulation되는 유전자,IFITM1을 세포내에 over-expression시켜 기능을 알아보고자 하였다.먼저 cDNA를 주형으로 XhoI,BamHIenzyme을 사용하 여 human IFITM1을 cloning하였다(Fig. 19). 먼저 human N-Ras activated epithelialfibrosarcomas,HT1080과 human H-Ras activated epithelialsarcomas, T24,두 celllines에 각각 pREP4vector(control)와 IFITM1을 over-expression시키 고,단백질을 추출하여 Western blotting을 통해 확인한 뒤,증식률을 관찰하였다. 그 결과 HT1080에서는 control에 비해 증식률이 증가한 반면,T24에서는 감소하였 다(Fig.20).또한 NF1cell에 vector(control)와 IFITM1을 over-expression시켜 총 단백질을 추출하여 그 변화를 Westernblotting으로 확인하고 증식률을 실험한 결과 transfection 하지 않은 NF1normalfibroblasts는 56.8%,malignantcells은 72.67% 로 나타났고,vector를 transfection한 control의 증식률은 normalfibroblasts58.35%, Malignantcells은 58.42%로 나타났으며,IFITM1을 over-expression시킨 normal fibroblasts는 63.24%,malignantcells은 67.2%로 나타났다.transfection하지 않은 NF1malignantcells의 증식률(72.67%)에 비하여 IFITM1을 over-expression 시킨 malignantcells에서 그 증식률이 감소(67.2%)하였다(Fig.21).
F
FFiiiggg...111999...AA sA sseeeqqquuueeennnccceeeooofffhhhuuummmaaannnIIIFFFIIITTTMMM111...
The 2 arrows indicate direction and position of primer used construction of IFITM1cloning with 2vectors,pREP4and pEYFP-C1using 2enzymes,XhoI andBamHI.SequenceofprimerareF,5´-TTCTCGAGCTATGCACAAGGAGGA ACATGAGGTGG-3´;R,5´-CTGGATCCAGCATTGCACAGTGGAGTGCA-3´.
AAA...
BBB...
F
FFiiiggg...222000...OOOvvveeerrr---eeexxxppprrreeessssssiiioononnooofffIIIFFFIIITTTMMM111iiinnnHHHTTT111000888000aaannndddTTT222444ccceeellllllllliiinnneeesss...
A, Forty μg of protein extracts from HT1080 and T24 cell lines' were over-expressed with IFITM1 and pREP4 vector were loaded onto 15% SDS-PAGE gelsandblottedontonitrocellulosemembrane.Westernblotting was performed using the specific antibody,IFITM1;B,NF1 cells'were seeded in 96wellplate(1 × 104cells/mlperwell)incubated at37℃ CO
2incubatorfor24
hours.Absorbanceat570 nm and 600 nm weredetected by spectrophotometer afterreactionwithAlamarBluefor4 hours.
AAA...
BBB...
F
FFiiiggg...222111...OOOvvveeerrr---eeexxxppprrereessssssiiioononnooofffIIIFFFIIITTTMMM111iininnNNNFFF111ccceeellllllsss...
A,Forty μg of protein extracts from NF1 cells' were over-expressed with IFITM1and pREP4vectorwereloaded onto15% SDS-PAGE gelsand blotted ontonitrocellulosemembrane.Westernblotting wasperformedusing thespecific antibody,IFITM1;B,NF1cells'wereseededin96wellplate(8× 103cells/mlper
well)incubated at37℃ CO2incubatorfor12hours.Absorbanceat570nm and
I
II...IIIFFFIIITTTMMM11o1oovvveeerr-r--eeexxxppprrreeessssssiiiooonnn에에에 의의의한한한 세세세포포포형형형태태태 변변변화화화
IFITM1을 NF1cell에 over-expression하여 세포내 기능 및 형태 변화를 관찰하 기 위하여 humanIFITM1의 cDNA를 pEYFP-C1vector에 cloning하고,NF1cells 에 transfection한 뒤,mitotracker로 mitochondria를,DAPI로 nucleus를 염색하고, 세포내 발현 및 mitochondria와 nucleus의 형태를 confocal현미경으로 400× water lenz를 사용하여 관찰하였다.각각 vector를 over-expression시킨 pYFP-C1 vector (control)와 IFITM1을 NF1 normal fibroblasts, benign, malignant cells에 transfection하였다.발현 결과 Normalfibroblasts,benign cell과 Malignantcells에 각각 pYFP-C1vector(control)를 발현한 경우는 mitochondira나 nucleus에 다른 차 이를 나타내지 않았으나, IFITM1을 발현시킨 경우에는 모든 세포에서 mitochondria의 fragmentation이 일어나는 것을 확인하였다(Fig.22,23,24).또한, 세 가지 cells에 transfection하여 관찰한 결과 normalfibroblasts와 benign cells에 비하여 malignantcells에서 celldeath가 많이 나타나는 것을 확인하였다.
I IIFFFIIITTTMMM111 DDDAAAPPPIII MMMiiittotootttrrraaaccckkkeererr MMMeeerrrgggeee ( ( (NNNuuucccllleeueuusss))) (((MMMiitittoooccchhhooonnndddrrriiiaaa))) AAA... BBB... CCC... DDD... EEE... FFF... F FFiiiggg...222222...CCoCoonnnfffooocccaaalllmmimiicccrrrooossscccoooppipiicccaaannnaaalllyyysssiiisssooofffIIIFFFIIITTTMMM111eeexxxppprrreeessssssiiinnngggNNNFF1F11ccceeellllllsss... (A,B)NF1normalfibroblasts,(C,D)NF1benigncells,(E,F)NF1malignantcells. ConfocalmicroscopicanalysisofthetransfectedcellswithpEYFP-C1vector(A,
Ⅳ
Ⅳ
Ⅳ.
.
.고
고
고찰
찰
찰
신경섬유종증 제1형은 3~4천명에 한 명꼴로 발생하는 높은 발병률을 나타내는 유 전성질환으로,남녀,민족의 구분이 없이 발병하며,환자의 약 50%는 자연발생적 돌 연변이에 의해 발병되고,50%의 자손에게 대물림이 되는 우성유전질환으로 환자수 가 크게 늘어나고 있다.임상증상으로는 밀크커피색반점과 몇 개의 피부신경섬유종 이 나타나는 경한 경우부터 심각한 합병증을 나타내는 증세까지 매우 다양한 질병 양상과 경과를 보인다.또한 전체 환자의 약 10%정도에서는 악성으로 변화하여 그 예후가 매우 나쁘나 현재 그 변화에 대한 예측이 불가능하다.특히 plexiform neurofibroma는 매우 추한 형태로 나타나며,환자들은 심각한 외모 콤플렉스와 대인 기피,사회생활 부적응 등의 심각한 문제를 갖고 있다.언제 생길지 모를 합병증과 악성으로의 전환,우성유전으로 인한 결혼 후 자녀를 갖는 문제 등 환자 개인에게 큰 스트레스 및 자포자기의 불안감을 갖게 된다.그러나 유전병이라는 특수한 상황 과,다기관에 다발적으로 발생하는 질환으로 병소의 절제 외에는 특이한 치료방법이 없다.그러나 수술로 종양을 제거했다 할지라도 가끔 재발하기도하며,뇌의 심부등 과 같이 수술이 불가능한 부위에 발생할 경우 심각한 문제를 나타낸다.신경섬유종 증의 경우 다양한 종양의 발생과 악성화에 대한 문제는 심각하지만 그 뚜렷한 기전 을 찾지 못하고 있다.하지만 현재 연구되고 있는 부분은 NF1환자 증례보고,특정 유전자에 대한 부분적 연구가 대부분이나,이러한 연구로는 악성화 기전이나 치료법 개발에 이용하는 데는 한계가 있다고 생각된다.이러한 점에서 최근 암 관련 유전자 의 발현량을 분석한 연구가 보고(PascaleLevy등.2004)되었다.그러나 암 관련 유 전자의 발현양상만 비교하였으며,단백질 단계의 실험은 확인하지 않아 미비한 점이 많다.그래서 본 연구에서는 genomic DNA상의 유전적 변형을 알기위해 최신의CGH-array방법과 DEG screening방법을 도입하여 세포의 악성암화에 관여하는 유 전자를 효율적이고 체계적으로 분석하고자 하였다.
본 연구에서는 CGH-array결과 의의 있는 변화가 있는 염색체를 발견하지 못하였 다.이는 normal과 benign,normal과 malignant,benign과 malignant에 있어 염색체 및 gDNA의 유전적 변화가 원인이 아님을 알고,유전자 발현량의 차이임을 더욱 확 실히 하였다.이어 정상 세포와 암세포가 혼재된 조직에서 순수 정상세포와 암세포 를 혼합 없이 분리하여,각 세포그룹별로 유전자 발현 양상을 비교함으로 높은 유전 자 발현양상의 비교를 시행하였다.미세한 차이의 검출,정확한 발현량 평가라는 장 점을 가진 (주)Seegene의 GeneFishingDEG screening 방법을 이용하였다.이에 64 개의 발현량의 차이가 있는 DEG를 발견하였고,발현량의 차이가 가장 뚜렷한 20개 의 DEG를 선정하여 염기서열분석을 실시하였다.그리고 악성화에 의의 있는 유전 자를 선정하였다.DYNLL1,TAGLN,ENC1,RDX similar,SERPINE1,DHRS3, IFITM1,ATP2A2의 8개의 유전자를 선정하였다.여기에서 120개의 다른 primer set를 이용하여 DEG screening을 실시한 결과 2개의 DEG에서 IFITM1이 동정되 어 이점에 주목하여 연구를 진행하였다.그리고 각 해당 유전자에 특이 primer를 제 작하여 RT-PCR로 평가하였다.그 결과 DYNLL1을 제외하고 발현량이 모두 정확 하게 일치하지 않았으나 증가하는 양상,또는 감소하는 양상은 일치하였다.또한 단 백질 발현량에 있어서도 그 차이를 확인하기 위하여 구입이 가능했던 6개의 유전자 에 대한 단백질을 확인한 결과 DEG 결과보다는 RT-PCR결과와 더욱 일치하는 것 으로 나타났다.이 중 similarRDX는 RT-PCR과 DEG 결과가 잘 일치하였으나,정 확하게 밝혀지지 않은 유전자로 RT-PCR primer를 만들 때 RDX를 대상으로 하여, 단백질 실험은 진행하지 못하였다.dynein1(DYNLL1)은 RT-PCR결과가 DEG와도 일치하지 않았으며,ectodermal-neuralcortex(ENC1)는 RT-PCR과 DEG 결과가 매
우 정확하게 나타났으나 구매한 항체가 특이적으로 반응하지 못하여 단백질 수준의 발현량의 변화를 확인 할 수 없었다.
RT-PCR과 Western-blotting으로 발현량의 차이를 평가하고 최종 선정된 네 개 의 유전자의 기능을 규명하였다. 악성세포에서 발현량이 증가하는 TAGLN, SERPINE1에 대한 RNAiconstructs를 구축하고,NF1 celsl에 적용하여 Western blotting을 통하여 발현량의 차이를 확인한 결과 normal에 비하여 malignantcells에 서 발현량의 감소가 크게 차이를 나타내지 못하였다.이 결과는 악성세포에서 과다 하게 발현하는 양에 비하여 RNAiconstructs의 양이 적었던 것으로 생각되어진다. PAI-1은 cellangiogenesis의 migration과 proteolyticactivity를 조절한다고 알려져 있는 단백질로 gastric cancer의 malignancy marker로서 보고되었다(Stefansson 등, 2003; Sakakibara 등, 2006). 그리고 최근 in situ hybridization과 immunohistochemistry를 이용하여 피부성 NF1관련 neurofibroma에서 PA와 PAI 의 발현이 보고 되었다(Siren등,2006).
또한 down-regulation 되는 유전자 중 ATP2A2는 cDNA가 약 4Kb로 cloning에 어려움이 있어 추가적으로 기능실험은 진행하지 못하였다.
IFITM1은 세포표면 단백질의 한 종류로서, cytoskeleton과 endoplasmic reticulum(ER)에 존재하며,leukocytes와 endothelialcells에서 항분화 신호전달 체계 (transduction ofantiproliferativesignal)에 관여하는 복잡한 단백질체로,퇴근 만성 골수성 백혈병 환자에서 IFITM1의 발현이 감소하며(Tanaka 등, 2005), Interferone-γ의 antiproliferativeaction에서 중요한 역할을 한다(Yang등,2006).본 연구에서 IFITM1을 NF1 normal과 malignant cell에 각각 over-expression시켜 Western blotting으로 확인한 결과 normal에서도 발현이 된 것으로 나타났는데 이 는 controlvector의 transfection에 의하여 나타난 변화로 생각되어 진다.또한 NF1
cells에서 over-expression 되었을 때 mitochondria의 fragmentation을 일으키고,특 징적으로 malignantcell에서 celldeath가 일어나는 것으로 apoptosis와 관련이 있을 것으로 생각되어져 이에 관련된 추가적인 연구가 필요할 것으로 생각된다.
본 연구에서 NF1의 악성화에 관여하는 3가지의 유전자에 대한 기능 연구에 있어 NF1 normal fibroblasts와 malignant cells만을 사용하여 실험을 진행하였으나, benigncell을 포함하여 발현량을 조절하였을 때 각 세포별로 증식량 등의 변화차이 가 모든 cell에 나타나는 효과인지 malignantcells에서만 특징적으로 나타나는지의 반복 실험이 필요하며,세포의 기능을 확인 할 수 있는 cellbiology에 대한 추가연 구가 필요하며,다른 유전형을 가진 NF1환자의 시료에서도 해당 유전자의 발현량 또는 기능이 같은지 추가적인 연구가 요구된다.
Ⅴ
Ⅴ
Ⅴ.
.
.결
결
결론
론
론
신경섬유종증 제1형(Neurofibromatosis,NF1)의 악성화에 관련된 유전자를 발굴 하기위하여,DEG(Differentially Expressed Gene)screening을 시행하였다.NF1환 자의 normal,benign,malignantcell간에 발현량의 차이를 나타내는 64개의 DEGs 를 발굴하였고,그 중 발현량의 차이가 가장 뚜렷한 20개의 DEGs를 선정하여, unknown을 제외한 16개의 DEGs를 동정하고,NF1의 악성화와 관련성이 놀다고 판 단된 8개의 DEG에 대해 RT-PCR 및 Westernblotting으로 평가를 실시하였다.그 결과 최종적으로 NF1의 악성화에 관여하는 3개의 candidategene을 선정하였다.악 성화된 NF1 세포에서 up-regulation되는 유전자는 TAGLN, SERPINE1이고, down-regulation되는 유전자는 IFITM1이다. 유전자 발현조절 시스템을 통하여, 악성화 된 NF1 세포에서의 이들 3종류의 유전자에 대한 기능 규명을 실시하였다. TAGLN,SERPINE1은 RNAi적용 결과 NF1malignantcell의 증식률이 감소하였 으며,특히,IFITM1의 over-expression의 경우 양성 및 악성 NF1 cell모두에서 mitochondria의 fragmentation을 유도 하였으나,악성세포 특이적인 celldeath를 확 인 하였다.본 연구결과가 NF1의 악성화 기전규명과 NF1질병 치료법 개발에 응용 되기를 기대한다.
참
참
참고
고
고문
문
문헌
헌
헌
1.AkyerliCB,Beksac M,Holko M,FrevelM,Dalva K,Ozbek U,Soydan E, Ozcan M,OzetG,Ilhan O,Gurman G,Akan H,Williams BR,Ozcelik T: Expression ofIFITM1 in chronic myeloid leukemia patients.Leuk Res 29: 283-286.2005
2.BallesterR,MarchukD,BoguskiM,SaulinoA,LetcherR,WiglerM,Collins F:TheNF1locusencodesaprotein functionally related tomammalian GAP andyeastIRA proteins.Cell63:851-859,1990
3.Bollag,G.McCormick,F:Regulatorsand effectorsofrasproteins.Ann.Rev CellBiol7:601-632,1991
4.Bridge RS Jr,Bridge JA,Neff JR,Naumann S,Althof P,Bruch LA.: Recurrent chromosomal imbalances and structurally abnormal breakpoints within complex karyotypes ofmalignantperipheralnervesheath tumourand malignanttriton tumour:a cytogenetic and molecular cytogenetic study.J ClinPathol57:1172-1178,2004
5.CawthonRM,WeissT,XuGF,ViskochilD,CulverM,StevensJ,Robertson M,Dunn D,Gesteland R,O'ConnellP,White T:A majorsegmentofthe neurofibromatosistype1gene:cDNA sequence,genomicstructure,and point mutations.Cell62:193-201,1990
6.CerignoliF,Guo X,CardinaliB,RinaldiC,Casaletto J,FratiL,ScrepantiI, Gudas LJ,Gulino A,Thiele CJ,GianniniG:retSDR1,a short-chain retinol dehydrogenase/reductase,is retinoic acid-inducible and frequently deleted in
7.DasguptaB,GutamannDH,Neurofibromatosis1:closingtheGAP between miceandmen.CurrOpinGenetDev13:20-27,2003
8.Daston MM and RatnerN:Neurofibromin,apredominantly neuronalGTPase activating protein in theadult,isubiquitously expressed during development. DevDyns195:216-226,1993
9.DastonMM,ScrableH,NordlundM,Sturbaum AK,NissenLM,atnerN:The protein productoftheneurofibromatosistype1geneisexpressed athighest abundance in neurons, Schwann cells, and oligodendrocytes.Neuron 8: 415-428,1992
10.DeClue JE,Cohen BD and Lowy DR:Identification and characterization of the neurofibromatosistype1proteinproduct.ProcNatlAcadSci.USA,88: 9914-9918,1991
11.Eisenbarth I,BeyerK,Krone W,Assum G:Toward a survey ofsomatic mutation of the NF1 gene in benign neurofibromas of patients with neurofibromatosistype1.Am JHum Genet66:393-401,2000
12.EndoY,UzawaK,MochidaY,ShiibaM,BukawaH,YokoeH,TanzawaH: Sarcoendoplasmicreticulum Ca(2+)ATPasetype2down-regulatedinhuman oralsquamouscellcarcinoma.IntJCancer10:225-231,2004
13.Evans DG,Baster ME,McGaughran JM SharifS,Howard E,Moran A: Malignantperipheralnerve sheath tumours in neurofibromatosis 1.J Med Genet39:311-314,2002