접수: 2020년 2월 7일, 승인: 2020년 2월 20일 연락처: 박병주, 03080, 서울시 종로구 대학로 103
서울대학교 의과대학 예방의학교실 Tel: (02) 740-7325, Fax: (02) 747-4830 E-mail: [email protected]
Correspondence to: Byung-Joo Park, MD, PhD
Department of Preventive Medicine, Seoul National University College of Medicine, 103 Daehak-ro, Jongno-gu, Seoul 03080, Korea
Tel: +82-2-740-7325, Fax: +82-2-747-4830 E-mail: [email protected]
환자-교차연구와 환자-환자시간대조군연구의 개념과 약물역학연구에의 적용
서울대학교 의과대학 예방의학교실
김선지ㆍ박병주
Concept and Application of Case-Crossover Study and Case-Case-Time-Control Study in Pharmacoepidemiologic Study
Seonji Kim, PhD and Byung-Joo Park, MD, PhD
Department of Preventive Medicine, Seoul National University College of Medicine, Seoul, Korea
The importance of observational studies for evaluating drug safety in the field of pharmacoepidemiology is increasing rapidly. However observational studies are susceptible to selection bias and confounding. Many researchers have tried to develop ways to solve these problems. Case-crossover study (CCO study), a case-only design, was developed to over- come the methodological limitations of the case-control study, which was developed by Maclure in 1991 to identify the relationship between transient exposure and acute outcome. However, if level of exposure has time trend over calendar time, the application of CCO study is inadequate because it could overestimate or underestimate risk estimates. Case- case-time-control study (CCTC study) is the most recently developed method among the case-only study designs, which can control bias due to temporal trends in exposure. This article introduces concept and method of CCO study and CCTC study, and compare the results of two study designs evaluating the relationship between antidepressants and the risk of gastrointestinal bleeding. Understanding the concept and method of CCO study and CCTC study should be need- ed for conducting more valid phamacoepidemiologic research. (JPERM 2020;12:8-14)
Key Words: Case-crossover study; Case-case-time-control study; Bias; Pharmacoepidemiologic research
서 론
특정 신약이 식품의약품안전처로부터 시판을 허가받기 위하 여 시판전 임상시험을 수행하여 신약의 유효성과 안전성에 관 한 정보를 수집하지만, 연구대상자 수와 연구기간의 제약으로 인하여 시판허가를 받은 후 많은 환자들이 장기간에 걸쳐 약물 을 복용하는 경우에 드물지만 중증의 약물유해반응이나, 장기 복용, 약물오남용 등을 통하여 발생하는 심각한 유해반응을 충 분하게 파악하기는 대단히 어렵다. 이러한 이유로 인하여 약물
의 안전성을 평가하기 위한 시판 후 관찰연구의 중요성이 더욱 커지고 있다.
1)관찰연구에 적용하고 있는 기본적이고 전통적인 연구설계는
환자-대조군연구와 코호트연구 등이 있다. 그러나 이 두 가지
연구설계는 타당성 높은 인과성 평가결과를 얻게 해주지만, 특
정 질병에 걸린 환자군과 대조군, 특정 위험요인에 노출된 노출
군과 비노출군으로 설정하여 서로 다른 사람들끼리 비교하는
연구설계의 특성상 연구대상자 선정과정에서 선택비뚤림(selection
bias) 이 개입될 가능성이 높고, 연구자료를 분석하는 과정에 교
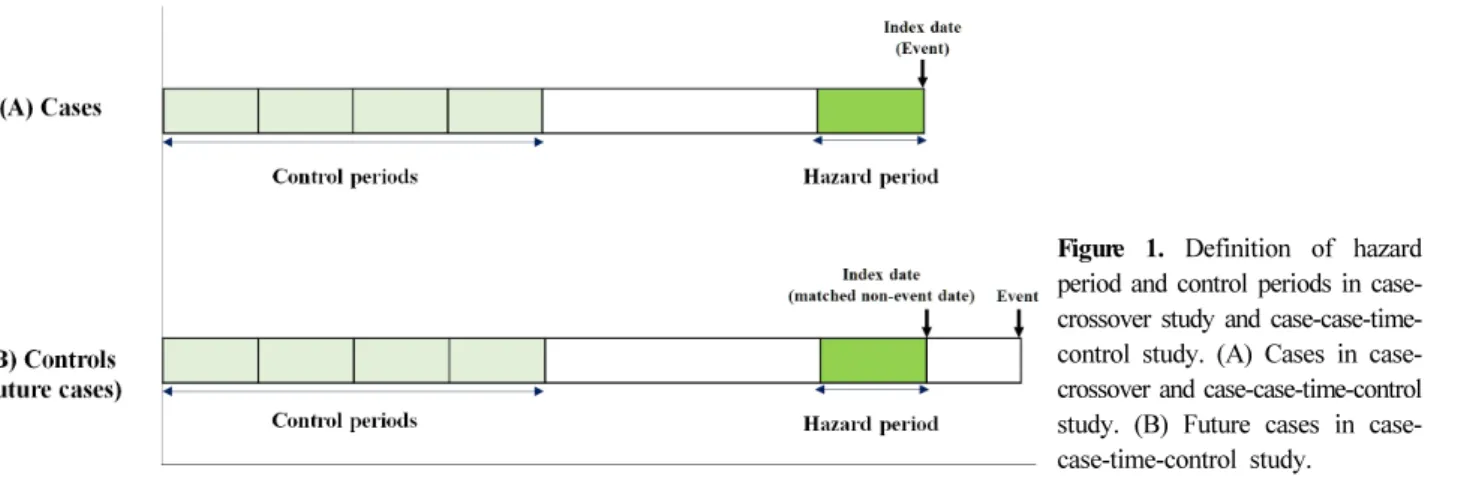
Figure 1. Definition of hazard period and control periods in case- crossover study and case-case-time- control study. (A) Cases in case- crossover and case-case-time-control study. (B) Future cases in case- case-time-control study.
란변수의 통제가 취약할 수 있기 때문에 이를 해결할 수 있는 방법이 필요하게 되었다.
2)이에 개별 환자를 스스로 자신의 대 조군으로 설정함으로써, 시간에 따라 변하지 않는 요인(time- invariant factor) 을 통제할 수 있는 새로운 연구설계들이 개발되 어 왔다.
3-6)환자-교차연구(case-crossover study)는 환자-대조군 연구에서 진화된 연구설계로서, 1991년 Maclure가 심근경색증 을 유발하는 위험요인을 파악하기 위하여 처음으로 적용하였 다.
3,7)이 연구방법은 약물역학분야뿐만 아니라 환경역학분야, 손상역학분야 등에서도 널리 사용되고 있다.
6,8-10)그 이후 환자- 교차연구에서 더욱 진화된 방법으로 2011년 Wang 등은 미래의 환자군을 대조군으로 적용한 기법인 환자-환자시간대조군연구 (case-case-time-control study) 를 개발하였는데, 환자군만을 연 구대상으로 하는 연구설계 가운데 가장 최근에 소개된 방법론 이다.
11)최근에는 환자-교차연구의 결과뿐만 아니라 환자-환자시간대 조군연구의 결과를 함께 제시하여 두 가지 결과의 차이에 대한 의미를 해석한 연구논문들이 발표되었다.
12,13)2016 년 흡입형 스테로이드의 사용시 천식의 악화를 환자-교차연구와 환자-환 자시간대조군연구 모두에서 유의하게 낮춘다는 연구결과를 발 표하였다.
12)그러나 상반되는 연구결과를 제시한 사례도 존재 한다. 2019년 Social Psychiatry and Psychiatric Epidemiology에 발표된 연구는 항우울제를 사용하였을 때 교통사고로 인한 사 망위험이 환자-교차연구로 수행한 경우에는 유의하게 증가하였 지만, 환자-환자시간대조군연구에서는 유의하지 않았다고 발표 하였다.
13)본 논문에서는 환자-교차연구와 환자-환자시간대조군연구의 개념과 방법을 소개한다. 또한 환자-교차연구와 환자-환자시간 대조군연구를 함께 적용하여 항우울제와 위장관계 출혈 발생간 의 관련성을 분석한 결과를 제시하여 향후 국내 연구자들이 적 극 활용할 수 있도록 하였다.
본 론 1. 환자-교차연구
환자-교차연구는 환자-대조군연구와 달리 환자가 자신을 대 조군으로 삼는데, 각각의 환자에서 질병 발생 직전의 일정기간 을 위험기간으로 정의하고, 그 이전의 질병 발생과 무관한 일정 기간을 대조기간으로 정의한다. 위험기간에서 위험요인에 대한 노출여부를 파악하여 대조기간에서의 노출여부와 비교하는 연 구방법이다(그림 1A). 환자-대조군연구는 같은 시점에 환자군 과 대조군에서의 특정 위험요인에 대한 노출여부를 비교하지 만, 환자-교차연구는 동일한 사람에서 다른 시간대에서 위험요 인에 대한 노출여부를 비교한다는 점에서 차이가 있다.
1)다른 관찰연구와 마찬가지로 환자-교차연구는 한 개의 위험기간에 대하여 대조기간을 여러 개로 두어 1:N 형태로 짝짓기하여 비 교할 수 있다.
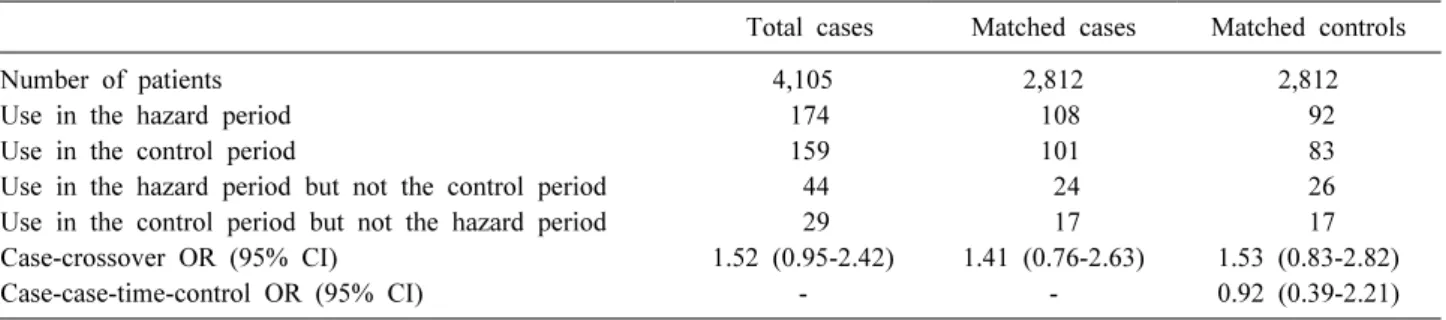
환자-교차연구는 위험기간과 대조기간을 짝지은 연구설계이 기 때문에, 위험기간과 대조기간에서 위험요인의 노출여부가 서로 다른 불일치쌍(discordant pair)만을 이용하여 교차비를 계 산한다. 상대위험도인 교차비를 산출하는 과정을 당뇨병 치료 제인 dipeptidyl peptidase-4 (DPP-4) inhibitors와 심부전증의 관 계에 대한 연구를 예로 이용하여 설명하고자 한다(표 1).
14)심 부전증환자 4,105명 중에서 위험기간에 DPP-4 억제제를 복용 하고 대조기간에서는 DPP-4 억제제를 복용하지 않은 환자는 44 명이었다. 반대로 대조기간에서만 DPP-4 억제제를 복용한 환자는 29명이었다. 그 결과 상대위험도인 교차비는 44/29=
1.52 로 산출할 수 있고, 95% 신뢰구간은 exp(ln(1.52)±1.96*
)을 이용하여 산출한 결과 0.95-2.42로 추정할 수 있다.
환자-교차연구를 적용하려면 위험요인의 노출은 인체에 일시
적으로 영향을 주고, 결과는 급성으로 나타나는 질병이라는 가
정이 성립되어야 한다.
3)환자-교차연구는 질병발생일을 기준으
로 위험기간과 대조기간을 정의하고, 이 두 기간에 의심되는 위
Total cases Matched cases Matched controls
Number of patients 4,105 2,812 2,812
Use in the hazard period 174 108 92
Use in the control period 159 101 83
Use in the hazard period but not the control period 44 24 26 Use in the control period but not the hazard period 29 17 17 Case-crossover OR (95% CI) 1.52 (0.95-2.42) 1.41 (0.76-2.63) 1.53 (0.83-2.82) Case-case-time-control OR (95% CI) - - 0.92 (0.39-2.21) CI, confidence interval; OR, odds ratio.
*Cited from 12. Dong Y-H, Wang SV, Gagne JJ, Wu L-C, Chang C-H. Comparison of Different Case-Crossover Variants in Handling Exposure-Time Trend or Persistent-User Bias: Using Dipeptidyl Peptidase-4 Inhibitors and the Risk of Heart Failure as an Example. Value Health. 2019.
Table 1. Calculation of odds ratio for dipeptidyl peptidase-4 inhibitors and heart failure in case-crossover study and case-case-time-control study*
험요인의 노출에 차이가 있는 지를 확인하여 의심되는 위험요 인이 질병발생의 원인으로 작용하였는지 판단하고자 개발된 연 구방법이다. 질병의 발생시점이 명확하여야 적절한 위험기간과 대조기간을 정의할 수 있다. 따라서 질병발생시점이 명확하지 않은 만성질환에는 환자-교차연구를 적용하기 어렵다. 노출의 영향이 일시적이지 않을 경우, 질병의 발생에 특정 위험요인의 노출을 포함한 다른 노출요인들에 의한 영향이 개입할 가능성 이 커진다.
15)마지막으로 위험기간과 대조기간에서 위험요인의 노출은 서로 독립적이어야 하며, 두 기간 사이에 잔류효과 (carry-over effect) 는 존재하지 않아야 한다.
5)특히 약물역학연 구의 경우, 한번 의료기관에 방문하여 수 일 혹은 수 주 동안 복용할 만큼의 약물을 처방받고, 일단 약물을 복용하면 체내에 서 영향을 미치는 지속시간이 존재하기 때문에 잔류효과를 고 려하는 것은 대단히 중요하다. 약물의 잔류효과로 인한 영향을 배제하기 위하여 특정 약물의 처방일수, 반감기 등을 고려하여 위험기간과 대조기간을 정의하여야 한다.
2. 환자-환자시간대조군연구
특정 약물의 사용수준이 시간경과에 따라 지속적으로 증가하 거나, 또는 감소하는 경향을 가지는 경우 즉 위험요인에 대한 노출수준이 시간적 경향성을 보일 경우에 환자-교차연구를 수 행하면 그 결과로 도출된 상대위험도가 과잉 또는 과소 추정될 가능성이 발생한다.
14)이러한 경우 특정 질병의 발생이 이후의 위험요인 노출에 영향을 미치지 않는다면, 양방향 환자-교차연 구로 시간적 경향성을 통제할 수 있다. 이 방법은 환경역학분야 에서는 많이 적용되어 왔다. 그러나 약물역학연구에서는 특정 약물을 복용한 후 환자의 의학적 상태가 변화한다면 해당 약물 의 처방을 중단하거나, 다른 약물로 변경할 가능성이 농후하기 때문에 양방향 환자-교차연구의 가정을 충족시키기 어렵다.
16)따라서 노출변수의 시간적 경향성을 보정하기 위한 다른 방법
으로 환자-교차연구를 확장한 연구설계인 환자-시간대조군연구 (case-time-control study) 와 환자-환자시간대조군연구가 개발되 었다.
5,11)환자-시간대조군연구는 Suissa가 질병발생 이후 약물사용의 시간적 경향성에 따른 비뚤림을 보정하기 위하여 환자-교차연 구와 환자-대조군연구의 방법을 결합하여 개발한 연구설계이 다.
5)환자-시간대조군연구에서 대조군을 선정할 때 고려할 점 은 특정 위험요인에 대한 노출은 각각의 환자군과 같은 시점에 서 측정하여야 한다는 점이다. 이 때 환자-시간대조군연구는 환 자-대조군연구와 마찬가지로 대조군이 적절하게 선정되지 못한 다면 다시 선택비뚤림을 야기할 수 있기 때문에 한계가 있다.
환자-환자시간대조군연구는 환자-교차연구와 환자-시간대조 군연구에서 확장된 연구설계로서 위험요인에 대한 노출의 시간 적 경향성과 적절한 대조군 선정을 모두 고려하기 위하여 미래 의 환자군을 대조군으로 선정하는 방법이다.
11)환자군에서 위 험요인의 위험기간에서의 노출여부와 대조기간에서의 노출여 부를 비교한 결과를 미래의 환자군에서 위험기간에서의 노출여 부와 대조기간에서의 노출여부를 비교한 결과를 다시 한 번 비 교하는 연구방법이다.
각각의 환자들에서 질병발생일을 확인한 후, 특정한 질병발
생일(index date)을 정하여 환자군으로 정의하고, 이 질병발생
일 이후에 질병이 발생한 환자들을 미래환자군(future cases)으
로 정의한다(그림 1A, B). 한 명의 환자군과 한 명 이상의 미래
환자군을 두고 연령, 성별, 시간 등을 변수로 하여 개별짝짓기
를 수행한다. 환자-환자시간대조군연구에서 환자군의 위험기간
과 대조기간의 정의는 환자-교차연구에서와 같다(그림 1A). 미
래환자군은 환자군에서의 위험기간과 대조기간의 시점에 맞추
어 정의한다(그림 1B). 즉 시간에 따라 단면적으로 확인한다면
위험기간 직후 환자군에서는 특정 질병이 발생하였지만, 미래
환자군에서는 결과가 아직 발생하지 않은 상태이다. 따라서 짝
지어진 환자군과 미래환자군에 대하여 각각의 위험기간과 대조 기간을 정의한다. 환자-환자시간대조군연구도 마찬가지로 불일 치쌍만을 이용하여 상대위험도인 교차비를 계산한다. 환자-교 차연구와 다른 점은 환자군에서와 미래환자군에서 상대위험도 를 각각 산출한 후, 산출된 두 상대위험도를 다시 비교하는 것 이다. 환자-환자시간대조군연구 또한 DPP-4 억제제와 심부전증 의 관계에 대한 연구결과를 예로 이용하여 상대위험도를 계산 하는 과정을 설명할 수 있다(표 1).
14)심부전증환자 4,105명 중 에서 환자군과 미래환자군을 연령, 성별, calendar time, 당뇨병 유병기간에 따라 1:1 짝짓기를 수행하여 총 2,812쌍이 매칭되 었다. 환자군에서 위험기간에서만 DPP-4 억제제를 복용한 환자 는 24명이었다. 대조기간에서만 DPP-4 억제제를 복용한 환자 는 17명이었다. 그 결과 상대위험도인 교차비는 24/17=1.41이었 고, 95% 신뢰구간은 exp (ln(1.41)±1.96* )을 이 용하여 산출하면 0.76-2.63으로 추정할 수 있다. 미래환자군에서 위험기간에서만 DPP-4 억제제를 복용하지 않은 환자는 26명이 었고, 대조기간에서만 DPP-4 억제제를 복용한 환자는 17명이었 다. 그 결과 상대위험도인 교차비는 26/17= 1.53이었고, 95% 신뢰 구간은 exp(ln(1.53)±1.96* )을 이용하여 산출하면 0.83-2.82 로 추정할 수 있다. 환자군에서의 상대위험도와 미래환 자군에서 상대위험도를 한 번 더 비교하여, DPP-4 억제제 노출 수준의 시간적 경향성을 보정한 환자-환자시간대조군연구에서 의 상대위험도는 1.41/1.53=0.92로 추정할 수 있고, 95% 신뢰구간 은 exp(ln(0.92)±1.96* )을 이용하 여 산출하면 0.39-2.21로 추정할 수 있다.
환자-환자시간대조군연구를 적용하려면 가장 먼저 환자-교차 연구에서와 마찬가지로 위험요인에의 노출은 인체에 일시적으 로 영향을 주고, 결과는 급성으로 나타나는 질병의 발생이어야 한다. 두 번째로 환자군과 미래환자군에서 시간에 따른 노출의 시간적 경향성은 동일하다는 가정이 성립되어야 한다. 이러한 가정은 환자-시간대조군연구에서와 마찬가지로 대조군에서의 선택비뚤림을 배제하기 위하여 충족되어야 한다. 또한 환자군 과 미래환자군의 짝짓기가 적절하게 수행될 수 있도록 적절한 추적관찰기간과 짝짓기 변수가 고려되어야 한다. 마지막으로 짝짓기를 수행하기 위하여 환자군과 미래환자군 사이에서 허용 가능한 지체시간(permissible lag time)를 고려해야 한다. 두 군 사이에 허용가능한 지체시간을 너무 가깝게 설정하면 짝짓기가 잘 수행되지 않아 선택비뚤림을 야기할 수 있고, 너무 멀게 설 정하면 약물 노출의 시간적 경향성을 적절하게 반영하기 어렵 기 때문이다. 따라서 노출수준의 시간적 경향성에 대한 양상을 확인한 후에 허용가능한 지체시간을 정의하는 것이 중요하며, 허용가능한 지체시간을 여러 개로 두어 민감도분석을 수행하는 방법도 추천된다.
3. 환자-교차연구와 환자-환자시간대조군연구의 적용사례 환자-교차연구와 환자-환자시간대조군연구를 함께 적용한 후 그 결과를 비교하기 위하여 항우울제의 사용과 위장관계출혈 발생과의 관계를 확인하는 연구를 수행하였다. 항우울제는 우 울증환자가 증가함에 따라 사용량이 시간경과에 따라 증가하고 있었다. 항우울제 중 Selective serotonin reuptake inhibitors (SSRIs) 는 가장 빈번하게 사용되는 약효군이다. 그러나 SSRIs 의 사용은 위장관계출혈을 포함한 출혈의 위험을 증가시키는 것으로 알려져 있다.
17)이는 SSRIs의 주요 신경조절물질인 세 로토닌이 혈소판의 기능에 관여하는데 세로토닌 재흡수를 억제 함으로써 혈소판의 세로토닌 함량을 감소시키고, 결과적으로 혈소판의 응집과 활성이 감소되어 출혈이 발생할 가능성이 높 아진다는 것이다.
18)세로토닌의 활성은 SSRIs 복용 후 7-14일 이내에 혈소판의 세로토닌 함량이 80% 이상 감소하여 혈소판 의 응집이 저해된다.
19,20)그러나 세로토닌은 SSRIs뿐만 아니라 다른 항우울제 약효군에서도 주요 조절인자로 관여하기 때문에 위장관계출혈의 위험을 높일 가능성이 있다. 따라서 항우울제 사용 후 급성으로 나타나는 위장관계출혈 발생과의 관련성을 2009 년 1월부터 2017년 7월까지 건강보험심사평가원 자료(심 평원 청구자료)를 이용하여 확인하였다.
21)연구대상자는 2009년 1월부터 2017년 7월까지 위장관계출혈 로 한 번 이상 입원하거나 응급실을 방문한 성인환자였다.
22,23)연구기간 첫 해인 2009년은 탐색기간으로 삼아 위장관계출혈 유병환자, 트라우마 손상으로 1번 이상 진단받은 환자, 위장관 계출혈 발생일 직전 관찰기간(index period)안에 항우울제를 처 방받지 않은 환자 등을 제외하였다. 또한 약물의 용량-반응관계 를 확인하기 위하여 일일상용량(Defined Daily Dose, DDD)이 약물안내서에 제시된 최대치 이상을 가지고 있는 환자는 이상 치로 판단하여 제외하였다.
환자 자신이 대조군이 되는 환자-교차연구를 설계하기 위하 여 연구대상에서 위험기간 1개와 대조기간 4개를 설정하여 1:4 개별짝짓기를 하여 위험기간과 대조기간에서 연구대상 약물의 노출빈도를 비교 분석하였다. 위험기간과 대조기간 사이에 잔 류효과를 배제하기 위하여 항우울제의 처방일수와 반감기, 혈 소판의 수명을 고려하였다. 첫 번째로 항우울제의 가장 긴 약물 인 fluoxetine의 반감기가 8일로 알려져 있어 8*4일로 산출하였 고, 두 번째로 항우울제 처방의 99%가 90일 이하로 처방되었 다.
24)세 번째는 혈소판의 수명은 7일로 알려져 있어, 약 2주 정도의 기간이 필요하다. 이를 종합적으로 고려하였을 때, 90일 의 휴약기간(washout period)을 설정하였다.
25)위험기간과 대조 기간은 각각 14일로 정의하였다.
22,26)연구에 포함된 항우울제는 약효군에 따라 Tricyclic anti-
depressants (TCAs), SSRIs, Serotonin-norepinephrine reuptake
inhibitors (SNRIs), Other antidepressants (Others) 로 구분하였
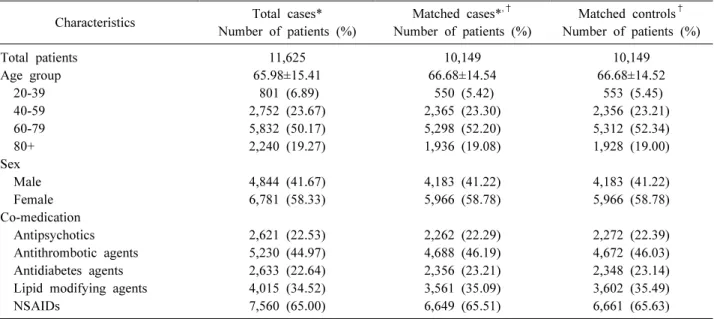
Characteristics Total cases*
Number of patients (%)
Matched cases*
,†Number of patients (%)
Matched controls
†Number of patients (%)
Total patients 11,625 10,149 10,149
Age group 65.98±15.41 66.68±14.54 66.68±14.52
20-39 801 (6.89) 550 (5.42) 553 (5.45)
40-59 2,752 (23.67) 2,365 (23.30) 2,356 (23.21)
60-79 5,832 (50.17) 5,298 (52.20) 5,312 (52.34)
80+ 2,240 (19.27) 1,936 (19.08) 1,928 (19.00)
Sex
Male 4,844 (41.67) 4,183 (41.22) 4,183 (41.22)
Female 6,781 (58.33) 5,966 (58.78) 5,966 (58.78)
Co-medication
Antipsychotics 2,621 (22.53) 2,262 (22.29) 2,272 (22.39) Antithrombotic agents 5,230 (44.97) 4,688 (46.19) 4,672 (46.03) Antidiabetes agents 2,633 (22.64) 2,356 (23.21) 2,348 (23.14) Lipid modifying agents 4,015 (34.52) 3,561 (35.09) 3,602 (35.49)
NSAIDs 7,560 (65.00) 6,649 (65.51) 6,661 (65.63)
NSAIDs, nonsteroidal anti-inflammatory drugs.
*Case-crossover study,
†Case-case-time-control study.
‡
Cited from 19. Seonji K. Evaluating the relationship between antidepressants by therapeutic class and brain hemorrhage in adults with depressive disorder: Seoul National University Graduate School; 2020.
Table 2. Characteristics of total study subjects and matched cases and controls for case-crossover study and case-case-time-control study
‡Case-crossover Adjusted OR* (95% CI)
(total cases)
Case-crossover Adjusted OR* (95% CI)
(matched cases)
Case-case-time-control Adjusted OR* (95% CI)
(matched pairs)
N=11,625 N=10,149 N=10,149 pairs
Total ADs 1.43 (1.34-1.53) 1.36 (1.27-1.46) 0.76 (0.69-0.84) TCAs 1.21 (1.10-1.35) 1.14 (1.02-1.27) 0.63 (0.55-0.74) SSRIs 1.62 (1.47-1.78) 1.61 (1.45-1.79) 0.94 (0.81-1.08) SNRIs 1.60 (1.31-1.95) 1.51 (1.22-1.87) 0.99 (0.75-1.32) Others 1.41 (1.28-1.55) 1.29 (1.17-1.43) 0.70 (0.61-0.80) CI, confidence interval; OR, odds ratio; ADs, antidepressants; TCAs, tricyclic antidepressants; SSRIs, selective serotonin reuptake inhibitors; SNRIs, serotonin-norepinephrine reuptake inhibitors.
*Adjustment for antipsychotics, antithrombotic agents, antidiabetes agents, lipid-modifying agents, and non-steroidal anti-inflammatory drugs.
†