대한소화기학회지 2000;35:458 - 465
비경구적 약물 남용자에서 C형 간염 바이러스 유전자형의 분포
가천대학교 의과대학 내과학교실, 분자생물학연구실*
김선숙・박동균・박종재・김유경・강동훈・최덕주・박현철・황유진*・김주현
D is tribu ti o n o f H e pa ti ti s C Viru s Ge n o t y p e s a m o n g In t ra v e n o u s Dru g U s e rs
S u n S u k Ki m , M .D., D o n g Ky u n P a r k , M .D., J o n g J a e P a r k , M.D., Yu Ky e o n g Ki m , M.D., D o n g H o o n Ka n g , M.D., D e ok J u Ch oi , M.D., Hyun Chul P ark, M.D., Yu J in Hw ang, Ph.D.* and J u Hyun Ki m, M.D.
Department of Internal Medicine, Laboratory of Molecular Biology*, Gachon Medical School, Gil Medical Center, Inchon, Korea
Background/Aims: The distribution of hepatitis C virus (HCV) genotypes is different according to
the geographic area, and intravenous drug users (IVDU) are quite susceptible to chronic hepatitis C.According to recent studies in Europe, IVDU was different from other risk groups in HCV genotype distribution. The aim of our study was to analyze the distribution of HCV-genotypes among IVDU in Korea. Methods: We studied 74 HCV-RNA-positive patients with chronic hepatitis C (male vs female: 2.7 vs 1; mean age: 40.8 years). HCV genotypes were determined using reverse transcription-polymerase chain reaction with genotype-specific primers according to Okamoto' s method. The patients were classified into 3 groups (IVDU group, blood transfusion group, and unknown cause group) according to the transmission route. The genotype distribution of IVDU group was compared with those of others groups. Results: For all patients examined, the genotype frequencies were as follows: genotype 1b, 59.5%; 2a, 33.8%; 1a, 1.4%; 2b, 1.4%; mixed genotype 1b+2a, 1.4%. Genotype 1b and 2a were the most prevalent (93.3%). Among IVDU, the genotype frequencies were as follows: genotype 1b, 59.5%; 2a, 33.3%; 1a, 0%; 2b, 0%; mixed genotype 1b+2a, 2.4%. The IVDU group showed similar pattern in the genotype frequencies as compared with other groups. However, the mean age of IVDU group was significantly younger than those of other risk groups. Conclusions: Among IVDU in Korea, genotype 1b and 2a were the most prevalent, and the distribution of HCV genotypes was not different from those of other causes. (Kor J
Gastroenterol 2000;35:458 - 465)
Key Words: HCV Genotype, Intravenous drug users, Chronic Hepatitis C
접수: 1999년 11월 8일, 승인: 2000년 3월 12일
연락처: 김선숙, 405-760, 인천 남동구 구월동 1198번지, 가천대학교 의과대학 부속 길병원 소화기내과 Tel: (032) 460-3188, Fax: (032) 460-3408
김선숙 외 8인. 비경구적 약물남용자에서 C형 간염 바이러스 유전자형의 분포 459
서 론
C형 간염 바이러스(hepatitis C virus : HCV)는 단 일가닥의 RNA 바이러스로 1년에 뉴클레오타이드 당 1.4-1.9×10-3의 높은 자가변이를 일으켜 대략 70%의 염기서열의 상동성을 보이는 다양한 바이러 스이다.1 이러한 유전적 이질성이 있어 계통발생적 으로 분류가 가능하여 최소 6개 이상의 유전자형으 로 분류된다.2 유전자형에 따라 임상경과, 인터페론 치료에 대한 반응 및 예후가 다르며, 세계적으로 지 역적 분포의 차이를 보여 감염경로를 찾는 역학적 연구에 유용성이 있다고 알려져 있다.1,3 한국, 일본, 동남아, 미국은 1, 2형이 주종을 이루나 유럽에서는 1, 3형이 많고 중동, 아프리카 등에서는 4, 5형이 많 다고 알려져 있다.3
HCV는 B형 간염 바이러스와 같이 비경구적 경 로로 전염되며 특히 수혈과 비경구적 약물 남용자 에서 호발한다. 수혈에 의한 C형 간염은 수혈전 검 색검사로 anti-HCV검사를 시행한 이후 현저히 줄었 지만 약물 남용에 의한 C형 간염은 크게 늘어 사회 적, 의학적 문제로 대두되게 되었다. 비경구적 약물 남용자의 40-90%에서 anti-HCV 양성을 나타낸다고 알려져 있고4-7 이들의 HCV 유전자형은 나라 및 지 역에 따라 다른 분포를 보인다고 한다. 최근 프랑스 등 일부 유럽 국가의 보고에 의하면 같은 지역 내에 서도 감염경로에 따라 HCV 유전자형의 분포가 달 라 비경구적 약물 남용자의 주 유전자형은 수혈이 나 원인미상인 경우와 다른 분포를 보인다고 한다.8 우리 나라의 비경구적 약물 남용자에서 HCV 유병 률에 대한 보고는 있으나9 아직까지 유전자형의 분 포에 대한 보고는 없다. 이에 저자들은 비경구적 약 물남용에 의한 만성 C형 간염 환자에서 HCV 유전 자형의 분포를 알아보고자 하였다.
대상 및 방법
1. 대 상
1994년 9월부터 1997년 3월까지 가천 의과대학 부속 길병원에 내원하여 만성 C형 간염으로 진단받
은 113예 중 HCV-RNA 양성으로 HCV 유전자형 검사가 가능한 74예를 대상으로 하였다. 만성 C형 간염의 진단은 anti-HCV (2세대 EIA) 양성이고 6개 월 이상 간기능 이상을 보이며 B형 간염, 술, 독성 물질, 대사 장애 등 다른 원인에 의한 간질환이 제 외된 경우로 하였다. 대상 환자 중 남자는 54예, 여 자는 20예였으며 이들의 평균 연령은 40.8세(19-75 세)였다.
2. 방 법
1) H CV - RNA 검출 및 유전자형 검사 이들 환자의 혈청 100 ul로부터 guanidinum- isothiocyanate-acid phenol procedure (TRI reagent, GIBCO BRL)을 이용하여 전체 RNA를 추출한 뒤, random hexamers (Promega)를 이용하여 94℃에서 5 분간 denaturation, 5분간 급냉하여 annealing시키고, 5x 역전사효소완충액, 10 mM dNTPs 혼합액, RNase inhibitor (RNasin) 40 U/ul, M-MLV (Molo- ney-Murine Leukemia Virus) 역전사효소(Promega) 200 U/ul을 섞어서 첨가한 후 42℃에서 60분간 반응 시켜 cDNA를 얻었다. 유전자형 검사를 위해 PCR 에 사용한 시발체는 Okamoto 등10에 의한 방법에 의하여 HCV의 Core 부위에 해당하는 염기서열을 선택하여 DNA 합성기를 사용하여 제조하였다 (Table 1). 먼저 universal primers (no. 256과 no.
186)로 94℃에서 60초, 55℃에서 60초, 72℃에서 60 초 조건으로 35회 1차 PCR을 수행하였다. 1차 PCR 생산물 중 1 ul을 취하여 universal primer (no. 104) 와 4개의 type-specific primers (no. 132, no. 133, no.
134, no. 135) 혼합물을 94℃에서 60초, 60℃에서 60 초, 72℃에서 90초 조건으로 30회 2차 PCR을 수행 하였다. 10 ul의 PCR 산물을 2% 한천 겔 전기영동 하여 각 유전자형에 특이한 크기의 PCR band를 확 인하였다. 이상의 1차 검사로 band가 불명확할 경우 4개의 type-specific primers를 두 개씩 묶어 만든 혼 합물로 각각 PCR을 시행하여 band를 확인하였으며 기대한 DNA band를 얻지 못한 경우는 undeter- mined로 분류하였다. 대상 예 중 35명의 혈청을 무작 위 추출하여 Chayama 등11에 의한 방법에 따라 NS5 부위에 해당하는 genotype-specific primer로 RT-PCR
460 The Korean Journal of Gastroenterology : Vol. 35, No. 4, 2000 을 시행하여 94% (33/35)의 일치율을 얻었다.
2) 분석 방법 및 요소
대상 환자는 문진을 통하여 분명한 비경구적 약 물남용의 병력이 있으면 약물 남용군, 수혈한 병력 이 있으면 수혈군, 특별한 원인이 없으면 원인 미상 군으로 분류하여 이들 간의 성, 연령, 간기능 이상의 기간, ALT 최고치 및 HCV 유전자형을 후향적으로 분석하였다.
3) 통계학적 분석
모든 측정치는 평균±표준오차로 표시하고 두 군 사이의 분석은 SAS 통계 분석 프로그램을 이용하여 Student`s t-test or chi-square test로 검증하였고 유의 수준은 p<0.05로 하였다.
결 과
1. 대상 환자의 임상적, 생화학적 특성 대상 환자 74명 중 58명(78%)에서 감염경로가 확 인되었다. 42명(56%)이 비경구적 약물 남용자였고 16명(22%)이 수혈을 받은 병력이 있었으며 16명 (22%)은 원인을 찾을 수 없었다. 비경구적 약물 남 용자의 남녀 구성은 남자가 34명, 여자가 8명이었고 사용한 약물의 종류는 누바인이라는 마약성 진통제 와 필로폰이었으며 사용 기간은 알려지는 것을 꺼리 는 관계로 정확히 파악할 수가 없었다. 평균 연령은 수혈군과 원인 미상군에서는 유의한 차이가 없었으 나(48.8±11.7세 vs. 44.7±16.9세) 약물 남용군에서 는 28.9±11.7세로 다른 군에 비해 유의하게 낮았다 (p<0.05). 약물남용군에서 간기능 이상의 기간이 짧 은 경향을 보였으나 통계적 유의성은 없었고 세
Table 1. Oligonucleotide Primers Used for HCV Genotyping
Primer number Sequence (5'-3') Nucleotide position
256 (S) 186 (AS) 104 (S) 132 (AS) 133 (AS) 134 (AS) 135 (AS)
CGCGCGACTAGGAAGACTTC ATGTACCCCATGAGGTCGGC AGGAAGACTTCCGAGCGGTC TGCCTTGGGGATAGGCTGAC GAGCCATCCTGCCCACCCCA CCAAGAGGGACGGGAACCTC ACCCTCGTTTCCGTACAGAG
139-158 391-410 148-167 185-204 272-291 302-321 251-270
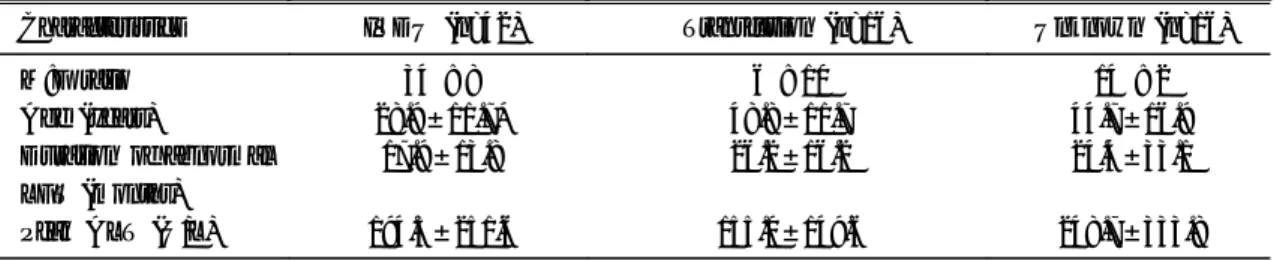
Table 2. Clinical and Biochemical Characteristics in 74 Patients with Chronic Hepatitis C
Characteristics IVDU (n=42) Transfusion (n=16) Unknown (n=16) M:F ratio
Age (years)
Duration of abnormal LFT (months) Peak ALT (U/L)
34 : 8 28.9±11.7*
17.9±13.8
194.5±251.6
6 : 10 48.8±11.7 26.2±16.2
155.0±149.6
14 : 2 44.7±16.9 24.4±33.1
248.7±333.8 IVDU, intravenous drug users; values are mean±SD.
* p<0.05 vs transfusion and unknown.
Kim, et al. Distribution of HCV Genotypes among Intravenous Drug Users 461
군간의 ALT 최고치에서도 유의한 차이가 없었다 (Table 2).
2. C 형 간염 감염경로에 따른 세 군간의 연령 분포
약물 남용군은 20대가 29명(69.9%), 30대가 8명 (19.0%)으로 대부분 젊은층이었고 수혈군은 50대가 7명(43.7%), 60대 이상이 2명(12.5%)로 대부분 노년 층이었으며 원인 미상군은 전체적으로 고른 연령 분포를 나타내었다(Table 3).
3. 감염경로에 따른 H C V 유전자형의 분포 전체 대상 환자의 HCV 유전자형의 분포는 II(1b) 가 44명(59.5%), III(2a)가 25명(33.8%), I(1a)가 1명 (1.4%), IV(2b)가 1명(1.4%), II+III(1b+2a) 혼합형이 1명(1.4%), 본 방법으로 유전자형을 알 수 없었던 예가 2명(2.7%)이었다. 감염경로에 따른 유전자형의 분포는 수혈군과 원인 미상군에서 I(1a)는 각각 0%
와 6.3%, II(1b)가 56.2%와 62.5%, III(2a)가 37.5%
와 31.3%, IV(2b)가 6.3%와 0%이었다. 약물 남용군 에서는 I(1a)가 0%, II(1b)가 59.5%, III(2a)가 33.3%, IV(2b)가 0%, II+III(1b+2a) 혼합형이 2.4%, 본 방법 Table 3. Age Distribution according to the Transmission Route of HCV Infection
Age (years) IVDU (n=42) Transfusion (n=16) Unknown (n=16) 0-29
30-39 40-49 50-59
≥60
29 (69.9%) 8 (19.0%) 1 ( 2.4%) 2 ( 4.8%) 2 ( 4.8%)
1 ( 6.3%) 3 (18.8%) 3 (18.8%) 7 (43.7%) 2 (12.5%)
2 (12.5%) 4 (25.0%) 4 (25.0%) 3 (18.8%) 3 (18.8%) IVDU, intravenous drug users.
Fig. 1. Distribution of HCV genotypes according to the route of transmission in 74 patients with chronic hepatitis C. Among IVDU, genotype 1b and 2a were the most prevalent and distribution of HCV genotypes was not different from those of other groups. U.d, undetermined.
462 대한소화기학회지 : 제 35 권 제 4 호 2000
으로 유전자형을 알 수 없었던 예가 4.8%로 다른 군과 유의한 차이를 보이지 않았다(p>0.05; Fig. 1).
비경구적 약물 남용자에서 각 유전자형별로 임상적, 생화학적 특성은 유의한 차이가 없었다.
고 찰
세계적으로 약물 남용자가 급속히 증가하고 있고 이들은 주사기구를 공유하고 집단행동 및 문란한 성생활을 하기 때문에 에이즈나 바이러스 간염의 발병률이 높다는 것은 잘 알려진 사실이다. 에이즈 양성률은 0-32%, B형 간염 양성률은 1-6%인데 비 하여9,12,13 C형 간염 양성률은 40-90%로 매우 높 다.4-9,12,13 같은 비경구적 경로로 전염되나 에이즈는 동성연애 등 성생활 패턴과 약물 남용이, B형 간염 은 주산기 수직감염과 성접촉을 통하여 주로 전염 되는데 비해 C형 간염은 수혈 및 비경구적 약물 남 용이 주 전염경로로 알려져 있다. 수혈 전 검색검사 로 anti-HCV검사를 시행하면서 수혈로 인한 C형 간 염은 현저히 감소했지만 젊은 사람을 중심으로 비 경구적 약물 남용자가 크게 늘면서 C형 간염의 주 감염경로로 대두되게 되었다.4-7 C형 간염이 아직까 지 예방주사가 개발되지 않았고 대부분 만성 간염 으로 진행되고 간경변, 간암 등의 치명적인 합병증 을 일으킨다는 사실을 고려할 때 C형 간염 양성인 비경구적 약물 남용자에서 HCV 유전자형을 분석하 여 분포 양식을 알아보는 것은 질환의 예방학적 측 면, 역학, 임상경과 및 인터페론치료에 대한 반응 등 을 연구하는 데 중요한 지침이 될 수 있다.
HCV 유전자형은 세계적으로 나라 및 지역에 따 라 다른 분포를 보인다고 알려져 있다. 유전자형 1, 2와 3형은 각각 빈도에는 차이가 있으나 전세계에 분포되어 있으며 4, 5와 6형은 특정 지역에 국한되 어 나타난다. 미국 및 일본은 1형과 2형이 대부분이 고 유럽 지역은 1형과 3형이 대부분이며 아프리카 및 중동 지역에는 4형과 5형이 많으며 홍콩에는 6 형이 많다.3 우리 나라의 경우 1b가 45%, 2a가 51%, 1a, 2b, 3a가 각각 1%로 보고14도 있고 1b가 71%, 2a가 23.9%, 1a가 2.1%, 2b가 1.5%, 미상형이 1.5%
라는 보고15도 있으며, 또다른 보고16에서는 1b가
57.7%, 2a가 32.2%, 1a가 1.3%, 혼합형이 9.0%로, 우리 나라 HCV 유전자형은 1b와 2a가 90% 이상을 차지하는 것으로 보고되고 있다. 본 연구에서도 1b 가 59.5%, 2a가 33.8%로 1형과 2형이 대부분으로 다른 보고와 다르지 않았다.
최근 프랑스, 이태리, 스페인을 비롯한 일부 유럽 국가를 중심으로 감염경로에 따라 유전자형의 분포 가 변하고 있다는 보고가 있다.8,17-20 프랑스에서의 연구에 의하면 수혈을 받은 환자나 원인 미상인 환 자의 경우 유전자형의 분포는 1b가 각각 52%와 54%, 1a가 19%와 14%, 3a가 10%와 19%, 나머지가 19%와 23%로 1b가 제일 많고 비경구적 약물 남용 자에서는 3a가 63%, 1a가 33%, 1b가 0%, 나머지가 5%로 3a가 유의하게 높은 분포를 나타내어 감염경 로에 따라 유전자형의 분포가 다르다고 한다.8 또한 프랑스 국경과 가까운 스페인 서부 Basque 지역에 서는 스페인 중부 및 남부 지역과 다르게 비경구적 약물 남용자에서 유전자형 3a가 75%, 1a가 12.5%, 혼합형이 12.5%로 유의하게 3a가 많다고 보고하였 고 이태리에서의 연구에서도 3a가 주종을 이루고 대부분 30대이며 계속 약물을 주사하기 때문에 2개 이상의 유전자가 공존하는 혼합형도 비교적 높게 나타난다고 한다.17,18 이와 같이 감염경로에 따라 HCV 유전자형의 분포가 다르다는 보고는 대부분 비경구적 약물 남용자가 많고 지역적 위치상 국가 와 국가가 근접해 육로로도 국가간 왕래가 잦은 유 럽 국가에서의 현상이다. 유전자형 1형과 2형이 80% 이상을 차지하는 미국이나 일본의 경우 이와 같은 보고가 아직까지 없다.21-23 미국의 경우 유전자 형 3형은 젊은 사람에서 많은 경향을 보이나 비경구 적 약물 남용자의 주 유전자형은 아니라고 보고하 고 있다.22 유전자형 3형이 최근에 미국에 유입되었 을 가능성을 시사할 수 있으나 비경구적 약물 남용 을 통하여 도입되었다고 결론지을 수 없으며 다른 원인을 고려해야 할 것이다. 본 연구에서 비경구적 약물 남용자에서 HCV 유전자형의 분포는 1b가 59.5%, 2a가 33.3%로 수혈군이나 원인 미상군의 분 포와 다르지 않아 우리 나라에서는 감염경로에 따 라 유의한 차이를 보이지 않았다.
비경구적 약물 남용자에서 특이한 HCV 유전자
김선숙 외 8인. 비경구적 약물남용자에서 C형 간염 바이러스 유전자형의 분포 463
형 분포를 나타내는 이유는 검사 방법상의 차이, HCV의 바이러스적 성질 및 감염경로에 따른 역학 적인 면에서 고려해야 한다고 생각된다. 각각 바이 러스 유전자를 증폭하여 염기서열을 비교 분석하는 것이 HCV 유전자형을 측정하는 가장 정확한 방법 이나 비용이 너무 비싸고 시간이 많이 걸리는 단점 이 있어 많은 환자를 대상으로 하는 임상연구에 사 용하기에는 어려운 점이 많다.10,11 몇몇 특이한 염기 서열의 변화에 기초하여 유전자형을 분석하는 유전 자-특이시발체를 사용한 중합효소연쇄반응(PCR), 제한효소를 사용하는 RFLP, 유전자형 특이소식자 를 사용한 differential hybridization, 혈청학적 분석 법 중 한 두 가지를 선택하여 연구가 시행되고 있는 데 대체로 각 방법간의 높은 일치율을 나타낸다고 알려져 있어 각 연구에서 사용된 검사 방법상의 차 이가 이런 현상을 설명해 주진 못하는 것 같다.24 본 연구에서 사용한 유전자형 특이시발체를 사용한 PCR 방법은 기술적으로 다른 방법에 비하여 간단 한 이점이 있으나 목표한 유전자형 이외에는 검출 이 안 되는 단점이 있다.10,11 본 연구에서는 Core 부 위에 기초하여 간편하게 1a, 1b, 2a, 2b형을 검출할 수 있는 Okamoto 등10의 방법을 택하였는데 우리 나라 HCV 유전자형의 분포는 1b와 2a가 90% 이상 을 차지하는 것으로 알려져 있어14-16 방법상의 큰 문제는 없으리라고 생각된다. 둘째로 바이러스 성질 상 자가변이율이 높은 바이러스이기 때문에 변이를 일으켰거나 비경구적 약물 남용자는 지속적으로 전 염 위험에 노출되므로 두 가지 유전자형의 혼합감 염이 상대적으로 높아 그 중 하나가 우세하게 되어 유전자형이 바뀌게 될 가능성이다. 오랜 기간 반복 적 수혈을 받는 혈우병 환자에서 HCV 유전자형이 변했다는 보고에서 간접적으로 추정해 볼 수 있으 나 극히 제한된 보고뿐이다.25 본 연구에서 혼합형이 1예(2.4%) 관찰되었으나 스페인과 이태리의 연구에 서처럼 높지 않았으므로, 반복적 약물 남용을 하는 사람을 대상으로 전향적 연구가 시행되어야 할 것 이다. 또 하나는 마약의 유입과 함께 다른 지역으로 부터 새로운 유전자형이 도입되고 이들은 주사기구 를 공유하고 그들만의 특수한 생활양상이 있기 때 문에 이 집단 내에서 독립된 형태로 전파되었을 가
능성이다. 프랑스의 연구에서 보면 최근 20년 이내 에 비경구적 약물 남용자가 급증하면서 유전자형 3a 가 도입되어 수혈 및 원인 미상의 약물 비남용군에 서 40여년 전부터 기존하는 유전자형 1b, 1a, 2a와 다르게 젊은 사람에서 3a가 우세하게 되어 약물 남 용군과 약물 비남용군의 2개의 독립된 전파양식으 로 존재하게 되었다고 보고하였다.8 아직까지 우리 나라는 비경구적 약물 남용자가 상대적으로 적고 이들 사이의 국제적 밀접한 신체적 접촉이 적으며 아마도 나라 및 지역에 따라 위치적 관계, 생활양식, 비경구적 약물 남용자의 생활패턴 등이 달라 이러 한 차이를 보이는 것으로 생각된다.
본 연구에서 한 가지 주목할 사실은 감염경로에 따라 유전자형의 분포에는 유의한 차이가 없었으나 비경구적 약물 남용자의 평균 연령이 수혈군이나 원인 미상군에 비하여 유의하게 낮았다는 사실이다.
이는 우리 나라에서도 최근 비경구적 약물 남용자 가 증가하면서 젊은 사람에서 C형 간염의 주 전염 경로가 비경구적 약물 남용으로 변화하고 있음을 시사하며 장차 20-30년 뒤에는 유럽국가처럼 새로 운 유전자형이 도입되어 이들 집단 사이에서 확산 되면서 유전자형의 분포가 바뀌어 비경구적 약물 남용자의 유전자형의 분포는 수혈이나 원인 미상인 경우와 다르게 독립된 역학현상을 보일지도 모른다.
사회적 분위기상 자신의 약물 남용 사실을 숨기는 경향이 있으므로 특히 젊은 사람에서 C형 간염으로 진단되면 자세히 문진을 하여 원인을 찾아보고 이 들을 교육하여 주사기구를 공유하는 습관을 방지한 다면 전염경로를 차단하게 되어 향후 C형 간염을 예방하는 데 큰 도움이 될 것이다.
결론적으로 우리 나라 비경구적 약물 남용자의 HCV 유전자형은 1b가 59.5%, 2a가 33.3%로 수혈이 나 원인 미상인 경우와 분포가 다르지 않았으며 감 염경로에 따라 유의한 차이가 없었다.
요 약
목적: HCV는 유전자형에 따라 임상경과, 인터페 론치료에 대한 반응이 다르며 세계적으로 지역적 분포의 차이를 보여 감염경로를 찾는 역학적 연구
464 The Korean Journal of Gastroenterology : Vol. 35, No. 4, 2000
에 유용성이 있다고 알려져 있다. 수혈로 인한 C형 간염이 크게 줄면서 비경구적 약물 남용자는 C형 간염의 주 전염경로로 대두되게 되었으며 최근 유 럽국가를 중심으로 이들 사이에서 유전자형은 수혈 이나 원인 미상의 경우와 다른 분포를 보인다는 보 고가 있다. 본 연구는 우리 나라 비경구적 약물 남 용자에서 HCV 유전자형의 분포를 알아보고자 하였 다. 대상 및 방법: HCV-RNA 양성인 만성 C형 간염 환자 74명(남녀 비; 2.7:1, 평균 연령; 40.8세)를 대상 으로 하였다. 유전자형은 혈청에서 HCV-RNA를 분 리한 후 Core 부위에 해당하는 유전자형 특이시발 체로 연쇄중합효소반응을 시행하여 검사하였다. 감 염경로에 따라 비경구적 약물 남용군, 수혈군, 기타 감염경로가 불명확한 원인 미상군으로 구분하여 비 경구적 약물 남용군에서 HCV 유전자형의 분포를 수혈군이나 원인 미상군과 비교 분석하였다. 결과:
전체 환자의 HCV 유전자형의 분포는 1b가 44명 (59.5%), 2a가 25명(33.8%), 1a가 1명(1.4%), 2b가 1 명(1.4%), 1b+2a 혼합형이 1명(1.4%), 본 방법으로 유전자형을 알 수 없었던 예가 2명(2.7%)이었고 약 물 남용군에서는 1a가 0%, 1b가 59.5%, 2a가 33.3%, 2b가 0%, 1b+2a 혼합형이 2.4%, 본 방법으 로 유전자형을 알 수 없었던 예가 4.8%로 수혈군이 나 원인 미상군과 유의한 차이를 보이지 않았으나 평균 연령은 28.9±11.7세로 다른 군에 비해 유의하 게 낮았다(p<0.05). 결론: 우리 나라 비경구적 약물 남용자의 HCV 유전자형의 분포는 1b, 2a가 대부분 으로 수혈이나 원인 미상인 경우와 분포가 다르지 않았으며 감염경로에 따라 유의한 차이가 없었다.
색인단어: HCV 유전자형, 비경구적 약물 남용자, 만성 C형 간염
참 고 문 헌
1. Major ME, Feinstone SM. The molecular virology of hepatitis C. Hepatology 1997;25:1527-1538.
2. Simmonds P, Alberti A, Alter HJ, et al. A proposed system for the nomenclature of hepatitis C viral genotypes. Hepatology 1994;19:1321-1324.
3. Simmonds P. Variability of hepatitis C virus. He- patology 1995;21:570-583.
4. van den Hoek JA, van Haastrecht HJ, Goudsmit J, de Wolf F, Coutinho RA. Prevalence, incidence, and risk factors of hepatitis C virus infection among drug users in Amsterdam. J Infect Dis 1990;
162:823-826.
5. Bolumar F, Hernandez-aguado I, Ferrer L, Ruiz I, Avino MJ, Rebagliato M. Prevalence of antibodies to hepatitis C in a population of intravenous drug users in Valencia, Spain, 1990-1992. Intern J Epid 1996;25:204-209.
6. Majid A, Holmes R, Desselberger U, Simmonds P, McKee TA. Molecular epidemiology of hepatitis C virus infection amongst intravenous drug users in rural communities. J Med Virol 1995;46:48-51.
7. Villano SA, Vlahov D, Nelson KE, Lyles CM, Cohn S, Thomas DL. Incidence and risk factors for hepatitis C among injection drug users in Bal- timore, Maryland. J Clin Microbiol 1997;35:3274- 3277.
8. Pawlotsky J-M, Tsakiris L, Roudot-Thoraval F, et al. Relationship between hepatitis C virus genotypes and sources of infection in patients with chronic hepatitis C. J Infect Dis 1995:171:1607-1610.
9. 김효석, 추동호. 우리 나라 약물남용자와 만성음주자 에서의 C형, B형 간염 바이러스 및 HIV 의 유병률.
대한내과학회지 1997;52:754-762.
10. Okamoto H, Sugiyama Y, Okada S, et al. Typing hepatitis C virus by polymerase chain reaction with type-specific primers: application to clinical surveys and tracing infectious sources. J Gen Virol 1992;
73:673-679.
11. Chayama K, Tsubota A, Arase Y, et al. Genotypic subtyping of hepatitis C virus. J Gastroenterol Hapatol 1993;8:150-156.
12. Chamot E, de Saussure P, Hirschel B, Deglon JJ, Perrin LH. Incidence of hepatitis C, hepatitis B and HIV infections among drug users in a methadone -maintenance programme. AIDS 1992;6:430-431.
13. Smyth BP, Keenan E, O’Connor JJ. Bloodborne viral infection in Irish injecting drug users. Ad-
Kim, et al. Distribution of HCV Genotypes among Intravenous Drug Users 465
diction 1998;93:1649-1656.
14. Han CJ, Lee HS, Kim HS, Choe JH, Kim CY.
Hepatitis C virus genotypes in Korea and their relationship to clinical outcome in type C chronic liver diseases. Korean J Intern Med 1997;12:21-27.
15. Lee DS, Sung YC, Whang YS. Distribution of HCV genotypes among blood donors, patients with chronic liver disease, hepatocellular carcinoma, and patients on maintenance hemodialysis in Korea. J Med Virol 1996;49:55-60.
16. 이영상, 정영화, 민영일, 문대혁, 나도선, 서동진. 한 국성인의 C형 간염바이러스 유전자형 분석-유전자형 특이 PCR법의 이용. 대한간학회지 1998;4:235-243.
17. Basaras M, Lombera N, de las Heras B, Lopez C, Arrese E, Cisterna R. Distribution of HCV geno- types in patients infected by different sources. Res Virol 1997;148:367-373.
18. Roffi L, Ricci A, Ogliari C, et al. HCV genotypes in Northern Italy: a survey of 1368 histologically proven chronic hepatitis C patients. J Hepatol 1998;
29:701-706.
19. Silini E, Bono F, Cividini A, et al. Molecular epidemiology of hepatitis C virus infection among intravenous drug users. J Hepatol 1995;22:691-695.
20. Berg T, Hopf U, Stark K, Baumgarten R, Lobeck H, Schreier E. Distribution of hepatitis C virus
genotypes in German patients with chronic hepatitis C: correlation with clinical and virological para- meters. J Hepatol 1997;26:484-491.
21. Zein NN, Rakela J, Krawitt EL, Reddy KR, Tominaga T, Persing DH. Hepatitis C virus geno- types in Unites States: epidemiology, pathogenicity, and response to interferon therapy. Ann Intern Med 1996;125:634-639.
22. Lau JYN, Davis GL, Prescott LE, et al. Distri- bution of hepatitis C virus genotypes determined by line probe assay in patients with chronic hepatitis C seen at tertiary referral centers in the United States.
Ann Intern Med 1996;124:868-876.
23. Sakugawa H, Nakasone H, Kinjo F, et al. Clinical features of patients with chronic liver disease associated with hepatitis C virus genotype 1a/I in Okinawa, Japan. J Gastroenterol Hepatol 1997;12:
176-181.
24. Lau JYN, Mizokami M, Kolberg JA, et al.
Application of six hepatitis C virus genotyping to sera from chronic hepatitis C patients in the United States. J Infect Dis 1995;171:281-289.
25. Eyster ME, Sherman KE, Goedert JJ, Katsoulidou A, Hatzakis A. Prevalence and changes in hepatitis C virus genotypes among multitransfused persons with hemophilia. J Infect Dis 1999;179:1062-1069.