접수: 2018년 6월 26일, 승인: 2019년 1월 30일 연락처: 이광정, 14051, 경기도 안양시 동안구 부림로
169 번길 30 6층 한국의약품안전관리원
Tel: (02) 2172-6713, Fax: (02) 2172-6703 E-mail: leekj@drugsafe.or.kr
Correspondence to: Kwang-Jung Lee, MD
Korea Institute of Drug Safety and Risk Management, 6th Fl., 30 Burim-ro 169beon-gil, Dongan-gu, Anyang 14051, Korea
Tel: +82-2-2172-6713, Fax: +82-2-2172-6703 E-mail: leekj@drugsafe.or.kr
한국, 일본, 대만의 의약품 부작용 피해구제 제도 현황 소개
한국의약품안전관리원
김수진ㆍ김종윤ㆍ송은혜ㆍ최문진ㆍ이광정ㆍ정수연ㆍ한순영
Introduction of Current Status of the Adverse Drug Reaction Relief System in Korea, Japan and Taiwan
Su-Jin Kim, MS, Jongyoon Kim, PharmD, Eunhae Song, ANP, Moonjin Choi, PharmD, BS, Kwang-Jung Lee, MD, Soo-Youn Chung, MD, PhD and Soon Young Han, PhD
Korea Institute of Drug Safety and Risk Management, Anyang, Korea
There has been moves to implement a novel system for the relief of injury from adverse drug reaction (ADR) in 2013 in Republic of Korea and the ADR Relief system was finally initiated in December 2014 by MFDS (Ministry of Food and Drug Safety) and KIDS (Korea Institute of Drug Safety and Risk Management). This national system is to protect victims such as the patients, manufacturers and suppliers from serious damages that can occur in spite of properly using licensed medical products. It expanded to include death, disability and serious illness cases sequentially from 2015 to 2017. Work process in KIDS is as follow. Once a claim is received, a pharmacoepidemiologic investigator reviews the case in various ways such as interview of patients and healthcare providers, visit to the hospitals or related institutions, or are also done as needed. The result of causality assessments is then reviewed by the Expert Committee. Then, the written investigation and appraisal is submitted to the ADR Deliberative Committee of MFDS, which finalizes the deci- sion for compensation. Since 2015, the funds for compensation have been collected from pharmaceutical companies.
Until December 2017, the total of 211 cases was received and 128 cases were compensated. We would introduce cur- rent state of the ADR Relief system, comparing with that of Japan and Taiwan which were operated similarly. From this we will continue to facilitate the ADR review process and actively promote the ADR Relief system in order to protect the public from unintended serious damages from drug use. (JPERM 2019;11:1-8)
Key Words: Ministry of Food and Drug Safety (MFDS); Korea Institute of Drug Safety and Risk Management (KIDS);
Adverse Drug Reaction (ADR) relief system
서 론
모든 의약품은 유익한 치료효과 이외에도 의도하지 않은 부작용이 발생할 가능성을 갖고 있다.
1)의약품 시판 전 임 상시험은 제한된 기간 및 피험자를 대상으로 실시하므로 모
든 부작용을 파악하기 어렵고, 시판 후에는 보다 대규모의,
다양한 기저질환을 가진 인구를 대상으로 긴 기간 동안 의
약품이 사용되므로 예기치 못했거나 중대한 부작용이 나타
날 수 있으며 위해성이 유익성을 상회한다면 시판을 철회하
기도 한다.
2)의약품을 정상적으로 복용하였음에도 불구하고
2
약물역학위해관리학회지 제11권 제1호, 2019위해성이 나타날 때 해당 의약품의 복용을 중단하거나 다른 의약품으로 교체하면 대부분의 경우 서서히 회복되지만, 드 물게는 중대한 부작용으로 인해 사망, 장애, 입원진료 등의 피해가 발생하는 경우가 있다. 정상적으로 제조, 처방, 투약 된 의약품 임에도 불구하고 이로 인한 부작용 피해 발생 시 보상받기 어려울 수 있다. 이와 같이 의약품 부작용으로 인 한 피해를 국가적 차원에서 구제가 필요하다는 사회적 요구 에 따라 대두된 것이 ‘의약품 부작용 피해구제 제도’이다.
‘ 의약품 부작용 피해구제 제도’란 이처럼 의약품에 본질 적으로 내재된 부작용의 위험을 사회적으로 인정하고 아주 낮은 확률로 누구에게나 발생할지 모르는 심각한 피해에 대 하여 피해자, 의약품제조자, 의료공급자 모두를 보호하는 제도이다. 외국에서는 일찍이 관련 제도를 도입해 왔는데, 일본, 대만, 뉴질랜드와 노르웨이 등 북유럽 국가가 있다.
특히 우리와 유사한 방식으로 제도를 운영하는 나라는 일본 과 대만으로, 일본은 1980년부터, 대만은 1999년부터 시행 하고 있다.
3)한국에서는 1991년 약사법에 의약품 부작용 피해구제 제 도가 최초로 명시되었고, 2012년 감기약 복용 후 스티븐스- 존슨증후군 발병 사례가 사회적으로 이슈가 되기 시작하여 의약품 부작용 피해구제 관련 약사법이 개정되었으며, 2014 년 12월 19일부터 제도가 시행되었다. 식품의약품안전처(이 하 식약처)에서는 한국의약품안전관리원(이하 의약품안전 원)에 의약품 부작용 피해구제 관련 사업을 위탁하여 운영 하고 있다. 적절한 처방·조제·투약 등 정상적인 의약품 사용 에도 불구하고 중대한 부작용으로 사망, 장애, 입원치료 등 의 피해를 입은 경우를 구제하는 무과실 보상을 원칙으로 하며 사망일시보상금, 장례비, 장애일시보상금, 진료비를 지 급하고 있다. 의약품이 정상적으로 사용되었음에도 의약품 부작용으로 인한 피해가 발생하였고, 제도 시행일자(2014.
12.19) 이후일 경우에 한해 피해구제 신청이 가능하다.
4)이 제도는 단계적으로 보상범위가 확대 시행되어, 2015년은 사 망일시보상금, 2016년은 장애일시보상금 및 장례비, 2017년 은 진료비까지 확대되었다.
본 논문은 한국에서 의약품 부작용 피해구제 제도 시행 이래 2015-2017년의 3년간의 운영 현황에 대해 소개하고자 한다. 또한 한국과 유사한 일본, 대만의 피해구제 제도 운영 현황과의 비교를 통해 한국 제도의 발전방향에 대해 살펴보 고자 한다.
한국의 의약품 부작용 피해구제 제도 운영 현황
한국은 의약품을 사용한 사람이 그 의약품의 부작용으로 인하여 질병(입원을 하거나 이와 같은 정도 이상의 상태에 해당)에 걸리거나 장애가 발생하거나 사망한 때에 피해구제
급여를 지급하고 있다.
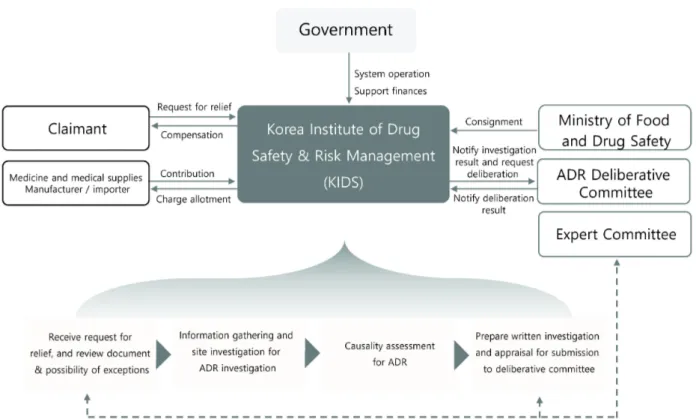
의약품 부작용에 따른 피해를 입었다면, 신청인은 의약품 안전원으로 신청서, 의사의 소견서 등을 제출해야 한다. 의 약품안전원은 신청서 접수 후 부작용 피해와 관련된 의무기 록, 문헌자료 검토, 사실관계 등을 조사하고 의약품 부작용 전문위원회의 자문 및 감정의견을 통해 식약처에 심의 안건 을 제출한다. 이러한 업무 수행을 위해 의약품안전원은 약 물역학조사관을 임용 또는 위촉할 수 있다. 식약처는 의약 품 부작용 심의위원회를 개최하고 의약품안전원에서 제출 한 심의 안건을 바탕으로 약물과 부작용간 인과관계, 피해 구제 급여 대상 여부 등에 대해 심의·의결하여 보상여부를 최종적으로 결정한다. 의약품안전원은 신청인으로부터 피 해구제 신청을 받은 날부터 90일 이내에 식약처에 심의요청 ( 의약품부작용 심의위원회)을 해야 한다. 다만, 새로운 부작 용 등의 이유로 조사 및 감정이 어려운 때에는 그 기간을 1 회에 한하여 30일까지 연장 가능하다(그림 1).
피해구제 신청 기한은 해당 진료행위 또는 장애 발생, 사 망한 날로부터 5년 이내 신청 가능하다. 신청인의 자격은 질병에 걸리거나 장애가 발생한 사람 및 의약품의 부작용으 로 인하여 사망한 사람의 유족 순이다(유족순위: 배우자>자 녀>부모>손자녀>조부모 및 형제자매).
피해구제급여에는 총 4가지가 있는데 사망일시보상금은 최저임금의 월환산액의 5년 치를, 장애일시보상금은 장애등 급에 따라 사망일시보상금의 25-100%를, 장례비보상금은 평균임금의 3개월 치를 보상한다. 진료비보상금은 질병 치 료에 소요되는 비용 중 국민건강보험법에 따른 본인부담금 중 급여비용에 해당하며, 입원 치료 등을 받은 후 본인부담 금이 30만원 이상인 경우를 지급 대상으로 한다.
의약품 부작용 심의위원회의 심의 결과 피해구제급여를 지급하기로 의결한 경우 의약품안전원은 지급 결정 통지서 를 신청인에게 보내고, 그 결정일부터 30일 이내에 신청인 에게 피해구제급여를 지급해야 한다. 약사법 제86조의3에 따라 피해구제급여의 지급제한 사유에 해당하여 지급하지 않은 때에는 신청인에게 그 사실 및 지급제한 사유를 통지 해야 한다. 이 경우 신청인이 민법이나 그 밖의 법령에 따라 배상을 받을 수 있다고 판단하는 때에는 의약품안전원은 총 리령으로 정하는 바에 따라 그 방법을 안내할 수 있다. 의약 품안전원은 심의위원회 심의 결과에 이의가 있는 경우에는 식약처에 재결정 요청이 가능한데, 이 경우 식약처에서는 중앙약사심의위원회에 자문하고, 그 결과를 의약품안전원 에 통보해야 하며, 의약품안전원은 식약처의 재결정이 있은 날부터 30일 이내에 피해구제급여를 지급해야 한다.
피해구제급여의 재원은 의약품을 제조하거나 수입한 제
약업체가 납부하는 부담금을 통해 마련된다. 부담금은 특정
공익사업과 관련하여 법률이 정하는 바에 따라 부과하는 조
Figure 1. The adverse drug reaction (ADR) relief system flow chart in Korea.
세 외의 금전지급의무의 성격으로 피해구제 부담금 납부대 상은 국내에서 의약품을 제조하거나 국내로 의약품을 수입 한 모든 제약업체가 해당되며, 매년 2회(1월, 7월) 납부하고 있다. 제도가 시행되고 3년이 된 2017년까지 납부된 부담금 은 약 140억원이며, 징수율도 100%에 가까워 모든 제약업 체가 적극적으로 참여하고 있다. 이 부담금은 전액 의약품 부작용으로 피해를 입은 피해자에게 지급하는 보상재원으 로만 활용되고 부작용의 원인조사에 필요한 인건비나 제도 운영에 소요되는 경상경비는 정부 출연금 지원으로 운영한다.
2014 년 12월 19일부터 2017년 12월 31일까지의 의약품부 작용피해구제 현황 분석결과, 총 211건 접수 중 사망 60건 (28.4%), 장례비 52건(24.6%), 장애 9건(4.3%), 진료비 90건 (42.9%) 이었는데 특히 2017년 진료비까지 확대 보상 실시한 이래 진료비 보상 신청 건이 급격히 증가하였다.
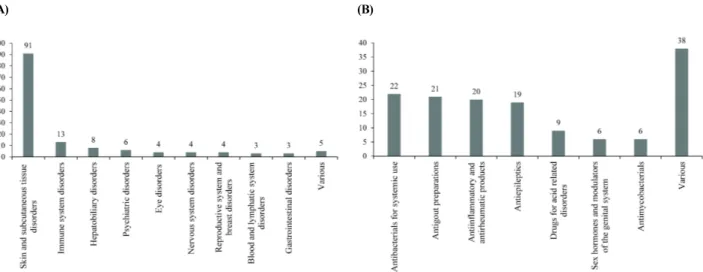
해당 기간까지 보상금이 지급된 총 128건의 분포현황을 살펴보면, 사망일시보상금 및 장례비 각각 36건(28.1%), 장 애일시보상금 6건(4.7%), 진료비 50건(39.1%)이었다. 이 중 원인 부작용과 의약품간의 조합정보 141건을 기준(다른 용 량의 동일성분 등 중복되는 정보 제거)으로, 발생된 부작용 (MedDRA SOC 분류 기준)을 질환별로 살펴보면 드레스 증 후군을 포함한 피부 및 피하조직 질환 91건(64.5%), 아나필 락시스 쇼크 등 면역계 질환 13건(9.2%), 담즙정체성 간손상 등 간담도 질환 8건(5.7%), 섬망 등 정신질환 6건(4.3%) 순
이었다. 원인 의약품(ATC 코드 3자리 기준)으로는 항생제 22 건(15.6%), 통풍치료제 21건(14.9%), 항염증 및 항류머티 즘성 약물계열 20건(14.2%), 항경련제 19건(6.4%) 등의 순이 었다(그림 2).
일본의 피해구제 제도 운영 현황
일본은 탈리도마이드로 인한 약화사고 및 위장약을 복용 한 환자 중 약 11,000명이 스몬(SMON)병에 걸려 제약회사 와 국가를 상대로 손해배상을 청구한 사건으로 인해 다른 나라에 비해 의약품 부작용 피해구제 제도가 빨리 발전했 다. 일본의 ‘의약품의료기기종합기구(PMDA: Pharmaceuticals and Medical Devices Agency, 이하 PMDA)’는 의약품의 이상 반응과 생물 유래 제품을 통한 감염 등에 의한 건강 피해에 대한 신속한 구제를 도모하기 위해 2004년 4월 1일 설립된 독립 기구로, 의약품 허가·심사, 의약품 시판 후 안전성에 대한 서비스도 제공하고 있다. PMDA의 전신인 ‘의약품 부 작용 피해구제·연구 진흥 조사기구’는 1979년 설립되어 그 이듬해 5월부터 의약품 부작용 피해구제 업무를 시작하였 다.
5)의약품(병원, 진료소에서 처방된 것 외에 약국에서 구입
한 것도 포함)을 적정하게 사용했음에도 불구하고 부작용으
로 인해 피해가 발생한 경우, 입원을 필요로 하는 정도의 질
4
약물역학위해관리학회지 제11권 제1호, 2019(A) (B)
Figure 2. Current operating status in the adverse drug reaction (ADR) relief system in Korea (2014.12.19.-2017.12.31.). (A) Distribution of ADR in the payment cases (MedDRA criteria). (B) Distribution of causative medicine in the payment cases (ATC criteria).
병에 대해 치료를 받은 경우, 일상생활이 현저히 제한되는 정도 이상의 장애가 발생한 경우 또는 사망한 경우 의약품 부작용 피해구제급여를 제공하고 있다.
5)피해구제급여를 받으려는 사람은 신청서와 필요한 서류 를 PMDA에 제출해야 하며, 피해자 본인 또는 피해자가 사 망한 경우 배우자 및 유족이 이를 대신하여 신청할 수 있다.
PMDA 는 신청 건에 대한 조사 후 후생노동성에 판정을 회 부하게 되며, 후생노동성 장관은 PMDA에서 제출한 판정 제안을 확인하고 의약품 부작용 여부, 의약품 사용의 적정 성과 같은 의학·약학적인 판단에 대해 후생노동성 산하의 약사·식품위생 심의회(부작용 감염 등 피해 판정 부회)에 의 견을 듣고 결정을 내린다. PMDA는 후생노동성으로부터 심 의 결과를 수신 후 피해자에게 통보하고 급여를 지급한다.
심의 결과에 대해 만족하지 않는 청구인은 후생노동성에 재 심의를 신청할 수 있다.
3,5)피해구제급여의 종류로는 의료비, 의료수당, 장애연금, 장 애양육연금, 유족연금, 유족일시금, 장례비가 있다. 입원을 필요로 하는 정도의 질병 치료를 받은 경우 의료비 및 의료 수당(의료비 이외의 질병 치료비용, 통원일수 및 입원일수 에 따라 설정된 월액)을 지급한다. 다만 의료비의 경우 비급 여 항목은 보상 범위에 속하지 않는데 비급여 진료에는 필 수적인 치료 이외의 특별서비스 및 고도의 선진의료를 포함 한다.
9)장애(일상생활이 현저히 제한되는 정도 이상)의 경 우, 18세 이상 성인에게 지급하는 장애연금과 18세 미만의 소아·청소년의 양육자에게 지급하는 장애양육연금이 있으 며, 장애 정도에 따라 1급과 2급으로 나누어 지급한다. 사망 한 경우, 생계유지자 사망에 따른 유족에게 연금을 지급하 는 유족연금, 생계유지자가 아닌 자의 사망에 따른 가족에
게 위로금을 지급하는 유족일시금, 그리고 장례비를 추가적 으로 지급할 수 있다.
3,5,7)의약품 부작용으로 인한 피해 보상금의 대부분은 허가 의 약품 제조·판매업체의 부담금으로 충당되고, PMDA 사무비 용의 50%는 정부의 지원금으로 충당된다. 부담금에는 기본 부담금과 추가 부담금 두 종류가 있다. 기본 부담금은 허가 의약품 제조·판매업체가 전년도 허가 의약품의 총 출하 수 량에 따라 신고·납부하여야 하는 부담금이며, 추가 부담금 은 의약품 부작용 피해구제 지급 결정된 의약품에 대해 해 당 의약품의 제조·판매업체가 추가로 신고·납부하여야 하는 부담금이다. 추가 부담금의 경우 시가에 상당하는 보상금액 합계의 25%로 계산되나 산정된 금액이 허가 의약품 제조·
판매업체의 작년도 허가 의약품의 출하액을 합한 금액의 1% 를 초과할 수 없다.
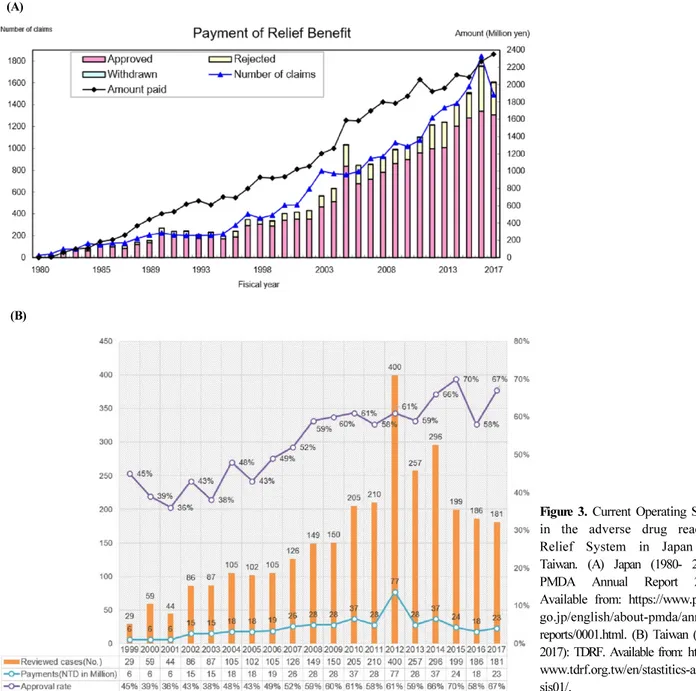
3,5)의약품 부작용 피해구제를 신청한 사례는 제도 도입 이후 꾸준히 증가하여 2003년 이후에는 한 해 700건을 훨씬 넘었 다. 2017년 기준 신청 건수는 1,491건이며 이 중 지급을 받 은 건은 1,305건(구제율 87.6%)이었다(그림 3A).
6,7)대만의 피해구제 제도 운영 현황
대만도 기본적으로 의약품의 제조·처방·조제·복용 등 전
과정에서 어느 누구의 과실도 없는 경우에만 보상을 해주는
무과실보상 방법을 채택하고 있다. 1996년에서 1997년 사이
발의 진균 감염을 치료하는데 흔히 사용되었던 2가지 약물
(terbinafine, itraconazole) 로 인한 사망 등 심각한 의약품 부
작용에 대해 언론이 많은 관심을 가지게 되었다. 그 결과 대
만의 행정원위생서(行政院衛生署)는 의약품 피해로 고통 받
(A)
(B)
Figure 3. Current Operating Status in the adverse drug reaction Relief System in Japan and Taiwan. (A) Japan (1980- 2017):
PMDA Annual Report 2016.
Available from: https://www.pmda.
go.jp/english/about-pmda/annual- reports/0001.html. (B) Taiwan (1999- 2017): TDRF. Available from: https://
www.tdrf.org.tw/en/stastitics-analy- sis01/.
는 피해자들의 고통과 분노를 적시에 해결하기 위해 무과실 보상 프로그램을 시작하였다. 이 구제 프로그램은 2000년에 입법되어 약해구제법으로 제정되었고, 정부에 의해 ‘재단법 인약해구제기금회(TDRF: Taiwan Drug Relief Foundation, 이 하 TDRF)’가 설립되어 약해구제 업무와 관련 분야의 연구 조사 업무를 수행하고 있다.
3,5)대만의 의약품 부작용 피해구제 제도는 합법적 약물의 정 당한 사용으로 사망, 장애, 중증질환이 발생한 경우 의약품 부작용 피해구제급여를 제공하고 있다. 약해구제법 제3조 용어의 정의에 따르면, ‘합법적 약물’은 행정원위생서가 발 급한 약물 허가증이 있는 제조·수입·판매 의약품을 말하며,
‘ 정당한 사용’은 의약 전문가 또는 약물 라벨의 지시에 따
른 사용을 말한다. 또한 ‘부작용(Adverse reaction)’은 약물의 복용으로 인한 유해한 반응을 의미하고, ‘장애’는 심신장애 자보호법령이 정한 장애 종류와 등급에 부합하는 것을 말하 며, 심리적인 요소로 인한 장애는 포함하지 않는다. ‘중증질 환’은 약물 부작용으로 입원이 필요한 경우나 입원을 연장 해야 하는 경우, 영구적인 손상을 방지하기 위해 필수적인 개입이 필요한 경우를 말한다.
1,2)특히, 2011년 5월 4일 약해구제법 개정 전까지는 모든 허
가사용 외(off-label) 약물 사용이 보상에서 제외 되었으나
개정 이후에는 위원회에서 판단하여 허가사용 외 약물 사용
이더라도 의약품 사용 당시의 의료 및 치료원칙을 준수한
경우에는 보상을 해주는 것으로 변경되었다.
3,5)6
약물역학위해관리학회지 제11권 제1호, 2019우리나라 일본 대만
운영 주체 한국의약품안전관리원
(Korea Institute of Drug Safety &
Risk Management, KIDS)
의약품의료기기종합기구 (Pharmaceuticals and Medical Devices Agency, PMDA)
재단법인약해구제기금회
(Taiwan Drug Relief Foundation, TDRF)
제도 시행
2014 년 12월 19일 이후 1980 년 5월
의약품부작용피해구제·연구진흥 조사기구에서 피해구제 업무를 시작
1998 년 의약품 피해 무과실 보상 프로그램으로 시작
피해 구제 대상
의약품을 사용한 사람이 그 의약품의 부작용으로 인하여 질병(입원을 하거나 이와 같은 정도 이상의 상태에 해당)에 걸리거나 장애가 발생하거나 사망한 경우 피해구제급여를 지급
의약품을 적정하게 사용했음에도 불구하고 발생한 부작용으로 인해 질병(입원치료를 필요로 하는 정도), 장애(일상생활이 현저히 제한되는 정도 이상), 사망한 경우
합법적 의약품의 정당한 사용으로 사망, 장애, 중증질환이 발생한 경우
* 장애: 신심장애자보호법령이 정한 장애 종류와 등급에 부합하는 경우로 심리적인 장애는 포함하지 않음
* 중증질환: 입원이 필요하거나 연장해야하는 경우, 영구적인 손상을 방지하기 위해 필수적인 개입이 필요한 경우
급여 종류 ① 사망일시보상금
- 최저임금의 월환산액의 5년치에 해당하는 금액
② 장애일시보상금
- 장애등급(1-4급) 기준에 따라 사망일시보상금의 25-100%에 해당하는 금액
③ 진료비
- 국민건강보험법에 따른 요양급여 비용 중 본인부담금에 해당하는 금액
④ 장례비
- 평균임금의 3개월치에 해당하는 금액
① 사망 관련
- 유족연금: 생계유지자 사망에 따른 유족에게 연금 지급 - 유족일시금: 생계유지자가 아닌
자의 사망에 따른 가족에게 위로금 지급
- 장례비
② 장애 관련
- 장애등급(1-2급) 기준에 따라 지급
- 장애연금(18세 이상) - 장애양육연금(18세 미만)
③ 질병 관련
- 의료비: 질병 치료와 관련된 의료비
- 의료수당: 의료비 이외의 질병 치료비용, 통원일수 및 입원일수에 따라 설정된 월액
① 사망지급
- 최대 200만 신대만달러
② 장애지급
- 심신장애등급에 따라 최대 200 만 신대만달러
③ 중증질환지급 - 대만국민건강보험
중증상해질병범위에 해당하는 질환
- 의료기관에서 사용한 의료비용으로 정식 영수증 필요하며 최대 60만 신대만달러
※ 보상금액은 피해구제 지급점수에 따라 차등 지급
보상금
재원 의약품의 제조업자·품목허가를 받은 자 및 수입자가 납부하는 부담금(기본 부담금, 추가 부담금)
의약품 제조·판매업체가 납부하는 부담금(기본 부담금, 추가 부담금)
의약품 제조·수입업체가 납부하는 부담금(기본 부담금, 추가 부담금)
* 심의위원회 심의 결과에 의거하여 2011년부터 추가 부담금 징수하지 않고 있음 Table 1. The Comparison with the adverse drug reaction relief system in Korea, Japan and Taiwan
피해구제급여 신청인은 신청서와 필요한 서류를 TDRF 홈페이지 및 우편을 통해 제출할 수 있으며, 피해자의 법정 대리인 또는 피해자 사망 시 피해자의 상속인이 이를 대신 하여 신청할 수 있다. 신청에 따라 TDRF는 피해자의 의무 기록 등을 조사하여 자료를 수집하고 전문가 의견을 첨부하 여 위원회에 제출한다. 위원회에서 심의하고 심의 결과는 최종적으로 행정원위생서가 확인 및 결정을 한 후 TDRF로
결과를 송부한다. 만일 피해구제 신청자나 제조·수입업체가 결정을 받아들일 수 없다면 약해구제법에 의거 행정소송을 제기할 수 있다.
3,5)피해구제급여의 종류로는 ‘사망지급’, ‘장애지급’, ‘중증질
환지급’ 세 가지로 분류되며, 최고 지급액이 각각 200만,
200 만, 60만 신대만달러이다. 보상금액은 차등적으로 지급
되는데, 의약품으로 인한 피해 외에 다른 요인(연령, 기저질
환, 인과관계 개연성 등)의 기여도를 고려한다.
3,5)의약품 부작용으로 인한 피해 보상금은 의약품 제조·수입 업체가 납부하는 부담금으로 운영되며, 약사법 상 기본 부 담금과 추가 부담금이 명시되어 있으나 심의위원회 심의 결 과에 의거하여 2011년부터 추가 부담금을 징수하지 않고 있 다. 허가된 모든 의약품 제조·수입업체는 연 판매액의 일정 비율로 부담금을 납부해야할 의무가 있다.
3,5)의약품 부작용 피해구제를 신청한 사례는 2004년 이후에 는 한 해 100건 이상 신청되고 있다. 2017년 기준 심의 건수 는 181건이며 지급률은 67%이다(그림 3B).
8)고찰 및 결론
의약품 부작용 피해구제 제도가 한국에 도입되기 이전에 는 부작용 피해를 입은 피해자가 직접 개별소송을 진행해 부작용 인과관계를 입증해야 하는 어려움이 있었고, 장기간 소요되었다. 그러나, 이 제도를 도입함으로서 약 4-5개월 이 내에 국가가 피해보상을 하여 피해자의 소송 비용 및 노력 을 경감시켜주고, 특히 신청 등의 절차를 간소화하는 등 그 도입에 의의가 있다.
한국은 이 제도의 운영 3년차를 맞이하여 진료비 보상 확 대 실시와 함께 접수 건수가 20건에서 211건으로 급격히 증 가하였다. 연도별 보상범위의 단계적 확대 실시에 따른 영 향이 일부 있을 수 있으나, 일본과 대만의 제도 도입 초기 5 년 이내 급격한 접수 건 상승을 참고해볼 때 한국도 앞으로 지속적인 접수 증가가 예상된다. 2014년 12월 19일 의약품 부작용 피해구제 제도 도입 이래 의약품안전원은 제도를 안 정적으로 정착시키기 위해 이에 필요한 각종 세부 기준을 마련하고, 부작용 인과성 평가 체계를 도입하였으며 인력 양성에 주력해 왔다. 2017년 이후부터는 피해구제급여 대상 에 사망일시보상금 및 장례비, 장애일시보상금에 이어 진료 비까지 포함되었으므로 그 간의 추진 현황을 살펴보고 문제 점 및 개선사항을 발굴하여 제도 운영을 보다 정교화 할 필 요가 있다.
일본과 대만의 제도 운영 사례를 살펴보면 피해구제급여 세부 운영 기준, 보상금 재원 마련, 운영비 활용, 보상 범위 등에 있어 한국의 제도 운영과의 차이점을 확인할 수 있었 다(표 1). 피해구제급여 세부 운영 기준에서는 일본은 사망 의 경우 유족연금 외에도 위로금 성격의 유족일시금을 지급 하고 있고, 장애의 경우 장애등급 기준에 따른 보상 외에도 나이에 따라 장애양육연금도 지급하고 있다. 질병의 경우 의료비 외에도 의료수당을 지급하고 있다. 일본과 한국은 비급여의 경우 보상하지 않고 있지만 양 국가의 의료보장 구조가 상이하여 세부 내용에서는 차이가 난다. 한국은 전 국민이 건강보험에 가입되어 있으나 일본에 비하여 의료보
험의 보장성이 낮고, 총의료비 대비 민간지출 비율과 본인 부담률이 높은 특징이 있다.
9)대만은 한국과 마찬가지로 보 상금을 일시에 지급하고 있는데 지급 상한치가 있고 피해구 제 지급점수에 따라 보상금을 차등지급하는 특징이 있다.
또한 대만의 구제대상 중 진료비의 경우 일본과 한국의 경 우와 달리 ‘중증질환’을 정의하고 있다. 여기에는 행정원위 생서가 전민건강보험 중대상병범위와 약물불량반응통보규 정에 의거 공고한 질병이 해당된다. 다만 약물 부작용으로 입원이 필요한 경우나 연장해야 하는 경우, 영구적인 손상 을 방지하기 위해 필수적입 개입이 필요한 경우를 말한다.
5)세 국가 모두 의약품 제조·수입업체가 납부하는 부담금으로 운영하고 있는데, 일본은 일부 비용을 사업 운영비로 활용 하고 있으며 대만은 2011년부터 추가 부담금을 징수하지 않 고 있다. 또한 대만의 경우 허가사용 외 약물 사용이더라도 현재의 의료 및 치료원칙을 준수한 경우에는 보상을 해주고 있다. 국가마다 제도에 대한 인식과 보건의료체계가 상이하 므로 차이점을 바로 도입하기는 어려울 수도 있으나, 한국 의 제도 운영상 보다 합리적이고 제도 운영 취지에 적합하 도록 이를 참고해볼 만하겠다.
이미 오래전부터 이 제도를 시행하고 있는 일본과 대만의 피해구제 실적을 비교할 때 한국의 실적은 아직 미미한 수 준이다. 이는 제도에 대한 국민의 인식이 낮아 피해구제 신 청이 적은 탓으로 생각되며 이에 대한 적극적인 홍보가 필 요하다. 의약품 부작용 피해구제 제도는 의도하지 않은 피 해를 입은 피해자를 보호하자는 사회적 연대의식에서 출발 하였기에 이 제도가 피해자, 제약업체, 의료기관 모두를 보 호하는 선의의 제도로 정착될 수 있도록 많은 관심과 지원 이 필요하다. 특히 제도를 몰라서 이용하지 못하는 국민이 없도록 대국민 홍보에 필요한 예산 확보노력은 물론이고, 의료기관 및 유관기관의 적극적인 협조가 뒤따라야 한다.
특히 의약품 부작용 피해를 미연에 방지하기 위하여 보건의 료인 및 일반인을 대상으로 지급사례에 대한 적극적인 공개 및 교육이 필요하다. 아울러, 의약품 부작용 피해구제 제도 가 유용한 사회안전망으로 자리매김하기 위해서는 의약품 부작용 피해를 전문적으로 조사할 수 있는 약물역학조사관 의 인력 육성과 보강이 필요하다.
REFERENCES