갑상선암의 방사성옥소 치료 성적
국민건강보험 일산병원 핵의학과
김선정
Clinical Outcome of Postoperative Radioiodine Therapy in Patients with Differentiated Thyroid Cancer
Sun Jung Kim
Department of Nuclear Medicine, National Health Insurance Service Ilsan Hospital, Goyang, Korea
Background: Postoperative radioiodine (RAI) therapy has been widely used for patients with differentiated thyroid cancer. The purpose of this study is to evaluate clinical outcome of patients with postoperative RAI therapy.
Methods: We reviewed retrospectively 625 differentiated thyroid cancer (DTC) patients, who underwent total thyroidectomy and postoperative high-dose RAI therapy in Ilsan Hospital from 2004 to 2014. Recurrence was defined as the reappearance of disease after RAI therapy, which was confirmed by cytologically or pathologically proven malignant tissue. Various factors including age, TSH-stimulated thyroglobulin (sTg) at RAI therapy (pre-ablative sTg), stage, American thyroid association (ATA) risk classifi- cation, reclassification by response to therapy were analyzed.
Results: Recurrence occurred in 22 of 625 patients (3.5%). There was no significant difference in age, sex, stage, ATA risk between recurred patients and remaining patients. However, pre-ablative sTg was significantly higher in recurred patients and reclassification by response to therapy was significantly different; recurred patients were more likely to have biochemical/structural incomplete response. Clinical status at final follow-up showed no evidence of disease (NED) in 82%, persistent structural disease in 2% and persistent biochemical evidence in 16%.
Conclusion: Pre-ablative sTg and reclassification system by response to therapy could be useful to predict the risk of recurrence and persistent disease.
Key Words: Thyroid neoplasms; Iodine radioisotopes; Local neoplasm recurrence; Thyroglobulin
책임저자 : 김선정
10444 경기도 고양시 일산동구 일산로 100 국민건강보험 일산병원 핵의학과 전화 : (031)900-0810, 팩스 : (031)900-0826 E-mail : sunjk32@nhimc.or.kr
*본 연구는 국민건강보험 일산병원의 연구비 지원으로 이루어졌음 (임의연 2015-36).
서 론
갑상선암은 2009년 이후 한국에서 가장 많이 발생하는 암 이 되었고, 근래의 폭발적인 증가율에 대한 원인이 뚜렷하게 밝혀지지는 않았지만 임상적인 특성은 변화된 모습을 보인 다. 즉 분화된 갑상선암이 94%에 이르며, 초음파 및 세침 흡 입 생검 등의 진단기술 향상에 힘입어 크기가 작은 암, 혹은
저위험군의 암이 상대적으로 많은 부분을 차지하게 되었다1-3. 갑상선분화암은 갑상선 절제술과 방사성옥소 치료 및 갑상선 호르몬 억제 요법 등의 치료법들이 확립되어 있으며, 방사성 옥소 치료는 정상 잔여 갑상선 조직을 완전히 제거함으로 재발 병소의 발견을 용이하게 하고, 국소 재발률을 낮추며, 특히 고위험군 환자에서는 지속적으로 남아있는 병을 치료함으로 무병 생존율과 질병 관련 생존율을 높이는 것으로 갑상선암 치료에 널리 이용되어 왔다4,5. 그러나 2009년 미국갑상선학회 (American thyroid cancer association, ATA) 가이드라인 발표 이후 방사성옥소 치료에 많은 변화가 있었다. 즉, 저위험군 환자에서는 방사성옥소 치료가 권고되지 않으며 중위험군에 서도 선택적으로 권고되어지고, 고용량보다는 저용량 치료로 대치하려는 경향이다2.
본원에서는 갑상선분화암으로 갑상선전절제술을 받은 환
자는 대부분 입원하여 고용량 치료를 시행하였기에 지금까지 본원에서 시행하였던 방사성옥소 치료에 대한 결과를 정리하 고 고찰해 보고자 한다.
대상 및 방법
1. 연구대상2004년 6월부터 2014년 12월까지 일산병원에서 갑상선분 화암으로 갑상선전절제술을 시행하고 고용량의 방사성옥소 치료를 받았던 625명의 환자들을 후향적으로 분석하였다. 연 구대상에 포함되는 기준은 (1) 분화암, 유두암(Papillary thy- roid cancer, PTC), 유두암의 여포변종(Follicular variant PTC), 여포암(Follicular thyroid cancer, FTC)이고, (2) 갑상선전절제 술과 중심/경부 임파절 절제술을 받은 후 고용량의 방사성 옥소 치료를 받은 환자이며, (3) 2015년 6월까지 지속적으로 추적 관찰이 가능하였던 경우이다.
2. 방사성옥소 치료와 추적관찰
방사성옥소 치료 전에 환자들은 최소 3주 이상 갑상선 호 르몬을 중단하고 2주 동안 저요오드 식이를 하였다. 타이로젠 을 주사한 경우에는 갑상선 호르몬의 중단 없이 저요오드 식 이를 하였다. 갑상선자극 호르몬(TSH)이 30 mIU/L 이상으로 증가된 경우에 방사성옥소를 투여하였으며 투여 용량은 다음 과 같다. (1) 갑상선암이 갑상선 내에 국한되어 있는 경우는 80 mCi 혹은 100 mCi, (2) 갑상선의 주변으로 침윤이 있거나 임파절 전이가 있는 경우는 150 mCi, (3) 이미 원격전이가 발견된 경우는 180 mCi 혹은 200 mCi를 투여하였다. 방사성 옥소 투여 후 3일과 7일(~10일)에 이중-헤드(dual-head) 감마 카메라를 이용하여 전신 영상을 얻었다. 방사성옥소 치료가 끝나고 다시 갑상선 호르몬을 복용하였으며, 정기적으로 내원 하여 갑상선 글로블린(thyroglobulin, Tg)과 갑상선 글로블린 항체(anti-thyroglobulin antibody), 경부초음파를 시행하였다.
갑상선 글로블린은 TSH-억제 갑상선 글로블린(TSH-suppre- ssed Tg, supTg) 혹은 TSH-자극 갑상선 글로블린(TSH-sti- mulating Tg, sTg)을 얻었으며, TSH-자극은 일부에서 타이로젠® (thyrotropin alpha, Genzyme)을 주사하는 방법을 사용하였다.
추적 관찰하면서 세포병리학적 또는 조직학적으로 다시 갑상선암이 확인된 경우 재발 부위를 수술하고 경우에 따라 추가적으로 방사성옥소 치료를 시행하였다. I-131 (혹은 123) 방사성옥소 진단 스캔(I-131 or I-123 diagnostic whole body scintigraphy, dxWBS)에서 잔존 갑상선조직이 남아있거나 다
른 부위에 잔존/재발 병소가 의심되는 경우, 구조적 질병의 근거는 없지만 Tg가 지속적으로 상승하는 경우에는 추가적 으로 방사성옥소 치료를 시행하였다.
3. 위험도, 초기 치료 반응 평가
환자들은 AJCC/UICC 병기 체계(7판)와 2009년 ATA에서 제시된 재발위험도에 따라 환자를 분류하였다.
갑상선전절제술과 방사성옥소 치료에 대한 초기 평가는 방사성옥소 치료가 끝나고 1년여(9개월-15개월)가 경과한 시 점에서 2015 ATA 가이드라인에서 제안된 치료 반응 평가 체계를 사용하였다. (1) 완전 반응(excellent response)은 임상 적, 생화학적(갑상선 글로블린 항체가 검출되지 않는 상태에 서 supTg <0.2 ng/mL 혹은 sTg <1 ng/mL), 구조적인 질병의 근거가 없는 경우, (2) 불명확 반응(indeterminate response)은 비특이적 생화학적 소견(supTg가 0.2 ng/mL 이상 - 1 ng/mL 미만이거나 sTg가 1 ng/mL 이상 - 10 ng/mL 미만), 영상 검사 에서 양성이나 악성으로 확실하게 분류할 수 없는 경우, 명백 한 구조적 질병의 근거가 없이 안정적이거나 감소하는 갑상 선 글로블린 항체를 갖는 경우, (3) 생화학적 불완전 반응 (biochemical incomplete response)은 구조적 질병의 근거가 없이 supTg가 1 ng/mL 이상이거나 sTg가 10 ng/mL 이상인 경우, 혹은 갑상선 글로블린 항체 수치가 상승하는 경우, (4) 구조적 불완전 반응(structural incomplete response)은 Tg 수 치와 관계없이 국소성 병변 또는 원격 전이가 지속되거나 새 로 생긴 경우이다.
4. 재발 및 최종 임상 상태의 평가
추적관찰 중 새롭게 세포병리 혹은 조직학적으로 갑상선 암이 확인된 경우를 재발(structural disease recurrence)이라고 정의하였다. 최종 임상 상태는 추적기간 동안의 재발여부와 상관없이 마지막 추적시점의 상태로서 다음과 같이 정하였 다. 갑상선 글로블린 항체가 검출되지 않는 상태에서 supTg 가 1 ng/mL 미만이며, 구조적 질병이 없는 경우를 무병(no evi- dence of disease, NED), 병리적으로 확인되거나 영상검 사에서 구조적 질병의 근거는 없지만 supTg ≥1 ng/mL, 혹은 sTg ≥2 ng/mL인 경우는 생화학적 잔존암(biochemical persis- tent disease), Tg의 수치와 상관없이 영상 검사에서 갑상선암 이 강력하게 의심되는 갑상선 부위 결절(thyroid bed nodule), 임파절 종대, 원격전이가 있으면 구조적 잔존암(structural per- sistent disease)으로 하였다.
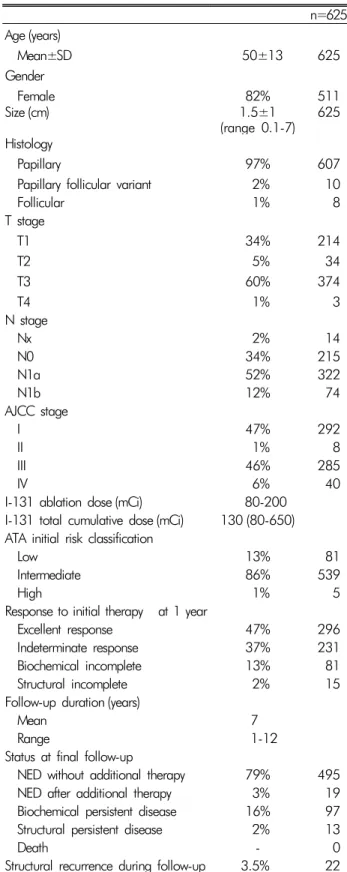
Table 1. Patient characteristics
n=625 Age (years)
Mean±SD 50±13 625
Gender
Female 82% 511
Size (cm) 1.5±1
(range 0.1-7) 625 Histology
Papillary 97% 607
Papillary follicular variant 2% 10
Follicular 1% 8
T stage
T1 34% 214
T2 5% 34
T3 60% 374
T4 1% 3
N stage
Nx 2% 14
N0 34% 215
N1a 52% 322
N1b 12% 74
AJCC stage
I 47% 292
II 1% 8
III 46% 285
IV 6% 40
I-131 ablation dose (mCi) 80-200 I-131 total cumulative dose (mCi) 130 (80-650) ATA initial risk classification
Low 13% 81
Intermediate 86% 539
High 1% 5
Response to initial therapy at 1 year
Excellent response 47% 296
Indeterminate response 37% 231
Biochemical incomplete 13% 81
Structural incomplete 2% 15
Follow-up duration (years)
Mean 7
Range 1-12
Status at final follow-up
NED without additional therapy 79% 495
NED after additional therapy 3% 19
Biochemical persistent disease 16% 97 Structural persistent disease 2% 13
Death - 0
Structural recurrence during follow-up 3.5% 22 AJCC, American joint cancer committee; ATA, American thy- roid association; NED, No evidence of disease; UICC, Union internationale contre le cancer.
5. 임상혈액 검사
2004년부터 2012년 2월까지는 Immulite Anti-Tg/Immulite Tg Kit (Immulite 2000, Siemens Healthineers, Erlangen, Ger- many)를 이용하여 Tg와 갑상선 글로블린 항체를 측정하였으 며, 각각의 민감도는 0.2 ng/mL와 20 IU/mL이었다. 2012년 3월 이후로는 Elecsys Anti-Tg/Elecsys Tg II (Cobas e 411/601/
602 immunoassay analyzer, Roche Diagnostics GmbH, Mann- heim, Germany)를 이용하였으며, Tg와 갑상선 글로블린 항체 의 민감도는 각각 0.04 ng/mL, 10 IU/mL이었다.
6. 통계 분석
분석 자료들은 평균값과 표준편차로 나타냈으며, 재발이 되었던 군과 재발이 되지 않았던 군 사이의 분석은 SPSS version 23을 사용하여 Fischer’s 정확 검정과 independent t-test로 하였으며, p값이 0.05 미만인 경우 통계학적으로 유 의한 차이가 있다고 평가하였다.
결 과
이 연구에 포함된 625명의 임상 소견 및 위험도, 치료 결과 는 Table 1에 요약하였다. 나이는 50±13세이며, 여자가 511 명(82%)이었고, 평균 추적 관찰 기간은 7년(1년 4개월-12년) 이었다. 대부분(97%)이 유두암이었고, 여포변형 유두암이 2%, 여포암 1%이었다. AJCC/UICC 병기는 I이 47%로 가장 많았 고, III (46%), IV (6%) 순이었다. ATA 재발위험도는 중간위 험군(86%)이 대부분이었고, 저위험군(13%), 고위험군(1%) 의 순이었다. 초기치료에 대한 반응은 623명에서 평가를 하 였는데, 완전 반응은 47%였고, 불명확 반응은 37%로 84%에 서 우수한 반응을 보였다. 생화학적 불완전 반응은 13%, 구조 적 불완전 반응은 2%였다.
갑상선암과 관련한 사망이나 이환율은 없었으며, 마지막 추적 관찰 때에 최종 임상 상태는 82%에서 무병이었고, 16%
는 생화학적 잔존암, 2%는 구조적 잔존암이었다. 초기치료 후 추적기간 중 재발이 확인되어 재수술을 받은 환자는 22명 (3.5%)이었다. 이들은 1-2회의 재수술을 받았으며, 경우에 따 라 1-3회의 추가적 방사성옥소 치료를 받았다. 22명 중 1명은 허벅지 근육의 원격전이로 수술하고 이후에 폐의 원격전이가 발견되었으며, 다른 1명은 기관지의 국소재발로 수술하고 후 에 폐전이가 발견되었다. 나머지 20명(22병소)은 국소재발로 임파절(20병소) 재발이 대부분이었으며, 갑상선 부위(1병소), 갑상선 수술부위 주변의 경피하조직(1병소)에 재발이 확인되
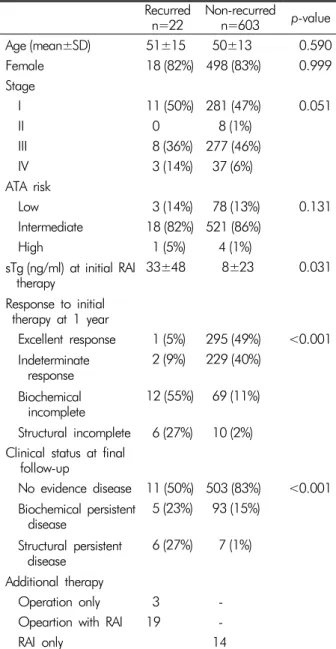
Table 2. Clinical findings between the recurred and the non-re- curred patients
Recurred
n=22 Non-recurred
n=603 p-value
Age (mean±SD) 51±15 50±13 0.590
Female 18 (82%) 498 (83%) 0.999
Stage
I 11 (50%) 281 (47%) 0.051
II 0 8 (1%)
III 8 (36%) 277 (46%)
IV 3 (14%) 37 (6%)
ATA risk
Low 3 (14%) 78 (13%) 0.131
Intermediate 18 (82%) 521 (86%) High 1 (5%) 4 (1%) sTg (ng/ml) at initial RAI
therapy 33±48 8±23 0.031
Response to initial therapy at 1 year
Excellent response 1 (5%) 295 (49%) <0.001 Indeterminate
response 2 (9%) 229 (40%) Biochemical
incomplete 12 (55%) 69 (11%) Structural incomplete 6 (27%) 10 (2%) Clinical status at final
follow-up
No evidence disease 11 (50%) 503 (83%) <0.001 Biochemical persistent
disease 5 (23%) 93 (15%) Structural persistent
disease 6 (27%) 7 (1%) Additional therapy
Operation only 3 -
Opeartion with RAI 19 -
RAI only 14
ATA, American thyroid association; sTg, TSH-stimulated thyro- globulin; RAI, Radioactive iodine
었다. 초기치료 후 평균 3년 5개월(8개월-6년 8개월) 뒤에 재발이 발견되었고, 2명의 환자에서는 첫번째 재발 후 평균 4년 1개월 뒤에 다시 재발이 확인되었다. 이 환자들에서 마지 막 추적 때의 임상 상태는 무병이 11명(50%), 생화학적 잔존 암이 5명(23%), 구조적 잔존암이 6명(27%)이었다.
재발이 없었던 603명 중에서 14명이 15회의 추가적 방사성 옥소 치료를 하였는데, 초기치료 1년 후 시행한 I-131 dxWBS 에서 갑상선 부위 및 다른 부위에 방사능 섭취가 남아있거나 (6명), 구조적 질병의 근거는 없지만 Tg가 지속적으로 상승하
여(1명), 초기치료 시에 이미 폐전이가 있었거나(4명), 추적 영상검사에서 폐전이로 생각되는 병변이 생겨서(2명), 위의 2가지 이상의 이유(1명) 등이었다. 마지막 추적 시의 임상 상 태는 무병이 83%, 생화학적 잔존암이 15%, 구조적 잔존암이 1%였다.
재발이 있었던 군과 없었던 군 사이에 나이 45세 이하의 비율, 성별, 병기, ATA 재발 위험도의 유의한 차이는 없었으 나 방사성옥소 치료 직전에 검사한 sTg 수치(pre-ablative sTg) 와 초기치료 반응에서는 유의한 차이가 관찰되었다(Table 2).
재발군에서 pre-ablative sTg는 33±48 ng/mL로 재발이 없는 군의 8±23 ng/mL보다 높았다. 초기치료 반응은 재발군의 82%에서 생화학적/구조적 불완전 반응을 보였고 재발이 없었 던 군의 87%에서 완전/불명확 반응을 보였다.
고 찰
갑상선분화암은 진행이 매우 느리고 암으로 인한 사망률 이 낮으므로 임상 경과를 논할 때 10년 이상의 장기 추적 결과를 가지고 분석하는 것이 타당하며, 표준적인 치료를 하 였을 때 완치율은 80% 이상으로 알려져 있지만6,7, 치료방법 이나 완치 판정 기준 등에 따라 다를 수 있다. 본 연구는 갑상 선분화암으로 갑상선전절제술 및 방사성옥소 치료를 시행 받 은 환자를 대상으로 하였고, 마지막 추적 때의 최종 임상상태 는 82%에서 무병, 16%에서 생화학적 잔존암, 2%에서 구조 적 잔존암을 보였으며, 추적관찰 동안 3.5%에서 재발을 보였 다. 본 연구의 평균 추적 기간은 7년으로 임상 경과를 논하기 에는 충분하지 않지만, 마지막 추적 때 82%의 환자에서 무병 상태를 보인 점은 기존 연구들에 부합할 가능성이 높다고 볼 수 있다.
본 연구에서는 갑상선전제술과 방사성옥소 치료 후 추적 관찰 동안에 세포학적/조직학적으로 갑상선암이 확인되어 재 수술을 받았던 경우를 재발이라고 정의하였고, 재발되었던 22명 중에서 18명은 생화학적 잔존암이 지속되던 상태에서 구조적 갑상선암으로 발현된 것이기에 엄밀한 의미에서는 잔 존암이라고 할 수 있겠다. 추적관찰 동안 어느 시점에 무병 상태가 성취되었다가 그 이후에 새롭게 생긴 생화학적 혹은 구조적 질병 상태를 재발로 정의한 Tuttle 등8의 관점을 적용 한다면 위의 18명을 뺀 나머지 4명과 마지막 추적 때에 새롭 게 생화학적 이상 소견만 발견된 2명을 합하여 총 6명(1%)이 재발된 것이고 그들의 결과와 유사하다. 그러나 현실적으로 Tuttle 등8의 정의를 도입하여 적용할 필요가 있을 것인가는 의문이다.
재발이 있었던 22명과 없었던 602명간의 임상 특성을 살 펴본 결과 나이, 성별, 병기, ATA 재발 위험도는 두 군 사이에 유의한 차이가 없었다. ATA 재발 위험도는 2009년 ATA에서 제안된 기준에 근거하였는데, 기존의 가이드라인에 포함되지 않았던 예후 인자들(임파절 침범 정도, 유전자 변이 여부, 여 포암에서 혈관 침범 정도 등)이 2015년에 추가되었지만9, 2014년 이전의 환자들은 대부분 위의 인자들에 대하여 확인이 어려워 2009년도 기준을 따랐으며, 향후 이런 인자들을 포함 한 재발 위험도에 대하여 전향적인 연구가 필요할 것이다.
추적관찰 동안 임상적, 생화학적, 영상학적(구조적/기능 적), 세포병리학적 검사 결과를 토대로 임상상태 및 치료에 대한 반응을 평가하게 되는데, Tuttle 등8은 위의 결과를 토대 로 초기치료에 대한 반응 정도를 평가하여 환자의 위험도를 재분류하는 체계를 제안하였다. 초기치료 후 첫 2년 기간에 가장 좋은 반응을 기술하도록 하였으나 최근에는 추적관찰 중 어느 시점에서도 사용할 수 있다9. 방사성옥소 치료 후 잔여 갑상선이나 잔존암이 제거되었는지를 알아보기 위하여 대부분 치료 1년여 시점에 I-131 (or 123) dxWBS를 시행하는 데 환자들이 dxWBS를 시행하기 위하여 갑상선 호르몬을 중 단하고 저요오드 식이를 해야 하는 고통을 감수하는 것보다 득이 있는지에 대하여 논란이 있다10. 뿐만 아니라, dxWBS를 통하여 잔여 갑상선 제거가 완전하게 되었는지는 알 수 있지 만, 완전한 제거 자체가 환자의 sTg 수치나 예후를 반영하는 것은 아니어서11,12 초기치료 1년 뒤의 dxWBS 소견을 반영하 여 평가하는 방사성옥소 치료 성공률(ablation success rate)은 큰 의미가 없다고 판단된다. 본 연구에서는 방사성옥소 치료 성공률에 대한 평가는 시행하지 않았으며, 앞서 언급한 Tuttle 등8의 평가체계를 사용하여 초기치료 평가를 하였고, 갑상선 전절제술과 방사성옥소 치료를 시행한 환자들에서는 유용한 초기평가 방법이라고 생각된다. 재발이 있었던 군에서 없었 던 군보다 생화학적 불완전반응과 구조적 불완전 반응이 유 의하게 높았고 완전/불명확 반응은 매우 낮았다. 수술 후 ATA 중간위험군으로 분류되었던 환자에서 완전반응을 보이는 2/3 의 환자는 잔존암/재발의 빈도가 1-2%로, 기존 분류에 의해 예측된 36-43%의 잔존암/재발보다 현저하게 낮아지는 것으 로 보고되고 있다. 따라서 치료에 대한 반응 평가 체계를 적극 적으로 활용하여 재발에 대한 초기 위험도를 재분류하고 향 후의 감시절차와 추가적인 치료 계획을 세워야 할 것이다.
본 연구에서 수술 후 방사성옥소 치료 때에 측정한 sTg 수치는 재발 군에서 재발하지 않은 군에 비하여 유의하게 높 았으며, sTg가 1-2 mg/mL 이상이면 재발의 위험이 높고13, 다
변량분석에서도 갑상선암의 잔존/재발의 독립적인 예측 인자 로 알려진 것과도 부합하는 결과이다14. Nascimento 등15은 수술 후 초음파에서 관찰되는 잔존암의 증거가 없는 상태에 서 sTg 수치가 측정 범위 이하라면 임파절 전이가 없고 공격 적인 세포형이 아닌 경우에 방사성옥소 치료를 하지 않을 것 을 제안하였지만, 지금까지 방사성옥소 치료를 결정지을 수 있는 기준치는 없는 상태이므로 이에 대한 연구가 이루어져 야 할 것이다.
마지막 추적관찰에서의 임상상태는 재발이 없던 군에서 83%가 무병 상태인 것에 비하여 재발 군에서는 50%가 무병 이었고, 27%에서 구조적 잔존암 상태였다. 뿐만 아니라, 생화 학적 잔존암도 23%으로 높아 장기적인 추적 관찰을 통하여 재발 군 내에서도 재발 및 예후를 예측할 수 있는 개별 인자들 을 찾아내는 것이 필요하리라 생각된다.
본 연구는 단일 병원에서 갑상선전절제술과 방사성옥소 치료를 시행한 환자만을 대상으로 하였던 점은 일관된 수준 의 치료를 유지할 수 있는 장점이 될 수 있겠으나, 전향적 연구가 아니므로 추적을 위한 합의된 프로토콜이 있는 것이 아니어서 임상의사들의 개인적 선호도에 따라 추적 검사의 빈도와 강도에 차이가 있을 수 있다. 또한 대상 환자들의 평균 추적기간이 7년으로 장기 치료 성적을 평가하기에는 추적 기 간이 짧다고 볼 수 있다. 재발이 있었던 22명 중 18명이 실질 적으로는 생화학적 잔존암에서 구조적 잔존암으로 발현된 경 우이며, 본 연구에서 재발로 정의되지는 않았지만 2명의 환자 는 초기치료 후에 무병상태를 유지하다가 마지막 추적에서 생화학적 재발이 발생하였기에 이들의 추후 경과를 주의하여 보아야 할 것이다. 초기치료 후에도 지속되는 생화학적 잔존 암의 임상 경과를 평가하는 데는 큰 무리가 없지만 뒤늦게 발생할 수 있는 재발에 대해서는 더 장기적인 추적 기간이 요구된다고 생각한다.
REFERENCES
1. Pacini F, Schlumberger M, lle H, Elisei R, Smit JWA, Wier- singa WM. European consensus for the management of patients with differentiated thyroid carcinoma of the folli- cular epithelium. European journal of endocrinology 2006;
154(6):787-803 .
2. Cooper DS, Doherty GM, Haugen BR, Kloos RT, Lee SL, Mandel SJ, et al. Revised American Thyroid Association Management Guidelines for Patients with Thyroid Nodules and Differentiated Thyroid Cancer. Thyroid 2009;19(11):
1167-214.
3. Yi KH, Park YJ, Koong SS, Kim JH, Na DG, Ryu JS, et al. Revised Korean Thyroid Association Management Gui- delines for Patients with Thyroid Nodules and Thyroid Can- cer. Endocrin Metab 2010;25(4):270.
4. Mazzaferri EL, Jhiang SM. Long-term impact of initial sur- gical and medical therapy on papillary and follicular thyroid cancer. Am J Med 1994;97(5):418-28.
5. Sawka AM, Thephamongkhol K, Brouwers M, Thabane L, Browman G, Gerstein HC. Clinical review 170: A systema- tic review and metaanalysis of the effectiveness of radioac- tive iodine remnant ablation for well-differentiated thyroid cancer. J Clin Endocrinol Metab 2004;89(8):3668-76.
6. Elisei R, Ugolini C, Viola D, Lupi C, Biagini A, Giannini R, et al. BRAF (V600E) mutation and outcome of patients with papillary thyroid carcinoma: a 15-year median follow- up study. J Clin Endocrinol Metab 2008;93(10):3943-9.
7. Ito Y, Fukushima M, Kihara M, Takamura Y, Kobayashi K, Miya A, et al. Investigation of the prognosis of patients with papillary thyroid carcinoma by tumor size. Endocr J 2012;59(6):457-64.
8. Tuttle RM, Tala H, Shah J, Leboeuf R, Ghossein R, Gonen M, et al. Estimating risk of recurrence in differentiated thy- roid cancer after total thyroidectomy and radioactive iodine remnant ablation: using response to therapy variables to modify the initial risk estimates predicted by the new Ame- rican Thyroid Association staging system. Thyroid 2010;
20(12):1341-9.
9. Haugen BR, Alexander EK, Bible KC, Doherty GM, Mandel SJ, Nikiforov YE, et al. 2015 American Thyroid Association Management Guidelines for Adult Patients with Thyroid Nodules and Differentiated Thyroid Cancer: The American Thyroid Association Guidelines Task Force on Thyroid No-
dules and Differentiated Thyroid Cancer. Thyroid 2016;
26(1):1-133.
10. Cailleux AF, Baudin E, Travagli JP, Ricard M, Schlumber- ger M. Is diagnostic iodine-131 scanning useful after total thyroid ablation for differentiated thyroid cancer? J Clin Endocrinol Metab 2000;85(1):175-8.
11. Pacini F, Capezzone M, Elisei R, Ceccarelli C, Taddei D, Pinchera A. Diagnostic 131-iodine whole-body scan may be avoided in thyroid cancer patients who have undetecta- ble stimulated serum Tg levels after initial treatment. J Clin Endocrinol Metab 2002;87(4):1499-501.
12. Kim EY, Kim WG, Kim WB, Kim TY, Ryu J, Gong G, et al. Clinical outcomes of persistent radioiodine uptake in the neck shown by diagnostic whole body scan in patients with differentiated thyroid carcinoma after initial surgery and remnant ablation. Clin Endocrinol (Oxf) 2010;73(2):
257-63.
13. Webb RC, Howard RS, Stojadinovic A, Gaitonde DY, Wal- lace MK, Ahmed J, et al. The utility of serum thyroglobulin measurement at the time of remnant ablation for predicting disease-free status in patients with differentiated thyroid cancer: a meta-analysis involving 3,947 patients. J Clin En- docrinol Metab 2012;97(8):2754-63.
14. Polachek A, Hirsch D, Tzvetov G, Grozinsky-Glasberg S, Slutski I, Singer J, et al. Prognostic value of post-thyroidec- tomy thyroglobulin levels in patients with differentiated thyroid cancer. J Endocrinol Invest 2011;34(11):855-60.
15. Nascimento C, Borget I, Al Ghuzlan A, Deandreis D, Chami L, Travagli JP, et al. Persistent disease and recurrence in differentiated thyroid cancer patients with undetectable po- stoperative stimulated thyroglobulin level. Endocr Relat Cancer 2011;18(2):29.