J. of Korean Orthopaedic Research Society Volume 8, Number 2, October, 2 0 0 5
악성 골육종에서 RECK (a novel MMP inhibitor) 단백의 발현 기전과 예후 관련 인자로서의 역할 규명 및 새로운
치료제로서의 가능성에 대한 연구
서울대학교 의과대학 정형외과학교실, 서울대학교병원 임상의학연구소*
김갑중・김한수・강현귀・오주한・이상훈・이상기・이미라*
= Abstract =
Analysis of RECK (a novel MMP inhibitor) Expression and its Roles as a Biomarker and Evaluation of RECK
as a Potential Therapeutic Agent for Osteosarcoma
Kap-Jung Kim, M.D., Han-Soo Kim, M.D., Hyun-Guy Kang, M.D.
Joo-Han Oh, M.D., Sang-Hoon Lee, M.D., Sang-Ki Lee, M.D., Mi-Ra Lee*
Department of Orthopaedic Surgery, Seoul National University College of Medicine, Clinical Research Institute of Seoul National University Hospital, Seoul, Korea*
Purpose: The purpose of this study is to analyze the mechanism of RECK gene (a novel MMP inhibitor) in human osteosarcoma and evaluation of RECK as a prognostic factor and therapeutic target.
Materials and Methods: Osteosarcoma cell lines were established from tumor samples of 23 patients who had been treated from March 2003 to April 2004 and 4 standard cell lines (HOS, MG-63, SaOS-2, U-2OS). We isolated the RNA from 27 cell lines and evaluated the expression level of RECK gene using quantitative real time-PCR method. MMP-2 and MMP-9 expression were evaluated by gelatin zymography. Five cell lines were selected which had a statistical significance between RECK gene up-regulation and MMP expression (p=0.01).
Then 5 cell lines and 3 standard cell lines were transfected by RECK gene. We compared RECK gene expres- sion with MMP down-regulation between transfected cell lines and non-transfected cell lines. Invasion of trans- fected cell lines were evaluated by invasion assay using matrigel.
Results: RECK genes were expressed in all cell lines and 1 cell line showed especially high expression. In zymography, pro-MMP-2 was expressed in almost cell lines whereas pro-MMP-9 was rarely expressed. RECK gene expressions were increasingly high and MMP expressions were low in transfected cell lines via zymogra- phy. Transfected HOS cells decreased invasiveness in matrigel invasion assay and showed small number of
※ 통신저자: 김 한 수
서울특별시 종로구 연건동 2 8 서울대학교 의과대학 정형외과학교실
TEL: 02) 2072-2362 FAX: 02) 764-2718 E-mail: [email protected]
✽ 본 논문의 요지는 2 0 0 5년 대한정형외과연구학회 학술대회에서 구연되었음.
서 론
대표적인 악성 골종양인 골육종 ( o s t e o s a r c o- m a )은 진단 당시 환자의 80% 이상이 이미 미세 전이를 가지고 있기 때문에 흔히 종양 조직의 수 술적 제거와 항암제 요법이 동시에 시행된다9 ). 근 래에 이르러 치료 방법의 발달로 5년 생존율이 65% 내지 75% 정도까지 높아졌으나, 최근 약 1 0여 년 동안은 더 이상의 생존율 향상이 없는 실 정이다. 그 주된 이유는 그 어떤 항암 요법을 사 용함에도 불구하고 30% 내지 5 0 %의 환자에서 전신적인 재발이 관찰되기 때문이다1 ).
Trimetrexate, ET-743, STI-571 등 비교적 최근에 개발된 약제들을 이용한 in vitro 연구 또 는 임상 시험이 시행되고 있으나, 아직까지는 어 떠한 새로운 약제도 골육종 또는 다른 악성 골종 양에 대하여 뚜렷한 치료 효과를 보여주고 있지 못하다. 따라서 이러한 약제 내성을 극복하기 위 한 방법으로, 종양의 진행이나 전이에 관련이 있 는 물질을 찾아 이를 억제함으로써 항암제의 효과 를 높이려는 연구가 많이 시행되고 있다. 대표적 인 시도로서 Epidermal growth factor recep- tor type2인 HER2 target으로 한 m o n o c l o n a l antibody (herceptin)를 이용한 치료가 골육종 에서도 현재 임상 시험 중이지만 현재까지의 결과 는 유방암에서와는 달리 희망적이지는 않다.
원발성 골육종의 치료 결과는 화학요법 및 방사 선 요법의 발전, 영상 기술의 발전 등으로 크게 호전되어 5년 생존율은 6 5 ~ 8 0 %에 이르렀지만, 최근 1 0여 년 동안은 생존율이 별로 향상되지 못 하고 있는 실정이다. 최근에 골육종 환자의 생존 율을 향상시키기 위한 방법으로 종양의 진행이나 전이에 관련이 있는 물질을 찾아내려는 연구가 많 이 시행되고 있으나 생존율 감소와 직접적으로 연 관되어 있는 원발성 골육종의 전이에 대한 연구
실적은 미미한 실정이다. 따라서 많은 암세포에서 암의 악성도 및 전이, 병기 등과 관련이 있다고 알려진 RECK 유전자와 M M P의 발현 양상을 골 육종 조직에서 조사하여 환자의 생존에 미치는 영 향을 알아보고 이를 치료에 적용하는 것은 골육종 환자의 생존율을 향상시키는 데 매우 의미 있는 연구일 것으로 사료된다.
본 연구의 목적은 악성 골종양인 골육종에서 새 로운 Transformation suppressor gene인 RECK gene (a novel MMP inhibitor)의 발 현 양상을 조사하고 세포 외 기질 ( e x t r a c e l l u a r m a t r i x )에서 생물학적 기능, 육종 세포의 성장 및 침윤에 미치는 기전을 연구하여 육종에서 항암 제 내성의 극복을 위한 새로운 치료법의 개발에 응용하고자 한다. 또한 골육종 환자에서 R E C K g e n e을 예후 관련 인자로 이용할 수 있는지에 대 하여 연구하고자 하였다.
대상 및 방법 1. 연구대상
2 0 0 3년 3월부터 2 0 0 4년 4월까지 본원에서 원 발성 골육종으로 진단, 수술 받은 환자 중에서 수 술 중 신선한 골육종 조직을 채취하여 모은 2 3예 의 골육종 세포와 4예의 표준 세포주 ( H O S , MG-63, SaOS-2, U-2OS) 총 2 8예의 골육종 세포주를 본 연구의 대상으로 하였다.
2. 연구방법
기존의 4가지 표준 세포주와 수집한 2 3예의 세 포주로부터 R N A를 추출하여 역 전사한 후 실시 간-중합 효소 연쇄 반응 (real time-PCR)을 이 용하여 RECK 유전자를 정량적으로 분석하였다.
골육종 조직에서 MMP-2 (matrix metallopro- migrated cells. It had a statistical significance (p<0.01).
Conclusion: It is expected that down-regulation of MMP by RECK gene expression can be used as a biolog- ic marker. It can be a new therapeutic strategies and valuable prognostic factors in treating osteosarcoma.
Key Words: Osteosarcoma, RECK gene, MMP, Transfection
teinases-2), MMP-9 (matrix metallopro- t e i n a s e s - 9 )의 발현은 Gelatin zymography를 이용하여 분석하였다. 24개의 세포주 중에서 RECK 유전자의 발현과 M M P의 발현간에 통계학 적으로 의의가 있는 5개의 세포주와 4개의 표준 세 포주에 RECK 유전자를 T r a n s f e c t i o n시켜 RECK 유전자의 과도한 발현과 M M P의 감소된 발현을 T r a n s f e c t i o n시키기 전과 비교하였다.
Transfection 시킨 세포주의 침습 능력은 m a t r i g e l을 이용하여 분석하였다. 표준 세포주는 HOS, MG-63, SaOS-2, U-2OS를 이용하였다.
1) 골육종 세포주 수립 및 배양
골육종 조직을 수술 후 즉시 무균적으로 모아서 잘게 자른 후 0.2% proteinase로 처리한 후 3 7
℃에서 3 0분간 흔들면서 배양한 후 0.2% colla- g e n a s e로 바꿔 처리하여 3 7℃에서 2 ~ 3시간 흔 들면서 배양하였다. Sterile filter통과 후 원심 분리하여 배지 (D-MEM with 10% FBS, penicillin & streptomycin)에서 배양하였다.
5 ~ 7일간 배양한 후 0.05% trypsin이 섞인 0.53mM EDTA-4Na로 분리하여 s u b c u l t u r e 하였다.
2) RNA 추출 및 Quantitative Real Time P C R
환자들의 조직과 표준 세포주에서 R N A를 분리 (RNeasy Mini kit, QIAGEN, 74104)한 후 SuperScript II RNase H Reverse Tran- s c r i p t a s e를 이용하여 c D N A를 생합성 하였다 (RTase, INVITROGEN, 18064-014).
Real time Quantitative PCR은 T a q m a n probe mixture (Applied Biosystems)를 이용 하여 ABI Prism 7000 SDS를 사용하였다.
P r i m e r는 Primer Express 2.0 프로그램을 이 용하여 제작하며 탐지자 ( P r o b e )의 5’말단 부위 에는 Reporter dye인 6 - F A M을 부착하고 3’말 단 부위에는 Q u e n c h e r로 T A M R A를 부착하였 다. RECK forward primer (5’-CGC GTG GCA GTC GAT TAC TAT-3’), Reverse primer (5’-GCT GCC AAG AGC GAA G G A - 3’)와 Probe (5’-FAM-AGC ACA GCT
CCG TCG CCG AGT G-TAMRA-3’)를 각각 제작하였다. GAPDH를 internal standard로 사용하였다.
P C R은 ABI prism 7000 SDS software version 1.0을 이용하여 P C R을 시행하고 RECK 유전자의 증폭을 위해 5 0℃ 2분, 95℃에 서 1 0분간의 변성 후 9 5℃ 1 5초, 60℃ 1분간 45cycles 조건으로 P C R을 시행하였다.
CT (threshold cycle)는 증폭된 타겟 유전자의 양이 일정한 역치에 이르게 될 때의 PCR cycle 수를 의미한다. ΔCT는 타겟 유전자의 CT 에서 G A P D H의 값을 뺀 값이 되며, 2-ΔΔC T 는 타겟 유전자와 reference cell line의 ΔCT 를 이용하 여 계산하였다. 이 값은 reference cell line 유 전자의 정상 발현에 상대적인 미확인 샘플 유전자 의 정상발현을 의미한다. 또한 이 자료는 r e f e r- ence gene에 상대적인 타겟 유전자 발현의 차이 를 배수로 나타나게 된다.
3) Gelatin zymography
세포를 1×1 06 c e l l s / w e l l이 되도록 6 - w e l l p l a t e에 p l a t i n g하여 4 8시간 동안 배양한 후 serum-free medium (SFM)으로 교환하였다.
4 8시간을 더 배양한 후 얻은 배양액을 농축하여 1 mg/ml의 젤라틴이 함유된 10% sodium dodecyl sulfate-polyacrylamide gel에서 전기 영동 하였다. 전기영동 후 젤을 r e n a t u r i n g buffer (2.5% Triton X-100)로 실온에서 3 0분 동안 두 번 배양하였다. 젤을 d e v e l o p i n g buffer (50 mM Tris base, 50 mM Tris- HCl, 0.2 M NaCl, 5 mM CaCl2, 0.02%
B r i j )로 3 0분간 실온에서 배양한 후 다시 3 7℃에 서 1 6시간 동안 배양하였다. 젤을 0.5% coom- masie brilliant blue-250으로 염색을 한 후 destaining solution (methanol : acetic acid : water = 50 : 10 : 40)을 이용해 M M P의 활 성을 관찰하였다. Positive control로는 H T - 1080 cell을 같은 조건으로 배양하여 얻은 배양액 을 사용하였다. RECK 유전자의 발현 감소와 MMP 활성의 증가 사이에 통계학적으로 유의한 5개의 세포주를 선택한 후 같은 방법으로 t r a n s- fection 전후의 MMP 활성을 관찰하였다.
4) Gene Construction.
R E C K은 CMV promoter를 가진 v e c t o r ( p C M Vβ- R E C K )에 삽입하였다. RECK은 human normal lung cell line (MRC-5)에서 R N A를 분리한 후 cDNA (Invitrogen kit)로 합성하여 P C R를 이용해서 +90 bp to +3018 bp (gene bank NM 021111) fragment를 분리하 였다. MRC-5 (ATCC, CCL-171) cell line은 1 4주된 male fetus에서 분리한 정상 폐 세포주 이다.
P C R을 하기 위해 제작한 sense primer 5’- GAC ATG GCG ACC GTC CGG GCC T-3’
와 antisense primer 5’-CCG TGG GCA GTC AGT TAT ATG-3’이다. Amplifica- tion 조건은 9 4°C에서 4 5초 동안 D e n a t u r e하였 으며, 62°C 에서 3 0초 동안 A n n e a l i n g하여 이 를 7 2°C에서 4 5초간 3 0회를 반복하였다. 이 과정 은 gene Amp PCR system 2700 (Applied Biosystems) 기기를 사용하였다.
얻어진 PCR product (2,922 bp)를 먼저 pGEM-T vector (Promega, A1380)에 삽입하 기 위하여 NotI 제한효소를 이용하여 l i g a t i o n하 였다. 다시 pGEM-T vector에서 잘라낸 2 , 9 2 2 bp fragment를 5’to 3’방향으로 p C M Vβ plasmid (BD Biosciences, 631719)에 N o t I를 이용 삽입하였다.
5) RECK gene transfection
4개의 표준 세포주 (HOS, MG-63, SaOS-2, U - 2 O S )와 선택된 5개의 환자 세포주를 1 0 % F B S가 포함된 배지로 100 mm dish (2×1 06 c e l l s )에 p l a t i n g하였다. 24시간 후에 세포를
Opti-MEM (Gibco, 31985-070)배지로 세척하 고 다시 Opti-MEM 배지에 D N A와 l i p o f e c t a- m i n e의 혼합물을 첨가하여 3 7℃에서 5시간 동안 배양하였다. 5시간 후에 D N A와 l i p o f e c t a m i n e 혼합물을 제거하고 F B S만 첨가된 배지로 배양하 였다. 48시간 후 각각의 샘플들에서 R N A를 분 리하고 RECK plasmid는 PvulI (Gibco-BRL, 25420-019) 제한효소를 이용하여 각각의 세포에 transfection 하였다.
6) Invasion assay using Matrigel
세포가 m a t r i g e l로 c o a t i n g된 f i l t e r를 통과하 여 이동하는 정도를 관찰하기 위해 B i o C o a t Matrigel Invasion Chamber (Becton Dick- inson, Bedford, MA)를 이용하였다. Upper c h a m b e r에 1×1 06 c e l l s / w e l l의 cell suspen- s i o n을 첨가하고 lower chamber에 c h e m o a t- t r a c t a n t로 10% FBS가 포함된 배지를 첨가한 후 3 7℃에서 1 6시간 배양하였다. Filter 상부에 있는 침윤하지 못한 세포는 제거하고 상위 c h a m b e r에서 하위c h a m b e r로 이동한 세포는 diff-quik stain solution (Dade Behring Inc., Newark, USA)을 이용하여 염색한 후 세 포수를 측정하였다.
결 과
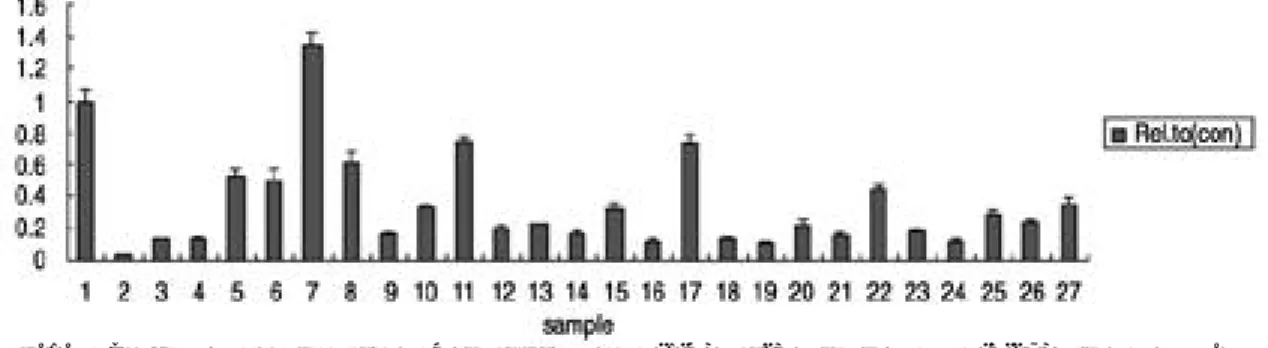
RECK 유전자의 발현은 2 3예의 환자 세포 중 2 2예 ( 9 6 % )에서 현저하게 낮게 발현 되었으며, 4예의 표준 세포주중 3예에서 RECK 유전자 발 현이 낮았다(Fig. 1). Gelatin zymography를 이용한 MMP 분석에서 p r o - M M P - 2는 표준 세
Fig. 1. RECK gene was expressed in all 4 standard cell lines (1-4) and 23 patients samples (5-27) with low level.
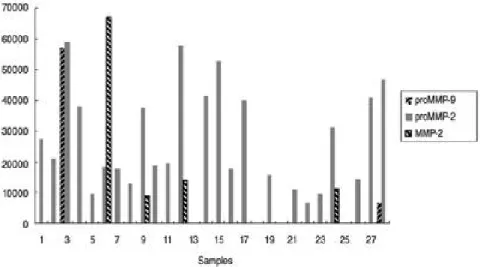
포주를 포함한 모든 세포주에서 발현 되었으며, M M P - 2는 단지 4예의 세포주에서 발현 되었다 (Fig. 2). Pro-MMP-9은 단지 1예의 환자 세포 주와 1예의 표준 세포주에서만 발현되었고, M M P - 9는 어느 세포주에서도 발현되지 않았다 (Fig. 2).
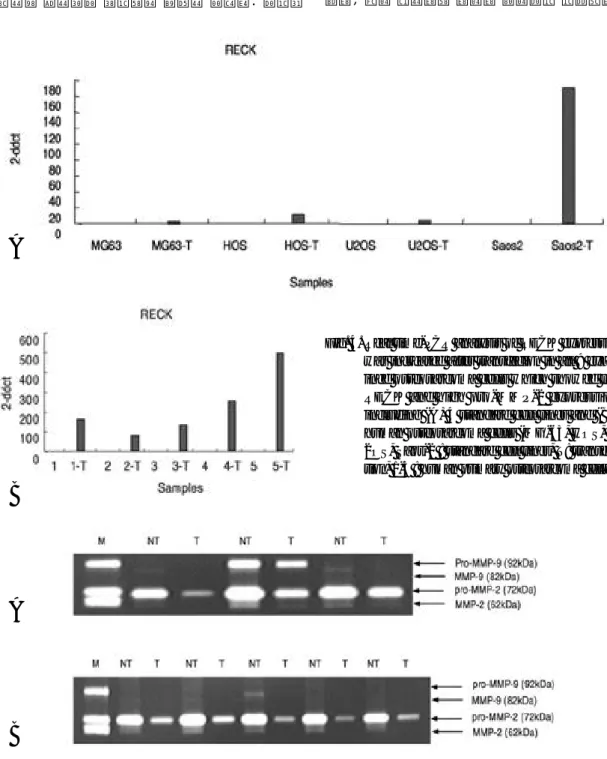
RECK 유전자 발현이 높은 세포주에서 p r o - M M P - 2의 발현은 현저히 낮았으며, 통계학적으 로 의의가 있었다(p=0.01)(Fig. 3). 이를 통해 RECK 유전자의 발현이 M M P의 강력한 억제 작 용을 함을 알 수 있었다. 특히 4예의 표준 세포주
와 5예의 환자 세포주를 선정하여 RECK 유전자 를 transfection 시킨 실험에서 모든 표준 세포 주에서 RECK 유전자를 transfection 시키기 전 보다 RECK 유전자의 발현이 높았으며 S a O S - 2 표준 세포주에서 특히 높은 발현을 보였다( F i g . 4A). 5예의 환자 세포주에서도 역시 RECK 유 전자를 transfection 시키기 전보다 t r a n s f e c- tion 후에 RECK 유전자의 높은 발현이 있었으 며 특히 1예의 환자 세포주가 높은 발현을 보였다 (Fig. 4B).
Gelatin zymography를 통한 t r a n s f e c t i o n 전과 후의 MMP 발현 에서 표준 세포주와 환자 세포주에서 transfection 후에 M M P - 2와 9의 발현이 현저하게 감소되었다(Fig. 5A, 5B). 이 실험을 통해 transfection 후 RECK 유전자의 발현이 M M P - 2와 9을 더욱 강력히 억제함을 알 수 있었다.
골육종 세포의 국소 침윤과 전이는 종양 세포가 기저막을 뚫고 종양 색전을 형성함으로서이루어지 는데 이에 관여하는 m a t r i g e l을 이용한 i n v a- sion assay에서 transfection 전 보다 t r a n s- fection 후에 HOS 세포주의 침습 능력이 현저히 감소하는 것을 보였고, 세포 이동성 역시 t r a n s- fection 후 에 유 의 적 으 로 감 소 하 였 다 (p<0.001)(Fig. 6A, 6B).
Fig. 2. Pro-MMP-2 was expressed in all 24 examined osteosarcoma cells including 4 standard cell lines (1-4) and 20 human osteosarcoma cells whereas pro-MMP-9 expressed in only 2 cell lines and no expressed MMP-9.
Fig. 3. Relationships of RECK expression and pro- MMP-2 in osteosarcoma. Tumors with high expression of RECK show a significantly low expression of pro-MMP-2. (p=0.01).
고 찰
골육종은 골 조직에서 발생하는 악성 신생물로 소아나 청년기에 호발하는 특징을 가진다. 원발성
악성 골종양 중 가장 흔히 발생하는 종양으로서 성장이 왕성한 부위에서 흔히 발생하는데 60% 이 상이 장골과 골간단 부위 즉, 원위 대퇴골, 근위 경골, 근위 상완골의 골간단 부위에서 발생한다.
Fig. 4. Real time-PCR analysis of RECK expression was increased after transfecion in all 9 exam- ined osteosarcoma cells which showed low RECK and high pro-MMP-2 expression, including (A) 4 standard cell lines and (B)5 human osteosarcoma cells (MG-63, HOS, U- 2OS, Saos-2 : standard cell lines, T: transfec- tion, 1-5 : human primary osteosarcoma cells)
Fig. 5. Zymographic analysis of MMP-2 and MMP-9 expression in (A) standard osteosarcoma cell lines (1,2 lane : HOS. 3,4 lane : U-2OS. 5,6 lane : Saos-2. M : marker, NT : not transfection, T : transfection) and (B) Human osteosarcoma cells.
A
A B
B
종양의 발생은 최초의 유전적 변형에서 시작하 여 점차적으로 국소 침윤과 전이를 할 수 있는 악 성 종양으로 진행한다2 ). 종양 세포가 기저막을 뚫 고 종양 색전을 형성함으로서 이루어진다. 이런 종양 세포의 침윤과 전이 과정은 종양 세포와 주 변 기질간의 상호 작용에 의해서 이루어지며, 여 기에는 기저막과 세포 외 기질을 분해하는 단백분 해효소가 작용을 한다1 0 ). 이 단백분해효소는 matrix metalloproteinase (MMPs), serine proteases, cystein proteases와 aspartic pro- t e a s e s로 크게 나눌 수 있으며 이중 M M P s는 가 장 강력하고 중요한 단백분해효소이다. MMPs는 구조와 기능에 따라 교원 분해효소 ( c o l l a g e- nase, MMP-1,8,13), 젤라틴 분 해 효 소 (gelatinase, MMP-2,9), stromelysin (MMP-3,10,11) 그리고 membrane type MMPs (MT-MMP1,2) 등 크게 4가지 종류로 나누어진다1 0 ). MMPs는 골육종의 국소 침윤과
예후에 매우 중요한 역할을 한다3 ). MMPs는 종 양 세포 뿐 아니라 기질 섬유아세포, 염증세포에 서도 만들어지며, 주변 세포로 하여금 M M P를 생산하게 유도 시키는 단백질과 싸이토카인을 생 산한다. 이 중 M M P - 2와 M M P - 9은 구강, 식 도, 위, 대장, 간 내 담도, 췌장, 요도, 방광, 난 소 종양의 국소 침윤이나 전이 과정과 관련된 연 구 보고가 있다2 , 1 0 ). 면역조직화학염색을 이용한 연구에서 골육종 환자의 7 4 %에서 종양 세포가 MMP-9 양성을 보이며 이것의 발현 정도가 예후 와 연관성을 가진다는 보고가 있다3 ). MMP의 성 질을 치료에 응용하여 주로 MMP-2, MMP-9, M T - M M P등을 타겟으로 한 MMP inhibitor들 이 개발되어 임상 시험이 시도되고 있다4 , 5 ). MMP inhibitor 역할을 하는 대표적인 물질로 TIMP (tissue inhibitor of metallopro- t e i n a s e )에 대하여 연구되어 왔지만 낮은 생체 이 용율로 실제로 임상에서 약제로서 사용하기는 어
Fig. 6. (A) Matrigel invasion assay of HOS cell line before transfection and after transfection of RECK gene. (B) The number of cells decreased after RECK transfection in matrigel invasion assay within mean±SD (*p < 0.001, NT : not transfection, T : transfection).
A
B
렵다.
최근 M M P를 통한 세포외 기질로의 종양 신호 를 억제하는 새로운 종류의 t r a n s f o r m a t i o n suppressor gene이 발견되었다1 3 ). RECK (reversion inducing cysteine rich protein with Kazal motifs)이라고 불리는 이 유전자는 활성화 된 RAS 항암 유전자에 의해 형태가 바뀐 쥐의 섬유아세포주에서 cDNA cloning을 통해 처음 분리 되었다7 ). RECK 유전자는 다양한 정 상 조직과 비종양성 세포주에서 발현되는데 종양 세포 또는 종양 세포주로 형태가 바뀐 세포주에서 는 발현되지 않거나 현저히 감소되어 있다.
Takahashi 등1 3 )에 의하면 2 0여종 이상의 암 세 포주를 조사한 결과 어떠한 세포주에서도 R E C K 유전자는 발현되지 않는다고 하였다. RECK m R N A는 폐, 소장, 갑상선, 신장, 난소를 비롯 하여 조사한 거의 모든 정상 조직에서 발현된다.
RECK 유전자는 골격근에서 많이 발현되는 것으 로 알려져 있으나, 뼈나 연골 등에서는 연구된 바 가 없다. RECK의 기능에 대해서 지금까지 MMP-2, MMP-9 그리고 MT1-MMP (MMP- 1 4 )의 분비를 억제하거나 활성도를 감소시키는 내제적인 MMP inhibitor의 역할을 가지고 있다 고 알려져 있다. 또한 종양의 혈관 신생에도 관여 하여 R E C K의 d o w n - r e g u l a t i o n은 종양의 진행 과 연관이 있는 것으로 보고되고 있으나 그 기전 에 대해서는 명확히 밝혀져 있지는 않지만6 , 1 2 , 1 4 , 1 5 )
, RECK 유전자가 MMP 활성화의 여러 단계에서 억제 작용을 가진다고 알려져 있다7 ). RECK 유 전자의 발현에 의해 MMP-2,9 모두 억제 되지만 이중 M M P - 9의 억제보다는 M M P - 2의 억제가 훨씬 더 중요하며 임상적 의의를 지니는 것으로 알려지고 있다1 1 ).
R E C K이 임상적으로 생물학적 표지자 또는 예 후 관련 인자로서의 의의가 있는 지에 대하여 최 근 몇 편의 임상 연구가 보고되고 있다. 유방암과 췌장암과 환자에서 환자의 생존율, 재발까지의 기 간 등과의 연관성이 밝혀졌으며, 이들 악성 종양 에서 R E C K이 독립적인 예후 관련 인자로서 의 미가 있다고 하였다8 , 1 1 ). Span 등은 유방암에서 R E C K의 발현을 R T - P C R을 이용하여 정량적으 로 분석하여 R E C K이 유방암 환자에서 독립적인
예후 관련 인자로서 의의가 있다고 하였고1 1 ), Masui 등은 췌장암 환자의 조직에서 면역조직화 학법을 이용하여 MMP-2 활성화를 억제함으로써 췌장암의 침윤을 억제하는 작용을 하며 역시 췌장 암의 예후를 예측하는 molecular marker로서 의의를 가진다고 하였다8 ).
본 연구에서도 RECK 유전자 발현으로 인한 M M P - 2 , 9의 발현 억제를 표준 골육종 세포주와 환자에서 수집한 골육종 세포주에서 확인하였는 데, 저자들은 이에 그치지 않고 RECK 유전자를 표준 세포주와 골육종 세포주에 transfection 시 켜 transfection 후에 RECK 유전자가 훨씬 많 이 발현되고, transfection 시킨 세포주에서 M M P - 2 , 9의 발현이 현저히 억제됨을 표준 세포 주와 환자의 세포주에서 실험을 통해 확인 한 것 이 본 연구의 큰 의의라 하겠다. 다른 장기의 암 에서 RECK 유전자의 발현과 MMP 발현의 억제 가 서로 밀접한 관계가 있다는 것은 전술한 바와 같이 여러 연구 보고가 있지만, 본 연구에서처럼 표준 세포주와 환자로부터 직접 수집한 골육종 세 포주에서 RECK 유전자가 발현됨에 따라 M M P 발현이 억제됨을 입증한 연구는 아직까지 많지 않 으며 최근 1 0여 년 동안 생존율 향상을 보이지 않 고 답보 상태에 있는 골육종 치료에 생존율을 향 상 시키고 이를 치료에 적응 시키려는 시도는 매 우 의의 있는 연구라고 사료된다.
향후에는 좀 더 많은 환자의 세포주 수집을 통 해 RECK 유전자의 발현에 의한 MMP 발현의 억제가 장기 추시 시 환자의 국소 재발 및 장기 생존율 등과 같은 종양학적 결과와의 상관 관계를 연구하는 것이 필요할 것으로 사료된다.
결 론
골육종 세포주에서 RECK 유전자 발현에 의한 MMP 억제의 기전을 연구하여 골육종의 진행과 전이 등 관련된 병태생리를 이해하는데 도움이 될 것으로 사료되며, 골육종의 임상 양상, 전이 등 예후 관련 인자와 치료 타겟으로 이용될 수 있을 것으로 예상된다. 향후 통계적 의의를 가질 수 있 을 정도까지 표본의 수를 늘려야 하며 관련 기전 에 대한 추가 연구가 필요하다고 사료된다.
R E F E R E N C E S
01) Bacci G, Picci P and Ferrari S et al: Primary chemotherapy and delayed surgery for non- metastatic osteosarcoma of the extremities.
Results in 164 patients preoperatively treated with high doses of methotrexate followed by cis- platin and doxorubicin. C a n c e r, 72:3227-3238, 1993.
02) Curran S and Murray GI: Matrix metallopro- teinase in tumor invasion and metastasis. J Pathol 189:300-308, 1999.
03) F o u k a s A F , D e s h m u k h N S , G r i m e r R J , Mangham DC, Mangos EG and Taylor S:
Stage-IIB osteosarcomas around the knee. A study of MMP-9 in surviving tumor cells. J Bone Joint Surg-Br, 84(5):706-711, 2002.
04) Hidalgo M and Eckhardt SG: Development of matrix metalloproteinase inhibitors in cancer therapy. J Natl Cancer Inst. 93(3):178-193, 2001.
05) Hoekstra R, Eskens FA and Verweij J: Matrix metalloproteinase inhibitors: Current develop- ments and future perspectives. O n c o l o g i s t, 65:415-427, 2001.
06) Junseo O, Takahashi R and Kondo S et al : The membrane-anchored MMP inhibitor RECK is a key regulator of extracellular integrity and angiogenesis. Cell, 107:789-800, 2001.
07) Makoto N, Junseo Oh, Rei T, Shunya K, Hitoshi K and Chiaki T: RECK: A novel sup- pressor of malignancy linking oncogenic signal- ing to extracellular matrix remodeling. C a n c e r and Metastasis Reviews, 22:167-175, 2003.
08) Masui T, Doi R and Koshiba T et al: RECK expression in pancreatic cancer: Its correlation with lower invasiveness and better prognosis.
Clin Cancer Res, 9:1779-1784, 2003.
09) Meyers PA, Heller G and Healey JH et al:
Osteogenic sarcoma with clinically detectable metastasis at initial presentation. J Clin Oncol, 11(3):449-453, 1993.
10) Nelson AR, Fingleton B, Rothenberg ML and Matisian LM: Matrix metalloproteinases: Bio- logic activity and clinical implications. J Clin Oncol 18:1135-1149, 2000.
11) Paul NS, Sweep CGJ, Peggy N, Louk V, David L and Raija L : Matrix metalloproteinase inhibitor Reversion-inducing-cysteine-rich pro- tein with Kazal motifs. A prognostic marker for good clinical outcome in human breast carcino- ma. Cancer, 97:2710-2715, 2003.
12) Sasahara RM, Brochado SM, Takahashi C et al: Transcriptional control of the RECK metasta- sis/angiogenesis suppressor gene. Cancer Detect Prev., 26(6):435-443, 2002.
13) Takahash C, Sheng Z and Horan TP et al:
Regulation of matrix metalloproteinase-9 and inhibition of tumor invasion by the membrane- anchored glycoprotein RECK. PNAS, 95:13221- 13226, 1998.
14) Weaver VM: Membrane-associated MMP regu- lators: Novel cell adhesion tumor suppressor pro- teins. Dev Cell, 2:6-7, 2002.
15) Welm B, Mott J and Werb Z: Developmental biology: Vasculogenesis is a wreck without RECK. Curr Biol. 12:R209-R211, 2002.