폐경기 여성에서 호르몬 요법과 랄록시펜이 골밀도 및 골대사에 미치는 영향
고신대학교 의과대학 산부인과학교실, 가정의학교실1
김남수1․이태화․김흥열
The Effects of Hormone Therapy and Raloxifen on the Bone Mineral Densities and Bone Metabolism of Postmenopausal Women
Nam Su Kim1, M.D., Tae Hwa Lee, M.D., Heung Yeol Kim, M.D.
Department of Obstetrics and Gynecology, Department of Family Medicine1, Department of Kosin Medical Center of Gaspel, Busan, Korea
Objectives: To evaluate the effects of hormone therapy and Raloxifen on the bone mineral density and bone metabolism in the postmenopausal women.
Methods: This prospective randomized clinical trial examined the effects of Raloxifene and conjugated equine estrogen, on bone mineral density (BMD) and biochemical markers of bone turnover in 149 women with low bone mass. Treatment included Raloxifen (group I, n=63), or conjugated equine estrogen (group II, n=86), for 12 months. Bone density measurements were performed at months 6 and 12 months at the lumbar spine and femur neck. Biochemical markers of bone turnover were also measured every six months.
Results: BMD of lumbar spine, it increased significantly during the treatment in Group I, Group II (P<0.005).
As for BMD of femur neck, it increased slightly during the treatment in Group I and Group II, but not significantly. Serum osteocalcin and urinary deoxypyridinoline in Group I and Group II decreased significantly at 12 months of treatment (P<0.005).
Conclusion: The treatment with Raloxifen and conjugated equine estrogen is effective in postmenopausal women with osteoporosis by decreasing bone biochemical markers and by increasing the BMD.
Key Words: Raloxifen, Bone biochemical markers, Bone mineral density, Osteoporosis
5)최근 의료기술의 급격한 발달과 건강에 대한 관심 의 증가로 평균수명이 연장됨에 따라 여성에서도 폐 경 후 기간이 전체 인생의 상당부분을 차지하게 되 었으며, 우리나라에서도 노년층의 인구증가로 폐경 여성의 수가 증가하는 추세이다1. 폐경기 초기에 나 타날 수 있는 증상으로는 안면홍조 및 수면장애 등 이 있으며 기간이 경과함에 따라 비뇨생식기의 위축
책임저자: 김흥열, 고신대학교 의과대학 산부인과학교실 Tel: 051)990-6226, Fax: 051)990-6226 E-mail: [email protected]
으로 인한 배뇨장애, 요실금, 성교통 및 노인성 질염 (senile vaginitis)이 나타날 수 있고, 특히 장기 후유증 으로 나타날 수 있는 골다공증과 심혈관질환은 폐경 기 이후의 중요한 공중보건문제로 대두되고 있다2. 폐경 후 여성에서 에스트로겐 요법은 장기적인 면 에서 심혈관계 질환의 예방과3,4 골다공증의 예방에 긍정적인 효과가 있는 것으로 알려져 예방의학 분야 에서 매우 중요한 자리를 차지하게 되었다5-8. 골다공증은 골조직에 있어서 골 미세조직의 파괴 와 골량 감소에 의한 골절에 대한 감수성이 증가를
특징으로 하는 전신적인 골질환이다9.
골다공증의 임상적인 중요성은 골절과 그 결과로 초래되는 합병증으로 인하여 높은 이환율과 사망률 을 야기하며, 경제적인 측면에 있어서도 재활을 위 한 의료이용을 증가시킨다는 것이다.
현재 폐경여성의 골다공증 예방과 치료에 관한 많 은 치료법이 제시되고 있으나 3차에 걸친 골다공증 에 관한 Consensus Development Conference에 의하면 에스트로겐은 폐경 후 골절을 감소시킬 수 있는 치 료제라고 규정하고 있다. 또한 에스트로겐은 이미 골다공증이 형성된 폐경여성에서도 치료제로서의 역할도 한다.
골소실을 예방하기 위한 폐경 후 호르몬 요법을 시행 시에 투여경로나 제제의 종류에 관계없이 일정 에스트로겐 혈중농도를 유지시킴으로서 골량 감소 를 방지할 수 있으며 그 농도는 50~70 pg/mL으로 알려져 있다4,10. 이러한 폐경 후 호르몬 요법에 의하 여 골절의 약 50% 정도를 감소시킬 수 있다11. 지난 20~30년간 골다공증과 심혈관 질환의 예방 목적으로 주로 여성호르몬 요법 (estrogen+progeste- rone)이 장기간 사용되어왔다. 그러나 최근의 연구결 과, 특히 WHI (Womens’ Health Initiative) 연구결과는 난포호르몬과 황체호르몬 병합요법이 심혈관질환 예 방 효과가 없음은 물론 오히려 초기에는 관상동맥질 환과 뇌혈관질환 및 정맥 혈전색전증 그리고 장기간 사용시 유방암의 위험성을 증가시킴을 보여 주었다12. 최근 미국식품의약품안전청 (FDA)에서는 여성호르 몬 제제를 폐경 후 안면홍조 등 혈관운동장애와 질 위축증 등의 폐경 후 증상을 완화하는 것을 위해 처 방하고, 골다공증의 예방 및 치료목적으로 사용할 때는 다른 약제를 사용하는 것을 먼저 고려하라고 권하고 있다13. 따라서 골다공증의 예방과 치료를 위 해서 기존의 난포호르몬과 황체호르몬 병합요법과 다른 골흡수 억제제와의 비교 연구가 활발히 진행되 고 있다. 한편 여성호르몬은 혈청지질에 영향을 주 어 일반적으로 중성지방을 증가시키는 것으로 알려 져 있다.
선택적 에스트로겐수용체조절제 (selective estrogen receptor modulator, SERM)인 랄록시펜은 자궁내막의 과증식으로 인한 질출혈을 유발하지 않고 골밀도를
가시키고 총콜레스테롤 및 저밀도-콜레스테롤을 감 소시키는 효과가 있다14. 또한 랄록시펜은 척추골절 의 발생빈도를 감소시킬 뿐만 아니라 유방암의 위험 성을 감소시키는 것으로 알려져 있다15,16.
이에 저자들은 난포호르몬 및 황체호르몬 치료와 랄록시펜 치료간의 골밀도 및 골대사에 미치는 효과 를 비교하고자 하였다.
대상 및 방법
1. 연구대상
2005년 4월부터 2007년 4월까지 고신의대 복음병 원 가정의학과, 산부인과를 방문한 환자 중 자연 폐 경된 여성으로 마지막 월경 후 최소한 12개월 이상 무월경인 여성 중에서 폐경과 관련된 증상이 있는 환자와 이미 자궁의 양성 질환으로 인하여 자궁절제 술을 받은 환자 149명을 대상으로 하였다.
폐경 여부의 확인은 혈중 난포자극호르몬 (folli- cular stimulating hormone: FSH) 농도가 50 mIU/mL 이상이고 혈중 17β-estradiol치는 25 pg/mL 이하인 경우로 하였다. 연구대상자에서는 최근 6개월간 호 르몬제제를 비롯한 골생성과 골흡수에 영향을 미친 다고 생각되는 약제 복용의 과거력이 없었다. 소화 성 궤양을 포함한 신장, 심장, 간장 질환이 있는 경 우와 호르몬 요법의 금기증인 급성 간질환, 만성 간 기증 저하, 급성 혈관질환, 유방암 환자 등도 제외하 였다.
2. 연구 방법
대상 환자에게 임상시험의 목적 및 내용 등을 설 명한 후 동의한 환자를 대상으로 무작위적으로 2종 류의 치료군, 즉 랄록시펜 투여군 (제 1군), 프레마린 투여군 (제 II군)에 각 군별로 63, 86명씩을 배정하였 다. 랄록시펜군은 랄록시펜 (EvistaⓇ, 한국 릴리) 60 mg을 매일 투여하였다. 프레마린은 경구용 conjugate equine estrogen (와이어스) 0.625 mg을 1일 1회, 취침 전에 복용하였다. 양군 모두에서 칼슘 600 mg을 추 가로 투여하였다. 각 군에서 체중, 혈중 FSH치 및 연령의 차이는 없었다. 각 군의 임상적 특징은 Table 1과 같다.
Table 1. General characteristics of the patient
Group I Group II
n Age
Menopausal age L2-4 BMD (g/cm2) Femur neck BMD (g/cm2) Serum Ostecocalcin (ng/nL Total alkaline phosphatase (u/L) Deoxypyridinoline*
63 56.23±3.75 49.21±5.73 0.735±0.083 0.729±0.114 17.45±5.32
121.21±3.8 8.39±0.5
86 51.15±4.98 48.87±2.54 0.865±0.104 0.885±0.086 16.32±4.78
116.31±4.3 7.56±0.8 Group I: treated with raloxifen, Group II: treated with estrogen.
* Deoxypyridinoline (p mol/u mol creatinine).
약제투여를 시행하기 전에 공복상태에서 혈액 및 소변을 채취하여 혈중 osteocalcin, total alkaline phosphatase, 척추 (L2-L4) 및 대퇴골 경부의 골밀도를 측정하였다. 이후 3개월 간격으로 폐경 클리닉을 방 문하게 하여 12개월까지 혈중 osteocalcin, total alka- line phosphatase의 변화, 척추 및 대퇴골 경부의 골밀도 변화를 측정하였다. 대상 환자들로부터 혈액을 5 mL 식 채취하여 3000xg에서 20분간 원심분리하여 혈청 을 채취하였다.
1) 혈청 검사
혈청 FSH는 Amerlaer-M FSH RIA kit (Amersham, England)를 사용하여 측정하였으며 intra-assay coeffi- cient of variation은 6.0%, inter-assay coefficient of variation은 4.3%이었다. 혈청 osteocalcin은 NovoCalcin kit (metra Biosyatem,Inc,, U.S.A.)를 사용하여 측정하 였으며 이 검사방법은 bovine osteocalcin에 대한 단일 항체를 이용하는 것으로 사람의 osteocalcin과 100%
의 교차반응을 가지며 그 민감도는 0.454 ng/mL이다.
혈청중의 alkaline phosphatase는 phenyl-D-sodium phos- phatase를 가수분해하여 phenol을 생성하는데 phenol 생성된 phenol을 산화제의 촉매 하에서 4-aminoanti- phyline과 축합하여 적색의 quinon이 형성되는데 이 를 비색정량하여 활성치를 구하였다 (Kind-king법).
2) 소변 검사
소변내의 deoxypyridinoline의 측정은 Metra Biosys-
tems (U.S.A.)사의 Pyrilink-D kit를 사용하였다. 이 검 사는 deoxypyridinoline에 대한 단일항체로 미리 처리 된 미세관 (micro title palte)에서의 경쟁성 효소면역 측정법이다. 채취한 소변을 30분간 실온에 방치하여 부유물을 제거한 후 완충용액으로 10배 되게 희석하 여 구하였다.
3) 골밀도 검사
골밀도 검사는 DXA (Dual Energy X-ray Absorp- tiometry, DPX, Lunar Co)를 이용하여 골다공증에 의 한 골절이 일어나며 유병률 및 사망률에 가장 큰 영 향을 미치는 척추 (L2-L4)와 대퇴골경부 (femur neck) 의 골밀도를 측정하였다.
4) 통계처리
모든 자료는 평균과 표준 오차 (mean±standard error) 로 표시하였고 자료 분석은 IBM PC와 SAS (verson 6.04)를 이용하여 각 치료군에 따른 골밀도와 혈중 osteocalcin, tatal alkaline phosphatase치의 각각 기저 치에 대한 비를 구한 후 paired t-test에 의하여 검정 하였고, 각 치료군 간의 비교는 Student t-test를 이용 하여 5% 유의수준에서 검색을 하였다.
결 과
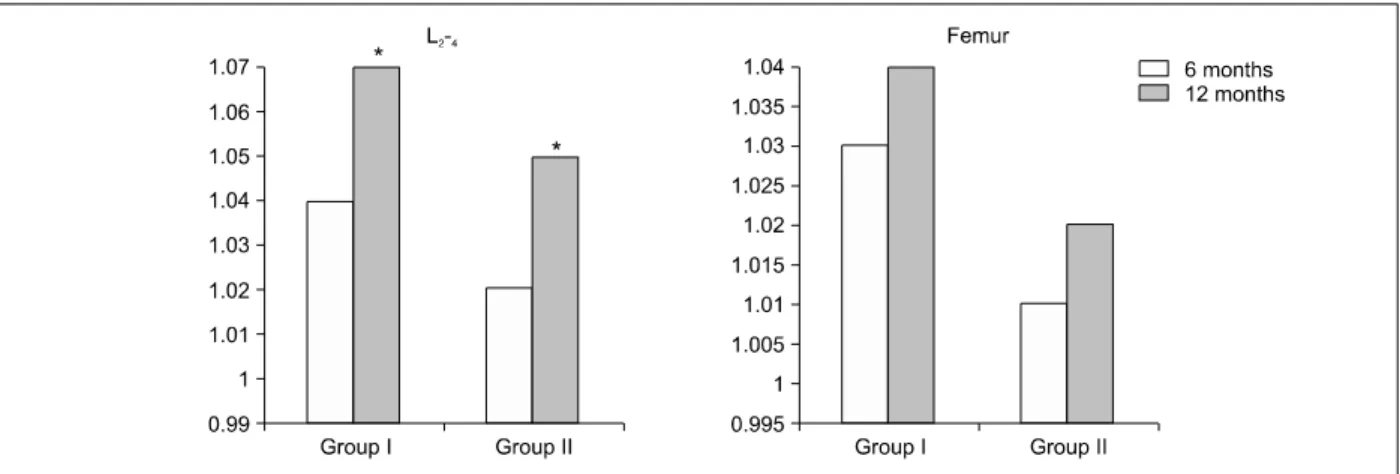
1. 척추 (L2-L4) 골밀도의 변화 (Fig. 1)
6개월, 12개월째에 기저치에 대한 척추 골밀도의
Fig. 1. Changes on the levels of bone mineral density of postmenopausal women according to study group (group I:
Raloxifen, group II: ERT) Values are expressed in precent of initial values (Significance:* P<0.05).
Fig. 2. Changes on the levels of bone metabolism of postmenopausal women according to study group (group I:
Raloxifen, group II: ERT). Values are expressed in percent of initial values (Significance:* P<0.05).
비는 랄록시펜을 단독으로 투여한 제 I군에서는 각 각 1.04±0.13, 1.07±0.16, 에스트로겐 단독으로 투여 한 제 II군에서는 각각 1.02±0.19, 1.05±0.21로 기저 치에 비해 12개월 치료 후의 결과가 제 I, II군 모두 통계학적으로 유의한 척추골밀도의 증가를 보였다 (P<0.05).
2. 대퇴골 경부 골밀도의 변화 (Fig. 1)
6개월, 12개월째에 기저치에 대한 대퇴골경부 밀 도의 비는 랄록시펜을 단독으로 투여한 제 I군에서 는 각각 1.03±0.11, 1.08±0.12, 에스트로겐을 단독 투여한 제II군에서도 각각 1.01±0.14, 1.02±0.12로
기저치에 비해 12개월 치료 후의 결과가 통계학적으 로 유의하지는 않았지만 약간의 골밀도의 증가를 보 였다.
3. 혈청 osteocalcin의 변화 (Fig. 2)
6개월, 12개월째에 기저치에 대한 혈중 osteocalcin 치는 랄록시펜을 단독으로 투여한 제 I군에서는 각 각 0.88±0.18, 0.70±0.21, 제II군에서는 각각 0.90±
0.16, 0.87±0.36 (P<0.05)로 기저치에 비해 12개월 치 료 후의 결과가 제 1, 2군 모두 통계학적으로 유의한 혈중 osteocalcin치 감소를 보였다 (P<0.05).
4. 혈중 total alkaline phosphatase의 변화 6개월, 12개월째에 기저치에 대한 total alkaline phosphatase의 비는 랄록시펜을 단독으로 투여한 제I 군에서는 각각 0.92±0.19, 0.85±0.23, 제II군에서는 각 각 0.96±0.12, 0.90±0.24로 기저치에 비해 12개월 치료 후의 결과가 통계학적으로 유의하지는 않았지만 약간 의 혈중 total alkaline phosphatase치의 감소를 보였다.
5. 요중 Deoxypyridnoline의 변화
6개월, 12개월째에 기저치에 대한 요중 Deoxypyri- dnoline치는 랄록시펜울 단독으로 투여한 제I군에서 는 각각 0.80±0.12, 0.77±0.17, 제II군에서는 각각 0.90±0.16, 0.84±0.16로 투여 12개월째 제I, II군 모두 유의한 감소를 보였다 (P<0.05).
고 찰
골은 일생을 두고 지속적으로 재형성되는 활발한 대사조직으로 골대사 과정에는 파골세포 (Osteoclast) 에 의한 골흡수 (bone resorption)와 조골세포 (Oste- oblast)에 의한 골형성 (bone formation)이 결합되어 반 복적으로 발생하며 이러한 현상을 통해 신체의 미네 랄 대사가 균형을 이루어 골의 재형성 (bone remol- ding)이 일어난다. 정상인에서는 골흡수와 골형성이 균형을 이루고 있으나 골다공증 환자에서는 이러한 골대사 과정에서 불균형이 나타난다.
폐경 후 골다공증이 나타나는 기전은 아직 확실치 않으나 난소에서 에스트로겐의 분비가 감소할 때 파 골세포의 의한 골흡수의 증가가 그 원인으로 추측된 다17. 폐경 후 매년 총 골량의 1~3% 정도가 손실되 며 따라서 수년 후에는 골절의 위험도가 2배 이상 증가한다고 하며18 에스트로겐 치료로써 골다공증에 의한 골절의 위험도는 50~60% 정도 감소시킬 수 있으나19 이미 발생한 골다공증에서 골량을 증가시 키는 것은 매우 어려우며 더 이상의 골소실을 방지 하는 것이 중요하다. 따라서 폐경 후 발생하는 골다 공증의 예방 및 치료를 위해서는 골다공증의 고위험 군을 조기에 파악하여 신속한 예방이 강구되어야 하 며 이미 발생한 골다공증 환자는 적절한 치료를 하
는 것이 중요하다.
또는 다른 골다공증의 진단으로는 골대사지표의 검사방법이 있는데 골대사 지표는 임상적으로 골다 공증의 요소를 가진 대상의 조기 선별검사와 골다공 증의 진행의 평가, 치료에 대한 반응을 쉽게 평가할 수 있다. 골대사지표는 파골세포와 조골세포에서 분 비되는 효소나 골흡수와 골형성시 유리되는 골기질 성분들을 지칭하는 것으로 혈액이나 소변에서 측정 할 수 있다17.
최근에 들어 골흡수의 새로운 지표로서 소변내의 pyridinium 교차결합물들이 제시되었다. 이들 교차결 합물들은 앞서 열거한 골흡수 표지물질들의 약점이 보완된 새로운 지표로서 Pyd와 Dpd가 있다. 이들은 콜라겐 섬유로부터 효소 (lysyloxydase)에 의해 세포 바깥에서 형성되고 콜라겐 분자구조의 바깥에 존재 하는 telopeptide 부위의 lysine 또는 hydroxylysine기 에 작용하여 알데하이드 반응에 의해 주위의 또 다 른 콜라겐 분자와 bifunctional cross link가 형성되는 것이며 골조직이나 연골조직에서 형성된 3-hydroxy pyridinium cross link가 바로 Pyd 및 Dpd로 형성되는 것이다. 이 교차결합물의 합성은 콜라겐의 성숙도에 의존적으로 일어나기 때문에 정상적인 골조직의 형 성과 흡수시에 지속적으로 합성되며 이들의 합성속 도는 수일에서 수주내에 일어난다고 한다20. 저자들 은 이번 연구에서 골흡수 표지물질로서 Dpd를 이용 했는데 이는 Dpd가 Pyd보다 골 흡수에 더 예민하기 때문으로21 그 이유는 Dpd는 물론 대동맥이나 치아, 인대에도 아주 소량이 함유되어 있었지만 이들로부 터의 콜라겐분해는 아주 미미해서 소변으로 유리되 어 Dpd는 순전히 콜라겐이 그 근원지라고 할 수 있 고, 유리형의 Dpd는 Pyd와는 1% 이하만, 펩타이드 결합형과는 2.5%이하에서만 교차반응을 보이며 또 한 항원-항체반응에서 흔히 볼 수 있는 소변의 간섭 현상도 그리 크지 않은 것이다. 여러 보고자들에 의 하면 pyridinium 교차결합물의 유리는 일중변화가 있 다고 하여 오후 8시경에 최저치에 이르렀다가 이후 서서히 증가하다가 새벽 2시경부터 급속히 증가한 후 오전 8시에 최고에 이르는데 이는 골흡수가 주로 사람이 수면을 취하고 있는 한밤중에 일어나기 때문 일 것이다21.
따라서 본 연구에서는 환자로 하여금 검사 전날은 금식을 지시하고 당일 새벽 6시에 소변을 본 후 내 원하여 아침 8시에 채취한 소변을 검사하였다. 또한 소변 내로 유리되어 나오는 Dpd는 소변량에 따라 변할 수 있기 때문에 소변량을 반영하는 소변내의 creatinine을 이용하는 교정이 필요하였다. 난소가 절 제된 생쥐에서 소변내의 pyridinium 교차결합물의 배 설량이 증가된 것에 대한 보고 외에 급속 골소실 여 성군에서만 폐경 후 pyridinium 교차결합물의 증가를 볼 수 있었다고 하였고 폐경 후 1년 이내에 그 배설 증가율이 가장 많고 그 이후는 감소한다고 하였다22. 저자들의 본 연구에서도 소변 내 Dpd 측정량이 제I, II군 모두에서 유의하게 감소하여 앞서 언급한 여러 연구자들의 결과와 일치되는 소견을 보였다. 이것으 로 소변 내 대사에 따른 변화 상태를 잘 반영한다고 판정할 수 있고, 이러한 pyridinium 교차결합물의 증 가는 폐경 등으로 인하는 에스트로겐의 결핍에 의한 골교체율의 증가 때문으로 생각된다. 이러한 현상은 적절한 골다공증치료로 그 치료효과에 따라 소변내 의 pyridinium교차 결합물의 배설이 다시 감소되는 것이 보고되어 폐경으로 인하는 골소실이 조기에 치 료하면 어느 정도 예방이 가능한 질환일 것으로 생 각되게 되었다. 본 연구에서도 랄록시펜과 에스트로 겐으로 1년간 치료한 폐경 여성에서 소변 내 Dpd량 이 유의하게 감소되었음이 발견되었다. 이와 같은 현상은 여러 가지 다른 질환에서도 발견되는데 즉, 갑상선 및 부갑상선 질환23, 류마티스 관절염24, Paget 씨 질환과 악성종양의 골절이22 등에서 소변으로 배 설되는 pyridinium 교차결합물의 배설이 증가되고 이 는 치료 후 감소되었고, 영양결핍증의 아동들이 정 상 아동들에 비해 소변내의 pyridinium 교차결합물의 배설이 적고 치료에 의해 그 배설이 증가한 것을 보 고하였다25.
Osteocalcin은 분자량이 작은 (4.9 kd) 비교원질단백 으로서 유일하게 칼슘과 결합할 수 있는 아미노산인 GLA (gamma-carboxyglutamic acid)을 3개 포함하고 있으며, 골조직과 치아조직에만 특이하게 발견된다.
정확한 기능은 아직 알려져 있지 않다. 주로 조골세 포에서 합성된 후 뼈의 세포의 기질에 결합되며, 새 로 합성된 osteocalcin의 일부가 혈액내로 흘러나오
는데, 이를 방사면역 방법을 이용하여 측정한다. 소 의 osteocalcin에 대한 항체가 사람의 항체와 교차 반 응을 하기 때문에 소의 osteocalcin을 이용하여 대개 의 측정 방법이 개발되었으며, 최근에는 방사면역 계수방법에 의해 예민도가 많이 향상되었다26. 여성에서는 30대부터 연령이 증가할수록 혈중 osteo- calcin이 점차 증가하는데, 특히 폐경이 되면 2배 이 상 증가하였다가 에스트로겐 등을 투여하게 되면 다 시 폐경 전 수치로 저하하는 것으로 알려져 있다27. 이는 본 연구에서도 osteocalcin치가 치료 후 통계학 적으로 유의하게 감소한 것과 동일하게 나타난다.
폐경이 된 여성을 아무 치료 없이 골밀도를 계속해 서 측정하면서 2~4년을 추적 관찰해본 결과, 혈중 osteocalcin이 가장 좋은 골교체율의 생화학적 지표 였다고 보고하고 있다28. 혈청 osteocalcin은 조골세포 에서 형성되는 골단백의 일종으로 조골세포의 활동 성을 평가하고 골형성 정도를 조사하는데 매우 도움 이 된다. 혈청 obteocalcin치는 폐경 후에 증가하고 에스트로겐 치료 후에는 감소된다. 이 표지물질은 골흡수와 골형성이 동일하게 이루어 질 때는 골전환 의 우수한 지표가 되고 동일하지 않을 경우에는 골 형성의 표지가 될 수 있다. 한편 골흡수 과정에서 유 리되는 osteocalcin은 골흡수를 반영할 수도 있다고 한다28. 그러나 osteocalcin에 대해 아직 해결되어야 할 문제점으로는 정상인과 비정상인에서의 clearance 의 차이점과 혈중 내로 유리된 osteocalcin이 다시 뼈 로 재이용되는데 그 양이 얼마나 되는지 등이 해결 되어야 할 점이다. 또한 혈청 alkaline phosphatase는 골형성에 의하여 상당한 골전환이 일어나는 Paget씨 질환이나 부갑상선 기능항진증 등에서는 증가하나, 대체적으로 검사의 민감도가 낮고 특히 골다공증 환 자에서는 큰 변화는 없다고 보고하였으며29 본 연구 에서도 마찬가지로 alkaline phosphatase의 변화는 통 계학적 의의가 없었다.
골다공증의 치료에 많은 약제들이 이용되고 있으 며 골흡수를 억제하는 약제가 현재까지 사용되는 약 제의 대부분을 차지하고 있다. 이중 대표적인 것이 여성호르몬으로 알려져 있으며, 칼시토닌과 알렌드 로네이트, 랄록시펜 등이 알려져 있다. 골흡수 억제 제를 골다공증 환자에게 사용하면 골흡수 지표가
1~2개월 내에 감소한다고 알려져 있으며, 이후 골 형 지표가 감소한다고 알려져 있다30.
조직 선택적으로 에스트로겐 수용체를 조절할 수 있는 랄록시펜은 난포호르몬처럼 골밀도를 증가시 키고 골절 발생률을 감소시키지만14, 자궁내막 증식 을 유발하지 않고 장기간 사용시 유방암의 위험성을 오히려 감소시키는 것으로 알려져 있다31. 그러나 랄 록시펜은 안면홍조를 증가시킬 수 있으므로, 본 연 구에서도 폐경 후 적어도 3년이 경과된 여성만을 대 상으로 하였다. Johnston 등은 3년간 랄록시펜을 각 각 30 mg 사용시 0.71%; 60 mg 사용시, 1.28%; 150 mg 사용시, 1.20% 요추 골밀도를 증가시킴을 보고하였 고32, 또한 MORE (The Multiple Outcomes of Raloxi- fene Evaluation) 연구에서도 3년간 랄록시펜 60 mg을 사용시 위약군에 비하여 골밀도가 대퇴골 경부에서 는 2.1% 증가, 척추에서 2.6% 증가함을 보고하였다.
골다공증의 예방과 치료를 위해서는 랄록시펜 60 mg 을 사용시 위약군에 비하여 골밀도가 대퇴골경부에 서는 2.1% 증가, 척추에서 2.6% 증가함을 보고하였 다. 골다공증의 예방과 치료를 위해서는 랄록시펜 60 mg을 투여하는 것이 효과적임을 알 수 있다16. 국 내에서 여성호르몬 병합요법에 의한 요추 골밀도의 1년 증가율은 4.5~7.5%까지 보고되어 있다5,8. 여성 호르몬 요법과 랄록시펜을 직접 비교한 연구 결과 살펴보면 양군 모두에서 척추 골밀도의 증가가 관찰 되었으나 랄록시펜 사용군에 비하여 여성호르몬 사 용군에서 척추 골밀도가 약 2배 정도 유의하게 높았 고, 대퇴골밀도의 경우 양군 간에 차이가 없었다15. 본 연구에서도 랄록시펜 사용시 척추 골밀도가 2.2% 증가하여 유의하였으며, 여성호르몬 사용군에 서는 척추 골밀도가 3.8% 증가하여 여성호르몬 사 용군에서 랄록시펜 사용군에 비하여 다른 연구들과 비슷한 약 2배 정도의 골밀도 증가를 관할 할 수 있 었다. 대퇴골의 경우는 양군 모두에서 골밀도의 증 가를 관찰할 수 없었다. 최근 Osteoporosis Research Advisory Group의 meta-analysis 결과를 보면 랄록시 펜과 여성호르몬이 모두 통계적으로 유의하게 요추 골밀도를 증가시켰으나, 척추골절 예방에 있어서는 랄록시펜만이 유의하게 골절을 예방하였다.
현재 골다공증의 일차적 치료를 위해 호르몬 요법
을 대신하여 비스포스포네이트 제제가 널리 사용되고 있으나 일부 환자에서 비스포스포네이트 제제의 부작 용인 식도염과 같은 위장장애와 공복시 과량의 물을 복용해야 하는 불편함으로 인해 사용이 제한되고 있 다34. 이상의 결과를 요약하면 랄록시펜군에서 골밀도 증가 정도가 난포호르몬 및 황체호르몬 병합요법군에 비하여 다소 낮았지만, 여성호르몬의 장기간 사용에 따른 위험성과 랄록시펜이 혈중 지질대사에 미치는 긍정적인 효과를 고려할 때, 특히 비스포스포네이트 사용에 따른 위장장애기 있는 환자나 여성 호르몬의 사용을 싫어하는 폐경 후 여성 골다공증 환자에서 랄 록시펜을 사용하는 것은 유용하리라 사료된다.
요 약
목적: 골다공증의 예방과 치료 목적으로 흔히 사 용되고 있는 호르몬 요법과 랄록시펜을 복용한 여성 을 대상으로 생화학적 표지자의 변화와 골밀도의 변 화에 어떤 연관성이 있는지를 알아보자 하였다.
방법: 2005년 4월부터 2007년 4월까지 고신대학 교 복음병원 가정의학과 및 산부인과를 방문한 환자 중 2종류의 치료군, 즉 랄록시펜 투여군 (제I군), 프 레마린 투여군 (제II군)에 각 군별로 63, 86명씩을 배 정하여 혈중 osteocalcin, total alkaline phosphatase, 척 추 (L2-L4) 및 대퇴골 경부의 골밀도를 측정하였다.
결과: 척추 골밀도의 비는 기저치에 비해 12개월 치료 후의 결과가 제I, II군 모두 통계학적으로 유의 한 척추골밀도의 증가를 보였다 (P<0.05). 혈중 osteo- calcin치는 기저치에 비해 12개월 치료 후의 결과가 제I, II군 모두 통계학적으로 유의한 감소를 보였다 (P<0.05). 요중 deoxypyridnoline치는 투여 12개월째 제 I, II군 모두 유의한 감소를 보였다 (P<0.05).
결론: 여성호르몬의 장기간 사용에 따른 위험성 과 랄록시펜이 혈중 지질대사에 미치는 긍정적인 효 과를 고려할 때, 특히 비스포스포네이트 사용에 따 른 위장장애가 있는 환자나 여성 호르몬의 사용을 싫어하는 폐경 후 여성 골다공증 환자에서 랄록시펜 을 사용하는 것은 유용하리라 사료된다
중심단어: 랄록시펜, 여성호르몬, 골대사표지물질, 골밀도, 골다공증
참 고 문 헌
1. 구병삼, 민부기. 한국여성의 폐경에 관한 연구 (1). 대한산부회지 1985;28:966-72.
2. Henderson BE, Ross RK, Paganini-Hill A, Mack TM. Estrogen use and cardiovascular disease. Am J Obstet Gynecol 1986;154:1181-6.
3. 유건재, 김흥열, 박은동. 폐경후 여성에서 에스 트로젠 보충요법시 병행투여된 황체호르몬제제 가 지질대사에 미치는 영향. 대한산부회지 1997;
40:1467-75.
4. 노미정, 차영수, 김흥열. 폐경후 여성에서 경용 및 경피적 에스트로젠 보충요법이 혈중 지질대 사에 미치는 영향. 대한폐경회지 1999;5:135-42.
5. 김흥열, 김성환, 김재도, 최영식, 어완규, 이재우 등. 폐경기 여성에서 호르몬 대치요법으로 인한 골대사표지자변화에 관한 연구. 대한골대사학회 지 1997;4:1-8.
6. 이천준, 김흥열, 박은동. 폐경기 여성의 호르몬 대치요법 후 혈청내의 Osteocalcin, 칼슘, Alka- line phosphatase 그리고 소변내의 칼슘의 변화에 관한 연구. 대한산부회지 1997;40:2733-40.
7. 김흥열, 박은동. 폐경후 여성에서 에스트로젠 보 충요법시 병행투여된 황체호르몬제제가 골밀도 와 골대사에 미치는 영향. 대한산부회지 1998;41:
564-575.
8. 양형일, 공은희, 어완규, 최영식, 김기찬, 김성한 등. 호르몬 보충요법시 병행 투여된 황체호르몬 제제가 골밀도 및 지질대사에 미치는 영향. 대한 가정지 1999;20:1000-11.
9. Consensus Development Conference. Diagnosis, pro- phylaxsis, and treatment of osteoporosis. Am J Med 1993;94:646-50.
10. 노선화, 김성한, 김흥열, 박은동. 폐경후 여성에 서 경피적 에스트로겐 보충투여시 병행투여된 활성형비타민 D의 골밀도와 골대사에 미치는 영향에 관한 연구. 대한산부회지 1998;41:968-78.
11. Ettinger B, Genant HK, Cann CE. Postmenopausal bone loss is prevented by treatment with low- dosage estrogen with calcium. Ann Intern Med
1987;106:40-5.
12. Rossouw JE, Anderson GL, Prentice RL, LaCroix AZ, Kooperberg C, Stefanick ML, et al. Risks and benefits of estrogen plus progestin in healthy postmenopausal women: principal results From the Women's Health Initiative randomized controlled trial. JAMA 2002;288:321-33.
13. North American Menopause Society. Amended report from the MANS Advisory Panel in Post- menopausal Hormone Therapy. Menopause 2003;
10:6-12.
14. Delmas PD, Bjarmason NH, Mitlak BH, Ravoux AC, Shah AS, Huster WJ, et al. Effects of raloxi- fene on bone mineral density, serum cholesterol concentrations, and uterine endometrium in post- menopausal women. N Engl J Med 1997;337:
1641-7.
15. Lufkin EG, Whiraker MD, Nickelsen T, Arguera R, Calpan RH, Knickerbocker RK, et al. Treatment of established postmenopausal osteoporosis with ralo- xifene: a randomized trial. J Bone Miner Res 1998;
13:1747-54.
16. Ettinger B, Black DM, Mitlak BH, Knickerbocker RK, Nickelsen T, Genant HK, et al. Reduction of vertebral fracture risk in postmenopausal women with osteoporosis treated with raloxifene: results from a 3-year randomized clinical trial. Multiple Outcomes of Ralixufene Evaluation (MORE) Investi- gators. JAMA 1999;282:637-45.
17. Garnero P, Delmas PD. New developments in biochemical markers for osteoporosis. Calcif Tissue Int 1996;59(Suppl. 1):S2-9.
18. Garnero P, Sornay-Rendu E, Chapuy MC, Delmas PD. Increased bone turnover in late postmenopausal women is a major determinant of osteoporosis. J Bone Miner Res 1996;11:337-49.
19. Weinstein MC, Schiff I. Cost-effectiveness of hormone replacement therapy in the menopause.
Obstet Gynecol Surv 1983;38:445-55.
20. Fujimoto D, Suzukl M, Uchlyama A, Miyamoto S,
Inoue T. Analysis of pyridinoline, a cross-linking compound of collagen fibers, in human urine. J Biochem 1983;94:1133-40.
21. Schlemmer A, Hassager C, Jensen MS, Christi- ansen C. Marked diurnal variation in urinary excre- tion of pyridinium cross-link in premenopausal women. J Clin Endocrnol Metab 1992;74:476-80.
22. Selby PL, Peacock M. The effect of transdermal oestrogen on bone, calcium-regulating hormones and liver in postmenopausal women. Clin Endo- crinol 1986;25:543-7.
23. Harvey RD, Mchardy KC, Reid IW, Paterson F, Bewsher PD, Duncan A, et al. Measurement of bone collagen degradation in hyperthyroidism and during thyroxine replacement therapy using pyri- dinium cross-links as specific urinary markers. J Clin Endocrinol Metab 1991;72:1189-94.
24. Black D, Duncan A, Robbins SP. Quantitative analysis of the pyridinium crosslinks of collagen in urine using ion-paired reversed-phase high-perfor- mance liquid chromatography. Anal Biochem 1998;
169:197-203.
25. Branca F, Robins SP, Ferro-Luzzl A, Golden MH.
Bone turnover in malnourished children. Lancet 1992;340:1493-6.
26. Price PA, Williamson MK, Lothringer JW. Origin of the vitamin K-dependent bone protein found in plasma and its clearance by kidney and bone. J Biol Chem 1981;256:12760-6.
27. Johansen JS, Riis BJ, Delmas PD, Christiansen C.
Plamsa BGP: an indicator of spontaneous bone loss and of the effect of estrogen treatment in post- menopausal women. Eur J Clin Invest 1988;18:
191-5.
28. Slovik DM, Gundberg CM, Neer RM, Lian JB.
Clinical evaluation of bone turnover by serum osteo- calcin measurements in a hospital setting. J Clin Endocrinol Metab 1984;59:228-30.
29. Crilly RG, Jones MM, Horsman A, Nordin BE.
Rise in plasma alkaline phosphatase at the meno- pause. Clin Sci 1980;58:341-2.
30. Braga de Castro Machado A, Hannon R, Eastell R.
Monitoring alendronate therapy for Osteoporosis. J Bone Miner Res 1999;14:602-8.
31. Cauley JA, Norton L, Lippman ME, Eckert S, Krueger KA, Purdie DW, et al. Continued breast cancer risk reduction in postmenopausal women treated with raloxifene: 4-year results from the MORE trial. Multiple outcomes of raloxifene evalu- ation. Breast Cancer Res Treat 2001;65:125-34.
32. Johnston CC Jr, Bjarnason NH, Cohen FJ, Shah A, Lindsay R, Mitlak BH, et al. Long-term effects of raloxifene on bone mineral density, bone turnover, and serum lipid levels in early postmenopausal women: three-year data from 2 double-blind, rando- mized, placebo-controlled trials. Arch Intern Med 2000;169:3444-50.
33. Cranney A, Guyatt G, Griffith L, Wells G, Tugwell P, Rosen C. Osteoporosis Research methodology group and the osteoporosis research advisory group.
Meta-analyses of therapies for postmenopausal osteoporosis. Ⅸ: Summary of meta-analyses of therapies for postmenopausal osteoporosis. Endocr Rev 2002;23:570-8.
34. Colina RE, Smith M, Kikendall JW, Wong RK. A new probable increasing cause of esophageal ulceration: alendronate. Am J Gastroenterol 1997;
92:704-6.