251
중등도-중증 궤양성 대장염 환자에서 infliximab의 치료효과에 대한 메타분석
김종윤1·이숙향2·유기연1*
1동덕여자대학교 약학대학, 2아주대학교 약학대학
(2012 년 8월 17일 접수·2012년 9월 14일 수정·2012년 9월 20일 승인)
Meta-analysis of the Efficacy of Infliximab in Patients with Moderate-Severe Ulcerative Colitis
Jong Yoon Kim 1 , Sukhyang Lee 2 , and Ki Yon Rhew 1 *
1College of Pharmacy, Dongduk Women's University, Seoul 136-714, Korea
2College of Pharmacy, Ajou University, Suwon 443-749, Korea
(Received August 17, 2012 ·Revised September 14, 2012·Accepted September 20, 2012)
Ulcerative colitis (UC) is characterized by a life-long chronic course with remissions and exacerbations. Use of biologi- cal therapies may reduce or delay the surgical procedures in patients with UC. The aim of this study was to determine the impact of infliximab (IFX) use on the rate of remission, surgical interventions, and the effect on quality of life in patients with moderate to severe UC. Literature was searched for studies that investigated the efficacy of IFX on the rate of remission, colectomy and quality of life (QoL) between January 1990 and June 2012 at MEDLINE, January 1988 and June 2012 at EMbase and others. Eleven trials were included in the meta-analysis; divided into placebo controlled 8 tri- als and intravenous corticosteroid controlled group 3 trials. In comparison to placebo control groups, patients who received IFX had an odds ratio (OR) of 3.712 (95% CI: 2.714, 5.079) for the short-term clinical remission, and 3.053 (95% CI: 2.044, 4.559) for the rate of long-term remission. In colectomy rate and quality of life (QoL), odds ratio were 0.566(95% CI: 0.387, 0.827) and 0.658 (0.505, 0.811) respectively. Any adverse reactions including infections, infusion reaction, rash and arthralgia were equivalent in both groups. Compared with intravenous corticosteroid controlled group, patients who received IFX had lower remission rate with short-term odds ratio 0.227 (95% CI: 0.033, 1.556) and long- term odds ratio 1.054 (95% CI: 0.317, 3.502) respectively. However, statistical significance was not showed with both two analyses. The higher adverse drug reaction (ADR) rates were occurred in the corticosteroid controlled groups. 73.3%
of patients treated corticosteroid reported Cushing-like syndrome with moon face. In conclusion, IFX does increase remission rate and decrease the rate of colectomy in patients with UC without elevating any adverse reactions signifi- cantly. IFX also improves QoL in moderate to severe UC patients. It would not exceed the efficacy of intravenous corti- costeroid, whereas intravenous corticosteroid also reported high rate of adverse reactions.
□ Key words - Infliximab, ulcerative colitis, meta-analysis, systematic review
궤양성 대장염(Ulcerative colitis, UC)은 상대적으로 유럽과 북미에서 호발하는 것으로 알려진 염증성 장질환으로, 우리나 라를 포함한 동아시아에서도 그 발병률이 급증하고 있다.1) 대 장의 점막 또는 점막하층 염증으로 인한 혈성 설사와 대변급 박감(urgency) 등이 주 증상으로, 호전과 악화가 반복적으로 나 타나는 것이 특징이다.2)궤양성 대장염 전체 환자의 약 15%
가 증상의 악화로 입원을 경험하고3), 입원환자 중 약 60%만이 corticosteroid 정맥주사 요법에 반응을 보인다. Corticosteroid 치
료에 불응하는 환자들의 경우 대장 절제술4), 혹은 cyclosporin5) 이나 infliximab등의 구조요법을 고려할 수 있다.
최근 발표된 cyclosporine과 infliximab의 궤양성 대장염 치료효과에 대한 무작위 임상 연구에 따르면6), corticosteroid 정맥주사에 불응하는 중증의 급성 궤양성 대장염 환자에서 cyclosporine의 단기간 관해 유도와 대장절제술 방지 효과가 infliximab과 유사한 것으로 보고되었다. 그러나 cyclosporine 정맥주사 요법은 신기능 손상, 진전 및 발작, 고혈압, 잇몸 비후, 다모증 등 여러 부작용의 위험을 가지고 있어 그 사용 이 제한적이다.7-10) 또 다른 메타분석 연구에서는 현재까지 보고된 무작위대조연구의 증례수가 적고 추적관찰기간이 짧 아 중증 궤양성 대장염에서 cyclosporin의 치료효과에 대한 근거는 제한적이며 향후 더 많은 연구가 필요하다고 발표한
Correspondence to : 유기연
동덕여자대학교 약학대학
서울 성북구 월곡동 23-1 동덕여자대학교 약학대학
Tel: +82-2-940-4519, Fax: +82-2-940-4159
E-mail: kiyon@dongduk.ac.kr
바 있다.11)
대장절제술을 시행한 환자에서는 ileoanal pouch가 생성됨 으로써, 약 50%의 환자에서 pouchitis12)가, 10%의 환자에서 pouch failure가 발생하며13), 여성의 생식 능력을 80% 저하시 킬 뿐만 아니라14), 24%의 환자에서는 야간 변실금을 유발하 여 삶의 질을 낮추는 것으로 보고되었다.15)이러한 후유증을 고려해볼 때 중증 궤양성 대장염 환자에게 대장 절제술은 약 물 구조요법보다 우선적으로 실시될 수 없다.
Infliximab은 TNF-α chimera 단일클론항체(chimeric monoclonal antibody)로, 중증 궤양성 대장염 치료에 도입된 최초의 생물학 적 치료제이다. 생물학적 치료제의 도입은 궤양성 대장염의 치 료 목표를 과거 증상 조절에서, 질병의 경과 변화로 발전시키 는 계기를 제공하였다.16) Infliximab은 장내 염증 유발 인자 인 TNF-α17)의 활성을 약화시킴으로써, 염증 세포의 자멸사 (apoptosis)를 유도할 뿐만 아니라18), 림프구와 단핵 세포의 자 멸사를 유도한다.19-20) Infliximab은 corticosteroid나 thiopurine (azathiopirne/6-mercaptopurine) 등 보편적인 치료 약재에 대해 적정한 반응을 나타내지 않거나 내약성이 없는 환자, 혹은 이러한 약제를 사용할 수 없는 중등도-중증의 궤양성 대장염 환자의 치료에 사용된다. 그러나 여러 연구에서 infliximab에 대한 반응률이 낮게는 20%에서 높게는 66%까지 상반된 결 과를 보이고 있어21-23) 약물 효과에 대한 종합적인 규명이 필요하다. 이에 본 연구는 중증-중등도 궤양성 대장염에서 infliximab의 치료효과에 대한 메타분석을 통해 해당 약물의 유효성과 안전성을 여러 평가조건으로 분석하고자 한다.
연구방법
문헌의 수집
Medline, EMbase, Koreamed의 전자 데이터 베이스를 사 용하여 검색하였다(Searched on June, 2012). 이외에도 대한 소화기내과학회지, 미국소화기내과학회지, 국회도서관, 제약 회사 웹사이트, clinicaltrials.com등을 검색하여 분석에 포함 하였다.
선정 및 제외 기준
선정기준은 다음과 같다; (1) 무작위 대조 임상연구, (2) 성 인(18세 이상) 궤양성 대장염 환자에서 inflliximab의 유효성 혹은 안전성을 규명, (3) 결과 변수로 관해(remission) 유도, 대장절제술(colectomy), 삶의 질 (quality of life) 개선, 약물유 해반응(ADR) 등을 관찰한 논문. 궤양성 대장염의 명확한 진 단 기준이 제시되지 않았거나, 실험군과 대조군 모두 infliximab이 투여된 경우에는 제외하였다.
문헌의 선정 방법 및 질 평가
수집된 문헌 중 선정기준에 적합한 문헌을 추출하기 위하 여 논문의 제목과 초록을 검토하여, 근거수준이 높은 것으로
판단되는 무작위 대조 임상연구만을 1차적으로 선정하였다.
1차 선정된 논문 각각의 원문을 검토하여 선정 및 제외 기 준에 적합한지 여부를 판단하였다.
선정된 논문은 Jadad’s quality assessment scale24)을 사용 하여 질 평가를 실시하였고, 총점 5점 중 2점 이상의 논문을 선정하여 본 연구에서 분석하였다.25) 또한 최종 선정된 논문 에서 질병의 중증도, 대상 피험자의 수, 시험군 및 대조군의 치료법(용법, 용량, 투여 횟수), 치료기간, 결과 변수의 종류 및 치료 효과 등을 추출하여 요약, 정리하였다.
이러한 논문의 선정, 질 평가, 필요한 자료의 추출 과정은 공저자 2인이 독립적으로 수행하여 동일한 자료만을 활용하 였다. 만일 불일치 하는 부분이 있을 경우 충분한 논의를 통 하여 의견이 합일되는 사항을 정리하였다.
통계 분석
관해 유도와 삶의 질평가, 대장 절제술의 빈도 등을 모두 odds ratio (95% CIs)로 분석되었으며, 동질성검정은 동질성 검 정 통계량(Q)를 사용하여 Chi-square test와 I2값으로 수량화하였 다. 동질성이 확보된 경우, fixed effect model(mantel-Haenszel method)를 이용하여 분석하였고, 통계적으로 만일 동질성이 확 보되지 않은 경우, random effect model을 사용하였다.26)
Publication bias를 측정하기 위해서 funnel plot으로 점검하였 으며, 비대칭의 정도는 Begg’s rank correlation method와 Egger’s regression method를 사용하였다(P < 0.05)
모든 통계 분석은 comprehensive Meta-analysis software version 2 (Biostat, Englewood, USA)을 사용하였고, 양측검 정으로 실시 되었다.
연구결과
문헌의 수집 결과
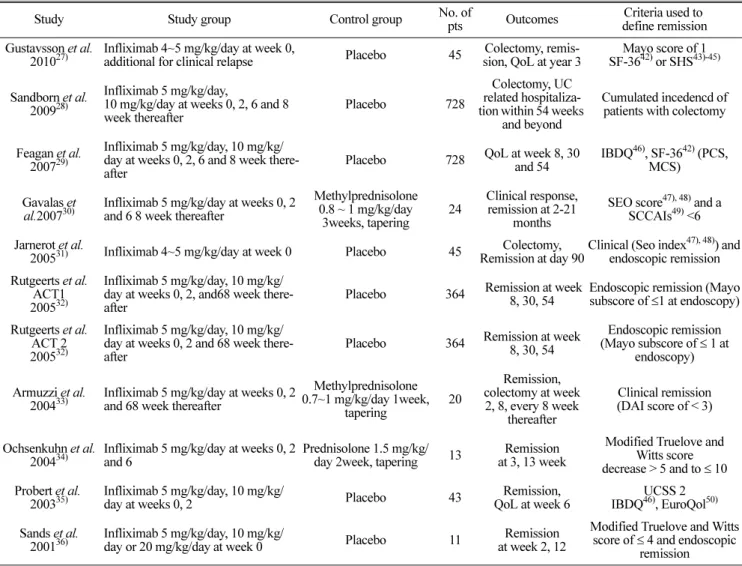
문헌검색 결과 Medline에서 ‘infliximab AND ulcerative colitis’로 검색하여 823편의 논문을 수집하였으며, 해당 논문 의 제목과 초록을 참고하여 선정, 제외기준에 적합한 13편의 논문을 1차적으로 선정하였다. 또한 EMbase에서 연관 검색 어를 포함하여 검색하였을 때 3,329편의 논문을 수집하였으 며, 해당 논문의 제목과 초록을 참고하여 동일한 방법으로 18편의 문헌을 1차적으로 선정하였다. 1차적으로 검색된 논 문 중 8편이 Medline과 EMbase에서 중복되었으므로 이를 제 외하고, 총 23개의 연구를 검토하였다. 검토 대상 23편 중, 13편은 무작위 과정 혹은 대조군의 성격이 적절하지 않는 등의 이유로 제외하였고, 최종적으로 10편의 논문을 선정하 였다(Figure 1).27-36)각 연구의 질 평가는 Jadad’s scale을 활 용하여 시행한 결과, 2편의 논문을 제외하고 모두 3점 혹은 4점으로 평가되어 우수한 질을 확보하고 있다고 할 수 있었 다(Table 2).
Rutgeerts et al. ACT 1, 2와 동일한 환자군으로 연구한
논문이 3편, Jarnerot et al.와 환자군이 같은 논문이 1편 있 었으나, 서로 다른 관점으로 치료효과를 평가하였으므로 분 석 대상 논문으로 최종 선정하였다. 총 환자수를 합산할 때 는, 같은 환자군을 사용한 경우 한번만 합산하였다. 연구 대 상 총 환자수는 860명으로, 그 중 562명은 infliximab을 투약 받았으며 298명의 환자는 위약 혹은 대조약을 투약 받았다.
10편의 논문 중 위약군을 대조군으로 설정한 논문이 7편, 활 성약(corticosteroid 약물)을 사용한 논문이 3편이었다. 수집된 논문 대상 환자의 중증도, 시험군과 대조군의 치료방법, 치료 효과 평가 시기 및 기준 등을 추출하여 Table 1에 요약하였 다. 대상환자는 중등도-중증 궤양성 대장염 환자였으며, corticosteroid 약물에 의존성 혹은 저항성이 있는 환자군을 포함하였다.
Fig. 1. Clinical literature search and selection process.
Table 1. Characteristics of randomized controlled trials included
Study Study group Control group No. of
pts Outcomes Criteria used to define remission Gustavsson et al.
201027)
Infliximab 4~5 mg/kg/day at week 0,
additional for clinical relapse Placebo 45 Colectomy, remis- sion, QoL at year 3
Mayo score of 1 SF-3642) or SHS43)-45)
Sandborn et al.
200928)
Infliximab 5 mg/kg/day,
10 mg/kg/day at weeks 0, 2, 6 and 8 week thereafter
Placebo 728
Colectomy, UC related hospitaliza- tion within 54 weeks
and beyond
Cumulated incedencd of patients with colectomy
Feagan et al.
200729)
Infliximab 5 mg/kg/day, 10 mg/kg/
day at weeks 0, 2, 6 and 8 week there- after
Placebo 728 QoL at week 8, 30 and 54
IBDQ46), SF-3642) (PCS, MCS)
Gavalas et
al.200730) Infliximab 5 mg/kg/day at weeks 0, 2 and 6 8 week thereafter
Methylprednisolone 0.8 ~ 1 mg/kg/day 3weeks, tapering
24
Clinical response, remission at 2-21
months
SEO score47), 48) and a SCCAIs49) <6 Jarnerot et al.
200531) Infliximab 4~5 mg/kg/day at week 0 Placebo 45 Colectomy, Remission at day 90
Clinical (Seo index47), 48)) and endoscopic remission Rutgeerts et al.
ACT1 200532)
Infliximab 5 mg/kg/day, 10 mg/kg/
day at weeks 0, 2, and68 week there- after
Placebo 364 Remission at week 8, 30, 54
Endoscopic remission (Mayo subscore of ≤1 at endoscopy) Rutgeerts et al.
ACT 2 200532)
Infliximab 5 mg/kg/day, 10 mg/kg/
day at weeks 0, 2 and 68 week there- after
Placebo 364 Remission at week 8, 30, 54
Endoscopic remission (Mayo subscore of ≤ 1 at
endoscopy)
Armuzzi et al.
200433)
Infliximab 5 mg/kg/day at weeks 0, 2 and 68 week thereafter
Methylprednisolone 0.7~1 mg/kg/day 1week,
tapering
20
Remission, colectomy at week
2, 8, every 8 week thereafter
Clinical remission (DAI score of < 3)
Ochsenkuhn et al.
200434)
Infliximab 5 mg/kg/day at weeks 0, 2 and 6
Prednisolone 1.5 mg/kg/
day 2week, tapering 13 Remission at 3, 13 week
Modified Truelove and Witts score decrease > 5 and to ≤ 10 Probert et al.
200335)
Infliximab 5 mg/kg/day, 10 mg/kg/
day at weeks 0, 2 Placebo 43 Remission,
QoL at week 6
UCSS 2 IBDQ46), EuroQol50) Sands et al.
200136)
Infliximab 5 mg/kg/day, 10 mg/kg/
day or 20 mg/kg/day at week 0 Placebo 11 Remission
at week 2, 12
Modified Truelove and Witts score of ≤ 4 and endoscopic
remission
*
QoL: Quality of Life
SF-36: Medical Outcomes Study 36-Item Short Form Health Survey SHS: Short Health Scale
IBDQ: Inflammatory Bowel Disease Questionnaire PCS: Physical component summary
MCS: Mental component summary
SCCAI: Simple Clinical Colitis Activity Index Scores DAI: Disease Activity Index
UCSS: Ulcerative colitis symptom score
유효성 분석
수집된 임상시험은 총 11개로, 10편의 논문으로 출판되었 으며, 해당 논문들을 대조군의 성격에 따라 위약 비교군 및 활성약 비교군으로 분류하여 관해 유도(임상적 반응(clinical response) 포함), 대장절제술 비율, 삶의 질 평가 등을 결과변 수로 분석하였다.
위약 비교군
관해 (remission) 유도
위약을 대조군으로 설정하여 infliximab의 관해 유도를 관찰 한 논문은 총 4개로 5개의 임상시험(Jarnerot et al., Rutgeerts et al. ACT 1, Rutgeerts et al. ACT 2, Probert et al., Sands et
al.)이 포함되어 있었다. 본 연구에서는 infliximab 투약 8주 이내에 나타나는 증상 및 조직학적 개선 효과를 ‘단기간 관 해 유도’, 그 이후에 지속되는 개선효과를 ‘장기간 관해 유 도’라 지칭하였다.32) 본 연구에 인용된 연구 중, 단기간 관해 유도를 관찰한 논문은 infliximab 투약 후 2~8주에, 장기간 관해 유도를 관찰한 논문은 투약 후 3~13달에 임상 증상 및 조직학적 개선 효과를 측정하여 보고하였다.
단기간 관해 유도를 관찰한 4개의 독립된 연구(Rutgeerts et al. ACT 1, Rutgeerts et al. ACT 2, Probert et al. Sands et al.)에서 치료군에 속하는 환자 총 515중 333명(65%)에서 infliximab 투약에 따른 관해가 관찰되었고, 대조군 267명 중 에서는 87명(33%)이 임상적 반응을 나타내었다. Odds ratio Table 2. Quality assessment of literatures by Jadad’s scale
Study Randomization Randomization assessment
Double blinding
Double blinding assessment
Withdrawals
and dropouts Jadad’s scale
Gustavsson et al. 2010 1 1 1 3
Sandborn et al. 2009 1 1 1 1 4
Feagan et al. 2007 1 1 1 1 4
Gavalas et al. 2007 1 1 2
Jarnerot et al. 2005 1 1 1 3
Rutgeerts et al. ACT 1, 2 2005 1 1 1 1 4
Armuzzi et al. 2004 1 1 2
Ochsenkuhn et al. 2004 1 1 1 3
Probert et al. 2003 1 1 1 1 4
Sands et al. 2001 1 1 1 3
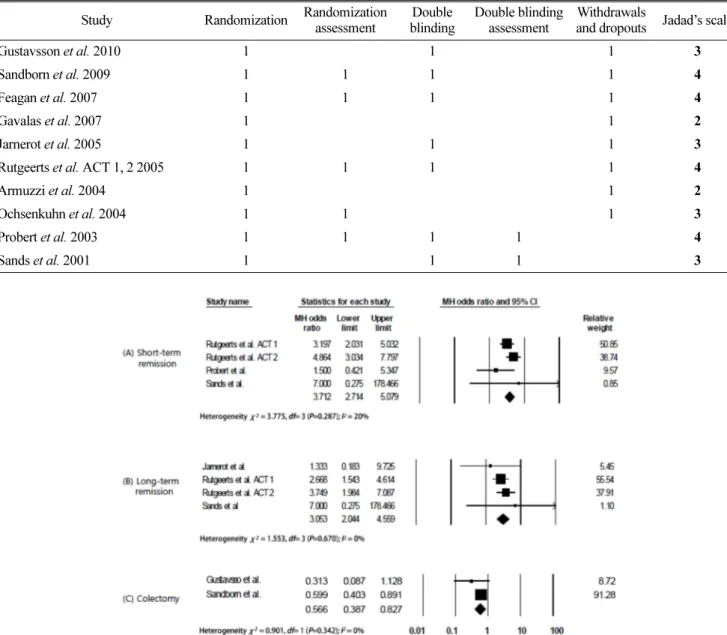
Fig. 2. Forest plot of the effect of short-term remission, long-term remission, and colectomy associated with placebo controlled studies. MH= Mantel Haenszel.
는 3.712 (2.714, 5.079)로 분석되었다(Figure 2).
궤양성 대장염 환자에서 infliximab의 장기간 관해 유도 효 과를 관찰한 4개의 연구(Jarnerot et al., Rutgeerts et al. ACT 1, Rutgeerts et al. ACT 2, and Sands et al.)에서 치료군 환 자 총 507명 중 168명(33%)에서 장기간 관해 유지가 관찰되 었고, 대조군 253명 중에서는 35명(14%)이 관해를 유지하였 다. Odds ratio는 3.053(95% CI: 2.044, 4.559)으로 분석되었 다. 따라서 위약을 대조군으로 하였을 때 infliximab의 장기간 관해 유도 효과는 통계적으로 유의미하게 크다(Figure 2).
대장절제술 비율 (colectomy rate)
궤양성 대장염의 수술적 치료를 결과변수로 관찰한 2개의 연구(Gustavsson et al., Sandborn et al.)에서 총 773명의 환자 를 대상으로 각각 infliximab 투여 1년, 3년 후 대장절제 여부 를 위약 대조군과 비교하였다. 치료군 총 508명의 환자 중 81 명(16%)의 환자가 대장절제술을 받았고, 대조군에서는 265명 중 69명(26%)이 대장절제술을 받은 것으로 나타났다. Odds ratio는 0.566 (95% CI: 0.387, 0.827)로 나타나, 위약 대조군과 비교했을 때, infliximab으로 치료한 환자를 1년 이상 장기간 모니터링 결과 대장절제술 예방효과가 있다(Figure 2).
삶의 질 평가(quality of life, QoL)
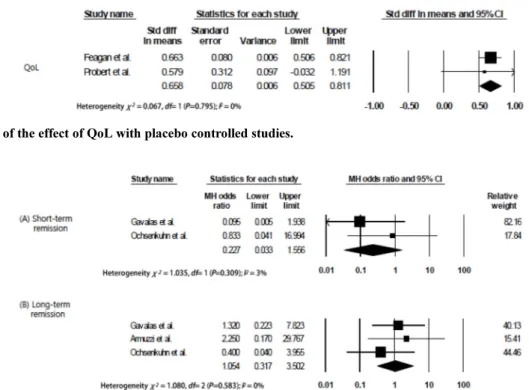
위약을 대조군으로 한 연구 2편(Feagan et al, Probert et al.)에서 inflammatory bowel disease questionnaire (IBDQ)37)를 이용하여 삶의 질을 평가 하였다. Odds ratio는 0.658 (95%
CI: 0.505, 0.811)로 제시되어, 위약 대조군에 비하여 IFX 치 료군이 삶의 질을 높이는 결과가 나타났다(Figure 3).
활성약 비교군
단기간 및 장기간 관해 (remission) 유도
중증 궤양성 대장염 환자 중에서 corticosteroid를 장기간 사 용하였거나 다른 이유로 steroid 사용을 지속해야 하는 환자군 에서 활성약을 대조군으로 설정한 연구가 3편 있었다(Gavalas et al., Armuzzi et al., Ochsenkuhn et al). 이 연구들은 corticosteroid 정맥주사를 대조약으로 설정하여 infliximab의 단기간 및 장기간 관해 유지 효과를 비교하였다. 위약 비교군에서와 동일하게 infliximab 투약 8주 이내에 나타나는 증상 및 조직학적 개선 효과를 ‘단기간 관해 유도’, 그 이후에 지속되는 개선효과를
‘장기간 관해 유도’로 분류하여 분석하였다. 단기간 관해 유 도는 infliximab 투약 후 2~8주에, 장기간 관해는 13주~21달 에 임상 증상 및 조직학적 개선 효과가 보고되었으며 이를 종합하여 분석하였다.
이 때 단기간 관해 유도에서 한편의 연구(Armuzzi et al.)에 서는 치료군과 대조군 환자 전체에서 단기간 관해가 유도되 어 다른 2편으로 odds ratio를 구하였고, 이는 0.227(95% CI:
0.033, 1.556)으로 나타났다(Figure 4). 또한 13주 이상 이후에 관해 유도 효과를 관찰하였을 때에는 세편의 논문으로 분석 가능 하였으며, odds ratio는 1.054(95% CI: 0.317, 3.502)으로 나타났다. 따라서 단기간, 장기간 관해 유도 효과 모두 corticosteroid 정맥주사 요법과 통계학적으로 동등하게 분석되
Fig. 3. Forest plot of the effect of QoL with placebo controlled studies.
Fig. 4. Forest plot of the effect of short-term remission and long-term remission associated with corticosteroid controlled studies.
MH= Mantel Haenszel.
었다(Figure 4).
안전성 분석
위약을 대조군으로 한 5개의 연구에서(Table 3), 그리고 활 성약을 대조군으로 한 3개의 연구에서 infliximab의 약물유 해반응(adverse drug reaction, ADR)을 보고하였다. 위약을 대조군으로 하는 연구에서 any adverse reactions, infections, infusion reaction, rash, arthralgia에 대한 약물유해반응을 분 석하였고 모든 약물유해반응의 빈도가 두 군에서 유사한 것 을 확인하였다(Table 3).
반면 활성약을 대조군으로 진행된 연구에서 infliximab의 약 물유해반응을 분석하였을 때, infliximab군에서는 rash 등 경미 한 사례 보고였으며 corticosteroid 정맥주사 요법 환자군에서는 15명 중 11명(73.3%)에서 moon face를 동반한 Cushing-like syndrome을 경험하였고, 1명은 steroid-associated psychiatric disorder를 나타내었다.
민감도 분석 및 Publication Bias
민감도 분석 결과 그 현저한 차이가 나타나지 않았고, 3개 이상의 분석 그룹에서 모든 publication bias를 분석하였을 때, funnel plot 역시 명확한 비대칭을 보여주지 않았다. Begg’s test와 Egger’s test 모두에서 publication bias가 나타나지 않았 다(data not shown).
고 찰
메타분석은 기존의 연구들을 기초하면서 객관적인 결론을 유도하고자 하는 방법론으로, 1954년 Lasagna et al.에 의해 공식적인 메타분석 결과가 처음으로 발표된 이후 국내 및 국제 의약학연구에 널리 활용되고 있다.38-39) 현재까지 수행 된 중등도-중증 궤양성 대장염 환자에서 infliximab의 효능에 대한 체계적 문헌고찰 선행 연구를 통해, 대조군과 비교한 치료군에서 추가적인 관해 유도 및 대장절제술 감소 효과를 확인하였다. 본 연구에서는 각 연구의 목적과 디자인을 분석 하여, 연구 기간, 대조군의 성격, 결과 변수의 성격 등에 따 라 subgroup analysis 함으로써 개별적 효과를 분석하고자 하였다.
염증성 장질환에 대한 생물학적 치료제의 효과를 분석한 Ford AC(2011) 등의 연구에서, infliximab이 위약에 비해 관 해 유도에 효과가 더 좋은 것으로 평가되었다(RR = 0.72; 95
% CI 0.57-0.91).40) 본 연구에서도 역시 infliximab은 중등도- 중증 궤양성 대장염 환자에게 위약 대조군에 비하여 단기간 (OR = 3.712. 95% CI 2.714, 5.079) 및 장기간 관해 유지 (OR = 3.053. 95% CI 2.044, 4.559)효과를 나타내는 것으로 분석되었다.
Huang X et al. (2011)의 연구에서 투약 후 90일, 12주, 54주 이내의 대장절제술의 비율을 통합하여 분석하였으며, 대조군에 비해 infliximab 투여군에서 대장절제술이 감소하는 것으로 보고하였다(OR = 0.31; 95 % CI 0.20, 0.48).41) 이에 본 연구에서는 장기간 투약 후(1년~3년) 대장절제술의 감소 정도를 대조군과 비교하여 관찰하였으며, OR = 0.566(95%
CI: 0.387, 0.827)로 대장절제술을 감소시키는 것으로 분석되 었다. 이는 1년 이내의 대장절제술을 분석한 기존의 연구보 다 효과가 적은 것으로 보이며, infliximab 투약 후 1년~3년 에는 대장절제술 감소 효과가 단기간의 효과와 비교하였을 때 낮아지는 것으로 사료된다.
염증성 장질환에 대한 삶의 질 평가 기준으로 질병의 활성 정도와도 상관관계가 있는 것으로 알려진 IBDQ(Inflammatory Bowel Disease Questionnaire)로 분석하였을 때 대장절제술이 필요한 환자군의 경우 그렇지 않은 군에 비하여 IBDQ가 현 저히 낮음이 입증되었다.46) 그러나 Huang X et al. (2011)의 연구에서는 중등도-중증 궤양성 대장염 환자에서 infliximab 의 삶의 질 개선에는 효과가 현저히 나타나지 않았다.41)그 러나 본 연구에서 IBDQ로 삶의 질을 평가한 논문들을 종합 하여, 중등도-중증 궤양성 대장염 환자에서 infliximab 투약 군이 대조군 환자군에 비해 삶의 질 개선효과를 분석하였을 때, infliximab 투약군에서 IBDQ의 개선 정도는 0.658(95%
CI: 0.505, 0.811)로 입증되었다.
현재까지 수행된 체계적 고찰에서는 corticosteroid 대조군 연구를 분석에 포함하지 않거나40), 혹은 위약 대조군 연구와 통합하여 분석하였다.41) 그러나 위약 대조군과 활성약 대조군 을 함께 분석하는 경우에는, 치료군 약물의 효능이 보다 객관 적으로 평가되기 어렵다. 따라서 본 연구에서는 corticosteroid 에 의존적인 궤양성 대장염 환자군에서 corticosteroid를 대조 Table 3. Adverse events with infliximab vs. placebo in inducing remission in moderate – severe UC
ADR Trials (n) ADR experiencing pts / total pts
RR 95% CI
infliximab group placebo group
Any 3 420 / 492 196 / 247 1.08 (0.999, 1.157)
Infection 4 67 / 522 29 / 270 1.20 (0.792, 1.800)
Arthralgia 3 70 / 499 25 / 250 1.40 (0.911, 2.157)
Rash 3 30 / 199 13 / 250 1.16 (0.614, 2.177)
Infusion reaction 5 56 / 530 24 / 273 1.20 (0.762, 1.895)
군으로 설정한 연구들을 따로 분류하여 분석하였고, 그 결과 단기간, 장기간 모두 infliximab 투여군과 corticosteroid 투여 군에서 동등한 정도의 관해 유도 효과를 나타내었다. 따라서 corticosteroid 의존적인 환자군에서도, infliximab 투여에 따른 효과가 corticosteroid군에 비교하여 동등한 임상적 관해 유도 효과를 갖는 것으로 해석된다.
한편, 활성약 대조군 시험인 Gavalas et al.과 Ochsenkuhn et al.에서 corticosteroid IV 투여군에서 Cushing-like syndrome 이 73.3% 보고되었고, 1명의 환자에서 steroid-associated psychiatric disorder가 보고되었다. Corticosteroid 투약에 따른 정신병(psychosis)과 Cushing-like syndrome뿐만 아니라 골다공 증, 고혈압, 당뇨 등의 부작용은 여러 연구를 통하여 잘 알려 져 있다.51-52)또한 위약을 대조군으로 한 연구에서 infliximab 사용에 따른 부작용을 분석하였을 때에는, 위약 대조군과 치료 군 간의 유의한 차이는 관찰되지 않았다. 따라서 안전성과 유효성을 동시에 고려하였을 때, 중등도-중증 궤양성 대장염 환자의 치료에서 infliximab의 활용도는 steroid 의존적인 환 자군을 포함할 수 있을 것으로 보인다.
Infliximab는 국내에서 corticosteroid나 6-mercaptopurine 또 는 azathioprine 등 보편적인 치료 약재에 대해 적정한 반응 을 나타내지 않거나 내약성이 없는 경우 또는 이러한 약제 가 금기인 중등도-중증의 궤양성 대장염에 사용이 허가되었 다. Infliximab의 도입으로 궤양성 대장염의 증상완화뿐만 아 니라, 질병의 경과 변화가 가능성을 보인 만큼, 본 연구에서 는 해당 약물의 실질적 효과를 분석하여 그 유익성을 분석하 고자 하였다. Infliximab은 중등도-중증 궤양성 대장염 환자에 게 위약 대조군에 비하여 단기간(OR = 3.712 2.714, 5.079) 및 장기간 관해 유지(OR = 3.053. 95% CI 2.044, 4.559)효과를 나타냈으며, 삶의 질을 향상시키고, 대장절제술에도 감소효과 가 있는 것으로 분석되었다. 또한, corticosteroid 의존성이 있 는 궤양성 대장염 환자군에서도, 관해 유지는 동등한 것으로 평가되어 infliximab의 활용도를 더 넓힐 수 있을 것으로 사 료된다.
그러나 현재 국내뿐만 아니라 국제적으로도 infliximab 사 용에 대한 경험과 연구 발표 결과가 아직 충분히 축적되지 않은 시점에 있다. 또한 인용된 10편의 논문 각각 환자군의 선정과 질병 진단 방법 등의 다양성으로 인하여 본 연구 결 과 활용의 한계점이 있다. 더 광범위하고 다양한 환자군을 포함한 임상 대조 시험이 발표되는 시점에 infliximab의 유 효성과 안전성을 더 면밀히 평가해볼 수 있을 것으로 기대 한다.
참고문헌
1. Lakatos PL. Recent trends in the epidemiology of inflammatory bowel diseases: up or down? World J Gastroenterol. 2006; 12:
6102-6108.
2. Kornbluth A, Sachar DB. Practice Parameters Committee of the American College of Gastroenterology. Ulcerative colitis practice guidelines in adults (update): American College of Gastroenterology, Practice Parameters Committee. Am J Gastroenterol. 2004; 99: 1371-1385.
3. Willert RP, Lawrance IC. Use of infliximab in the prevention and delay of colectomy in severe steroid dependent and refractory ulcerative colitis. World J Gastroenterol. 2008; 14:
2544-2549.
4. Järnerot G, Rolny P, Sandberg-Gertzén H. Intensive intravenous treatment of ulcerative colitis. Gastroenterology.
1985; 89: 1005-1013.
5. Lichtiger S, Present DH, Kornbluth A, et al., Cyclosporine in severe ulcerative colitis refractory to steroid therapy. N Engl J Med. 1994; 330: 1841-1851.
6. Laharie D, Bourreille A, Branche J. et al., Cyclosporin versus infliximab in severe acute ulcerative colitis refractory to intravenous steroids: A randomized trial. Gastroenterology.
Conference: Digestive Disease Week, DDW 2011 Chicago, IL United States. Conference Publication: (var.pagings). 140 (5 SUPPL. 1) (pp S112), 2011.
7. Arts J, D'Haens G, Zeegers M, et al., Long-term outcome of treatment with intravenous cyclosporine in patients with severe ulcerative colitis. Inflamm Bowel Dis. 2004; 10: 73- 78.
8. Pham CQ, Efros CB, Berardi RR. Cyclosporine for severe ulcerative colitis. Ann Pharmacother. 2006; 40: 96-101.
9. Van AG, Vermeire S, Rutgeerts P. Treatment of severe steroid refractory ulcerative colitis. World J Gastroenterol.
2008; 14: 5508-5511.
10. Kim SH, Kim KI, Yun HY, et al., Population Pharmacokinetics of Cyclosporine after Hematopoietic Stem Cell Transplanta- tion in Leukemic Patients. Kor J Clin Pharm. 2010; 20: 9-16.
11. Shibolet O, Regushevskaya E, Brezis M, et al., Cyclosporine A for induction of remission in severe ulcerative colitis.
Cochrane Database Syst Rev. 2005; CD004277.
12. Penna C, Dozois R, Tremaine W, et al., Pouchitis after ileal pouch-anal anastomosis for ulcerative colitis occurs with increased frequency in patients with associated primary sclerosing cholangitis. Gut. 1996; 38: 234-239.
13. McIntyre PB, Pemberton JH, Wolff BG, et al., Comparing functional results one year and ten years after ileal pouch- anal anastomosis for chronic ulcerative colitis. Dis Colon Rectum. 1994; 37: 303-307.
14. Hahnloser D, Pemberton JH, Wolff BG, et al., The effect of aging on function and quality of life in ileal pouch patients: a single cohort experience of 409 patients with
chronic ulcerative colitis. Ann Surg. 2004; 240: 615-621.
15. Ording OK, Juul S, Berndtsson I, et al., Ulcerative colitis:
female fecundity before diagnosis, during disease, and after surgery compared with a population sample. Gastroenterology.
2002; 122: 15-19.
16. Kim KO, Jang BI Jang. Emerging Drugs in the Treatment of Inflammatory Bowel Disease: Beyond Anti-TNF-α.
Korean J Gastroenterol. 2011; 58: 235-244.
17. Papadakis KA, Targan SR. Tumor necrosis factor: biology and therapeutic inhibitors. Gastroenterology. 2000; 119:
1148-1157.
18. Hove T, Montfrans C, Peppelenbosch MP, et al., Infliximab treatment induces apoptosis of lamina propria T lymphocytes in Crohn’s disease. Gut. 2002; 50: 206-211.
19. Rutgeerts P, Van Assche G, Vermeire S. Optimizing anti-TNF treatment in inflammatory bowel disease. Gastroenterology.
2004; 126: 1593-1610.
20. Travassos WJ, Cheifetz AS. Infliximab: Use in Inflammatory Bowel Disease. Curr Treat Options Gastroenterol. 2005; 8:
187-196.
21. Regueiro M, Curtis J, Plevy S. Infliximab for hospitalized patients with severe ulcerative colitis. J Clin Gastroenterol.
2006; 40: 476-481.
22. Yamamoto-Furusho JK, Uzcanga LF. Infliximab as a rescue therapy for hospitalized patients with severe ulcerative colitis refractory to systemic corticosteroids. Dig Surg. 2008; 25:
383-386.
23. Talley NJ, Abreu MT, Achkar JP, et al., An evidence-based systematic review on medical therapies for inflammatory bowel disease. Am J Gastroenterol. 2011; 106: S2-S25.
24. Jadad AR, Carroll D, Jenkinson C, et al., Assessing the quality of reports of randomized clinical trials: is bliniding necessary? Control Clin Trials. 1996; 17: 1-12.
25. Clark HD, Wells GA, Huët C, et al., Assessing the quality of randomized trials: reliability of the Jadad scale. Control Clin Trials. 1999; 20: 448-452.
26. Cochran WG. The combination of estimates from different experiments. Biometrics. 1954; 10: 101-129
27. Gustavsson A, Jarnerot G, Hertervig E, et al., Clinical trial:
colectomy after rescue therapy in ulcerative colitis 3-year follow-up of the Swedish-Danish controlled infliximab study. Aliment Pharmacol Ther. 2010; 32: 984-989.
28. Sandborn WJ, Rutgeerts P, Feagan BG, et al., Colectomy rate comparison after treatment of ulcerative colitis with placebo or infliximab. Gastroenterology. 2009; 137: 1250- 1260.
29. Feagan BG, Reinisch W, Rutgeerts P et al., The effects of
infliximab therapy on health-related quality of life in ulcerative colitis patients. Am J Gastroenterol. 2007; 102:
794-802.
30. Gavalas E, Kountouras J, Stergiopoulos C, et al., Efficacy and safety of infliximab in steroid-dependent ulcerative colitis patients. Hepatogastroenterology. 2007; 54: 1074- 1079.
31. Jarnerot G, Hertervig E, Friis-Liby I, et al., Infliximab as rescue therapy in severe to moderately severe ulcerative colitis: a randomized, placebo-controlled study. Gastroenterology 2005;
128: 1805-1811.
32. Rutgeerts P, Sandborn WJ , Feagan BG, et al., Infliximab for induction and maintenance therapy for ulcerative colitis.
N Engl J Med. 2005; 353: 2462-2476.
33. Armuzzi A, De Pascalis B, Lupascu A. et al., Infliximab in the treatment of steroid-dependent ulcerative colitis. Eur Rev Med Pharmacol Sci. 2004; 8: 231-233.
34. Ochsenkühn T, Sackmann M, Göke B. Infliximab for acute, not steroid-refractory ulcerative colitis: a randomized pilot study. Eur J Gastroenterol Hepatol. 2004; 16: 1167- 1171.
35. Probert CJ, Hearing SD, Schreiber S, et al., Infliximab in moderately severe glucocorticoid resistant ulcerative colitis:
a randomised controlled trial. Gut. 2003; 52: 998-1002.
36. Sands BE, Tremaine WJ, Sandborn WJ, et al., Infliximab in the treatment of severe, steroid-refractory ulcerative colitis: a pilot study. Infl amm Bowel Dis. 2001; 7: 83-88.
37. Irvine EJ. A quality-of-life index for inflammatory bowel disease. Can J Gastroenterol. 1993; 7: 155-159.
38. Egger M, Davey SG. Meta-analysis: potentials and premise.
BMJ. 1997; 315: 1371-1374.
39. Choi YY, Sohn HY, Shin HT. Clinical Benefits of Self- monitoring of blood glucose in non-insulin treated patients with type 2 diabetes: a systematic review and meta- analysis. Kor J Clin Pharm. 2010; 20: 183-192.
40. Ford AC, Sandborn WJ, Khan KJ, et al., Efficacy of biological therapies in inflammatory bowel disease:
systematic review and meta-analysis. Am J Gastroenterol 2011; 106: 644-659.
41. Huang X, Lv B, Jin HF, et al., A meta-analysis of the therapeutic effects of tumor necrosis factor-α blockers on ulcerative colitis. Eur J Clin Pharmacol. 2011;67:759-766 42. Samsa G, Edelman D, Rothman ML, et al., Determining
clinically important differences in health status measures: a general approach with illustration to the health utilities index mark II. Pharmacoeconomics. 1999; 15: 141-155.
43. Hjortswang H, Jarnerot G, Curman B, et al., The Short
Health Scale: a valid measure of subjective health in ulcerative colitis. Scand J Gastroenterol. 2006; 41: 1196- 1203.
44. Sullivan M, Karlsson J, Ware JE Jr. The Swedish SF-36 Health Survey – I. Evaluation of data quality, scaling assumptions, reliability and construct validity across general populations in Sweden. Soc Sci Med. 1995; 41: 1349-1358.
45. Taft C, Karlsson J, Sullivan M. Performance of the Swedish SF-36 version 2.0. Qual Life Res. 2004; 13: 251- 256.
46. Irvine EJ, Feagan B, Rochon J, et al., Quality of life: a valid and reliable measure of therapeutic efficacy in the treatment of inflammatory bowel disease. Canadian Crohn's Relapse Prevention Trial Study Group. Gastroenterology. 1994; 106:
287-296.
47. Walmsley RS, Ayres RC, Pounder RE, et al., A simple
clinical colitis activity index. Gut. 1998; 43: 29-32.
48. Seo M, Okada M, Maeda K, et al., Correlation between endoscopic severity and the clinical activity in ulcerative colitis. Am J Gastroenterol. 1998; 93: 2124-2129.
49. Higgins PD, Schwarts M, Mapili J, et al., Is endoscopy necessary for the measurement of disease activity in ulcerative colitis? Am J Gastroenterol. 2005; 100: 355-361.
50. Williams A. EuroQol-a new facility for the measurement of health-related quality of life. Health Policy. 1990; 16:
199-208.
51. Gurwitz JH, Bohn RL, Glynn RJ, et al., Glucocorticoids and the risk for initiation of hypoglycemic therapy. Arch Intern Med. 1994; 154:97-101.
52. Clowes JA, Peel N, Eastell R. Glucocorticoid-induced osteoporosis. Curr Opin Rheumatol. 2001; 13:326-332.