혈액투석 접근로 구제요법으로서의 약물방출 풍선카테터
황진호, 박상우
건국대학교 의학전문대학원 건국대학교병원 영상의학교실
Drug Coated Balloon for Vascular Access Salvage
Jin Ho Hwang, Sang Woo Park
Department of Radiology, Konkuk University Medical Center, Konkuk University School of Medicine, Seoul, Korea
서 론
장기적인 투석로 확보를 위해서는 자가혈관 동정맥루(arterio
venous fistula, AVF) 혹은 인조혈관 동정맥루(arteriovenous graft, AVG)가 필요하다. 하지만 혈액투석로에 발생하는 협착은 투석로 기 능이상을 초래하게 되는데, 이는 대부분 자가혈관의 경우 문합부 주 위 정맥, 인조혈관의 경우 인조혈관-정맥 문합부에 발생하는 신생 내 막증식증(neointimal hyperplasia, NIH)이 원인이 된다[1].
경피경관혈관성형술(percutaneous transluminal angioplasty, PTA) 은 혈액투석로 협착을 치료하기 위해 선호하는 방법이다. 하지만, 혈 관성형술 후 6개월 누적 개통률은 2338% 밖에 되지 않으며[2], 이를 극복하기 위해 cutting balloon, cryoplasty를 이용한 혈관확장술에 대 해 연구가 이루어졌지만, 일반 풍선을 사용한 혈관확장술에 비해 개 통률이 개선되지 않았다[3,4]. 2010년에 발표된 연구에서는 인조혈관 정맥문합부 협착에 대해 stent graft를 사용하는 것이 전통적인 혈관 성형술의 유효한 대안이 될 수 있을 것이라고 했으며, 6개월 개통률
은 51%로 높게 보고되었다[5].
Metallic scaffold를 혈관 내에 삽입하는 것은 혈관 벽에 지속적인 염증반응과 기계적 자극을 초래하는 것으로 알려져 있어서 영구적인 scaffold 없이 투석로 협착을 치료하는 방법에 관심도가 증가하게 되 었다[6]. 약물코팅풍선(drugcoated balloon, DCB)을 사용한 혈광성형 술은 초기에 관상동맥과 하지동맥질환에 사용되었으며, NIH를 억제 하여 비코팅 풍선(uncoated balloon)보다 더 적은 재협착 빈도를 보여 주었다[79]. DCB를 혈액투석로 협착에 적용하려는 시도는 관상동 맥, 하지동맥질환에서 효과를 보이는 것처럼 AVF와 AVG의 동맥화 된 정맥에도 유사하게 작용할 것이라는 기대에서 시작되었다.
본 종설에서는 혈액투석로 협착의 원인과 기존 치료방법들을 살 펴보고, 최근 관심을 받고 있는 DCB에 대한 소개와 더불어 혈액투석 로 적용 연구결과들에 대해 정리해보고자 한다.
Received: Oct 11, 2019, Revised: Nov 1, 2019, Accepted: Nov 15, 2019 책임저자 : 박상우
우 05030, 서울시 광진구 능동로 120-1, 건국대학교 의학전문대학원 건국대학교병원 영상의학교실 Tel: 02-2030-5487, Fax: 02-2030-5549, E-mail: psw0224@kuh.ac.kr
*본 종설은 2019년 6월 16일 대한투석혈관학회 및 대한중재신장학연구회 제1회 공동 심포지엄에서 발표한 내용을 추가 편집하였습니다.
Maintaining vascular access (VA) is very important for hemodialysis (HD) patients. Neointimal hyperplasia (NIH) in VA frequently develops, which may lead to its thrombosis or abandonment sometimes. The choice as a primary treatment of HD VA is the use of high pressure balloon percutaneous angioplasty. However, restenosis rates are also very high.
Drug-coated balloon (DCB) delivering a paclitaxel has proven its usefulness in treating coronary and peripheral artery lesions. Paclitaxel reduces NIH so its use in HD VA can also be an attractive option. Here, we will summarize the basic conception of DCB and the recent DCB trials in HD VA.
Key Words: Hemodialysis, Stenosis, Drug-coated balloon
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Copyright © The Korean Society for Dialysis Access | eISSN: 2635-8603
본 론
1. 신생 내막증식증(Neointimal hyperplasia)
혈관성형술 이후 일어나는 조직반응은 동맥과 투석로 혈관이 유 사한 것으로 보인다. 효과적인 혈관성형술이 되려면 풍선카테터가 intimal layer, internal elastic lamina, 그리고 tunica media 일부까지 찢 어야 하는데, 이는 협착이 있는 혈관에서 탄성 반동이 일어나는 것을 막기 위함이다. 하지만, 이런 혈관벽 구조의 손상에 대응해서 복구하 려는 후속 반응으로 NIH가 일어나게 되며, 결국 혈관성형술 후 시간 이 지남에 따라 재협착이 발생하게 된다.
혈관벽이 손상되면 손상된 혈관내피세포와 혈관평활근세포 (smooth muscle cell, SMC)는 중막에서 SMC의 증식을 촉진하는 basic fibroblast growth factor (bFGF)와 같은 성장인자를 방출한다. 또 한, 혈소판에서 분비된 혈소판유리성장인자(plateletderived growth factor, PDGF)는 혈관 손상을 입은 부위에 달라붙어 중층에서 내층 으로 SMC의 이동을 촉진한다. SMC는 세포외기질을 신생내막에 분 비하게 되어서 결국 신생내막층은 연속된 내피세포층에 덥힌 SMC, macrophage, lymphocyte, collagen, elastin, proteoglycan으로 구성된 다. 완전한 내막층이 형성되면 내피세포에서 nitric oxide와 heparin sulfate를 분비해서 신생내막 형성 과정도 끝나게 된다.
혈액투석로는 고압력 유체를 저압력 기관으로 보내는 비생리적인 직통 도관이므로 독특한 혈역학적 특성이 있다. 높은 shear stress, 와 류, 동맥-정맥 혹은 인조혈관-정맥 사이에 탄성 불일치는 완전한 내 피층을 형성하더라도 NIH 발생을 지속적으로 촉진하려고 한다[10].
2. 투석로 재협착을 막기 위한 전략(Strategies against dialysis access restenosis)
NIH에 따른 재협착 문제를 줄이기 위해 다양한 치료방법들이 시 도되었다. 혈관성형술 과정에서 internal elastic lamina의 파열은 SMC 증식과 이동의 중요한 방아쇠 역할을 하기 때문에, cutting balloon을 사용하여 낮은 압력으로 잘 조정된 혈관 벽 절개를 가해서 지나친 압 력으로 인한 혈관 벽 파열을 막으려고 시도한 연구가 있었다. 하지 만, 340명의 협착 혹은 혈전성 폐쇄를 가진 AVG 환자들을 대상으 로 한 무작위대조시험에서 6개월 표적병변 개통률은 cutting balloon/
conventional balloon (47.9%/40.5%, p=.373)으로 의미 있는 차이가 없 었다[3].
Cryoplasty의 경우 nitrous oxide를 사용하여 풍선을 확장시키면 주변 혈관 조직이 –10℃까지 냉각되어 apoptosis가 일어나게 된다. 하
지만, AVF 혹은 AVG를 가진 20명의 환자들을 대상으로 한 예비연구 에서 6개월 개통률은 25%에 불과했으며, 모든 환자들이 진정치료 상 태에서 풍선확장술을 진행했음에도 불구하고 통증점수(visual analog scale) 710점 정도로 심한 통증을 호소했다[4].
Radiation은 apoptosis를 촉진해서 NIH를 억제하는 것으로 알려 져 있다. 하지만, BRAVO II trial에서는 thrombosed AVG 환자에 대해 radiation군의 3개월 개통률이 51.7%로 대조군의 50%과 차이가 없는 것으로 보고했다(p=1.00) [11].
Bare metal stent (BMS)는 혈액투석로에서 중심정맥협착증에 대 해 혈관확장술 후 탄성반동이 발생했을 때 bailout 전략으로 흔히 사 용하고 있다. 최근에는 혈전제거술 후 인조혈관-정맥 문합부 협착에 대해 PTA 단독 혹은 PTA+BMS를 비교한 연구에서, 6개월, 12개월 개통률이 63%, 49% (PTA+BMS), 24%, 14% (PTA 단독) (p<0.001)으 로 PTA+BMS군에서 더 좋은 결과를 보인 보고도 있다[12].
Haskal 등은 인조혈관-정맥 문합부 협착 치료를 위해 stent graft 를 사용한 무작위대조시험에서 6개월 개통률이 단순 풍선확장술에 비해 더 좋은 것으로 보고했는데(51% vs. 23%, p<0.001), stent graft 를 설치하면 수술로 endtoside 문합을 했던 부위가 endtoend 문 합으로 바뀌면서 혈류의 흐름이 laminar flow로 전환되어 결과적으로 turbulent flow와 shear stress를 줄일 수 있기 때문에 좋은 결과를 보여 줄 수 있었다고 언급했다[5].
3. 약물코팅풍선의 개념(Concepts of DCBs)
DCB는 풍선 플랫폼과 풍선의 외표면에 위치하는 약물, 그리고 약물을 풍선에 결합시키는 역할을 하는 excipient, 이 세 개의 구성요 소로 이루어져 있다. DCB에 사용되는 풍선은 혈관성형술 그 자체의 의미보다는 혈관성형술용 풍선의 보조역할로 성공적인 혈관성형술 후에 혈관벽에 약물을 전달하는 것을 목적으로 한다.
DCB에 주로 사용하는 약제는 paclitaxel로 세포증식억제 작용 을 하는 항종양물질이며, βtubulin에 결합하여 중합된 세포미세관 (microtubule)을 안정화시키는 역할을 한다. 최근 10년 간 다양한 말 초혈관용 DCB가 출시되었으며(Table 1), 모두 paclitaxel (23.5 mg/
mm2)이 코팅되어 있다[9].
Paclitaxel로 치료한 세포는 미세관이 비정상적이고 체계적이 지 못한 상태가 되며, 상피모양유사세포 형태를 초래하게 되어 세 포 재복제와 이동이 불가능하다. 세포주기의 M phase를 억제하며 apoptosis를 유발하여 내막증식을 억제한다. Paclitaxel은 친지질성 (lipophilic)이므로 소수성(hydrophobic) 세포막 장벽을 쉽게 통과할 수 있어서 세포에 빠르게 흡수된다. 따라서 저용량의 paclitaxel이라
Table 1. Currently available drug-coated balloons for peripheral arterial disease in Korea
Name IN.PACT Lutonix Passeo-18 Lux Ranger
Company Medtronic Bard (BD) Biotronik Boston Scientific
Drug Paclitaxel Paclitaxel Paclitaxel Paclitaxel
Dose (mg/mm2) 3.5 2 3 2
Excipient Urea Polysorbate+sorbitol BTHC Citrate ester
도 SMC에 대해 지속적인 항증식효과를 기대할 수 있으며, 내막세포 보다는 SMC의 증식억제 효과가 더 심하기 때문에 내막층 치유라는 관점에서 바람직할 수 있다. 하지만, 동맥경화와 달리 투석 동정맥루 에서는 비생리적 혈역학 때문에 혈관벽 스트레스가 계속되어 국소 약물 전달의 이점이 적을 수도 있다[10].
DCB의 혈관벽 접촉 시간은 풍선팽창시간(약 3분)으로 제한되 어 있기 때문에 빠르고 균일한 약물 전달이 매우 중요하다. 효과적 인 약물 전달을 위해 urea, polysorbate and sorbitol, butyryltrihexyl citrate, citrate ester와 같은 다양한 excipient가 paclitaxel에 붙어서 약 물이 혈관 벽에 균일하게 전달될 수 있도록 해준다.
4. 현재 약물코팅풍선의 투석로 적용 연구결과(Current results of DCBs in dialysis access)
관상동맥과 하지동맥 병변에 대한 DCB 치료의 고무적인 결과들 이 보고되었음에도 불구하고 이 결과를 투석로 병변에 적용하는 것 에 대해서는 논란이 있었다. 투석로에 문제가 생기는 병변은 정맥에 위치하는데, 정맥은 internal elastic lamina가 동맥에 비해 구조적으로 덜 명확하기 때문에 SMC와 myofibroblast가 중막에서 내막으로 더 잘 이동하게 되어 협착이 훨씬 빠르게 발생하는 것으로 알려져 있기 때문이다[7].
하지만, 2012년 Katsanos 등이 failing AVF 혹은 AVG 정맥 협착 병변에 대해 풍선확장술 시에 DCB군(70%)이 plain balloon군(25%) 에 비해 6개월 개통률이 더 좋은 것으로 보고한 이후[13], Kitrou 등 도 failing AVF에 대해 DCB와 noncoated balloon을 비교한 연구결과
에서 target lesion revascularization (TLR)free survival (308 days vs.
161 days, p=.03)과 access circuit primary patency (270 days vs. 161 days, p=.04) 모두 DCB에서 나은 결과를 보고했다[14]. 2015년에는 Kitrou 등이 2012년 발표된 Katsanos 등의 6개월 중간 결과 보고 후 최종 결과를 발표했는데, 표적병변 1년 누적개통률이 DCB군에서 plain balloon군에 비해 높으며(35% vs. 5%, p<0.001), median primary patency는 0.64년/0.36년(p<0.0007)으로 DCB군이 더 길고, 경제적인 유용성도 있다고 하였다[15].
투석로 협착 환자들에 대해 DCB 풍선확장술을 시행한 연구들을 종합한 메타분석(Table 2) 결과 역시 DCB군이 plain balloon군에 비해 6개월 누적 개통률(71% vs. 49.2%) 및 12개월 누적 개통률(44.2% vs.
20.6%)에 대해 나은 결과를 보였다[7].
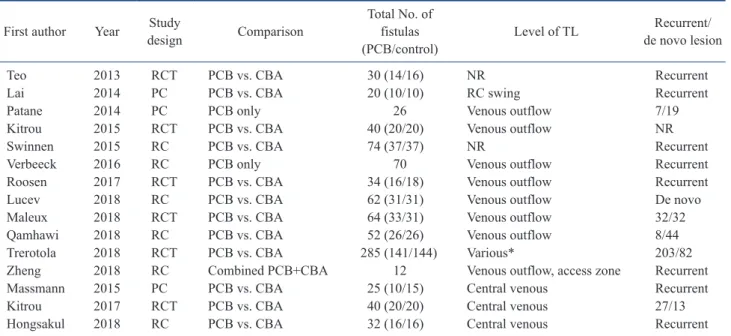
중심정맥 협착증에 필요한 풍선 직경은 1014 mm에 이르는데, 2017년에 FDA 승인을 받은 DCB (Lutonix AV)의 경우 풍선 직경이 12 mm까지 상용화 되어있다. Kitrou 등은 이 풍선을 이용하여 혈액 투석 환자에서 증상이 있는 중심정맥 협착증에 대해 치료한 무작위 대조시험 결과를 발표했으며, DCB군(179 days)이 고식적 풍선을 사 용한 군(124.5 days)에 비해 clinicallyassisted interventionfree period 에 대해 좋은 결과를 보이는 것으로 보고했다[16]. 또한, 중심정맥협 착증에 대한 메타분석 결과 역시 6개월 개통률(60.3% vs. 22.1%), 12 개월 개통률(41.2% vs. 10.3%) 모두 DCB 군에서 나은 결과를 보여주 었다(Fig. 1) [7].
투석로 풍선확장술 시에는 15 atm 이상의 고압력 풍선이 주로 필 요하지만[17], 현재 사용되는 DCB는 고압력 풍선을 기반으로 하지
Table 2. Studies using drug-coated balloons for treatment of stenosis in hemodialysis circuit First author Year Study
design Comparison Total No. of fistulas
(PCB/control) Level of TL Recurrent/
de novo lesion
Teo 2013 RCT PCB vs. CBA 30 (14/16) NR Recurrent
Lai 2014 PC PCB vs. CBA 20 (10/10) RC swing Recurrent
Patane 2014 PC PCB only 26 Venous outflow 7/19
Kitrou 2015 RCT PCB vs. CBA 40 (20/20) Venous outflow NR
Swinnen 2015 RC PCB vs. CBA 74 (37/37) NR Recurrent
Verbeeck 2016 RC PCB only 70 Venous outflow Recurrent
Roosen 2017 RCT PCB vs. CBA 34 (16/18) Venous outflow Recurrent
Lucev 2018 RC PCB vs. CBA 62 (31/31) Venous outflow De novo
Maleux 2018 RCT PCB vs. CBA 64 (33/31) Venous outflow 32/32
Qamhawi 2018 RC PCB vs. CBA 52 (26/26) Venous outflow 8/44
Trerotola 2018 RCT PCB vs. CBA 285 (141/144) Various* 203/82
Zheng 2018 RC Combined PCB+CBA 12 Venous outflow, access zone Recurrent
Massmann 2015 PC PCB vs. CBA 25 (10/15) Central venous Recurrent
Kitrou 2017 RCT PCB vs. CBA 40 (20/20) Central venous 27/13
Hongsakul 2018 RC PCB vs. CBA 32 (16/16) Central venous Recurrent CBA, Conventional balloon angioplasty; HD, hemodialysis; NR, not reported; PC, prospective cohort; PCB, paclitaxel-coated balloon;
RC, retrospective cohort; RC swing, “swing segment” of a distal radial-cephalic native arteriovenous fistula; RCT, randomized controlled trial; TL, target lesion.
*Including venous outflow, RC swing, inflow, cannulation zone, cephalic arch, anastomotic.
않았으며 rated burst pressure (RBP)는 대부분 15 atm 이하이다. 투석 로 협착병변에 대해 DCB와 plain balloon의 device 성공률을 비교한 연구에서는 DCB의 성공률(45%)이 plain balloon (100%)에 비해 낮은 결과를 보였다(p<0.001) [13]. 따라서, DCB는 고압력 풍선을 사용했 을 때에 비해 anatomic success를 얻지 못하는 경우들이 많으며, 이에 대해 추가로 고압력 풍선의 도움을 받아야 하는 경우들이 생긴다는 것을 유념해야 한다.
결 론
현재까지 연구들을 보면 DCB는 conventional balloon에 비해 자가 혈관 및 인조혈관 혈액투석 동정맥루 협착증 및 중심정맥 협착증에 대한 혈관성형술 후 추적관찰 시 더 높은 개통률을 제공하는 것으로 보인다. 대규모 RCT나 장기간 추적관찰 연구 결과가 보고된다면 이 를 더 뒷받침할 수 있을 것으로 생각한다.
REFERENCES
1. Lee T, Roy-Chaudhury P. Advances and new frontiers in the pathophysiology of venous neointimal hyperplasia and dialysis access stenosis. Adv Chronic Kidney Dis. 2009;
16(5): 329-38.
2. Aruny JE, Lewis CA, Cardella JF, et al. Quality improvement guidelines for percutaneous management of the thrombosed
or dysfunctional dialysis access. J Vasc Interv Radiol. 2003;
14(9 Pt 2): S247-53.
3. Vesely TM, Siegel JB. Use of the peripheral cutting balloon to treat hemodialysis-related stenoses. J Vasc Interv Radiol.
2005; 16(12): 1593-603.
4. Gray RJ, Varma JD, Cho SS, et al. Pilot study of cryoplasty with use of PolarCath peripheral balloon catheter system for dialysis access. J Vasc Interv Radiol. 2008; 19(10): 1460-6.
5. Haskal ZJ, Trerotola S, Dolmatch B, et al. Stent graft versus balloon angioplasty for failing dialysis-access grafts. N Engl J Med. 2010; 362(6): 494-503.
6. Krokidis M, Spiliopoulos S, Katsanos K, et al. Peripheral applications of drug-coated balloons: past, present and future.
Cardiovasc Intervent Radiol. 2013; 36(2): 281-91.
7. Yan Wee IJ, Yap HY, Hsien Ts'ung LT, et al. A systematic review and meta-analysis of drug-coated balloon versus conventional balloon angioplasty for dialysis access stenosis.
J Vasc Surg. 2019; 70(3): 970-9.
8. Loh JP, Barbash IM, Waksman R. The current status of drug- coated balloons in percutaneous coronary and peripheral interventions. EuroIntervention. 2013; 9(8): 979-8.
9. Boitet A, Massy ZA, Goeau-Brissonniere O, et al. Drug- coated balloon angioplasty for dialysis access fistula stenosis.
Semin Vasc Surg. 2016; 29(4): 178-85.
10. Portugaller RH, Kalmar PI, Deutschmann H. The eternal tale of dialysis access vessels and restenosis: are drug-eluting
A
B
Fig. 1. An example of PTA with drug-coated balloon for hemodialysis circuit stenosis. This 78 year-old female patient with a left forearm arteriovenous graft has history of stent placement in the left brachiocephalic vein. She had left arm edema and elevated venous pressure during hemodialysis. (A) No residual stenosis was noted after PTA with a 12 mm diameter balloon for severe focal stenosis at left brachiocephalic-subclavian vein junction. (B) Symptoms reemerged after 3 months, and PTA was performed for severe focal stenosis at the same location, with a 7 mm drug-coated balloon followed by a 12 mm plain balloon. Patient is symptom-free for 10 months.
balloons the solution? J Vasc Access. 2014; 15(6): 439-47.
11. Roy-Chaudhury P, Arnold P, Seigel J, et al. From basic biology to randomized clinical trial: the Beta Radiation for Arteriovenous Graft Outflow Stenosis (BRAVO II). Semin Dial. 2013; 26(2): 227-32.
12. Kakisis JD, Avgerinos E, Giannakopoulos T, et al. Balloon angioplasty vs. nitinol stent placement in the treatment of venous anastomotic stenoses of hemodialysis grafts after surgical thrombectomy. J Vasc Surg. 2012; 55(2): 472-8.
13. Katsanos K, Karnabatidis D, Kitrou P, et al. Paclitaxel- coated balloon angioplasty vs. plain balloon dilation for the treatment of failing dialysis access: 6-month interim results from a prospective randomized controlled trial. J Endovasc Ther. 2012; 19(2): 263-72.
14. Kitrou PM, Spiliopoulos S, Katsanos K, et al. Paclitaxel- coated versus plain balloon angioplasty for dysfunctional arteriovenous fistulae: one-year results of a prospective
randomized controlled trial. J Vasc Interv Radiol. 2015;
26(3): 348-54.
15. Kitrou PM, Katsanos K, Spiliopoulos S, et al. Drug- eluting versus plain balloon angioplasty for the treatment of failing dialysis access: final results and cost-effectiveness analysis from a prospective randomized controlled trial (NCT01174472). Eur J Radiol. 2015; 84(3): 418-23.
16. Kitrou PM, Papadimatos P, Spiliopoulos S, et al. Paclitaxel- Coated Balloons for the Treatment of Symptomatic Central Venous Stenosis in Dialysis Access: Results from a Randomized Controlled Trial. J Vasc Interv Radiol. 2017;
28(6): 811-7.
17. Trerotola SO, Kwak A, Clark TW, et al. Prospective study of balloon inflation pressures and other technical aspects of hemodialysis access angioplasty. J Vasc Interv Radiol. 2005;
16(12): 1613-8.