약학회지제
46
권제2
호124~128 (2002) **■"■*
Yakhak Hoeji Vol. 46, No. 2
-粮學 • 출 확횐쥐에서 nitrone 계 항산화제인 a-phenyl-/?_te/t-butyl nitrone(PBN) 의
뇌 투고성 및 체내동태 ~
이나영
•
강영숙#
숙명여자대학교 약학대학
(Received January 21, 2002; Revised February 20, 2002)
The Blood-Brain Barrier Permeability and Pharmacokinetics of Nitrone Based Spin Trapping Agent, a-Phenyl-w-fe^-Butyl Nitrone (PBN) in Rats
Na-Young Lee and Young-Sook Kang#
College of Pharmacy, Sookmyung Women's University, Seoul 140-742’ Korea
Abstract — The nitxone-based free radical trapping reagent, a-phenyl-w-fe
作-butyl nitrone (PBN) has been proposed as therapeutic agent for stroke. We used this for model drug of development of new drug for neuroprotection. The purpose of this study was to evaluate the blood-brain barrier (BBB) permeability of PBN in Sprague-Dawly (SD) rats. The BBB transport of PBN was investigated in SD rats using internal carotid artery perfusion (ICAP) method at a rate of 4 m //min for 15 second. We also obtained pharmacokinetic parameters of PBN using single intravenous injection technique. When we estimated BBB permeability of PBN with ICAP method, the brain volume of distribution of PBN was 60.0
土12.0 (ig//.
The brain uptake of PBN after IV injection at 120 min was 0.15
土0.01%ID/g. The PBN was transported to the brain through the BBB well in rats, because PBN is small molecule (MW 177) and lipid-soluble (log P 1.23) compound.
Keywords □ a-phenyl-w-tert-butyl nitrone (PBN), blood-brain barrier (BBB) permeability
In
야Vo
에서허혈에 의해유도된free radical
이세포손상을일 으킨다는사실은이미여러논문에서밝혀져 있다. 15그러므로이 러한산화적스트레스를 억제하는물질은허혈에의해유도된뇌 졸중의 치료에효과를나타낼 것으로기대되어진다. cx-phenyl-
«-tert-butyl nitrone(PBN)
은nitrone-based spin trapping agent
의하나로써free radical
과결합하여상대적으로안정한부산물 을 형성하는radical scavenger
로 작용한다.2)
실제로PBN
이global ischemia
동물모델에서 뇌손상을 억제시키는 결과를나 타낸다는것이보고되어 있고3〉흰쥐의focal ischemia
모델에서 도 역시뇌신경 손상을보호하는 작용을나타낸다는것이보고 되었다.4'5)
또한free radical
에의해유발되는 질환인 간질,노화등을 억제하는효과가있다는것이보고되어 있다
.6’7)
그러나약물이뇌혈관이나뇌세포내에작용하기 위해서는 혈 액•뇌관문을통과하여야하는데실제로
PBN
의혈액뇌관문의 투 과성을정확히 평가한 연구보고는 거의 찾아보기 어렵다•
그래#본 논문에 관한 문의는 저자에게로 (전화) 02-710-9562 (팩스) 02-715-9498 (E-mail) [email protected]
서본 연구에서는뇌신경 손상을보호하는물질의 개발을위하 여우선
PBN
을모델물질로사용하여PBN
의뇌투과성을내 경동맥 관류법(internal carotid artery perfusion method, ICAP
법)과정맥투여법(/w vivo intravenous injection technique)
을이 용하여실험하고혈액중의약물량과뇌투과량을' high performance liquid chromatography(HPLC
)법으로 정량하여 검토하였다.
실 험 방 법
시약및기기
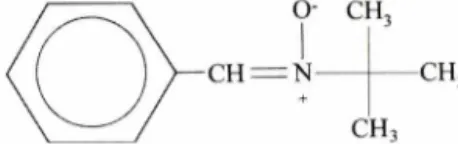
a-Phenyl-w-tert-b\ity\ nitrone (Fig. 1)
은Aldrich Chemical Co.에서 구입하여 시용하였다. 생리식염수와 헤파린은 중외제약 제품을,마취제로 사용한 염산 ketamine은 유한양행 제품을,근 이완제인 xylazine은 Sigma에서 각각 구입하여 사용하였다.
O- C H ,
I
C H = N --- C H 3
c h
3Fig. 1 - Chemical structure of PBN used in the present study.
124
흰쥐에서 nitrone 계 힘신:화제인 a-phenyl-w-te?f-butyl nitrone(PBN) 의 뇌 투과성 및 체내동태 125
Acetonitrile
은HPLC
용으로덕산이화학(
주)
에서구입하였다.
기 타시약은일급이상의 제품을덕산이화학(
주)에서 구입하여사 용하였다.
실험에시용한기기는원심분리기 (한일과학산업(
주),Union 55R, Micro 17TR), Infusion/withdrawl pump(KD Scientific, model 210), thermal blanket (temperature control unit, Letica, HB10 1/2), bipolar coagulator (Union Medical Co., Surgitor UM 880-A),
단두기(
대종기기), pH meter (Mettler, delta 340),balance (Sartorius, AC2115), freeze dryer system (LABCONCO 7522900
),수술 기구 등이다.
한편Sprague-
Dawley (SD
)계웅성 흰쥐는셈타코에서 구입하여 일주일간동물실에서사육하여사용하였다
.
Standard dose curve
작제헤파린이 첨가된 혈액을
(heparin
1 0 0unit/m/)
1 , 0 0 0 용에서1 0분간원심분리하여혈장을얻었다
.
흰쥐를희생하고뇌를꺼내 어실험에 사용하였다.
혈장100
야에PBN
이각각1
,2, 5, 10
매이 되도록넣고chloroform 0.5 m
/로5
분간추출하였다.
추출 액을4
0C
에서800 g, 10
분간 원심분리하여 유기층만을 취하고freeze dryer
에적용하여용매를완전히날린후acetonitrile
1 0 0 10/에녹여그중50 (
0/를HPLC
에적용하였다.
뇌를약1 g
이되 도륙취하고생리완충액(PB, 10 mM HEPES, 141 mM NaCl, 4 mM KC1, 2.8 mM CaCl2, 1 mM MgS04, 1 mM NaH
2P04, 10 mM D-glucose, pH 7.4) 500
를넣고균질화한후PBN
이 각각1, 2
,5
,10, 20,50 (ig
이 되도록homogenate
에 넣고chloroform 3 m
/로5
분간 추출하였다. 4
0C
에서800 g, 10
분간 원심분리하여 유기증 만을취하고freeze dryer
에적용하여 용 매를완전히날린후acetonitrile
2 0 0(i
/에녹여pore size
가0 . 2jim
인syringe filter (National Scientific Co
.)를시용하여여과하 고그중100 (
0/를HPLC
에적용하였다.
내경동맥 관류법
(Inte rn al carotid artery perfusion technique, ICAP
법)
250—300
용의웅성 흰쥐에ketamine (100 mg^kg)
과xylazine
( 2
mg/kg)
을근육주사하여 마취시키고이미 보고된논문의 방 법대로목부위를절개하여 혈관들을전기결찰하였다.8)
오른쪽외 경동맥에PE-10
관(Natsume Co.)
을삽입하여infusion pump
에 연결하였다.
수술하는동안에는thermal blanket
을이용하여 흰 쥐의 체온을37°C
로유지하였다. PBN 100 |ig
을1% DMSO
에 녹이고Kreb’s-Henseleit buffer (KHB, pH 7.4:119 mM NaCl, 4.7 mM KC1, 2.5 mM CaCl2, 1.2 mM MgS04, 1.2 mM KH
2P04, 25 mM NaHC03, 10 mM D-glucose, 10 g/dl BSA)
를잘혼합하여4 ml/min
으로주입함과동시에총경동맥을결찰 하였다.
주입후정확히15
초가되었을때즉시단두하여뇌를적출하고 무게를 측정한 후
PB 500
야를 넣고 균질화한 후chloroform
으로5
분간추출하였다.
추출액을4
0C
에서800 g, 10
분간원심분리하여 유기증만을취하고freeze dryer
에 적용하여 용매를 완전히 날린후acetonitrile
2 0 0jo
/에녹여pore size
가0.2 !jjn
인syringe filter(National Scientific Co.)
를사용하여 여과한후그중
100 |i
/를HPLC
에적용하였다.
ICAP
법을이용한후에뇌의분포용적(volume of distribution, V
D)과뇌투과고유상수(permeability-surface area product, PS)
를구하는식은다음과같다.
[brain
중PBN(g)/brain(g)]
VD (| 그 //g) = --- ---
[Perfusate-
5" PBN(g)/perfusate(ji/) PS (j
그//min/g) = VD perfusion time
정맥투여법 (S in g le in tr a v e n o u s in je c tio n m e th o d )
PBN
의pharmacokinetic profile
을즉정하기 위하여,이미 보 고된 논문의 방법9〉과 마찬가지로ketamineb
( 1 0 0mg/kg
)과xylazine (2 mg/kg
)을근육주사하여 마취시킨250—300 g
흰쥐 의대퇴동맥과 대퇴정맥에PE-50
관(Natsume Co
.)을 삽입하였 다. PBN 0.5 mg
을' 2% DMSO
로용해시키고20% Polyethylene glycol 200
과Ringes Herpes buffer (RHB, 10 mM HEPES, 141 mM NaCl, 4 mM KC1, pH 7.4
)로 잘혼합하여1 m
/가 되 도록만들고대퇴정맥을통해정확히500
가되도록 투여하였 다.
약액을 투여한후 대퇴동맥에서0.25
,1, 2, 5, 15
,30
,60,
1 2 0분에 혈액을취하고 1 2 0분에단두하였다
.
채취한 혈액을 원심분리하여 얻은혈장을
chloroform
으로5
분간추출하고4
0C
에 서800 g,
1 0분간원심분리하여 유기층만을취하고freeze dryer
에적용하여 용매를완전히 날린후acetonitrile
1 0 0(j
/에녹여 그중5 0
^/를HPLC
에적용하였다.
적출한뇌는PB 500 (
0/를 넣고균질화한후chloroform
으로5
분간추출하여 유기층만을 취하고freeze dryer
에서용매를완전히날린후acetonitrile
2 0 0(j
/에녹여pore size
가0 . 2(im
인syringe filter
를사용하여 여과 하고그중100 |i
/를HPLC
에적용하였다.
HPLC
분석HPLC
분석은Shimadzu LC-10AS gradient liquid chromato
graphic system
을사용하여UV detector
로280 nm
에서즉정하 였다. Column
은C18 reverse phase column (CLC-ODS 5 jim, 4 mm 250 mm
)을사용하였다. HPLC
이동상은A
액과B
액을 각각 0.
1% phosphoric acid in water,
0.
1% phosphoric acid in acetonitrile
로 구성하여A
액과B
액을각각4 :
6의비율 로하고flow rate
는 1m//min
로적용하였다.
P h a r m a c o k in e tic p a r a m e te r 분석
Pharmacokinetic parameter
는각peak
넓이를농도로환산하 여UCLA Health Science Computing Facilities
에서 개발한126 이나영 • 강영숙
4 J I I
(A) (B) (C)
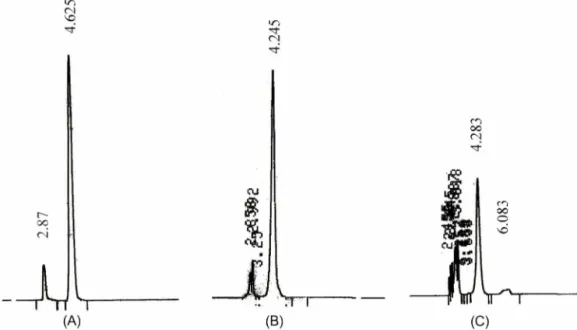
Fig. 2 - Typical chrom atogram s from H P L C injection o f injectate (A), brain extract obtained at 0.25 m in after internal carotid artery perfusion (B), brain extract obtained at 120 m in after intravenous injection (C) of P B N
d e riv a tiv e - fre e n o n lin e a r r e g re s s io n a n a ly s is ( P A R B M D R
Biomedical Compute P Series)
를 이용하여biexponential equation
에적용하여계산하였다.
A(t) = +A
2e 'k
2t
여기에서
A(t)
는혈장중약물농도의%ID/m
/이며ID
는투여량 이다.
Data
는weight=V(concentration
) 2를이용하였다.
정맥 부여120
분후PBN
의뇌의분포용적(VD, m//g)
은투여후120
분•에서 의뇌의약물농도를뇌의무게로나눈값을같은시간의종말혈 장중의 약물농도를 혈장용적으로나누어서 얻어진 값이다.
전 신혈장중클리어런스(CLt), steady-state
분포용적(Vdss),
혈 징중농도•시간곡선하면적(area under the plasma concentration
time curve, AUC)
과평균체류시간(mean residence time, MRT)
은Gibaldi
와Perrier
의정의에 따라Ah A2, k
l7k
2로부터 구하 였다.10)
PBN
의뇌투과고유상수(permeability-surface area product, PS)
는다음과같이 계산되었다.
p[
:_[V „- V
0]Cp(T) J^C p (t)d t
Cp(T) = 종말기의 혈징중 농노
Vo =
혈관내용적표시체의장기분포용적VD =
뇌에서의물질의분포•용격정맥투여 일정 시간후에 뇌내로송달된 약물량은
%ID/g
로나타내어지며 다음과같이
ps
와AUC
로나타내어진다.
% ID /g (t) = P S > A U C (t) A U C (t) = [ ^ C p ( t ) d t
실험결고卜 및 고 찰
N itro n e 계 항산화제인 P B N 의 뇌 투과성을 내경동맥 관류법
(IC A P ) 과 정맥투여법으로 검토하기 위하여 언어진 대표적인
c h ro m a to g ra m 을 Fig. 2 에 나타내었다. A , B , C ᅵ 각 각 실험에 사용한 in je ctate 의 peak, IC A P 법으로 P B N 을 내경동맥으로 주 입한 후 15 초에서 적출한 뇌에서 얻은 pe ak, P B N 을 정맥투여한 후 120 분에서 적출한 뇌에서 얻은 peak 이다. H P L C 에 적용한
후약 4 3 분에서 P B N 의 p e a l # 얻을 수 있었다. H P L C chrom atogram
의 결과를 바탕으로 혈장과 뇌 에서의 P B N 의 standard dose
cu rv e 를 작성한 결과 직선 상관계수가 각각 r 2= 0 .9 6 3
인 회귀직선을 얻을 수 있었고 이 직 선을 시용하여 혈장과 뇌 내
의 P B N 의 농도를 정량하였다.
흰쥐의 대퇴정맥으로 PBN을 투여한 후
1 2 0분간의 혈장 중 을 Fig. 3 에 나타내었다. P B N 은 혈장 중에서 biexponential equation 에 따라 소신됨을 알 수 있었다. P A R B M D P p ro g ra m 을 이용하여 계산된 P B N 의 p h a rm a c o k in e tic p a ra m e te r 는 Table I
에 나열하였다. 120 분까지의 P B N 의 혈장 중 농도 곡선하 면적
(A U C ) 은 4 5 .7 ± 6 .2 % ID - m in /m /, 혈장 중 전신 클리어런스 (C L ) -!: - 6 .2 4 ± 0 .8 1 m //m in/kg, 소싶 반감기는 약 57 분을 나타내었다.
P B N 을 대퇴정맥으로 투여한 후 120 분에서의 뇌 투과량과 뇌투
과 고유상수 (P S ) 는 Fig. 4 에 나타내었다. P B N 의 뇌 투과량을 표시하는 % ID / g 값은 0 .1 5 ± 0 . 이이었다. IC A P 방법으로 P B N 을
m 00 o ^6
e 00n
7 9
寸
이 寸
S 9
•寸
SS.
CN
J. Pharm . Soc. Korea
흰쥐에서 nitrone 계 항산화제인 a-phenyl务 fer^-butyl nitrone(PBN) 의 뇌 투과성 및 체내동태 127
0 20 40 60 80 100 120
minutes
Fig. 3 - Plasma clearance profile of PBN in SD rats after intravenous injection of the injectate for up to 120 min. Data values are means
土S.E.M. (n=3).
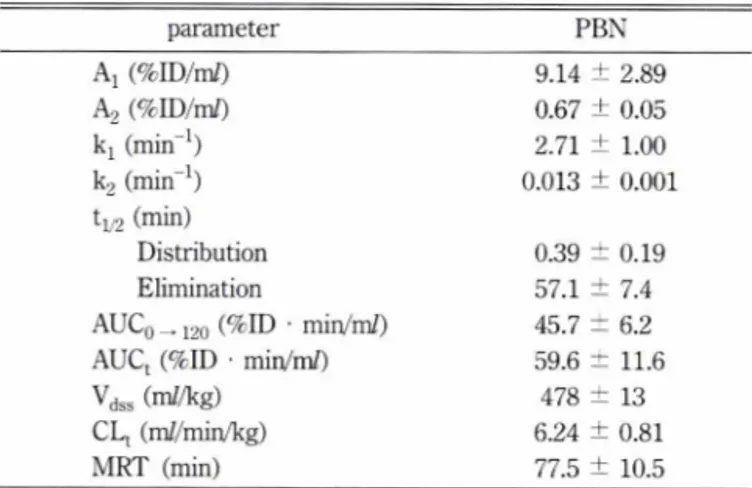
Table I - Pharmacokinetic parameters of PBN obtained with intravenous injection technique in SD rats
parameter PBN
A1 (%ID/m/) 9.14 ± 2.89
A
2(%ID/m/) 0.67 ± 0.05
kx (min-1) 2.71 ± 1.00
k
2(min-1) 0.013 ± 0.001
t
V 2(min)
Distribution 0.39 ± 0.19
Elimination 57.1 ± 7.4
AUC
0— 1 20(%ID . min/m/) 45.7 ± 6.2
AUCt (%ID • min/m/) 59.6 ± 11.6
Vdss (m//kg) 478 ± 13
CLt (m//min/kg) 6.24 ± 0.81
MRT (min) 77.5 ± 10.5
Pharmacokinetic parameters were estimated from plasma profile data up to 120 min in SD rats. Data values are means
士S.E.M (n=3)
t
1/2: half time, Vdss : volume of distribution at the steady-state CLt : plasma clearance, MRT : mean residence time
경동맥에적용하였을때뇌의분포용적
(vu)
과뇌투과고유상수(PS)
값을구히여Table II
에나타내었다. PBN
의뇌분포용적은60.0±12.0 |i//g
이었다.
ICAP
법은흰쥐의 혈류속도인1.25
해/면노보다빠른속도인4 mZ/minsL
물질을infUsion
하여물질이 혈액의 영향을받거나혈관 에침착되는것을방지하면서 뇌로이행시키-;:?
방법이다.8) ICAP
법으로
PBN
의뇌이행량을 조사한 결과혈관용적 표지자인sucrose
의뇌분포용적과비교하였을때약10
배정도큰값을나0.05-
0.00
Fig. 4
ᅳThe brain delivery amount measured as %ID/g of brain, the blood-brain barrier permeability surface area (PS) product and under the plasma concentration curve at
1 2 0min for PBN. Values are expressed as means
士S.E.M. (n=3).
Table II - The blood-brain barrier permeability of PBN using ICAP method
brain uptake PBN
VD i[xl/g) 60.0 ±
1 2 . 0PS (|i//min/g) 240 ± 48
Brain were perfused for 15 second at rate 4 ml/min by internal carotid artery perfusion method in rats. Data values are means
土S.E.M. (n=3)
타내었다
.11)
분자량이 약400-600 Da
이하인 소분자약물일경우 물-옥탄올분배계수(log P)
즉,
지용성이 클수록 뇌투과성(PS)
은커진다는논문의보고가있다.1^
이와길미PBN
이뇌내로비 교적많은양이이행되는것은PBN
이분자량이 적고(MW 177),
지용성(log P 1.23
)인약물이기때문일 것으로사료된다.
정맥투여법을이용하여
PBN
의뇌이행링을구했을때에도이 와유사한 결과를나타내었다. In w'w
에서 정맥투여 투진통효 과를보이는morphine
의경우brain uptake
는약0.08 %>ID/g
을 나타내었고13) BBB
에존재하는transferrin receptor
를통해 뇌 내로 이행하는neutral avidin-OX26 conjugate (NLA-OX26)
의 경우에는 약0.2 %ID/g
을 나타내었다.14)
실험 결과PBN
은morphine
에비해서는2
배가량많은 양이, BBB
에수용체가존재하는
NLA-
ᄋX26
와유사한 정도로뇌로 이행되는 것을알수있었다
. PBN
을정맥투여하고120
분에서의brain chromatogram
을 살펴보면(Fig. 2)
약6분에서 대사체의peak
를볼수 있으며 본 실험에서는intact
한PBN peak
인4.3
분대의 것만을 계산에 사용하였다.
% I D / g P S A U C
(jjJ/m in /m l) ( % I D m in / m l)
0 . 2 0
- "
ᄊ128 이나명
•강영숙
결 론
이상의결과에서
a-phenyl-w-te/f-butyl nitrone (PBN
)의뇌이 행량을정맥투여법과내경동맥관류법(ICAP)
의두가지방법으 로살펴본결과유의한뇌이행량을나타내었다.
그러므로PBN
은뇌로이행하여free radical
에의해유도된 여러뇌신경질환 에효과를나타내며,
이를모델물질로사용하여 새로운치료제 의개발이 가능하리라사료된다.
감사의 말씀
본연구의 일부는숙명여자대학교2 0 0 2년도교내 연구비지원 에의해수행되었으며 이에감사드립니다
.
문 헌
1) Facchinetti E, Dawson V L. and Dowson T. M. : Free radicals as mediators of neuronal injury. Cell Mol. Neurobiol. 18,667 (1998).
2) Knecht K. T. and Mason R. P. : In vivo spin trapping of xenobiotic free radical metabolites. Arch. Biochem. Biophys.
303,185 (1993).
3) Phillis J. and Clough-Helfman C. : Protection from cerebral ischemic injury in gerbils with the spin trap agent a-phenyl-w- ter^-butyl nitrone (PBN). Neurosci. Lett. 116,315 (1990).
4) Cao X. and Phillis J. : a-pheny 1-w-tert-bu.ty\ nitrone reduced cortical infarct and edema in rats subjected to focal ischemia.
Brain Res. 644,267 (1994).
5) Zhao Q., Pahlmark K., Smith M. L. and Siesjo B. K. : Delayed treatment with the spin trap a-phenyl-w-ter^-butyl nitrone
(PBN) reduces infarct size following transient middle cerebral artery occlusion in rats. Acta Physiol Scand. 152,349 (1994).
6
) He Q. R, Smith M. L.,Li E A. and Siesjo B. K. : Necrosis of the substania nigra, pars reticulate, in flurothyl-induced status epilepticus is ameliorated by spin trap a-phenyl-w -te^-buty 1 nitrone. Free Radical Biol Med. 22, 917 (1997).
7) Edumatsu R., Mori A. and Packer L. : The spin trap a-phenyl- n-tert-b\ity\ nitrone prolongs the life span of the senescence accelerated mouse. Biochem. Biophys. Res. Commun. 211, 847 (1995).
8
) Takasato Y., Rapoport S. I. and Smith Q. T : An in situ brain perfusion technique to study cerebrovascular transport in the rat. Am J. Physiol 247
,H484 (1984).
9) Kang YS.,Saito Y. and Pardridge WM. : Pharmacokinetics of [
3H]biotin bound to different avidin analogues. J. Drug Target.
3, 159 (1995).
10) Gibaldi, M. and Perrier, D .: Pharmacokinetics, Marcel Dekker Inc., New York p. 1 (1982).
1 1