대한소화기학회지 2008;52:134-141 □ REVIEW □
연락처: 김정욱, 140-757, 서울시 용산구 한강로 3가 65-207 중앙대학교 용산병원 내과
Tel: (02) 748-9941, Fax: (02) 790-2068 E-mail: ekg001@cau.ac.kr
Correspondence to: Jeong Wook Kim, M.D.
Department of Internal Medicine, Chung-Ang University Yong- san Hospital, 65-207, Hangangno 3-ga, Yongsan-gu, Seoul 140-757, Korea
Tel: +82-2-748-9941, Fax: +82-2-790-2068 E-mail: ekg001@cau.ac.kr
비스테로이드소염제 유발 위창자병증
중앙대학교 의과대학 내과학교실
김 정 욱
NSAID-induced Gastroenteropathy
Jeong Wook Kim, M.D.
Department of Internal Medicine, Chung-Ang University College of Medicine, Seoul, Korea
Non-steroidal anti-inflammatory drugs (NSAIDs) are used for the management of various conditions, such as pain, fever, inflammation, cancer, or cardiovascular diseases. These drugs may induce injury throughout the gastro- intestinal tract. NSAIDs are associated with diverse upper gastrointestinal adverse effects, including dyspepsia, ero- sions, peptic ulcer diseases and complications such as bleeding perforation. Established risk factors for these ad- verse effects include age, prior ulcer, types, doses and duration of NSAIDs, concurrent other NSAIDs admin- istration, and the concomitant uses of corticosteroids or anticoagulants. Misoprostol, proton pump inhibitors, and cyclooxygenase-2 selective inhibitors have been used to reduce the risk of NSAID-associated upper gastrointestinal events. NSAID-induced enteropathy is more common than complications of the stomach and duodenum and is usually manifested by occult blood loss or hypoalbuminemia. Furthermore, NSAIDs induce small intestinal injuries causing gut barrier damage, and bacterial translocation that have been proposed to be associated with the burden of illness in decompensated chronic heart failure. However, the risk factors for NSAID-induced enteropathy and bacterial translocation, as well as its preventive measures, are not well documented. (Korean J Gastroenterol 2008;52:134-141)
Key Words: Anti-inflammatory drugs, Non-steroidal; Adverse effects; Gastrointestinal disease
서 론
비스테로이드소염제(Non-steroidal anti-inflammatory drug, NSAID)는 진통, 해열, 항염증 효과가 있으며 전세계적으로 흔히 사용되고 있는 약물이다. 1899년 아세틸살리실산(ace- tylsalicylic acid)이 처음 사용되기 시작한 이후로 아세틸살리 실산과 유사한 효과를 보이는 아스피린양 약물, 즉 비스테 로이드소염제가 현재 골관절질환과 류마티스질환의 치료,
허혈심질환과 뇌질환의 예방 등의 목적으로 널리 사용되고 있다.1
지난 20년간 비스테로이드소염제 개발은 매우 활발하여 사용되는 약물의 종류가 2배 이상 증가하였으며 전 세계적 으로 매일 3천만 명 정도가 비스테로이드소염제를 복용하 고 있다. 하지만 비스테로이드소염제의 우수한 효과에도 불 구하고 그 부작용으로 약물 복용을 중지하거나 이차적인 합 병증으로 고통을 당하게 되는 경우가 빈번하다. 미국에서는
김정욱. 비스테로이드소염제 유발 위창자병증 135
소화기 합병증을 포함한 비스테로이드소염제의 합병증으로 연간 7만 명 이상이 입원치료를 받고 있으며 이 중 10% 정 도가 사망한다.2 이러한 이유로 비스테로이드소염제의 사용 은 항상 치료 효과뿐만 아니라 부작용을 염두에 두고 사용 하게 된다.
가장 흔히 발생하는 부작용은 소화기계 합병증으로 약물 사용 1년 내에 2%의 환자에서 위장관 출혈, 천공, 협착 등 의 합병증이 발생한다.3 또한 소장에서 합병증을 유발하여 출혈, 협착, 천공과 같은 주요 합병증 이외에 만성적인 빈혈 과 단백소실을 유발한다.4 비스테로이드소염제의 소화기계 부작용 발생과 임상증상과는 연관성이 없는 경우도 많다.
식도위샘창자내시경검사에서 출혈 병터가 관찰된 환자의 30% 정도에서 전혀 증상이 없으며,5 소화궤양과 같은 상부 소화기 병터가 치유되더라도 소장 병터에 의한 위장관출혈 로 만성빈혈이 개선되지 않는 환자들도 있다.6
비스테로이드소염제에 의한 상부소화기합병증
1. 발생기전과 임상양상
비스테로이드소염제에 의한 위샘창자점막 손상은 다양한 기전에 의해 발생한다. 비스테로이드소염제는 점막상피세 포에 직접적인 손상을 주기도 하고 점막장벽부전, 위장의 프로스타글란딘 생성억제, 위장점막혈류 감소를 유발하여 조직손상회복을 방해한다. 이 과정에서 위산은 복구과정을 방해하고 지혈과정을 간섭한다. 또한 점막방어와 복구에 중 요한 성장인자들을 비활성화하여 비스테로이드소염제에 의 한 궤양과 출혈을 유발한다.7
비스테로이드소염제를 복용하는 환자의 10-60%는 복통, 가슴쓰림, 팽만감, 소화불량과 같은 위장관 합병증을 겪게 된다.8 항궤양제를 복용하는 환자의 30% 정도가 비스테로이 드소염제에 의한 소화불량을 호소하며, 비스테로이드소염 제를 6개월간 복용한 류마티스 관절염 환자의 10-20%에서 소화불량으로 약물복용을 중단한다.9,10 하지만 소화불량은 내시경 소견과 연관성이 없으며 소화궤양 발생의 예측에 도 움이 되지 않는다.10 단기간의 비스테로이드소염제의 투여 는 위장에서 점막내 출혈과 점막미란을 유발한다. 약물 투 여 일주일 내에 얕은 궤양이 발생하지만 미란과의 연관성은 명확하지 않으며, 아스피린의 경우 투여 15-30분 후에 급성 위점막손상이 발생하나 대부분의 경우 임상적인 의미는 없 다.11,12
비스테로이드소염제 복용하는 환자는 복용하지 않는 경 우에 비해 20-30배의 소화궤양 발생률을 보인다. 약물 복용 자의 15%와 10%에서 위궤양과 샘창자궤양이 발생하는데 대부분 증상이 없다. 비스테로이드소염제 투여 후 4주간 관
찰하였을 때 약물복용자의 8%에서 위궤양이 발생하고 4%
에서 샘창자 궤양이 발생한다.13 비스테로이드소염제는 소 화궤양뿐만 아니라 출혈, 천공과 같은 합병증을 유발한다.
비스테로이드소염제의 복용은 소화궤양에 의한 출혈위험성 을 3배 이상 증가시키고, 소화궤양에 의한 천공은 그 발생 빈도가 낮지만 위험성이 6-7배 증가한다.14,15 그러나 지난 30 년간의 궤양치료제 개발과 발전에도 불구하고 소화궤양의 합병증에 의한 사망률은 개선되지 않았으며 소화궤양 출혈 에 의한 사망률은 6-12%에 달한다.16
2. 소화궤양과 합병증의 위험인자
비스테로이드소염제에 의한 소화기합병증을 예방하기 위 한 가장 좋은 방법은 약물을 사용을 하지 않는 것이다. 하지 만 실제 임상에서는 허혈심질환과 같이 상기약물의 사용이 생명 연장에 도움이 되거나 비스테로이드소염제의 사용 이 외에는 적절한 치료법이 없는 경우가 있다. 비스테로이드소 염제에 의한 상부소화기 합병증 발생은 연령, 성별, 소화궤 양의 과거력, 음주와 같은 약물복용자의 특성과 사용한 약 제의 종류와 용량, 복합사용 유무, 병용사용 약물과 같은 다 양한 요인에 의해 영향을 받는다.1
비스테로이드소염제에 의한 소화궤양의 발생 위험성은 복용자의 나이가 많을수록 증가한다.17 비스테로이드소염제 를 복용하지 않은 소화궤양 환자에서는 남자가 여자보다 합 병증 발생 위험이 2배 이상 높으나, 비스테로이드소염제에 의한 소화궤양에서는 여자가 남자보다 합병증 발생 위험이 높다.14 소화궤양 과거력이 있는 환자에서 소화궤양과 합병 증의 발생 위험도가 높고,18 흡연의 영향은 아직 명확하지 않으나 과도한 음주는 위험성을 증가시킨다.1
합병증 발생은 사용하는 비스테로이드소염제의 특성에 따라 차이가 있다. 이부프로펜(ibuprofen)은 상대적으로 위험 성이 낮으며 이에 비해 피록시캄(piroxicam)과 케토프로펜 (ketoprofen), 디클로페낙(diclofenac)은 위험도가 높다.14 그러 나 임상적으로 소화궤양과 그 합병증을 가장 많이 유발하는 약물은 아스피린이다. 사용 약물의 용량이 증가하고 여러 가지 비스테로이드소염제를 혼합 복용할수록 소화궤양의 위험도가 증가하는데, 아스피린을 장기간 복용하던 환자가 아스피린의 복용을 중지하지 않고 비스테로이드소염제를 같이 복용하는 경우에 소화궤양의 발생 위험이 증가한다.
또한 스테로이드와 항응고제의 복합사용도 소화궤양과 합 병증의 위험성을 증가시킨다.19 약물 사용 후 3개월까지는 상부위장관이 약물에 적응하여 소화궤양의 발생이 감소하 나 그 이후에는 오히려 증가하는 양상을 보인다(Fig. 1).20 그러므로 고령의 여성, 소화궤양의 과거력이 있는 환자, 다량의 알코올 섭취자, 스테로이드와 항응고제, 아스피린 복용자에서는 아세트아미노펜과 같은 위장관 손상이 없는
136 The Korean Journal of Gastroenterology: Vol. 52, No. 3, 2008
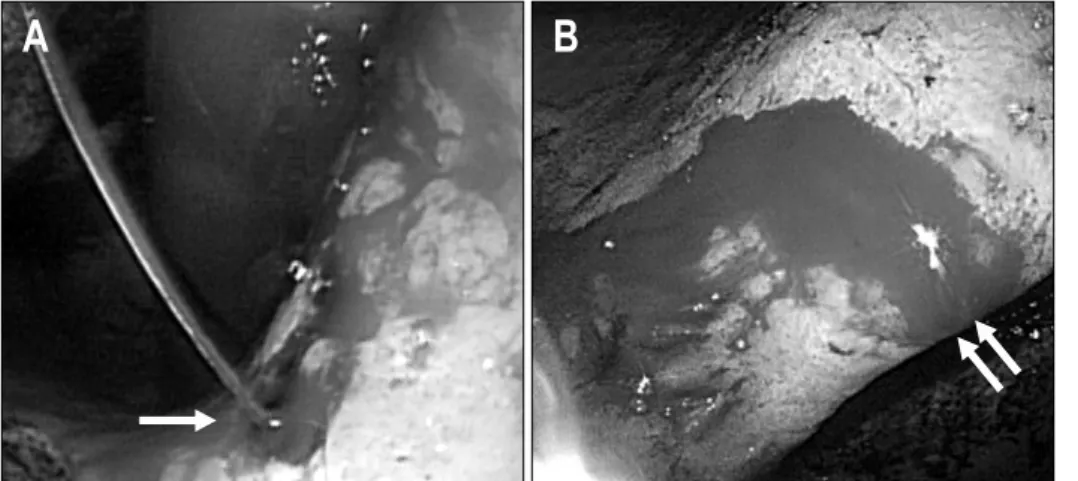
Fig. 1. Endoscopic images show active gastric ulcers bleeding in a patient taking NSAID and warfarin (A, arrow) and a pa- tient taking two different kinds of NSAIDs (B, double arrow).
NSAID, non-steroidal anti-inflam- matory drug.
진통소염제를 사용하거나 비스테로이드소염제 투여를 대체 할 수 있는 다른 치료방법을 찾는 것이 좋다. 또한 약물을 투여 할 때에는 되도록 위험도가 낮은 안전한 약물을 선택 하며 작은 용량으로 단기간에 투여하여야 한다.
3. 예방과 치료
비스테로이드소염제를 복용하는 환자에서 소화궤양과 같 은 합병증이 발생하면 대부분 비스테로이드소염제의 사용 을 중단하고 소화궤양을 치료한다. 그러나 비스테로이드소 염제 투여 후 발생하는 소화기증상이나 합병증을 치료하기 보다는 미리 예방을 하는 것이 더욱 효과적이다.
비스테로이드소염제에 의한 합병증 발생 위험성이 높은 대상군에서 약물을 일정기간 이상 사용해야 할 경우 소화궤 양과 합병증을 피하기 위하여 선택 COX-2억제제를 사용하 거나 위험을 감소시키는 약물을 같이 사용한다. 선택 COX-2억제제는 위점막 보호, 프로스타글란딘 합성에 관여 하는 cyclooxygenase (COX)-1에는 영향을 미치지 않고 염증 등과 연관이 있는 COX-2를 선택적으로 억제한다. 선택 COX-2억제제인 celecoxib, rofecoxib은 비선택적으로 COX를 억제하는 약물과 비교하여 소화기 증상뿐만 아니라 소화궤 양과 소화궤양에 의한 합병증 발생이 적다.21,22 그러나 선택 COX-2억제제는 트롬본산(thromboxane) A2와 프로스타시클 린(prostacyclin) 사이의 불균형에 의한 전혈전상태의 강화로 심혈관계 합병증을 유발하므로 심혈관계 질환이 있는 환자 에서는 매우 주의하여 사용하여야 한다. 참고로 Rofecoxib 은 심혈관 부작용으로 판매가 금지되었다.23
비스테로이드소염제를 복용하는 환자에서 소화궤양을 예 방하기 위한 동시 사용을 고려할 수 있는 약물로는 미소프 로스톨(misoprostol)과 양성자펌프억제제(proton pump inhibi- tor)가 있다. 미소프로스톨은 프로스타글란딘 E1 유사물질로 일일 800μg 복용으로 비스테로이드소염제에 의한 소화궤 양을 예방할 수 있다. 하지만 미소프로스톨은 설사와 복통
과 같은 부작용으로 그 사용에 제한이 있다.24 65세 이상의 아스피린이나 비스테로이드소염제 복용자에서 양성자펌프 억제제의 예방적인 투여는 급성과 만성 위장관 손상을 억제 하고25 혈소판억제제인 클로피도그렐(clopidogrel)을 사용한 경우보다 아스피린과 양성자펌프억제제를 병합 투여한 경 우에서 소화궤양과 합병증의 위험성이 낮다.26
최근 연구에 의하면 비스테로이드소염제에 의한 상부소 화기 부작용의 예방은 선택 COX-2억제제의 사용이 비선택 COX억제제와 저용량의 미소프로스톨의 병합사용보다 효과 적이었다. 비선택 COX억제제와 양성자펌프억제제의 병합 사용에는 차이가 없었다. 또한 가장 위험도가 낮은 방법으 로는 선택 COX-2억제제와 양성자펌프억제제의 병합사용이 었다.27 제산제, 수크랄페이트(sucralfate), H2수용체대항제(H2- receptor antagonist)는 효과가 적거나 큰 용량을 사용하여야 비스테로이드소염제에 의한 위장관 손상을 억제할 수 있어 대부분 추천되지 않는다.1
헬리코박터 파이로리 감염의 비스테로이드소염제에 의한 소화궤양 발생에 미치는 영향에 대해서는 다양한 보고가 있 다. 헬리코박터 파이로리에 감염된 비스테로이드소염제 복 용자에서 소화궤양의 발생이 높다는 보고가 있으나, 헬리코 박터 파이로리 제균 후 비스테로이드소염제 복용자에서 소 화궤양의 발생율의 변화는 감소한다는 보고와 그렇지 않다 는 상반된 보고들이 있다. 아직 헬리코박터 파이로리에 감 염된 비스테로이드소염제 복용자에서의 약물 복용 전 제균 요법에 대해서는 결정된 것이 없으며 효율성에 대해서 충분 한 검토가 필요하다.28
비스테로이드소염제에 의한 소화기증상의 치료에는 제산 제와 H2수용체대항제가 많이 사용되고 있다. H2수용체대항 제는 시메티딘(cimetidine)에 대한 초기 연구에서 소화기증 상 개선 효과가 보고되었으나 치료 후 유지요법에서는 비효 과적이었다.29 그러나 비스테로이드소염제에 의해 발생하는 소화기 증상은 특별한 조치 없이도 약물 투여 2주 후 상당
Kim JW. NSAID-induced Gastroenteropathy 137
수에서 개선되므로, 특별한 조치가 없는 경우와 일반적인 용량의 H2수용체대항제의 치료 사이에 소화기증상 개선에 서 크게 차이를 보이지 않는다는 보고도 있다.30 또한 파모 티딘(famotidine), 니자티딘(nizatidine)과 같은 H2수용체대항 제와 제산제의 효과에 대한 연구결과는 없다. 미소프로스톨 은 이론적인 효과에도 불구하고 충분한 효과를 위해서는 투 여용량을 증가하여야 하며 이에 따라 약물 자체의 소화기 부작용도 증가하므로 임상 사용에는 제한이 있다.1 비스테 로이드소염제에 의한 소화기 합병증 예방에 효과적인 양성 자펌프억제제는 비스테로이드소염제와 같이 일정기간 복용 하는 경우 비스테로이드소염제에 의한 소화기 증상을 감소 시키나 라니티딘이나 미소프로스톨과 효과에서 차이가 없 었다.31,32
비스테로이드소염제에 의한 창자병증과 장내세균전위
1. 발생기전과 임상양상
비스테로이드소염제의 소장손상의 기전은 정확히 밝혀지 지는 않았으나 다음과 같은 가설로 설명되고 있다. 우선 비 스테로이드 소염제의 COX 억제에 의한 직접적인 손상으로 장관세포표면의 인지질이 손상되고 세포 안 사립체의 손상 이 발생한다. 사립체의 손상으로 세포내에서 에너지 생성이 감소하며 자유라디칼이 생성된다. 이로 인해 세포 사이의 통합성이 감소하면서 장관장벽이상(gut barrier dysfunction), 즉 장투과성(intestinal permeability) 증가가 발생한다. 증가된 장투과성에 의하여 장관은 장내의 쓸개즙, 음식, 세균, 효소 와 같은 각종 물질에 의한 손상을 받으며, 장내세균의 과증 식에 이어 세균 침범이 발생하고 호중백혈구가 활성화되면 염증이 발생한다.4 창자간순환(enterohepatic circulation)도 중 요한 역할을 한다. 비스테로이드소염제가 창자간순환을 하 지 않은 경우 소장에 손상을 주지 않지만 창자간순환을 통 하여 혈류에 의해 장관에 약물이 계속 노출되면 손상이 발 생한다.33
위장이나 샘창자와 같은 상부소화기의 합병증은 내시경 검사나 영상의학적인 검사법으로 비교적 용이하게 검사가 가능한데 비해, 소장의 합병증은 관찰하기가 어려워 유병률 을 알기 힘들다.3 일부 부검결과에 따르면 비스테로이드소 염제를 복용하지 않는 경우 0.6%에서 소장궤양이 관찰되는 것에 비해 복용자는 8.4%에서 관찰된다.34 지속적으로 비스 테로이드소염제를 투여 받는 환자의 70% 이상에서 출혈과 단백소실을 동반한 장의 염증이 유발되며 약제투여를 중단 하더라도 16개월 이상 지속될 수 있다. 또한 비스테로이드 소염제를 복용하는 류마티스 관절염 환자의 41%에서 소장
에서의 혈액손실로 인한 철결핍빈혈이 동반된다.35 비스테로이드소염제에 의한 창자병증의 합병증으로는 빈 혈, 단백소실, 협착, 천공, 장내세균전위 등이 있다. 비스테 로이드소염제에 의한 소장손상은 심하지 않더라도 지속적 인 출혈을 유발하여 철결핍빈혈을 일으킨다. 비스테로이드 소염제에 의한 창자병증을 보이는 환자에서 장관의 염증을 반영하는 111Indium-labeled neutrophils과 출혈을 나타내는 technetium-99m-RBC를 신티그래피로 측정하면 염증 부위와 출혈부위가 동일하다는 것을 알 수 있다. 비스테로이드소염 제를 복용하고 빈혈을 동반하지만 식도위샘창자내시경과 대장내시경검사에서 출혈병소가 확인되지 않는 류마티스 관절염 환자에서 소장내시경을 시행하면 47%에서 소장의 궤양이 관찰된다. 환자의 대부분에서 심한 출혈이 동반하지 않지만 일일 2-10 mL의 정도의 혈액손실이 있다.3,5,36 비스테로이드소염제 장기복용에 의한 단백소실은 저알부 민혈증을 유발한다. 이전에는 출혈에 의한 이차적인 것으로 생각했으나 빈혈과 상관없이 단백소실이 발생하기도 한다.
단백소실이 동반된 창자병증환자의 장관에서 육안적인 출 혈병소가 관찰되지 않는 경우도 있으며, 현재 단백소실병증 은 염증, 미란, 궤양과 같은 병터 없이 발생할 수 있는 것으 로 생각되고 있다.3,35,36
비스테로이드소염제에 의해 발생한 만성궤양은 섬유증과 가로막 형태의 협착을 유발한다. 소장 중간부위에서 2-4 mm 정도의 가로막 형태의 사이막이 형성되며 장관의 내강 이 좁아지면 폐쇄가 발생하는데, 비스테로이드소염제에 의 한 소장궤양을 보이는 환자의 17%에서 관찰된다.3 이는 약 물의 사용 용량, 기간과 연관성이 있으며 설사와 체중감소, 철결핍빈혈, 단백소실이 동반된다.36 하지만 천공은 흔히 관 찰되는 합병증은 아니며 비스테로이드소염제에 의한 출혈 과 유사한 위험도를 보인다.
비스테로이드소염제에 의한 장내세균전위(bacterial trans- location)는 임상적으로 매우 중요한 합병증이다. 장내세균전 위는 장내세균무리와 같은 장관 내의 존재하는 세균과 지질 다당질(lipopolysccharide)과 같은 내독소(endotoxin) 등의 세 균의 분해산물이 장관장벽을 넘어 유입되어 장관 이외의 곳 으로 파급되는 현상이다.37,38
인체에서 장관장벽은 정상적으로 일정한 정도의 투과성 을 보이므로 장내세균전위는 병적인 상태가 아닌 경우라도 발생할 수 있다. 그러나 흡수된 장내세균이나 분해산물은 창자연관림프조직(gut-associated lymphatic tissue, GALT), 장 간막림프절, 간, 비장과 같은 그물내피계통(reticuloendothe- lial system)에서 제거되므로 인체에 큰 영향을 주지 않는다.
하지만 장투과성의 증가와 장내세균의 과증식이 발생하고 그물내피계통 등의 면역기능이 감소하게 되면 장내세균과 분해산물의 흡수와 전신으로의 파급이 증가된다.37
138 대한소화기학회지: 제52권 제3호, 2008
Fig. 2. A capsule endoscopic view shows a small bowel ulcer resulting from non-steroidal anti-inflammatory drug usage.
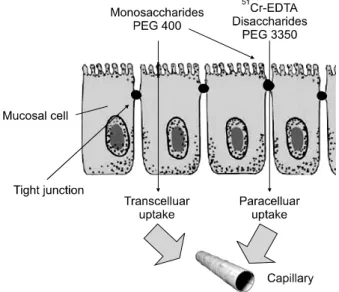
Fig. 3. Assessment of the intestinal permeability.
PEG, polyethylene glycol; 51Cr-EDTA, chromium-51 labelled ethylene diamine tetra-acetic acid.
비스테로이드소염제는 장관장벽손상과 장내세균과증식 을 유발하여 장내세균전위를 증가시키며 이때 흡수된 내독 소 등은 인체에서 이상 면역반응을 일으킬 수 있다.39 내독 소인 지질다당질은 죽경화증을 발생시킨다. 심부전 환자에 서는 비대상 상태에서 장관벽 부종에 의한 장투과 증가가 동반되기도 하는데, 이때 비스테로이드소염제 사용에 의한 추가적인 장관장벽손상에 의해 내독소혈증의 증가한다. 내 독소혈증은 심장에서 면역반응을 활성화시켜 심부전을 악 화시키고 재발을 증가시킨다.39-41 이외에도 내독소는 심한 경우 다발장기부전, 전신염증반응증후군 등 심각한 감염 합 병증을 유발한다. 비스테로이드소염제의 장관장벽손상과 장내세균전위에 대한 영향은 장관부종이나 다른 원인으로 인하여 장투과가 증가하는 질환에서도 발생할 수 있으며, 아직 심부전을 제외한 다른 질환에서 비스테로이드소염제 가 미치는 영향에 대해서는 충분히 연구가 이루어지지 않았 으나 약물 사용에 주의가 필요하다.
이외에도 비스테로이드소염제는 염증성 장질환인 크론병 과 궤양성대장염 환자에서 질환의 활성도를 증가시킨다. 이 는 약물에 의해 유발된 장관장벽손상, 장내세균 과증식 등 의 영향에 의한 것이며 선택 COX-2억제제도 염증성 장질환 을 악화시킨다.4
2. 진단방법
비스테로이드소염제에 의한 창자병증을 진단하는 방법으 로 캡슐내시경검사와 이중풍선소장내시경 검사가 있다. 이 검사법들은 비스테로이드소염제에 의해 발생한 염증, 미란, 궤양과 같은 병터와 출혈과 협착 등의 합병증을 진단할 수 있다. 특히 비침습적검사인 캡슐내시경검사는 매우 유용하
여 약물복용자의 70%에서 소장의 병터를 진단하며, 장관의 염증을 측정하는 대변 calprotectin 검사와 높은 연관성을 보 인다. 이에 비해 이중풍선소장내시경 검사는 출혈병태에 대 한 직접적인 치료와 병터에 대한 조직검사가 가능하다는 장 점이 있으나 검사에 많은 시간이 소모되고 침습적인 검사이 다. 또한 두 검사 모두 아직 많은 비용이 소요하므로 임상적 인 사용에는 제한이 있다(Fig. 2).3
111Indium-labeled neutrophils를 이용한 신티그래피로 장관 염증을 측정하면 비스테로이드에 의한 장관염증을 측정 할 수 있다. 장기 약물 복용자의 50-70%에서 저도의 장관 염증 증가가 관찰되고 약물복용을 중지하더라도 16개월 후까지 측정될 수 있다. 그러나 매우 고가의 검사이므로 임상에서 적용하기가 어렵다. 대변에서의 calprotectin의 검출도 비스 테로이드소염제에 의한 장관염증 측정에 사용되며 장기간 약물 복용자의 44-70%에서 양성소견이 관찰된다. 그러나 염 증성장질환과 대장암이 있을 때에도 증가하여 이와 같은 질 환과 구분하기가 어렵다.3,4
장투과 검사는 장관장벽이상을 알아보는 검사로 검사시약 을 경구로 투여한 후 소변에서 배출되는 시약의 양을 측정 하는 방법을 사용한다. 장투과 검사에서 사용하는 물질은 장관장벽기능이 정상일 때 일정량이 흡수되지만, 장관장벽 의 이상이 발생하면 흡수량이 증가하여 소변으로 많이 배출 된다. 또한 일정 시간 내에 소변으로 대부분 배출되고 생체 내에서는 대사되지 않은 특징이 있다(Fig. 3).3 장투과 검사 에서 사용되는 물질로는 PEG (polyethylene glycol), 방사선 동위원소인 51Cr-EDTA (chromium-51 labelled ethylene dia- mine tetra-acetic acid ), 락툴로스와 만니톨과 같은 당류가
김정욱. 비스테로이드소염제 유발 위창자병증 139
있다. 이 중 비스테로이드소염제에 의한 장관장벽이상의 측 정에 51Cr-EDTA이 가장 많이 이용되며 이 물질은 장내세균 에 의해 분해되지 않고 대장의 장투과성을 일부 반영하며 측정법이 비교적 간단하다. 비스테로이드소염제 장기복용 자의 50-70% 정도에서 장투과 증가현상이 관찰된다. 또한 비스테로이드소염제에 의한 장관손상을 억제하는 식품이나 약물의 효과를 관찰하는 임상연구에서 장투과 검사는 많이 사용되고 있다.3,4
3. 예방과 치료
비스테로이드소염제에 의한 창자병증과 합병증을 유발하 는 위험인자는 아직 입증되지 않았으나 이를 예방하거나 억 제하기 위한 여러 가지 시도가 있었다. 약물을 프로드러그 (prodrug)나 장용정(enteric-coated) 형태로 제조하거나 약물의 배출 형태를 변형시킨 약품들이 있으나 소장손상을 억제하 지 못한다. 또한 H2수용체대항제, 수크랄페이트도 치료나 예방효과가 없으며 점막방어제와 양성자펌프억제제의 효과 는 아직 입증되지 않았다. 설파살라진이 효과가 있다는 보 고가 있으나 추가적인 연구가 필요하다.4,35
선택적 COX-2억제제는 비스테로이드소염제에 의한 상부 위장관 합병증을 줄이나 소장의 합병증에 대한 효과는 아직 입증되지 않았으며, 단기간 투여한 환자에서 창자병증의 증 상을 관찰하지 못했다는 일부 보고가 있다. 그러나 비스테 로이드소염제에 의한 창자병증의 발생기전에서는 상부위장 관 합병증과는 달리 COX가 미치는 영향이 크지 않으며, 선 택 COX-2억제제는 단기 투여에서 위샘창자투과성(gas- troduodenal permeability)에는 영향이 없는데 비하여 소장의 장투과성은 증가시키므로 실제적으로 창자병증에는 크게 도움이 되지 않을 가능성이 높다.42
메트로니다졸(metronidazole)은 혐기 감염균 감염에 사용 하는 항생제로 장투과성의 변화에는 영향이 없으나 비스테 로이드소염제 의한 장관의 염증과 혈액손실을 감소시킨다.
하지만 메트로니다졸 이외의 항생제는 비스테로이드소염제 에 의한 창자병증에 효과가 없다. 메트로니다졸의 효과는 장내세균에 대한 효과보다는 장관세포 내의 사립체에서 발 생하는 산화적 인산화반응의 억제에 의한 것이다.4
미소프로스톨은 비스테로이드소염제에 의한 상부위장관 부작용을 효과적으로 억제하지만 창자병증에 대한 효과는 아직 명확히 입증되지 않았다. 비스테로이드소염제 의한 소 장의 장투과성을 억제하고 창자병증에 뚜렷한 효과를 보이 는 증례가 있음에도 불구하고, 인도메타신 투여 환자에서 시행한 무작위대조시험에서 유의한 효과를 보이지 않았다.
그러나 이 연구에서는 저용량의 미스프로스톨을 사용하였 으므로 추가 연구가 필요하다.3,4
비스테로이드소염제에 의한 창자병증의 예방목적으로의
특정 물질을 사용할 때에는 일정기간 투여가 필요한 경우가 많으므로, 부작용이 동반 할 수 있는 약물보다는 상대적으 로 위험도가 낮은 약리작용을 보이는 영양소(pharmaco- nutrient)와 같은 식품을 사용하는 것이 유리할 수 있다. 글 루타민(glutamine)은 면역영양(immunonutrition)에 사용되는 물질 중에 하나로 인체 전체에 걸쳐 분포하고 있는 비필수 아미노산이다. 글루타민은 소장 장관세포의 영양 상태를 개 선하고, 면역계의 상태를 개선하여 면역장벽을 강화시키고 장내세균전위를 억제한다.43,44 글루타민의 비스테로이드소 염제의 단기투여에 의한 창자병증에 대한 효과는 임상적으 로 입증되었다.44
유제품에 있는 각종 성장인자들도 비교적 안전하게 비스 테로이드소염제의 장관손상을 억제하는 데 사용할 수 있다.
특히 젖소초유(bovine colostrum) 등에서 IGF (insulin-like growth factor), EGF (epidermal growth factor), TGF (transforming growth factor) 등을 획득할 수 있으며, 각종 면역글로불린과 락토페린(lactoferrin)과 같은 항균 펩티드를 이용하여 비스테 로이드소염제에 의한 장내세균의 과증식을 억제할 수 있
다.45,46 이와 같은 특성을 이용하여 비스테로이드소염제에
의한 소장손상을 감소시킨다.45 또한 글루타민과 같이 병합 하여 사용하였을 때 효과가 증가한다.46 하지만 글루타민과 유제품에서 추출한 성장인자 모두 비스테로이드소염제의 장관손상에 대한 단기간의 효과만 연구되어 있으므로 장기 간 사용에 따른 효과 관찰이 필요하다.
결 론
비스테로이드소염제의 가장 흔히 발생하는 부작용은 소 화기 합병증으로 위장과 샘창자와 같은 상부위장관뿐만 아 니라 소장에서도 발생한다. 비스테로이드소염제는 상부위 장관에서 소화불량, 속쓰림과 같은 소화기 증상과 미란, 궤 양, 출혈, 협착, 천공과 같은 합병증을 유발한다. 이러한 소 화기증상이나 합병증을 치료하기보다는 미리 예방을 하는 것이 더욱 효과적이다. 상부위장관에서 발생하는 합병증을 예방하기 위해서는 고령의 여자, 과거 소화궤양의 과거력이 있는 환자, 다량의 알코올 섭취자, 스테로이드와 항응고제, 아스피린 복용자와 같이 위험성이 높은 대상에서 비스테로 이드소염제의 사용을 피하는 것이 좋다. 또한 약물 중 위험 도가 낮은 안전한 약물을 선택하여야 하며 작은 용량으로 단기간에 투여하여야 한다. 선택 COX-2억제제는 심혈관계 질환이 있는 환자에서는 주의하여 사용하여야 하며 미소프 로스톨은 부작용이 많아 사용이 제한되며 양성자펌프억제 제가 유용한 예방방법으로 제시되고 있다.
비스테로이드소염제는 소장에서 출혈, 협착, 천공, 철결핍 빈혈, 단백소실과 같은 합병증을 유발하며 상부위장관보다
140 The Korean Journal of Gastroenterology: Vol. 52, No. 3, 2008
더 흔히 발생한다. 또한 염증성 장질환을 악화시키고 장내 세균전위를 증가시켜 심부전을 악화시킨다. 비스테로이드 소염제에 의한 창자병증을 진단하기 위하여 장투과검사, 신 티그래피를 이용한 장관염증 측정, 캡슐내시경, 이중풍선내 시경과 같은 검사를 이용할 수 있으나 아직 임상적으로 제 한적이다. 그러나 아직 합병증 발생의 위험인자나 치료와 예방법은 명확히 입증되지 않았다.
참고문헌
1. Aalykke C, Lauritsen K. Epidemiology of NSAID-related gas- troduodenal mucosal injury. Best Pract Res Clin Gastroenterol 2001;15:705-722.
2. Committee on the Safety of Medicine. Non-steroidal anti-in- flammatory drugs and serious gastrointestinal adverse reac- tions-2. Br Med J 1986;292:1190-1191.
3. Adebayo D, Bjarnason I. Is non-steroidal anti-inflammaory drug (NSAID) enteropathy clinically more important than NSAID gastropathy? Postgrad Med J 2006;82:186-191.
4. Fortun PJ, Hawkey CJ. Nonsteroidal antiinflammatory drugs and the small intestine. Curr Opin Gastroenterol 2007;23:134- 141.
5. Silvoso G, Ivey KJ, Butt J. Incidence of gastric lesions in pa- tients with rheumatic disease on chronic aspirin therapy. Ann Intern Med 1979;91:517-520.
6. Morris AJ, Wasson LA, Mackenzie JF. Small bowel entero- scopy in undiagnosed gastrointestinal blood loss. Gut 1992;
33:887-889.
7. Wallace JL. How do NSAIDs cause ulcer disease? Baillieres Best Pract Res Clin Gastroenterol 2000;14:147-159.
8. Larkai EN, Smith JL, Lidsky MD, Graham DY. Gastroduode- nal mucosa and dyspeptic symptoms in arthritic patients dur- ing chronic nonsteroidal anti-inflammatory drug use. Am J Gastroenterol 1987;82:1153-1158.
9. Hogan DB, Campbell NR, Crutcher R, Jennett P, MacLeod N. Prescription of nonsteroidal anti-inflammatory drugs for elderly people in Alberta. CMAJ 1994;151:315-322.
10. Singh G, Triadafilopoulos G. Epidemiology of NSAID in- duced gastrointestinal complications. J Rheumatol 1999;56(suppl):
18-24.
11. Graham DY, Smith JL, Dobbs SM. Gastric adaptation occurs with aspirin administration in man. Dig Dis Sci 1983;28:1-6.
12. McCarthy DM. Nonsteroidal antiinflammatory drug-induced ulcers: management by traditional therapies. Gastroenterology 1989;96:622-674.
13. Koch M, Dezi A, Ferrario F, Capurso I. Prevention of non- steroidal anti-inflammatory drug-induced gastrointestinal mu-
cosal injury. A meta-analysis of randomized controlled clin- ical trials. Arch Intern Med 1996;156:2321-2332.
14. Hernández-Díaz S, Rodríguez LA. Association between non- steroidal anti-inflammatory drugs and upper gastrointestinal tract bleeding/perforation: an overview of epidemiologic stud- ies published in the 1990s. Arch Intern Med 2000;160:
2093-2099.
15. Lanas A, Serrano P, Bajador E, Esteva F, Benito R, Sáinz R.
Evidence of aspirin use in both upper and lower gastro- intestinal perforation. Gastroenterology 1997;112:683-689.
16. Tramèr MR, Moore RA, Reynolds DJ, McQuay HJ. Quantita- tive estimation of rare adverse events which follow a bio- logical progression: a new model applied to chronic NSAID use. Pain 2000;85:169-182.
17. García Rodríguez LA, Jick H. Risk of upper gastrointestinal bleeding and perforation associated with individual non-ster- oidal anti-inflammatory drugs. Lancet 1994;343:769-772.
18. Fries JF, Williams CA, Bloch DA, Michel BA. Nonsteroidal anti-inflammatory drug-associated gastropathy: incidence and risk factor models. Am J Med 199;91:213-222.
19. Piper JM, Ray WA, Daugherty JR, Griffin MR. Corticoste- roid use and peptic ulcer disease: role of nonsteroidal anti-in- flammatory drugs. Ann Intern Med 1991;114:735-740.
20. MacDonald TM, Morant SV, Robinson GC, et al. Association of upper gastrointestinal toxicity of non-steroidal anti-in- flammatory drugs with continued exposure: cohort study.
BMJ 1997;315:1333-1337.
21. Silverstein FE, Faich G, Goldstein JL, et al. Gastrointestinal toxicity with celecoxib vs nonsteroidal anti-inflammatory drugs for osteoarthritis and rheumatoid arthritis: the CLASS study: a randomized controlled trial. Celecoxib Long-term Arthritis Safety Study. JAMA 2000;284:1247-1255.
22. Bombardier C, Laine L, Reicin A, et al. Comparison of upper gastrointestinal toxicity of rofecoxib and naproxen in patients with rheumatoid arthritis. VIGOR Study Group. N Engl J Med 2000;343:1520-1528.
23. Brophy JM. Cardiovascular effects of cyclooxygenase-2 inhi- bitors. Curr Opin Gastroenterol 2007;23:617-624.
24. McCarthy DM. Prevention and treatment of gastrointestinal symptoms and complications due to NSAIDs. Best Pract Res Clin Gastroenterol 2001;15:755-773.
25. Pilotto A, Franceschi M, Leandro G, et al. Proton-pump in- hibitors reduce the risk of uncomplicated peptic ulcer in eld- erly either acute or chronic users of aspirin/non-steroidal an- ti-inflammatory drugs. Aliment Pharmacol Ther 2004;20:1091- 1097.
26. Chan FK, Ching JY, Hung LC, et al. Clopidogrel versus as-
Kim JW. NSAID-induced Gastroenteropathy 141
pirin and esomeprazole to prevent recurrent ulcer bleeding. N Engl J Med 2005;352:238-244.
27. Targownik LE, Metge CJ, Leung S, Chateau DG. The rela- tive efficacies of gastroprotective strategies in chronic users of nonsteroidal anti-inflammatory drugs. Gastroenterology 2008;
134:937-944.
28. Chan FK, Chung SC, Suen BY, et al. Preventing recurrent upper gastrointestinal bleeding in patients with Helicobacter pylori infection who are taking low-dose aspirin or naproxen.
N Engl J Med 2001;344:967-973.
29. Rugstad HE, Giercksky KE, Husby G, Holme I. Effect of ci- metidine on gastrointestinal symptoms in patients taking non- steroidal anti-inflammatory drugs. A large double-blind place- bo controlled study. Scand J Rheumatol 1994;23:177-182.
30. Bijlsma JW. Treatment of endoscopy-negative NSAID-in- duced upper gastrointestinal symptoms with cimetidine: an in- ternational multicentre collaborative study. Aliment Pharmacol Ther 1988;2(suppl 1):75-83.
31. Yeomans ND, Tulassay Z, Juhász L, et al. A comparison of omeprazole with ranitidine for ulcers associated with non- steroidal antiinflammatory drugs. Acid Suppression Trial:
Ranitidine versus Omeprazole for NSAID-associated Ulcer Treatment (ASTRONAUT) Study Group. N Engl J Med 1998;338:719-726.
32. Hawkey CJ, Karrasch JA, Szczepañski L, et al. Omeprazole compared with misoprostol for ulcers associated with non- steroidal antiinflammatory drugs. Omeprazole versus Miso- prostol for NSAID-induced Ulcer Management (OMNIUM) Study Group. N Engl J Med 1998;338:727-734.
33. Reuter BK, Wallace JL. NSAID enteropathy in rats: role of permeability, bacteria, and enterohepatic circulation. Gastroen- terology 1997;112:109-117.
34. Allison MC, Howatson AG, Torrance CJ. Gastrointestinal damage associated with the use of nonsteroidal anti-in- flammatory drugs. N Engl J Med 1992;327:749–754.
35. Davies NM. Review article: non-steroidal anti-inflammatory drug-induced gastrointestinal permeability. Aliment Pharmacol Ther 1998;12:303-320.
36. Thiefin G, Beaugerie L. Toxic effects of nonsteroidal antiin- flammatory drugs on the small bowel, colon, and rectum.
Joint Bone Spine 2005;72:286-294.
37. Berg RD. Bacterial translocation from the gastrointestinal tract. Adv Exp Med Biol 1999;473:11-30.
38. van Deventer SJ, ten Cate JW, Tytgat GN. Intestinal endoto- xemia. Clinical significance. Gastroenterology 1988;94:825- 831.
39. Krack A, Sharma R, Figulla HR, Anker SD. The importance of the gastrointestinal system in the pathogenesis of heart failure. Eur Heart J 2005;26:2368-2374.
40. Page J, Henry D. Consumption of NSAIDs and the develop- ment of congestive heart failure in elderly patients: an under- recognized public health problem. Arch Intern Med 2000;
160:777-784.
41. Feenstra J, Heerdink ER, Grobbee DE, Stricker BH. Associa- tion of nonsteroidal anti-inflammatory drugs with first occur- rence of heart failure and with relapsing heart failure: the Rotterdam Study. Arch Intern Med 2002;162:265-270.
42. Smecuol E, Bai JC, Sugai E, et al. Acute gastrointestinal per- meability responses to different non-steroidal anti-inflam- matory drugs. Gut 2001;49:650-655.
43. Ann JY, Kim SJ, Han SP, et al. Effect of glutamine on the non-steroidal anti-inflammatory drug-induced bacterial translo- cation. Korean J Gastroenterol 2004;44:252-258.
44. Hond ED, Peeters M, Hiele M, Bulteel V, Ghoos Y, Rut- geerts P. Effect of glutamine on the intestinal permeability changes induced by indomethacin in humans. Aliment Phar- macol Ther 1999;13:679-685.
45. Playford RJ, MacDonald CE, Calnan DP, et al. Co-admin- istration of the health food supplement, bovine colostrum, re- duces the acute non-steroidal anti-inflammatory drug-induced increase in intestinal permeability. Clin Sci (Lond) 2001;100:
627-633.
46. Kim JW, Jeon WK, Kim EJ. Combined effects of bovine co- lostrum and glutamine in diclofenac-induced bacterial trans- location in rat. Clin Nutr 2005;24:785-793.