약학회지 제
54
권제2
호102~105 (2010) Yakhak Hoeji Vol. 54, No. 2
102
에스트로젠 수용체알파에 의한 Hypoxia Inducible Factor-1의 전사 활성조절
유광희·이영주# 세종대학교 생명공학과
(Received September 24, 2009; Accepted December 3, 2009)
Activation of Hypoxia Inducible Factor-1 Alpha by Estrogen Receptor Alpha
KwangHee Ryu and YoungJoo Lee#
College of Life Science, Institute of Biotechnology, Department of Bioscience and Biotechnology, Sejong University, Seoul 143-747, Korea
Abstract
— Our previous results showed that hypoxia inducible factor-1 (HIF-1) activated estrogen receptor (ER) in the absence of ligand. In this study, we have studied the effect ER overexpression on the activation of HIF-1. ER overexpression induced transcription activation of hypoxia response element driven luciferase and vascular endothelial growth factor. As a negative control, the effect of ER on androgen receptor response element was used. Our result indicate that the two ER
αand HIF-1 signaling pathways shares part of the activation pathway.
Keywords □
hypoxia, ER
α, HIF-1, VEGF
저산소상태는혈관신생
,
에너지대사,
적혈구생성등세포내 다양한반응을조절한다.
1)저산소상태에서의대표적인조절인 자는hypoxia-inducible factor-1
α(HIF-1
α)
로정상상태에서는분해되어전사활성이없는반면저산소상태에서는안정화되어 산소항상성유지에필요한당대사
,
혈관신생에관련된유전자 들의발현을조절하는중요한역할을수행한다.
2)HIF-1
α는Aryl Hydrocarbon Receptor Nuclear Translocator(ARNT)
와dimer
로작용을한다
.
3)ARNT
단백질은HIF-1
α의파트너로서의역할 이외에도에스트로젠수용체의coactivator
로서도작용하고ARNT
의또다른파트너인
AhR
역시에스트로젠수용체와의결합을통하여작용을조절함이발표되었다
.
4,5)이러한일련의연구결과를통하여저산소의신호전달체계가에스트로젠수용체및기 타핵호르몬수용체의전사활성에영향을미친다는주요연구 결과들이축적되고있다
.
하지만역으로핵호르몬수용체가저산소의신호전달에영향을미친다는연구결과는아직거의없다
.
에스트로젠수용체는핵수용체
superfamily
의한멤버이며,
에 스트로젠에의해활성화되는전사인자이다.
6)에스트로젠의작용모델은세포내에있는에스트로젠수용체와호르몬이결합하여
특정 유전자의 거울상의 염기서열을 가진
15 bp
의 인핸서(hormone responsive element)
에결합하여basal transcription machinery
와각종coregulator
와결합하여전사활성을조절한다고알려져있다
.
6)여성호르몬인에스트로젠은난소에서생성 되어혈관을통해표적세포에도달하여단순확산에의해표적 세포내로들어가,
표적세포의핵내에존재하는전사인자인에스트로젠수용체를통하여표적유전자의전사활성도에영향을 미침으로써그기능을나타낸다
.
6)에스트로젠수용체는성장인 자경로와의cross-talk
에의한활성, DNA
결합없이AP-1
과의interaction
에의한 활성,
세포막에존재하는 수용체를통한nongenomic
경로등에의해서도세포내여러작용에영향을미친다고알려져있다
.
7-9)많은연구결과들에의해에스트로젠의신호전달체계에관여하는약
300
종류의단백질들과복잡한조 절기전이밝혀져있다.
10)에스트로젠수용체는유방암세포성장에관여하는많은유전 자와신호를조절함으로써유방암의발달과진행에매우중요한 역할을한다
.
11)에스트로젠수용체는유방암의치료와진행추이를결정하는데매우중요한요소이다
.
11)최근저산소에의해에스트로젠수용체단백질이조절된다고보고된바있으며
,
에스 트로젠수용체양성유방암에서HIF-1
알파의양이높다는관찰이보고된바도있다
.
12,13)그리고HIF-1
α양성유방종양에서에스트로젠수용체의농도가적음도관찰되었다
.
13)이러한일련의#본논문에관한문의는저자에게로
(
전화) 02-3408-3640 (
팩스) 02-3408-4334 (E-mail) yjlee@sejong.ac.kr
종설
에스트로젠수용체알파에의한
Hypoxia Inducible Factor-1
의전사활성조절103
Vol. 54, No. 2, 2010
관찰은저산소와 에스트로젠수용체가상호 조절 함으로서
tumorigenesis
에영향을미칠수있다는가능성을의미한다.
본논문에서는에스트로젠수용체알파가저산소신호에영향을미 치는가능성에대해고찰해보았다
.
실험방법
실험재료
E
2는Sigma(St. Louis, MO, USA)
에서구입하였고, 100%
에탄올에녹였다
. RPMI
역시Sigma(St. Louis, MO, USA)
에서구입하였고
, Fetal Bovine Serum(FBS), Trizol Reagent,
그리고penicillin/streptomycin
은GIBCO Invitrogen(Grand Island, NY, USA)
에서구입하였다.
또한HRE-Luc DNA
는서울대학교김규원박사님께제공받았으며
, ARE-Luc DNA
는Rochester
대학 의Dr. Chawnshang Chang
에게제공받았다.
세포배양및저산소처리
본실험에서는유방암세포주인
MCF-7
세포주를사용하였다. MCF-7
세포주는10% FBS
을함유하는RPMI
에서배양하였다.
플라스미드의트랜스팩션에는
PEI(Polysciences)
를사용하였다.
배지는
1~2
일간격으로교환하고시약을처리할때새배지로갈아주었으며
,
약물을처리시에는최소24
시간이상석탄으로처리한혈청을사용한배지에서배양한후약물을처리하였다
.
대 조군에는에탄올용매를처리하였다.
저산소상태에서의세포는5%
의CO
2level
과1%
미만의O
2그리고N
2로balance
가맞춰진
Hypoxia chamber(Forma)
를사용하여배양하였다.
루시퍼라아제활성측정
플라스미드를트랜스팩션한 세포를
PBS
로세척하고lysis buffer(125 mM Tris pH 7.8, 10 mM CDTA, 10 mM DTT, 50% glycerol, 5% Triton X-100)
를넣고세포를파괴한후상층액을얻었다
.
루시퍼라아제활성측정은20
µlcell extract
에20
µlassay buffer(Promega)
를가한후light emmision
을Luminometer (LUMAT LB 9501/16)
를사용하여20
초간측정하였다.
RNA분리및 Reverse Transcription-Polymerase Chain Reaction(RT-PCR)
Total RNA
추출은Trizol Reagent(Invitrogen)
를이용하였다. cDNA
합성은5
µg
의total RNA
와Random primer(Promega),
그리고
8
µlDEPC
처리된물을넣고70
oC
에서5
분동안둔다.
그리고
40 unit
의M-MuLV
역전사효소(Promega), 5× reaction buffer(250 mM Tris-HCl; pH 8.3 at 25
oC, 375 mM KCl, 15 mM MgCl
2, 50 mM DTT)
와1 mM dNTP mixture,
그리고ribonuclease inhibitor 20 unit
을넣고37
oC
에서1
시간반응시키고
70
oC
에서10
분동안반응시킨다.
만들어진cDNA 2
µl, 10×
buffer(100 mM Tris-HCl; pH 8.3 at 25
oC, 500 mM KCl, 15 mM MgCl) 5
µl, 25 unit
의rTaq polymerase(Takara, Japan), 4
µl의2.5 mM dNTP mixture, 100 pmoles
의primer(Geno Tech), total volume 50
µl로PCR
을하였다.
β
-actin, VEGF, ER
α의oligonucleotide
서열은 β-actin:
sense; 5'-CCTGACCCTGAAGTACCCCA-3', antisense; 5'- CGTCATGCAGCTCATAGCTC-3', VEGF: sense; 5'-ATGAA- CTTTCTGCTCTCTCTGG-3', antisense; 5'-TCATCTCTCCT- ATGTGCTGGC-3', ER
α: sense; 5'-CATAACGACTATATGT- GTCCAGCC-3', antisense; 5'-AACCGAGATGATGTAGCCAG- CAGC-3'
이다.
그리고VEGF
와ER
α의PCR
조건은다음과같다. 94
oC
에서3
분, 94
oC 45
초, 55
oC 45
초, 72
oC 45
초(24 cycle),
마지막으로
72
oC
에서10
분간 반응시킨다.
그리고 β-actin
은20 cycle
로조건을잡았다.
이는 β-actin
을20 cycle
이상으로할경 우포화상태에이르러정량분석을하기가힘들기때문이다.
정량적분석은각실험
sample
의cDNA
를희석하는방법을사용 하였다. PCR
산물은2% gel
로전기영동하여분석하였다. bands
의상대적강도는
Gel Doc 2000(BIO-RAD, USA)
을통해정량화되었다
.
실험결과 및 고찰
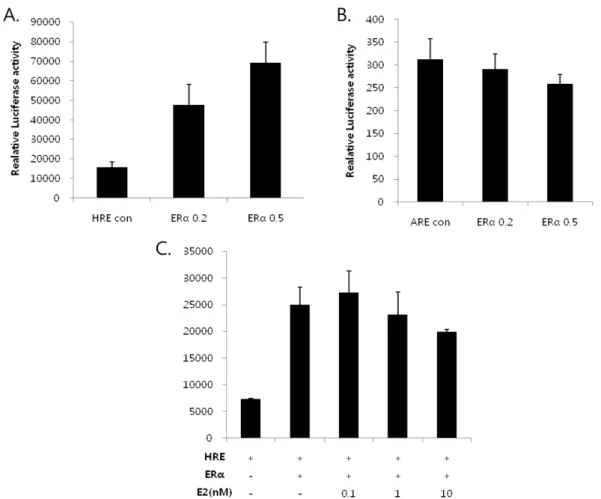
에스트로젠수용체알파에의한Hypoxia Response Element (HRE)-Luciferase의증가
HRE(Hypoxia Response Element)-Luciferase
와에스트로젠 수용체알파플라스미드를293
세포에농도별로24 h transfection
하여
HRE-luciferase
활성을측정한결과luciferase
의활성이증가하였다
(Fig. 1A).
하지만Androgen Response Element (ARE)-Luciferase
와에스트로젠수용체알파플라스미드를함께transfection
하여negative control
로실험한ARE-luciferase
측 정결과에서는luciferase
의활성이보이지않았으며(Fig. 1B),
에스트로젠수용체알파의
ligand
로알려진E2
를같이처리하여
HRE-luciferase
를측정하였을때synergy
한활성효과는관 찰할수없었다(Fig. 1C).
이결과들은에스트로젠수용체의과발현이
HIF-1
에의한전사에영향을미칠수있다는것을제시한다
.
에스트로젠 수용체 알파에 의한 Vascular Endothelial Growth Factor(VEGF)발현
VEGF(Vascular Endothelial Growth Factor)
는성체에서혈관 생성뿐만아니라배아발달과정에서혈관발달을조절하는중요한 인자이며, HIF-1
α와ARNT
가interaction
을이뤄HRE
서열부위 에결합하여발현되는것으로알려져있다.
14)에스트로젠수용104
유광희·이영주J. Pharm. Soc. Korea
체알파가발현되는
cell line
이며,
유방암세포인MCF-7
세포에에스트로젠 수용체 알파 플라스미드를
1
µg
의 농도로24 h trnasfection
하여과발현시켰으며,
저산소상태에서HIF-1
에의해발현되는
VEGF
의mRNA
발현정도를RT-PCR
로측정하였 다.
그결과에스트로젠수용체알파의과발현에의해서도VEGF
의
mRNA
가발현되는것을볼수있었다(Fig. 2).
Fig. 1 −
HRE-luciferase activation was assessed by cotransfection of the ER
α(0.2, 0.5
µg) with either HRE-luciferase (A) or ARE-luciferase (B) expression plasmids in HEK 293 cells, using the PEI method. At 24 h post-transfection, cells were treated with 0.1, 1 and 10 nM E
2(C). Cell extracts were prepared by reporter lysis buffer and analyzed using a luciferase assay.
Fig. 2 −
MCF-7 cells were transiently transfected with ER
αusing the PEI method. Total RNA was prepared and analyzed for
ER
α, VEGF and
β-actin mRNA expression by RT-PCR.
Fig. 3 −HEK 293 cells were transiently transfected with ER
α(0.2,
0.5
µg) and HRE-luciferase using the PEI method. At 24 h
post-transfection, cells were incubated for 24 h hypoxic
condition. Cell extracts were prepared by repoter lysis
buffer and analyzed using a luciferase assay.
에스트로젠수용체알파에의한
Hypoxia Inducible Factor-1
의전사활성조절105
Vol. 54, No. 2, 2010
저산소상태에서에스트로젠수용체알파의활성변화 저산소상태에서
HRE
와에스트로젠수용체알파를293 cell
에농도별로
24 h transfection
하여HRE-luciferase
를측정한결 과normoxia
상태와는다르게HRE-luciferase
의활성이약하게저하되는것을관찰할수있었다
(Fig. 3).
이러한결과는에스트 로젠수용체알파가정상상태와저산소상태에서HIF-1
에미치 는영향이다름을의미한다.
결 론
우리는
Normoxia
상태에서Hypoxia Response Element
(HRE)
부위에에스트로젠수용체알파가관여를하여HRE-
luciferase
의활성을 증가시키는것을보았다.
다른Response
Element
부위에서는에스트로젠수용체알파가어떠한관여도하지않는것으로보이며
, ligand
인E2
역시HRE-luciferase
의 활성을추가적으로증가시키지못하는것으로밝혀졌다.
또한에스트로젠수용체알파의과발현은저산소상태에서
HIF-1
에의해조절되는
VEGF
와같은유전자를발현시켰다.
그러나저산소상태에서에스트로젠수용체알파에의한
HRE-luciferase
활성증가는
Normoxia
상태와는달리약한감소를보였다.
이러한결 과는에스트로젠수용체와HIF-1
α가서로작용이있음을의미하며그상호작용이정상상태와저산소상태에서동일하지않 음을암시한다
.
에스트로젠수용체와HIF-1
α의상호작용에대 해서는향후추가연구가요구된다.
감사의 말씀
이논문은
2008
년도세종대학교교내연구비지원에의한논문임.
참고문헌
1) Taylor, C. T. and Colgan, S. P. : Therapeutic targets for hypoxia- elicited pathways. Pharm. Res.
16, 1498 (1999).
2) Ohtake, F., Takeyama, K., Matsumoto, T., Kitagawa, H., Yamamoto, Y., Nohara, K., Tohyama, C., Krust, A., Mimura, J., Chambon, P., Yanagisawa, J., Fujii-Kuriyama, Y. and Kato, S. : Modulation of oestrogen receptor signalling by association with the activated dioxin receptor. Nature
423,545 (2003).
3) Wang, G. L., Jiang Bing-Hua., Rue, E. A. and Semenza, G. L. : Hypoxia-inducible factor 1 is a basic-helix-loop-helix-PAS
heterodimer regulated by cellular O
2tension. Proc. Natl. Acad.
Sci. USA
92, 5510 (1995).
4) Brunnberg, S., Pettersson, K., Rydin, E., Matthews, J., Hanberg, A. and Pongratz, I. : The basic helix-loop-helix-PAS protein ARNT functions as a potent coactivator of estrogen receptor-dependent transcription. Proc. Natl. Acad. Sci. USA
100
, 6517 (2003).
5) Gu, Y.-Z., Hogenesch, J. B. and Bradfield, C. A. : The PAS superfamily: sensors of environmental and developmental signals. Annu. Rev. Pharmacol. Toxicol.
40, 519 (2000).
6) Nilsson, S., Makela, S., Treuter, E., Tujague, M., Thomsen, J., Andersson, G., Enmark, E., Pettersson, K., Warner, M. and Gustafsson, J. A. : Mechanisms of estrogen action. Physiol.
Rev.
81, 1535 (2001).
7) Kato, S. : Estrogen receptor-mediated cross-talk with growth factor signaling pathways. Breast Cancer
8, 3 (2001).
8) Weatherman, R. V. and Scanlan, T. S. : Unique protein determinants of the subtype-selective ligand responses of the estrogen receptors (ERalpha and ERbeta) at AP-1 sites. J. Biol.
Chem.
276, 3827 (2001).
9) Kelly, M. J. and Levin, E. R. : Rapid actions of plasma membrane estrogen receptors. Trends Endocrinol Metab.
12, 152 (2001).
10) Lonard, D. M. and O'Malley, B. W. : Nuclear receptor coregulators: judges, juries, and executioners of cellular regulation. Mol. Cell.
27, 691 (2007).
11) Shao, W. and Brown, M. : Advances in estrogen receptor biology: prospects for improvements in targeted breast cancer therapy. Breast Cancer Res.
6, 39 (2004).
12) Stoner, M., Saville, B., Wormke, M., Dean, D., Burghardt, R. and Safe, S. : Hypoxia induces proteasome-dependent degradation of estrogen receptor alpha in ZR-75 breast cancer cells. Mol. Endocrinol.
16, 2231 (2002).
13) Bos, R., Zhong, H., Hanrahan, C. F., Mommers, E. C., Semenza, G. L., Pinedo, H. M., Abeloff, M. D., Simons, J. W., van Diest, P. J. and van der Wall, E. : Levels of hypoxia- inducible factor-1 alpha during breast carcinogenesis. J. Natl.
Cancer Inst.
93, 309 (2001).
14) Kazi, A. A. and Koos, R. D. : Estrogen-induced activation of hypoxia-inducible factor-1 alpha, vascular endothelial growth factor expression, and edema in the uterus are mediated by the phosphatidylinositol 3-kinase/Akt pathway. Endocrinology
148