의학 석사학위 논문
파킨슨병치매
환자에게
콜린분해효소억제제
치료를
한
뒤
보이는
뇌포도당대사의
변화
아 주 대 학 교 대 학 원
의 학 과
용 석 우
파킨슨병치매
환자에게
콜린분해효소억제제
치료를
한
뒤
보이는
뇌포도당대사의
변화
지도교수 주 인 수
이 논문을 의학 석사학위 논문으로 제출함.
2008
년 8 월
아 주 대 학 교 대 학 원
의 학 과
용 석 우
용석우의
의학
석사학위
논문을
인준함
.
인준서 원본필요
감사의
감사의
감사의
감사의
글
글
글
글
논문 착수 때부터 이번 논문이 완성될 때까지 성심으로 지도해 주신 주인수 선생님께 가장 먼저 감사를 드립니다. 선생님께서는 늘 훌륭한 교육자이자 정신적으로도 든든한 후원자이셨습니다. 또한 바쁘신 일정 중에도 아낌없는 지도 편달을 해주신 조기홍 선생님, 김병곤 선생님, 그리고 이필휴 선생님께도 깊은 감사를 드립니다. 논문의 진행과 결과의 도출에 큰 도움을 주신 안영실 선생님 또한 깊은 감사를 드립니다. 이 논문을 준비해온 지난 3 년은 개인적으로 큰 변화를 겪은 시절이었습니다. 전공의 시절을 마치고 전문의 시험을 통과한 뒤 연구강사 시절을 거쳐 대우전임강사로 신분이 변하였습니다. 존경해 마지않는 두 분의 스승님을 더 이상 곁에서 모시지 못하게 되었고, 사랑하는 아내를 맞아 결혼을 하고 새 가정을 시작하였습니다. 주변의 많은 분들의 도움으로 이런 변화의 시기를 무사히 통과할 수 있었습니다. 우선 신경과 의사가 된 시점부터 저에게 일종의 표상이신 허균 선생님, 저에게 둘도 없는 동료이자 재산인 아주대병원 신경과 의국 선후배님께 진심으로 감사를 드립니다. 특히 이진수 선생님과 신동훈 선생님은 계속된 학술적인 교류를 통해 서로를 성장시켜 올 수 있었다는 점에서 각별하게 생각합니다. 마지막으로 오늘의 저를 있게 해주신 부모님과, 미래의 삶을 계속 같이할 사랑하는 아내에게 진심으로 고마운 마음을 전합니다.i - 국문요약 -
파킨슨병치매
파킨슨병치매
파킨슨병치매
파킨슨병치매 환자에게
환자에게
환자에게
환자에게 콜린분해효소억제제
콜린분해효소억제제
콜린분해효소억제제 치료를
콜린분해효소억제제
치료를
치료를
치료를 한
한
한 뒤
한
뒤
뒤
뒤
보이는
보이는
보이는
보이는 뇌포도당대사의
뇌포도당대사의
뇌포도당대사의 변화
뇌포도당대사의
변화
변화
변화
파킨슨병치매는 파킨슨병 환자의 약 40%에서 나타나며, 주로 주의집중력의 장애, 기억력 장애, 집행기능 장애를 보인다. 알츠하이머병에서 사용되는 콜린분해효소억제제가 파킨슨병치매 환자에서도 인지 기능을 호전시키는 효능이 있는 것으로 알려져 있으나, 이러한 치료 효과를 기능적인 두뇌 영상에서 분석하고자 한 시도는 거의 없었다. 이에 저자는 11 명의 파킨슨병치매 환자를 대상으로 donepezil 혹은 galantamine 으로 치료를 하기 전과 치료를 한 뒤의MMSE 와 F18-FDG PET 영상을 분석하였다. 결과적으로 환자들은 MMSE
점수에서 평균 5.5 점의 향상을 보였고, 특히 기억력, 계산력 검사에서 호전 소견이 두드러졌다. PET 영상을 SPM 을 사용하여 비교한 결과 치료를 받은 후의 영상에서 좌뇌의 상/중간전두고랑(superior / middle frontal gyrus)과 각이랑/모서리위이랑(angular / supramarginal gyrus)의 포도당대사 증가소견과, 우뇌의 내측 측두엽(medial temporal bobe)의 포도당대사 감소소견을 관찰할 수 있었다. 특히 MMSE 의 호전정도와 우뇌의 내측 측두엽의 포도당대사 저하 정도에서 유의한 상관관계를 나타내었다. 이러한 포도당대사의 변화 소견은 알츠하이머병에서 보이는 소견과 비슷하며, 따라서 두 개의 병이 서로 다른
ii 증상과 병리를 보임에도 불구하고, 콜린분해효소억제제의 치료 효과는 두 개의 병에서 비슷한 기전을 갖고 있다고 생각된다. ________________________________________________________________________ 핵심어 핵심어핵심어 핵심어 ; 파킨슨병치매, 콜린분해효소억제제, 18 F-FDG PET
iii
차례
차례
차례
차례
국문요약 ………. i 차례 ……… iii 그림차례 ……….... v 표차례 ……… vi I. 서론 ……… 1 II. 재료 및 방법 ……….. 4 A. 대상 ……….……… 4 B. 연구 과정 ……… 6 C. 18F-FDG PET/CT 영상 ……… 6 D. 두뇌 당대사의 통계적 모수 지도화 (SPM) 분석……… 7 1. 치료 전과 후의 당대사의 비교 분석 ……… 7 2. 포도당대사변화와 MMSE 가 상관관계가 있는 부위의 분석 ……… 8 III. 결과 ………. 9 A. 환자군의 특성 ……… 9 B. MMSE 검사결과 ……… 11 C. 두뇌 포도당대사의 SPM 분석 결과 ……… 13 IV. 고찰 ……… 16 V. 결론 ……… 21 참고문헌 ……… 22iv
v
그림
그림
그림
그림 차례
차례
차례
차례
Fig. 1. Statistical parametric maps showing the spatial distribution of significant metabolic increase (Puncorrected< 0.001) after cholinesterase therapy in patients with Parkinson’s
disease dementia ………14
Fig. 2. Statistical parametric maps showing the spatial distribution of significant metabolic decrease (Puncorrected< 0.001) after cholinesterase therapy in patients with
Parkinson’s disease dementia ……… 14
Fig. 3. Statistical parametric maps showing the regions where significant metabolic decrease is seen when correlated with increase in MMSE score by using conditions and covariates method Puncorrected< 0.005)……… 15
vi
표
표
표
표 차례
차례
차례
차례
Table 1. Detailed information of 11 patients included in this study ……… 10
Table 2. Comparison of MMSE (Mini-mental state examination) results in patients before and after cholinesterase inhibitor therapy ……… 12
Table 3. Areas showing significant difference in glucose metabolism after cholinesterase therapy in patients with Parkinson’s disease dementia ……… 13
1
I. 서론
서론
서론
서론
파킨슨병은 가장 흔한 신경계 퇴행성 질환의 하나로서, 65 세 이상의 인구에서의 유병율이 약 2%에 달한다고 알려져 있다. 파킨슨병에서 두드러지는 증상은 보통 진전(손, 발, 두부의 떨림), 서동(움직임의 시작이 느리고 지속이 되지 않음), 경직(사지와 경부가 뻣뻣해짐) 등으로 대표되는 운동계 증상상상상이지만, 여러 가지 비운동계 증상도 자주 동반된다. 그 중에 한 증상이 치매인데, 파킨슨병 치매는 전체 파킨슨병 환자의 약 40%에서 나타나는 것으로 보고되었으며, 이는 일반인에 비해 약 4 배에서 6 배 정도로 높은확률이다( Byrne 등, 1991; Hughes 등, 2000; Aarsland 등, 2002; Emre 등, 2007).
파킨슨병 치매에서 동반되는 인지 기능 장애의 양상은 비교적 잘 연구되어 있다. 대부분 주의집중력의 장애를 보이며(Beatty 등, 2003; Rahkonen 등, 2003),
기억력 장애로 인하여 새로운 정보를 학습하는 능력도 저하되나,
알츠하이머병만큼 심하지는 않다(Aarsland 등, 2001). 또한 자유 연상 (free recall) 능력이 저하되나, 재인 검사 (recognition)에서는 상당히 호전되는 점도 알츠하이머병과의 차이이며(Pillon 등, 1993), 이는 파킨슨병 치매 환자들이 새로운 정보를 저장을 시키는 능력은 보존되어 있으나, 이를 인출하는 단계에서 장애가 있음을 시사한다. 위의 장애들보다도 더욱 두드러지는 파킨슨병 치매의 특징은 집행기능 장애(dysexecutive function)이다(Ballard 등, 2002; Rahkonen 등, 2003). 치매가 동반되지 않은 파킨슨병 환자에서 조차도 어느 정도의 집행기능 장애가
2 자주 동반되는 것으로 알려져 있으며 규칙 발견, 문제 해결 능력, 계획 수립능력, set-shifting 등의 장애가 모두 보이게 된다. 시공간 능력의 장애(Pillon 등, 1991), 언어 유창성의 장애 역시 자주 나타나는 것으로 알려져 있으나(Stern 등, 1993), 다른 언어 장애나 실행증은 잘 동반되지 않는 특징이 있다. 파킨슨병에서 치매가 잘 동반되는 기전은 명확하지 않다. 치매와 연관된 병리소견으로 제시되는 것에는 크게 세 가지의 주장이 존재해 왔는데, 흑질과 뇌간의 병리가 원인이라는 가설과, 변연계와 신피질에 존재하는 루이소체가 원인이라는 가설, 그리고 마지막으로 루이 소체와 동반되어 나타나는 알츠하이머 병리가 원인이라는 가설이다. 그러나 alpha-synuclein 면역조직화학염색을 통하여 루이소체를 좀 더 잘 관찰할 수 있게 된 이후로는(Spillantini 등, 1997), 알츠하이머 병리보다는 신피질의 루이소체가 가장 파킨슨병 치매와 연관이 깊은 병리로 받아들여지는 추세이다(Emre 등, 2007). 파킨슨병 치매환자에게서는 치매가 동반되지 않은 파킨슨병 환자보다 신피질에서의 도파민 농도가 감소되어 있어(Scatton 등, 1983), 중뇌피질 도파민성 회로(mesocortical dopaminergic pathway)의 이상이 있을 것으로 추측된다. 또한, MPTP 의 독성으로 인해 도파민계에만 국한된 신경손상을 받은 환자에서도 인지기능의 장애가 관찰되며(Stern 등, 1990), 따라서 도파민의 감소가 인지기능의 저하와 연관이 있음은 분명한 사실인 듯하다. 그러나, 인지기능의 저하 정도와 도파민 결핍에 의해서 나타나는 서동이나 경직 등의 운동 증상과 잘 비례하지 않고, 도파민 치료에 의해 인지기능의 호전이 잘 보이지 않아 단순히 도파민의 결핍만으로 치매의 기전을 설명하기에는 무리가 있다. 이에 따라 최근에는 도파민보다는 아세틸콜린의 결핍이 치매의 발생에 더 큰 역할을 하는 것으로
3
주목 받고 있다. 파킨슨병 환자의 경우 마이너트기저핵(basal nucleus of Meynert)의 신경세포 소실과 신피질에서의 콜린성 활동의 저하가 있는데, 인지기능저하의 정도와 이러한 콜린계 신경세포의 변성과 밀접한 연관이 있는 것으로 밝혀졌다( Whitehouse 등, 1983 ;Perry 등, 1985). 이러한 사실이 밝혀지면서 여러 가지의 콜린분해효소억제제 (cholinesterase inhibitors)의 효능에 대한 연구가 이루어졌고, 어느 정도의 효과가 있는 것으로 나타났다. Hutchinson 등이 tacrine 치료로 6 명의 파킨슨병 치매 환자에서의 인지 기능이 호전되었음을 1996 년에 발표한 것을 시작으로(Hutchinson 와 Fazzini, 1996), rivastigmine(Reading 등, 2001; Emre 등, 2004; Burn 등, 2006), donepezil(Aarsland 등, 2002; Bergman 와 Lerner, 2002; Fabbrini 등, 2002; Leroi 등, 2004), galantamine(Aarsland 등, 2003) 치료 모두에서 인지기능의 향상이 있음을 보고하였다. Mini-mental state examaination(MMSE)과 같이 전반적인 인지 기능의 평가에서도 호전이 보였고(Reading 등, 2001; Aarsland 등, 2002; Aarsland 등, 2003; Emre 등, 2004), 특히 기억력 점수에서 호전이
되거나(Leroi 등, 2004), 주의집중력과 집행기능의 장애가 개선되기도
하였다(Emre 등, 2004).
알츠하이머병의 경우 이러한 치료를 통해 호전되는 임상 양상을 PET 이나 기능적 자기공명영상(functional MRI)과 같은 기능적 영상(functional imaging)에서 보이는 변화와 비교하여 분석하고자 하는 연구가 많이 시도되어 왔다(Mega 등, 2001; Potkin 등, 2001; Goekoop 등, 2006; Stefanova 등, 2006; Teipel 등, 2006; Venneri, 2007). 그러나 파킨슨병 치매 환자에게서 약물치료를 한 뒤에 이러한 기능적 영상에서 어떠한 변화가 보이는 지에 대해서는 연구된 바가 거의 없다. 저자들은 본 연구에서 파킨슨병 치매 환자와, 치매가 없는 파킨슨병 환자에서 PET 영상을
4 분석하고, 또한 파킨슨병 치매 환자의 치료 전후의 PET 영상을 비교분석 하고자 한다. 이를 통하여 파킨슨병 치매의 치료에 의한 뇌의 당대사의 변화를 관찰함으로서, 약물이 가져오는 인지 기능의 호전이 영상에도 반영되는 지를 조사할 것이다. 또한 이를 토대로 하여, 아직 확실하게 밝혀지지 않은 파킨슨병 치매의 병태생리를 이해하는데 있어서 실마리를 제공하고자 한다.
5
II. 재료
재료
재료 및
재료
및
및
및 방법
방법
방법
방법
A. 대상
아주대학교 병원 신경과에서 진단 받은 11명의 파킨슨병 치매환자를 대상으로 하였다. 파킨슨병의 진단은 UK Parkinson’s Disease Society Brain Bank 진단기준을 만족할 경우로 했다(Hughes등, 1992). 파킨슨병 치매는 파킨슨병의 진단 기준을 만족하는 환자가운데 DSM-IV에 의한 치매의 정의에 부합하는 인지기능의 저하를 보이는 자로서, 파킨슨 증상이 발현된 후 적어도 1년 이상이 경과한 뒤 처음으로 인지기능의 저하 증상이 나타난 경우로 정의한다. 치매의 진단을 위한 자세한 신경심리학적 검사를 진행하고, 파킨슨병 치매가 아닌 다른 인지기능의 장애를 일으키는 이차적인 원인이 없는 지에 대해 조사하였는데, 여기에는 갑상선 기능 검사, 비타민 B12, 엽산, 매독 혈청검사와, 두뇌 자기공명영상(MRI) 검사가 포함되었다. Beck의 우울증 척도를 통해 16점 이상의 우울증상을 보이는 환자는 배제하였다. 또한 이전에 항콜린약제나 콜린분해효소억제제를 복용한 환자도 배제하였다. 그러나 레보도파, 도파민 효능제(dopamine agonists), monoamine oxidase 억제제를 투여 받은 기왕력의 경우는 연구에서 배제하지 않았다. 파킨슨병과 파킨슨 증후군의 구별이 명확치 않을
경우 심근 123
I-metaiodobenzylguanidine (MIBG) 단일광자방출전산화단층촬영 (SPECT)의 검사 결과를 참조하였다. 세시간 뒤의 지연영상에서 심장 대 종격동의 방출계수의 비율이 정상치에서 2 표준편차 이상 감소할 경우에만
6 파킨슨병에 합당한 것으로 간주하였다(Lee등, 2006). B. 연구과정 환자들은 처음 진단 당시에 MMSE를 시행하였고, 첫 번째 18 F-fluorodeoxyglucose(FDG) PET를 촬영한 뒤 콜린분해효소억제제를 복용하였다. 약물은 하루 일회의 donepezil 5mg으로 시작하여 4주간 복용하였고, 증상에 호전이 보이지 않을 경우 10mg으로 증량하였다. Denepezil에 부작용이 있는 경우 galantamine 4mg으로 바꿔서 처방을 하였다. 레보도파나 도파민 효능제와 같은 파킨슨 증상을 호전시키는 약물은 각 환자의 운동증상에 따라 조절하였다. 연구의 종결은 환자가 콜린분해효소억제제로 3개월 이상의 치료를 하였고, 환자나 보호자들이 인지기능에서 호전이 있다고 보고하였을 때로 하였다. 이 두 가지 조건을 만족하면 두 번째 MMSE와 18 F-FDG PET검사를 시행하였다. C. 18F-FDG PET/CT 영상
PET 는 Discovery ST scanner (General Electric Medical Systems, USA)를 사용, 4 시간 금식 후 300 MBq 의 18F-fluorodeoxyglucose (FDG)를 정주한 뒤 촬영하였다. 주사 후 환자들은 30 분간 가만히 누워 안정을 취하도록 지시되었다. 먼저 전산화 단층촬영(computed tomography ; CT)을 시행하고 (tube-rotation time ; revolution 당 1 초; 120 kV; 70 mA; rotation 당 5mm), 곧바로 3 차원 모드로 프레임당
7
reconstruction)으로 재구성하였으며, CT data 를 이용하여 감쇠보정(attenuation correction)하였다.
D. 두뇌 당대사의 통계적 모수 지도화 (Statistical Parametric Mapping ; SPM) 분석
1. 치료 전과 후의 당대사의 비교 분석
PET 영상을 MATLAB 7.1 소프트웨어(Mathworks Inc., Natick, MA, U.S.A)를 사용하여 SPM2(Statistical Parametric Mapping 2, Institute of Neurology, University of London, U.K.)에 의해 제공된 표준 템플릿에 공간적으로 표준화 시킨다. 표준화된 데이터는 신호 대 잡음 비율을 향상시키기 위해 16mm FWHM (full-width at half-maximum) 가우시안 커널(Gaussian Kernel)로 평편화 하였다. 통계적인 분석은 치료전 영상과 치료후 영상 그룹간에 voxel-by-voxel 로 paired t-test 를 사용하여 SPM 영상을 만들어 비교하였다. 높이역치(height threshold)는 P<0.001(uncorrected for multiple comparison)로 하였고, 범위역치(extent threshold)는 Ke≥100 을 기준으로 하였다. 통계적으로 t-score 가 의미 있는 부위를 3 차원 두뇌모형이나 SPM2 에 의해 제공된 고해상도 MRI 템플릿 위에 투사하여 영상화하였다. 각 부위의 MNI 좌표(Montreal Neurological Institute coordinate)는 AAL(anatomical automatic labeling, GIN, UMR6095, CYCERON, Caen, France)를 이용하여 구하였다.
8
위에서 얻은 표준화 된 데이터와 MMSE 에서의 호전 정도를 conditions and covariates method 를 사용하여 통계적으로 유의한 부위를 구한다. 역시 위에서와
9
III. 결과
결과
결과
결과
A. 환자군의 특성 이번 연구에 대상이 된 11 명 환자의 특성은 다음과 같다. (Table 1) 남성이 6 명, 여성이 5 명이었으며 평균 나이는 74.5±4.3 세였다. 파킨슨병의 유병 기간은 평균 6.7±4.1 년이었고, 치매 증상의 유병 기간은 짧게는 3 개월에서 길게는 24 개월로 다양했다. 모든 환자가 levodopa 를 복용 중이었고, 5 명이 추가로 entacapone 을, 1 명은 ropinirole 을 복용 중이었다. 평균 치료 기간은 8.4±4.5 개월이었으며, 10 명의 환자는 donepezil 로(5mg ; 6 명, 10mg ; 4 명) 치료하였고, 한 명의 환자는 galantamine 4mg 으로 치료받았다. 일곱 명의 환자에서 좀 더 정확한 파킨슨병의 진단을 위하여 123 I-MIBG SPECT 촬영을 하였고, 표에서와 같이 모든 환자에서 유의한 감소 소견을 보였다. (이 검사는 본 연구가 시작되기 이전에 파킨슨병을 초기에 진단할 때 이루어진 것이다.)10
Table 1. Detailed information of 11 patients included in this study
Name Sex Age (years) Parkinson Medications (mg) 파킨슨 증상(년) 치매 증상(월) MMSE Cholinesterase Inhibitor (mg) 치료기간 (월) MIBG 1 장OO M 81 La 600 / Rb 6 14 4 15 Donepezil 5mg 6 1.4 2 박OO F 78 L 450 5 24 22 Donepezil 10mg 8 3 이OO M 75 L 600 3 6 16 Donepezil 10mg 6 1.16 4 이OO F 72 L 300 10 18 12 Galantamine 4mg 16 5 홍OO M 68 L 450 / Ec 600 3 3 21 Donepezil 5mg 7 1.27 6 바OO F 67 L 450 2 5 20 Donepezil 5mg 17 7 김OO F 77 L 600 / E 800 10 3 16 Donepezil 5mg 8 1.28 8 홍OO M 78 L 600 / E 800 3 6 19 Donepezil 10mg 10 1.14 9 박OO F 77 L 450 10 9 17 Donepezil 5mg 8 10 윤OO M 73 L 450 / E 600 4 12 23 Donepezil 5mg 3 1.29 11 이OO M 73 L 700 / E 800 10 12 22 Donepezil 10mg 3 1.1
11 B. MMSE 검사 결과
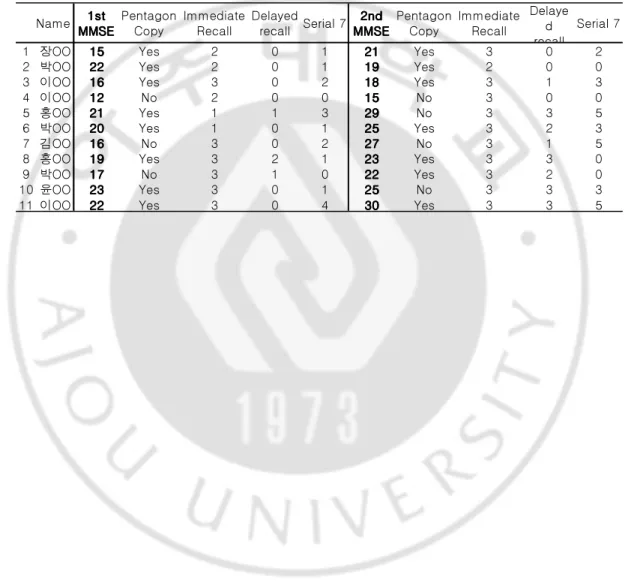
환자들이 콜린분해효소억제제 치료 전과 치료 후에 받은 MMSE 의 검사 결과는 다음과 같다.(Table 2) 약물 치료 전의 MMSE 는 17.6±4.0 점이었고, 약물 치료 후의 MMSE 는 23.1±4.7 로 유의하게 증가했다. (p=0.002, paired sample t-test) 다시 말해 약 8.4 개월의 치료 후에 MMSE 점수가 5.5 점 정도 향상된 것으로서, 이는 이전에 파킨슨병 치매 환자를 대상으로 한 연구들보다(Reading 등, 2001; Aarsland 등, 2002; Leroi 등, 2004) 월등한 성적이다. 이러한 차이는 본 연구에서 비교적 치료의 기간이 길었고, 또한 환자나 보호자가 약물의 효과가 있다고 보고한 시점에서 다시 검사를 하였기 때문이라고 생각된다. 실제로 본 연구에서는 11 명의 환자 중 #2 환자를 제외한 10 명의 환자에서 MMSE 의 호전을 보였는데, 이것 또한 이전의 연구보다 높은 확률이었다.
MMSE 점수 중에서도 immediate recall, delayed recall, serial 7 에서 호전의 소견이 뚜렷하였다. Immediate recall 의 경우 5 명에서 하나 이상을 따라 하지 못했던 첫 검사와 달리 두 번째에는 1 명이 하나를 따라 말하지 못했다. Delayed recall 에서는 8 명이 하나도 대답하지 못했던 첫 검사와 달리, 두 번째에는 3 명만이 하나도 대답을 못했고, 처음에 3 개를 모두 말한 사람이 없었으나, 추적검사에서는 5 명이 3 가지 항목 모두를 기억해 내었다. Serial 7 에서는 첫 검사에서 평균 1.5 개의 항목을 계산해 내었는데 비해 두 번째검사에는 2.4 개의 항목을 계산해 내었다. (p=0.04, paired sample t-test) 한편 pentagon copy 에서는 겹쳐진 5 각형 모형을 잘 그린 사람이 7 명으로 치료 전후에 차이가 없었다. 종합해 볼 때 상기
12
소견은 콜린분해효소억제제 치료로 기억력과, 집중력이 좋아졌다는 기존의 보고와(Emre 등, 2004; Leroi 등, 2004) 어느 정도 부합한다.
Table 2. Comparison of MMSE (Mini-mental state examination) results in patients before and after cholinesterase inhibitor therapy
Name 1st1st1st1st MMSE MMSE MMSE MMSE Pentagon Copy Immediate Recall Delayed recall Serial 7 2nd 2nd 2nd 2nd MMSE MMSE MMSE MMSE Pentagon Copy Immediate Recall Delaye d recall Serial 7
1 장OO 15151515 Yes 2 0 1 21212121 Yes 3 0 2
2 박OO 22222222 Yes 2 0 1 19191919 Yes 2 0 0
3 이OO 16161616 Yes 3 0 2 18181818 Yes 3 1 3
4 이OO 12121212 No 2 0 0 15151515 No 3 0 0
5 홍OO 21212121 Yes 1 1 3 29292929 No 3 3 5
6 박OO 20202020 Yes 1 0 1 25252525 Yes 3 2 3
7 김OO 16161616 No 3 0 2 27272727 No 3 1 5
8 홍OO 19191919 Yes 3 2 1 23232323 Yes 3 3 0
9 박OO 17171717 No 3 1 0 22222222 Yes 3 2 0
10 윤OO 23232323 Yes 3 0 1 25252525 No 3 3 3
13
C. 두뇌 당대사의 SPM(통계적 모수 지도화) 분석 결과
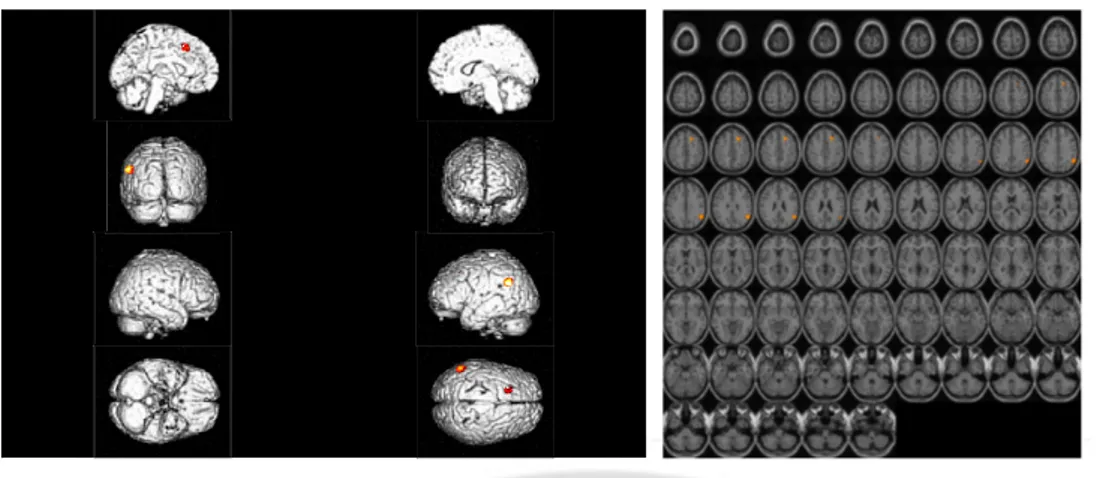
SPM 분석 결과 높이 역치 Puncorreted<0.001 수준에서 당대사가 증가한
부위와,(Table 3, Fig. 1) 감소된 부위가(Table 3, Fig. 2) 각각 관찰되었다. 당대사가
증가한 부위는 좌뇌에서 두 개의 cluster 에서 나타났다. 한 곳은
상/중간전두고랑(superior / middle frontal gyrus)이었고, 다른 곳은 각이랑/모서리위이랑(angular / supramarginal gyrus) 부위 인 것으로 나타났다. 당대사가 오히려 감소한 부위는 한 개의 cluster 로서 우뇌의 방추이랑(fusiform gyrus), 해마옆이랑(parahippocampal gyrus), 그리고 해마(hippocampus)부위였다.
Table 3. Areas showing significant difference in glucose metabolism after cholinesterase therapy in patients with Parkinson’s disease dementia.
Increased Metabolism Decreased Metabolism x-, y-, z- co-ordinates Anatomical Locations x-, y-, z- co-ordinates Anatomical Locations -20,20,44
Sup. Frontal gyrus,L Mid. Frontal gyrus, L
-50, -54, 28 Angular gyrus, L Supramarginal gyrus ,L 34, -30, -18 Fusiform gyrus, R Parahippocampal gyrus, R Hippocampus, R
14
Fig. 1. Statistical parametric maps showing the spatial distribution of significant metabolic increase after cholinesterase therapy in patients with Parkinson’s disease dementia. Lt. superior / middle frontal gyrus and Lt. inferior parietal gyrus shows
significantly increased glucose metabolism (Puncorrected< 0.001) after treatment.
Fig. 2. Statistical parametric maps showing the spatial distribution of significant metabolic decrease after cholinesterase therapy in patients with Parkinson’s disease dementia. Rt. medial temporal lobe shows significantly decreased glucose metabolism
15
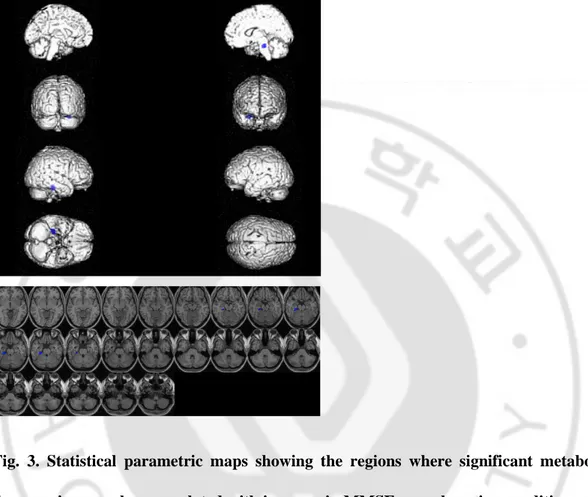
포도당대사량의 변화가 MMSE 의 호전 정도와 상관관계가 있는 부위를 분석한 결과, 당대사의 증가 부위 중에서는 상관관계가 있는 곳이 없는 것으로 나타났고, 당대사의 감소 부위 중에서는 위에서 언급한 부분의 당대사 감소 정도가 MMSE 의 호전 정도와 상관관계가 있는 것으로 나타났다. (Fig. 3, Puncorreted<0.005)
Fig. 3. Statistical parametric maps showing the regions where significant metabolic decrease is seen when correlated with increase in MMSE score by using conditions and covariates method. (Puncorrected< 0.005)
16
IV. 고찰
고찰
고찰
고찰
본 연구에서는 11 명의 파킨슨병치매 환자에게 콜린분해효소억제제 치료를 한 뒤 18 F-FDG PET 영상에서 보이는 뇌포도당대사의 변화를 SPM 을 이용하여 분석하였다. 포도당대사가 증가한 부위는 좌뇌의 상/중간전두고랑(superior / middle frontal gyrus)과 각이랑/모서리위이랑(angular / supramarginal gyrus)이었고, 감소한 부위는 우뇌의 내측 측두엽(medial temporal bobe)이었다. 특히 내측 측두엽의 당대사 감소는 MMSE 의 변화와 가장 상관관계가 높은 부위인 것으로 나타났다. 이러한 변화가 과연 파킨슨병치매에 특징적으로 나타나는 소견으로 볼 수 있을까? 총 4 개의 기존 논문에서 치료를 받지 않은 파킨슨병치매 환자의 18 F-FDG PET 을 이용한 뇌포도당대사의 특징에 관해 기술한 바가 있다. Peppard 등에 의한 연구에 의하면(Peppard 등, 1990; Peppard 등, 1992), 파킨슨병치매 환자는 알츠하이머병 환자와 비슷하게 대뇌 전체의 대사가 감소하는 18 F-FDG PET 소견을 보이며, 특히 perirolandic, angular gyrus 부위가 현저한 대사 감소를 보인다 하였다.다른 두 건의 연구에서는 후두엽의 대사 저하가 두드러지는 것이
알츠하이머병과 구별되는 특징으로 지목되었다(Piert 등, 1996; Vander Borght 등, 1997). 만일 약물 치료가 알츠하이머병과 파킨슨병치매에서 다른 기전에 의해 효과를 보인다면 위에 언급한 부위에서의 변화를 두드러지게 볼 수 있으리라
17 각이랑(angular gyrus)을 제외하면 파킨슨병치매에 특징적이라 할 수 있는 부위와는 일치하지 않는 소견을 보였다. 흥미로운 점은, 알츠하이머병 환자에게서 약물치료 후의 18F-FDG PET 의 변화를 관찰한 연구 중에서 본 연구와 매우 비슷한 결과를 얻은 논문이 있다는 것이다. Teipei 등은 알츠하이머병 환자에게 8 주간의 donepezil 치료를
교차설계(crossover design) 형식으로 진행하였다(Teipel 등, 2006). Donepezil 치료를 받은 군에서의 안정시 18
F-FDG PET 소견을 분석한 결과, 좌측 하전두고랑(inferior frontal gyrus)과 우측 해마의 포도당대사 감소소견을 관찰할 수 있었다. 우측
해마의 포도당대사 감소는 영화를 보여주는 activation 환경에서 PET 을
촬영하였을 경우에는 역전되어 오히려 위약군보다 대사가 증가하는 것을 관찰할
수 있었다. 또 다른 한 연구에서도 Snodgrass Picture Naming activation 환경에서
PET 을 촬영한 결과 rivastigmine 으로 치료를 받은 군에서 전반적인
뇌포도당대사가 26.6%증가하였으며, 특히 해마의 대사는 32.5% 증가하는 것을 관찰하였다(Potkin 등, 2001). 기능적 자기공명영상(functional MRI ; fMRI)를 통한 연구에서도 1 일간 galantamine 을 사용한 뒤 얼굴 인식 수행할 경우의 fMRI 에서는 양측 해마의 활성화가 관찰되었으나, 5 일간 galantamine 을 사용한 뒤에 같은 방식으로 fMRI 촬영을 한 결과 양측 해마의 활성이 현저히 감소하는
것을 발견하였다(Goekoop 등, 2006). 그러나 다른 한 fMRI 연구에서는
경도인지장애(mild cognitive impairment) 환자에게 7 일간 galantamine 을 사용한 결과 양측 해마의 활성이 증가한다고 보고하였다(Gron 등, 2006). 이렇듯이 약물 치료 후에 해마의 활성에 대해서는 다양한 결과를 보일 수 있는데, 아쉽게도 이에 대한 정확한 기전은 설명된 바가 없다. 반복적인 아세틸콜린 수용체의
18 자극이 수용체의 탈감작(desensitization)을 불러일으킨다는 사실은 잘 밝혀져 있는데(Quick 와 Lester, 2002), 이것을 통해 한가지의 가설을 세워 볼 수 있다. 즉, 약물로 인해 시냅스내의 아세틸콜린 농도가 만성적으로 증가함으로서 수용체의 탈감작이 일어나게 되고, 이로 인해 안정시의 대사는 오히려 약물 치료 전보다 감소하게 된다는 것, 그리고 특정한 인지기능의 수행시에는 시냅스전뉴런에서의 아세틸콜린의 다량 분비을 통해 수용체의 탈감작을 극복하고, 오히려 향상된 인지기능을 보일 수 있다는 것이다. 이 가설이 사실이라 하더라도, 본 연구에서 MMSE 의 증가 정도가 클수록 우측 해마의 포도당대사 저하 정도가 심하다는 소견을 설명하기에는 한계가 있으며, 이에 대해서는 추가적인 연구가 필요할 것이다. 한편, 본 연구에서 포도당대사가 증가된 부위로 밝혀진 좌측 전두엽과 두정엽의 경우 역시 다른 알츠하이머병을 대상으로 한 연구에서 비슷한 소견을 관찰할 수 있다(Tune 등, 2003; Stefanova 등, 2006; Teipel 등, 2006). 결론적으로 볼 때
파킨슨병치매 환자에게서 콜린분해효소억제제를 투여한 후에 18 F-FDG PET 의 변화를 관찰한 최초의 시도인 본 연구에서는 알츠하이머병을 대상으로 했던 기존의 연구와 비슷한 결과를 관찰할 수 있었고, 파킨슨병치매의 병리나 임상적인 증상과의 관련성은 오히려 적은 것으로 나타났다. 따라서 파킨슨병치매와 알츠하이머병의 임상적인 특징이 서로 다르고, 파킨슨병치매의 병리소견과 (신피질의 루이소체) 알츠하이머병의 병리소견이 서로 다르지만 약물에 의한 인지 기능의 호전은 공통된 기전에 의하는 것으로 추정할 수 있다. 마이너트기저핵(basal nucleus of Meynert)의 신경세포 소실로 인한 신피질에서의 콜린성 활동의 저하가 파킨슨병치매와( Whitehouse 등, 1983; Perry 등, 1985),
19 알츠하이머병에서 공히 중요한 치매의 기전으로 추정되는데, 아마도 콜린분해효소억제제는 이러한 기저핵 변성으로 인한 콜린성 뉴런의 구심로 차단(deafferentation)으로 인한 인지기능에 호전을 준다는 기존의 가설을 뒷받침하는 결과라 할 수 있다. 본 연구에 참여한 환자에게서 약물 치료 후 뚜렷한 집중력, 기억력의 향상과 계산능력의 향상을 관찰할 수 있었다. 그러나 포도당대사가 증가를 보인 부위는 이런 소견과 크게 관련이 없는 곳들이었다. 이러한 상이한 소견이 보이는 이유는 아마도 18 F-FDG PET 영상이 인지 기능의 정도를 정확하게 반영하지 못하기 때문일 가능성이 있다. 실제로 파킨슨병치매에서 가장 두드러진 인지기능의 저하는 집행기능의 저하와(Ballard 등, 2002; Rahkonen 등, 2003), 재인 검사에서 호전되는 기억력의 장애를 특징으로 하는 전두엽 기능의 장애이다(Pillon 등, 1993). 그러나 18 F-FDG PET 의 이상 소견은 앞서 기술하였듯이 전두엽보다는 두정엽, 후두엽 부위에서 두드러진다(Peppard 등, 1990; Peppard 등, 1992; Piert 등, 1996; Vander Borght 등, 1997). 실제로 MP4T PET 을 사용하여 파킨슨병치매 환자의 대뇌에서의 콜린계 활성화 정도를 측정한 연구에서도, 전두엽보다 후두엽 / 두정엽의 저하가 두드러졌다(Hilker 등, 2005). 따라서 좀 더 정확히 환자의 인지 기능 이상을 반영할 수 있는 영상을 통해서 연구해야만 이러한 문제를 보완할 수 있을 것이나, 현재로서는 더 나은 방법이 없는 상태이다. 본 연구의 경우 참여한 환자의 특성이 불균일하여 다양한 정도의 치매 단계와, 약물 치료 기간과 영상 검사 기간을 보였는데, 이것은 연구가 처음부터 전향적으로 계획되지 않고 약물 치료를 받아오던 환자가 중간에 참여한 경우가 포함되었기 때문이다. 또한 환자의 수가 적고, 자세한 신경심리 검사가
20 이루어지지 못한 점, 대조군 환자가 없이 환자 본인이 치료 받기 전의 영상에 대한 변화만을 본 것이 아쉬운 점이다. 향후 연구에서는 이러한 부분을 보완하여야 할 것으로 생각된다. 또한, 안정시 PET 촬영 뿐만 아니라, 활성시 PET 촬영을 같이 병행하거나, 부검을 통한 병리 조직과의 직접적인 관련성을 관찰하는 방법도 고려할 수 있겠다.
21
V. 결
결
결
결론
론
론
론
11 명의 파킨슨병치매 환자에게 콜린분해효소억제제 약물치료를 하기 전과 하고 난 뒤의 MMSE 와 18 F-FDG PET 의 결과를 비교하여 다음과 같은 결론을 얻을 수 있었다. 1. 콜린분해효소억제제 치료 후 환자들은 MMSE 의 호전과 함께 기억력, 집중력, 계산능력의 향상을 보였다. 2. 18F-FDG PET 영상을 SPM 을 사용하여 비교한 결과 치료를 받은 후의 영상에서 좌뇌의 상/중간전두고랑(superior / middle frontal gyrus)과 각이랑/모서리위이랑(angular / supramarginal gyrus)의 포도당대사 증가소견과, 우뇌의 내측 측두엽(medial temporal bobe)의 포도당대사 감소소견을 관찰할 수 있었다. 3. MMSE 의 변화와 18F-FDG PET 에서의 포도당대사 변화의 상관관계를 분석한 결과, MMSE 가 호전될수록 우뇌의 내측 측두엽의 포도당대사 저하가 심하게 나타났다. 4. 파킨슨병치매 환자에게 보이는 포도당대사의 변화 소견은 알츠하이머병에서 보이는 소견과 비슷하며, 따라서 두 개의 병이 서로 다른 증상과 병리를 보임에도 불구하고, 콜린분해효소억제제의 치료 효과는 두 개의 병에서 비슷한 기전을 갖고 있음을 시사한다. 5. 18F-FDG PET 과 인지 기능의 장애의 관련성은 확인할 수 없었다.22
참고문헌
참고문헌
참고문헌
참고문헌
1. Aarsland D, Ballard C, Larsen JP, McKeith I: A comparative study of psychiatric symptoms in dementia with Lewy bodies and Parkinson's disease with and without dementia. Int J Geriatr Psychiatry 16: 528-536, 2001
2. Aarsland D, Hutchinson M, Larsen JP: Cognitive, psychiatric and motor response to galantamine in Parkinson's disease with dementia. Int J Geriatr Psychiatry 18: 937-941, 2003
3. Aarsland D, Laake K, Larsen JP, Janvin C: Donepezil for cognitive impairment in Parkinson's disease: a randomised controlled study. J Neurol Neurosurg Psychiatry 72: 708-712, 2002
4. Ballard CG, Aarsland D, McKeith I, O'Brien J, Gray A, Cormack F, Burn D, Cassidy T, Starfeldt R, Larsen JP, Brown R, Tovee M: Fluctuations in attention: PD dementia vs DLB with parkinsonism. Neurology 59: 1714-1720, 2002
23
5. Beatty WW, Ryder KA, Gontkovsky ST, Scott JG, McSwan KL, Bharucha KJ: Analyzing the subcortical dementia syndrome of Parkinson's disease using the RBANS. Arch Clin Neuropsychol 18: 509-520, 2003
6. Bergman J, Lerner V: Successful use of donepezil for the treatment of psychotic symptoms in patients with Parkinson's disease. Clin Neuropharmacol 25: 107-110, 2002
7. Burn D, Emre M, McKeith I, De Deyn PP, Aarsland D, Hsu C, Lane R: Effects of rivastigmine in patients with and without visual hallucinations in dementia associated with Parkinson's disease. Mov Disord 21: 1899-1907, 2006
8. Byrne EJ, Lennox GG, Godwin-Austen RB, Jefferson D, Lowe J, Mayer RJ, Landon M, Doherty FJ: Dementia associated with cortical Lewy bodies: proposed clinical diagnostic criteria. Dementia. Vol 2: Karger, 283-284, 1991
9. Emre M, Aarsland D, Albanese A, Byrne EJ, Deuschl G, De Deyn PP, Durif F, Kulisevsky J, van Laar T, Lees A, Poewe W, Robillard A, Rosa MM, Wolters E, Quarg P, Tekin S, Lane R: Rivastigmine for dementia associated with Parkinson's disease. N Engl J Med 351: 2509-2518, 2004
10. Emre M, Aarsland D, Brown R, Burn DJ, Duyckaerts C, Mizuno Y, Broe GA, Cummings J, Dickson DW, Gauthier S, Goldman J, Goetz C, Korczyn A, Lees A, Levy R,
24
Litvan I, McKeith I, Olanow W, Poewe W, Quinn N, Sampaio C, Tolosa E, Dubois B: Clinical diagnostic criteria for dementia associated with Parkinson's disease. Mov Disord 22: 1689-1707, 2007
11. Fabbrini G, Barbanti P, Aurilia C, Pauletti C, Lenzi GL, Meco G: Donepezil in the treatment of hallucinations and delusions in Parkinson's disease. Neurol Sci 23: 41-43, 2002
12. Goekoop R, Scheltens P, Barkhof F, Rombouts SA: Cholinergic challenge in Alzheimer patients and mild cognitive impairment differentially affects hippocampal activation--a pharmacological fMRI study. Brain 129: 141-157, 2006
13. Gron G, Brandenburg I, Wunderlich AP, Riepe MW: Inhibition of hippocampal function in mild cognitive impairment: targeting the cholinergic hypothesis. Neurobiol Aging 27: 78-87, 2006
14. Hilker R, Thomas AV, Klein JC, Weisenbach S, Kalbe E, Burghaus L, Jacobs AH, Herholz K, Heiss WD: Dementia in Parkinson disease: functional imaging of cholinergic and dopaminergic pathways. Neurology 65: 1716-1722, 2005
25
15. Hughes AJ, Daniel SE, Kilford L, Lees AJ: Accuracy of clinical diagnosis of idiopathic Parkinson's disease: a clinico-pathological study of 100 cases. J Neurol Neurosurg Psychiatry 55: 181-184, 1992
16. Hughes TA, Ross HF, Musa S, Bhattacherjee S, Nathan RN, Mindham RH, Spokes EG: A 10-year study of the incidence of and factors predicting dementia in Parkinson's disease. Neurology 54: 1596-1602, 2000
17. Hutchinson M, Fazzini E: Cholinesterase inhibition in Parkinson's disease. J Neurol Neurosurg Psychiatry 61: 324-325, 1996
18. Lee PH, Kim JS, Shin DH, Yoon SN, Huh K: Cardiac 123I-MIBG scintigraphy in patients with drug induced parkinsonism. J Neurol Neurosurg Psychiatry 77: 372-374, 2006
19. Leroi I, Brandt J, Reich SG, Lyketsos CG, Grill S, Thompson R, Marsh L: Randomized placebo-controlled trial of donepezil in cognitive impairment in Parkinson's disease. Int J Geriatr Psychiatry 19: 1-8, 2004
20. Mega MS, Cummings JL, O'Connor SM, Dinov ID, Reback E, Felix J, Masterman DL, Phelps ME, Small GW, Toga AW: Cognitive and metabolic responses to metrifonate therapy in Alzheimer disease. Neuropsychiatry Neuropsychol Behav Neurol 14: 63-68, 2001
26
21. Peppard RF, Martin WR, Carr GD, Grochowski E, Schulzer M, Guttman M, McGeer PL, Phillips AG, Tsui JK, Calne DB: Cerebral glucose metabolism in Parkinson's disease with and without dementia. Arch Neurol 49: 1262-1268, 1992
22. Peppard RF, Martin WR, Clark CM, Carr GD, McGeer PL, Calne DB: Cortical glucose metabolism in Parkinson's and Alzheimer's disease. J Neurosci Res 27: 561-568, 1990
23. Perry EK, Curtis M, Dick DJ, Candy JM, Atack JR, Bloxham CA, Blessed G, Fairbairn A, Tomlinson BE, Perry RH: Cholinergic correlates of cognitive impairment in Parkinson's disease: comparisons with Alzheimer's disease. J Neurol Neurosurg Psychiatry 48: 413-431, 1985
24. Piert M, Koeppe RA, Giordani B, Minoshima S, Kuhl DE: Determination of regional rate constants from dynamic FDG-PET studies in Parkinson's disease. J Nucl Med 37: 1115-1122, 1996
25. Pillon B, Deweer B, Agid Y, Dubois B: Explicit memory in Alzheimer's, Huntington's, and Parkinson's diseases. Arch Neurol 50: 374-379, 1993
27
26. Pillon B, Dubois B, Ploska A, Agid Y: Severity and specificity of cognitive impairment in Alzheimer's, Huntington's, and Parkinson's diseases and progressive supranuclear palsy. Neurology 41: 634-643, 1991
27. Potkin SG, Anand R, Fleming K, Alva G, Keator D, Carreon D, Messina J, Wu JC, Hartman R, Fallon JH: Brain metabolic and clinical effects of rivastigmine in Alzheimer's disease. Int J Neuropsychopharmacol 4: 223-230, 2001
28. Quick MW, Lester RA: Desensitization of neuronal nicotinic receptors. J Neurobiol 53: 457-478, 2002
29. Rahkonen T, Eloniemi-Sulkava U, Rissanen S, Vatanen A, Viramo P, Sulkava R: Dementia with Lewy bodies according to the consensus criteria in a general population aged 75 years or older. J Neurol Neurosurg Psychiatry 74: 720-724, 2003
30. Reading PJ, Luce AK, McKeith IG: Rivastigmine in the treatment of parkinsonian psychosis and cognitive impairment: preliminary findings from an open trial. Mov Disord 16: 1171-1174, 2001
31. Scatton B, Javoy-Agid F, Rouquier L, Dubois B, Agid Y: Reduction of cortical dopamine, noradrenaline, serotonin and their metabolites in Parkinson's disease. Brain Res 275: 321-328, 1983
28
32. Spillantini MG, Schmidt ML, Lee VM, Trojanowski JQ, Jakes R, Goedert M: Alpha-synuclein in Lewy bodies. Nature 388: 839-840, 1997
33. Stefanova E, Wall A, Almkvist O, Nilsson A, Forsberg A, Langstrom B, Nordberg A: Longitudinal PET evaluation of cerebral glucose metabolism in rivastigmine treated patients with mild Alzheimer's disease. J Neural Transm 113: 205-218, 2006
34. Stern Y, Richards M, Sano M, Mayeux R: Comparison of cognitive changes in patients with Alzheimer's and Parkinson's disease. Arch Neurol 50: 1040-1045, 1993
35. Stern Y, Tetrud JW, Martin WR, Kutner SJ, Langston JW: Cognitive change following MPTP exposure. Neurology 40: 261-264, 1990
36. Teipel SJ, Drzezga A, Bartenstein P, Moller HJ, Schwaiger M, Hampel H: Effects of donepezil on cortical metabolic response to activation during (18)FDG-PET in Alzheimer's disease: a double-blind cross-over trial. Psychopharmacology (Berl) 187: 86-94, 2006
37. Tune L, Tiseo PJ, Ieni J, Perdomo C, Pratt RD, Votaw JR, Jewart RD, Hoffman JM: Donepezil HCl (E2020) maintains functional brain activity in patients with Alzheimer
29
disease: results of a 24-week, double-blind, placebo-controlled study. Am J Geriatr Psychiatry 11: 169-177, 2003
38. Vander Borght T, Minoshima S, Giordani B, Foster NL, Frey KA, Berent S, Albin RL, Koeppe RA, Kuhl DE: Cerebral metabolic differences in Parkinson's and Alzheimer's diseases matched for dementia severity. J Nucl Med 38: 797-802, 1997
39. Venneri A: Imaging treatment effects in Alzheimer's disease. Magn Reson Imaging 25: 953-968, 2007
40. Whitehouse PJ, Hedreen JC, White CL, 3rd, Price DL: Basal forebrain neurons in the dementia of Parkinson disease. Ann Neurol 13: 243-248, 1983
30 - ABSTRACT -
Changes in cerebral glucose metabolism in patients with Parkinson’s
disease with dementia after cholinesterase inhibitor therapy
Seok Woo Yong
Department of Medical Sciences The Graduate School, Ajou University
(Supervised by Professor In Soo Joo)
Objective : To evaluate changes in cerebral glucose metabolism in Parkinson’s disease dementia (PDD) patients after cholinesterase inhibitor therapy.
Background : Cholinesterase inhibitors (ChEI) are now widely used with proven efficacy in patients with PDD. There have been several reports describing how the drugs are benefiting the PDD patients in terms of clinical and neuropsychological scales. But there has never been a study on how the drug effect is represented on brain images. We performed serial 18 F-FDG PET studies in patients with PDD before and after ChEI therapy.
31
with either donepezil or galantamine. End point was when patients were treated for at least 3 months and when the patient or family members reported improved cognition. 18F-FDG PET scan was done before initiation of treatment and after completion drug trial. SPM images were created by comparisons between groups on a voxel-by-voxel basis using paired t-statistics.
Results : Patients were treated for mean duration of 8.4±4.5 months. Cognitive testes done by MMSE showed improvement after ChEI therapy in 10 patients, especially on memory and serial 7 tasks. Mean improvement in MMSE score was 5.5 points. SPM analysis showed increased glucose metabolism in left superior / middle frontal gyrus and left inferior parietal gyrus, mainly angular gyrus. There was also a region of decreased glucose metabolism in right medial temporal cortex, including fusiform, parrahippocampal gyrus and hippocampus. The degree of improvement in MMSE score only correlated with degree of decreased glucose metabolism on right medial temporal cortex.
Discussion : Our study has shown that PDD patients treated with ChEI have increased glucose metabolism in left superior / middle frontal and inferior parietal cortices, and decreased metabolism in right medial temporal cortex. It would be interpreted as that it shows poor correlation with changes in cognitive domains in these patients, and bears little similarities with prior resting FDG-PET studies involving PDD patients. Similar pattern of metabolic changes have been demonstrated before in similarly designed studies with patients with Alzheimer’s disease. The authors conclude that ChEI therapy in PDD patients restores
32
cognitive function by enhancing cholinergic neurotransmission in certain common areas regardless of the underlying pathologic process.
_________________________________________________________________________ Key Words ; Parkinson’s disease dementia, Cholinesterase inhibitors, 18F-FDG PET