저작자표시-비영리-변경금지 2.0 대한민국 이용자는 아래의 조건을 따르는 경우에 한하여 자유롭게 l 이 저작물을 복제, 배포, 전송, 전시, 공연 및 방송할 수 있습니다. 다음과 같은 조건을 따라야 합니다: l 귀하는, 이 저작물의 재이용이나 배포의 경우, 이 저작물에 적용된 이용허락조건 을 명확하게 나타내어야 합니다. l 저작권자로부터 별도의 허가를 받으면 이러한 조건들은 적용되지 않습니다. 저작권법에 따른 이용자의 권리는 위의 내용에 의하여 영향을 받지 않습니다. 이것은 이용허락규약(Legal Code)을 이해하기 쉽게 요약한 것입니다. Disclaimer 저작자표시. 귀하는 원저작자를 표시하여야 합니다. 비영리. 귀하는 이 저작물을 영리 목적으로 이용할 수 없습니다. 변경금지. 귀하는 이 저작물을 개작, 변형 또는 가공할 수 없습니다.
의학 석사학위 논문
유방암 환자에서
Adr
i
amyci
n/
docet
axel(
AD)과
Adr
i
amyci
n/
cycl
ophosphami
de
- pacl
i
t
axel(
AC-T)
선행항암화학요법의 비교
아 주 대 학 교
대 학 원
의학과/
의학전공
유방암 환자에서
Adr
i
amyci
n/
docet
axel(
AD)과
Adr
i
amyci
n/
cycl
ophosphami
de
- pacl
i
t
axel(
AC-T)
선행항암화학요법의 비교
지도교수
강 석 윤
이 논문을 의학 석사학위 논문으로 제출함.
2013년
2월
아 주 대 학 교
대 학 원
의학과/
의학전공
전 자 영
전자영의 의학 석사학위 논문을
인준함.
심사위원장
강
석
윤
인
심 사 위 원
정
용
식
인
심 사 위 원
한
재
호
인
아 주 대 학 교
대 학 원
2012년 12월 14일
i
-
국문요약-유방암
환자에서
Adr
i
myc
i
n/
doc
e
t
a
xe
l (
AD) 과
Adr
i
a
myc
i
n
/
c
yc
l
opho
s
phami
de-pac
l
i
t
axe
l(
AC-T)선행항암화학요법의 비교
연구배경 :선행항암화학요법은 국소 진행 유방암 환자의 표준 치료로 알려져 있 다.보조항암화학요법에서 사용되는 anthracycline 과 taxane 이 주로 사용되고 있으나 아직 어떠한 방법의 항암화학요법이 우월한지 확립되어 있지는 않다.
대상 및 방법 :본 연구에서는 2005년 1월부터 2011년 9월까지 선행항암화학요법 으로 adriamycin 과 docetaxel (AD) 을 투약 받은 군과 adriamycin, cyclophosphamide투여 후 paclitaxel(AC-T)으로 치료 받은 두 군을 후향적으 로 비교분석하였다.AD 군은 3주 간격으로 6차례 투약받았고 (50mg/m2 and 75mg/m2),AC-T 군은 3주 간격으로 AC (60mg/m2and600mg/m2)를 4차례 투 여 후 T (175mg/m2)를 4차례 투약하였다.선행항암화학요법 종료 후 5주 이내 에 모든 환자들은 근치적 수술을 받았다.두 군에서 병리학적 완전관해율,임상 적 반응,유방 보존술 시행률 및 약물부작용을 비교하였으며 FOX M1,gankyrin 에 대한 면역조직화학검사를 시행하였다. 결과 :37명은 AD 로 38명은 AC-T 로 치료받았다.양군간 기본 특성의 차이는 관찰되지 않았으나 AD군에서 T4를 포함한 병기가 높은 환자들이 더 많이 포함 되어 있었다.선행항암화학요법의 전체반응률은 AD 군 89%,AC-T 군 87% 로 차이가 없었고 병리학적 관해율도 11%,8% 로 유사한 결과를 보였다.유방 보존 율 및 유방 보존술식으로의 변경율도 AD군 각각 62%,24%,AC-T 군에서는 76%,29% 로 통계적 차이가 없었다.부작용면에서 비혈액학적 부작용은 차이가
ii 없었으나 AD 군에서 대부분의 환자들에서 3등급 이상의 호중구 감소증 및 호중 구 감소증을 동반한 발열이 있었고 이는 AC-T 군과 통계적 차이를 보였다.(각 각 p<0.001,p<0.001).Gankyrin의 발현과 환자들의 기본특성 및 임상반응과 비 교시 양군간 차이가 없었으나 진단시 HER-2양성인 군에서 gankyrin 이 더 많 이 발현됨이 확인되었다.(p=0.028) 결론 :선행항암화학요법으로 AD 또는 AC-T 투여 후 근치적 수술이 가능했던 두 군에서 병리학적 관해율,임상적 반응율,유방보존율은 차이가 없었으나 혈액 학적 부작용 측면에서 AD군에서 의미있게 많았고 심각한 부작용으로 입원치료 가 필요한 경우가 많아 AC-T 요법이 견딜만한 치료법으로 생각된다. 핵심어 :유방암,선행항암화학요법,종양 반응,병리학적 완전관해율,Gankyrin
iii
차
례
국문요약 ···i 차례 ···iii 그림차례 ···iv 표차례 ···v I.서론···1 II.대상 및 방법···3 A.대상 ···3 B.치료 ···3 C.평가 ···4 D.면역화학조직염색 ···5 E.통계 분석 ···5 III.결과 ···6 IV.고찰 ···13 V.결론 ···16 참고문헌 ···17 ABSTRACT ···20iv
그림 차례
Fig.1.Gankyrinexpressiononnormalbreasttissueandbreastcancer
v
표 차 례
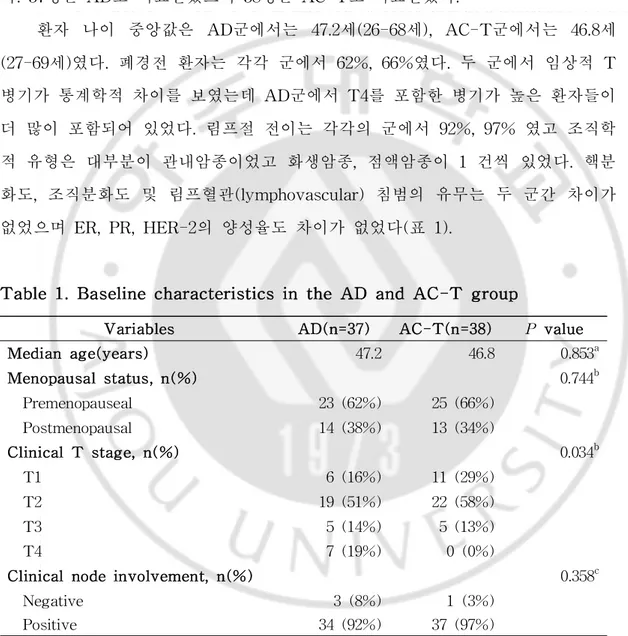
Table1.BaselinecharacteristicsintheAD andAC-T group···6
Table2.Chemotherapyresponse···8
Table3.Toxicity···9
Table4.Associationbetweenclinicopathologicvariablesandgankyrin
1
-I
.서론
유방암은 2009년 국가 암 등록통계 자료에 따르면 여성암 발생률 14.4% 로 2위 를 차지하며 인구 10만 명 당 54.1명이 발생하여 10년 전에 비해 2배 정도 증가 하였다(중앙암등록본부,2011).과거 유방암에서 선행항암화학요법은 진단 당시 수술이 불가능한 국소진행성 유방암이나 염증성 유방암 환자들을 대상으로 선행 항암화학요법의 반응에 따라 수술이 가능하게 하는 것이 목적이었다.그러나 최 근에는 수술이 가능한 조기 유방암 환자에서 수술의 범위를 줄이고 술 전 항암 화학요법의 반응을 미리 평가 할 수 있다는 몇 가지 장점을 활용해 2,3기 유방 암 환자에서 많이 시행되고 있다. 선행항암화학요법에서 사용되는 약제들은 이미 보조항암화학요법에서 효과가 알려진 anthracycline과 taxane을 병합하는 요법이 반응율 및 병리학적 관해율 측면에서 효과적임이 입증되었다(Rastoqi 등, 2008; Evans 등, 2005; von Minckwitz등,2005).또한 보조항암화학요법에 비해 수술 전 항암치료로 병기를 낮춰 유방 보존율을 높이며 병리학적 완전관해를 이룬 경우에는 전체생존율의 향상이 보고되어 수술이 가능한 유방암 환자에서 선행항암화학요법은 표준치료 의 한가지로 선택되어 질 수 있다(Kaufmann 등,2006;van der Hage,2001, Wolmark등,2001;Mauri등,2005).최근 들어 다양한 생물학적 치료제의 발견에 따라 임상적으로는 병리학적 완전 관해 및 항암화학요법의 반응을 예측할 수 있는 생물학적 표지자에 대한 관심이 높아졌다.호르몬수용체 음성은 병리학적 관해율을 예측할 수 있는 가장 강력한 인자로 확인되었고 비 소엽성(non-lobular)조직형,luminalB 아형 등도 보고되 고 있다(Kaufmann등,2006;Minckwitz등,2005).
저자 등은 후향적 의무기록 분석을 통해 유방암 진단되어 선행항암요법으로 adriamycin 과 docetaxel(AD)혹은,adriamycin,cyclophosphamide순차적으로 paclitaxel(AC-T)투여 후 수술을 시행했던 환자에서 병리학적 완전관해율,임
2
-상적 반응,유방 보존술 시행률 및 약물부작용을 비교하였다.또한 수술 병리조 직을 이용하여 병리학적 관해 및 임상적 반응을 예측할 수 있는 생물학적 표지 자를 찾아 보고자 하였다.
3
-I
I
.대상 및 방법
A.대상 2005년 1월부터 2011년 9월까지 아주대학교병원 유방암센터에서 2기,3기 원발성 유방암으로 진단받고 AD 또는 AC-T로 선행항암화학요법 시행 후 근치 적 수술을 받은 환자를 후향적으로 분석하였다.유방암은 조직생검으로 진단하였 고 치료 전 신체검사와 유방 촬영술,유방 초음파,유방 자기공명영상촬영을 시 행하였다.이전에 유방암 치료를 받았던 경우,진단시 원격전이가 있었던 경우, 치료 전 혹은 치료 중 다른 악성종양이 있는 환자는 배제하였다.모든 환자들은 전신수행상태가 양호하였고(Eastern Cooperative Oncology Group performance status≤ 2)치료 전 적절한 혈액학적 수치(혈색소 ≥ 10g/dl;절대호중구수 ≥ 1,500/mm3;혈소판 ≥ 100,000/mm3),심장 기능(심전도상 심각한 허혈성 변화 혹은 심각한 부정맥이 없고 심초음파상 좌심실 구축율≥ 50%),신기능(serum creatinine 1.5mg/dl), 간기능(aspartate aminotransferase, AST; alanine aminotransferase,ALT;bilirubin ≤ 1.5 uppernormallimits)을 보였다.본 연 구는 아주대학교 병원의 임상연구윤리위원회 심의 후에 진행되었다.
B.치료
선행항암화학요법은 AD 또는 AC-T로 수술 전 투여되었다.AD 요법은 3주 간격으로 adriamycin50mg/m2,docetaxel75mg/m2을 3회 혹은 6회 투여하였 다.AC-T 요법은 3주 간격으로 adriamycin 60 mg/m2,cyclophosphamide 600 mg/m2를 4회 투여하고 이어서 3주 간격으로 paclitaxel175mg/m2을 4회 투여하 였다.선행항암화학요법 동안에 호르몬치료,표적치료 및 방사선치료는 시행하지 않았다.선행항암화학요법 동안 common toxicity criteria for adverse events
4 -(CTCAE)version 4.0.기준에 의해 3등급 이상의 부작용이 나타났을 경우에는 치료를 1주 연기하였고 부작용이 일주일 이내로 회복되지 않거나 두 번 이상 발 생시에는 투여 용량을 최대 50%까지 순차적으로 감량하였다.또한 세 번 이상 3 등급 이상의 심각한 부작용이 발생하거나 질병의 진행이 확인된 경우에는 선행 항암화학요법을 중단하고 수술을 시행하였다.모든 환자들은 선행항암화학요법 종료 후 5주 이내에 근치적 절제술을 시행받았다. C.평가 임상적 종양크기와 림프절 침범 여부는 선행항암화학요법 시행 전,선행항 암화학요법 중(AD 군은 3회 투여 후,AC-T 군은 AC 4회 투여 후),선행항암 화학요법 종료하고 수술 전에 신체 검진 및 영상학적 검사로 평가하였다.영상학 적 검사는 선행항암화학요법 전 유방 촬영,유방 초음파 및 유방 자기공명영상 촬영을 하였고 선행항암화학요법 중간 및 종료 후에는 유방 초음파와 유방 자기 공명영상 촬영을 시행하였다.진단시 병기 설정을 위해 골주사검사,복부 초음파 및 양전자방출단층촬영을 시행하였다.신체검진은 매 항암화학요법 주기마다 시 행하였다.임상적 반응 평가는 Response evaluation criteria in solid tumor version 1.1 (RECIST 1.1)을 참고하였고 다음과 같은 기준을 사용하였다. Completeresponse(CR)알려진 병소가 모두 사라진 경우이며 partialresponse (PR)은 종양의 장축의 길이가 30% 이상 감소한 경우이고 stabledisease(SD)는 30%이상 이하로 감소하거나 25% 이상 증가하지 않은 경우이며 progressive disease(PD)는 25%이상 증가하거나 새로운 병소가 생긴 경우로 하였다.Overall response는 complete response 와 partial response를 보인 경우로 하였다 (Eisenhauer등,2009).부작용은 각 항암화학요법 주기마다 평가하였고 common toxicitycriteriaforadverseevents(CTCAE)version4.0.으로 등급화 하였다.
5
-조직유형을 확인하고 estrogen receptor (ER), progesterone receptor (PR), human epidermalgrowth factorreceptor2 (HER2),FOX M1 및 Gankyrin의 발현여부는 면역조직화학염색으로 확인하였다.근치적 수술 후 절제된 조직으로 병리학적 관해 및 병기를 확인하였다.병리학적 완전 관해는 유방 및 림프절에서 침습적 악성종양이 없는 것으로 정의하였다(Bear등,2003;Minckwitz등 2005) 근치적 절제는 유방 전절제술 혹은 유방보존술 중 한 가지를 시행하였다. 진단시 전절제술이 필요했다가 선행항암화학요법 시행 후 유방보존술로 변경가 능한 경우를 1인의 유방외과 의사가(KuSangKim)수술 전 평가하였다. D.면역조직화학염색
Fox M1, Gankyrin의 발현은 염색강도와 범위에 따른 German semi-quantitativescoring system을 사용하였다(Meng 등,2010)염색강도는 네 그룹으로 나누었다;0,no signal;1,weak staining;2,moderate stainin;3, strong stainin. 염색범위는 다음과 같이 점수화하였다; 0%, no signal; 1, staining of1-24%;2,staining of25-49%;3,staining of50-74%;4,staining of75-100%.총 점수는 염색강도와 염색범위를 곱한 값으로 최저 0 에서 최고 12점으로 분류하였다.
E.통계 분석
통계분석은 SPSS 18.0을 이용하였다. 연속형 변수는 t-test 와 Mann-Whitney U test를 범주형 변수는 Chi-squaretestorFisher’sexacttest 를 사용하여 P값을 산출하였고,P<0.05의 범위를 통계적으로 유의 하다고 판정 하였다.
6
-Variables AD(n=37) AC-T(n=38) P value Median age(years) 47.2 46.8 0.853a Menopausalstatus,n(%) 0.744b Premenopauseal 23(62%) 25(66%) Postmenopausal 14(38%) 13(34%) ClinicalT stage,n(%) 0.034b T1 6(16%) 11(29%) T2 19(51%) 22(58%) T3 5(14%) 5(13%) T4 7(19%) 0(0%)
Clinicalnodeinvolvement,n(%) 0.358c Negative 3(8%) 1(3%) Positive 34(92%) 37(97%)
I
I
I
.결과
A.대상 2005년 1월부터 2011년 9월까지 아주대학교병원 유방암센터에서 유방암으로 진단받고 AD 또는 AC-T로 선행항암화학요법을 받은 75명의 환자를 분석하였 다.37명은 AD로 치료받았으며 38명은 AC-T로 치료받았다. 환자 나이 중앙값은 AD군에서는 47.2세(26-68세),AC-T군에서는 46.8세 (27-69세)였다.폐경전 환자는 각각 군에서 62%,66%였다.두 군에서 임상적 T 병기가 통계학적 차이를 보였는데 AD군에서 T4를 포함한 병기가 높은 환자들이 더 많이 포함되어 있었다.림프절 전이는 각각의 군에서 92%,97% 였고 조직학 적 유형은 대부분이 관내암종이었고 화생암종,점액암종이 1건씩 있었다.핵분 화도,조직분화도 및 림프혈관(lymphovascular)침범의 유무는 두 군간 차이가 없었으며 ER,PR,HER-2의 양성율도 차이가 없었다(표 1).7
-Histologicsubtype,n(%) 0.385b Intraductalcarcinoma 35(95%) 37(97%)
Metaplasticcarcinoma 1(3%) 0(0%) Mucinouscarcinoma 0(0%) 1(3%) Unknown 1(3%) 0(0%)
Nucleargrade,n(%) 0.056b High 16(43%) 19(50%) Low/intermediate 10(27%) 15(39%) Unknown 11(30%) 4(11%) Histologicgrade,n(%) 0.09b High 20(54%) 13(34%) Low/intermediate 9(24%) 20(53%) Unknown 8(22%) 5(13%)
Lymphovascularinvasion,n(%) 0.711b Positive 16(43%) 14(37%)
Negative 15(41%) 19(50%) Unknown 6(16%) 5(13%)
Estrogen receptorstatus,n(%) 0.740b Negative 16(43%) 15(39%)
Positive 21(57%) 23(61%)
Progesteron receptorstatus,n(%) 0.294b Negative 15(41%) 20(53%) Positive 22(59%) 18(47%) HER2status,n(%) 0.941b Negative 26(70%) 27(71%) Positive 11(30%) 11(29%) a.studentt-test
b.Pearson'schi-squaretest c.Fisher'sExactTest
B.항암화학요법에 따른 반응
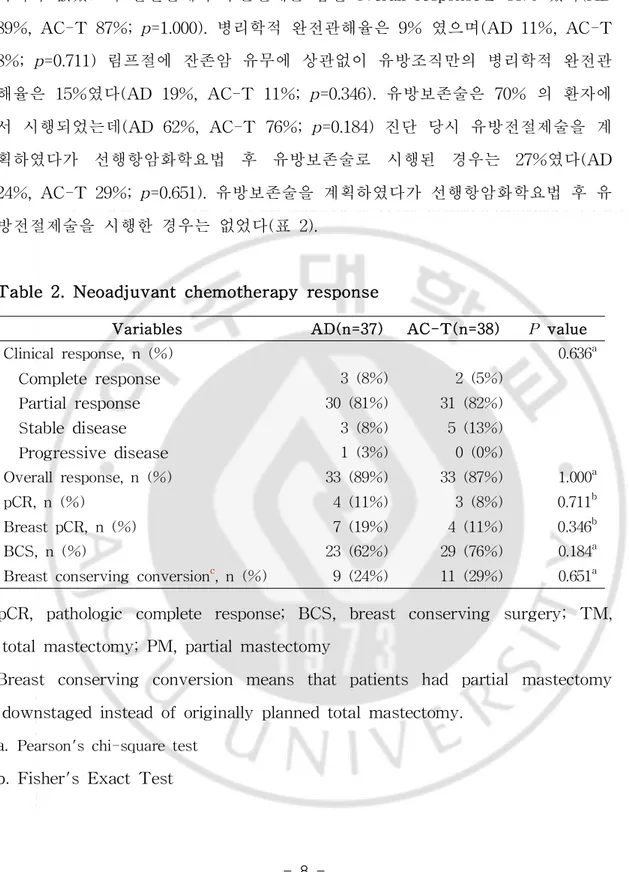
8 -차이가 없었으며 완전관해와 부분관해를 합친 overallresponse은 88% 였다(AD 89%,AC-T 87%;p=1.000).병리학적 완전관해율은 9% 였으며(AD 11%,AC-T 8%;p=0.711)림프절에 잔존암 유무에 상관없이 유방조직만의 병리학적 완전관 해율은 15%였다(AD 19%,AC-T 11%;p=0.346).유방보존술은 70% 의 환자에 서 시행되었는데(AD 62%,AC-T 76%;p=0.184)진단 당시 유방전절제술을 계 획하였다가 선행항암화학요법 후 유방보존술로 시행된 경우는 27%였다(AD 24%,AC-T 29%;p=0.651).유방보존술을 계획하였다가 선행항암화학요법 후 유 방전절제술을 시행한 경우는 없었다(표 2).
Table2.Neoadjuvantchemotherapy response
Variables AD(n=37) AC-T(n=38) P value Clinicalresponse,n(%) 0.636a
Completeresponse 3(8%) 2(5%) Partialresponse 30(81%) 31(82%) Stabledisease 3(8%) 5(13%) Progressivedisease 1(3%) 0(0%)
Overallresponse,n(%) 33(89%) 33(87%) 1.000a pCR,n(%) 4(11%) 3(8%) 0.711b BreastpCR,n(%) 7(19%) 4(11%) 0.346b BCS,n(%) 23(62%) 29(76%) 0.184a
Breastconserving conversionc,n(%) 9(24%) 11(29%) 0.651a
pCR,pathologic complete response;BCS,breast conserving surgery;TM, totalmastectomy;PM,partialmastectomy
Breast conserving conversion means that patients had partialmastectomy downstagedinsteadoforiginallyplannedtotalmastectomy.
a.Pearson'schi-squaretest
9 -C.항암화학요법에 따른 부작용 선행항암화학요법 후 발생된 부작용으로는 호중구 감소,간독성 순으로 발 생 빈도가 많았다.빈혈 및 호중구 감소,호중구 감소를 동반한 발열과 같은 혈 액학적 부작용이 AD군에서 AC-T군에 비해 통계학적으로 유의하게 높았다(각각 p=0.012,p<0.001,p<0.001).그 외 혈소판 감소와 신경합병증을 제외한 모든 부 작용이 AD군에서 많이 발생하였지만 통계학적 차이는 없었다(표 3). Table3.Toxicity
Variables AD (n=37) AC-T (n=38) P value Hematologictoxicitya
Anemia 6(16%) 0(0%) 0.012c Thrombocytopenia 0(0%) 1(3%) 0.507c Neutropenia 37(100%) 7(18%) <0.001c Neutropenicfever 20(54%) 0(0%) <0.001c Nonhematologictoxicity
Hepatictoxicityb 11(30%) 9(23%) 0.554d Nausea/vomiting 5(14%) 5(13%) 0.615c Diarrhea 6(16%) 1(3%) 0.200c Abdominalpain 3(8%) 1(3%) Constipation 4(11%) 0(0%) 0.054c Mucositis 4(11%) 0(0%) 0.054c Neuropathy 1(3%) 2(5%) 1.000c Infection 0(0%) 1(3%) 1.000c
a.OverGrade3byCTCAE version4.0
b.Over Grade 2; upper normallimit < aspartate aminotransferase/alanine aminotransferase < upper normallimit x 2.5 or upper normallimit < bilirubin< uppernormallimitx2.5
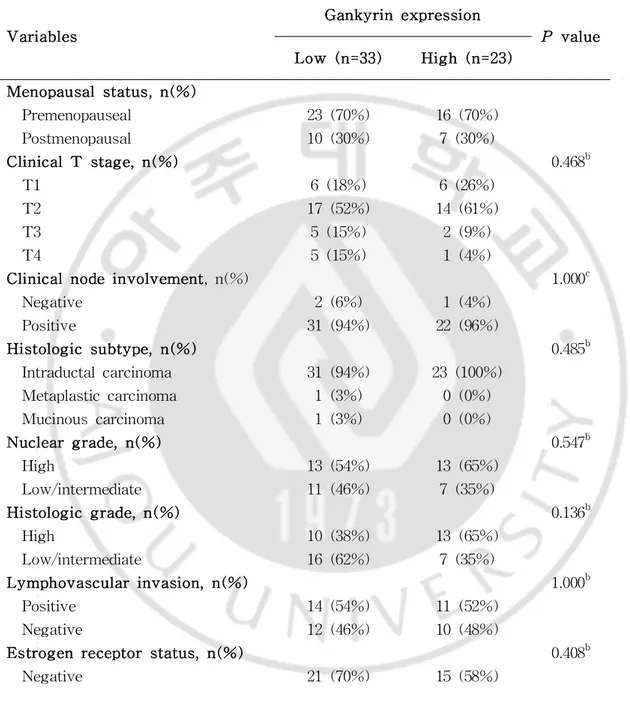
10 -d.Pearson'schi-squaretest D.생물학적 표지자 진단 시 획득한 유방암 조직으로 FOX M1및 gankyrin면역조직화학염색을 시행하였다.FOX M1의 경우 암세포의 세포질과 핵의 일부에서 발현되어 염색되 는데 본 연구에서는 유방암 조직 염색시 암세포에 염색되지 않고 기질 및 혈관 에만 염색되는 양상을 보여 결과를 얻지 못하였다.유방 조직이 포함된 일부에서 정상 유방조직보다 유방암 조직에서 gankyrin 발현이 높았으나 주변 정상 조직 과 유방암조직의 gankyrin 발현 차이를 점수로 비교할 순 없었다(그림 1). Gankyrin 발현정도를 점수화하였을 때 평균점수는 4.16 이었고 점수가 평균 미 만의 경우 저 발현군,평균 이상의 경우를 고 발현군으로 구분하였다.Gankyrin 의 발현 정도에 따른 환자의 기본특성 및 선행항암화학요법의 반응을 비교하였 고 진단시 HER-2 양성인 군에서 gankyrin 이 더 많이 발현됨이 확인되었 다.(p=0.028)그 외 의미있는 차이를 보이는 특성은 없었다(표 4).
Figure 1. Gankyrin expression in normal breast tissue and breast cancer. a. Adjacent normal breast tissues exhibiting weak gankyrin staining b.Breastcancerexhibiting strong staining
11 -Variables
Gankyrin expression
P value Low (n=33) High (n=23) Menopausalstatus,n(%) Premenopauseal 23(70%) 16(70%) Postmenopausal 10(30%) 7(30%) ClinicalT stage,n(%) 0.468b T1 6(18%) 6(26%) T2 17(52%) 14(61%) T3 5(15%) 2(9%) T4 5(15%) 1(4%)
Clinicalnodeinvolvement,n(%) 1.000c Negative 2(6%) 1(4%)
Positive 31(94%) 22(96%)
Histologicsubtype,n(%) 0.485b Intraductalcarcinoma 31(94%) 23(100%)
Metaplasticcarcinoma 1(3%) 0(0%) Mucinouscarcinoma 1(3%) 0(0%)
Nucleargrade,n(%) 0.547b High 13(54%) 13(65%)
Low/intermediate 11(46%) 7(35%)
Histologicgrade,n(%) 0.136b High 10(38%) 13(65%)
Low/intermediate 16(62%) 7(35%)
Lymphovascularinvasion,n(%) 1.000b Positive 14(54%) 11(52%)
Negative 12(46%) 10(48%)
Estrogen receptorstatus,n(%) 0.408b Negative 21(70%) 15(58%)
gankyin wasmainly locatedin both thecytoplasm andnucleiofcells.
Table 4.Association between clinicopathologic variables andgankyrin expression
12
-Positive 9(30%) 11(42%)
Progesteron receptorstatus,n(%) 0.789b Negative 17(57%) 13(50%) Positive 13(43%) 13(50%) HER2status,n(%) 0.028b Negative 19(86%) 8(50%) Positive 3(14%) 8(50%) Clinicalresponse,n (%) 0.651b c Completeresponse 2(6%) 1(4%) Partialresponse 29(88%) 19(83%) Stabledisease 2(6%) 3(13%) Overallresponse,n (%) 31(94%) 20(87%) 0.330b pCR 0.636c Yes 3(9%) 1(4%) No 30(91%) 22(96%) BCS 22(67%) 17(74%) 0.562b TM 11(33%) 6(26%)
Breastconservingconversion,n(%) 9(27%) 8(35%) 0.569b
pCR,pathologic complete response;BCS,breast conserving surgery;TM, totalmastectomy
Breast conserving conversion means that patients had partialmastectomy downstagedinsteadoforiginallyplannedtotalmastectomy.
a.studentt-test
b.Pearson'schi-squaretest c.Fisher'sExactTest
13
-I
V.고찰
유방암에서 선행항암화학요법은 염증성 유방암 혹은 수술로 제거가 불가능 한 국소 진행 유방암의 치료 뿐 아니라 많은 연구에서 조기 유방암의 표준치료 의 한 가지 방법으로 알려져 있다(Kaufmann등,2012;Bear등,2003;Mauri등, 2005;van derHage 등,2001).이에 사용되는 약제들은 보조항암화학요법으로 가장 많이 사용되고 있는 anthracycline기반에 taxane을 추가한 요법이 주로 이 용된다(Guarneri등,2006).NSABP B27연구에서 AC 와 AC 에 docetaxel을 추 가한 선행항암화학요법을 비교하였고 전반적인 반응률과 병리학적 완전관해 면 에서 docetaxel을 추가한 군이 우월함을 보고 하였다.또한 병리학적 완전관해가 이루어진 경우 전체생존 및 무진행 생존기간이 연장됨을 확인하였다(Bear 등, 2003).GeparDuo연구에는 anthracycline과 docetaxel을 동시에 투여하는 군과 연속 투여하는 방법을 비교하여 결과를 보고하였다. 치료 반응률(68.6% vs 78.6%)및 병리학적 완전관해율(7.0% vs14.3%)이 통계적으로 의미있게 연속 투 여군이 우세하였다(Minckwitz등 2005).
본 연구에서는 anthracycline에 taxane을 추가한 항암화학요법으로 AD 와 AC-T로 치료한 환자들의 결과를 비교하였는데 후향적 연구여서 두 군간 임상적 특성인 T 병기가 통계적으로 차이가 있었고 AD군에 T 병기가 높은 환자들이 포함되어 있었다.이는 AD군의 임상적 반응율,병리학적 관해율 및 유방보존술 에서 부정적인 영향을 줄 수 있음으로 만약 T 병기가 보정되었다면 AD군에서 좀 더 좋은 치료 결과를 나타낼 수 있을 것으로 생각된다.AD군에서는 진단 시 수술이 불가능한 국소적으로 진행된 T4유방암 환자가 7명(19%)포함되었고 선 행항암화학요법 후 근치적절제가 가능하였다.본 연구에서 전반적인 반응률은 88%,병리학적 완전관해율은 9% 로 기존의 연구들의 결과 반응률 60-90%,병리 학적 완전관해율 10-30% 와 비교해보면 크게 다르지 않았다(Guarneri등,2006; Sachelarie등,2006).병리학적 완전관해가 다소 적게 나왔지만 각 연구마다 다
14 -양한 기준을 적용하였는데 본 연구에서는 유방조직뿐 아니라 임파절에서도 잔존 악성세포가 없는 것을 기준으로 하였고,또한 대상 환자들 중 진행된 T4환자가 포함되어 있어 진단 시 수술가능한 환자들만을 대상으로한 연구보다 병리학적 관해율이 낮을 수 있음을 고려해 보면 거의 유사한 결과로 생각해 볼 수 있다. 유방보존술은 AD 및 AC-T군에서 각각 62%,76% 에서 시행되었으며 이는 이 전 연구들에서 보고된 결과와 유사하다(p=0.184)(von Minckwitz등,2005).유방 보존술로 변경하여 수술의 범위를 줄인 경우는 AD 및 AC-T군에서 각각 24%, 29% 였으며 타 연구들의 결과보다 우월하였다(p=0.615)(Wolmark등,2002). 항암치료 중 발생된 부작용을 보면 AD군에서 혈액학적 부작용의 빈도가 통 계적으로 유의하게 높았다.AC-T군에 비해 호중구 감소증은 AD군 37명 모두 에서 발생하였고 호중구 감소증을 동반한 발열도 환자의 54% 에서 발생하여 입 원치료가 필요하였다.혈액학적 부작용 측면에서 AC-T 항암화학요법이 AD 항 암화학요법에 비해 좀 더 우수한 방법으로 생각할 수 있다.만약 AD 환자들의 경우 예방적 백혈구 성장촉진인자를 동시에 사용 하였다면 호중구 감소의 빈도 를 줄이고 발열도 감소시켜 AC-T와 유사한 결과를 보였을 가능성도 있었을 것 으로 생각된다. Gankyrin은 1998년에 Tanaka등에 의해 처음 분리된 단백질로 26S 프로테 오솜의 조절 소단위(regulatory subunit)이다(Hori등,1998).Gankyrin은 대표적 종양억제단백질로 알려진 Rb와 p53을 억제하여 종양발생을 유발하는 것으로 알 려져 있는데 cyclin-dependentkinase 4 와 결합하여 Rb1 의 분해와 인산화를 촉진하고 ubiqutineligaseMDM2를 통해 p53의 분해함이 그 기전으로 알려져 있다.(Lozano 등,2005;Higashitsuji등,2005).Gankyrin은 악성 종양에 질환에 서 발현이 높을 것으로 기대할 수 있으며 간암,대장암,식도암,폐암,췌장암 등 에서 발현이 높음이 보고되었고 세포주기를 촉진하여 각 암에서 기전의 차이는 있으나 암화과정에 중요한 역할을 담당하고 있음이 확인되었다.(Higashisuji등, 2000;Tang 등 2010;Ortiz등,2008;Man등 2012;Yung등,2010)최근 유방암
15 -에서도 주변 정상조직에서보다 발현이 높으며 암세포이동에 필수 조절 역할을 한다는 것이 알려졌는데 임파절 전이가 있는 유방암에서 gankyrin 의 발현이 높 고 임파절 전이와 gankyrin 발현정도가 유의한 상관관계가 있어 유방암세포의 이동 및 조직침범에 gankyrin이 관여할 수 있음이 제기되었다.(Zhen등,2012) 본 연구에서 gankyrin의 발현정도를 면역조직화학염색의 빈도와 강도를 점 수화 하여 비교하였고 환자의 임상병리학적 특성 및 선행항암화학요법의 효과와 의 연관성을 분석하였으나 대부분 통계적으로 의미있는 차이를 보이지 못하였다. 하지만 HER-2 양성의 환자들에서 선행항암화학요법의 종류와 상관없이 gankyrin의 발현이 많음을 확인하였다.이에 대한 정확한 이유를 설명하기 어렵 지만 gankyrin 의 과발현이 유전자의 안정성에 반드시 필요한 p53단백의 불안 정성을 유발하고 그 결과 유방세포의 Erb-B2 유전자의 증폭을 유도할 수 있다 는 가설을 제시할 수 있을 것으로 생각된다(Chernova 등,1995;Tavassoli등, 1995).하지만 이에 대한 분자생물학적 기전에 대한 연구와 규명이 있어야 겠다. 본 연구는 후향적 연구로 두 군의 T 병기 분포에 차이가 있어 결과로 보고 자 하였던 병리학적 관해율,임상적 반응율,유방보존율에 영향을 미쳤을 것이라 는 제한점이 있다.AD군은 환자의 상태에 따라 3회 또는 6회를 시행하여 항암제 의 용량의 차이가 있어 비교적 일정하게 치료받았던 AC-T 군과 단순한 비교는 어렵다.또한 유방암의 치료에 있어 선행항암화학요법에 HER-2 양성인 환자에 게 표적치료를 추가 했다면 치료 반응면에서 더 좋은 결과를 얻었을 가능성이 있다.부작용 보고에 있어 혈액학적 부작용 및 간독성 등은 혈액검사를 통해 결 과를 얻을 수 있었으나 오심,구토,설사,복통,변비,점막염,신경독성 등의 부 작용은 의무기록을 통한 자료수집이어서 제한점이 있다.향후 장기적인 추적관찰 을 통해 2가지 선행항암화학요법이 환자의 예후와 관련이 있는지 확인해 봐야 할 것이며 다양한 치료반응을 예측할 수 있는 분자생물학적 표지자에 대한 추가 연구가 필요하겠다.
16
-V.결론
선행항암화학요법으로 AD 또는 AC-T 투여 후 근치적 수술이 가능했던 유 방암 환자에서 병리학적 완전관해율,임상적 반응율,유방보존율 및 치료 부작용 을 비교하여 우월한 항암화학요법을 확인하고 병리학적 관해 및 임상적 반응을 예측하는 생물학적 표지자를 찾고자 하였다.두 군에서 병리학적 관해율,임상적 반응율,유방보존율은 통계적으로 유의하지 않았으나 AD군에서 진행된 환자들이 더 많이 포함되었음을 고려할 때 결론내리기는 어렵다.부작용 측면에서는 AD군 에서 혈액학적 부작용이 의미있게 많았고 심각한 부작용으로 입원치료가 필요한 경우가 많아 AC-T 요법이 견딜만한 치료법으로 여겨진다.향 후 두군간의 예후 를 비교하면 유방암 환자에게 좀 더 효과적인 치료 방법의 선택하는데 도움이 될 것으로 생각된다.17
-참고문헌
1.중앙암등록본부:2009년 중앙암등록통계.보건복지부,2011
2.Bear HD,Anderson S,Brown A,Smith R,Mamounas EP,Fisher B, Margolese R,TheoretH,Soran A,Wickerham DL,Wolmark N :The effecton tumor response ofadding sequentialpreoperative docetaxelto preoperative doxorubicin and cyclophosphamide:preliminary results from NationalSurgicalAdjuvantBreastand BowelProjectProtocolB-27.J
ClinOncol21:4165-4174,2003
3.Chernova OB,Chernov MV,AgarwalML,TaylorWR,Stark GR :The roleofp53in regulating genomicstability when DNA andRNA synthesis areinhibited.TrendsBiochem Sci20,431-434,1995
4.EisenhauerEA,TherasseP,BogaertsJ,SchwartzLH,SargentD,FordR, Dancey J,Arbuck S,GwytherS,Mooney M,Rubinstein L,ShankarL, Dodd L,Kaplan R,Lacombe D,VerweijJ :New response evaluation criteria in solid tumours:revised RECIST guideline (version 1.1).EurJ
Cancer45:228-47,2009
5.EvansTR,YellowleesA,FosterE,EarlH,Cameron DA,Hutcheon AW, Coleman RE,Perren T,Gallagher CJ,Quigley M,Crown J,Jones AL, Highley M,Leonard RC,MansiJL :Phase III Randomized Trial of Doxorubicin and Docetaxel (DA) versus Doxorubicin and Cyclophosphamide (AC) as Primary MedicalTherapy in Women with Breast Cancer:An Anglo-Celtic Cooperative Oncology Group Study.J
ClinOncol23:2988-2995,2005
6.GuarneriV,FrassoldatiA,GiovannelliS,BorghiF,Conte P :Primary systemictherapyforoperablebreastcancer:areview ofclinicaltrialsand perspectives.Cancerlett248:175-185.2007
7.HigashitsujiH,Liu Y,MayerRJ,Fujita J.:The oncoprotein gankyrin negatively regulates both p53 and RB by enhancing proteasomal degradation.Cellcycle4:1335-1337.2005
8.HoriT,Kato S,SaekiM,DeMartino GN,Slaughter CA,TakeuchiJ, Toh-e A,Tanaka K :cDNA cloning and functionalanalysis of p28
18
-(Nas6p) and p40.5 (Nas7p),two novelregulatory subunits of the 26S proteasome.Gene216:113-122.1998
9.Kaufmann M,von MinckwitzG,Mamounas EP,Cameron D,Carey LA, CristofanilliM,DenkertC,Eiermann W,GnantM,Harris JR,Karn T, LiedtkeC,MauriD,RouzierR,RuckhaeberleE,Semiglazov V,Symmans WF, Tutt A, Pusztai L : Recommendations from an international consensus conference on the current status and future of neoadjuvant systemictherapy in primary breastcancer.Ann Surg Oncol19:1508-1516, 2012
10.Lozano G,ZambettiGP :Gankyrin :an intriguing name fora novel regulatorofp53andRB.Cancercell.8:3-4.2005
11.ManJH,LiangB,GuYX,ZhouT,LiAL,LiT,JinBF,BaiB,Zhang HY,ZhangWN,LiWH,GongWL,LiHY,ZhangXM :Gankyrinplays anessentialroleinRas-inducedtumorigenesisthroughregulationofthe RhoA/ROCK pathwayinmammaliancells.JClinInvest120:2829-2841.
2010
12. Mauri D, Pavlidis N, Ioannidis JP : Neoadjuvant versus adjuvant systemictreatmentin breastcancer:ameta-analysis.J NatlCancerInst
97:188-194.2005
13.OrtizCM,ItoT,TanakaE,TsunodaS,NagayamaS,SakaiY,
HigashitsujiH,FujitaJ,ShimadaY :Gankyrinoncoproteinoverexpression asacriticalfactorfortumorgrowthinhumanesophagealsquamouscell carcinomaanditsclinicalsignificance.IntJCancer122:325–.332.2008 14.RastogiP,Anderson SJ,BearHD,GeyerCE,Kahlenberg MS,Robidoux
A,MargoleseRG,HoehnJL,VogelVG,DakhilSR,TamkusD,KingKM, Pajon ER,WrightMJ,RobertJ,Paik S,Mamounas EP,Wolmark N : Preoperative Chemotherapy:Update ofNationalSurgicalAdjuvantBreast and BowelProjectProtocols B-18 and B-27.J Clin Oncol26:778-785. 2008
15.Sachelarie I,Grossbard ML,Chadha M,Feldman S,GhesaniM,Blum RH :Primary systemic therapy ofbreastcancer.Oncologist11:574-89. 2006
19
-16.TangS,YangG,MengY,DuR,LiX,FanR,WangY,WuK,LiuJ, FanD :Overexpressionofanovelgenegankyrincorrelateswiththe
malignantphenotypeofcolorectalcancer.CancerBiolTher9:88-95.
2010
17.TavassoliM,AlagozM,LeeJ,GibsonB,Farzaneh F,Kirkham N :Loss of wild-type p53 and C-erbb2 amplification correlates with high-grade breastcarcinomas.IntJOncol6:181-186.1995
18.van der Hage JA,van de Velde CJ,Julien JP,Tubiana-Hulin M, Vandervelden C,Duchateau L :Preoperative chemotherapy in primary operable breast cancer: results from the European Organization for ResearchandTreatmentofCancertrial10902.J ClinOncol19:4224-4237. 2001
19.vonMinckwitzG,RaabG,CaputoA,SchutteM,HilfrichJ,BlohmerJU, GerberB,Costa SD,Merkle E,Eidtmann H,Lampe D,Jackisch C,du Bois A,Kaufmann M :Doxorubicin with cyclophosphamide followed by docetaxelevery 21 days compared with doxorubicin and docetaxelevery 14 days as preoperative treatment in operable breast cancer: the GEPARDUO study of the German Breast Group. J Clin Oncol
23:2676-2685.2005
20.Wolmark N,Wang J,Mamounas E,BryantJ,FisherB :Preoperative chemotherapy in patients with operable breastcancer:nine-year results from NationalSurgicalAdjuvantBreastand BowelProjectB-18.J Natl CancerInstMonogr30:96-102.2001
21.Meng Y,HeL,GuoX,Tang S,ZhaoX,Du R,Jin J,BiQ,LiH,Nie Y, Liu J, Fan D : Gankyrin promotes the proliferation of human pancreaticcancer.CancerLett297:9-17.2010
22.ZhenC,ChenL,ZhaoQ,Liang B,GuYX,BaiZF,WangK,XuX,Han QY,Fang DF,Wang SX,ZhouT,XiaQ,GongWL,Wang N,LiHY,Jin BF, Man JH : Gankyrin promotes breast cancer cell metastasis by regulatingRac1activity.Oncogene2012
20
-ABSTRACT
Compar
i
s
onoft
wone
oa
dj
uva
ntc
he
mot
he
r
apyi
nl
oc
a
l
l
yadvanc
e
d
br
e
a
s
tc
anc
e
rpa
t
i
e
nt
s
;Adr
i
amyc
i
nandDoc
e
t
a
xe
l(
AD)ve
r
s
us
Adr
i
amyc
i
n,Cyc
l
ophos
pha
mi
def
ol
l
owe
dbyPac
l
i
t
a
xe
l(
AC-T)
JaYoungJeon
DepartmentofMedicalSciences,GraduateSchool,AjouUniversity (SupervisedbyProfessorSeokYunKang)
Background: Neoadjuvant chemotherapy (NAC) is one of the standard treatment for the patients with locally advanced breast cancer and is an option for the patients with operable breast cancer. Such as adjuvant chemotherapy inbreastcancer,anthracyclineandtaxane-basedregimenshave been studied and investigated as neoadjuvantsetting.But,no one regimen hasbeenshowntobesuperiorinefficacyandtoxicityview.
Materials and Methods:We compared thewomen received adriamycin and docetaxel (AD) with adriamycin, cyclophosphamide followed by paclitaxel (AC-T) as neoadjuvant chemotherapy from 1 November 2005 to 31 September2011.TheAD groupwasscheduled for6cyclesofAD (50mg/m2 and75mg/m2,respectively)in theintervalof3weeks.TheAC-T groupwas scheduled for4cyclesofAC regimen (60mg/m2and 600mg/m2,respectively) followedby 4cyclesofpaclitaxel(175mg/m2)in theintervalof3weeks.All patients received complete resection for localcontrolwithin 5 weeks after neoadjuvantchemotherapy.
21
-Results:The patients enrolled in this study were totally 75 (AD 37 and AC-T 38).Among thepatients’baselinecharacteristics,clinicalT stagewas differentbetween two groups.More advanced cases were included in AD group.Theresponsesofchemotherapywereequivalent,whichwereestimated by overallresponse rate (AD 89% versus AC-T 87%,p=1.000),pathologic completeresponse(pCR)rate(breastand axilla;AD 11% versusAC-T 8%,
p=0.711,breastonly ;AD 19% versusAC-T 11%,p=0.346),breastconserving surgery rate (AD 62% versus AC-T 76%,p=0.184)and breastconserving surgery conversion rate (AD 24% versus AC-T 29%,p=0.651).Although non-hematologictoxicitieswerecomparable,hematologictoxicitiesweremore severe in AD group.Mostwomen in AD group suffered from grade 3/4 neutropenia (p<0.001) and neutropenic fever (p<0.001). Also, Gankyrin expressions were not different between two groups except HER-2 positivity(p=0.028).
Conclusions:AC-T regimenwasmoretolerablewithsimilarclinicaloutcome thanAD regimeninpatientswithbreastcancerreceivingNAC.
Key Words: Breast cancer, Neoadjuvant chemotherapy, Tumor response, Pathologiccompleteresponse,Gankyrin