서론
안구건조증은 눈물 결핍이나 과도한 눈물 증발로 인한 눈 물막의 장애로 안구 표면의 손상을 가져와서 눈이 불편한 증상을 일으키는 질환이다[1]. 2006년에 델파이 그룹은 안 구건조증의 새로운 이름인 ‘눈물이상 증후군(dysfunctional tear syndrome)’을 제안했으며, 안구건조증이란 질병이 임 상적으로 명백한 염증이 있거나 없을 때를 분류하여 치료에 대한 가이드라인을 제시하였다[2].2007년에는, 안구건조증에 대한 Tear Film and Ocular Surface Society (TFOS)의 International Dry Eye-Workshop (DEWS)에서는 눈물의 삼투압 증가로 인한 안구 표면의 염증을 언급하여 다음과 같이 정의하였다[3]. “안구 건조증은 눈물과 안구 표면의 다요인성 질병으로, 눈의 불편 함, 시각장애, 눈물막 불안정과 안구표면의 잠재적인 손상을 유발한다. 이는 눈물막의 삼투압의 증가와 안구 표면의 염증 을 동반한다.” 최근에 안구건조증의 연구가 발달함에 따라 개정된 TFOS DEWS II 글로벌 안구건조증 정의가 발표되었다. “안구건조 증은 안구표면의 다요인성 질병으로 눈물막의 항상성을 상 실하고 안구증상에 동반되는 특징을 가지는 데, 눈물막의 불 안정과 고 삼투압, 안구 표면의 염증 및 손상, 신경감각 이상 이 원인적인 역할을 한다”[4]. 이는 안구건조증이 눈물의 항
안구건조증의 진단과 치료
김 은 철 | 가톨릭대학교 의과대학 부천성모병원 안과Diagnosis and treatment of dry eye syndrome
Eun Chul Kim, MD
Department of Ophthalmology, Bucheon St. Mary's Hospital, The Catholic University of Korea College of Medicine, Bucheon, Korea
Received: May 9, 2018 Accepted: May 23, 2018 Corresponding author: Eun Chul Kim
E-mail: eunchol@hanmail.net © Korean Medical Association
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons. org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Dry eye syndrome is a multifactorial disease of the ocular surface characterized by a loss of homeostasis of the tear film, and accompanied by ocular symptoms. Tear film instability and hyperosmolarity, ocular surface inflammation and damage, and neurosensory abnormalities play etiological roles. Symptom screening with the Five-item Dry Eye Questionnaire or Ocular Surface Disease Index can be used to identify the possibility that a patient might have DED dry eye syndrome and triggers. The results of these screening tools can lead to performing diagnostic tests of (ideally non-invasive) breakup time, osmolarity and ocular surface staining with fluorescein and lissamine green (observing the cornea, conjunctiva and eyelid margin). Meibomian gland dysfunction, lipid thickness/dynamics and assessments of the volume and severity of tear allow the subclassification of dry eye syndrome as predominantly evaporative or aqueous deficient, which informs the management of dry eye syndrome. A staged management algorithm was derived that presents a stepwise approach to implementing the various management and therapeutic options according to disease severity.
상성 상실이 주된 원인이며 신경감각 이상까지 원인으로 포 함시키는 의미를 가진다.
눈물막의 정의와 안구건조증의 분류
1. 눈물막 눈물분비의 기능적 단위는 안구 표면(각막, 결막, 덧눈물 샘, 마이봄샘), 주눈물샘, 눈물을 확산시키는 눈깜빡임 기전, 그리고 이들을 연결하는 감각과 운동신경으로 구성된 통합 적 구조이다[5]. 과거에는 눈물막은 점액층, 수성층, 지방층 의 세 층으로 구성된다고 알려져 있었으나, 현재의 눈물막-안구 표면 구조의 개념은 수성겔과 눈물막-안구 표면에서 안쪽 지방 층까지 점점 줄어드는 점액 성분으로 이루어진 준안전성의 눈물막으로 이해하고 있다. 수성과 점액성 구성성분이 상호 작용하여 눈깜빡임 사이 사이의 수성 눈물의 증발로 인한 손 실을 늦추고 눈물막의 안정성에 기여하고 있다[1]. 2. 안구건조증의 분류 안구건조증은 일반적으로 병인에 따라 수성눈물 생성 부 족에 의한 안구건조증과 눈물막 증발 증가에 의한 안구건조 증으로 나눠진다. 최근 DEWS II분류에 따르면 두 가지 모두 포함된 혼합형이 존재하며 눈물막 증발 증가에 의한 안구건 조증이 더 많은 부분을 차지한다. 1) 수성눈물 생성 부족 안구건조증 (1) 쇼그렌 증후군 쇼그렌 증후군(Sjogren’s syndrome)은 눈물샘과 침샘을 침범하는 자가면역질환으로, 류마티스관절염에 이어 두 번 째로 흔한 자가면역 류마티스질환이다. 눈물샘과 침샘에 활 성화된 T세포가 침윤하며, 샘꽈리세포와 세관세포가 파괴되 어 눈물과 침의 분비가 감소되는 질환이다. 염증반응에 의해 표피세포에서 fodrin, Ro, La 등과 같은 자가항체가 발현되 고81 조직특이적 CD4와 CD8 T세포가 정체된다[6]. 쇼그렌 증후군에는 두 가지 형태가 있는데, 원발성 쇼그렌 증후군은 다른 연관된 전신 결제조직 질환이 없는 경우이고, 속발성 쇼그렌 증후군은 류마티스관절염이나 전신홍반루프스, 결절 다발동맥염, 베게너육아종증(Wegener’s granulomatosis), 전신성 경화증, 원발성 담즙성 경화증 등의 결체조직질환과 함께 쇼그렌 증후군이 나타나는 경우를 말한다. (2) 비쇼그렌 증후군 비쇼그렌 증후군은 눈물샘의 기능저하에 의한 수성눈물 생성 부족 안구건조증에 속하나, 전신 자가면역질환이 배제 된 경우가 해당된다. 원발성 눈물샘 결핍, 이차성 눈물샘 결 핍, 눈물관의 폐쇄, 반사 눈물의 분비저하가 원인으로 꼽히 며 가장 흔한 경우는 노화에 의한 안구건조증이다. 2) 눈물막 증발 증가 건성안 (1) 내인적 요인 ① 마이봄샘 기능장애 마이봄샘(meibomoian gland) 기능장애 혹은 후눈꺼풀염 증은 마이봄샘의 폐쇄를 일으키며 눈물막 증발 증가 건성안 의 가장 흔한 원인이다[7]. 마이봄샘 기능장애는 건성안을 일 으키기도 하고 건성안에 의해 더욱 유발되기도 한다. 마이봄 샘 기능장애는 주로 마이봄샘의 입구가 막혀서 생기는 저분비 성으로 마이봄샘의 염증과 위축을 일으켜 눈물의 불안정성을 초래한다. 그 외에 과분비성 마이봄샘 기능장애도 눈물의 지 방층의 장애를 일으켜 눈물막의 불안정성을 초래할 수 있다. ② 눈꺼풀 형태의 장애 두개골협착증, 갑상선안병증에 의한 안구돌출, 토안 등 눈 꺼풀 형태와 눈깜빡임의 기능이 저하된 경우 눈물의 증발이 증가되어 건성안이 발생한다. ③ 눈깜빡임 횟수의 감소 눈깜빡임 횟수가 줄게 되면 안구 표면의 수분 증발이 커 져 건성안이 유발되는데, 장시간 비디오 스크린을 보거나, 현미경을 보는 등의 집중력을 요하는 작업을 하는 경우, 파 킨슨씨병과 같은 추체외로장애에서 발생한다. (2) 외부적 요인 ① 안구표면 질환 안구표면 질환으로 인해 안구표면이 충분히 적셔지지 못하 고, 눈물막 파괴 시간이 짧아지고, 눈물의 오스몰농도가 높아 져서 건성안이 생기는데, 만성 안구표면 질환인 알레르기성 결막염, 뮤신 생성이 줄어드는 비타민A 결핍과 같은 질환에 서 발생한다[8]. 점안액에 의해서도 각막상피독성과 눈물막파괴가 일어나는데, 염화벤잘코늄(benzalkonium chloride) 이 가장 흔한 원인물질로 각막상피세포의 손상과 점상상피각 막염을 일으켜 안구 표면의 습윤성을 방해하게 된다[9]. ② 콘택트렌즈 착용 콘택트렌즈 착용에 어려움을 겪는 주요 원인은 불편한 착 용감과 건조함이다. 콘택트렌즈 착용자를 대상으로 한 연구 에서 다양한 요인이 건성안과 관련 있었는데, 렌즈 앞 눈물 막이 얇아지는 시간이 가장 건성안과 관련이 깊었으며, 콘택 트렌즈의 함수율과 굴절률이 뒤를 이었다[10].
진단
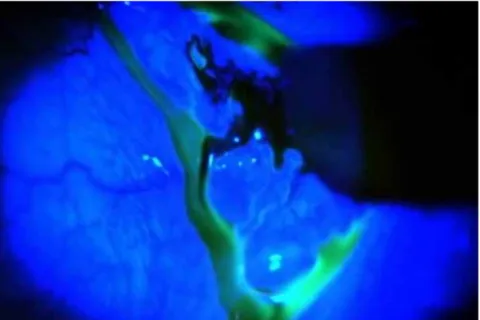
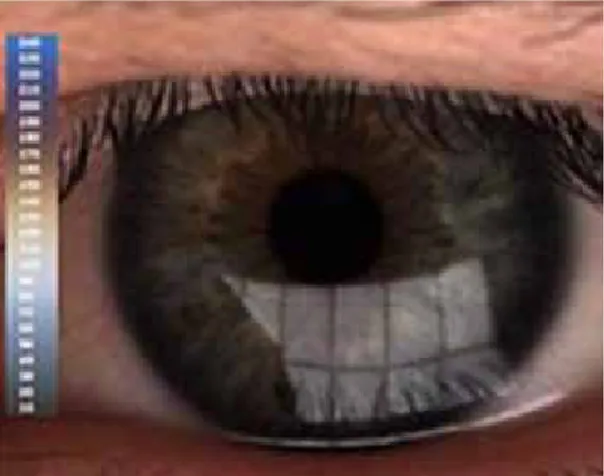
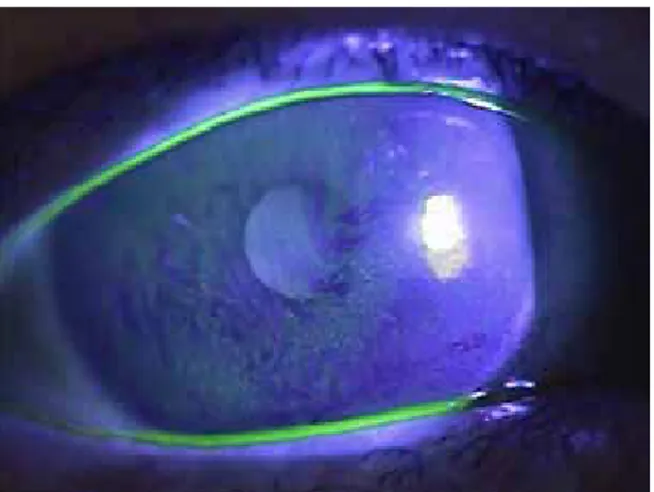
1. 병력 안구건조증은 주관적 증상이 다양한 형태로 나타난다. 이 물감, 작열감, 콕콕 찌르는 아픔, 가려움, 뻑뻑함, 쓰라림, 눈 꺼풀이 무거운 느낌, 눈부심, 안구 피로감, 눈물흘림 등으로 나타난다. 일반적으로 수성 눈물 결핍에 의한 건성안에서는 오후가 되면 증상이 악화되고, 마이봄샘 질환에 의한 건성안 에서는 아침에 증상이 더욱 심하다. 또한, 표준화된 설문조 사를 통한 병력청취도 진단에 도움이 되는데 스크리닝과 치 료효과의 경과 관찰에도 활용된다. 설문조사에는 심한 정도, 일상생활에 대한 영향, 삶의 질을 포함 한 다양한 질문이 포함된다[11]. 눈물 분비에 영향을 미칠 수 있으므로 현재와 과거의 환자 약물 복용력을 조사 하는 것도 중요하다. 폐경 여부와 호르 몬 치료 여부 또한 조사해야 한다. 마지 막으로 전신 검사를 통해 구강건조 여부 와 치과적 질환 병력을 조사하여 쇼그렌 증후군이나 건성안과 관련된 다른 전신 적 질환이 있는지 알아봐야 한다. 2. 이학적 검사 충분한 병력 청취 후, 주의 깊게 이학 적 검사를 하여 건성안의 진단과 그 원 인을 찾는 것이 중요하다. 얼굴과 눈꺼풀 검사를 통해 rosa-cea와 floppy lid 등을 찾아내고, 검사 중 눈깜빡임과 눈꺼 풀 위치를 파악한다. 눈깜빡임의 횟수, 눈깜빡임 사이 간격 의 변화, 눈꺼풀 틈새의 간격, 눈이 적절히 감기는지를 중점 적으로 평가한다. 눈꺼풀 위치이상도 눈물의 순환을 방해하 므로, 눈꺼풀속말림, 눈물점 외반, 반흔성 눈꺼풀이상, 눈꺼 풀 피부이완증, 눈물샘 비대로 인한 이측 눈꺼풀의 부종 여 부 등을 주의 깊게 살펴본다. 세극등 현미경 검사를 통해 눈꺼풀테(충혈, 혈관확장, 두 꺼워짐, 반흔, 각질화, 궤양, 눈물 찌꺼기, 마이봄샘 개구부 의 이상, 마이봄샘 분비물의 양상), 속눈썹(방향이상, 위치 이상, 가피형성, 포도알균성 눈꺼풀 염증), 결막(충혈, 부 종, 각질화, 유두, 여포, 검열반, 결막이완증), 각막(침윤, 흉터, 점상 염색, 궤양, 혈관화, 판누스[pannus], 익상편) 의 이상 여부를 확인해야 한다. 눈물막에서는 실모양체, 점 액, 거품 여부를 살펴봐야 한다. 각막 지각 검사도 모든 환 자에서 필요하다. 상당수의 경도 혹은 중등도 건성안 환자 에서 세극등 현미경 검사만으로 불충분하여 건성안의 진단 과 단계를 나누는 데에 다른 검사가 필요하다. 그 외 현미 경으로 눈물샘의 나오는 부분인 위 바깥쪽의 결막낭을 누 르면 눈물이 나오는 것을 플루레신 검사상 발견할 수 있다 (Figure 1) [12].3. 진단적 검사 1) 마이봄샘 검사 마이봄샘은 눈물막의 지방층을 형성하는 마이붐을 분비하 는 피지샘이다. 마이봄샘에 의해 형성된 지질층은 눈물막의 과도한 증발을 막고 눈물막의 안정성을 유지시킴으로써 눈 물막을 유지하는데 큰 역할을 한다고 알려져 있다. 이러한 마이봄샘의 형태를 관찰할 수 있는 검사로 비접촉 적외선 마 이보그래피가 많이 이용되고 있다. 마이봄샘의 위축 및 탈락 된 정도를 측정하여 grade 1-4로 평가 한다(Figure 2). 2) 눈물막 안정성의 평가 눈물막 중 가장 바깥쪽에 있는 막인 지방층은 눈물이 증발되는 것을 막고 눈 물막 안정성을 유지하는데 큰 역할을 한 다. 눈물의 지방층의 안정성은 광간섭촬 영계를 사용하여 눈물의 지방층의 두께 와 분포를 측정할 수 있다(Figure 3). 모든 건성안 환자에서 눈물막의 안정 성이 감소되어 있는데, 눈물막 파괴 시 간 검사로 평가한다. 주로 사용되는 방 법은 형광염색액이 묻은 검사지에 보존 제를 첨가하지 않은 식염수를 적셔 아 래 결막낭에 묻혀서 검사한다. 이때 염 화벤잘코늄 같은 보존제는 눈물막 파괴 를 더 빠르게 할 수 있으므로 유의한다. 눈을 깜빡여 염색약을 눈물막에 펴지게 한 후, 세극등 현미경을 이용하여 눈을 뜨고 있을 때 염색된 눈물막에 첫번째 깨어짐이 관찰될 때 까지의 시간을 측정 하는 것이다[11]. 눈물막의 안정성을 평 가하는 다른 방법으로 형광염색액을 사 용하지 않는 비침습적 눈물막 파괴 시간이 있다. 이 방법은 타겟을 눈물막의 볼록한 표면에 비춰 그 상이 깨어지기까지 의 시간을 측정하는 것으로, 각막곡률계로도 측정할 수 있다 [11] (Figure 4). 건성 각결막염, 점액질 결핍, 마이봄샘질환에서 눈물막 파괴 시간이 짧게 나타난다. 정상인에서 눈물막 파괴 시 간은 변이가 심하지만, 눈물막 파괴 시간과 비침습적 눈물 막 파괴 시간 검사 모두에서 기준을 10초 이하로 잡는 것 Figure 2. Noncontact infrared meibography (grade 1, 2, 3, 4, respectively).
Figure 3. Lipid tear film interferometer with lipid thickness.
이 눈물막의 불안정성을 스크린하는데 특이도가 있다고 알 려져 있다. 기준을 달리하여 5초 미만을 비정상으로 하기 도 한다[11]. 3) 진단적 염색법: 안구표면 건강상태의 평가 염색액을 이용한 검사는 안구표면 손상과 건강상태를 평 가하는 방법으로 흔히 사용된다. 손상의 심한 정도를 단계화 할 수 있으며, 치료에 대한 반응을 평가하는 데에도 이용된 다. 형광염색, 로즈벵갈(rose Bengal), lissamine green 등 이 있으며, 형광염색이 가장 많이 사용된다. 상피세포가 탈 락되거나 느슨해졌을 때, 형광염색액이 세포 사이 공간에 침 투하게 되며 상피세포의 투과성이 증가하였음을 의미한다 [11]. 점액층이 떨어져 나갔을 때 각막 상피에 침투하기도 한다. 형광염색은 일반적으로 결막보다는 각막에 강하게 염 색된다(Figure 5). 염색이 되는 정도에 따라 점수화 하여 단 계를 나누기도 하며, 황색 필터를 이용할 경우, 염색된 것을 보다 진하게 관찰할 수 있다. 로즈벵갈 염색은 형광염색액에 비해 덜 잘 보이나, 결막에 서는 오히려 더 잘 염색된다. 염색 시 종종 자극감을 주고 반 사 눈물을 증가시킨다. 로즈벵갈은 죽은 상피세포 외에도 정 상적인 점액으로 보호되지 않는 상피세포 또한 염색한다. 로 즈벵갈은 염색액이 묻은 검사지가 주로 사용되나, 1% 용액 형태로도 사용된다. 건성안에서 로즈벵갈 염색의 해석은 염 색 강도와 위치, 두 가지 요소로 평가된다. van Bijsterveld [13]는 염색 위치에 따라 비측 결막, 이측 결막, 각막의 세 구 역으로 나누고 염색 강도를 0에서 3점까지 나누어 최고 9점 까지 평가등급을 제시했다. 수성눈물 결핍에서 로즈벵갈 염 색의 일반적 위치는 눈꺼풀틈새 결막 부위로, 각막윤부를 기 저로 대칭되는 두 개의 삼각형 모양으로 염색된다[11]. 각막 에 비해 결막에 더 강하게 염색되며, 특히 눈알 결막이 가 장 뚜렷하게 잘 보인다(Figure 6). Red-free light을 이용하 면 더욱 잘 보이게 된다. 로즈벵갈의 염색강도는 수성 눈물 의 결핍 정도, 눈물막 파괴 시간으로 측정되는 눈물막 불안 정성, 결막 술잔 세포와 비술잔 상피세포에서 생성되는 점액 의 감소와 좋은 상관관계를 갖는다. Lissamine green B는 로즈벵갈과 염색의 특징 면에서 유사하나, 점안 후 자극 증 상이 적다[11]. 4) 각막 지각의 검사 각막 지각의 감소는 건성안의 원인이자 결과이기도 하다. 감각신경의 차단은 다음 기전에 의해 건성안을 일으킨다. 첫 째, 수성 눈물 분비를 자극하는 구심성 신경신호를 차단하 고, 둘째, 눈깜빡임 횟수를 감소시켜 안구표면을 건조하게 만들고, 셋째, 삼차신경의 영양작용에 영향을 미쳐 안구표 면 상피세포의 성장과 분화를 변형시킨다. 마찬가지로, 오 래된 건성안에서 이차적으로 각막 지각이 감소된다. 이는 안 구표면 눈물분비의 기능적 단위의 이상으로 인한 이차적인 신경 민감도의 감소를 반영한다. 각막 지각을 측정하는 가 장 간단한 방법은 면봉을 이용하는 것으로, 면봉 끝에서 몇 개의 섬유 가닥을 뽑아내어 각막과 결막의 표면에 조심스럽 Figure 5. Fluorescein stain (×16) of cornea in patient of dry eye syndrome.
Figure 6. Rose Bengal stain (×16) of conjunctiva in patient of dry eye
게 닿게 하여 측정한다. 환자의 객관적이고 주관적인 반응을 점수화하게 된다. 촉각측정계는 보다 정확하고 정량적인 검 사 방법으로, Cochet-Bonnet 촉각측정계를 사용한다. 나 일론 단섬유의 길이를 0에서 6 cm까지 조절하여 각막 중앙 을 향해 직각으로 다가가며 측정하고, 최소 4번의 자극에서 50% 이상 반응하면 양성으로 기록한다. 정상치는 4.5 cm이 며, 그 이하일 경우 각막 지각이 감소되었다고 평가한다. 이 러한 각막 지각의 측정은 건성안을 평가하는 중요한 검사 중 의 하나이다. 5) 눈물막의 구성요소 (1) 눈물 오스몰농도
눈물 오스몰농도의 측정은 National Eye Institute에서 제시한 객관적인 건성안의 진단법 중의 하나이다[14]. 일 반적으로 316 mmol/L을 건성안의 기준으로 하며, 진단에 있어서 89%의 정확도를 보인다. 눈물 오스몰농도의 측정 은 건성안의 진단에 민감한 검사이지만 특이도가 낮으며, 눈물샘질환으로 인해 눈물 분비가 감소된 경우와 노출, 눈 깜빡임의 이상, 마이봄샘 질환으로 인해 눈물막 증발이 증 가된 경우에서도 이차적으로 눈물 오스몰농도가 증가될 수 있다[11]. (2) 눈물막 단백질 분석 눈물 내의 단백질은 안구 표면 질환에 중요한 역할을 한다. 리소자임(lysozyme)은 전체 눈물 단백질의 20-40%를 차지하며 나이가 들수록, 건성안에서 감소한다[15]. 매우 민 감도가 높은 검사지만, 특이도가 없는 것이 단점으로, 헤르페 스 각막염, 세균성 결막염, 연기에 의한 자극, 영양실조 때에 도 감소된다. Lactoferrin은 상당한 항균력이 있는 눈물 단백질로 눈물샘 에서 생성되며 눈물샘의 기능을 나타내는 지표로 사용된다. 눈물의 lactoferrin은 Lactocard라는 상용화된 비색계 고체 상 ELISA로 측정되며, 심한 건성안에서 임상증상, 세극등 현미경 소견, Schirmer 검사, 로즈벵갈 염색, 눈물막 파괴시 간과 높은 상관관계를 보인다[16]. 이들 눈물 단백질을 측정 하는 정확하고 상용화된 장비가 나온다면, 눈물 단백질의 분 석은 건성안의 진단과 치료 반응에 대한 평가에 유용하게 사 용될 것이다. 6) 수성 눈물의 생성과 눈물 교체의 검사 Schirmer 검사는 눈물 생성을 측정하는 데에 가장 흔 히 사용되는 검사이다. Schirmer I 검사는 점안 마취를 하지 않으며 반사 눈물을 측정한다. van Bijsterveld는 Schirmer I 검사를 이용해 5분간 검사지 5.5 mm가 젖 는 것을 경계로 수성 눈물 결핍을 진단하였다[15]. 그 결 과 건성안 환자의 83%를 정확하게 진단할 수 있었다. 또한 6-10 mm를 건성안 의심, >10 mm를 건성안으로 분류하 였다. 코를 자극한 후 측정하는 것을 Schirmer II 검사라고 한다. 쇼그렌 증후군에서는 코 자극 후 눈물 생성이 증가 되는 능력이 현저히 감소되어 있으며, 진단적 가치가 있다 [11]. Jones [17]는 국소 점안 마취를 이용하여 반사 눈물 과는 독립된 눈물의 기본 분비를 측정하는 Schirmer 검사 를 대중화시켰다. 점안 마취를 이용한 Schirmer 검사에서 는 일반적으로 3-5 mm 를 기준으로 분류한다. 쇼그렌 증 후군과 같이 심한 건성안에서는 환자의 잔여 눈물 분비 기 능을 측정하기 위해 점안 마취를 하지 않고 Schirmer I 검 사를 하는 것이 도움이 된다. Schirmer 검사는 아래 눈꺼풀의 가쪽 1/3 지점에 검사 지를 넣어 결막을 자극하여 반사 눈물을 측정하는 방법이 다. 하지만, 높은 변이도와 낮은 재현성이 문제가 되어왔다. 점안 마취를 하여 눈물의 기본 분비를 검사하는 경우는 약 간 덜하지만, 검사를 반복할 경우 변이도가 높았는데 이는 Schirmer 검사에 의해 유발된 반사의 정도가 다양하기 때 문이다[11]. 1 mm/min (5분간 5 mm 젖는 것)을 진단기 준으로 Schirmer 검사를 한 경우, 건성안 진단에 90%의 특 이도를 보이나 25%의 낮은 민감도를 보였다[18]. Marci와 Pflugfelder의 연구에 따르면, 수성 눈물 결핍군과 마이봄샘 질환군, 정상군에서 Shirmer I 검사치를 비교해 보면 큰 차 이가 있었다[18]. 정상군과 마이봄샘 질환군에서는 양안 모 두에서 Schirmer I 검사치가 5 mm 이상이었으나, 쇼그렌증 후군 수성 눈물 결핍군의 5%, 비쇼그렌 증후군 수성 눈물 결 핍군의 33%만이 5 mm 이상이었다. Shirmer 검사는 특히 심한 수성 눈물 결핍을 보이는 중증 건성안의 진단에 유용하며, 경도의 수성 눈물 결핍을 보이는 환자의 스크린 검사로 적당하지 않다. 일반적으로 사용되는
10 mm의 진단 기준은 수성 눈물 결핍을 의미하나, 쇼그렌 증후군과 비쇼그렌성 원인으로 세분되어야 하며 쇼그렌 증 후군 환자에서는 대개 5 mm 미만을 보인다.
눈물 분비를 측정하는 또다른 검사는 페놀레드(phenol red)를 함입시킨 특수면사를 이용한 phenol red test 검사 이다. 이 면사를 아래구석결막의 이측에 15초간 넣고, 10 mm 젖는 것을 경계로 진단하며, 56%의 민감도와 69%의 특이도 를 갖는다[19]. 아직까지는 널리 쓰이지 않아 임상적 자료가 많지 않다. 7) 눈물 청소율 검사 눈물 청소율의 감소는 건성안의 발병 기전에 관여한다. 눈 물 교체는 안구표면으로부터 염증성 사이토카인을 제거하 고 새로운 성장인자를 공급하는 데에 중요하다. 눈물 청소율 의 감소는 눈물 사이토카인의 농도를 증가시키고, 만성염증 을 일으킨다[20]. 눈물 교체를 객관적으로 측정하는 방법 중 하나로 형광청 소율검사가 있다. 이는 일정량의 형광염색액을 결막낭에 넣 고 시간 내에 형광염색액이 남아있는 정도로 눈물 청소율을 계산한다. Schirmer 검사지를 이용하여 남은 형광염색액의 양을 알아내는 방법과 형광광도계를 이용하는 방법이 있다. 즉 눈물의 교체가 감소된 경우에는 Schirmer 검사지에 계 속 형광염색액이 남아 있게 되므로 진단할 수 있으며, 형광 염색액이 묻어 나오는 길이로 판정한다. 형광청소율검사는 Schirmer I 검사에 비해 수성 눈물 결핍과 마이봄샘 질환에 서 각막 상피와 눈꺼풀 손상의 정도와 연관관계가 높다고 알 려져 있으나, 검사시간과 노력이 필요하여 임상적으로 널리 사용되지는 않는다. 8) 안구건조증의 정도 눈물의 Shirmer 검사와 눈물막 파괴시간 검사 및 안구표면의 염색 검사를 종합하여 경도에서 심한 정 도까지 네 단계의 grade로 나뉜다 (Table 1) [21]. 안구건조증의 정도 는 치료방침에 밀접하게 반영되고 있다. 4. 전신적 검사 쇼그렌 증후군이 의심되면, 자세한 전신검사와 anti-SS-A, anti-SS-B, 류마티스인자, 항핵항체, ESR (sedi-mentation rate), C-reactive protein과 같은 혈액검사를 시행해야 한다. 추가 검사 필요 시 류마티스 내과의와 협진 을 시행하여 진행한다.
건성안의 치료
건성안의 치료목적은 눈을 보다 편안하게 하고 삶의 질을 높이며 안구표면과 눈물막 본래의 항상성을 회복시키는 데 에 있다. 건성안의 기저 원인을 진단함으로 적절한 치료를 할 수 있다. 1. 인공눈물약 인공눈물, 연고, 겔을 포함하는 윤활제는 모든 단계의 건 성안의 치료에 기본적으로 사용되며, 단독 혹은 다른 치료와 병합하여 사용된다[22]. 대부분의 눈물 대치제는 윤활작용을 하며 그 외 눈물 구성성분의 대체, 염증성 물질의 희석, 눈물 오스몰농도의 감소, 오스몰농도의 증가에 대한 보호 등의 기 능이 있다[23]. 윤활제는 저장성 혹은 등장성 용액으로 전해질, 계면활 성제와 다양한 점성물질을 포함한다. 이상적인 인공눈물 은 무방부제여야 하고, 전해질을 함유하고(특히 칼륨과 중 탄산염), 중합체 형태로 보존시간이 길어야 한다. 또한 중 Table 1. Korean Corneal Disease Study Group guidelines for the diagnosis of dry eye diseaseLevel I Level II Level III Level IV Symptoms Ocular symptoms Sometimes Often Always Daily life limited
Visual symptoms Sometimes Often Always Daily life limited
Signsa) Staining scoreb) <Grade I Grade II Grade III >Grade IV
TBUT Variable 6-10 sec 1-5 sec Immediate
Schirmer-1 Variable <5 to ≤10 mm <2 to ≤5 mm <2 mm Reproduced from Hyon JY, et al. Korean J Ophthalmol 2014;28:197-206, according to the Creative Commons license [21].
a)Positive ocular signs may include conjunctival injection, lid abnormalities (blepharitis, trichiasis, keratinization, and
sym-blepharon), and tear film abnormalities (debris, decreased tear meniscus, and mucus clumping). However, these findings are not considered in the grading of disease severity; b)Oxford system.
성에서 약알칼리성이어야 한다. 인공눈물의 오스몰농도는 181-354 mmol/L로 다양하게 측정된다. 오스몰농도 스트 레스가 있을 때 각막상피세포는 수분을 잃게 되고 부피를 유지하기 위해 세포내 전해질 농도를 올려 보상하려 하지 만, 이로 인해 세포 스트레스 신호 기전이 활성화되고 결국 세포에 손상을 가져오게 된다. 따라서 인공눈물에는 오스몰 농도 스트레스로부터 보호하기 위한 글리세린과 같은 물질 이 포함된다[22]. 인공눈물에 포함된 고분자 결합체들은 점성 물질의 역할 을 한다. 이러한 점성 물질은 인공눈물의 청소율을 감소시 켜 안구에 머무르는 시간을 연장시키므로 환자의 눈이 오 랫동안 편안하게 한다. 또한 점성 물질은 안구표면 점액질 의 보호작용을 유지하고 스스로도 코팅효과를 지니므로 마 찰 손상을 감소시키는 효과가 있다. 인공눈물에 포함되는 점성 물질로는 carboxymethylcellulose, polyvinyl alchol, polyethylene glycol, propylene glycol, hydroxypropyl-guar, 피마자유나 파라핀 등의 지질성분 등이 있다[24]. 지질성분을 함유한 인공눈물은 눈물막의 지질층을 보호 하여 눈물의 증발을 감소시키므로, 마이봄샘 기능장애 환 자의 경우 유용하게 사용할 수 있다. Hydroxypropyl-guar 은 안구의 pH에 노출되면 생접착성분을 형성하는 것으로 알려져 있는데, 이는 안구표면 수분의 저류를 일으키고 눈 물막의 점액층 역할을 함으로서 안구표면을 보호한다[22]. 히알루론산은 자연적으로 발생하는 점탄성 물질이다. 소규 모 비교연구에 의하면, 히알루론염을 포함하는 인공눈물 은 생리 식염수나 기타 점성물질(CMC19, hydroxypropyl-methylcellulose/dextran)을 사용한 군에 비해 건성안 증상 이 뚜렷하게 개선되는 효과를 보였다. 높은 점도의 인공눈물 은 일시적으로 흐려보일 수 있어서, 경도나 중등도의 건성안 에서는 낮은 점도의 인공눈물이 선호된다. 그러나 심한 건 성안에서는 증상호전을 위해 높은 점도의 안약을 사용하기 도 한다[23]. 일반 인공눈물은 오염의 위험이 있기 때문에 미생물의 번 식을 막고 유통기간을 늘이기 위해 보존제를 포함하고 있다 [22]. 보존제에는 계면활성제와 산화물질 두 종류가 있다. 계면활성제는 세균의 세포막 투과도를 변화시키는 작용을 하지만, 안구표면 상피세포에도 독성효과를 나타낼 수 있으 며, 자주 사용할 경우 상피세포의 자극과 손상을 일으킬 수 있다. 눈물막이 손상된 환자는 고위험군이다. 염화벤잘코늄 은 계면활성제 계열의 보존제로 안과 점안액에 가장 널리 쓰 이는 물질이다[22]. 산화물질은 직접 세균 세포막에 침투하 여 세포내 대사를 방해한다. 그러나 점안할 경우 안구와 접 촉하자마자 물이나 산소로 바뀌는 특징이 있어 눈에 손상을 유발하지 않는다. 염화산소 복합체도 산화 보존제의 한 종 류이다. 보존제가 포함된 인공눈물은 경도의 건성안 환자에 게 하루 4-6회 사용을 넘지 않는 선에서 무리 없이 사용할 수 있다[22]. 이때 녹내장 치료제와 같은 다른 점안액이 추 가로 필요할 경우 고려하여 결정한다. 만약 이보다 더 잦은 사용이 필요한 경우라면, 보존제가 포함되지 않은 인공눈물 이 추천된다. 안연고와 겔 역시 건성안 치료에 사용된다. 연고는 파라핀 과 바셀린의 특수한 혼합물이다. 어떤 제품은 lanolin을 포 함하는데, 이는 안구 자극 또는 각막의 상처 치유를 지연시 킬 수 있다[22]. 일반적으로 연고는 세균증식과 무관하므로 보존제가 필요하지 않다. 안연고와 겔은 점성이 높으므로 점 안액보다 오랜 시간 유지된다. 수면 중과 같이 수성 눈물 분 비가 감소되는 상황에서도 안구표면을 잘 도포하므로 야간 에 혹은 환자가 눈을 감고 있어야 하는 경우에 주로 사용된 다[22]. 고분자 아크릴산 중합체를 포함하는 겔은 인공눈물 보다 유지시간은 길고 바셀린 연고보다 흐려 보이는 현상은 덜한데, 눈물 내 salt 성분에 의해 아크릴산의 점도가 빠르게 감소하기 때문으로 추측된다. 2. 기존 눈물의 보존 1) 눈물점 폐쇄 눈물점 폐쇄는 수성 눈물 결핍 건성안 환자에서 눈물을 보존하는 유용한 방법이다[22]. 눈물점과 눈물소관을 막는 방법은 가역적 폐쇄 방법이며, 전기소작술이나 레이저를 이 용한 방법은 비가역적 폐쇄 방법이다. 아르곤 레이저는 환 자의 눈물 기능에 따라 눈물점 폐쇄의 정도를 조절할 수 있 는 장점이 있다. 가역적 방법들이 많아지면서 비가역적인 수술 방법의 필요성이 줄어들게 되었다[25]. 눈물점 마개는
흡수성과 비흡수성 두 가지 종류가 있다. 흡수성 눈물점 마 개는 콜라겐이나 중합체로 만들어 졌으며 3일에서 6개월까 지 지속기간이 다양하다. 비흡수성 눈물점 마개는 실리콘이 나 친수성 아크릴 재질로 Freeman 스타일로 위쪽은 깃 모 양으로 솟아있고, 좁은 목 부위와 넓은 바닥 부위로 구성되 어 있다. 여러 연구에서 눈물점 마개의 효능은 입증되었는데, 쇼그 렌과 비쇼그렌 수성 눈물 결핍 건성안 환자에서 객관적 및 주관적 호전을 보였다[22]. 눈물점 마개는 Shirmer I 검사 에서 5분간 5 mm 미만이고, 안구 표면 염색 검사에 양성이 며, 건조증 증상을 보이는 건성안 환자에 적응된다[22]. 안구 표면 염증을 보이는 건성안 환자에서는 금기인데, 기존 눈물 의 배출을 막음으로써 염증성 사이토카인을 포함하는 비정 상 눈물과 안구표면과의 접촉을 길게 하기 때문이다. 따라서 눈물점 마개를 삽입하기 전에 안구표면 염증을 치료하는 것 이 추천된다. 눈물점 마개의 흔한 합병증은 눈물흘림이다. 따라서 이 러한 문제를 겪어보기 위해 비흡수성 눈물점 마개를 삽입 하기 전에 처음에는 단기 흡수성 눈물점 마개를 사용하는 것이 권장된다[25]. 다른 합병증은 눈물점 마개의 빠져버 림, 안쪽으로의 이동, 육아종형성, 눈물소관의 염증과 감 염 등이 있다. 2) 콘택트렌즈 다른 치료가 실패할 경우 심한 건성안 환자에서 콘택트렌 즈를 사용할 수 있는데, 각막표면을 보호하고 수분을 공급 하고 눈물막을 보존하고 안구표면의 치유를 촉진할 수 있다. 그러나 콘택트렌즈 자체가 건성안을 악화시킬 수 있기 때문 에 주의 깊게 관찰해야 한다. 실리콘 재질의 렌즈와 경성 콘 택트렌즈가 주로 사용되며, 각막 상피 주변의 눈물막을 유지 하여 마찰을 줄여 안구표면 상피를 보호한다. 눈이 편하고 시력이 호전되며 각막상피 손상이 줄고, 지속각막상피결손 이 치유된다[26]. 그러나 세균성 각막염의 위험이 있으므로 심하게 각막이 망가져 있거나 실모양체 각막염이 심한 중등도 이상의 건성 안에서만 고려하는 것이 좋다. 사용할 경우에도 자주 렌즈를 교체해야 하며, 스테로이드 점안제의 사용을 피하고, 예방적 항생제를 점안하도록 한다. 심한 수성 눈물 결핍 환자의 경 우에는 금기이다. 3. 눈꺼풀봉합 눈꺼풀봉합은 중증 건성안에서만 사용되는데, 심한 epi-theliopathy, 지속각막상피결손, 심한 기질 궤양이 있는 환자 에서 안구표면의 노출을 줄이기 위해 고려해 볼 수 있다[22]. 4. 눈물분비 자극: 분비촉진제 3% 디쿠아포솔나트륨은 P2Y2 수용체 길항제로서 결 막상피세포에서 눈물 분비를 촉진시키고 결막 술잔세포에 서 뮤신 당단백질 분비 증가를 유도하여, 눈물막의 안정성 을 증가시키고 각결막의 상피장애를 호전시킬 수 있는 약 제로 알려져 있다[27]. 특히 무방부제 눈물과 같이 사용했 을 때 더욱 효과를 나타낸다고 보고되었다[27]. Pilocarpine, cevilemine과 같은 콜린 작용약들이 눈물샘에 눈물 분비를 자극하여 심한 수성 결핍 건성안에 사용된다. 5. 눈물 대체제 1) 자가혈청 정상 눈물 속에는 활성단백과 다양한 성장인자가 존재하 는데, 혈청 내에는 이러한 눈물과 유사한 성분들이 다량 함 유되어 있어 심한 건성안 치료에 이용된다. 방부제 없이 냉 동보존되어 3-6개월까지 사용할 수 있다. 기존 연구에서 자 가혈청은 심한 건성안의 증상과 징후를 호전시켜주며, 굴절 교정수술 후 발생한 건성안에서 인공눈물에 비해 로즈벵갈 염색과 눈물막 파괴시간을 줄여주는 것으로 밝혀졌다. 또한 지속각막상피결손의 치료에 이용되며[28], 알부민 성분이 각 막과 결막 상피의 apoptosis를 억제한다. 2) 침샘 자가이식 침샘 악하선의 자가이식은 점액질과 수성 눈물막의 결핍 을 대체할 수 있으며, 완전 수성 눈물 결핍(Schirmer 검사 1 mm 이하)을 동반한 심한 건성안 환자, 눈물점 폐쇄를 시 행한 후에도 지속되는 통증을 호소하는 환자, 무방부제 인공 눈물을 최소한 한 시간 간격으로 점안해야 하는 건성안 환자 에게 적응된다.
6. 염증치료 염증은 건성안의 병인에 중요한 부분이므로, 항염치료는 치료의 중요한 부분을 담당한다. 염증은 오스몰농도의 증가, 만성 자극성 스트레스(콘택트렌즈 등), 전신적 염증성/자가 면역 질환(류마티스관절염 등)에 의해 발생한다. 1) 사이클로스포린 점안 사이클로스포린(cyclosporin)은 건성안의 치료에만 특화하여 미국 식품의약국 승인을 받은 유일한 치료약제이다. 이는 건성안 환자에서 염증성 사이토카인(결막내 IL-6 수치 등)과 결막 내 활성화된 림프구, 염증성 apoptotic marker 를 감소시키고, 결막의 술잔세포의 수를 증가시킨다[22]. 여 러 임상연구에서 사이클로스포린은 다른 전신적 국소적 부 작용 없이 건성안의 증상과 징후를 호전시켰다. 건성안의 항 염치료를 위한 점안 사이클로스포린의 개발로 건성안의 치 료에 있어서 보다 근본적인 기전에 대한 치료로 초점이 바뀌 는 계기가 되었다. Pimecrolimus와 tacrolimus와 같은 다 른 면역 기전에 작용하는 약제들에 대한 연구도 이루어 지 고 있다[29]. 2) 스테로이드 스테로이드는 비특이적으로 여러 염증 반응을 억제하여 면역억제 효과를 나타내게 되는데, activator protein-1과 nuclear factor kB의 활성을 억제하게 된다. 여러 연구에서 4주 가량의 단기간 점안 스테로이드는 건성안의 증상과 징후 를 호전시킨다고 보고되었다. 건성안 환자에서 loteprednol etabonate 0.5% 점안액을 하루 4번 사용하여 유의한 호전을 보고하였으며, 각막 상피가 매끄러워짐을 확인할 수 있었다 [29]. 또한 건성안 환자에서 무방부제 methylprednisolone 점안액을 2주간 사용하고 눈물점 폐쇄를 한 군(1군)과 눈물 점 폐쇄 단독 시행군(2군)을 비교한 연구에서, 스테로이드 사용군에서 건성안 증상과 각막상피 염색 소견의 호전이 유 의하게 높았다. 쇼그렌 증후군과 같은 심한 염증성 질환 환자에서 점안 스 테로이드로 항염효과가 불충분할 경우 단기간의 전신적 스 테로이드를 사용해 볼 수 있다[30]. 스테로이드 점안제는 매우 빠른 반응을 보이는데 효과적 이다. 그러나 감염의 위험을 높일 수 있고, 안압상승, 백내장 발생 등의 제한점이 있어 건성안의 장기간 치료에 적합하지 않다. 따라서 건성안의 악화를 조절하는 단기간 펄스 요법으 로 사용하며, 하루 1-2회로 감량하거나 합병증 발생률이 비 교적 낮은 potency의 스테로이드(loteprednol estabonate나 fluorometholone)로 변경하는 것이 필요하다[29]. 3) 테트라사이클린 건성안에서 테트라사이클린은 항세균성, 항염, 단백질 분 해효소 억제 효과를 근거로 사용된다. 또한 기존 연구에서 만성 눈꺼풀염증에 minocycline과 doxycycline이 효과가 있 다고 알려졌다. 테트라사이클린 유도체인 minocycline과 doxycycline은 조직 내에서 높은 농도를 보이며, 낮은 신청 소율, 긴 반감기, 혈청내 단백질과의 높은 결합력, 낮은 광 감작율로 임상적으로 유용하다. 다양한 농도가 사용되는데, 하루 1회 50-100 mg의 doxycycline 사용 혹은 첫 2주간 50 mg 복용하다가 100 mg으로 2.5 개월 복용하는 용법 등 이 있다. 최근에는 눈꺼풀염증에는 테트라사이클린 약제뿐 만 아니라 눈꺼풀을 마사지해서 마이봄샘의 분비를 촉진하 는 치료와 눈꺼풀 주위의 피부에 강한 빛자극을 주어서 주위 혈관의 리모델링과 마이봄샘 분비를 치료하는 시도도 임상 적으로 활발히 하고 있다. 4) 필수지방산 필수지방산 중 오메가-3 지방산은 염증성 지질 성분 (PGE2, LTB4)의 합성을 억제하고 IL-1과 TNF-α의 생산 을 차단한다[31]. 건성안에서 두 가지 기전으로 유용한데, 첫 째, 염증을 감소시키며, 둘째, 마이봄샘의 지질의 구성을 변 화시킨다[32]. 여성건강연구(Women’s Health Study)의 연 구에 따르면, 오메가-3 지방산을 많이 섭취할수록 건성안의 위험이 낮다고 보고하였다. 동물 건성안 모델을 이용한 연구 에서도, 알파-리놀렌산과 오메가-3 지방산의 국소 점안군 에서 각막 상피 염색과 안구표면 염증이 유의하게 적게 나 타났다[33]. 7. 국소 비타민A 비타민A의 결핍은 건성안을 유발한다. 눈물 내에 레티놀 이 존재하기 때문에, 건성안은 안구표면의 국소적인 레티놀 결핍이라는 가정 하에 여러 연구가 진행되고 있다[31].
8. 점액용해제 눈물의 양이 감소하면 점액 침착물이 눈물층에 생기며 실 모양 각막침착물을 형성할 수 있는데, 국소 acetylcysteine 이 치료에 이용되기도 하는데[34], 5-20%의 희석액을 만들 어 점안한다.
치료지침
기존의 치료지침은 건성안의 원인에 근거하여 사용되었 으나, 치료계획을 세우기에 도움이 되지 않는 경우가 종종 있어왔다. 이에 2003년 Wilmer Institute에서 건성안의 전 문가들이 모여 델피패널(Delphi Panel)을 통한 증상과 징 후에 따른 진단과 단계별 치료지침을 합의하였고 2006년 에 보고되었다. 최근에는 개정된 진단 및 치료법이 2017년 에 보고된 바 있다[2]. 진단에 활용하는 방법으로는 형광염 색(100%), 눈물막 파괴시간(94%), Shirmer 검사(71%), 로 즈벵갈 염색(65%), 각막지형도 검사(41%), 압흔세포 검사 (24%), 눈물 청소율 검사(24%), 안구표면질환 설문지(18%), 눈물 오스몰농도(6%), 결막생검(6%)의 순으로 조사되었다. 또한 눈물기능이상증이라는 개념을 도입하여 눈꺼풀에 병 변을 동반한 경우, 눈물의 분배에 장애가 있는 경우, 눈꺼풀 병변이 없는 경우의 세 가지로 분류하고 각각의 경우에 따 른 치료를 권장하였다. 최근 한국외안부학회에서 건성안에 서 증상과 징후에 근거하여 심한 정도에 따라 4단계로 분류 하고, 각각의 단계에서 한국인에 맞는 건성안의 치료를 체계 적으로 제시하였다(Table 2) [21].결론
안구건조증은 눈물의 결핍과 과도한 눈물의 증발로 인해 생기는 질환으로 눈물의 삼투압이 증가되고 눈물항상성이 상실되어 안구표면의 염증과 눈의 불편감을 일으키는 질환 이다. 안구건조증의 진단에는 불편감에 대한 설문과 눈물분비, 눈물막파괴시간, 눈물오스몰 농도, 각결막 염색 및 지질층 과 마이봄샘 분석 등이 이용되며 안구건조증의 정도에 따라 단계를 나누어 인공누액, 항염증제, 눈물분비 촉진제, 자가 혈청 및 눈꺼풀 치료 등이 치료법으로 사용된다. 안구건조증은 원인에 따라 올바른 진단 및 치료를 해야 완 화될 수 있으며 지속적인 안과 전문의의 치료가 필요한 질환 이다. 찾아보기말: 안구건조증; 눈물막; 마이봄샘 ORCIDEun Chul Kim, http://orcid.org/0000-0002-0310-5663
REFERENCES
1. Lemp MA. Report of the National Eye Institute/Industry workshop on clinical trials in dry eyes. CLAO J 1995;21:221-232.
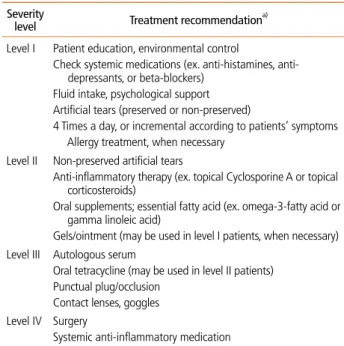
Table 2. Treatment recommendations according to the severity level of dry
eye disease Severity
level Treatment recommendation
a)
Level I Patient education, environmental control
Check systemic medications (ex. anti-histamines, anti- depressants, or beta-blockers)
Fluid intake, psychological support Artificial tears (preserved or non-preserved)
4 Times a day, or incremental according to patients’ symptoms Allergy treatment, when necessary
Level II Non-preserved artificial tears
Anti-inflammatory therapy (ex. topical Cyclosporine A or topical corticosteroids)
Oral supplements; essential fatty acid (ex. omega-3-fatty acid or gamma linoleic acid)
Gels/ointment (may be used in level I patients, when necessary) Level III Autologous serum
Oral tetracycline (may be used in level II patients) Punctual plug/occlusion
Contact lenses, goggles Level IV Surgery
Systemic anti-inflammatory medication
Reproduced from Hyon JY, et al. Korean J Ophthalmol 2014;28:197-206, accord-ing to the Creative Commons license [21].
a)Accompanying ocular surface disease such as blepharitis or ocular allergies should
2. Behrens A, Doyle JJ, Stern L, Chuck RS, McDonnell PJ, Azar DT, Dua HS, Hom M, Karpecki PM, Laibson PR, Lemp MA, Meisler DM, Del Castillo JM, O'Brien TP, Pflugfelder SC, Rolando M, Schein OD, Seitz B, Tseng SC, van Setten G, Wilson SE, Yiu SC; Dysfunctional tear syndrome study group. Dysfunctional tear syndrome: a Delphi approach to treatment recommendations. Cornea 2006;25:900-907.
3. The definition and classification of dry eye disease: report of the Definition and Classification Subcommittee of the International Dry Eye WorkShop (2007). Ocul Surf 2007;5:75-92.
4. Nelson JD, Craig JP, Akpek EK, Azar DT, Belmonte C, Bron AJ, Clayton JA, Dogru M, Dua HS, Foulks GN, Gomes JAP, Hammitt KM, Holopainen J, Jones L, Joo CK, Liu Z, Nichols JJ, Nichols KK, Novack GD, Sangwan V, Stapleton F, Tomlinson A, Tsubota K, Willcox MDP, Wolffsohn JS, Sullivan DA. TFOS DEWS II introduction. Ocul Surf 2017;15: 269-275.
5. Stern ME, Gao J, Siemasko KF, Beuerman RW, Pflugfelder SC. The role of the lacrimal functional unit in the pathophy-siology of dry eye. Exp Eye Res 2004;78:409-416.
6. Zoukhri D. Effect of inflammation on lacrimal gland function. Exp Eye Res 2006;82:885-898.
7. Foulks GN, Bron AJ. Meibomian gland dysfunction: a clinical scheme for description, diagnosis, classification, and grading. Ocul Surf 2003;1:107-126.
8. Tei M, Spurr-Michaud SJ, Tisdale AS, Gipson IK. Vitamin A deficiency alters the expression of mucin genes by the rat ocular surface epithelium. Invest Ophthalmol Vis Sci 2000; 41:82-88.
9. Jee D, Park M, Lee HJ, Kim MS, Kim EC. Comparison of treatment with preservative-free versus preserved sodium hyaluronate 0.1% and fluorometholone 0.1% eyedrops after cataract surgery in patients with preexisting dry-eye syndro-me. J Cataract Refract Surg 2015;41:756-763.
10. Nichols JJ, Sinnott LT. Tear film, contact lens, and patient-related factors associated with contact lens-patient-related dry eye. Invest Ophthalmol Vis Sci 2006;47:1319-1328.
11. Wolffsohn JS, Arita R, Chalmers R, Djalilian A, Dogru M, Dumbleton K, Gupta PK, Karpecki P, Lazreg S, Pult H, Sullivan BD, Tomlinson A, Tong L, Villani E, Yoon KC, Jones L, Craig JP. TFOS DEWS II diagnostic methodology report. Ocul Surf 2017;15:539-574.
12. Kim EC, Doh SH, Chung SY, Yoon SY, Kim MS, Chung SK, Shin MC, Hwang HS. Direct visualization of aqueous tear secretion from lacrimal gland. Acta Ophthalmol 2017;95: e314-e322.
13. van Bijsterveld OP. Diagnostic tests in the Sicca syndrome. Arch Ophthalmol 1969;82:10-14.
14. Tomlinson A, Khanal S, Ramaesh K, Diaper C, McFadyen A. Tear film osmolarity: determination of a referent for dry eye diagnosis. Invest Ophthalmol Vis Sci 2006;47:4309-4315. 15. Nelson JD. Diagnosis of keratoconjunctivitis sicca. Int
Oph-thalmol Clin 1994;34:37-56.
16. McCollum CJ, Foulks GN, Bodner B, Shepard J, Daniels K, Gross V, Kelly L, Cavanagh HD. Rapid assay of lactoferrin in keratoconjunctivitis sicca. Cornea 1994;13:505-508.
17. Jones LT. The lacrimal secretory system and its treatment. Am J Ophthalmol 1966;62:47-60.
18. Serin D, Karsloglu S, Kyan A, Alagoz G. A simple approach to the repeatability of the Schirmer test without anesthesia: eyes open or closed? Cornea 2007;26:903-906.
19. Labetoulle M, Mariette X, Joyeau L, Baudouin C, Kirsch O, Offret H, Frau E. The phenol red thread first results for the assessment of the cut-off value in ocular sicca syndrome. J Fr Ophtalmol 2002;25:674-680.
20. Afonso AA, Monroy D, Stern ME, Feuer WJ, Tseng SC, Pflugfelder SC. Correlation of tear fluorescein clearance and Schirmer test scores with ocular irritation symptoms. Oph-thalmology 1999;106:803-810.
21. Hyon JY, Kim HM, Lee D, Chung ES, Song JS, Choi CY, Lee J; Korean Corneal Disease Study Group. Korean guidelines for the diagnosis and management of dry eye: development and validation of clinical efficacy. Korean J Ophthalmol 2014; 28:197-206.
22. Jones L, Downie LE, Korb D, Benitez-Del-Castillo JM, Dana R, Deng SX, Dong PN, Geerling G, Hida RY, Liu Y, Seo KY, Tauber J, Wakamatsu TH, Xu J, Wolffsohn JS, Craig JP. TFOS DEWS II management and therapy report. Ocul Surf 2017;15:575-628.
23. Asbell PA. Increasing importance of dry eye syndrome and the ideal artificial tear: consensus views from a round discussion. Curr Med Res Opin 2006;22:2149-2157.
24. Argueso P, Tisdale A, Spurr-Michaud S, Sumiyoshi M, Gipson IK. Mucin characteristics of human corneal-limbal epithelial cells that exclude the rose bengal anionic dye. Invest Ophthalmol Vis Sci 2006;47:113-119.
25. Taban M, Chen B, Perry JD. Update on punctal plugs. Compr Ophthalmol Update 2006;7:205-212.
26. Pullum KW, Whiting MA, Buckley RJ. Scleral contact lenses: the expanding role. Cornea 2005;24:269-277.
27. Hwang HS, Sung YM, Lee WS, Kim EC. Additive effect of preservative-free sodium hyaluronate 0.1% in treatment of dry eye syndrome with diquafosol 3% eye drops. Cornea 2014; 33:935-941.
28. Schulze SD, Sekundo W, Kroll P. Autologous serum for the treatment of corneal epithelial abrasions in diabetic patients undergoing vitrectomy. Am J Ophthalmol 2006;142:207-211. 29. Pflugfelder SC, Maskin SL, Anderson B, Chodosh J, Holland
EJ, De Paiva CS, Bartels SP, Micuda T, Proskin HM, Vogel R. A randomized, double-masked, placebo-controlled, multicenter comparison of loteprednol etabonate ophthalmic suspension, 0.5%, and placebo for treatment of keratocon-junctivitis sicca in patients with delayed tear clearance. Am J Ophthalmol 2004;138:444-457.
30. Aronowicz JD, Shine WE, Oral D, Vargas JM, McCulley JP. Short term oral minocycline treatment of meibomianitis. Br J Ophthalmol 2006;90:856-860.
31. Lemp MA. Management of dry eye disease. Am J Manag Care 2008;14(3 Suppl):S88-S101.
32. Pinna A, Piccinini P, Carta F. Effect of oral linoleic and gam-ma-linolenic acid on meibomian gland dysfunction. Cornea 2007;26:260-264.
33. Rashid S, Jin Y, Ecoiffier T, Barabino S, Schaumberg DA, Dana MR. Topical omega-3 and omega-6 fatty acids for treatment of dry eye. Arch Ophthalmol 2008;126:219-225.
34. Albietz J, Sanfilippo P, Troutbeck R, Lenton LM. Management of filamentary keratitis associated with aqueous-deficient dry eye. Optom Vis Sci 2003;80:420-430.
Peer Reviewers’ Commentary
이 논문은 가장 흔한 안과 질환으로 진단은 어렵지 않지만 치료 가 잘 되지 않는 안과 질환 중 하나인 안구 건조증의 역학, 병태 생리, 진단적 접근방법, 실질적인 치료 방법을 체계적으로 기술 하고 있다. 2017년 개정된 안구건조증의 정의를 소개하면서 최 근에 새로 나온 안구건조증의 진단법과 새로 개발된 안약에 대 해서 체계적으로 기술하고 있어 안과 전문의는 물론 전공의, 혹 은 일선 진료 현장에서 안구 건조증 환자를 마주하는 임상의에게 도 진단과 치료를 진행하는데 많은 도움이 될 것으로 기대된다. [정리: 편집위원회]