의학
의학
의학
의학 석사학위
석사학위
석사학위
석사학위 논문
논문
논문
논문
탈출된
탈출된
탈출된
탈출된 추간판
추간판
추간판
추간판 조직의
조직의
조직의 Matrix
조직의
Metalloproteinase-1
과
과
과
과 Matrix
Metalloproteinase-2
의
의
의
의 발현에
발현에
발현에 대한연구
발현에
대한연구
대한연구
대한연구
아주대학교대학원
아주대학교대학원
아주대학교대학원
아주대학교대학원
의학과
의학과
의학과
의학과
강
강
강
강 용
용
용
용 호
호
호
호
탈출된
탈출된
탈출된
탈출된 추간판
추간판
추간판
추간판 조직의
조직의
조직의 Matrix
조직의
Metalloproteinase-1
과
과
과
과 Matrix
Metalloproteinase-2
의
의
의
의 발현에
발현에
발현에 대한연구
발현에
대한연구
대한연구
대한연구
지도교수
지도교수
지도교수
지도교수
전
전
전
전
창
창
창
창
훈
훈
훈
훈
이
이
이
이 논문을
논문을
논문을
논문을 의학
의학
의학
의학 석사학위
석사학위
석사학위
석사학위 논문으로
논문으로
논문으로 제출함
논문으로
제출함
제출함
제출함
200
200
200
2001 년
년
년
년
2
월
월
월
월
아주대학교대학원
아주대학교대학원
아주대학교대학원
아주대학교대학원
의학과
의학과
의학과
의학과
강
강
강
강 용
용
용
용 호
호
호
호
강용호의
강용호의
강용호의
강용호의 의학
의학
의학 석사학위
의학
석사학위
석사학위
석사학위 논문을
논문을
논문을
논문을 인준함.
인준함.
인준함.
인준함.
심사
심사
심사
심사
위원장
위원장
위원장
위원장
김
김
김
김
병
병
병
병
석
석
석
석
인
인
인
인
심
심
심
심 사
사
사 위
사
위
위 원
위
원
원
원
전
전
전
전
창
창
창
창
훈
훈
훈
훈
인
인
인
인
심
심
심
심 사
사
사 위
사
위
위 원
위
원
원
원
이
이
이
이
환
환
환
환
모
모
모
모
인
인
인
인
아
아
아
아
주
주
주
주
대
대
대
대
학
학
학
학
교
교
교
교
대
대
대
대
학
학
학
학
원
원
원
원
2000년
2000년
2000년
2000년 12 월
월
월
월 22 일
일
일
일
감사의
감사의
감사의
감사의 글
글
글
글
이 논문을 끝맺기까지 부족한 저를 위하여 한없이 격려하여 주시고 자상 하게 지도하여 주신 전창훈 교수님께 진심으로 감사 드립니다. 또한 항상 사랑과 격려로써 보살펴 주시고 배움에 눈을 뜨게 해주신 김 병석 교수님께 깊은 감사를 드리며, 특별히 논문을 심사해 주시고 귀한 조언 을 주신 심사위원님 들께도 마음 깊이 감사 드립니다. 끝으로 오늘의 작은 결실을 맺기까지 항상 사랑과 희생으로 자식을 위해 모든 것을 바쳐 주신 부모님께 감사 드립니다. 2000년 11 월 강 용 호−−−−국문국문국문국문 요약요약요약요약−−−−
탈출된 탈출된 탈출된
탈출된 추간판추간판추간판 조직의추간판 조직의조직의조직의 Matrix Metalloproteinase-1 과과과 Matrix 과
Metalloproteinase-2의의의의 발현에발현에발현에 대한발현에 대한대한대한 연구연구연구 연구 추간판 조직의 퇴행성 변화는 추간판의 탈출된 정도뿐만 아니라, 조직의 분해를 일으키는데 관여하는 생체내 효소인 특히, Matrix Metalloproteinase(MMPs)등과 관계가 있다. 이런 MMPs 는 특히 탈출된 추간 판 조직에서 발견되었고, 특히 거대세포, 섬유모세포, 반흔조직과 관련지어 발현되고 있다. 또한, 반흔조직의 형성이 많을수록 수핵 및 섬유륜에 있는 세포와 반흔 조직 내의 세포에서 더 발현이 잘된다고 보고되었다. MMP-1 은 특히 제 I, II, III, X 형의 교원질의 분해에 관여하는 것으로 알려져 있고, MMP-2 의 발현은 무 혈관 조직으로 알려진 추간판 조직에서 혈관 형성과 관련이 있는 것으로 사료된다. 본 연구에서는 정상 상태가 아닌 탈출된 추간 판 조직에서 matrix 1(MMP-1)과 matrix metalloproteinase-2(MMP-2)의 발현의 상태를 비교하여 탈출된 추간판의 형태, 연령별 및 성별 의 차이에 다른 발현의 차이를 연구하고, 어떤 MMPs 가 병리학적인 상태인 탈출된 추간판 조직에서 주로 발현되는가를 연구하고자 하였다. 연구방법으 로 탈출된 추간판 조직을 Hematoxylin-eosin 염색하여 단핵세포의 침윤 및 염증 반응이 관찰되는 반흔 조직을 관찰하고 MMP-1 과 MMP-2 항체를 이용 한 면역염색을 실시하여 MMP-1 과 MMP-2 의 추간판 조직내에서의 발현을
관찰하였다. 본 연구 결과에서는 MMP-1 과 MMP-2 의 발현은 성별, 연령별 및 추간판 조직의 탈출된 정도와는 관련이 없었으며, 탈출된 추간판 조직 내에서 주로 MMP-1 이 관찰되었다. MMP-2 의 발현이 혈관형성과의 관계성에 대해서는 통계학적 의미가 없었으며 검출된 예가 너무 적었기에 추간판 조직에서의 혈관형성에 관여하는 다른 성분과의 비교분석이 필요하였다.
차 례 논문인준서 −−−−−−−−−−−−−−−−−−−−−−−−−−−−− ⅰ 감사의 글 −−−−−−−−−−−−−−−−−−−−−−−−−−−−− ⅱ 국문 요약 −−−−−−−−−−−−−−−−−−−−−−−−−−−−− ⅲ 차례 −−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−− ⅴ 그림 차례 −−−−−−−−−−−−−−−−−−−−−−−−−−−−− ⅵ 약 어 −−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−− ⅶ I.서론 −−−−−−−−−−−−−−−−−−−−−−−−−−−−−−− 1 Ⅱ. 연구내용 ..−−−−−−−−−−−−−−−−−−−−−−−−−−−− 3 III. 연구방법 −−−−−−−−−−−−−−−−−−−−−−−−−−−− 4 A 조직학적 관찰..−−−−−−−−−−−−−−−−−−−−−−−−.4 1. Hematoxylin-eosine 염색법 −−−−−−−−−−−−−−−−− 4 2. 면역 조직화학염색 −−−−−−−−−−−−−−−−−−−− 5 3. Hematoxylin-eosine 염색과 면역 조직화학적 염색판독−− 6 B. 결과분석−−−−−−−−−−−−−−−−−−−−−−−−−−−− 6 Ⅲ.결과 −−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−.7 Ⅳ.고찰 −−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−.8 참고 문헌 −−−−−−−−−−−−−−−−−−−−−−−−−−−−− 12 도 표..−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−−.16 그림 설명 −−−−−−−−−−−−−−−−−−−−−−−−−−−−−19
영문 요약..−−−−−−−−−−−−−−−−−−−−−−−−−−−−− 20
그림 차례
Fig 1. Herniated disc tissue stained with positive immunoexpression with
MMP-1 (x400) ..−−−−−−−−−−−−−−−−−−−−−−− 22 Fig 2. Herniated disc tissue stained with positive immunoexpression with
MMP-1 (x1000) ..−−−−−−−−−−−−−−−−−−−−−−−23 Fig 3. Herniated tissue showing granulation tissue with MMP-2 (x100) .−
약 어
MMPs
.: Matrix Metalloproteinase
.
MMP-1
.
: Matrix Metalloproteinase-1
MMP-2
.
: Matrix Metalloproteinase-2
.. MMP-3
.
: Matrix Metalloproteinase-3
H-E : Hematoxylin-eosine
PBS : Phosphate Buffered Saline
탈출된
탈출된
탈출된
탈출된 추간판
추간판
추간판 조직의
추간판
조직의
조직의 Matrix Metalloproteinase-1
조직의
Matrix Metalloproteinase-2
의
의
의
의 발현에
발현에
발현에 대한
발현에
대한
대한
대한 연구
연구
연구
연구
지도교수
지도교수
지도교수
지도교수 전
전
전 창
전
창
창 훈
창
훈
훈
훈
아주대학교대학원
아주대학교대학원
아주대학교대학원
아주대학교대학원
의학과
의학과
의학과
의학과
강
강
강
강 용
용
용
용 호
호
호
호
I.
서
서
서
서 론
론
론
론
추간판 조직의 생화학적 대사 및 염증 반응에서 세포키나제(cytokine) 및 matrix metalloproteinase(MMP)의 역할은 중요하다고 알려져 있다. 특히 MMP 는 추간판 조직의 대사작용 중 퇴행성 변화 및 병리학적 상태에 따라서 작 용하는 상태가 다르게 나타나며, 또한 이런 과정에 관여하는 MMP 종류도 다르다고 알려져 있다29 . MMP 는 이제까지 약 20 가지 종류가 발견되었으며, 이중 주로 MMP-1, MMP-2 및 MMP-3 가 추간판 조직의 생화학적 반응에 관여하는 것으로 알려 져 있다. MMP-1 는 interstitial collagenase 로 추간판 조직의 세포 외 기질의 대 사에 관여하며, 추간판 조직의 세포 배양에서는 그 존재가 확인되었으나 퇴행성 변화를 보이는 추간 판 조직에서는 발현의 정도 및 추간 판 조직의 부 위에 따른 작용의 차이는 알려져 있지 않다 29 . MMP-2 는 제 4 형 교원질의 대사에 관여하는 것으로 알려져 있다23 . 본 연구에서는 탈출된 추간판 조직에서 MMP-1 과 MMP-2 의 발현의 상 태를 비교하여 어떤 MMP 가 병리학적인 상태인 탈출된 추간판 조직에서 주 로 발현되는가를 연구하고자 한다.
II.
연구
연구
연구
연구 내용
내용
내용
내용
저자가 추간판 탈출증으로 수술하여 얻은 환자 68 명의 추간판 조직을 대 상으로 하였다. 수술시 추간판 조직을 분절화된 상태와 enbloc 의 형태로 채 취하여 섭씨 -70 도로 급냉하여 보관하였다. 조직표본의 일부를 Hematoxylin-eosine 염색하여 단핵세포의 침윤 및 염증 반응이 관찰되는 반흔 조직을 관찰한다. 추간판 조직 내에서 관찰되는 반흔 조직 내에서 MMP-1 과 MMP-2 항체를 이용한 면역염색을 실시하여 각 MMP-1과 MMP-2 의 추간판 조직 내에서의 발현을 관찰한다. 면역 반응의 결과와 성별, 연령별 및 탈출된 추간판의 정도에 따른 발현 의 차이를 연구한다.III.
연구
연구 방법
연구
연구
방법
방법
방법
추간판 탈출증 환자는 수술전 이학적 검사로 하지직거상 검사, 지각 및 운동신경검사, 심부건 반사를 실시하였으며 자기공명 영상 검사를 실시하여 진단하였다. 전 환자는 1 명의 정형외과 척추전문의에 의해서 수술(부분 추궁 판 제거 술 및 추간판 제거술)을 하였다. 추간판 조직의 적출은 추간판에 칼로 창을 낸 후 pituitary forcep 을 이용하여 적출하였으며, 추간판 조직은 수술시 첫번 째로 얻은 조직을 연구대상으로 하였다. 모든 추간판 조직은 수술직후 -70℃ 로 급냉하여 보관하였다. 추간판 탈출의 정도에 대한 분류는 미국 정형외과 학회에서 분류한 방법 을 사용하여 분류하였다15 .A.
조직학적
조직학적
조직학적
조직학적 관찰
관찰
관찰
관찰
추간판 조직을 통상적인 Hematoxylin-eosine 염색법과 MMP-1 과 MMP-2 의 항체를 이용한 면역 조직화학염색법을 이용하여 추간판 조직내의 혈관형성 을 관찰하였다. 염색방법은 다음과 같이 실시하였다.1.
Hematoxylin-eosine 염색법염색법염색법염색법 70℃로 냉동시킨 조직을 실온에서 서서히 녹힌 후 Bouin 용액에 30 분에서 40 분간 고정한 후 흐르는 물에 고정액을 제거하고 Formalin 용액에 고정 하였다. 저농도에서 고농도 알코올까지 이동하여 수분을 제거하고 탈알코올 과정과 Xylene 으로 투명과정을 거친 후 연질 파라핀부터 경질 파라핀까지 항온기에 침투시켜 파라핀 포매 블럭을 만들었다. 박절기로 조직을 얇게(6±2
µm) 짜른 후, 각각의 조직은 4% neutral buffered solution 으로 고정하였으며, 다시 파라핀으로 고정하였다. 각각의 조직(6±2 µm)을 Hematoxylin-eosine 으로 염색하였다(Fig 1). 2. 면역면역면역면역 조직화학염색조직화학염색조직화학염색조직화학염색 각각의 조직절편을 30 분에서 60 분간 56℃ - 60℃ 항온기에서 가온시켜 조직을 슬라이드에 잘 부착시킨 후 60℃ 항온기에서 충분히 건조시켰다. 이 후 Xylene 으로 10 분간 3 회에 걸쳐 탈파라핀시키고 증류수로 세척하였다. 내재성 peroxidase 를 억제하고자 3% 과산화수소(H2O2)와 Methanol 을 섞은 용 액으로 10 분에서 15 분간 처리한 후 증류수로 3 분간 세척하였다. Phosphate buffered solution(PBS)으로 5 분간 3 회에 걸쳐 반복 세척하였다. 비특이성 반 응을 억제하고자 정상 Goat 혈청으로 20 분에서 30 분간 처리한 후 1 차 항체 로 실온에서 1 시간에서 2 시간정도 감작시킨다. 이후 PBS 로 5 분간 3 회에 걸쳐 세척하고. 2 차 항체로 20 분에서 30 분간 반응한 후 5 분씩 3 회에 걸쳐 PBS 로 세척하였다. Labelled serum 으로 20 분간 처치 후 PBS 로 세척하였다. AEC (3amino-9-Ethyl-Carbazone) 용액으로 처리한 후 다시 PBS 로 세척하였다. Hematoxylin - Eosine 염색법으로 대조 염색을 실시하였다.
MMP-1과 MMP-2 항체 (MMP-1 and MMP-2 antibody, Dikopatt, Copenhagen, Denmark)는 1:100 의 농도로 염색하여 탈출된 추간판조직내의 MMP-1 과 MMP-2의 발현을 관찰하였다(Fig 2, 3).
3.
Hematoxylin-eosine 염색과염색과염색과염색과 면역면역면역면역 조직화학적조직화학적조직화학적조직화학적 염색판독염색판독염색판독염색판독 Hematoxylin-eosine 염색의 판독과 MMP-1 과 MMP-2 항체를 이용한 면역 조직화학염색의 판독은 현미경으로 판독하였으며, 면역 염색 상 갈색에서 적 색으로 염색되는 것에 한해 양성으로 판독하였다. 면역 조직 화학 염색 상 양성 반응을 보이는 세포도 양성으로 판독하였다. 조직의 관찰은 2 명이 환 자의 임상기록 및 수술 결과에 대해 숙지되지 않은 상태에서 동시에 조직표 본을 관찰하여 결과가 일치하는 경우에 한해 양성으로 하였으며, MMP-1 과 MMP-2 를 이용하여 면역 조직 화학 염색한 조직은 3 차례에 걸쳐 별도로 관 찰하여 판독 후 결과가 일치하는 경우에 한하여 양성으로 판독하였다. .B.
결과
결과
결과
결과 분석
분석
분석
분석
연령별 및 성별에 따라 MMP-1 과 MMP-2 의 발현의 차이를 연구한다. 탈 출된 추간판의 정도에 따른 MMP-1 와 MMP-2 의 발현의 차이로 비교 분석 한다. 통계처리는 각 지표에 따라서 Chi-square test 를 사용하여 p 값이 0.05 이 하인 경우에 한해 통계학적 의미가 있다고 판정한다.IV.
결
결
결
결 과
과
과
과
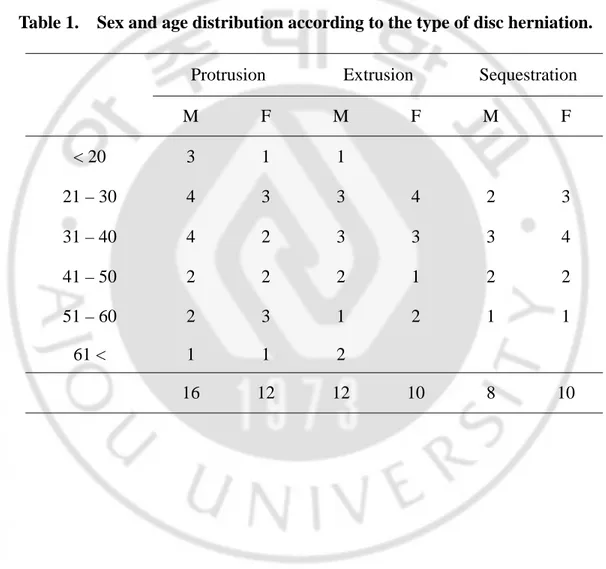
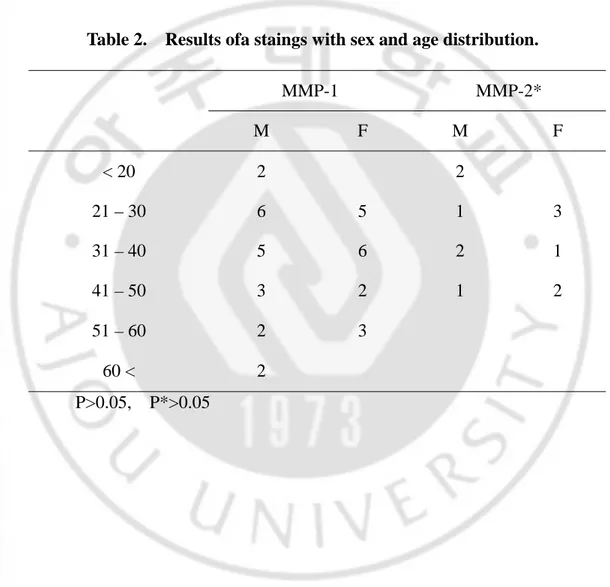
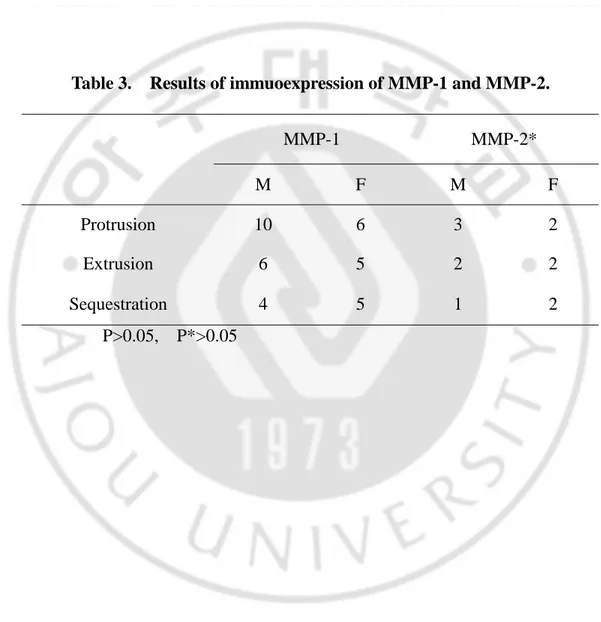
추간판 탈출증으로 연구대상이 된 환자는 남자는 36 례 여자는 32 례로, 연령분포는 17 세에서 67 세였으며 평균연령은 36.9 세였다. 성별에 따라서 돌 출 추간판은 남자 16 례, 여자 12 례, 탈출 추간판은 남자 12 례, 여자 10 례였 고, 격리된 추간판은 남자 8 례, 여자 10 례였다(Table 1). 탈출된 추간판의 정 도와 연령별 분포에서는 20, 30 대에서 가장 많았다(Table 1). 성별 및 연령별 MMP-1과 MMP-2 의 발현의 통계학적 차이는 없었다(p=0.691)(Table 2). 탈출된 추간 판의 정도와 MMP-1 과 MMP-2 의 발현은 탈출 추간 판에서 MMP-1(50%)와 MMP-2(18.2%)의 발현이 제일 많았으나(Table 3), 탈출 된 정 도에 따라서 MMP-1 과 MMP-2 의 발현의 차이는 없었다(p=0.815)(Table 3).V.
고
고 찰
고
고
찰
찰
찰
추간판 조직은 수핵과 섬유륜으로 구성되어 있다. 수핵은 단백다당 (proteoglycan)기질 내에 교원질 섬유가 치밀하지 않게 분포되어 있고, 수분을 많이 포함하고 있다. 수핵은 건조 중량(dry weight)의 65%가 단백다당, 20%가 교원질이며, 나머지는 다른 요소로 구성되어 있다 6, 7. 섬유륜에서는 인접한 척추체 사이에 치밀한 교원질 섬유가 서로 교차하면서 구성하고 있고, 3 차원 적 구성 형식을 이루고 있다. 섬유륜은 건조 중량의 60%가 Collagen, 20%가 단백다당이다6, 7. Matrix Metalloproteinase(MMPs)는 포유동물의 발견되는 4 군의 proteinase(serine, cystein, aspartic, metallo)등이 기질의 분해에 관여한다12. 이제 까지 MMPs 군은 최소한 18 개이상이 확인되었다 20
. MMPs는 다시 4 개의 군 으로 나누어진다 5
. 이중 MMP-1 는 Collagenase 1, interstitial Collagenase, fibroblast Collagenase등으로도 불리며, 교원질(I, II, III, VII, VIII, X)의 분해에 관여한다21
. MMP-2는 72-kd Gelatinase A 72-kd type IV Gelatinase 로 불리며, 교원질 (IV, V, VII, X, XZ), fibronectin, elastin, 당단백 등의 분해에 관여한다21
.
MMPs 에 의한 세포의 기질의 분해정도는 MMPs 의 활동형의 증감에 따라 다르다.
추간판 조직의 퇴행성 변화는 일반적으로 요통에 중요한 역할을 하며, 탈 출된 추간판 조직에 의한 방사통과 관계가 있다. 그러나 이런 질환에 대한
병리 소견에 대해서는 명확히 밝혀진 것은 없다. 추간판 조직의 퇴행성 변화 는 추간판의 탈출된 정도 뿐만 아니라, 조직의 분해를 일으키는데 관여하는 생화학적 매개체 특히, MMPs 등과 관계가 있다. 추간판 조직에서 MMPs 의 역할에 대해서는 세포키나제(Cytokines), 성장인자(growth factor), 추간 판 내 세포 등이 서로 상관관계를 이루고 있다고 한다 12 . MMP-1 은 인체의 조직 에 광범위하게 분포되어 있다고 알려져 있다. MMP-2 는 여러 조직과 세포, 혈장등에 존재한다고 알려져 있다8, 16. 여러 개의 MMPs 중, MMP-1 은 류마토이드 관절염15, 19과 퇴행성 관절염17 의 관절 연골 기질의 분해에 관여하는 것으로 알려져 있다. MMP-1 은 제 2 형 교원질과 단백다당 응집체(Proteoglycan aggrecan)를 포함하고 있는 관절 연 골이 포함된 요추 추간판 조직에서도 발견되었다 29 . MMP-1 은 특히 제 I, II, III, X형의 교원질의 분해에 관여하는 것으로 알려져 있고28 , MMP-1의 추간 판 조직에서의 작용은 조직의 분해 및 퇴행성 변화에는 관여하는 것으로 사 료된다. 최근에는 이런 MMP-1 은 특히 탈출된 추간판 조직에서 발견되었고, 특히 거대세포, 섬유모세포, 반흔 조직과 관련지어 발현되고 있다 29. 또한, 반흔조직의 형성이 많을수록 수핵 및 섬유륜에 있는 세포와 반흔 조직 내의 세포에서 더 발현이 잘된다고 보고되었다 29. 반흔 조직 내의 세포와 수핵 및 섬유륜내의 연골세포 내에서 MMP-1 의 발현은 거대세포에서 분비된 세포키 나제에 의해 증가된 합성의 결과로 보고하고 있다 11, 23. 탈출된 추간판 조직 이 경막의 혈관계에 노출되면 이런 반흔 조직의 형성이 증가하기 때문이며, MMP-1 의 발현도 관계가 있다고 보고되고 있다 29 . 탈출된 추간판 조직의 정
도에 따른 발현의 차이는 반흔조직내에 존재하는 거대세포, 섬유모세포 등의 침윤이 많을 때 나타난다고 보고하고 있다 29 . 추간 판의 탈출된 정도에 따른 MMP-1 의 발현의 차이는 후종인대의 파열과 관계가 있다고 보고된 논문도 있으며, 그 이유로는 두가지를 보고하고 있다 29 . 첫 번째 이유로 proteinase 가 풍부한 반흔조직은 추간판의 분해에 관여할 뿐만 아니라 후종인대의 파열과 도 관계가 있다고 한다. 후종인대의 파열시 인대 내에 포함된 MMP-1 가 proteinase 에 의해서 더 쉽게 분해되어 구조적인 약화가 일어난다고 한다 29. 둘째로, 염증성 반흔 조직이 후종인대 파열로 인해 경막의 혈관계에 노출되 므로써 더 쉽게 형성된다는 이론이다. 그러나 탈출된 추간판 조직에서 신생 혈관 및 섬유 모세포인자의 발현은 탈출된 정도와는 관계가 없다는 보고도 있기에 21,29 두 번째 이론에 대해서는 좀 더 연구가 필요할 것으로 사료된다. 본 연구 결과에서는 탈출된 추간판의 정도와 MMP-1 의 발현은 탈출 추간판 에서 제일 많았으나, 성별, 연령별 및 탈출 된 정도에 따라서 MMP-1 의 발 현의 차이는 없었다. 본 연구에서는 MMP-1 의 발현에 대해서 단순히 추간판 의 탈출된 정도에 따라서 그 발현의 차이를 비교하였으며, 다른 저자들이 보 고하는 탈출된 정도나, 퇴행성 변화의 정도에 대해서는 비교 분석하지 않았 다21, 29.
Matrix Metalloproteinase-2(MMP-2)는 72-KDa gelatinase 또는 72-K-Da type IV collagenase 로 알려져 있고, 최근까지도 MMP-2 의 in vivo 에서 기질 특이성 (substrate specificity)에 대해서는 알려져 있지 않았지만, 주로 gelatin, 제 4, 5 및 7 형 교원질을 분해하는 것으로 알려져 있다 17, 18
에서 발현되며 세포 표면 활성의 특성 (cell surface mode of activation)을 가지 고 있다. 특히 MMP-2 는 세포의 분화, 유착, 이동 및 혈관 형성등에 관여하 며, 세포의 이동을 제한하는 세포의 기질의 방어 벽(barrier)을 제거하는데도 관여한다1, 4, 10, 13, 22, 24, 25, 26 . MMP-2는 잠재성 단백다당의 형태로 분비되어 세 포의 기질에서 활성화되는데, Brown 등 2 은 MMP-2 의 비활성화된 형태인 pregelatinase 의 생리학적 활성화는 세포 표면에서 membrane-associated activator 의 형태로 조절되는 것으로 발표하였다. MMP-2 의 membrane-associated specific activator는 concanavalin A, cytochalasin D, phorbel esters, TGE-β 등에 의해서 여러 세포에서 유도된다 3, 19, 27. 본 연구에서는 MMP-2 의 발 현은 세포질내에서 관찰되었기에 세포 표면에서의 MMP-2 의 활성화에 대해 서 좀 더 연구가 필요하다고 사료된다. 또한 MMP-2 는 세포의 기질의 재형 성에 관여하여 배발생(embryonic development), 영양모 세포(trophoblast) 침습 (invation), 혈관형성(angiogenesis), T 형 세포 이행(transmigration)과 창상치유에 관여한며1, 4, 10, 13, 22, 24, 25, 26 , 신생혈관 형성에도 중요한 역할을 하는 것으로 알 려져 있다. MMP-2 의 발견은 무혈관 조직으로 알려진 추간판 조직에서 혈관 형성과 관련이 있는 것으로 사료되었으나, 본 연구에서는 MMP-2 의 발현의 특성이 탈출된 추간판 조직에서 성별, 연령분포 및 탈출된 추간판의 정도에 따라서 차이를 보이지 않았으며, 발현하는 개체가의 수가 너무 적었기 때문 에 정확한 분석을 하기가 어려웠다. 탈출된 추간판 조직내에서 발견되는 신 생혈관의 발현과의 상관관계는 MMP-2, 섬유모세포 인자 및 신생혈관의 형 성 과정에 대한 더 많은 연구가 필요할 것으로 사료된다
참
참
참
참 고
고
고
고 문
문
문
문 헌
헌
헌
헌
1. Agren MS : Gelatinase activity during wound healing. Br. J. Dermatol, 131:634-640, 1994
2. Brown PD, Levy AT, Margulies IM, et al : Independent expression and cellular
processing of MR 72,000 type IV collagenase and interstitial collavenase in
human tumorigenic cell lines. Cancer Res, 50:6184-6191, 1990
3. Brown PD, Kleiner DE, Unsworth EJ : Cellular activition of the 72 kDa type IV procollagenase/TIMP-2 complex. Kidney Int, 43:163-170, 1993
4. Casasco A , Casasco M, Reguzzoni M : Occurence and distribution of
matrix metalloproteinase-2-immumoreactivity in human embryonic tissues. Eur.
J. Histochem, 39:31-38, 1995
5. Cawston TE and Billington C : Metalloproteinases in the rheumatic disease. J Pathol, 180:115-7, 1996
6. Eyre DR and Muir H : Types I and II collagens in intervertebral disc. Interchanging radical distribution in annulus fibrosus. Biochem J, 157:267-70,
1975
7. Eyre DR and Muir H : Quantitative analysis of type I and II collagens in human intervertebral discs at various ages. Biochim Biophys Acta. 492:29-42, 1977
8. Fujimoto N, Mouri N, Iwata K, Ohuchi E : A one-step sandwich enzyme immunoassay for human matrix metalloproteinase 2 (72-kDa gelatinase/type
IV collagenase) using monoclonal antibodies. Clin Chim Acta, 221:91-103,
1993
spontaneously produce matrix metalloproteinases, nitric oxide, interleukin-6,
and prostaglandin E2, Spine, 21:271-277, 1996
10 Lelongt B, Trugan G, Murphy G and Ronco PM : Matrix
metalloproteinasesMMP2 and MMP9 are produce in early stage of kidney
morphogenesis but only MMP9 is required for renal organogenesis in vitro. J.
Cell Biol, 136:1363-1373, 1997
11 Liotta LA, Abe S, Robey PG and Martin GR : Preferential digestion of
basement menbrance collagen by an enzyme derived from a metastatic
murine tumor. Proc. Natl.Acad. Sci. USA, 76:2268-2272, 1979
12 Matrisian LM : Metalloproteinases and their inhibitor in matirx remodeling.
Trends Genet, 6:121-5, 1990
13 McLaughlin B and Weiss JB : Endothelial-cell-stimulating angiogenesis
factor(ESAF) activates proglatinase A (72 kDa type IV collagenase),
prostromelysin 1 and procollagenase and reactivaties their complexes with
tissue inhibitors of metalloproteinases: A role for ESAF in
non-inflammatory angiogenesis. Biochem. J, 317:739-745, 1996
14 Mizel S, Dayer J-M, Krane SM and Mergenhagen SE : Stimulation of
rheumatoid synovical cell collagenase and prostaglandin production by
partially purified lymphocyte-activating factor (interleukin-1). Proc Natl Acad
Sci USA, 198(78):2474-7
15 Ohshima H, Hirano N, Osada R, Matsui H and Tsuji H : Morphologic
variaton of lumbar posterior longitudinal ligament and the modality of disc
16 Okata Y, Morodomi T, Enghild JJ, Suwuki K : Matrix metalloproteinase 2
from human rheumatoid synovical fibroblasts. Purification and activation of
the precursor and enzemic properties. Eur J Biochem, 194:721-30, 1990
17 Okata Y, Shinmei M, Tanaka O : Localization of matrix metallo-proteinase 3
(stromelysin) in osteoarthritic cartilage and synovium. Lab Invest, 66:680-90,
1992
18 Okada Y, Takeuchi N, Tomita K, Nakanishi I and Nagase H :
Immunolocalisation of matrix metalloproteinase 3 (stromelysin) in
rheumatoid synovioblasts (B cells): Correlation with rheumatoid arthritis.
Ann Rheum Dis, 48:645-53, 1989
19 Overall CM and Sodek J : Concanavalin A produces a matrix-degradative
phenotype in human fibroblasts. Induction and endogenous activation of
collagenase, 72-kDa gelatinase, and Pump-1 is acconpanied by the
suppression of the tissue inhibitor fo matrix metalloproteinases. J. Biol. Chem,
256:21141-21151, 1990
20 Pendas AM, Knauper V, Puente XS : Identificationand characterization of a
novel human matrix metalloproteinase with unique structural characteristics,
chromosomal location, and tissue distribution. J Biol Chem, 272:4281-6, 1997
21 Philippe G, Malcom I. VJ, Jean-Pierre V and Anthomy JF : Matrix
Metallooproteinases: the clue to intervertebral disc degeneration. Spine,
23(14):1612-1626, 1998
22 Romanic AM and Madri JA : Extracellular matrix-degrading proteinases in
23 Seltzer JL, Adams SA, Grant GA and Eisen AZ : Purification and properties
of a gelatin-specific neutral protease from human skin. J. Biol. Chem,
256:4662-4668, 1981
24 Sharkey ME, Adler RR, Brenner CA and Neider GL : Matrix
metalloproteinase expression during mouse peri-implantation development.
Am. J. Reprod. Immunol, 36:72-80, 1996
25 Shimonovitz S, Hurwitz A, Dushnik M : Developmental regulation of the
expression of 72 and 92 kd type IV collagenases in human trophoblasts:A
possible mechanism for control of trophoblast invasion (see comments). Am.
J. Obstet. Gynecol,171:832-838, 1994
26 Stetler-Stevenson WG and Corcoran ML : Tumor angiogenesis: functional
similarities with tumor invasion. In "Regulation of Angiogenesis" (ID
Goldberg and EM Rosen eds), 413-418, 1997, Birkhauser Verlag, Basel
27 Ward RV, Atkinson SJ, Slocombe PM : Tissue inhibitor of
metalloproteinases-2 inhibits the activation of 7metalloproteinases-2 kDa progelatinase by fibroblast membranes.
Biochim. Biophys. Acta, 1079:242-246, 1991
28 Welgus HG, Jeffrey JJ and Eisen AZ : The collagen substrate specificity of
human skin fibroblast collagenase. J. Biol. Chem, 256:9511-9515, 1981
29 Yasumoto M, Matsuyoshi M, Wakao N Hisashi I : The involvement of Matrix
Metalloproteinases and inflammation in lumbar disc herniation. Spine,
Table 1. Sex and age distribution according to the type of disc herniation.
Protrusion Extrusion
Sequestration
M F M F M F
<
20 3 1 1
21
–
30 4 3 3 4 2 3
31
–
40 4 2 3 3 3 4
41
–
50 2 2 2 1 2 2
51
–
60 2 3 1 2 1 1
61
< 1 1 2
16 12 12 10 8 10
Table 2. Results ofa staings with sex and age distribution.
MMP-1 MMP-2*
M F M F
<
20
2 2
21 – 30
6
5
1
3
31 – 40
5
6
2
1
41 – 50
3
2
1
2
51 – 60
2
3
60
<
2
P>0.05, P*>0.05
Table 3. Results of immuoexpression of MMP-1 and MMP-2.
MMP-1 MMP-2*
M F M F
Protrusion 10
6
3
2
Extrusion 6
5
2
2
Sequestration 4 5 1 2
P>0.05, P*>0.05
Legend of figures
Fig. 1. Herniated disc tissue stained with positive immunoexpression with
MMP-1. (x400)
Fig. 2. Herniated disc tissue stained with positive immunoexpression with
MMP-1. (x1000)
-
---Abstracts-
--
-
The study for the correlation between the expression of matrix
matalloproteinase-1 and matrix matallproteinase-2
in the herniated disc tissue
Yong Ho Kang
Department of Medical Sciences
The Graduate School, Ajou University
(Directed by Professor Chang Hoon Jeon)