!\or. J. App/. Micrvbio/. Hivcng Vv/. 15
,I\
‘0.1
,39-42 19871
유전자 조작된 Escherichia coli 에서 생산된 사람 인터페론-(1 주사제의 변이원성에 관한 연구
조남진정인환·정재경·복혜숙·김제학·김현수·유무영 저 1 일제당 (주) 증힐연구소
Mutagenicity Tests pf Human Interferon-a produced by Recombinan t Escherichia coli
Cho ‘ Nam Jin *, In Whoan Jung , Jae Kyung Jung , Hae Suk Bok , Je Hak Kim , Hyun Su Kim and Moo Yung Yoo
Clzνi!
S
lI!{or R & D
CνJl hγ,Dokþyong
,IcJwn 172-75 , Korea
Human interferon-a (Hu rIFN-a )produced by recombinant Escherichia coli was studied for mutagenicity using the Ames method and in vivo cytogenotics. Hu rI FN- a had no mutagenic effect on S. typhimurium(TA 1535 , TA 1537 , TA 1538 , TA 98 and TA 100) at concentrations of 30 , 3000 or 300000 IUjplate. In the cytogenetic study , Hu rIFN-a had no cI astogenic effect on rat ’ s bone marrow cells at concentrations of 1 X 10
6‘3 X 1 0
6or 3 X 10
7IU. These resu It s suggest that Hu rI FN -a has no mutagenic potentia l.
인터퍼1 론이 바이라스에 디|한 저항성을 유발시 킨다는 사설(l)이 발견턴 이후 디1 양 생산볍에 관한 많은 연구가 진행되어 왔으며 (2, 3, 4, 5) 현재는 유전 자 조작법에 의해 대장권 등의 셔l 균에서도 인간의 인터페론을 생산한 수 있게 도 l 였다. 그더나 이와같 이 재조합
DNA
공볍을 이용하여 생산된 인터퍼1 론 (이하Hu rI F N- a
호 칭한)등의 물질을 인체에 샤 용 가능한 제제로 개발하기 위해서는 안전성 시험을 실시하여야 한다.본 연구에서는 대장닫에서 생산된
Hu rI FN-a
의 돌연변이원성 맺 생체내 염색처l 이상 시험을 실시하 여, 변이원성 여부를 조사하였다.재료 및 망법
시료 및 사용용량
유전자 조작된 대장균에서 생산, 정제된
Hu rI FN - a
주사제를vial
당3X 10
6international units(IU)
(국제표준 시료code #
G←023-901-527에 비교한 정량 단위)를 동결깐조시킨 후 -200C 에 보관하였으며, 사Key words
‘Human Interferon-a , l\1 utagenicity
* Corresponding author
39
용시 주/、L용 증류수에 용해시켜 평요한 농도로 희석,
샤용하였다. 또한 본 사험에 사용한
Hu rI FN
•0 의 용로본ß -IFN 3X 10
6I. U
를 사람에 게 정맥주사한 직 후의 혈중농도가320IU j m !
인 정 (6) 을 고려하여Ames
시험의 갱우plate
당30- 3x 10
5 I. U의 농도을 사용하였으여, 영세내 염씩셰 이상시험의 경우 Sprague-Da、、 ley 웅성 렛트에 복강 투여한 결과 LDso 치가3X 10'
I. U인 것으로 관명되어3X
10'과 인 체 사용 예정 농도인3X 10
6 및1X 10'
I. U의3
가지 농도를 사용하였다.대조시료
음성 대조 사료늠
Hu rIFN - a
주사제에서 인터페론 성분을 제외한 것을 사용하였다 Ames 시험의 경우 양 성 대 조 시 료로 서2-aminoanth racene(Wako) , 2 - ni trofl
uorene(Aldrich)은dimeth ylsulfox ide
에,N - methy l- N I- nitro- N -nitro sogu an idin e( N TG ,
Sigma}은 증류수에 용해시켜 사용하였다(
6) .
체내 염색체 이 상시험에서는 양성 대조 사료로 간에서 대사릉 받지 않고 영썩처1
01
^oL을 유발시키는 것으로 알려진(7)ethylmethane sulfonate (E MS)
빚EMS
와 동일한,40
염색체 이 ÃJ-을 유발시키는 NTG 를 열 jE 증류수에 용
해시 켜 사용하였으며 , 사용 용량은 Sprague- Dawley
웅성 랫트에 복강 투여하여 독성을 나타내는 농도로 하였다.
사용균주
제일제당(주)에서 보관중인 Salmo ηella t)φhimur.
IIμn 의
histidine
영양 요구주를 유전형질 확인 시험 (8) 을 통하여 선별한 후 사용하였a며,
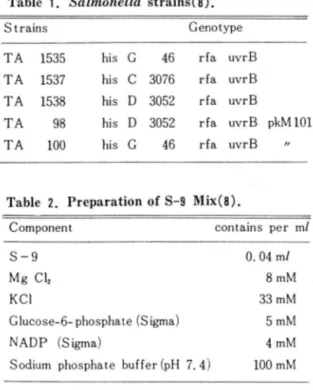
종류 및 유전적특성은 Table 1에 나타내었다.
S-9 Mix
조제 (8)포유동물의 체내대사 상태에 밀접하게 연관시키기 위 해
rat
의 간homogenate
을 균주에 가하게 되는데 그 제조 방법은 다음과 같다.Aroclor 1254(Analab)
200mg 을 1ml 의corn
oil 에 녹인 다응 그0.5ml
을 체중
205g Sprague-Dawley
웅성 랫트의 복%에 주사하여 발암 물질에 대한 간의 효소를 활성화 시켰다. 5 일후 척추분리로
도살시킨후 간을 적출하여 O.
15M KCl
용액으로 혈액 성분을 충분히 씻어내고, 간무 게 g 당 3 배 의 0.15M KCl 용 액 을 가 하 여 homogenizer
로homogenize
시 켰 다 Sorvalcentrifuge SS- 34
rotor 로8700 rpm(9 ,
OOoxg)에서 1 0-분간 원심분리 시켜서 상등액 (S-9) 을 얻은 후S-9
Table 1. Salmonella strains (8).
S trains Genotype
TA 1535 his G 46 rfa uvrB TA 1537 his C 3076 rfa uvrB TA 1538 his 0 3052 rfa uvrB
TA 98 his 0 3052 rfa uvrB pkM 101 TA 100 his G 46 rfa uvrB
Table 2. Preparation of 8-9 Mix(8).
Component
S -9
Mg Cl ,
KCl
Glucose-6- phosphate (S igma) NADP (Sigma)
s 。이um
phosphate buffer (pH 7.4)
contains per ml 0.04 ml
8mM 33 mM 5mM 4 mM 100 mM
Kor. J. Appl. Microbio l. Bioeng.
Mix를 조제하였으며, 그 조성은
Table 2
와 같다.돌연변이 복귀 시힘 (8)
Nutrient broth(Oxoid
No.2) 에서 12시간 암소배양 한 균현탁액0.1ml ,
각 시료 용액O. 1ml , S-9 Mix
0.5ml 을 45"C 로 유지된 2ml 의top
agar 를 넣은 시 험관에 넣고 흔합한 후minimal glucose plate
에 부 어 고루 퍼지게 하여 굳혔다. 굳은 plate 은 3TC 에서 48시간 배양한 후 군집수을 세었다. 이때S-9
Mix 를넣지않고 증류수를 사용한 대조 실험도 병행하였다.
생체내 염색체 이상시험
1)
시료의 투여Sprague- Dawley
웅성 빛 자성랫트 각 3 마리씩을 1 개군으로 하여 음성 대조군 양성
대조군 및 시험물질 처리군의3
개군으로 나누어, 처리 농도 별로1
회 또는 수회 복강 투여하였다.2)
염색체 표본 제작:
척추 분리로 도살하기2
시간 전에colcemid(Sigma) 0.8 mg
을 복강 투여하였다(7).
대퇴부를 절단하여 골수에26-gauge
주사 바능을 삽입한 후 생리식염액을 주입하여 원심관에 골수 세 포를 수거하였다. 800rpm 으후
5
분간 원심분려하여 상등액은벼라고 침전된 세포에 O. 075M KCl 용액 3
ml을 첨가하여 부유시키고 3TC 로 미리 조절된 항온 수조에서 15분간 정치시켰냐. 다시 원심분리한 후 새롭 게 안은 고정액 (glacialacetic acid:methanol , 1 : 3)
을 첨가하였다. 얼음 상에서 15분간 정치시킨 후 원심 분리를 하였다. 고정은 고정액을3
번 정도 갈아주었으 며, 마지약 고정에서는 침전된 세포의 %벼! 따라 고정액의 %L을 변화시켰다. 세포흔 고정시킨 후 20-30cm
의 높이에서 깨끗한 슬라이드에 부유시킨 세포들을 떨 어뜨린 후 공기 건조법에 의해 자연건조 시켰다.3)
염색체의 염색:
슬라이드플 2-3일간 상온에 방치 시 킨 후 0.15 M N aCl(pH 7. 0) 에 용해시 킨 0.025%
트링신 용액에
넣였다 (9). 트럽신 처리 시간은 4 분을
전후하여 슬라이드의 상태에 따라 다르게 하였다.2%
Gurr Giemsa(pH 6.
8) 로 20-분간 염색하였고 증류수로 씻어내었다. 현미갱 하에서, 낮은 배율에서 중기 염색 체가 잘 퍼져있고 높은 배율에서 염색체들이 서로 잘 구분되는 세포안을 선멸하여 사진 촬영후 현상, 인화하 였다.염 색체 이상은 인화된 사진 -^J(에서
Evans
등 (10) 의정의에 따라 본 실험 조건 하에서 판별 가능한 gap ,
breakage, ring formation, dicentric and fragment
맞 숫적 이상의 유무을 조사하였다.
VoL .15 , No . l , 4 1
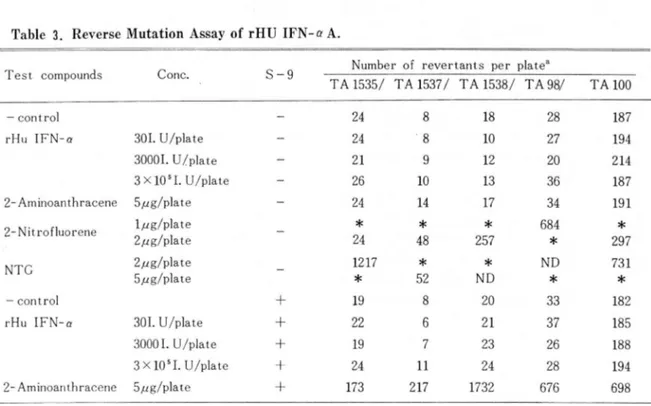
Table 3. Rever se Mutation Assay of rHU IFN-a A.
T est compounds Conc. S-9 Number of revertants per p!ate'
T A 1535/ T A 1537/ T A 1538/ T A 98/ T A 100
- contro ! 24 8 18 28 187
rHu
IFN-α30I. U/p!ate 24 8 10 27 194
3000I. U/p!ate 21 9 12 20 2 14
3X lO ' I. U/p!ate 26 10 13 36 187
2- Aminoanth racene
5μg/p!ate24 14 17 34 19 1
2- Nitro fluorene
2μg/p!ate 1μg/p!ate24 * 48 * 257 * 684 *
* 297
NTG
2μg/p!ate 5μg/p!ate12 17 * * ND 73 1
* 52 ND * *
- contro! + 19 8 20 33 182
rHu IFN-a 30 I. U/p!ate + 22 6 21 37 185
3000 1. U/p!ate + 19 7 23 26 188
3 x 10' 1. U/plate + 24 11 24 28 194
2- Am inoanthracene
5μg/p!ate+ 173 217 1732 676 698
a; Mean of 3 p!ates
* ; not tested ND: N ot determined
Ta ble 4. Effec ts of Hu rI FN- m o n the chromoso mes of r at ’ s bone ma rrow celIs.
concen- No.of No.of No.of chromosome aberration No. of l' compounds
cell sex chromo
tratlon
1njectlon Gaos Ereaks Ring Dicentric and
examined aps creaKS formation fragment some
contro! 50 F 3 0 0 0 4 1. 5
50 M 0 1 0 0 42
Hu rIFN - a 1 X lQ' I. U 50 F 2 0 0 0 41. 7
50 5 F 1 0 0 41. 3
3X lO'I. U 50 l F 0 2 0 0 42. 4
50 2 F 2 0 0 42. 2
3 x 10' I. U 50 1 F 0 0 0 0 43
50 2 F 0 1 0 0 42.4
50 5 F 2 0 0 0 41. 8
50 2 M 0 0 42
50 5 M 0 0 0 43
NTG 2 mg 50 F 12 4 0 42.8
EMS 0. 1 ml 50 F 10 5 1 40. 8
1) average number of chromosomes in 50 cells tested.
42
결과 및 고찰
돌연변이 복귀 시험
Ames
의 방엽(8)
에 따라S.
typhimμη;umhis-
tidine
영양 요구주의 복귀 시험을 실시한 결과Table
3에 서 볼 수 있듯이S-9 Mix
의 첨 가 유무에 관계없이 음성 대조군과IFN
처리군 간의 통계학적 인 차이가 없응을 알 수 있었다.2- aminoanthracene
처 리 군에 서 는S-9 Mix
비 첨 가시 돌연변이성이 관찰되지 않았지만,S-9 Mix
처리 후에는 돌연변이 유말성을 나타내었다. 그러냐 다른 양성 대조 시료의 경우에는 S-9 Mix 를 처리
하지 않았을 때에도 몇몇 균주에서 돌연변이 유발성 을 나타내 였 다 Spontaneousmutation frequency
를 시험하기 위한S-9 Mix
비처리 음성 대조군의revertant colony
수는 운헌상의s.
tyφhimμrium5
개 균주의spontaneous revertant
수 범 위(6, 8)
내 에 있는 것으로 판명되었다. 따라서Hu rI FN-a
는s.
l)φhimurium
T A 1535, T A 1537, T A 1538, T A 98
빛 TA100의5
개 균주에 대해 돌연변이 유발성 을 나타내지 않는 것으로 사료되었다.생체내 염색체 이상 시험
랫트의 골수 (bone
marrow)
세포을 이용하여 iηvzvo
에서 엽색처1 이상을 유말시키는 지의 여부를 시 험 한 결과Table
4에서 보듯이Hu rI FN-a
주사제 처리군은 읍성 대조군에 비교하여 이상 염색체의 갯 수에 통계학적 유의치를 보이지 않았으며, 처리 농 도에 비려l 하여 증가하지도 않았다. 유발된 염색처}이상은 gaps 과
breaks
등 실험조건 (10) 에 따라 발생될 수 있는 종류의 이상이고 양성 대조군에서와
같이ring formation , dicentric and fragment
의 이 상은 관찰되지 않았다.이상의 결과로 본 실험 조건하에서
Hu rI FN - a
주사제는 염색체 이상을 유발시키지 않음을 알 수。 10<r l
λλ λ人「
요 。 t-,
S.
l)φhiη2μ rium 과 랫트의 골수 세포를 이용하여Kor. J. App/. Microbio/. Bioeng
유전자 조작된
E. coli
에서 생 산된Hu rI FN- a
를이용하여 제조된
주사제의 변。1 원성을조사하였다.
s.
l)φhimμriumT A 1535, T A 1537, T A 1538, TA98
빛 TA100의5
개 균주는30-3X10
5I.U/
plate 의 인터페론 농도에서 돌연변이성을 나타내지 않았으며 ,
zn vzvo
실험으로 랫트의 골수 세포를 이 용한 염색처l 이상 시험에서는 처리된Hu rI FN- a
의 농도차에 대한 이상 염색체 유말성이 나타나지않았고, 성에 관계없이 웅성과 자성 랫트에서 유의 성 있는 양성 반응도 나타나지 않았다.
이상의 실험 결과로
HurIFN-a
주사제는 변이원 성을 갖지않는 것으로 판병되었다.참고문헌