대한소화기학회지 2005;45:174-180
ꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏ 접수: 2004년 7월 12일, 승인: 2005년 1월 10일 연락처: 이승규, 138-736, 서울시 송파구 풍납 2동 388-1
울산대학교 의과대학 서울아산병원 외과학교실 Tel: (02) 3010-3480, Fax: (02) 474-9027
E-mail: sglee2@amc.seoul.kr
ꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏ Correspondence to: Sung-Gyu Lee, M.D.
Division of Hepatopancreatobiliary Surgery and Liver Transplan- tation, Department of Surgery, University of Ulsan College of Medi- cine, Asan Medical Center, 388-1 Pungnap-dong, Songpa-gu, Seoul 138-736, Korea
Tel: +82-2-3010-3480, Fax: +82-2-474-9027 E-mail: sglee2@amc.seoul.kr.
간이식 수술 후 재발된 B형 간염 환자 및 de novo 감염 환자에서 Adefovir의 치료 효과에 대한 예비 보고
울산대학교 의과대학 서울아산병원 외과학교실
김건국․김기훈․황 신․안철수․문덕복․하태용․이승규
Therapeutic Effect of Adefovir Dipivoxil on Recurrent or de novo Infection of Hepatitis B Virus after Liver Transplantation:
A Preliminary Report
Keon-Kuk Kim, M.D., Ki-Hun Kim, M.D., Shin Hwang, M.D., Chul-Soo Ahn, M.D., Deok-Bog Moon, M.D., Tae-Yong Ha, M.D., and Sung-Gyu Lee, M.D.
Division of Hepatobiliary Surgery and Liver Transplantation, Department of Surgery, University of Ulsan College of Medicine and Asan Medical Center, Seoul, Korea
Background/Aims: Anti-viral therapy using hepatitis B immune globulin and lamivudine could not prevent HBV recurrence after liver transplantation (LT) completely. Adefovir dipivoxil is a acyclic nucleotide phosphate analogue and known to have potent anti-HBV effect. In this study, we analyzed the therapeutic effect of adefovir for recurrent or de novo HBV infection after LT. Methods: From December 2002 to October 2004, adefovir was administered in 12 post-LT patients of HBV infection (11 recurrent and 1 de novo infection). In these patients, lamivudine and other combined therapies were used before the introduction of adefovir. Thereafter, adefovir combined with lamivudine was administered to all patients. Results: The duration of adefovir administration was 5.5-18 (median, 15.5) months. The median values of serum AST and ALT levels were significantly reduced from 86±80 IU/L and 140±103 IU/L, respectively before the adefovir administration to 42±19 IU/L and 38±33 IU/L after 2 months of administration. This trend of improved liver function persisted throughout the follow-up period.
HBeAg seroconversion was achieved in 4 of 10 patients (40%) and HBsAg seroconversion was observed in 1 of 10 patients (10%). HBV DNA levels have decreased to undetectable levels by hybridization assay in 6 of 7 patients within the first 2 months of therapy. Nephrotoxicity and hypophosphatemia were not found in all of these patients. Conclusions: Based on this preliminary result, adefovir dipivoxil seems to be an effective and safe antiviral agent leading to viral inhibition and clinical improvement in post-LT patients with recurrent or de novo HBV infection. (Korean J Gastroenterol 2005;45:174-180)
ꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏ
Key Words: Adefovir; Hepatitis B virus; Liver transplantation; Lamivudine
김건국 외 6인. 간이식 수술 후 재발된 B형 간염 환자에서 Adefovir의 치료 효과 175
서 론
1980년대까지만 해도 B형 간염 환자의 간이식 재발률과 사망률은 높았지만,1,2 B형 간염 면역글로불린(HBIG)이 도입 되면서 B형 간염의 재발률은 현저하게 낮아졌고,3 B형 간염 재발 방지를 위해 세계적으로 많은 이식센터에서 HBIG을 투여하고 있다. 또한 뉴클레오티드 유사체인 라미부딘의 항 바이러스 효과가 인정되면서 B형 간염 재발 방지를 위해 라미부딘 단독요법 또는 HBIG과 병합요법이 흔히 이용되 고 있다. 라미부딘은 HBIG을 이용한 예방요법 시 재발된 B 형 간염환자에게 일차적인 치료약제로는 사용 가능하다. 그 러나 라미부딘을 장기 투여 시 YMDD (tyrosine-methionine- aspartate-aspartate) 변종 바이러스가 발생하고 이로 인해 임 상 및 혈청, 생화학 악화로 귀결된다는 문제점이 있다.
YMDD 변종에 의한 돌파현상의 발생률은 라미부딘 투여 1 년 경과 후에는 30%,4 2년에 45%,5 3년에 63%6이다.
한편 라미부딘의 장기 투여로 인한 YMDD 변종 바이러 스의 치료제로 adefovir가 뛰어난 바이러스 증식억제 효과와 안정성을 가지며,7,8 2002년 말부터 국내에 도입되어 사용 중 이지만 adefovir의 치료효과에 대한 국내보고는 아직 없다.
이 연구는 만성 B형 간염에 의한 간경변으로 간이식을 받 은 후 재발된 경우와 간이식 후 발생한 de novo B형 간염 환자를 대상으로 투여한 adefovir의 치료 효과를 임상, 혈청, 생화학 측면에서 분석하여 그 유용성에 대해 알아보고자 하 였다.
대상 및 방법
1. 연구대상
2002년 12월부터 2004년 10월까지 병원에서 B형 간염 재 발이 확인된 14명의 간이식 환자에게 adefovir를 투여하였 고, 이 중 섬유성 담즙정체 간염(fibrosing cholestatic hepa- titis, FCH)의 진행으로 인해 재이식 수술에도 불구하고 사망 한 1예와 HBsAg 양성인 기증자로부터 이식 편을 받은 1예 의 환자를 제외한 12명의 환자를 대상으로 하였다. Ade- fovir를 투여한 12명의 환자 중 11명에서 B형 간염이 재발하 였고, 원발 질환이 C형 간염이었던 1명에서 발생한 de novo 감염이 포함되었다. 연령의 중앙값은 46 (40-58)세, 남녀비 는 9:3이었다.
2. 연구 방법
1) B형 간염 재발 방지요법
본원에서 사용하는 B형 간염 재발 방지요법은 고용량의 HBIG를 이용한 수동면역법이다. 간이식 수술 중 무간기
(anhepatic phase)부터 HBIG (HEPA-BIG, Green Cross Phar- macy, Seoul, Korea) 10,000 U를 투여하기 시작하여 수술 후 첫 1주일간 매일, 다음 한 달 동안은 매주, 그리고 이후에는 매달 10,000 U를 투여하는 방식이다. HBIG의 투여는 anti- HBs 역가에 따라 투여 간격을 개인적으로 다르게 조정하였 고, anti-HBs 역가를 수술 후 6개월까지는 1,000 IU/L, 그 이 후에는 500 IU/L 이상 유지시켰다.
2) B형 간염의 재발 진단 및 Adefovir 투여 전까지의 치료요법
B형 간염의 진단은 혈청 진단을 이용하였고, 혈청검사에 서 음성이더라도 간생검의 면역조직화학염색에서 HBsAg 이나 HBcAg이 검출된 경우에 B형 간염 재발로 진단하였 다.
HBsAg, anti-HBs, HBeAg 및 anti-HBe는 방사선 면역측정 법(DiaSorin, Vercelli, Italy)을 이용하였고, 혈청 HBV DNA는 액상 교잡법(Hybridization Assay, Abbott, Chicago, IL)으로 측 정하였다. HBsAg, HBcAg에 대한 면역조직화학염색은 상품 화된 I-VIEW DAB Detection Kit (VENTANA, USA)를 이용 하여 immunoperoxidase 염색을 시행하였다.
B형 간염이 재발 또는 처음 진단된 시점에서 adefovir를 투여하기까지의 기간은 1-25 (중앙값 8)개월이었다. B형 간 염 진단 후 면역억제제는 최소한의 용량으로 제한하고, HBIG 투여는 중단하였다. 이와 함께 재발 또는 de novo B형 간염의 치료를 위해 모든 예에서 라미부딘을 100-300 mg 투 여하였다. 또한 8예에서는 famciclovir와 병합요법을, 1예에 서는 famciclovir와 interferon 병합요법을 시행하였다.
3) Adefovir 투약 및 치료 효과 평가
Adefovir가 도입되기 시작한 2002년 12월부터 라미부딘 단독 또는 병합요법에도 불구하고 바이러스 돌파현상이 관 찰된 환자에게 우선 투여하였고, 혈청검사에서 돌파현상이 보이지 않더라도 지속적으로 혈청 AST 및 ALT의 상승(정 상범위 상한가의 1.3배 이상)을 보이는 환자에게 라미부딘 과 함께 adefovir 10 mg을 매일 투여하였다. 약제 투여 후 2 개월 간격으로 외래를 통해 추적 및 관찰을 하면서 투약의 효과 및 부작용을 확인하였다. 내원 시마다 전혈검사, 혈청 전해질, 간기능검사, HBV DNA를 포함한 간염 혈청검사 및 소변검사를 시행하였다.
Adefovir의 치료 효과 평가는 임상, 혈청, 생화학 측면에 서 분석하였고, 각각의 검사치를 adefovir가 도입되기 전에 시행했던 라미부딘 단독 또는 병합요법과 비교하였다.
4) 통계
이 연구에서의 결과치는 각 변수가 정규분포를 보이지 않
176 The Korean Journal of Gastroenterology: Vol. 45, No. 3, 2005
았기 때문에 중앙값과 범위로 표시하였고, 통계 분석에는 SPSS for windows (release 11.0, SPSS Inc., Chichago, IL, USA) 통계 프로그램을 이용하였다. 약물 투여 효과에 대한 분석은 표본 수가 적고 각 쌍의 차이의 분포가 모수 가정을 시행하기에는 너무 불규칙하여 two-related-samples test를 사 용하였고, 비모수 검정법인 Wilcoxon's signed rank test로 검 정하였다. p값은 0.05 미만을 통계적으로 의미가 있는 것으 로 판정하였다.
결 과
1. Adefovir에 의한 B형 간염 바이러스 억제 효과
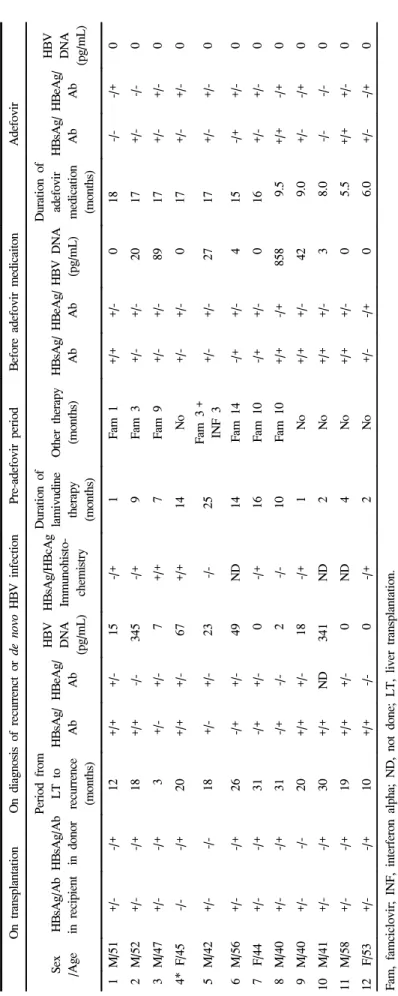
간이식 수술 후 재발까지의 기간은 3-31 (중앙값 19.5)개 월이었다. Adefovir의 투여 기간은 5.5-18 (중앙값 15.5)개월 이었고, 투약이 중간에 중단된 경우는 없었다. 재발된 모든 환자에서 adefovir가 도입되기 전에 라미부딘을 1-25 (중앙 값 8.0)개월 투여하였고, 이 중 7예에서는 famciclovir와 병합 요법, 1예에서는 famciclovir와 interferon의 병합요법을 시행 하였다. 또한 재발된 모든 환자들은 간이식 수술 전 라미부 딘을 3-9개월 복용한 기왕력이 있었다(Table 1).
Adeforvir 도입 전 라미부딘 단독 또는 병합요법은 HBsAg 및 HBeAg를 소실시키지 않았다. HBV DNA는 양성을 보인 9명의 환자 중 4명(44%)에서 음전되었다가 2명에서 돌파현 상이 발생하여 2명(22%)에서만 adefovir 투여 직전에 검출되 지 않았다(p=0.678). 또한 12개월 이상 라미부딘을 사용한 4명의 환자를 대상으로 했을 때, HBV DNA가 3명(75%)에서 음전되었다가, 이 중 2명(66%)에서 라미부딘 투여 7개월, 12 개월 후에 돌파현상이 발생하였다.
Adefovir 투여로 HBsAg 양성이었던 10명의 환자 중 1명 (10%)에서 HBsAg이 소실되었으며, 10명의 환자 중 4명 (40%)에서 HBeAg 혈청전환이 되었다. Adefovir 투여 직전 7 명의 환자에서 HBV DNA가 검출되었는데, 이 중 6명(86%) 의 환자에서 투여 2달 후부터 HBV DNA가 소실되었다. 이 후 모든 환자에서 HBV DNA가 소실되었다(p<0.005). HBV DNA가 소실된 환자 중 돌파현상은 발생하지 않았다(Table 2).
2. Adefovir 투여로 인한 임상, 생화학 효과
Adeforvir 투여 전 라미부딘 단독 또는 병합 투여로 혈청 AST 및 ALT는 다소 호전되었으나, 유의한 차이는 없었다 (Table 3). 또한 adefovir 투여로 혈청 AST, ALT의 중앙값은 각각 86±80 (27-249) IU/L, 140±103 (25-310) IU/L에서 투여 2달 후 42±19 (25-79) IU/L, 38±33 (14-121) IU/L로 유의 하게 감소하였다(p<0.05). 이러한 간기능검사치의 호전은
adefovir 투여기간 내내 지속되었다(Fig. 1).
대부분의 환자들은 B형 간염 재발 및 de novo 감염 후 임 상상이 안정되었지만, 한 환자에서는 재발 직후부터, 또 다 른 1예의 환자에서는 라미부딘 치료 도중 바이러스 돌파현 상이 발생하면서 복수가 증가하고 간기능이 악화되어 Child- Pugh B 등급이 되었다. 이들 2명의 환자에서 adefovir 투여 2 달 후에 Child-Pugh A 등급으로의 호전 및 복수의 소실 등 이 관찰되었다.
3. Adefovir 투여로 인한 합병증 및 부작용
Adefovir 투여 시 무력증, 두통, 오심, 구토, 복통, 신독성 및 저인혈증 등과 같은 부작용이 관찰된 예는 없었다. 모든 환자는 약물 투여로 인한 불편을 호소하지 않았고, 약물 중 단은 없었다.
고 찰
한국에서 간경변의 가장 중요한 원인은 B형 간염 바이러 스 감염으로 전체 만성 간염 원인의 약 70% 정도를 차지한 다.9 간경변 환자의 사망 원인은 간부전, 정맥류 출혈 및 간 신 증후군 등으로 이들의 궁극적인 치료방법은 간이식뿐이 다. 간이식 경험 초창기에 B형 간염에 의한 간경변은 이식 후 높은 재발률과 사망률을 보여 상대적인 금기로 간주되어 왔고, 간이식 후 간염 재발 방지요법을 하지 않으면 80-90%
에서 간염이 재발한다.2 그러나 HBIG 도입 후 B형 간염의 재발률은 현저히 낮아졌다. HBIG를 이용한 B형 간염 예방 요법은 크게 HBIG 단일요법과 다른 항바이러스 제제와 병 합요법이 있는데, 전자의 경우 저용량 요법과 고용량 요법 으로 나뉜다. HBIG 저용량 요법은 대부분의 유럽 이식기관 에서 사용하는데, anti-HBs 역가를 100 IU/L 이상 유지하는 방법이다.10 이 경우 HBeAg과 HBV DNA가 양성인 고위험 군에서 높게는 96%까지 B형 간염이 재발한다.11,12 이런 간 염 재발 고위험군에서의 재발률을 낮추기 위해 anti-HBs 역 가를 500 IU/L 이상으로 높게 유지하는 고용량의 HBIG 요 법이 시도되고 있다.13
한편 HBIG와 라미부딘의 병합요법은 최근에 시도되는 방법으로, 재발률이 0-18%14-16로 효과적으로 재발을 줄인다.
그 외 HBIG가 매우 비싸므로 HBIG를 근주하면서 라미부딘 을 평생 복용하는 방법17 및 이식 직후 HBIG을 단기간 사용 한 후 라미부딘을 평생 복용하는 방법18,19 등이 시도되고 있 다.
B형 간염이 재발되었을 때 치료의 목적은 간병변의 조절 및 이식간 기능의 안정화에 있는데, 이러한 목적을 이루기 위한 일차적인 치료로써 항바이러스제인 라미부딘을 투여 하는 방법이 널리 사용되어 왔다. 재발 B형 간염에 대한 라
Table 1. Demographic and Serologic Characteristics in Recurrent or de novo Infection of Hepatitis B Virus On transplantationOn diagnosis of recurrenct or de novo HBV infectionPre-adefovir periodBefore adefovir medicaitonAdefovir Sex /AgeHBsAg/Ab in recipientHBsAg/Ab in donor Period from LT to recurrence (months)
HBsAg/ AbHBeAg/ Ab
HBV DNA (pg/mL)
HBsAg/HBcAg Immunohisto- chemistry Duration of lamivudine therapy (months)
Other therapy (months)HBsAg/ AbHBeAg/ AbHBV DNA (pg/mL) Duration of adefovir medication (months)
HBsAg/ AbHBeAg/ Ab
HBV DNA (pg/mL) 1M/51+/--/+12+/++/-15-/+1Fam 1+/++/-018-/--/+0 2M/52+/--/+18+/+-/-345-/+9Fam 3+/-+/-2017+/--/-0 3M/47+/--/+3+/-+/-7+/+7Fam 9+/-+/-8917+/-+/-0 4*F/45-/--/+20+/++/-67+/+14No+/-+/-017+/-+/-0 5M/42+/--/-18+/-+/-23-/-25Fam 3+ INF 3+/-+/-2717+/-+/-0 6M/56+/--/+26-/++/-49ND14Fam 14-/++/-415-/++/-0 7F/44+/--/+31-/++/-0-/+16Fam 10-/++/-016+/-+/-0 8M/40+/--/+31-/+-/-2-/-10Fam 10+/+-/+8589.5+/+-/+0 9M/40+/--/-20+/++/-18-/+1No+/++/-429.0+/--/+0 10M/41+/--/+30+/+ND341ND2No+/++/-38.0-/--/-0 11M/58+/--/+19+/++/-0ND4No+/++/-05.5+/++/-0 12F/53+/--/+10+/+-/-0-/+2No+/--/+06.0+/--/+0 Fam, famciclovir; INF, interferon alpha; ND, not done; LT, liver transplantation. *de novo hepatitis B infection (primary disease-HCV).
178 대한소화기학회지: 제45권 제3호, 2005
미부딘의 초기 치료효과는 매우 양호하지만, 라미부딘을 장 기간 사용할 경우 라미부딘 내성 변종 바이러스의 출현빈도 가 높아진다. 이런 변종 바이러스의 출현 및 이로 인한 바이 러스 돌파현상은 치료 시작 후 8-15개월에 발생한다.4-6 라미 부딘 내성 변종 바이러스는 대부분 HBV DNA polymerase 유전자 C domain의 YMDD motif에서 변이가 발생하여 출현 하는데, 552번 codon의 methionine이 valine (M552V)이나 isoleucine (M552I)으로 치환되어 나타난다. M552V 변이는 종종 L528M의 변이를 동반한다.20 이런 일련의 변이는 poly- merase의 구조 변화를 일으켜 라미부딘의 결합력을 약화시 킨다. 변종 바이러스는 야생형에 비해 증식력이 현저히 떨 어져 가볍게 진행하지만,21 간이식 후 면역력이 저하된 환자 에서는 섬유성 담즙정체 간염로 발현되어 재감염된 지 수 주 이내에 환자가 사망하는 급성경과를 취하기도 하므로,22 라미부딘 내성이 발생한 경우 이에 대한 적극적인 대처가 필요하다. 또한 간이식을 받은 환자에서 라미부딘의 투여 효과는 이식 전 비대상 B형 간염 환자에 비해 떨어지는데, 이는 이식수술 전 라미부딘 투여로 인한 돌파현상 발생에 기인하므로, 라미부딘 내성 바이러스의 억제를 위해 라미부 딘 투여를 간이식 수술 전 6개월 이내에 시작해야 한다.23
이 연구에서도 adefovir 투여 전 라미부딘 단독 및 병합요법 의 치료 효과가 미미했던 이유가 이식 수술 전 모든 환자에 서 라미부딘을 복용하였다는 사실과 관계가 있다.
YMDD 변종 출현 시 라미부딘 투여 중단은 증식력이 강 한 야생형의 재발현을 유발하고, 변종 바이러스가 야생형에 비해 증식력이 낮아 라미부딘 투여 전보다 혈청 HBV DNA 와 ALT가 낮게 유지되기 때문에 라미부딘을 계속 투여해야 한다.24,25
한편, adefovir는 야생형 및 YMDD 변종에 의한 B형 간염 모두에 효과가 있으며,7 또한 섬유성 담즙정체 간염 환자에 서도 도움이 된다.26,27 Adefovir는 acyclic nucleotide phosphate analogue로 세포 내 활성 대사물질인 adefovir diphosphate가 HBV DNA polymerase를 억제함으로써 B형 간염 바이러스 의 증식을 효과적으로 억제한다. 간이식 후 재발된 196명의 환자가 포함된 대규모 다기관 임상 연구에서 48주간의 adefovir 투여로 4.3log10 copies/mL 감소 및 96%의 환자에서 Child-Pugh 점수의 호전이 관찰되었으며,28 60주간의 장기간 투여에도 불구하고 바이러스 저항성이 발생하지 않았다.29 이번 연구에서도 약 65주간의 adefovir 투여로 모든 대상 환 자에서 HBV DNA 소실이 관찰되었으며, 돌파현상도 관찰 Table 3. Comparison of Liver Function Test before and
after Adefovir Medication
Median±SD (range) p-value On recurrence
AST (IU/L) 82.5±118 (20-372) ALT (IU/L) 117±158 (14-509) Total bilirubin (mg/dL) 1.0±0.24 (0.8-1.6)
Lamivudine therapy (before adefovir medication)
AST 86±80 (27-249) 0.666 ALT 140±103 (25-310) 0.480 Total bilirubin 1.1±2.7 (0.8-10.5) 0.591
After adefovir medication
AST 26±11.7 (21-55) 0.003 ALT 28±22.3 (12-93) 0.005 Total bilirubin 1.1±0.3 (0.7-1.9) 0.757
Table 2. Comparison of Viral Markers before and after Adefovir Medication
Before adefovir medicaton After adefovir medication p-value
Patients with HBsAg-positive (No.) 10 9 NS
Patients with HBeAg-positive (No.) 10 6 NS
HBV DNA (pg/mL)* 0-858 (median, 3.5) 0-0 (median, 0) 0.018 NS, not significant.
* range (median).
Fig 1. The median values of serum AST and ALT were sig- nificantly decreased during initial 2 months after adefovir dipivoxil treatment. This trend of improved liver function persisted through- out the follow-up period.
김건국 외 6인. 간이식 수술 후 재발된 B형 간염 환자에서 Adefovir의 치료 효과 179
되지 않았다. 그러나 96주간 adefovir를 투여한 124명의 환 자 중 2예에서 변이종이 발견되었고, 변종은 둘다 HBV poly- merase의 D domain에 있는 reverse transcriptase 236번 codon 의 asparagines이 threonine으로 치환된다(rtN236T).30 이 변이 종은 라미부딘에 대해 in vitro 및 in vivo에서 감수성을 보였 다.
최근에 adefovir 외에 emtricitabine, entecavir, telbivudine, clevudine과 같은 새로운 항바이러스제들에 대해 임상 시험 을 진행하고 있으나, 이들 약물들이 YMDD 변종 바이러스 의 증식을 억제하는 데 얼마나 효과적일지는 향후 연구 결 과를 좀 더 지켜본 후 판단해야 할 것으로 보인다.
결론적으로 이 연구의 증례 수 및 관찰기간이 짧기는 하 지만, 연구 결과로 미루어 볼 때 adefovir는 간이식 후 재발 한 B형 간염 또는 de novo 감염 환자에게 바이러스 증식 억 제 및 임상 호전을 위해 효과적이고 안전하게 사용할 수 있 는 항바이러스제제라고 생각한다. 또한 간이식 수술 전 라 미부딘 투여의 기왕력이 있고 돌파현상을 경험한 환자에서 간이식 수술 후 B형 간염 재발 시 일차적으로 adefovir의 신 속한 투여가 필요하다.
요 약
목적: 간이식 후 B형 간염 재발 방지를 위해 HBIG과 라 미부딘을 투여했는데도 재발된 환자에서 이제까지는 별다 른 치료방법이 없었다. YMDD 변종 바이러스의 새로운 치 료제로 각광받는 adefovir가 2002년 말부터 국내에 도입되어 사용 중이지만 adefovir 치료효과에 대한 국내보고가 없는 실정이다. 이 연구는 B형 간염에 의한 간경변으로 간이식을 받은 후 재발된 환자와 de novo 감염 환자를 대상으로 투여 한 adefovir의 치료 효과를 알아보고자 하였다. 대상 및 방 법: 2002년 12월부터 2004년 10월까지 혈청학적으로 B형 간염이 재발되어 adefovir를 투여한 12명의 환자를 대상으로 하였다. B형 간염 재발은 11명이었고, de novo 감염은 1명이 었다. B형 간염이 확인된 시점에서 adefovir 투여까지의 기 간은 1-25 (중앙값 8)개월이었으며, B형 간염 진단 후 HBIG 투여를 중단하고 전 예에서 라미부딘을 100-300 mg 투여하 였다. 또한 8예에서는 famciclovir와 병합요법을, 1예에서는 famciclovir와 인터페론 병합요합을 시행하였다. 이들 12명 의 환자에게 라미부딘과 함께 adefovir 10 mg을 매일 투여하 면서 2달에 한 번씩 투약 효과를 추적 관찰하였다. 결과:
Adefovir의 투여 기간은 5.5-18 (중앙값 15.5)개월이었고, 투 약을 중단한 환자는 없었다. Adefovir 투여 전 혈청 AST, ALT의 중앙값은 각각 86±80 IU/L, 140±103 IU/L이었으며, 투여 2달 후 각각 42±19 IU/L, 38±33 IU/L로 통계적으로 유의하게 감소하였다(p<0.05). 이러한 간기능검사의 안정화
는 추적기간 동안 계속 유지되었다. Adefovir 투여 전 HBsAg 양성이었던 10명의 환자 중 1예(10%)에서 HBsAg가 소실되었으며, HBeAg 혈청전환은 10명의 환자 중 4예(40%) 에서 관찰되었다. Adefovir 투여 전 7명의 환자에서 혈청 HBV DNA가 검출되었는데, 이 중 6명의 환자에서 투여 2달 후부터 HBV DNA가 소실되었다(p<0.005). Adefovir 투여 시 신독성 및 저인혈증 등과 같은 부작용이 발생한 환자는 없었다. 결론: 이 연구의 증례 수 및 관찰기간이 짧기는 하 지만, adefovir는 간이식 후 재발한 B형 간염 또는 de novo 감염 환자에게 바이러스 증식 억제 및 임상 호전을 위해 효 과적이고 안전하게 사용할 수 있는 항바이러스제제로 생각 한다.
ꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏꠏ 색인단어: Adefovir, B형 간염, 간이식, 라미부딘
참고문헌
1. Todo S, Demetris AJ, Van Thiel D, Teperman L, Fung JJ, Starzl TE. Orthotopic liver transplantation for patients with hepatitis B virus-related liver disease. Hepatology 1991;13:
619-626.
2. O'Grady JG, Smith HM, Davies SE, et al. Hepatitis B virus reinfection after orthotopic liver transplantation. Serological and clinical implications. J Hepatol 1992;14:104-111.
3. Samuel D, Muller R, Alexander G, et al. Liver transplantation in European patients with the hepatitis B surface antigen. N Engl J Med 1993;329:1842-1847.
4. Perrillo R, Rakela J, Dienstag J, et al. Multicenter study of lamivudine therapy for hepatitis B after liver transplantation.
Lamivudine Transplant Group. Hepatology 1999;29:1581-1586.
5. Fontana RJ, Hann HW, Wright T, et al. A multicenter study of lamivudine treatment in 33 patients with hepatitis B after liver transplantation. Liver Transpl 2001;7:504-510.
6. Ben-Ari Z, Mor E, Shapira Z, Tur-Kaspa R. Long-term experience with lamivudine therapy for hepatitis B virus infec- tion after liver transplantation. Liver Transpl 2001;7:113-117.
7. Perrillo R, Schiff E, Yoshida E, et al. Adefovir dipivoxil for the treatment of lamivudine-resistant hepatitis B mutants.
Hepatology 2000;32:129-134.
8. Mutimer D, Feraz-Neto BH, Harrison R, et al. Acute liver graft failure due to emergence of lamivudine resistant hepa- titis B virus: rapid resolution during treatment with adefovir.
Gut 2001;49:860-863.
9. Kim DH, Jo CM, Keum MS, et al. Pathological and clinical factors associated with progression to decompensated cirrhosis in patient with chronic hepatitis B. Korean J Gastroenterol 1999;34:764-773.
180 The Korean Journal of Gastroenterology: Vol. 45, No. 3, 2005
10. Samuel D, Bismuth A, Mathieu D, et al. Passive immunopro- phylaxis after liver transplantation in HBsAg-positive patients.
Lancet 1991;337:813-815.
11. Nymann T, Shokouh-Amiri MH, Vera SR, Riely CA, Alloway RR, Gaber AO. Prevention of hepatitis B recurrence with indefinite hepatitis B immune globulin (HBIG) prophylaxis after liver transplantation. Clin Transplant 1996;10:663-667.
12. Lok AS. Prevention of recurrent hepatitis B post-liver trans- plantation. Liver Transpl 2002;8(suppl 1):67S-73S.
13. McGory RW, Ishitani MB, Oliveira WM, et al. Improved outcome of orthotopic liver transplantation for chronic hepatitis B cirrhosis with aggressive passive immunization. Trans- plantation 1996;61:1358-1364.
14. Han SH, Ofman J, Holt C, et al. An efficacy and cost-effec- tiveness analysis of combination hepatitis B immune globulin and lamivudine to prevent recurrent hepatitis B after ortho- topic liver transplantation compared with hepatitis B immune globulin monotherapy. Liver Transpl 2000;6:741-748.
15. Angus PW, McCaughan GW, Gane EJ, Crawford DH, Harley H. Combination low-dose hepatitis B immune globulin and lamivudine therapy provides effective prophylaxis against posttransplantation hepatitis B. Liver Transpl 2000;6:429-433.
16. Seehofer D, Rayes N, Naumann U, et al. Preoperative anti- viral treatment and postoperative prophylaxis in HBV-DNA positive patients undergoing liver transplantation. Transplan- tation 2001;72:1381-1385.
17. Yao FY, Osorio RW, Roberts JP, et al. Intramuscular hepa- titis B immune globulin combined with lamivudine for prophylaxis against hepatitis B recurrence after liver transplan- tation. Liver Transpl Surg 1999;5:491-496.
18. Naoumov NV, Lopes AR, Burra P, et al. Randomized trial of lamivudine versus hepatitis B immunoglobulin for long-term prophylaxis of hepatitis B recurrence after liver transplan- tation. J Hepatol 2001;34:888-894.
19. Park SJ, Paik SW, Do JH, et al. Comparison of the efficacy in HBV prophylaxis after liver transplantation between la- mivudine with one-week HBIg and long-term high dose HBIg. Korean J Gastroenterol 2001;37:26-34.
20. Allen MI, Deslauriers M, Andrews CW, et al. Identification and characterization of mutations in hepatitis B virus resistant to lamivudine. Lamivudine Clinical Investigation Group. Hepa-
tology 1998;27:1670-1677.
21. Seehofer D, Rayes N, Steinmuller T, et al. Occurrence and clinical outcome of lamivudine-resistant hepatitis B infection after liver transplantation. Liver Transpl 2001;7:976-982.
22. Ben-Ari Z, Pappo O, Zemel R, Mor E, Tur-Kaspa R. Asso- ciation of lamivudine resistance in recurrent hepatitis B after liver transplantation with advanced hepatic fibrosis. Trans- plantation 1999;68:232-236.
23. Papatheodoridis GV, Sevastianos V, Burroughs AK. Preven- tion of and treatment for hepatitis B virus infection after liver transplantation in the nucleoside analogues era. Am J Trans- plant 2003;3:250-258.
24. Marzano A, Debernardi-Venon W, Condreay L, Rizzetto M.
Efficacy of lamivudine re-treatment in a patient with hepatitis B virus (HBV) recurrence after liver transplantation and HBV DNA breakthrough during the first treatment. Transplantation 1998;65:1499-1500.
25. Chayama K, Suzuki Y, Kobayashi M, et al. Emergence and takeover of YMDD motif mutant hepatitis B virus during long-term lamivudine therapy and re-takeover by wild type after cessation of therapy. Hepatology 1998;27:1711-1716.
26. Walsh KM, Woodall T, Lamy P, Wight DG, Bloor S, Alexander GJ. Successful treatment with adefovir dipivoxil in a patient with fibrosing cholestatic hepatitis and lamivudine resistant hepatitis B virus. Gut 2001;49:436-440.
27. Lo CM, Cheung ST, Ng IO, Liu CL, Lai CL, Fan ST. Fibro- sing cholestatic hepatitis secondary to precore/core promoter hepatitis B variant with lamivudine resistance: successful retransplantation with combination adefovir dipivoxil and hepatitis B immunoglobulin. Liver Transpl 2004;10:557-563.
28. Schiff ER, Lai CL, Hadziyannis S, et al. Adefovir dipivoxil therapy for lamivudine-resistant hepatitis B in pre- and post- liver transplantation patients. Hepatology 2003;38:1419-1427.
29. Yang H, Westland CE, Delaney WE 4th, et al. Resistance surveillance in chronic hepatitis B patients treated with adefovir dipivoxil for up to 60 weeks. Hepatology 2002;36:
464-473.
30. Angus P, Vaughan R, Xiong S, et al. Resistance to adefovir dipivoxil therapy associated with the selection of a novel mutation in the HBV polymerase. Gastroenterology 2003;125:
292-297.