Abstract : Bortezomib acts by disrupting ubiquitin-proteasome pathway which regulates protein homeostasis within the cell and has demonstrated significant activity mainly against recurrent or newly diagnosed multiple myeloma(MM). Among bortezomib-related side effects, peripheral neu- ropathy(PN) as main dose-limiting non-haematological toxicity can substantially affect the quality of life of patients. It typically requires dose-reduction, delay, or even premature termi- nation of successful treatment. Therefore, predicting the risk for neuropathy before the therapy and a proper management of neurotoxicity are very important considerations.
The aim of this study was to evaluate the incidence of PN, risk factors, and prior exposure to potentially neurotoxic chemotherapy. A total of 108 patients with multiple myeloma(MM) were included, who received bortezomib in Seoul National University of Hospital(SNUH) from May
회원학술보고
다발성 골수종 환자에서 Bortezomib에 의한 말초신경병증 발생과 위험인자 분석
전아영
�, 김성환, 김귀숙, 이혜숙, 김향숙 서울대학교병원 약제부
Analysis of Incidence and Risk Factors for Bortezomib-induced Peripheral Neuropathy in Multiple Myeloma
Ah Young Jeon
�, Sung Hwan Kim, Kwi Suk Kim, Hye Suk Lee and Hyang Suk Kim
Department of Pharmacy, Seoul National University Hospital, 101 Daehak-ro, Jongno-gu, Seoul, 110-744, Korea
투고일자 2014.5.22; 심사완료일자 2014.6.18; 게재확정일자 2014.6.25
�교신저자 전아영 Tel:02-2072-2602 E-mail:30485@snuh.org
연구 배경 및 목적
다발성 골수종(Multiple Myeloma, MM)은 단일클 론 면역글로불린을 만들어내는 형질세포의 neoplastic proliferation으로, 악성형질세포클론이 골수에서 증 식하며 osteolytic lesion, osteopenia, pathological fracture를 동반한 심각한 골격계 파괴를 초래하는 질 환이다.
1)십 만명 당 5명 정도로 발병하며 모든 혈액암 의 약 10% 정도를 차지하는데,
2)새로운 치료법이 도입 되기 이전에는 다발성 골수종 환자의 대부분이 진단 후 5~10년 내에 사망하였지만 고용량 치료에 이은 조혈 모세포이식이나 thalidomide, lenalidomide, borte- zomib과 같은 새로운 약제가 사용되면서, 진단 또는 재발 이후로부터의 median survival time이 50%까 지 증가했다.
3)그 중 이전에 치료경험이 없거나 표준요 법에 실패한 다발성 골수종 환자에서 효과적이며 단독
또는 dexamethasone이나 다른 항암제와 병용되는
4)bortezomib은 세포의 항상성 유지에 필수적인 ubiq- uitin-proteasome pathway를 저해하는 protea- some inhibitor
5)로서 두 가지 치료에 실패한 불응성 다발성 골수종 환자의 치료에 2003년 FDA허가, 한 가 지 이상의 치료를 받은 다발성 골수종 환자 2005년 FDA허가, 이전 치료경험이 없는 다발성 골수종 환자 의 1차 치료로 2008년 FDA허가까지 허가 범위를 넓혀 왔다.
6)하지만 Mateos M.V.의 review 논문에 따르면 재발 또는 불응성(relapsed and/or refractory MM, RRMM), 그리고 새로 진단된 MM(newly diagnosed MM, NDMM)에서 bortezomib을 단독으로 사용한 경 우 나타나는 주된 부작용은 thrombocytopenia, neutropenia, 말초신경병증이었고
3), 669명의 RRMM 에서 고용량 dexamethasone과 bortezomib 단독치 2005 to April 2008. A retrospective chart review was performed on SNUH patients’Electronic Medical Records(EMR), and the SPSS Statistics 19.0 was used for analysis.
In univariate analysis, no correlation was found between the development of PN, sex, or age, but creatinine level (Scr≥2)(48% vs 78%, p=0.007, OR=0.264), presence of DM(50% vs 76%, p=0.034, OR=0.324) and number of therapy cycles(N>3)(84% vs 57%, p=0.002, OR=4.046) were significantly correlated with PN incidence. In a multivariate logistic regression, the risk of borte- zomib-related PN was lower in patients whose creatinine level was high(Scr≥2)(OR=0.248) and greater in patients treated with high number of bortezomib cylces(N>3)(OR=4.235).
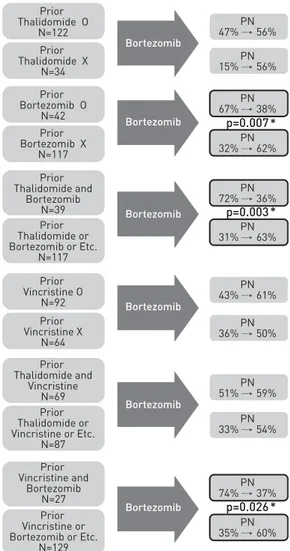
Concerning that the prior exposure to chemotherapy could exacerbate neurotoxicity, there was lower incidence of PN in the prior bortezomib treated group(38% vs 62%, p=0.007), prior borte- zomib with thalidomide treated group(36% vs 63%, p=0.003), and prior bortezomib with vin- cristine treated group(37% vs 60%, p=0.026).
[Key words] Bortezomib, Multiple Myeloma(MM), Peripheral Neuropathy(PN), Risk factor
료를 비교한 phase Ⅲ trial
7)에 의하면 bortezomib 치 료 환자의 75%에서 보고된 grade 3 또는 4 부작용은 thrombocytopenia(30%), neutropenia(14%), 말초 신경병증(8%)였다. 그 외에 전체 환자의 37%에서 치료 초기중단으로까지 연관된 위장관계 장애, 피로감, 고칼 슘혈증, 척수압박 등의 부작용이 각각 2% 정도에서 발 견됐다고 하는데 특히 고위험군과 노인 환자를 대상으 로 한 subgroup analysis 결과 dexamethasone 보다 bortezomib 치료군에서(75% vs 64%), 이전에 1번 이 상의 치료이력이 있는 군에서(75% vs 64%), 그리고 ISS(International Staging System) stage Ⅱ/Ⅲ 질 환에서(46% vs 38%) grade 3 또는 4 부작용 비율이 더 높았다.
8)한편 bortezomib에 의한 말초신경병증 발 생률을 연구한 682명의 환자 대상 randomized phase Ⅲ study
9)에 의하면 MP(melphalan + pred- nisolone) 단독보다는 bortezomib을 병용한 VMP(bortezomib + melphalan + prednisolone)에 서 더 자주 말초신경병증이 나타났고(all grades: 44%
vs 5%) 그 중 74%는 평균 2개월 내에 해결되거나 (56%) 1단계 이상 감소(18%)했다고 한다.
Bortezomib의 대표적인 용량의존적, 비혈액학적 부 작용인 말초신경병증은 치료 기간 중 초반부터 발생할 수 있고 상∙하지의 저린감과 같이 주로 감각효과로 나 타나며, 전격통증이나 경련으로까지 발전 가능하다.
Grade 1과 2의 말초신경병증은 재발 또는 새로 진단된 다발성 골수종에서 각각 75%, 33%, grade 3과 4 말초 신경병증은 각각 30%, 18% 이하에서 발생하는 것으로 보고되었으며
10), 환자의 삶의 질을 떨어뜨리고 용량 감 량, 치료지연 및 조기 중단에까지 이르게 할 가능성이 있다.
2)말초신경병증이 필수적으로 용량의존적인 반응 은 아니지만 Mateos M.V. 등의 전향적 다기관 ran- domized trial에 의하면, 새로 진단된 다발성 골수종 환자를 대상으로 첫 번째 cycle에 1주 2회 투여 후, 이 어지는 5번의 cycle에는 1주 1회로 감량하여 투여함으 로써 grade 3 이상의 말초신경병증 발생률을 5% 정도 감소시켰다는 보고가 있었다.
11)Bortezomib에 의한 말 초신경병증의 증상을 치료하기 위해 진통제, 삼환계 항 우울제, 항경련제 등이 사용되고 있지만, 용량 감량과 regimen 변경보다 더 효과적인 치료방법은 없기 때문 에
10)NCI(National Cancer Institute) CTCAE
(Common Toxicity Criteria for Adverse Events) grade와 말초신경병증 증상의 중증도에 따른 권장 용 법∙용량의 조절이 중요하고, 치료 이전에 신경병증을 악화시킬 수 있는 약물의 조합이나 위험인자를 파악할 필요성이 있다.
12)Corso 등의 연구에서는 bortezomib 에 의한 말초신경병증의 위험인자로 나이를 꼽았으며, 1세 증가 시 6%의 위험도 증가를 보이면서도 thalido- mide 같은 신경독성 약물의 사용 이력과 말초신경병 증의 상관관계는 없다고 보고하였다.
13)유사한 연구로 bortezomib을 투여받은 78명의 환자를 대상으로 한 Badros등의 연구에서는 나이나 thali-domide 사용력 과 말초신경병증 위험도는 관계 없었지만, 약물 투여 전 기저의 말초신경병증이나 당뇨를 가진 환자에서 말 초신경병증 위험도가 높았다는 결과를 보이며 말초신 경병증 grade를 예측할 수 있는 가능성을 언급했다.
4)이처럼 bortezomib에 의한 말초신경병증의 위험인자 에 관한 여러 연구들이 있으나, 아직 대규모 연구가 부 족하며 확실한 결론이 도출되지 않은 실정이다. 이에 본 연구에서는 서울대학교병원에서 bortezomib을 투 여받은 환자를 대상으로 투여 전과 후 말초신경병증의 발생 경향과 말초신경병증 발생에 영향을 미치는 위험 인자를 분석하고 영향을 미칠만한 항암제의 투약력을 평가해 보고자 하였다.
연구방법
1. 연구 대상 및 기간
2005년 5월부터 2008년 4월까지 서울대학교병원에 서 bortezomib을 투여받은 18세 이상의 성인 환자를 대상으로 하였다.
2. 연구방법
환자의 전자의무기록을 이용한 후향적 검토방법을
이용하였으며 bortezomib 투여 전과 후의 말초신경병
증 grade는 NCI CTCAE grade 기준으로 분류되어 전
자의무기록에 기재된 내용을 참고하였고 다음에 제시
된 내용을 조사하여 SPSS ver. 19.0의 카이제곱 검정
과 로지스틱 회귀분석을 이용해 통계처리 하였다.
(1) 대상 환자의 기본 특성 조사
대상 약물이 처방된 환자의 성별, 나이, 초기 ISS stage, 세포 유전적 이상, 질병상태(처음진단/재발), M component(g/dL), 헤모글로빈(g/dL), 혈소판, 기저 말초신경병증 존재 유무, neurotoxic 약물의 투약력, 병존질환, 신기능 이상 유무를 수집하였다.
(2) 대상 약물 투여 전과 후 말초신경병증의 발생 경 향 분석
NCI CTCAE grade에 따라 grade 0에서 4까지 분 류하여 전자의무기록에 기재된 신경병증 grade 값 을 이용하였고 그 외 증상만 기재된 경우 분류기준 에 따라 판단하였다.
(3) 대상 약물의 말초신경병증 발생 위험인자 분석 Bortezomib 투여 후 발생한 말초신경병증 정도와 환자의 성별, 나이, 기저 serum creatinine 수치, 당뇨 유무, bortezomib 투여 횟수 등이 통계적으로 유의한 연관성이 있는지 판단하였다. 그 중 연관 있 는 항목을 선택하여 로지스틱 다변량 분석으로 말초 신경병증 발생의 odds ratio를 구해 말초신경병증 의 발생에 영향을 줄 만한 요인인지 분석하였다.
(4) 대상 약물의 투여 이전, 말초신경병증을 일으키는 항암제의 투약력 평가
신경독성이 있다고 알려진 항암요법의 투약력이나 이들 약품의 조합이 말초신경병증의 중증도와 연관 이 있는 지에 대한 분석을 위해 이전 thalidomide 투여군, vincristine 투여군, bortezomib 투여군, thalidomide+vincristine 투여군, thalidomide +bortezomib 투여군, vincristine+bortezomib 투 여군으로 나누어 각각 그렇지 않은 군에 비한 말초 신경병증 발생률을 분석하였다.
연구결과
1. 대상 환자의 기본 특성
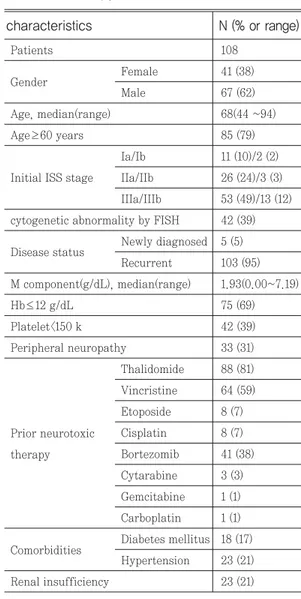
연구 기간 중 서울대학교병원에서 bortezomib을 투 여받은 성인 환자는 Table 1과 같이 108명이고 환자의
성별분포는 남자 67명(62%), 여자 41명(38%)이었고, 평균 연령은 68(44-94)세이었으며 60세 이상 환자는 85명(79%)이었다(Table 1). 다발성 골수종의 치료와 예후를 예측하는 데 쓰이는 ISS(International Staging System) stage는 Ⅰa/Ⅰb 11명(10%)/2명 (2%), Ⅱa/Ⅱb 26명(24%)/3명(3%), Ⅲa/Ⅲb 53명 (49%)/13명(12%)이었고 FISH 결과 cytogenetic abnormality를 보인 환자는 42명(39%)이었다(Table 1). 다발성골수종으로 처음 진단되어 bortezomib을
characteristics N (% or range)
Patients 108
Female 41 (38)
Male 67 (62)
Age, median(range) 68(44 ~94)
Age≥60 years 85 (79)
Ia/Ib 11 (10)/2 (2) IIa/IIb 26 (24)/3 (3) IIIa/IIIb 53 (49)/13 (12) cytogenetic abnormality by FISH 42 (39)
Newly diagnosed 5 (5) Recurrent 103 (95) M component(g/dL), median(range) 1.93(0.00~7.19)
Hb≤12 g/dL 75 (69)
Platelet<150 k 42 (39)
Peripheral neuropathy 33 (31)
Thalidomide 88 (81) Vincristine 64 (59) Etoposide 8 (7) Cisplatin 8 (7) Bortezomib 41 (38) Cytarabine 3 (3) Gemcitabine 1 (1) Carboplatin 1 (1) Diabetes mellitus 18 (17) Hypertension 23 (21)
Renal insufficiency 23 (21)
Gender
Initial ISS stage
Disease status
Prior neurotoxic therapy
Comorbidities
Table 1. Patients characteristics at the start of
bortezomib therapy
Fig. 1 Incidence of PN at baseline and after bortezomib therapy
+ ADL : activities of daily living
투여받은 환자는 5명(5%), 다른 약제 치료 후 재발하 여 투여된 환자는 103명(95%)으로 거의 대부분이었으 며 악성 형질세포에서 생산되는 비정상 면역글로불린 인 혈청 M단백은 평균 1.93 g/dL(0.00-7.19)정도였 고, Hb≤12 g/dL의 환자는 75명(69%), platelet<150
×10³ /μ l의 환자는 42명(39%)이었다(Table 1). 한편 bortezomib 투여 전부터 기저에 말초신경병증이 있었 던 환자는 33명(31%)이고 대부분 신경독성이 있는 항 암제(thalidomide, vincristine, etoposide, cis- platin, bortezomib, cytarabine, gemcitabine, carboplatin 등)의 치료를 받은 이력이 있었으며, 병존
질환으로 당뇨환자는 18명(17%), 고혈압은 23명(21%) 에 해당, 신기능이 완전하지 못한(Scr≥2) 환자는 23 명(21%)이었다(Table 1).
2. 대상 약물의 투여 전과 후 말초신경병증의 발생 경향 분석
NCI CTCAE grade에 따라 분류된 grade에 의하면 bortezomib 투여 전 base line 신경병증 grade는 Gr0 75명, Gr1 30명, Gr2 3명이었고 투여 이후 Gr0 31명, Gr1 28명, Gr2 30명, Gr3 16명, Gr4 3명이었다(Fig.
1).
Neuropathy Grade
(NCI CTCAE) Grade 0: NormalGrade 1: Loss of reflexes or paresthesia (tingling) without pain or less of function Grade 2: Objective sensory loss or paresthesia
(tingling and pain); motor neuropathy indicate symptomatic weakness, interfering with function but not ADL+
Grade 3: Sensory loss paresthesia; motor PN indicates weakness interfering with ADL+
Grade 4: Life-threatening, disabling(e.g. paralysis)
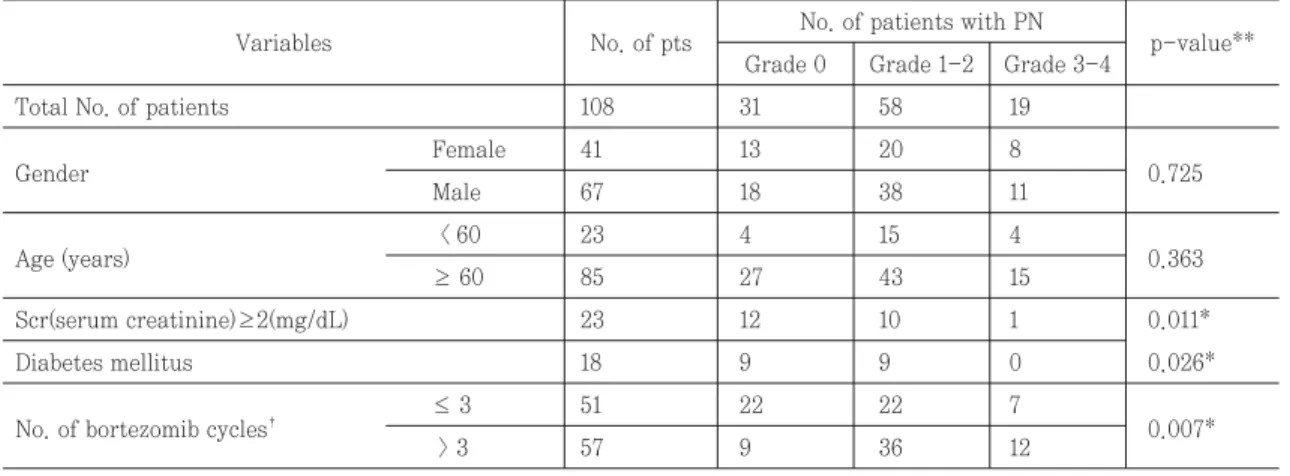
Table 2. Risk factors for developing PN in patients receiving bortezomib
Total No. of patients 108 31 58 19
Gender Female 41 13 20 8
0.725
Male 67 18 38 11
Age (years) < 60 23 4 15 4
0.363
≥ 60 85 27 43 15
Scr(serum creatinine)≥2(mg/dL) 23 12 10 1 0.011*
Diabetes mellitus 18 9 9 0 0.026*
No. of bortezomib cycles�
≤ 3 51 22 22 7
0.007*
> 3 57 9 36 12
p-value**
Grade 3-4 Grade 1-2
Grade 0
No. of patients with PN No. of pts
Variables
*P < 0.05
**chi-squared test
�Ref : A Multicenter Retrospective Analysis of Adverse Events in Korean Patients Using Bortezomib for MM.
Int J Hematol. 2006 May;83(4):309-13.
3. 대상 약물의 말초신경병증 발생 위험인자 분석
Bortezomib 투여 후 발생한 말초신경병증 정도와 위 험인자일 것으로 예상되는 요인과의 연관성을 카이제 곱 검정을 통해 분석한 결과, Table 2와 같이 기저 serum creatinine 수치(Scr≥2)와 bortezomib 투여 횟수(N>3)가 통계적으로 유의한 연관성을 보였고 Table 3의 로지스틱 단변량 분석 결과 당뇨유무도 함께 유의한 결과를 보였다(Table 2, 3). 각각의 신경병증 발 생에 대한 odds ratio는 기저 serum creatinine 수치
(Scr≥2)의 경우 0.264(48% vs 78%, p=0.007), bortezomib 투여 횟수(N>3)에서 4.046(84% vs 57%, p=0.002), 당뇨가 있을 때 0.324(50% vs 76%, p=0.034)이었다(Table 3). 이 세 가지 항목을 선택하여 로지스틱 다변량 분석으로 변수들의 연관성을 보정했 을 때는 Table 4에서 보는 바와 같이 creatinine level 이 높은 경우에는 말초신경병증의 위험도가 낮았고 (OR=0.248), bortezomib cycle(N>3)이 거듭될수록 말초신경병증의 위험도가 높았다(OR=4.235)(Table 4).
p-value***
(univariate) PN
incidence
Odds Ratio (95% CI) Variables
Gender Female 28/41 (68%) Male 49/67 (73%)
1.264 (0.540- 2.961)
0.59
Table 3. Univariate logistic regression analysis of risk factor
Fig. 2 Evaluation of the prior combinations of chemotherapy that could exacerbate neurotoxicity
Age <60 19/23 (83%)≥60 58/85 (68%) 0.452 (0.140- 1.458)
0.184
Scr <2 66/85 (78%)
≥2 11/23 (48%) 0.264 (0.101- 0.692)
0.007*
DM Absent 68/90 (76%) Present 9/18 (50%)
0.324 (0.114- 0.917)
0.034*
No. of cycles�
≤3 29/51 (57%)
>3 48/57 (84%) 4.046 (1.641- 9.973)
0.002*
***logistic regression analysis
p-value***
(multivariate) Odds Ratio
(95% CI) Variables
Scr≥2 0.248 (0.089-0.696) 0.008*
DM present 0.451 (0.148-1.375) 0.161 No. of cycles�>3 4.235 (1.648-10.877) 0.003*
Table 4. Multivariate logistic regression analysis of risk factor
***logistic regression analysis