대한소화기학회지 2008;51:319-322 □ EDITORIAL □
연락처: 김효종, 130-702, 서울시 동대문구 회기동 1번지 경희대학교 의과대학 내과학교실
Tel: (02) 958-8199, Fax: (02) 968-1848 E-mail: hjkim@khmc.or.kr
Correspondence to: Hyo Jong Kim, M.D.
Department of Medicine, Kyunghee University College of Me- dicine, 1, Hoegi-dong, Dongdaemun-gu, Seoul 130-702, Korea Tel: +82-2-958-8199, Fax: +82-2-968-1848
E-mail: hjkim@khmc.or.kr
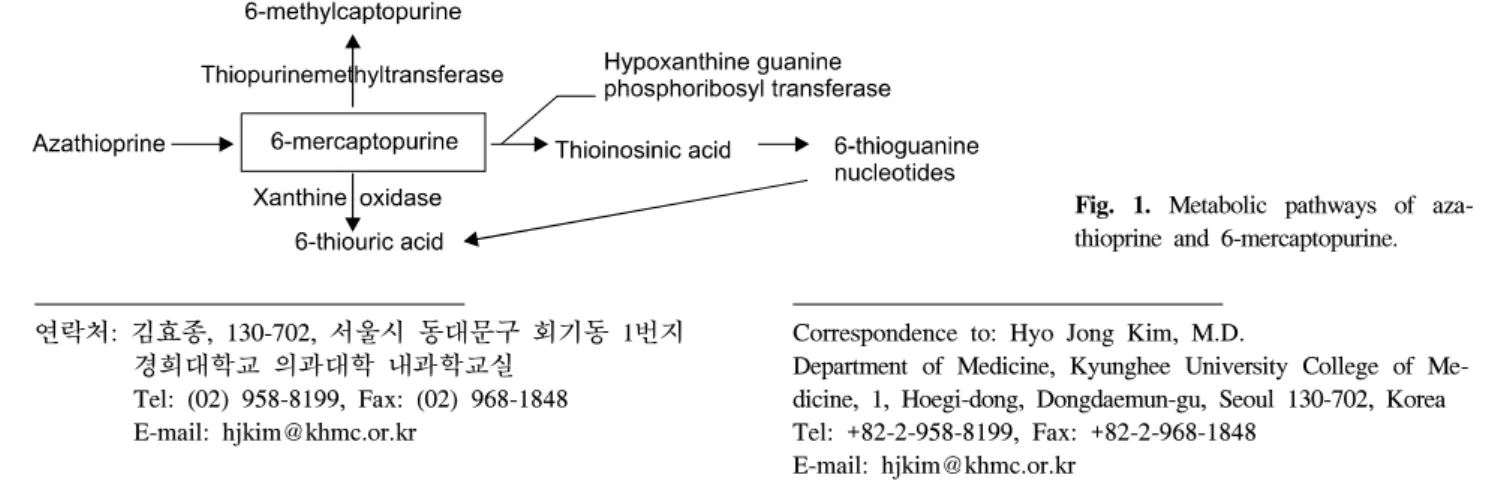
Fig. 1. Metabolic pathways of aza- thioprine and 6-mercaptopurine.
염증성 장질환 환자에서 Azathioprine/6-Mercaptopurine 치료의 부작용: 빈도와 경과
경희대학교 의과대학 내과학교실
차재명ㆍ김효종
The Frequency and the Course of the Adverse Effects of Azathioprine/6-Mercaptopurine Treatment in Patients with
Inflammatory Bowel Disease
Jae Myung Cha, M.D. and Hyo Jong Kim, M.D.
Department of Medicine, Kyunghee University College of Medicine, Seoul, Korea
면역억제제 또는 면역조절제로 분류되는 azathioprine (AZA)/6-mercaptopurine (6MP)은 생체 내에서 핵산 대사를 방해함으로써 세포증식과 면역억제 기능을 나타내는 약물 들로, 최근 전세계적으로 염증성 장질환에 대해 사용이 증 가하고 있다.1,2 면역억제제의 안전성과 지연 효과에 대한 우려 때문에 사용이 제한적이었으나, 최근 들어 효능에 대 한 인식이 제고되고 부작용에 대한 우려가 낮아지면서 사용 이 증가하였다. 경구 투여한 AZA은 장에서 흡수된 후 비효 소 매개 과정을 거쳐 6MP로 변환되며, 6MP는 활동 대사산 물인 6-thioguanine nucleotide (6TGN)로 대사되거나, 다른 경 로를 통해 비활동 대사산물인 6-thiouric acid나 6-methylmer- captopurine (6MMP)으로 대사된다(Fig. 1).1 AZA/6MP의 골수억 제 및 면역억제 효과는 활성 대사산물인 6TGN이 세포의 DNA에 끼어들어 DNA 절단과 림프구 증식 억제를 초래하
기 때문이다.3
일반적으로 AZA/6MP에 의한 부작용의 빈도는 10-39%로 비교적 높은 편이며,4 5-10% 환자들이 부작용 때문에 AZA/
6MP를 사용할 수 없다고 알려져 있다. AZA/6MP 약제의 부 작용은 과민 반응과 비과민 반응의 2가지로 분류할 수 있 다.1 면역학적으로 매개가 되는 과민 반응은 대개 3-4주 이 내에 발생하며 용량 의존적이지 않고, 췌장염, 발열, 발진, 권태감, 오심, 설사, 복통, 간염 등으로 나타난다. 처음에 과 민 반응을 보였던 환자들은 일반적으로 약제를 다시 투여할 경우 훨씬 심하고 빠르게 부작용이 나타나기 때문에 대부분 의 경우 약제를 계속 사용할 수 없고 methotrexate와 같은 다 른 면역조절제로 전환해야 한다.5 비과민 반응은 대개 수개 월에서 수년 후에 발생하며 용량 의존적이라 6TGN의 농도 증가와 관련이 있고, 백혈구감소증, 혈소판감소증, 감염, 악
320 대한소화기학회지: 제51권 제5호, 2008
성종양, 용량 의존 간염 등으로 나타난다.
가장 흔한 용량 의존형 부작용인 골수 억제는 주로 백혈 구감소증으로 나타나며, 2.2-15%의 다양한 빈도로 보고되고 있다.5 대부분의 백혈구감소증은 용량을 줄이거나 약을 끊 을 경우 가역적이지만, 백혈구수가 2,000/mm3 이하로 감소 할 경우에는 감염 합병증이 증가할 수 있고, 스테로이드나 infliximab과 같은 다른 면역억제제를 같이 투여할 경우에는 감염 위험이 더욱 증가할 수 있기 때문에 주의해야 한다.5 골수억제로 혈소판 감소증도 발생할 수 있지만, 용량을 줄 이거나 약을 끊을 경우 가역적이지 않다면 간독성과 같은 다른 합병증을 고려해야 한다. 상당수 환자들에서 경미한 아미노기전이효소(transaminase)의 상승이 관찰되는 데 이는 용량 의존성으로 대부분 용량을 감량하면 호전이 된다.1 보 다 심각한 간독성으로는 결절성재생증식(nodular regenera- tive hyperplasia)이 보고된 바 있는데,6 정확한 기전은 밝혀지 지 않았지만 용량 의존성보다는 특발성일 가능성이 높다.
AZA/6MP의 발암성에 대해서는 논쟁의 여지가 있다.
AZA/6MP 치료 후 악성 림프종이 3% 발생했다는 보고가 있 는 반면,4 Connel 등7은 30년간 치료한 755명의 환자들에서 악성 종양의 위험이 전혀 증가하지 않았다는 상반된 보고를 하였다. 크론병 환자들을 대상으로 한 인구조사에서도 크론 병에 의해 악성 종양의 발생이 약간 증가할 수는 있지만, 그 위험이 면역억제제의 사용에 의해 더 증가하지는 않는다고 보고하였다.8 Mayo Clinic에서는 AZA/6MP로 치료했던 염증 성 장질환 환자들에서 엡스타인바(Epstein-Barr) 바이러스 양 성 림프종의 발생 위험이 약간 증가한다고 보고하였다.9 따 라서, 아직까지는 AZA/6MP의 발암성에 대한 추가 연구가 더 필요하며, 특히 AZA/6MP 대사에 대한 유전 변이가 영향 이 있는지 연구가 필요하다.
임산부에 대한 AZA/6MP의 안전성에 대해서는 연구 자료 가 부족한 편이다. 현재 6MP는 동물실험 결과에 근거하여 미국 식품의약국에서 생명을 위협하는 질환에서만 사용이 가능한 D군 약물로 분류되고 있다. 덴마크의 코호트 연구 결과 임신 도중 AZA/6MP로 치료받았던 산모들에서 선천 기형, 주산기 사망률, 미숙아 출생 등의 위험이 증가한다고 보고하였으나 대상군이 9명으로 매우 작았다.10 6MP를 복용 하던 중 임신이 되었던 155명의 산모들을 대상으로 한 연구 에서 Francella 등11은 임신 전이나 임신 중에 6MP를 복용하 였더라도 대조군에 비해 유산율의 차이가 없어서 임신 중 6MP의 복용이 안전하다고 주장하였다. 따라서, 임신하기 이전에 부작용을 우려하여 AZA/6MP를 중단할 이유가 없으 며 임신 중에도 위험과 효능을 평가한 다음 필요하다면 계 속하여 사용할 것을 권하는 전문가가 많다.12-14 모유 수유를 할 경우 모유에서 AZA이 낮은 농도로 검출되지만, 소아에 서 면역 억제나 발암성에 대한 장기 위험성이 알려져 있지
않기 때문에 수유 중 복용은 금기이다.5
AZA/6MP의 대사 과정 중 작용하는 thiopurine methyltrans- ferase (TPMT)의 유전형과 활성도에 의해 효능과 부작용에 대한 다양한 개인차가 발생할 수 있다.15 TPMT 활성도가 정 상보다 낮을 경우 6TGN 농도가 현저하게 증가할 수 있기 때문에, AZA/6MP의 효능과 부작용에서 TPMT와 6TGN 농 도의 역상관 관계가 매우 중요하다.16 또한, TPMT의 활성도 는 TPMT 대립유전자 다형성과 관련이 있는데, 인구의 약 89%는 정상 또는 높은 TPMT 활성도를 보이는 반면, 11%는 중간 정도, 0.3%는 매우 낮은 TPMT 활성도를 가지고 있
다.17-19 따라서, 치료 전에 TPMT 유전형 또는 활성도를 검사
하면 AZA/6MP로 치료할 때 발생할 수 있는 백혈구감소증 을 피할 수 있어서 이론적으로 안전성을 극대화할 수 있 다.15 실제로, Colombel 등20은 염증성 장질환 환자들 중 27%
가 TPMT 활성도 때문에 골수억제가 나타났다고 보고하였 다. 그러나, TPMT 활성도가 정상인 환자에서도 흔히 부작 용이 나타나고, TPMT 활성도를 측정하기 위해서는 10- 20 mL의 신선혈액이 필요하며 혈액을 보관했다가 나중에 측정 할 수 없을 뿐만 아니라 TPMT 활성도를 측정하는 것이 쉽 지 않기 때문에 일상적인 진료에 이용하기는 어렵다.21 적혈구 6TGN 농도가 너무 높으면 부작용이 증가하고, 반 대로 너무 낮으면 치료 효과를 나타내지 못하기 때문에, 적 혈구 6TGN 농도를 측정하여 AZA/6MP의 치료 효능과 부작 용을 예측할 수 있다.21 6TGN 농도가 235 pmol/8×108 RBC이 하에서는 치료에 대한 반응이 크게 향상되지 않았으며, 6TGN 농도가 235 pmol/8×108 RBC 이하에 비해 235 pmol/
8×108 RBC 이상에서 치료반응이 5배나 더 양호하였다. 뿐 만 아니라, 대사 산물을 측정하여 치료 실패를 정의할 수 있 는데, 저용량 처방이나 부실한 복약(순응도)을 하고 있는 환 자들에서는 6TGN과 6MMP 농도가 모두 낮게 측정된다. 반 면, AZA/6MP 약물 저항성 환자들에서는 6TGN 수치는 낮 고(<235 pmol/8×108 RBC) 6MMP 수치는 증가(>3,000 pmol/8×108 RBC)하며,22 내약성(refractory) 환자들에서는 6TGN 수치가 235 pmol/8×108 RBC 이상으로 높거나 심지어 는 450 pmol/8×108 RBC 이상으로 독성 수준까지 증가하더 라도 치료에는 반응이 없다.4 실제 임상에서 6TGN을 측정 하는 것이 표준 치료는 아니지만, 충분한 용량의 AZA/6MP 를 사용하고도 치료에 실패했던 환자들을 대상으로 대사 산 물을 측정하면, 환자의 복용 순응도, 약물 저항성, 내약성 등에 대한 정보를 얻을 수 있다는 데에는 대부분의 전문가 들이 동의하고 있다.
이번 호에 게재된 김 등의 연구는 염증성 장질환 환자에 서 AZA/6MP 치료에 따른 부작용의 빈도와 그 경과에 대해 조사한 훌륭한 연구이다. 지금까지 염증성 장질환 환자들을 대상으로 한 AZA/6MP의 부작용에 대한 국내 연구는 초록
차재명 외 1인. 염증성 장질환 환자에서 Azathioprine/6-Mercaptopurine 치료의 부작용: 빈도와 경과 321
으로만 보고되어 개략적인 빈도를 아는 데 그치고 있었으
나,23-25 이번 발표에서는 장기간 동안 많은 환자들을 대상으
로 AZA/6MP의 부작용에 대해 연구하였다. 이번 발표에서 김 등은 AZA/6MP의 부작용 빈도는 71%였으며, 부작용으로 치료를 중단한 경우도 29%에 달한다고 보고하였다. 뿐만 아니라, 백혈구감소증 빈도에 대해서도 과거 다른 국내 보
고들23-25의 19-41%에 비해 56%로 훨씬 높은 빈도를 보고하
였다. 따라서, 우리나라 염증성 장질환 환자들에 대한 AZA/
6MP 치료의 부작용 빈도와 경향은 서양 환자들과 상이할 가능성이 있으며, 향후 AZA/6MP의 부작용에 대한 전향 연 구가 필요하다. 이번 발표에서 백혈구감소증은 AZA/6MP 투여 시작 후 3개월 이내에 35% 환자들에서 발생하였으며, 최대 관용 용량 투여 후 3개월 이내에 59%로 가장 많이 발 생했다고 보고했는 데, 이 역시 외국의 보고26에 비해 백혈 구감소증의 발현이 빠른 편이다. 하지만, 백혈구감소증의 중증도는 심하지 않아서 대부분 용량 조절, 투여 중단, 지속 적인 투여 등을 통해 회복이 되었으며, 과립구집락자극인자 를 투여할 정도로 심한 백혈구감소증은 1예에 불과하였다.
이번 발표에서는 TPMT 유전형이나 활성도에 대해서는 언 급이 없었지만, 최근에 김 등25이 우리나라 염증성 장질환 환자들에 대한 TPMT 유전형 및 활성도와 골수기능억제와 상관관계가 없다고 보고하였기 때문에 우리나라 환자들에 서 백혈구감소증의 빈도가 더 높은 이유는 아직 규명되지 않았다. 또 한 가지 흥미로운 점은, 일반적으로 AZA/6MP에 의한 백혈구감소증은 용량 의존적이라고 알려져 있지만, 이 번 발표에서는 AZA을 2.0 mg/kg 이상 투여한 군과 2.0 mg/kg 미만으로 투여한 군 사이의 백혈구감소증의 빈도 차 이를 관찰할 수 없었다. 따라서, AZA 치료 용량에 따른 백 혈구감소증의 발생에 대한 전향 연구가 필요하다. 이번 발 표에서 그 외 부작용들로 오심/구토(24%), 관절통(4.5%), 간 염(4.5%), 피부 발진(3%), 기타(3.1%) 등을 보고했는데, 혈소 판감소증이나 췌장염은 관찰되지 않았고 AZA/6MP 치료로 인한 사망도 없었다.
치료 전에 TPMT 유전형이나 활성도를 측정하기 어렵고 심각한 부작용이 발생할 수 있기 때문에, Nielsen 등27은 AZA을 50 mg/일(0.5-1.5 mg/kg/일)과 같이 저용량으로 시작 하여, 2주 이내에 2.5 mg/kg/일의 용량으로 점차 증량하고, 치료 유지 용량에 도달할 때까지 매주 말초혈액검사와 간기 능검사를 시행한 후 치료 기간 동안에는 매달 또는 격달로 지속적인 모니터링을 하도록 권유하고 있다. 6MP는 AZA 용량의 50% 정도이기 때문에 6MP는 0.25-0.5 mg/kg/일로 시 작하여, 1.0-1.5 mg/kg/일로 증량할 수 있다. 모니터링 도중 백혈구감소증(<3,000/mm3)이 발생하면 약물을 끊거나 감량 하도록 권고하고 있다. 하지만, 국내에서는 부작용의 빈도 가 훨씬 높고 비교적 일찍 나타났었기 때문에 향후 우리나
라 염증성 장질환 환자들을 대상으로 부작용 감시를 위한 적절한 모니터링 지침이 제시되어야 한다.
이번 연구는 후향적으로 진행되었고 부작용이 발생한 후 처치 지침이 치료자 간에 통일되지 않아서 처치에 대한 기 준이 다양하였으며, 각종 검사의 주기가 일정하지 않았고, 그 결과 최저 백혈구 수, 최저 백혈구 도달시간, 백혈구 회 복 기간 등의 범위가 넓게 관찰되었다는 점 등이 제한점이 다. 그렇지만, 이번 발표는 많은 염증성 장질환 환자들을 대 상으로 장기간 AZA/6MP 치료에 따른 부작용의 빈도와 그 경과에 대해 조사한 의미있는 논문으로, 앞으로 염증성 장 질환 환자들에 대한 AZA/6MP의 치료에 대한 국내 연구에 좋은 밑바탕이 될 것이다.
요약하면, 염증성 장질환 환자들에 대한 AZA/6MP의 부 작용이 생각보다 심하지 않기 때문에 이들 약물 사용이 점 차 보편화되고 있지만, 우리나라 염증성 장질환 환자들에서 는 부작용의 빈도가 더 높게 보고되고 있기 때문에 주의 깊 은 약제 사용과 모니터링이 필수이다.
참고문헌
1. Sandborn WJ. Azathioprine: state of the art in inflammatory bowel disease. Scand J Gastroenterol 1998;225(suppl):S92-S99.
2. Fraser AG, Orchard TR, Jewell DP. The efficacy of azathio- prine for the treatment of inflammatory bowel disease: a 30 year review. Gut 2002;50:485-489.
3. Christie NT, Drake S, Meyn RE. 6-Thioguanine induced DNA damage as a determinant of cytotoxicity in cultured hamster ovary cells. Cancer Res 1986;44:3665-3671.
4. Present DH, Meltzer SJ, Krumholz MP, Wolke A, Korelitz BI. 6-Mercaptopurine in the management of inflammatory bowel disease: shot- and long-term toxicity. Ann Intern Med 1989;111:641-649.
5. Dubinsky MC. Azathioprine, 6-mercaptopurine in inflam- matory bowel disease: pharmacology, efficacy, and safety.
Clin Gastroenterol Hepatol 2004;2:731-743.
6. Daniel F, Cadranel JF, Seksik P, et al. Azathioprine induced nodular regenerative hyperplasia in IBD patients. Gastroenter- ol Clin Biol 2005;29:600-603.
7. Connel WR, Kamm MA, Dickson M, Balkwill AM, Ritchie JK, Lennard-Jones JE. Long-term neoplasia risk after azathio- prine treatment in inflammatory bowel disease. Lancet 1994;
343:1249-1252.
8. Bernstein CN, Blanchard JF, Kliewer E, Wajda A. Cancer risk in patients with inflammatory bowel disease: a population based study. Cancer 2001;91:854-862.
9. Dayharsh GA, Loftus EV Jr, Sandborn WJ, et al. Epstein-
322 The Korean Journal of Gastroenterology: Vol. 51, No. 5, 2008
Barr virus positive lymphoma in patients with inflammatory bowel disease treated with azathioprine or 6-mercaptopurine.
Gastroenterology 2002;122:72-77.
10. Norgard B, Pedersen L, Fonager K, Rasmussen SN, Sorensen HT. Azathioprine, mercaptopurine and birth outcome: a pop- ulation-based cohort study. Aliment Pharmacol Ther 2003;17:
827-834.
11. Francella A, Dyan A, Bodian C, Rubin P, Chapman M, Pre- sent DH. The safety of 6-mercaptopurine for childbearing pa- tients with inflammatory bowel disease: a retrospective cohort study. Gastroenterology 2003;124:9-17.
12. Ramsey-Goldman R, Schilling E. Immunosuppressive drug use during pregnancy. Rheum Dis Clin North Am 1997;23:
149-167.
13. Tennenbaum R, Marteau P, Elefant E, et al. Pregnancy out- come in inflammatory bowel diseases. Gastroenterol Clin Biol 1999;23:464-469.
14. Armenti VT, Moritz MJ, Davison JM. Drug safety issue in pregnancy following transplantation and immunosuppression:
effects and outcome. Drug Saf 1998;19:219-232.
15. Black AJ, McLeod HL, Capell HA, et al. Thiopurine methyl- transferase genotype predicts therapy-limiting severe toxicity from azathiopurine. Ann Intern Med 1998;129:716-718.
16. Lennard L, Gibson BE, Nicole T, Lilleyman JS. Congenital thiopurine methyltransferase deficiency and 6-mercaptopurine toxicitiy during treatment for acute lymphoblastic leukemia.
Arch Dis Child 1993;69:577-579.
17. Otterness D, Szumlanski C, Lennard L, et al. Human thio- purine methyltransferase pharmacogenetics: gene sequence polymorphisms. Clin Pharmacol Ther 1997;62:60-73.
18. Park-Hah JO, Klemetsdal B, Lysaa R, Choi KH, Aarbakke J.
Thiopurine methyltransferase activity in a Korean population sample of children. Clin Pharmacol Ther 1996;60:68-74.
19. Jang IJ, Shin SG, Lee KH, et al. Erythrocyte thiopurine
methyltransferase activity in a Korean population. Br J Clin Pharmacol 1996;42:638-641.
20. Colombel JF, Ferrari N, Debuysere H, et al. Genotypic analy- sis of thiopurine S-methyltransferase in patients with Crohn's disease and severe myelosuppression during azathiopurine therapy. Gastroenterology 2000;118:1025-1030.
21. Szumlanski CL, Honchel R, Scott MC, Weinshilboum RM.
Human liver thiopurine methyltransferase pharmacogenetics:
biochemical properties, liver-erythrocyte correlation and pres- ence of isozymes. Pharmacogenetics 1992;2:148-159.
22. Dubinsky MC, Yang H, Hassard PV, et al. 6-MP metabolite profiles provide a biochemical explanation for 6-MP resist- ance in patients with inflammatory bowel disease. Gastroen- terology 2002;122:904-915.
23. Lee HJ, Yang SK, Kim BK, et al. The safety and efficacy of azathioprine/6-mercaptopurine in the treatment of Korean pa- tients with Crohn's disease. Intest Res 2007;5(suppl):63S.
24. Kim JH, Choi CH, Kim TI, et al. Clinical implication of thi- opurine methyltransferase genotyping. Korean J Med 2002;
63(suppl):67S.
25. Kim JH, Cheon JH, Hong SS, et al. Correlation between thio- purine methyltrasferase genetic polymorphism and activity or inosine triphosphate pyrophosphatase genetic polymorphism and myelotoxicity in patients with inflammatory bowel dis- ease during Azathioprine/6-Mercaptopurine treatment. Intest Res 2008;6(suppl 1):73S.
26. Fraser AG, Orchard TR, Jewell DP. The efficacy of azathio- prine for the treatment of inflammatory bowel disease: a 30 year review. Gut 2002;50:485-489.
27. Nielsen OH, Vainer B, Rask-Madsen J. Review article: the treatment of inflammatory bowel disease with 6-mercaptopur- ine or azathioprine. Aliment Pharmacol Ther 2001;15:1699- 1708.