대한소아혈액종양학회지
제 11 권 제 1 호 2004 92
책임저자:국 훈, 광주광역시 동구 학동 8번지 전남대학교병원 소아과, 501-757 Tel: 062-220-6645, Fax: 062-222-6103 E-mail: [email protected]
Defibrotide를 이용한 치료경험
전남대학교 의과대학 1소아과학교실, 충북대학교 의과대학 2소아과학교실
이준선1․국 훈1․노하영1․백희조1․김소연1․손경란1․최익선1․박현진2․황태주1
Defibrotide Treatment for Hepatic Veno-occlusive Disease after Umbilical Cord Blood Transplantation
Jun Sun Yi, M.D.1
, Hoon Kook, M.D.
1, Ha Young Noh, M.D.
1, Hee Jo Baek, M.D.
1 So Youn Kim, M.D.1, Kyoung Ran Sohn, M.D.
1, Ik Sun Choi, M.D.
1, Hyun Jin Park, M.D.
2and Tai Ju Hwang, M.D.
1Department of
1Pediatrics, Chonnam National University Medical School, Gwangju, Department of
2Pediatrics, Choongbook National University Medical School, Cheong-ju, Korea
Veno-occlusive disease (VOD) of the liver is a life-threatening complication occurring early after blood or bone marrow transplantation (BMT). Effective treatment has not been established in case of severe forms of VOD. Defibrotide, a single-stranded polydeoxyribonucleotide, has been used on a compassionate basis in recent clinical trials with promising results. We report here with the first Korean experience of using defibrotide for the treatment of hepatic VOD occurring after unrelated umbilical cord blood transplant in a 2-year-old child with acute lymphoblastic leukemia.
Defibrotide was administered for 23 days without any significant side effects with resolution of signs and symptoms of VOD. (Korean J Pediatr Hematol Oncol 2004;11:92~96)
Key Words: Venoocclussive disease, Umblical cord blood transplantation, Defibrotide
서 론
소아 백혈병의 치료로 동종 골수 및 제대혈 조 혈모세포 이식이 많이 시행되고 있는데
1), 이식과 관련된 중한 합병증 중의 하나로 간정맥폐쇄질환 이 발생할 수 있다. 이는 주로 이식 후 30일 이내 에 발생하는 것으로 급격한 체중 증가, 상복부 통
증, 간비대, 황달을 특징으로 하며 심할 경우 여 러 장기의 기능 부전을 동반할 수 있다
2-4). 이러한 간정맥폐쇄질환은 이식 시 이용된 전처치 및 간 의 상태, 골수 이식의 형태, 유전적 요인과 관계 가 있다고 알려져 있다
5,6).
중증이 아닌 경우는 비교적 예후가 양호하지만
특히 여러 장기의 기능 부전을 동반한 경우에는
최근까지도 효과적인 치료나 예방법이 없는 실정
이다. 그 동안 heparin
7,8), tissue plasminogen activ-
ator (tPA)
9)등의 약물로 일부 환자들에서 성공적
인 치료가 보고되었으나, 중한 출혈이 나타날 수
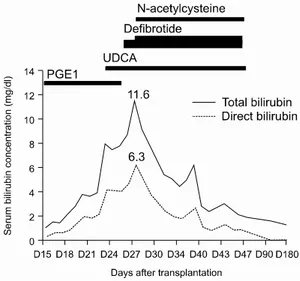
Fig. 1. Bilirubin changes as a manifestation of hepatic veno-occulsive disease after umbilical cord transplantation. Treatment modalities are also illustrated. UDCA, ursodeoxycholic acid.
있어 이중 20~50%는 사망할 수 있다
9). Defibro- tide (DF)는 single-stranded polydeoxyribonucleotide 로 최근에 간정맥폐쇄질환의 치료에 비교적 안전 하며 효과적이라고 알려진 약제이나
10-12), 아직 시 판되지 않아 국내에서는 사용 경험이 없다.
저자들은 재발한 급성림프구성백혈병(ALL)으 로 제대혈 이식을 받은 환아에서 발생한 간정맥 폐쇄질환을 무상으로 공급받은 DF를 이용하여 성 공적으로 치험하였기에 이를 보고하는 바이다.
증 례
환 아: 조OO, 2세, 여아
주 소: 재발된 ALL에서 비혈연간 제대혈 이식 위해
현병력: 8개월 전 쉽게 멍이 들어 내원하였으며 말초혈액검사상 백혈구 수 68,600/mm
3, 골수검사 및 면역표현형 검사에서 precursor B ALL (L1), 로 진단되었다. 세포유전학 검사상 세포가 배양되지 않았으나, BCR-ABL, E2A-PBX1, MLL-AF4에 대한 FISH 및 multiplex RT-PCR은 음성이었고, 뇌척수 액 검사상 중추신경계 침범은 없었다. 환아는 고 위험군으로 관해유도 요법을 시행하여 14일 만에 관해를 성취하였고, 공고요법 및 중추신경예방요 법과 중간 유지요법을 시행하였다. 그러나, 항암 치료 도중 4개월 만에 ALL이 재발하였고, 고용량 ara-C가 포함된 2차례 재관해 요법으로 관해가 되 었다. 환아는 2차관해 상태에서 1개 항원 불일치 제대혈 이식을 위하여 입원하였다.
과거력 및 가족력: 특이사항 없음.
진찰 소견: 입원 당시 몸무게는 12.0 kg이었고, 활력징후는 특이소견 없었다. 진찰소견상 간비종 대는 없었다.
치료 및 경과: 이식을 위한 전처치로 ara-C (3.0 g/m
2/dose, 정주, 12시간 간격 3일간), cyclophosph- amide (45 mg/kg/day, 정주, 2일간), 전신방사선(총 1,200 cGy, 6회 분할)조사를 시행하였다. 이식된 제대혈의 총유핵구수는 5.8×10
7/kg, CD34 양성 세포수는 2.0×10
5/kg이였다. 급성 이식편대숙주반
응의 예방으로 cyclosporine을 사용하였으며, 간정 맥폐쇄질환의 예방목적으로 PGE1 (Eglandin
®)을 1μg/kg/day로 지속 주입하였다.
환아는 이식 후 18일째 갑자기 체중이 급증(13.7 kg, 14%)하며, 상복부 통증과 압통을 호소하였으 며, 간비대를 보여 시행한 검사상 총빌리루빈이 2.2 mg/dL로 증가되었다. 단순흉부 방사선 및 복 부 방사선 사진상 간비대 소견 외 특이 소견 보이 지 않았으며, 간기능 검사, 신기능 검사 또한 특 이 소견 없었다. 제대혈 이식 후 발생한 간정맥폐 쇄질환을 의심하고 PGE1을 증량하며 ursodeoxy- cholic acid (UDCA)를 추가 복용하였으나 총빌리 루빈은 계속 상승하였다. 이식 25일째 총빌리루빈 이 7.9 mg/dL까지 증가하여 DF (Prociclide
®, Gent- ium, Como, Italy)를 사용하기 시작하였다. DF 50 mg을 생리식염수 50 mL에 섞어 2시간에 걸쳐 하 루 4회 주입하였다(15 mg/kg/day). 이때 PGE1의 사용은 중단하였다. 이식 27일째 총빌리루빈이 11.6 mg/dL까지 증가하여 DF 용량을 하루 300 mg (23 mg/kg/day)으로 증량하였으며, N-acetylcysteine
(NAC, 100 mg/kg/day)을 추가로 사용하였다. 이식
28일째부터 점차 체중과 총빌리루빈이 감소하였으 며 간비대, 상복부 통증 및 압통은 호전을 보였다.
이식 34일째 총빌리루빈은 4.4 mg/dL까지 감소 하였다가, 다시 6.3 mg/dL까지 증가하여 DF를 400 mg/day (31 mg/kg/day)까지 증량하였다. 하지 만 당시에 체중 증가 및 간비대 소견은 보이지 않 고 피부 발진과 설사가 증가하여서 급성 이식편 대숙주반응의 치료로 methylprednisolone 1 mg/kg/
day를 병용 투여하였다. 3일 이후 총빌리루빈, 피 부발진, 설사의 호전을 보였다. 이식 47일째 총빌 리루빈이 2 mg/dL 이하로 감소하여 DF, NAC, UDCA 투여를 중단하였다. DF는 총 23일간 투여 되었으며 이와 연관된 부작용은 관찰되지 않았다 (Fig. 1). 이식 후 28일째 중성구 500/mm
3이상, 32 일째 중성구 1,000/mm
3이상 소견을 보였고, 혈소 판은 이식 후 74일째에 20,000/mm
3이상으로 3일 연속 증가하였다.
환아는 이식 후 4개월경부터 거대세포바이러스 에 의한 장염, 폐렴과 포도막염이 발생하여 ganc- iclovir, 정주용 감마글로불린을 사용하였고, 만성 이식편대숙주반응이 발생하여 methylprednisolone, cyclosporine, tacrolimus, thalidomide 등을 사용하였 으나 호전을 보이지 않아 이식 후 276일째 사망 하였다. 사망 당시 골수에서는 재발 소견 없이 공 여자 키메리즘을 유지하고 있었다.
고 찰
이식 후 발생하는 간정맥폐쇄질환은 busulphan, cyclophosphamide, 전신방사선 등을 이용한 전처 치와 관계가 많은 것으로 알려져 있으며
5,6), 동종 골수 이식 후 진단기준의 차이와 보고자에 따라 5~40% 정도에서 발생한다
8,12). 간정맥 폐쇄질환 의 진단기준으로 McDonald 등
2,4)은 이식 후 20일 이내 다음 3개 기준 중 2개를 만족하는 경우로 하 였다: 1) 고빌리루빈혈증 (>2 mg/dL); 2) 간종대 혹은 간성 우상복부 통증; 3) 체액저류에 의한 급 속 체중증가 (>2%). 또한 Jones 등
13)은 이식 후 21일 이내에 간기능 이상으로 고빌리루빈혈증(>
2 mg/dL)과 함께 다음 소견 중 2 가지 이상(복수, 간종대-주로 압통동반, 5% 이상의 체중증가)이 있 으면 진단하였다. 간정맥폐쇄질환의 중증도는 대 부분 후향적으로 평가되며, 임상적으로 명백한 간 정맥폐쇄질환을 보이지만 특별한 치료 없이 호전 을 보이는 경우를 경증, 치료를 요하였으나 완전 히 치료되는 경우를 중등도, 간부전과 관련된 증 상을 보이며 치료를 하였으나 100일 이상 간정맥 폐쇄가 지속되는 경우, 혹은 다장기 부전이 동반 되는 경우를 중증으로 분류하며, 다장기 부전이 동반된 중증 간정맥폐쇄질환의 경우 90% 이상의 높은 사망률을 보인다
4,6,12).
따라서 간정맥폐쇄질환의 발생을 예방하기 위 하여 heparin
7,8), PGE1
14)등이 시도되었으나 유의 한 효과를 보지 못하였고, 진단 당시 중증질환을 예견해보려는 시도가 있었으나 미흡하며
15), 또한 혈전용해제 등의 적극적인 치료를 언제 시작할 것인지에 대한 지침도 부족한 실정이다
8). 간정맥폐쇄질환이 심하게 발생한 경우의 치료 는 매우 어려운데, tPA와 heparin을 사용한 Seattle 연구에서 42명의 성인 환자 중 29%에서만 반응하 였고, 생명을 위협하는 출혈경향이 있었다
9). 또한 Mayo Clinic의 보고에서도 10%의 생존율을 보고하 여 tPA의 치료가 효과적이질 못하였으며
16)더욱이 소아에서 효과적이라는 보고는 전무한 실정이다.
그 외의 약물로 ursodeoxycolic acid을 사용하여 대조군에 비해 간정맥 폐쇄질환의 빈도가 줄었다 는 보고
17)와 NAC가 도움이 될 수 있음을 시사하 였으나
18)더 연구가 필요하다.
DF는 최근에 간정맥폐쇄질환의 치료로서 관심
을 받고있는 제제로 돼지의 조직에서 얻어진 sin-
gle-stranded polydeoxyribonucleotide이다
10). 이는
prostacyclin의 혈관이완과 혈소판 응집억제작용을
증가시키며, tPA의 기능 증가, plasminogen activa-
tor inhibitor 1 (PAI-1)의 감소, tissue factor pathway
inhibitor의 억제 작용을 통한 혈전용해 작용과 항
염증성, 항허혈성 작용을 갖는다. 또한 시험관내
에서 adenosine 수용체 A1과 A2에 친화성이 있어
thrombin 길항작용을 나타내고, 전임상 연구에서
손상된 미세혈관계에를 보호하는 역할을 하는 것 으로 알려져 있다
10,19). 그러나, heparin이나 tPA제 재와는 달리 전신성 출혈성 부작용은 거의 없는 것으로 알려져 있다.
유럽의 최근 무상 연구에서는 40례의 간정맥폐 쇄질환에서 DF 10~40 mg/kg/day를 평균 18일간 사용하여 43%에서 완전 회복을 보였으며, 중증 질환에서도 36%에서 완전 회복을 보고하였다
20). Richardson 등
11)은 다장기 부전을 동반한 중증 간 정맥폐쇄질환을 가진 88명의 환자에서 DF을 5~
60 mg/kg/day를 평균 15일 사용하여 36%의 완전 회복을 보였으며, 이식 후 100일째 35%의 생존율 을 보고하였다. 최근에 다기관 연구에서는 DF로 치료한 45명의 소아 간정맥폐쇄질환 환자에서 76%의 완전회복과 64%의 이식 후 100일 생존율 을 보고하였으며, 중증 질환의 경우에도 50%의 완전회복과 36%의 장기 생존율을 보고하였다
12). 이는 기존의 치료방법에 비해 매우 고무적인 성 적이고, 완전회복을 이루기 위해서는 DF를 빨리 사용하는 것이 가장 중요한 인자라고 하였다
12). 이 환아는 cyclophosphamide와 전신방사선 요법 이 포함된 전처치를 받았으나, 특별한 간정맥폐쇄 질환의 위험인자는 없었다. 이 환아에서 사용되었 던 PGE1 예방요법은 별 도움이 되지 않았었으며, 이식 18일째 McDonald 등의 진단기준에
4)따라 간 정맥폐쇄질환으로 진단하였다. 진단 당시 간기능 은 정상이였으며, 다른 장기들의 기능부전을 의심 할 만한 소견은 없는 경증 간정맥 폐쇄질환으로 생각되어 보존적 처치만을 시행하였으나, 호전을 보이지 않고 중둥도 질환으로 진행하였다. 환아는 골수기능 회복되지 않은 상태로 매일 혈소판을 수혈 받았으며, 경한 장출혈 증상을 동반하여 tPA 와 heparin을 사용할 수 없어 NAC와 DF를 사용하 였다. DF는 총 23일간 투여하였으나 이와 연관된 부작용은 보이지 않았다.
저자들은 제대혈 이식 후 발생한 간정맥폐쇄질 환을 가진 환아에서 무상으로 공급받은 DF를 사 용하여 특별한 부작용 없이 간정맥폐쇄질환을 치 험 하였기에 이를 보고하는 바이다.
참 고 문 헌
1. Cho B. Pediatric allogeneic hematopoietic stem cell transplantation in Korea-April 2000-The Korean Soc- iety of Pediatric Hmeatology-Oncology. J Pediatr Hematol Oncol 2001;8:1-8
2. McDonald GB, Sharma P, Matthews DE, Shulman HM, Thomas ED. Venocclusive disease of the liver after bone marrow transplantation: diagnosis, incide- nce, and predisposing factors. Hepatology 1984;4:
116-22
3. Shulman H, Hinterberger W. Hepatic veno-occlusive disease-liver toxicity syndrome after bone marrow transplantation. Bone Marrow Transplant 1992;10:
197-214
4. McDonald GB, Hinds MS, Fisher LD, Schoch HG, Wolford JL, Banaji M, et al. Veno-occlusive disease of the liver and multiorgan failure after bone marrow transplantation: a cohort study of 355 patients. Ann Intern Med 1993;118:255-67
5. Coppell JA, Brown SA, Perry DJ. Veno-occlusive disease: cytokines, genetics, and haemostasis. Blood Rev 2003;17:63-70
6. Vogelsang GB, Dalal J. Hepatic venoocclusive disease in blood and bone marrow transplantation in children:
incidence, risk factors, and outcome. J Pediatr Hem- atol Oncol 2002;24:706-9
7. Carreras E, Bertz H, Arcese W, Vernant JP, Tomas JF, Hagglund H, et al. Incidence and outcome of hepatic veno-occlusive disease after blood or marrow transplantation: a prospective cohort study of the euro- pean group for blood and marrow transplantation. eu- ropean group for blood and marrow transplantation chronic leukemia working party. Blood 1998;92:
3599-604
8. Reiss U, Cowan M, McMillan A, Horn B. Hepatic venoocclusive disease in blood and bone marrow transplantation in children and young adults: inci- dence, risk, and outcome in a cohort of 241 patients.
J Pediatr Hematol Oncol 2002;24:746-50
9. Bearman SI, Lee JL, Baron AE, McDonald GB. Trea- tment of hepatic venoocclusive disease with recomb- inant human tissue plasminogen activator and heparin in 42 marrow transplant patients. Blood 1997;89:
1501-6
10. Bianchi G, Barone D, Lanzarotti E, Tettamanti R, Porta R, Moltrasio D, et al. Defibrotide, a single-
stranded polydeoxyribonucleotide acting as an adenos- ine receptor agonist. Eur J Pharmacol 1993;238:327-34 11. Richardson PG, Mrakami C, Jin Z, Warren D, Momtaz P, Hoppensteadt D, et al. Multi-institutional use of defibrotide in 88 patients after stem cell transplan- tation with severe veno-occlusive disease and mult- isystem organ failure: response without significant toxicity in a high-risk population and factors pred- ictive of outcome. Blood 2002;100:4337-43
12. Corbacioglu S, Greil J, Peters C, Wulffraat N, Laws HJ, Dilloo D, et al. Defibrotide in the treatment of children with veno-occlusive disease (VOD): a ret- rospective multicentre study demonstrates therapeutic efficacy upon early intervention. Bone Marrow Trans- plant 2004;33:189-95
13. Jones RJ, Lee KSK, Beschorner WE, Vogel VG, Grochow LB, Braine HG, et al. Venoocclusive disease of the liver following bone marrow transplantation.
Transplantation 1987;44:778-83
14. Bearman SI, Shen DD, Hinds MS, Hill HA, McDonald GB. A phase I/II study of prostaglandin E1 for the prevention of hepatic venocclusive disease after bone marrow transplantation. Br J Haematol 1993;84:
724-30
15. Bearman SI, Anderson GL, Mori M, Hinds MS, Shulman HM, McDonald GB. Veno-occlusive disease
of the liver: development of a model for predicting fa- tal outcome after marrow transplantation. J Clin Oncol 1993;11:1729-36
16. Litzow MR, Repoussis PD, Schroeder G, Schembri- Wismayer D, Batts KP, Anderson PM, et al. Veno- occlusive disease of the liver after blood and marrow transplantation: analysis of pre- and post-transplant risk factors associated with severity and results of therapy with tissue plasminogen activator. Leuk Lym- phoma 2002;43:2099-107
17. Essell JH, Schroeder MT, Harman GS, Halvorson R, Lew V, Callander N, et al. Ursodiol prophylaxis aga- inst hepatic complications of allogeneic bone marrow transplantation. A randomized, double-blind, placebo- controlled trial. Ann Intern Med 1998;128:975-81 18. Ringden O, Remberger M, Lehmann S, Hentschke P,
Mattsson J, Klaesson S. N-acetylcysteine for hepatic veno-occlusive disease after allogeneic stem cell trans- plantation. Bone Marrow Transplant 2000;25:993-6 19. Palmer KJ, Goa KL. Defibrotide. A review of its pha-
rmacodynamic and pharmacokinetic properties, and therapeutic use in vascular disorders. Drugs 1993;
45:259-94
20. Chopra R, Eaton JD, Grassi A, Potter M, Shaw B, Salat C, et al. Defibrotide for the treatment of hepatic veno-occlusive disease: results of the European com- passionate-use study. Br J Haematol 2000;111:1122-9