서 론
Mycoplasma pneumoniae에 의해 발생하는 마이코플라스마 폐 렴은 소아청소년의 지역사회 획득 폐렴의 중요한 원인균으로 유행 시기에 높은 발생률을 보인다.1 전 세계적으로 3년에서 7년의 유행 주기를 보이며, 국내에서는 마이코플라스마 폐렴에 대한 메타분석 에서 3년마다 유행하는 것으로 보고되었다.1,2
마이코플라스마 폐렴은 특별한 치료 없이 스스로 호전되기도 하
지만 소아의 경우 괴사성폐렴, 폐쇄성기관지염 등의 심한 합병증을 야기시켜 생명을 위협하는 경우도 발생한다.3,4 치료를 요하는 마이 코플라스마 폐렴의 일차 선택약으로 마크로라이드계 항생제가 사 용되며 입원 기간을 단축시키고 빠른 증상 회복에 도움이 된다.4,5 그러나 마크로라이드계 항생제를 사용함에도 불구하고 발열 및 기침 증상이 지속되고 흉부 엑스선 소견이 악화되는 치료 불응성 마이코플라스마 폐렴에 대한 보고가 많아지고 있으며,3,4,6-8 저자들 역시 치료 불응성 마이코플라즈마 폐렴을 경험하였다. 이는 2000년 Allergy Asthma Respir Dis 6(1):62-67, January 2018 https://doi.org/10.4168/aard.2018.6.1.62 ORIGINAL ARTICLE
Correspondence to: Kunsong Lee https://orcid.org/0000-0001-7318-2296 Department of Pediatrics, Dankook University College of Medicine, 119 Dandae-ro, Dongnam-gu, Cheonan 31116, Korea
Tel: +82-41-550-3968, Fax: +82-41-550-3949, E-mail: pdlks@dankook.ac.kr Received: June 28, 2017 Revised: August 20, 2017 Accepted: August 30, 2017
© 2018 The Korean Academy of Pediatric Allergy and Respiratory Disease The Korean Academy of Asthma, Allergy and Clinical Immunology This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License
소아에서 치료 불응성 마이코플라스마 폐렴의 위험 인자에 대한 임상적 분석
최서열,1 서주희,1 이건송,1 최규태2
단국대학교 의과대학 1소아과학교실, 2진단검사의학과교실
Clinical analysis of risk factors in refractory mycoplasma pneumonia in children
Seo Yeol Choi,1 Ju-Hee Seo,1 Kunsong Lee,1 Qute Choi2
Departments of 1Pediatrics and 2Laboratory Medicine, Dankook University College of Medicine, Cheonan, Korea
Purpose: Refractory Mycoplasma pneumonia (RMP) has been increasing not only in Korea but worldwide. We investigated the inci- dence of M. pneumonia resistant to macrolides and risk factors for RMP.
Methods: From October 2015 to May 2016, 62 pediatric patients who were admitted due to pneumonia diagnosed on the basis of chest x-ray with respiratory symptoms and positive for M. pneumoniae in polymerase chain reaction with no evidence of other bac- terial or viral infections were included. Sequence analysis of the 23S rRNA gene in M. pneumoniae was performed to identify macro- lide resistance. Patients with congenital anomalies, history of pulmonary disease, and unclear information on antibiotic use were ex- cluded.
Results: Mutations in the 23S rRNA gene were detected in 50 of 62 patients (80.6%). Risk factors were analyzed in only 45 patients.
The RMP group consisted of 26 patients (57.8%) who had fever lasting more than 5 days and deteriorating chest x-ray findings. The lactate dehydrogenase (LDH) and C-reactive protein (CRP) levels were significantly higher in the RMP group than in the non-RMP group (LDH: 300± 79 U/L vs. 469± 206 U/L, CRP: 4.9± 4.3 mg/dL vs. 2.5± 1.7 mg/dL; P= 0.04 vs. P= 0.026). In univariate analysis, the RMP group was significantly associated with 23S rRNA gene mutation, lobar pneumonia, and pleural effusion (odds ration [OR]:
10.8, 4.1, 5.3; P= 0.004, P= 0.036, P= 0.046). The presence of macrolide resistance was found to be only a significant risk factor in lo- gistic regression (OR; 8.827; 95% confidence interval, 1.376–56.622; P= 0.022).
Conclusion: Macrolide resistance was a significant risk factor in patients with RMP and identification of macrolide resistance might be helpful in predicting RMP and establishing target therapy for RMP. (Allergy Asthma Respir Dis 2018;6:62-67)
Keywords: Mycoplasma, Refractory, Mutation, Resistant, Child
2017-03-16 https://crossmark-cdn.crossref.org/widget/v2.0/logos/CROSSMARK_Color_square.svg
이후로 마크로라이드계 항생제에 내성을 보이는 M. pneumoniae 의 발생 빈도가 높아지는 것과 연관이 있을 수 있으며 이러한 내성 균주의 발생은 마이코플라즈마 폐렴의 임상 경과에 영향을 줄 수 있다.9 마크로라이드계 항생제에 내성을 보이는 M. pneumoniae에 대한 첫 보고가 2001년에 있은 후 전 세계적으로 증가하고 있고 중 국에서는 M. pneumoniae의 92%가 내성 균주임을 보고하였다.10 국내에서는 2010년과 2011년의 M. pneumoniae의 56.1%에서 마크 로라이드계 항생제에 내성을 보인다고 보고하였으며,10,11 2015년에 는 87.2%에서 내성이 관찰되어 최근에는 대부분의 M. pneumoni- ae에서 마크로라이드계 항생제에 내성을 갖고 있음을 알 수 있다.12 이에 저자들은 마크로라이드계 항생제에 내성을 가진 M. pneu- moniae 빈도와 함께 치료 불응성 마이코플라즈마 폐렴의 임상적 특징 및 위험 인자에 대해 알아보고자 연구를 시행하였다.
대상 및 방법
1. 대상
2015년 10월부터 2016년 5월까지 호흡기 증상과 함께 흉부 엑스 선 사진에서 폐렴 소견이 있어 단국대학교병원에 입원한 18세 이하 의 환자에서 비인두액을 채취하여 중합효소연쇄반응(polymerase chain reaction, PCR)검사에서 M. pneumoniae이 양성이며 이외의 세균이나 바이러스의 중복 감염의 증거가 없었던 62명의 의무기록 을 후향적으로 분석하였다. M. pneumoniae의 마크로라이드 내성 에 대한 검사는 약물 결합 부위인 23S 리보솜 RNA (23S rRNA) 유 전자의 점 돌연변이의 유무를 확인하기 위해 염기 서열 분석을 62명 모두에서 시행하였다. 선천성기형이나 폐질환의 병력, 항생제 사용 의 정보가 불명확한 환아 17명을 제외한 45명에서 치료 불응성에 대한 임상적 특징과 위험 인자 분석을 수행하였다. 이 연구는 의무 기록 수집 및 분석에 대해 단국대학교병원 연구심의위원회(승인번 호: 2017-04-013-001)의 심의를 통과하였다.
2. M. pneumoniae 검출 및 23S rRNA 돌연변이 검사
호흡기 증상과 흉부 엑스선 사진에서 폐렴 소견이 있어 입원한 환아에서 입원 24시간 이내에 8 French 무균 카테터를 점액 추출기 에 연결시킨 후 외비공을 통해 약 5–7 cm 정도 삽입시켜 음압 60–
80 mmHg하에 흡입하여 비인두액을 채취하였다. 채취한 검체는 가능한 빨리 검사실로 의뢰하였다. 지연된 경우는 DNA 추출 전까 지 4°C에 보관하였고, 추출한 DNA는 –70°C에 보관하였다. 비인두 액에서 RNA를 분리하여 cDNA로 재구성한 후 Seeplex Pneumo- Bacter ACE Detection (V3.0) Kit (Seegene, Seoul, Korea)를 사용하 여 PCR을 수행하였다. PCR은 94°C에서 30초, 60°C에서 1.5분, 72°C 에서 1.5분의 과정을 40회 반복하였고, 마지막으로 72°C에서 10분 간 진행하였다. 증폭된 산물은 screen tape system (Lab901, Scottland,
United Kingdom)에 전기 영동하여 키트 내에 포함되어 있는 표지자 와 비교하여 M. pneumoniae의 양성 유무를 확인하였다.
23S rRNA 돌연변이 검사는 23S rRNA 유전자 특이 PCR 검사를 위해 23S rRNA 유전자의 도메인 V 부위를 5´-AACTATAACG- GTCCTAAGGTAGCG-3´ and 5´-GCTCCTACCTATTCTCTA- CATGAT-3´의 시발체 PCR을 시행한 후 Applied Biosystems 8-capillary 3500 system (Forster City, CA, USA) 기기를 이용하여 증폭 산물인 도메인 V 부위를 직접 염기 서열 분석하여 돌연변이 유무를 확인하였다.
3. 마크로라이드계 항생제 치료 불응성에 대한 위험 인자 및 통계 분석
대상 환자 62명 중 마크로라이드계 항생제 복용에 대한 병력이 명확한 45명의 환아를 대상으로 마크로라이드계 항생제 사용 후 5일 이상 발열이 지속되고 흉부 엑스선 소견이 악화되는 환아를 치 료 불응성으로 정의하였다.3 치료 반응성 환자들과 치료 불응성 환 자들에 대한 혈액검사 소견, 연령, 마크로라이드 복용 후 발열 기 간, 입원 기간의 연속변수의 평균값에 대한 분석은 Mann-Whitney U-test 검정을 이용하였고 치료 불응성에 대한 연관 인자들의 범주 형 변수의 단변량 분석은 Pearson의 카이제곱 검정을 이용하였다.
만 7세를 기준으로 학령 전기 소아와 학령기 소아로 구분하여 치료 불응성과 연령과의 연관성 유무를 확인하고자 하였다. 단변량 분 석에서 위험 인자로 확인된 변수를 연령 및 성별과 함께 보정하여 로지스틱 회귀분석을 이용하여 다변량 분석을 시행하였다. 통계프 로그램은 IBM SPSS Statistics ver. 23 (IBM Co., Armonk, NY, USA)을 사용하였고 P값이 0.05 미만인 경우 통계적으로 유의하다 고 판단하였다.
결 과
1. 대상 환자에 대한 분석의 개요
연구에 포함된 총 62명의 환자 중 치료 반응에 대한 분석을 시행 할 수 있었던 남아 25명, 여아 20명에서 치료 불응성 마이코플라즈 마 폐렴(refractory Mycoplasma pneumonia, RMP)군은 26명 (57.8%)이었으며, 치료 반응성 마이코플라즈마 폐렴(nonrefractory Mycoplasma pneumonia, NRMP)군은 19명(42.2%)이었다(Fig. 1).
23S rRNA 유전자의 분석에서 돌연변이가 확인된 경우는 총 62명 의 환자 중 50명(80.6%)이었으며, 50명 모두 2,063번째 염기가 gua- nine으로 치환된 “A2063G” 점 돌연변이로 확인되었다(Fig. 2).
2. RMP와 NRMP 환자군의 임상적 특징
RMP 환자군과 NRMP 환자군의 입원 전 발열 기간과 평균 연령 은 유의한 차이가 없었으며 입원 시 C-반응단백질과(C-reactive
protein), 젖산탈수소효소(lactate dehydrogenase)의 RMP 환자군 의 평균 수치가 각각 4.9±4.3 mg/dL, 469.6±206.2 U/L로 NRMP 환자군의 2.5±1.7 mg/dL, 300.9±79.9 U/L보다 유의하게 높았다 (P = 0.04, P = 0.026) (Table 1). 마크로라이드계 항생제 치료 시작 후 평균 발열의 지속 기간은 RMP군에서 6.0±1.9일로 NRMP군 의 1.8±0.9일보다 유의하게 길었다(P<0.001) (Table 1).
3. RMP 환자군의 위험 인자 분석
RMP 환자군의 위험 인자에 대한 단변량 분석에서 23S rRNA의 돌연변이가 있을 경우(odds ratio [OR], 10.80; 95% confidence in- terval [CI], 1.97–59.15), 입원 시 흉부 엑스선 검사에서 흉막 삼출액 이 있는 경우(OR, 5.31; 95% CI, 1.01–28.07), 대엽성 폐렴인 경우 (OR, 4.09; 95% CI, 1.16–14.43)가 각각 위험 인자로 확인되었다(Ta- ble 2). 환자의 성별 및 연령 등을 보정하고 단변량 분석에서 위험 인 자로 확인된 변수들을 포함하여 다변량 분석을 시행한 결과 23S rRNA 유전자 돌연변이가 있는 경우에만 유의한 RMP의 위험 인자
로 확인되었다(OR, 8.83; 95% CI, 1.38–56.62) (Table 2).
고 찰
M. pneumoniae에 의한 폐렴은 자연적으로 호전이 되지만 치료 에 반응하지 않는 불응성의 경우는 급성호흡곤란증후군, 괴사성 폐렴, 전격성폐렴 등의 생명을 위협하는 질환으로 발전될 수 있다.7 최근 심한 증상을 일으키는 치료 불응성 마이코플라즈마 폐렴의 예가 세계적으로 보고되고 있으며,7,8,13 아직 기전에 대해서는 명확 하게 밝혀진 바 없으나 일부 연구자들은 마크로라이드계 항생제에 내성을 보이는 M. pneumoniae의 증가와 연관이 있을 것으로 생각 하고 있다.7 그러나 이러한 가설은 마크로라이드 항생제에 내성을 Table 2. Analysis of risk factors on refractory mycoplasma pneumonia patients
Variable RMP
(n= 26) Unadjusted OR
(95% CI) Adjusted OR (95% CI) P-value Male sex 14 (53.8) 1.18 (0.36–3.89) 0.86 (0.19–3.90) 0.862 Age ≥ 7 yr 8 (30.8) 0.49 (0.15–1.68) 0.44 (0.09–2.06) 0.295 Mutation* 24 (92.3) 10.80 (1.97–59.15) 8.83 (1.38–56.62) 0.022 Lobar pneumonia 17 (65.4) 4.09 (1.16–14.43) 3.14 (0.57–17.38) 0.190 Pleural effusion 10 (38.5) 5.31 (1.01–28.07) 1.77 (0.19–16.88) 0.620 RMP, refractory Mycoplasma pneumoniae pneumonia; OR, odds ratio; Cl, confidence interval.
*23S rRNA gene mutation, A2063G.
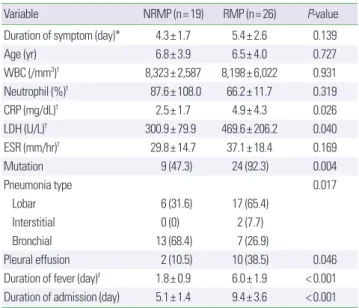
Table 1. The difference of clinical characteristics between NRMP and RMP pa- tients
Variable NRMP (n= 19) RMP (n= 26) P-value
Duration of symptom (day)* 4.3± 1.7 5.4± 2.6 0.139
Age (yr) 6.8± 3.9 6.5± 4.0 0.727
WBC (/mm3)† 8,323± 2,587 8,198± 6,022 0.931
Neutrophil (%)† 87.6± 108.0 66.2± 11.7 0.319
CRP (mg/dL)† 2.5± 1.7 4.9± 4.3 0.026
LDH (U/L)† 300.9± 79.9 469.6± 206.2 0.040
ESR (mm/hr)† 29.8± 14.7 37.1± 18.4 0.169
Mutation 9 (47.3) 24 (92.3) 0.004
Pneumonia type 0.017
Lobar 6 (31.6) 17 (65.4)
Interstitial 0 (0) 2 (7.7)
Bronchial 13 (68.4) 7 (26.9)
Pleural effusion 2 (10.5) 10 (38.5) 0.046
Duration of fever (day)‡ 1.8± 0.9 6.0± 1.9 < 0.001 Duration of admission (day) 5.1± 1.4 9.4± 3.6 < 0.001 Values are presented as mean± standard deviation or number (%).
NRMP, nonrefractory Mycoplasma pneumoniae pneumonia; RMP, refractory Myco- plasma pneumoniae pneumonia; WBC, white blood cell; CRP, C-reactive protein;
LDH, lactate dehydrogenase; ESR, erythrocyte sedimentation rate.
*Duration of symptom (fever) before admission. †Initial laboratory results at admis- sion day. ‡Duration of fever after starting medication.
Fig. 2. Electropherogram shows the point mutation A2063G in domain V of 23S rRNA.
Fig. 1. The schematic outline of study. PCR, polymerase chain reaction.
Mycoplasma PCR (+), x-ray (+), symptoms (+), and other infections (–) Total = 62 (50, 80.6%): 23S rRNA mutation, A2063G)
Nonrefractory: 19 Refractory: 26 (57.8%) Boys: 25, Girls: 20: Analysis of risk factors Underlying disease: 5
Uncertain history of medication: 12
보이는 M. pneumoniae의 비율이 83%에서 95%에 이르는 중국에 서는 치료 불응성을 보이는 것과 항생제 내성을 갖고 있는 것과의 직접적인 연관성을 찾기에는 어려운 점이 있다.7 그래서 저자들은 항생제 내성을 갖는 것이 치료 불응성의 가장 중요한 요인이라는 점을 확인하고자 이번 연구를 수행하였다. 치료 불응성을 보이는 경우 여러 연구들에서 보이는 공통점들은 흉부 엑스선 소견이 심 하고 사이토카인들의 수치가 높음을 볼 수 있어7,8,14 미생물의 직접 적인 영향과 이에 대한 숙주의 심한 면역반응이 치료 반응에 기인 한다고 생각하고 있다.7
마크로라이드계 항생제에 내성을 갖는 M. pneumoniae 내성균 에 대한 보고는 2000년 이후 세계적으로 보고되고 있으며 국가마 다 발생률에는 차이를 보이고 있다.9,10,15 내성을 갖는 기전은 약물 의 결합 부위인 23S rRNA 유전자의 domain II, V에 점 돌연변이가 발생하면 마크로라이드가 리보솜에 결합하는 능력이 감소하면서 내성을 나타내게 된다.9 점 돌연변이 중 A2063G과 A2064G의 변이 가 가장 흔한 것으로 알려져 있으며 14와 15원 고리를 갖는 마크로 라이드 계열의 항생제에서는 최대항생제억제 농도가 >32 mg/L인 고도 내성을 갖는다.9,16 국내의 마크로라이드 항생제에 내성을 가 지는 마이코플라즈마 폐렴 발생률은 Kim 등17의 연구에서 2000년 에서 2003년 동안은 1.6%였으나 Hong 등11은 2011년에는 62.9%까 지 증가한 것으로 보고하였다. 최근 Kim 등17의 연구에 따르면 2015년 유행 시에는 87.2%로 보고되어 마크로라이드계 항생제에 내성을 갖는 M. pneumoniae에 의한 마이코플라즈마 폐렴의 대부분을 차 지함을 알 수 있으며 이 연구에서의 80%의 비율에 비해 다소 높게 확인되었다. 이는 지역적 특성에 의한 차이보다는 환자의 특성이 기관별로 다르기 때문이라고 생각한다. 이번 연구에서는 2015년에 서 2016년 전반기에 확인된 마크로라이드 항생제 내성을 갖는 마 이코플라즈마 폐렴 발생률은 80%로 확인되었으며 이를 통해 동아 시아에 위치한 다른 국가인 일본 및 중국에서 보고된 90%의 내성 률에 근접하였음을 알 수 있었다.
마크로라이드 항생제 내성을 가진 M. pneumoniae와 임상적 상 관성에 대한 부분에 대해 지금까지 연구된 결과들에 따르면, 마크 로라이드 내성 유무에 따라 명확하게 구분될 수 있는 임상적 특징 차이는 없다. 여러 연구에서 마크로라이드 항생제 내성을 보이는 경우 발열 기간과 입원 기간이 감수성을 보이는 경우보다 더 길다 고 보고하였고,9 Kawai 등6은 기관 분비물에 더 많은 M. pneumoni- ae가 확인됨을 보고하였다. 이번 연구에서도 치료 시작 후 평균 발 열 기간은 6.0±1.9일로 내성을 보이지 않았던 환자들의 1.8±0.9 일에 비하여 유의하게 길었음을 확인할 수 있었다. Wang 등7은 마 크로라이드 항생제 내성보다는 감염된 인체의 세포 매개성 면역반 응에 의한 과도한 사이토카인 및 호중구 등의 침입이 치료 불응성 마이코플라즈마 폐렴 발생과 연관성이 크다고 주장하였다. 그러나 이러한 염증반응은 M. pneumoniae의 존재하에 인체의 면역반응
에 의하여 생성되므로 항생제에 내성을 보이는 경우 M. pneu- moniae의 개체 수는 감소하지 않고 유지되므로 사이토카인의 증 가 및 호중구의 과도한 침입 등의 근본 원인은 마크로라이드계 항 생제에 내성을 보이는 것이라고 할 수 있겠다. 앞으로 마크로라이 드계 항생제에 내성을 가진 M. pneumoniae와 감수성이 있는 M.
pneumoniae균에 감염된 경우 사이토카인 농도에 대한 비교 연구 와 함께 항생제 내성의 유무를 같이 분석한다면 치료 불응성에 대 한 보다 정확한 연관성 분석이 가능할 것으로 생각한다.
이번 연구는 체내 사이토카인 및 M. pneumoniae의 폐포 내의 농도 등은 실제로 측정하지 않았으나 초기 흉부 엑스선 소견 및 염 증 표지자 등에 대한 인자들과 마크로라이드계 항생제에 내성을 갖는 부분을 함께 분석하여 치료 불응성 마이코플라즈마 폐렴의 위험 인자에 대한 회귀분석을 시행하여 치료 불응성과 가장 연관 성 있는 위험 인자로 마크로라이드계 항생제에 내성을 갖는 것임 을 확인한 것에 의의가 있다.
최근 치료 불응성을 보이는 마이코플라즈마 폐렴의 증가와 함께 치료 방법에 대한 고민도 증가하고 있다. 우리 기관에서는 마이코 플라즈마 폐렴이 의심되어 입원한 환자는 입원 당일 비인두액을 채 취하여 PCR 검사를 시행 후 roxithromycin을 경구로 투여하고 5일 이후에도 발열이 지속되고 흉부 엑스선 소견이 악화되는 환자는 azithromycin으로 변경하여 경구 혹은 경구로 복용이 힘든 경우 는 정맥으로 투여하였다. 치료 시작 후 일주일 이후에도 지속적인 발열과 함께 흉부 엑스선 소견이 호전되지 않는 환자의 경우는 메 틸프레드니솔론 3 mg/kg/day를 3일 동안 투여하였다. 항생제 치료 기간은 azithromycin 총 5일, roxithromycin은 총 10일을 사용하였 다. 이번 연구에서는 치료 불응성 마이코플라즈마 폐렴의 경우 92%에서 마크로라이드계 항생제에 내성을 갖고 있는 것으로 분석 되어 치료 불응성을 보이는 경우 임상 경과의 호전과 M. pneumoni- ae의 개체 수 감소를 위해서는 비록 마크로라이드계 항생제에 대 한 최저억제농도 및 감수성 검사를 시행하지 못하였으나 기존 항생 제를 계속 유지하기보다는 다른 약제로의 변경 및 염증 소견을 감 소시키기 위한 스테로이드 치료를 고려해 보아야 할 것으로 생각한 다. 이번 연구에서 스테로이드는 임상적 분석이 가능하였던 45명 중 7명(15.5%)에게 투여되었으며 이들 중 6명이 마크로라이드계 항 생제에 내성을 갖고 있었다. 7명 모두 투여 중 특이 부작용 등은 나 타나지 않았으며 이들 중 5명은 투여 후 3일 이내 발열과 흉부 엑스 선 소견의 호전이 관찰되었다. 그러나 마크로라이드 항생제에 내성 을 보이는 M. pneumoniae에 의한 폐렴 치료에 대해 현재까지 확립 된 원칙은 없으며 각 기관의 경험을 토대로 치료가 이루어지고 있 는 실정이다.18 Morozumi 등19의 연구에 따르면 마크로라이드 항생 제 내성을 보이는 경우 clarithromycin과 azithromycin은 bacterio- cidal의 효과는 없었으며 minocycline과 doxycycline이 tosufloxa- cin보다 항생제 투여 후 효과가 좋은 것으로 보고하였다. 그러나
minocycline과 doxycycline은 8세 미만의 소아에서 사용하기에는 한계가 있어 마크로라이드계 항생제에 내성이 있으면서 약물 투여 후에도 지속적인 발열과 영상 소견이 악화되는 소아에게 현재까지 가장 많이 사용되고 있는 약물은 스테로이드이며 증상 호전의 경 험에 대한 문헌들이 보고되었으나 정확한 치료적 원칙은 아직 없는
실정이다.4,13,20 그러나 다행인 부분은 현재까지 다른 문헌들의 보고
와 이번 연구를 통해 마크로라이드계 항생제에 내성을 갖는 M.
pneumoniae에 의한 폐렴에 의해 사망한 경우가 없거나 드물어 내 성을 가지고 있지 않는 M. pneumoniae에 의한 폐렴에 의한 사망률 과의 차이가 없다는 것을 확인할 수 있었다.13,17,20 이번 연구에서는 62명의 환자 중 사망한 경우는 없었으며 마크로라이드계 항생제에 내성을 가진 M. pneumoniae에 의한 폐렴 환자 중 한 명의 4세 남 아에서 치료 종료 후 지속적인 폐기종이 관찰된 예가 있었다. 그러 나 그 이외의 환자들은 발열과 입원 기간이 길었지만 다른 합병증 없이 회복된 점으로 보아 마크로라이드계 항생제 내성을 가지고 있는 M. pneumoniae에 의한 폐렴도 다행히 증상 호전이 된다는 점은 이번 연구에서도 확인할 수 있었다.
이 연구는 후향적 연구로 마크로라이드계 항생제에 내성을 가지 고 있는 군에서 각각의 항생제 치료 효과에 대해서는 정확한 언급 을 할 수가 없다는 것과 단일기관의 연구로 대상 환자의 수가 적다 는 것 그리고 마크로라이드 항생제 투여 후 치료 불응성에 대한 정 의를 다른 연구들을 참고하여 5일로 정한 부분, M. pneumoniae에 대해 항생제 감수성 검사를 시행하지 못한 점 등이 한계점이라고 할 수 있겠다. 마이코플라즈마 폐렴의 치료 불응성에 대한 기준은 현재 명확하게 제시되지 않고 있어 이 연구에서는 기존에 보고된 논문들을 참고하여 5일로 정하였으나 일부 연구에서는 7일을 기준 으로 한 경우도 있다. 그러나 일반적으로 항생제 투여 후 3일이 지 났음에도 증상의 호전과 검사 소견의 호전이 없다면 치료 반응이 없다고 할 수 있기에 5일로 정하고 분석한 부분은 큰 오류를 범한 것으로 생각하지 않는다.
이번 연구를 통해 저자들은 2015년부터 2016년도에 발병한 국내 M. pneumoniae의 마크로라이드계 항생제의 내성 빈도를 알 수 있 었고 내성을 갖는 경우 NRMP 환자에서도 관찰되는 경우가 적지 않았지만 마크로라이드 항생제 치료 5일 이후에도 증상 호전이 되 지 않는 RMP의 가장 유의한 위험 인자임을 알 수 있어 M. pneu- moniae에 의한 폐렴의 진단과 함께 마크로라이드 항생제에 대한 내성 유무를 검사함으로써 다른 항생제로의 변경 및 적합한 치료 를 결정하는 데 올바른 근거가 될 수 있을 것으로 생각한다.
앞으로 다기관이 함께 전향적으로 연구를 시행하여 국내 소아의 치료 불응성 마이코플라즈마 폐렴 치료의 명확한 기준 마련이 필 요할 것으로 생각한다.
REFERENCES
1. Kim EK, Youn YS, Rhim JW, Shin MS, Kang JH, Lee KY. Epidemiological comparison of three Mycoplasma pneumoniae pneumonia epidemics in a single hospital over 10 years. Korean J Pediatr 2015;58:172-7.
2. Kim JW, Seo HK, Yoo EG, Park SJ, Yoon SH, Jung HY, et al. Mycoplasma pneumoniae pneumonia in Korean children, from 1979 to 2006: a meta- analysis. Korean J Pediatr 2009;52:315-23.
3. Shin JE, Cheon BR, Shim JW, Kim DS, Jung HL, Park MS, et al. Increased risk of refractory Mycoplasma pneumoniae pneumonia in children with atopic sensitization and asthma. Korean J Pediatr 2014;57:271-7.
4. You SY, Jwa HJ, Yang EA, Kil HR, Lee JH. Effects of methylprednisolone pulse therapy on refractory Mycoplasma pneumoniae pneumonia in children. Allergy Asthma Immunol Res 2014;6:22-6.
5. Shah SS, Test M, Sheffler-Collins S, Weiss AK, Hall M. Macrolide therapy and outcomes in a multicenter cohort of children hospitalized with My- coplasma pneumoniae pneumonia. J Hosp Med 2012;7:311-7.
6. Kawai Y, Miyashita N, Yamaguchi T, Saitoh A, Kondoh E, Fujimoto H, et al. Clinical efficacy of macrolide antibiotics against genetically deter- mined macrolide-resistant Mycoplasma pneumoniae pneumonia in pae- diatric patients. Respirology 2012;17:354-62.
7. Wang M, Wang Y, Yan Y, Zhu C, Huang L, Shao X, et al. Clinical and lab- oratory profiles of refractory Mycoplasma pneumoniae pneumonia in children. Int J Infect Dis 2014;29:18-23.
8. Zhang Y, Zhou Y, Li S, Yang D, Wu X, Chen Z. The clinical characteristics and predictors of refractory Mycoplasma pneumoniae pneumonia in children. PLoS One 2016;11:e0156465.
9. Principi N, Esposito S. Macrolide-resistant Mycoplasma pneumoniae: its role in respiratory infection. J Antimicrob Chemother 2013;68:506-11.
10. Xin D, Mi Z, Han X, Qin L, Li J, Wei T, et al. Molecular mechanisms of macrolide resistance in clinical isolates of Mycoplasma pneumoniae from China. Antimicrob Agents Chemother 2009;53:2158-9.
11. Hong KB, Choi EH, Lee HJ, Lee SY, Cho EY, Choi JH, et al. Macrolide re- sistance of Mycoplasma pneumoniae, South Korea, 2000-2011. Emerg Infect Dis 2013;19:1281-4.
12. Lee E, Cho HJ, Hong SJ, Lee J, Sung H, Yu J. Prevalence and clinical man- ifestations of macrolide resistant Mycoplasma pneumoniae pneumonia in Korean children. Korean J Pediatr 2017;60:151-7.
13. Cheong KN, Chiu SS, Chan BW, To KK, Chan EL, Ho PL. Severe macro- lide-resistant Mycoplasma pneumoniae pneumonia associated with macrolide failure. J Microbiol Immunol Infect 2016;49:127-30.
14. Lu A, Wang C, Zhang X, Wang L, Qian L. Lactate dehydrogenase as a biomarker for prediction of refractory Mycoplasma pneumoniae pneu- monia in children. Respir Care 2015;60:1469-75.
15. Matsuoka M, Narita M, Okazaki N, Ohya H, Yamazaki T, Ouchi K, et al.
Characterization and molecular analysis of macrolide-resistant Myco- plasma pneumoniae clinical isolates obtained in Japan. Antimicrob Agents Chemother 2004;48:4624-30.
16. Oh CE, Choi EH, Lee HJ. Detection of genetic mutations associated with macrolide resistance of Mycoplasma pneumoniae. Korean J Pediatr 2010;
53:178-83.
17. Kim JH, Kim JY, Yoo CH, Seo WH, Yoo Y, Song DJ, et al. Macrolide resis- tance and its impacts on M. peumoniae pneumonia in children: compar- ison of two recent epidemics in Korea. Allergy Asthma Immunol Res 2017;9:340-6.
18. Yu J. Clinical issues regarding increased macrolide-resistant Mycoplasma pneumoniae in children. Allergy Asthma Respir Dis 2017;5:1-2.
19. Morozumi M, Okada T, Tajima T, Ubukata K, Iwata S. Killing kinetics of
minocycline, doxycycline and tosufloxacin against macrolide-resistant Mycoplasma pneumoniae. Int J Antimicrob Agents 2017;50:255-7.
20. Shan LS, Liu X, Kang XY, Wang F, Han XH, Shang YX. Effects of methyl-
prednisolone or immunoglobulin when added to standard treatment with intravenous azithromycin for refractory Mycoplasma pneumoniae pneumonia in children. World J Pediatr 2017;13:321-7.