의
의
의학
학
학 석
석
석사
사
사학
학
학위
위
위 논
논
논문
문
문
다
다
다계
계
계통
통
통위
위
위축
축증
축
증
증 환
환
환자
자
자에
에
에서
서
서
중
중
중배
배
배엽
엽
엽 줄
줄
줄기
기
기세
세포
세
포
포 치
치
치료
료
료의
의
의 적
적
적용
용
용
아
아
아 주
주
주 대
대
대 학
학
학 교
교
교 대
대
대 학
학
학 원
원
원
의
의
의 학
학
학 과
과
과
김
김
김 지
지
지 원
원
원
다
다
다계
계
계통
통
통위
위
위축
축증
축
증
증 환
환
환자
자
자에
에
에서
서
서
중
중
중배
배
배엽
엽
엽 줄
줄
줄기
기
기세
세포
세
포
포 치
치
치료
료
료의
의
의 적
적
적용
용
용
지
지
지도
도
도교
교
교수
수
수 이
이
이 필
필
필 휴
휴
휴
이
이
이 논
논
논문
문
문을
을
을 의
의학
의
학
학 석
석
석사
사
사학
학
학위
위
위 논
논
논문
문
문으
으
으로
로 제
로
제
제출
출
출함
함
함.
.
.
2
2
20
0
00
0
07
7
7년
년
년 2
2
2월
월
월
아
아
아 주
주
주 대
대
대 학
학
학 교
교
교 대
대
대 학
학
학 원
원
원
의
의
의 학
학
학 과
과
과
김
김
김 지
지
지 원
원
원
김
김
김지
지
지원
원
원의
의 의
의
의
의학
학
학 석
석
석사
사
사학
학
학위
위
위 논
논
논문
문
문을
을 인
을
인
인준
준
준함
함
함.
.
.
심
심
심사
사
사위
위
위원
원
원장
장
장
허
허
허
균
균
균
인
인
인
심
심
심 사
사
사 위
위
위 원
원
원
주
주
주 인
인
인 수
수
수
인
인
인
심
심
심 사
사
사 위
위
위 원
원
원
이
이
이 필
필
필 휴
휴
휴
인
인
인
아
아
아 주
주
주 대
대
대 학
학
학 교
교
교 대
대
대 학
학
학 원
원
원
2
2
20
0
00
0
06
6
6년
년
년 1
1
12
2
2월
월
월 2
2
22
2
2일
일
일
i - 국문요약 -
다계통위축증
다계통위축증
다계통위축증
다계통위축증 환자에서
환자에서
환자에서
환자에서 중배엽
중배엽
중배엽 줄기세포
중배엽
줄기세포
줄기세포
줄기세포 치료의
치료의
치료의 적용
치료의
적용
적용
적용
다계통위축증(multiple system atrophy, MSA)은 진행이 매우 빠르고
약물이나 다른 대증적인 치료에 반응이 없는 질환이기 때문에, 소실된 신경세포를 재생시키거나 대체할 수 있는 치료가 필요하다. 본 저자는 다계통위축증 환자를 대상으로 중배엽 줄기세포 (mesenchymal stem cell,
MSC) 치료를 시행하였으며 그 안정성과 효과에 대해서 분석하였다.
대상은 MSC 치료군 (n=11)과 대조군 (n=18)으로 나누어 시행하였다. 치료는 총 4회(동맥 1회, 정맥 3회) 에 걸쳐 시행되었으며 12개월 동안
2개월 간격으로 the unified multiple system atrophy rating scale (UMSARS)를
시행하였다. MSC군은 대조군과 비교하여 12개월간의 기간 동안 UMSARS 점수의 현저한 호전소견을 보였으며 특히, 자율신경계 이상과 운동실조증 등의 항목에서 호전이 있는 것으로 분석되었다. 또 세포 치료 후 시행한 뇌 FDG-PET 검사를 치료 전에 시행한 검사와 비교한 결과 소뇌와 백질 부위에서 당질대사의 증가 소견을 보였다. 이외 치료 시행 중과 관찰 기간 중에 특별한 합병증이나 부작용은 관찰되지 않았다.
ii 본 연구에서는 중배엽 줄기세포치료를 시행한 환자군에서 신경학적, 기능적인 측면에서 그 진행 속도가 늦어지는 유의한 결과를 보여주었다. 따라서 본 저자는 중배엽 줄기세포치료를 MSA환자에서 치료 방법으로 제시하는 바이다. 핵심어 핵심어 핵심어
iii
차
차
차
차 례
례
례
례
국문요약 ··· i 차례 ··· iii 그림차례 ··· iv 표 차례 ··· vi . Ⅰ 서론 ··· 1 . Ⅱ 연구대상 및 방법 ··· 4 A. 환자선정 ··· 4 B. 자료수집 ··· 5 C. 골수채취 및 중배엽세포 추출과 세포 배양 ··· 5 D. 세포 주입을 위한 준비 ··· 6 E. FDG-PET CT ··· 7 F. 합병증의 확인 ··· 8 G. 통계 분석 ··· 9 . Ⅲ 결과 ··· 10 A. 인구통계학적인 특성 ··· 10 B. UMSARS 비교 ··· 12 C. PET data ··· 15 D. 합병증의 종류와 빈도 ··· 17iv .
Ⅳ 고찰 ··· 19 참고문헌 ··· 24
v
그림
그림
그림
그림 차례
차례
차례
차례
Fig. 1. The mean change of UMSARS and UMSARS I from baseline
among the group ··· 13
Fig. 2. The mean change of UMSARS subgroups (on UMSRAS part I and Part II) from baseline among the group ··· 14
Fig. 3. The mean change of UMSARS from baseline comparing
between two groups with similar baseline scores. ··· 15
Fig. 4. The difference of glucose metabolism between baseline and
follow up FDG-PET/CT. ··· 16
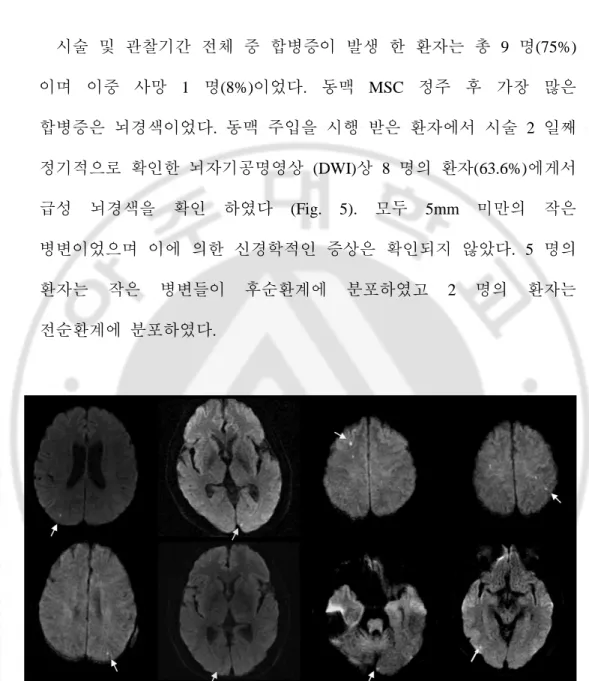
Fig. 5. The acute infarct lesions on brain MRI (DWI) after intra-arterial injection ··· 17
vi
표
표
표
표 차례
차례
차례
차례
I. 서
서
서
서 론
론
론
론
다 계통 위축증 (multiple system atrophy, MSA)은 산발적으로 발생하는 신경변성질환이며 특징적으로 운동 완서, 강직, 진전, 보행 장애의 파킨슨 증후군의 증상 및 운동실조 등의 소뇌 증상, 자율신경계증상,
추체로증상 등을 보이는 질환이다 (Wenning 등, 2004). 유병율은
100,000 명 당 4~5 명 정도이며 기대여명은 6 년에서 9 년정도로 대개의
경우 10 년 이내 무능력 상태에 놓이게 된다(Bower 등, 1997;
Ben-Shlomo 등, 1997; Schrag 등, 1999). MSA 는 특발성 파킨슨 병 (Idiopathic Parkinson disease, IPD)과는 달리 병의 경과를 호전시키거나 중단시킬
치료 방법은 없는 상태이며 80% 이상의 MSA 환자는 도파민성 약물에 대한 반응을 기대 할 수 없다. 약물 반응이 없는 첫 번째 이유로는 주로 흑질에 국한된 병리학적인 변화가 생기는 IPD 과는 달리 MSA 의 경우 흑질 외에도 기저핵, 소뇌, 뇌교, 척수 등의 광범위한 중추신경계에 병리학적인 변화가 발생하는 것 이 그 원인으로 생각되며 (Nadia 등, 2005;Kurt, 2005), 두번째로 신경세포사의 기전이 단독으로 작용하는 것이 아니라 명확하게 밝혀지지 않은 여러 기전들이 서로 중층적으로 연관되어 있는 이유 때문에 임상영역에서의 치료가 쉽지 않은 것으로 생각되고 있다. 이러한 질환의 특성상 중추신경계의 일정부위나 기전만을 목표로 하는 치료 약제는 그 효과가 제한적일 수 밖에 없다.
- 2 - 따라서 이러한 퇴행성 질환에서 소실된 신경세포를 재생시키거나 대체 할 수 있는 치료가 필요하며 본 저자들은 이러한 근본적인 치료로서 세포 대체 요법을 제안하는 바이다. 세포 대체 요법은 재생능력이 없는 신경세포의 세포사 과정에서 손상된 구조가 회복되거나 재 분화 할 수 있는 생물학적인 대체 세포를 제공 할 수 있다는 측면에서 임상적인 새로운 가능성을 제시하고 있다. 최근 골수내단핵구세포 (주로 조혈모세포)의 혈관신생을 포함한 임상적인 효과는 급성심근경색, 사지 허혈 등에서 보고된바 있다 (Bodo
등, 2002; Strauer 등, 2002; Tateishi-Yuyama 등, 2002; Tse 등, 2003).
퇴행성 신경계 질환에서 세포대체 요법은 태아 도파민 신경원을
IPD 환자의 기저핵에 이식하면서 시작되었다. 손상된 구조에 태아
도파민 신경원이 이식되면 기존 기저핵의 신경원들과 시냅스를 형성하면서 그 기능을 복원하는 것으로 알려져 있으며 이는 임상적인 증상 호전 외에도 Positron emission tomography (PET)/ computer tomography
(CT) 등을 이용한 기능적 영상소견에서도 입증되고 있다.
현재 줄기세포를 이용한 퇴행성신경계 질환에서의 연구는 배아 줄기세포, 성인 뇌세포의 줄기세포, 골수 등의 다른 체세포 내 줄기세포를 이용한 도파민 신경원의 분화 등이 동물실험에서 이루어 지고 있다. 그러나 배아 줄기세포의 경우 윤리적인 문제뿐만 아니라
- 3 - 배아 내에서 줄기세포를 추출하는 기술적인 문제 등이 있으며, 타종 줄기세포이식술은 시술의 부작용과 이식 후 자가면역 억제 치료가 지속적으로 필요하고 성인 뇌 줄기세포의 경우 자가이식 시 추출한 본인의 세포 역시 이미 퇴행성 변화가 진행되었을 가능성 등 임상적인 적용에 있어 큰 한계가 있는 것이 사실이다. 따라서 골수줄기세포 중 중배엽줄기세포 (Mesenchymal stem cell, MSC)를 이용한 세포대체요법은 자가이식을 통해 안정성과 더불어 윤리적인 문제 역시 해결 할 수 있는 방법이라 할 수 있다. 또한 뇌경색 환자에서 성체줄기세포를 투여한
결과 그 유용성 및 안정성에 있어서 이미 보고 된 바 있다 (Bang 등,
2005). 본 저자는 골수줄기세포의 자가이식을 이용한 세포대체 요법을 MSA 환자들에게 적용하였으며 그 효과에 관하여 이야기 하고자 한다.
- 4 -
II. 대상
대상
대상
대상 및
및
및
및 방법
방법
방법
방법
A. 환자환자환자환자 선정선정선정선정 본 연구는 2004 년 12 월부터 2006 년 5 월의 기간 동안 실시되었다. 실험은 MSC 주사군과 대조군의 두 군으로 나누어 시행되었다. MSC 주사군은 아주대학교 의료원 신경과에 내원한 임상적으로 MSA 에 부합하는 환자 중에서 75 세 이하의 환자로서 중등도내지 중증의 신경학적 결함을 보이며, 혈액학적으로 이상이 없는 자로 골수기능 부전의 의심되지 않는 자, 연구 동의 승낙서를 자의로 필 한 자의 조건에 부합되는 자로 선정되었고 심한 내과적 질환이 병존하는 경우이거나, 심한 발열성 상태인 경우, 혈청 SGOT/SGPT 수치가 정상의 3 배 이상 또는 creatine 수치가 정상의 1.5 배 이상, 환자의 장기 생존에 영향을 주는 질환이 있는 경우, 의식이 혼미 또는 혼수상태로 재활치료가 불가능한 경우, 신경학적 검사상 치매(알츠하이머성 혹은 혈관성 치매)가 존재하는 경우에는 대상에서 제외되었다. 대조군의 환자는 (1) 임상적으로 MSA 에 부합하는 75 세 이하의 환자 (2) 경도내지 중증의 신경학적 결함을 보이는 환자 (3) 연구 동의 승낙서를 자의로 필한 자가 선정되었다.- 5 -
B. 자료자료 수집자료자료 수집수집수집
임상적인 지표는 the Unified Multiple System Atrophy Rating Scale
(UMSARS)로 평가되었고 실시 첫 주에 기준 점수를 측정하고 12개월 동안 2개월의 간격으로 측정하였다. UMSARS평가는 2명의 독립적인 평가자에 의해 실시되었다 (K.J.W., L.M.A.). 평가 결과에 대한 평가자간의 합의는 양호하였다 (kappa=0.92). 세포 치료 전 환자의 해부학적 혹은 기능적 뇌의 상태를 파악하기 위하여 자율신경계 평가, 뇌 자기공명 영상 및 brain FDG-PET을 시행하였다. C. 골수골수골수골수 채취채취채취 및채취 및및및 중중배엽세포중중배엽세포배엽세포 추출과배엽세포 추출과추출과추출과 세포세포세포세포 배양배양배양 배양 골수(5ml)는 장골 마루의 후방에서 국소 마취 한 후 추출되었다. 골수 단핵구는 Ficoll density centrifugation 으로 분리하였고 이렇게 적혈구가
제거된 단핵구 (1x 106
/ml)는 175cm2 의 flask (Falco, Franklin Lakes. NJ)내 10% fetal bovin serum (FBS) (Hyclone, Irvine, CA)과 1% penicillin/streptomycin
(Sigma, St. Louis, MO)이 함유된 Dulbecco’s Modified Eagles medium(DMEM)에서 배양하였다. 5 일 후 응집되지 않은 세포는 제거 된
후 남은 세포들이 군집을 형성하는데 5~7 일정도 소요 된다. 이렇게 배양된 MSC 는 필요량의 80%정도 되며 이 세포들은 0.25% trypsin 을
- 6 - 통해 모아져 재배양된다. 자가 MSC 는 환자당 1×108 개 이상의 세포로 증식되었다. 세포의 생존능력은 95%이상으로 측정되었다 (trypan blue 를 통해 측정). 모든 flask 는 매주 세균, 곰팡이균, 바이러스 및 mycoplasma 유무를 조사하였다. D. 세포세포세포세포 주입을주입을주입을 위한주입을 위한위한위한 준비준비준비 준비 모아진 MSC 는 SH antigen 의 높은 표현률과 함께 균등한 밀도를 보였으며 (>93%) CD34, CD45, human leukocyte antigen-D related 나 class I
human leukocyte antigen 은 관찰되지 않았다. 모든 flask 는 매주 세균,
곰팡이균, 바이러스 및 mycoplasma 유무를 조사하였다. 모든 처치는
GMP (Good Manufacturing Practice) conditions (FCB-파미셀 Co Ltd,
Korea )에서 시행되었다..
MSC 주입은 환자 1 인당 총 4 회 시행되었으며 1 차 주입은 두개 내
동맥에, 나머지 3 회의 주입은 매 1 개월마다 정맥주사로 시행되었다. 1 차 동맥주입은 경피적인 시술로 시행되어 우측 대퇴동맥을 통해 6Fr guiding
catheter(Guider, Target therapeutics, Freemont, USA)를 통해 실시되었다.
MSC 는 50ml 생리식염수에 희석되어 주입 펌프를 통하여 일정한 시간
동안 정주되었다. 총 4×108
개의 세포를 양측 내경동맥 (각 2×107
- 7 - 우세한 척추동맥(2×107개)의 말단부에 주입하였다. 정맥 주입은 1 개월의 간격으로 초 3 회에 걸쳐 실시되었으며 매회 4×108 개의 MSC 를 100ml 생리 식염수에 희석하여 전완정맥을 통하여 주사하였다. E. FDG-PET CT scan
PET/ computed tomography (CT) 결과는 Discovery ST scanner (General Electric Medical Systems, USA)에서 얻었다. 4 시간이상 금식한 상태에서
18- FDG 를 300 MBq 주사한 후 30 분간 같은 자세를 유지하도록 교육한
후 검사를 실시하였다. 일차 촬영 (tube-rotation time of 1 s per revolution;
120 kV; 70 mA; 5.0 mm per rotation and an acquisition time of 11.8 s for a scan length of 150.42 mm.) 후에 3 차원 기법을 통하여 1 프레임의 emission PET
data 를 얻었다 (8 min per frame). PET 영상은 촬영된 CT 영상을 이용하여
재구성되었다.
기초 영상과 추적 관찰된 FDG-PET 영상은 MATLAB software ver 7.1
(Mathworks Inc., Natick, MA, U.S.A.)내 SPM2 (Statistical Parametric Mapping 2,
Institute of Neurology, University of London, U.K.) 의 standard template 로
규정된 구조적인 정상 값이다. 정상 값은 Gaussain kernel (full-width at
half-maximum=16mm)을 통해 다듬어 졌고, Talairach system 에 기록되었다. MSC 치료 후 대사 활동이 변화된 뇌 부위를 찾기 위해서 두 영상들을
- 8 -
voxel-by-voxel manner (paired t-test)로 분석하였고, p value 는 0.05 미만 extent threshold (Ke)는 100 이상이 되어야 통계적인 의미를 두었다.
대조군의 뇌 대사 작용을 분석하는데도 같은 방법을 사용하였다. 두 군의 대사작용 변화를 비교하기 위해서는 SPM2 의 SISCOM software 를 사용하였다. F. 합병증의합병증의합병증의합병증의 확인확인확인확인 MSC 주입 치료의 안정성 확보를 위하여 다음의 부작용을 예측하고 각각에 관하여 적절한 시행 규칙 및 대책을 수립하였다. 천자부 출혈, 골수천자 전에 일반 혈액검사, PT, PTT, BT를 실시하며 골수 천자 후 충분한 국소 압박을 시행하였다. 골수염, 골수천자 시 무균적으로 시술하며 발열, 통증 및 피부상태에 관하여 추적 관찰하였다. 골수줄기세포배양과정에서의 감염, MSC를 환자에게 주입하기 전 감염여부에 관해서 충분히 확인하였다. 골수줄기세포의 주입으로 인한 혈관의 폐색이나 과량의 세포가 급속히 주입되는 것을 막기 위하여 생리식염수에 충분히 희석하고 (50~100ml) 최소 30분간 천천히 정주하였으며 시술 후 뇌경색의 확인을 위하여 신경학적인 검사 시행 및 brain MRI를 시행하였다. 면역반응, 면역반응이 발생하는지 발열 등 환자 상태를 수일간 관찰하며 혈액검사를 통하여 혈액 내 염증세포의 증가
- 9 -
여부를 확인하였다. Fetal bovin serum (FBS)를 이용한 배양법 및 세포 전처치에 사용되는 약물에 대한 과민반응을 확인하고 penicillin skin test를 시행하며 양성반응 시 streptomycin으로 전처치를 시행하였다.
G. 통계통계통계통계 분석분석분석 분석
치료 효과에 대한 통계분석은 2개월간 총 12개월에 걸쳐 시행된 두 군 간의 UMSARS의 변화를 기준으로 실시되었다. 두 군 간의 차이를 확인하기 위해 Mann-Whitney U test가 사용되었고, 각 변수(성별과 MSA의
분류)의 비교를 위해서는 χ2
test가 사용되었다. 모든 값은 p values가
- 10 -
III. 결
결
결
결 과
과
과
과
A. 인구인구인구인구 통계학적인통계학적인통계학적인 특성통계학적인 특성특성 특성 상기의 조건을 만족하는 총 29 명의 MSA 환자가 대상으로 선정되었으며 이중 MSC 치료 군이 11 명 (남자 58, 여자 7, 평균연령 57.5 ± 6.5 년, 평균 유병기간 5.8 ± 1.2 년), 대조군이 18 명 (남자 12, 여자 6, 평균연령 57.2 ± 6 년, 평균 유병기간 4.0 ± 1.2 년)으로 구성되었다 (Table 1). 두 군에서 MSA 아형에 대한 분포는 차이가 없었다; MSC 군에서는MSA-C (소뇌형) 9 명, MSA-P (파킨슨형) 2 명이었고 대조군에서는 MSA-C
15 명, MSA-P 3 명이었다. 기본 UMSARS 점수는 MSC 치료군이 대조군에
- 11 -
Table 1. Demographic characteristics at baseline
Control group MSC group p
Whole 30 <UMSARS ≤ 65
Whole 30 <UMSARS ≤ 65
Patients (n) 18 14 11 5
Age (yr) 57.2 ± 6.5 57.3 ± 6.7 57.5 ± 6.5 54.8 ± 6.5 NSA,B
Age at onset (yr) 53.2 ± 6.3 54.3 ± 7.1 51.9 ± 6.7 48.6 ± 5.6 NSA,B
Sex (female, %) 6 (33.3) 7 (50) 3 (27.3) 3 (60) NSA,B
Disease duration (yr) 4.0 ± 1.2 4.2 ± 1.2 5.8 ± 1.2 5.6 ± 1.5 0.001,A NSB
MSA-C/-P 15/3 11/3 9/2 4/1 NSA,B
UMSARS 39.1 ± 14.8 44.3 ± 11.9 71.6 ± 19.8 52.5 ± 10.1 <0.001,A NSB
PET scan interval 12.0 ± 0.9 11.9 ± 0.9 NS
Plus-minus values are mean ± SD. A Comparison of all the patients between the control and MSC groups. B Comparison of the patients whose baseline UMSARS score ranged from 31 to 65 between the control and MSC groups. MSC: mesenchymal stem cell, UMSARS: Unified Multiple System Atrophy Rating Scale, MSA-C/-P: multiple system atrophy-cerebellar/-parkinsonian, NS: not significant
- 12 -
B. UMSARS 비교비교비교 비교
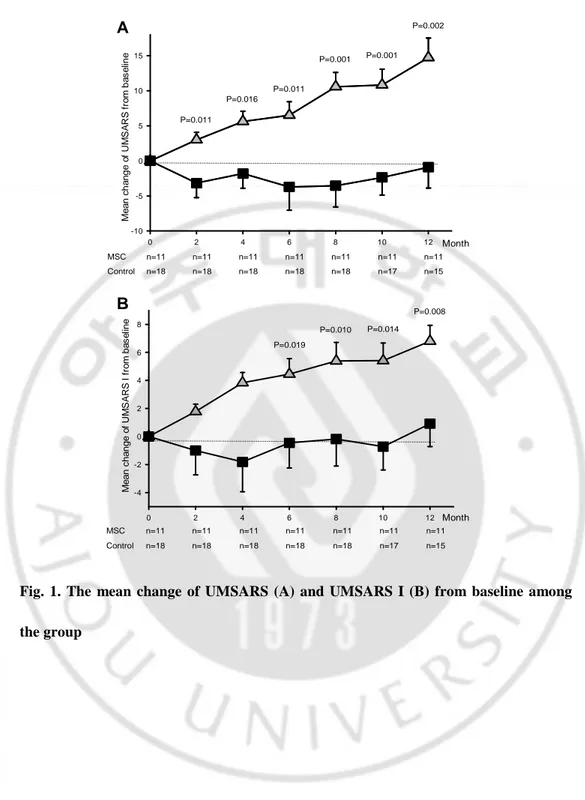
MSC 군의 환자들은 대조군에 비하여 12 개월간 측정된 UMSARS 의
확연한 호전을 보였다 (Fig. 1A). MSC 군에서 12 개월 후에 측정된 평균
UMSARS 점수는 baseline 에 비해서 낮아졌으나 대조군에서는
baseline 보다 증가된 소견을 보였다. 각각의 UMSARS part 들을
비교해보면, UMSARS part I 만이 2 개월째 측정에서부터 의미 있는
차이를 보였다 (Fig. 1B).
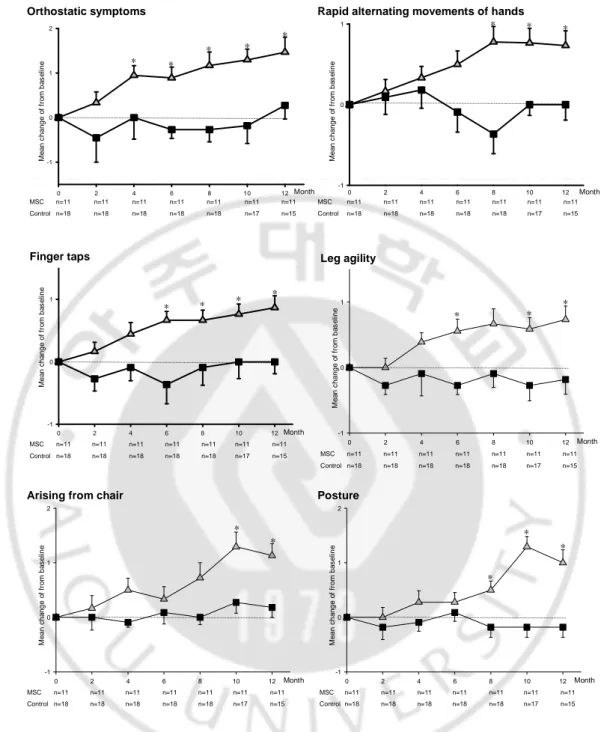
UMSARS 의 각 항목별 비교를 해보면 UMSARS part I
에서 orthostasis 항목, UMSARS part II 에서 finger tapping, rapid alternating
movement, arising form chair, leg agility 및 posture 항목들에서 두 군 간의
의미 있는 차이를 보였다 (Fig. 2)
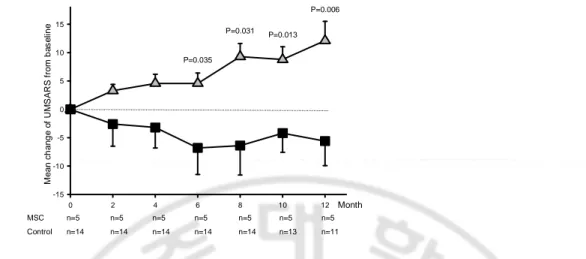
MSC 치료의 효과를 명백하게 확인하기 위하여 기본 UMSARS 점수가 31 점에서 65 점 사이에 속하는 MSC 군 (n=5)과 대조군 (n=14)을
선정하였다 (52.5 ± 10.1in the MSC group and 44.3 ± 11.9 in the control group,
p>0.05). 이 두 군간의 통계학적인 비교에서 3 회 측정값부터 MSC 군이
- 13 - 0 2 4 6 8 10 12 -10 -5 0 5 10 15 A MSC Control n=11 n=18 n=11 n=18 n=11 n=18 n=11 n=17 n=11 n=18 n=11 n=18 n=11 n=15 Month M e a n c h a n g e o f U M S A R S f ro m b a s e lin e 0 2 4 6 8 10 12 -4 -2 0 2 4 6 8 B MSC Control n=11 n=18 n=11 n=18 n=11 n=18 n=11 n=17 n=11 n=18 n=11 n=18 n=11 n=15 Month M e a n c h a n g e o f U M S A R S I f ro m b a s e li n e P=0.011 P=0.016 P=0.011 P=0.001 P=0.001 P=0.002 P=0.019 P=0.010 P=0.014 P=0.008
Fig. 1. The mean change of UMSARS (A) and UMSARS I (B) from baseline among
- 14 - 0 2 4 6 8 10 12 -1 0 1 2 Orthostatic symptoms MSC Control n=11 n=18 n=11 n=18 n=11 n=18 n=11 n=17 n=11 n=18 n=11 n=18 n=11 n=15 Month M e a n c h a n g e o f fr o m b a s e lin e 0 2 4 6 8 10 12 -1 0 1
Rapid alternating movements of hands
MSC Control n=11 n=18 n=11 n=18 n=11 n=18 n=11 n=17 n=11 n=18 n=11 n=18 n=11 n=15 Month M e a n c h a n g e o f fr o m b a s e lin e 0 2 4 6 8 10 12 -1 0 1 Finger taps MSC Control n=11 n=18 n=11 n=18 n=11 n=18 n=11 n=17 n=11 n=18 n=11 n=18 n=11 n=15 Month M e a n c h a n g e o f fr o m b a s e lin e 0 2 4 6 8 10 12 -1 0 1 Leg agility MSC Control n=11 n=18 n=11 n=18 n=11 n=18 n=11 n=17 n=11 n=18 n=11 n=18 n=11 n=15 Month M e a n c h a n g e o f fr o m b a s e lin e 0 2 4 6 8 10 12 -1 0 1 2
Arising from chair
MSC Control n=11 n=18 n=11 n=18 n=11 n=18 n=11 n=17 n=11 n=18 n=11 n=18 n=11 n=15 Month M e a n c h a n g e o f fr o m b a s e lin e 0 2 4 6 8 10 12 -1 0 1 2 Posture MSC Control n=11 n=18 n=11 n=18 n=11 n=18 n=11 n=17 n=11 n=18 n=11 n=18 n=11 n=15 Month M e a n c h a n g e o f fr o m b a s e lin e ∗ ∗ ∗ ∗ ∗ ∗ ∗ ∗ ∗ ∗ ∗ ∗ ∗ ∗ ∗ ∗ ∗ ∗ ∗ ∗
Fig. 2. The mean change of UMSARS subgroups (part I & II) from baseline among group
- 15 - 0 2 4 6 8 10 12 -15 -10 -5 0 5 10 15 MSC Control n=5 n=14 n=5 n=14 n=5 n=14 n=5 n=13 n=5 n=14 n=5 n=14 n=5 n=11 Month M e a n c h a n g e o f U M S A R S f ro m b a s e li n e P=0.035 P=0.031 P=0.013 P=0.006
Fig. 3. The mean change of UMSARS from baseline comparing between two groups with similar baseline scores (baseline UMSARS score ranged from 31 to 65 (52.5 ± 10.1in
the MSC group and 44.3 ± 11.9 in the control group, p>0.05) .
C. PET data
Positron emission tomography (PET) data 의 baseline 과 추적검사는
MSC 군에서 5 명, 대조군에서 10 명의 환자에서 실시되었다. 평균
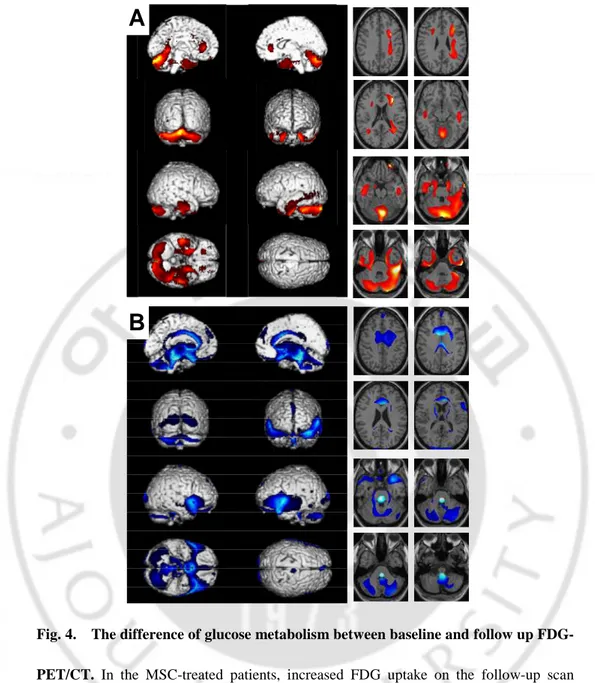
추적기간은 MSC 군에서 11.9 개월, 대조군에서 12 개월이었다. MSC 군에서 초기 검사에 비해 추적검사에서 소뇌와 백질 부위에서 FDG
uptake 가 증가되는 소견을 보였다 (fig. 4A).
이와는 대조적으로 대조군에서는 추적검사에서 초기검사보다 소뇌와 뇌간의 FDG uptake 감소가 관찰되었다 (Fig. 4B).
- 16 -
A
B
Fig. 4. The difference of glucose metabolism between baseline and follow up
FDG-PET/CT. In the MSC-treated patients, increased FDG uptake on the follow-up scan
compared to the initial scan was noted in the cerebellum and white matter (A). In contrast, the FDG uptake in the follow-up scan of the control group decreased significantly in the cerebellum and brainstem (B).
- 17 - D. 합병증의합병증의합병증의합병증의 종류와종류와종류와종류와 빈도빈도빈도 빈도 시술 및 관찰기간 전체 중 합병증이 발생 한 환자는 총 9 명(75%) 이며 이중 사망 1 명(8%)이었다. 동맥 MSC 정주 후 가장 많은 합병증은 뇌경색이었다. 동맥 주입을 시행 받은 환자에서 시술 2 일째 정기적으로 확인한 뇌자기공명영상 (DWI)상 8 명의 환자(63.6%)에게서 급성 뇌경색을 확인 하였다 (Fig. 5). 모두 5mm 미만의 작은 병변이었으며 이에 의한 신경학적인 증상은 확인되지 않았다. 5 명의 환자는 작은 병변들이 후순환계에 분포하였고 2 명의 환자는 전순환계에 분포하였다.
- 18 - 정맥 정주 후 가장 많이 관찰 되었던 합병증은 발열이었으며 총 6 명(54.5%)의 환자에게서 발생하였다. 이중 4 명은 1 차, 2 차 정맥주입에서 발열이 발생하였고 2 명은 1 차 주입에서만 발열이 발생하였다. 대개 acetaminophen 외에 특별한 치료 없이 1~3 시간 후 해열되었다. 이외 12 개월간의 관찰기간 중 장기적인 시술 합병증은 관찰되지 않았다. 1 명의 환자에서 급성담낭염이 발생하였으나 시술 전부터 담석이 진단되었던 환자로 수술적인 치료를 통해 완치되었다. 이 외 질환 자체에 의한 신경학적인 저하가 원인이 되어 발생한 합병증이 4 명의 환자에게서 관찰되었으며 각각 비뇨기계 감염, 흡인성 폐렴, 욕창, 수면 무호흡증에 의한 호흡부전이 있었고 이중 1 명(8%)은 사망하였다.
- 19 -
IV. 고
고
고
고 찰
찰
찰
찰
MSA 는 IPD 보다 빠른 진행경과를 보이며 기대 여명이 짧은 질환이나 약물 치료에 반응이 없고 증상 치료 역시 쉽지 않아 무능력 상태로 진행하는 기간 역시 짧다. 하지만 현재로서는 환자들의 증상 호전이나 수명 연장에 도움이 될 수 있는 치료가 거의 없다. 최근에는 중배엽 줄기세포 (MSC) 이식술이 다른 의학영역에서뿐만 아니라 신경계 퇴행질환 (뇌경색, 근위축성측삭경화증, 파킨슨 병 등)에서도 활발히 연구되고 있으며 (Li 등, 2001; Akiyama 등, 2002), 동물 모델 에서의 골수 줄기세포는 뇌-혈류 장벽을 통과하여 병변 부위로 이동하며 신경세포 및 교세포 등으로 분화 될 수 있다고 알려져 있다(Li 등, 2002). 또한 이런 병리학적 소견 외에도 behavioral recovery 및 신경학적인 결손의 호전에서 유의한 결과 등이 보고 되고 있다 (Chen 등, 2001; Li 등, 2002; Modo 등, 2002; Chen, 2002). 하지만 MSA 에 대한 줄기 세포 치료의 보고는 없으며 이는 MSA 의 다양한 증상 발현과 광범위한 영역의 병리학적인 변화 때문으로 생각된다. 본 저자들은 MSA 환자에 대한 임상적인 중배엽 줄기세포 치료를 시행하였으며 MSA 의 진행 경과를 늦출 수 있는 치료로서의 유용성을 가지고 있는 가에 초점을 맞추어 연구를 진행하였다.- 20 -
환자의 상태를 시사하는 측정 도구에 관한 연구는 매우 드물고 그 결과
역시 큰 의미를 가지지 못하고 있다 (Klockgether 등,1998; Mu¨ller 등,
2000; Seppi 등, 2005;Geser 등, 2006). 이는 UPDRS scale이 MSA에서
보이는 자율신경계이상증상과 소뇌 증상에 관하여 충분히 반영하지
못하기 때문으로 생각 된다. 따라서 이를 반영할 수 있는 다른
판정도구가 필요하며 최근 발표된 임상 연구 및 보고에서는 UMSARS
가 MSA 환자에서 기능적인 문제의 심한 정도와 진행을 표현 할 수
있는 새로운 척도라고 제시하였다 (Wenning 등, 2004; Geser 등, 2006).
UMSARS는 Part I (Historical Review), Part II (Motor Examination Scale), Part III (Autonomic Examination), Part IV (Global Disability Scale)의 4개 항목으로
구성되어 있다. 보고에 따르면 MSA 환자에서 12개월간 UMSARS의 평균 증가율은 17.2점 이다 (Geser 등, 2006). 본 연구에서도 역시 UPDRS 및 ataxia scale은 치료군과 대조군 모두에서 유의할 만한 차이를 가지지 못하였고, UMSARS만이 두 군간의 의미 있는 값의 차이를 보였다. 즉 MSC 치료군에서의 UMSARS 진행률은 대조군에 비하여 낮은 것을 확인 할 수 있고, 기초값과 비교한 점수에서 MSC 주입 후 10개월까지 UMSARS가 감소되어 있었으며 이후 12개월에 평균 증가 값이 1.6 점으로 대조군의 평균 증가 값, 14.7점과 비교할 때 큰 차이를 보이는 것을 알 수 있었다. UMSARS의 항목 중에서는 UMSARS part I에서 두 군 간의 유의한 차이를 보이는 것으로 조사되었으며 이는 세포 치료에 의한
- 21 -
증상 호전은 운동 분야에서 보다 자율 신경계 이상 및 운동실조증 등의 소뇌 증상과 연관 되어 일상 생활 유지에 더 큰 영향을 줄 수 있음을 시사한다. 하지만 UMSARS part IV에서 유의한 차이를 보이지 않음은 결과적으로 질환의 진행률은 MSA의 무능력 정도 와는 크게 연관이 없음을 보여준다.
PET scan에서 5명의 MSC군의 환자는 대조군과 비교하여 소뇌와
백질부에서 FDG uptake가 증가되는 소견을 모였는데 이는 소뇌위축과
백질의 변성이 MSA의 중요한 병리학적인 소견이라는 점에서 그 의미가
크다고 하겠다 (Dickson 등, 1999; Burn 등, 2002; Ozawa 등, 2004). 그러나
기저핵 역시 MSA에서 중요한 병리학적인 위치이나 FDG uptake의 증가 소견은 관찰되지 않았다. 이는 앞서 기술한 UMSARS의 part I 항목에서 두 군간의 유의한 차이를 보이는 결과와 부합되는 소견이라고 생각된다.
MSC 치료의 정확한 기전은 밝혀져 있지 않지만 MSC는 병변에 대한
유도(homing), 융합(engraft) 및 분포(disseminate) 등 다양한 특성을 가질 뿐 아니라, 여러 유도 물질들을 발생 시켜 기능적인 회복이나 신경세포의 유지와 재건에 도움을 줄 것으로 생각된다 (Barry 등, 2004). 다른 연구에서처럼, MSC 주입 초기에 보인 기능적인 회복 (UMSARS I)은 MSC에 의한 유도인자의 발현으로 생각 할 수 있다 (Bang 등, 2005). 하지만 UMSARS II의 다섯 가지 항목에서의 증상 호전 및 초기 효과가 12개월 간에 걸쳐 지속된 점, 추적관찰 된 뇌 PET영상에서 FDG uptake가
- 22 - 증가 된 것 등은 유도 인자에 의한 기전 만으로는 설명하기 힘들다. 여러 in vitro 연구에서 MSC는 뉴런 내에서 다양한 표현형 및 형태학적 특징을 가지는 것으로 알려 졌다 (Woodbury 등, 2000; Wislet-Gendebien 등, 2005). 게다가 최근의 병리 연구에서는 골수 이식 후 MSC가 푸르키니에세포 (Purkinje cell)나 해마 뉴런 등 다양한 형태의 뉴런으로 분화됨이 보고 되었다 (Weimann 등, 2003; Cogle 등, 2004). 따라서 본 연구에서도 기능적 및 대사적 측면에서의 결과를 볼 때 주입된 MSC가 뉴런에서 분화되었음을 시사한다고 볼 수 있다. 이번 연구에서는 뇌에 도달하는 세포의 수를 늘리기 위해 동맥주사 방법을 시도하였다. 결과적으로 특별한 증상이 없는 작은 뇌경색이 발생한 것 외에는 안정성에 문제가 없는 것으로 나타났다. 발생한 뇌경색은 모두 일정한 형태를 가지며 매우 작은 크기라는 점을 볼 때 세포 주입에 의해 발생한 것이라기 보다는 뇌혈관조영술 자체의 합병증일 가능성이 더 높을 것으로 판단된다. 따라서 세포의 동맥 주사와 반복적인 정맥 주사 모두 세포 치료의 방법으로 사용하기에 안전한 것임을 보여준 것에 또한 이 연구의 의의가 있다고 하겠다. 본 연구의 문제점으로는 우선 두 group 간의 초기 UMSARS 점수와 유병기간의 차이가 있으며 대조군에서 그 값들이 더 낮다는 점이다. 이 전의 연구에 따르면 질병의 유병기간 이 짧을수록 또 질병의 초기
- 23 - 단계에서 UMSARS score의 악화 속도가 더 빠르다고 보고 된 바 있다 (Geser 등, 2006). 하지만 여기에서는 치료군과 대조군의 각 변수가 유사한 환자를 따로 모아 하위 집단을 만들어 비교하였으며 이 결과 역시 무작위로 실시된 실험 결과와 차이가 없음을 제시 하였다. 둘째로 MSA에서 증상의 불안정에 관여하는 인자 중에서 위약효과를 무시 할 수 없다는 점이다 (Raúl 등, 2002; Fabrizio 등, 2005). 따라서 이에 따르면 본 연구가 open-labeled study인 점을 감안할 때 세포 주입 후 증상의 호전을 보이는 임상적인 결과가 참 값인 지는 감별 할 수 없게 된다. 우선 본 연구에서는 위약효과에 의한 오류를 가능한 제거하기 위하여 치료 시행 후 1개월까지의 결과값은 통계에 포함하지 않았으나, 이중맹검법으로 연구를 진행하지 않는 한 상기의 문제점을 제거하기는 쉽지 않다. 이중맹검법으로 검사를 시행 할 경우 본 질환의 짧은 기대 여명과 혈관 조영술 시행 및 골수 천자 시 발생 할 수 있는 부작용 등을 고려할 때 윤리적인 문제가 제기 될 수 있어 진행이 쉽지 않을 것으로 생각된다. 하지만 비록 전 환자에서 실시되지는 않았으나 일부 환자에서 시행된 FDG-PET의 대조군과의 비교 결과 및 UMSARS와의 연관성은 본 임상적인 호전이 단지 위약효과에 의한 것이 아님을 입증하는 증거라고 할 수 있겠다. 셋째, 본 연구에서는 현재 생존해 있는 환자를 대상으로 연구를 진행하여 부검를 실시 할 수 없었기 때문에 주입된 세포가 병리적으로 어떤 위치에서 어떤 형태로 분화되었는지 확인 할 수 없다는
- 24 - 점이며, 넷째, 세포분화에 관하여 아직은 명확이 알려진 바가 없어 뇌척수액 및 혈청 내 cytokine 등 보조 인자를 확인 할 수 없었다는 점이다. 이러한 문제점에도 불구하고 본 연구는 치료 약제가 알려져 있지 않은 MSA에서 세포대체요법을 임상적으로 적용한 국내외 첫번째 보고이며, 뿐만 아니라 본 치료가 질환의 진행 경과를 늦추어 연구가 진행된 12개월 동안 대조군에 비해 낮은 진행률이 관찰되었다는 점에서 그 의의가 있다고 하겠다. 앞으로는 질환의 조기 단계에서 연구가 진행 되어 질병의 조기발견과 이에 따른 조기 세포대체 요법이 환자의 질병경과에 도움이 될 수 있는 지에 대한 것과, 세포대체요법에서 세포의 분화에 영향을 주는 인자들에 대한 더 많은 연구가 필요할 것으로 생각된다.
- 25 -
참고문헌
참고문헌
참고문헌
참고문헌
1. Akiyama Y, Radtke C, Honmou O, Kocsis JD: Remyelination of the spinal
cord following intravenous delivery of bone marrow cells. Glia 39(3):229-36, 2002
2. Bang OY, Lee JS, Lee PH, Lee G: Autologous mesenchymal stem cell
transplantation in stroke patients. Ann Neurol. 57: 874-882, 2005
3. Barry FP, Murphy JM: Mesenchymal stem cells: Clinical applications and biological characterization. Int J Biochem Cell Biol. 36: 568-584, 2004
4. Ben-Shlomo Y, Wenning GK, Tison F, Quinn NP: Survival of patients with pathologically proven multiple system atrophy: a meta-analysis. Neurology 48:384 –393, 1997
5. Bodo E. Strauer, Michael Brehm, Tobias Zeus, Matthias Köstering, Anna Hernandez, Rüdiger V. Sorg, Gesine Kögler, Peter Wernet: Repair of infarcted myocardium by autologous intracoronary mononuclear bone marrow cell transplantation in humans. Circulation 106:1913–1918, 2002
- 26 -
6. Bower JH, Maraganore DM, McDonnell SK, Rocca WA: Incidence of progressive supranuclear palsy and multiple system atrophy in Olmsted County, Minnesota, 1976 to 1990. Neurology 49:1284 .1288, 1997
7. Burn, D.J., and Jaros, E: Multiple system atrophy: cellular and molecular pathology. Mol Pathol.54: 419-426, 2001
8. Chen J, Li Y, Wang L, Zhang Z, Lu D, Lu M, Chopp M: Therapeutic benefit of intravenous administration of bone marrow stromal cells after cerebral
ischemia in rats. Stroke 32:1005-11, 2001
9. Chen J, Li Y, Wang L, Lu M, Chopp M: Caspase inhibition by Z-VAD increases the survival of grafted bone marrow cells and improves functional
outcome after MCAo in rats. J Neurol Sci 199:17-24, 2002
10. Cogle CR, Yachnis AT, Laywell ED, Zander DS, Wingard JR, Steindler DA, Scott EW: Bone marrow transdifferentiation in brain after transplantation: a
- 27 -
11. Dickson, D.W., Liu, W., Hardy, J., Farrer, M., Mehta, N., Uitti, R., Mark, M., Zimmerman, T., Golbe, L., Sage, J: Widespread alterations of
alpha-synuclein in multiple system atrophy. Am J Pathol. 155: 1241-1251, 1999
12. Fabrizio Benedetti, Helen S. Mayberg, Tor D. Wager, Christian S. Stohler, and Jon-Kar Zubieta: Neurobiological Mechanisms of the Placebo Effect. J
Neurosci. 25(45):10390 –10402, November 9, 2005
13. Geser F, Wenning GK, Seppi K, Stampfer-Kountchev M, Scherfler C, Sawires M, Frick C, Ndayisaba JP, Ulmer H, Pellecchia MT, Barone P, Kim
HT, Hooker J, Quinn NP, Cardozo A, Tolosa E, Abele M, Klockgether T, Ostergaard K, Dupont E, Schimke N, Eggert KM, Oertel W, Djaldetti R,
Poewe W:the European MSA Study Group.: Progression of multiple system atrophy (MSA): a prospective natural history study by the European MSA
Study Group (EMSA SG). Mov Disord. Vol. 21, No. 2, pp. 179–186, 2006
14. Klockgether T, Ludtke R, Kramer B, Abele M, Burk K, Schols L, Riess O, Laccone F, Boesch S, Lopes-Cendes I, Brice A, Inzelberg R, Zilber N,
Dichgans J: The natural history of degenerative ataxia: a retrospective study in 466 patients. Brain 121(Pt 4):589–600, 1998
- 28 -
15. Kurt A. Jellinger, Klaus Seppi, Wenning GK : Grading of Neuropathology in Multiple System Atrophy: Proposal for a Novel Scale. Mov Disord. Vol. 20, Suppl. 12, pp. S29–S36,2005
16. Li Y, Chen J, Wang L, Zhang L, Lu M, Chopp M: intracerebral transplantion
of bone marrow stromal cells in a 1-methyl-4-phenyl-1,2,3,6-tetraheropyridine mouse model of parkinson's disease. Neurosci Lett.
316:67-70, 2001
17. Li Y, Chen J, Chen XG, Wang L, Gautam SC, Xu YX, Katakowski M, Zhang LJ, Lu M, Janakiraman N, Chopp M: Human marrow stromal cell
therapy for stroke in rat: neurotrophins and functional recovery. Neurology 59:514-23, 2002
18. Modo M, Stroemer RP, Tang E, Patel S, Hodges H: Effects of implantation
site of stem cell grafts on behavioral recovery from stroke damage. Stroke 33:2270-8, 2002
- 29 -
19. Mu¨ller J, Wenning GK, Jellinger K, McKee A, Poewe W, Litvan I: Progression of Hoehn and Yahr stages in parkinsonian disorders: a clinicopathologic study. Neurology 55:888–891, 2000
20. Nadia Stefanova, Markus Reindl, Werner Poewe, Gregor K. Wenning : In Vitro Models of Multiple System Atrophy. Mov Disord. Vol. 20, Suppl. 12, pp. S53–S56,2005
21. Ozawa, T., Paviour, D., Quinn, N.P., Josephs, K.A., Sangha, H., Kilford, L., Healy, D.G., Wood, N.W., Lees, A.J., Holton, J.L : The spectrum of
pathological involvement of the striatonigral and olivopontocerebellar systems in multiple system atrophy: clinicopathological correlations. Brain
127: 2657-2671, 2004
22. Raúl de la Fuente-Fernández and A. Jon Stoessl : The placebo effect in Parkinson’s disease. Trends Neurosci. Vol.25 No.6 June 2002
23. Schrag A, Ben-Shlomo Y, Quinn NP: Prevalence of progressive supranuclear palsy and multiple system atrophy: a cross-sectional study. Lancet Nov 20;354(9192):1771-5, 1999
- 30 -
24. Seppi K, Yekhlef F, Diem A, Luginger Wolf E, Mueller J, Tison F, Quinn
NP, Poewe W, Wenning GK: Progression of parkinsonism in multiple system atrophy. J Neurol. 252:91–96, 2005
25. Tateishi-Yuyama E, Matsubara H, Murohara T, Ikeda U, Shintani S, Masaki
H, Amano K, Kishimoto Y, Yoshimoto K, Akashi H, Shimada K, Iwasaka T, Imaizumi T; Therapeutic Angiogenesis using Cell Transplantation (TACT)
Study Investigators.: Therapeutic angiogenesis for patients with limb ischaemia by autologous transplantation of bone-marrow cells: a pilot study
and a randomised controlled trial. Lancet 360:427–435, 2002
26. Tse HF, Kwong YL, Chan JK, Lo G, Ho CL, Lau CP: Angiogenesis in ischaemic myocardium by intramyocardial autologous bone marrow mononuclear cell implantation. Lancet 361:47– 49, 2003
27. Weimann JM, Charlton CA, Brazelton TR, Hackman RC, Blau HM: Contribution of transplanted bone marrow cells to Purkinje neurons in human
- 31 -
28. Wenning GK, Colosimo C, Geser F, Poewe W: Multiple system atrophy.
Lancet Neurol. 3:93.103, 2004
29. Wenning GK, Tison F, Seppi K, Sampaio C, Diem A, Yekhlef F, Ghorayeb I, Ory F, Galitzky M, Scaravilli T, Bozi M, Colosimo C, Gilman S, Shults CW, Quinn NP, Rascol O, Poewe W; Multiple System Atrophy Study Group: Development and validation of the Unified Multiple System Atrophy Rating Scale (UMSARS). Mov Disord. 19:1391–1402, 2004
30. Wislet-Gendebien S, Hans G, Leprince P, Rigo JM, Moonen G, Rogister B:
Plasticity of cultured mesenchymal stem cells: switch from nestin-positive to excitable neuron-like phenotype. Stem Cells. 23: 392-402, 2005
31. Woodbury D, Schwarz EJ, Prockop DJ, Black IB: Adult rat and human bone
marrow stromal cells differentiate into neurons. J Neurosci. Res. 61: 364-370, 2000
- 32 - - Abstract -
The Application of Mesenchymal Stem Cell therapy
on Multiple System Atrophy
Kim Ji Won
Department of medical sciences The Graduate School, Ajou University
(Supervised by Associate Professor Lee Pil Hyu)
Since disease progression in multiple system atrophy (MSA) is much faster and no drug treatment consistently benefits MSA patients in the long-term,
neuroprotective or regenerative strategies are inevitable in the management of MSA patients. We divided two group, MSC-treated (n=11) and control patients
(n=18). We evaluated the feasibility and safety of therapy with mesenchymal stem cells (MSCs) through consecutively intraarterial and 3 repeated intravenous
injections for 3 months and compared the long-term prognosis between tow groups. The MSC-treated patients showed significantly greater improvement on the unified
- 33 -
visits throughout the 12-month study period. Dysautonomia and ataxia items (UMSARS part I, UMSARS part II) were statistically different in favor of MSC
treatment compared to controls. In the MSC-treated patients, increased glucose metabolism on the follow-up positron emission tomography compared to the initial
scan was noted in the cerebellum and white matter. No serious adverse effects occurred that were related to MSC therapy. This study demonstrated that MSC
therapy in patients with MSA delayed the progression of neurological deficits with achievement of functional improvement in the follow-up period.