서론
치매는 기억력을 비롯한 인지기능의 장애로 인해, 사회생
활 및 일상생활의 장애를 유발하는 증후군을 지칭한다. 치매
의 가장 흔한 원인은 알츠하이머병이며, 혈관성 치매, 루이
소체 치매 순으로 유병률이 높다[1]. 세계적으로 평균수명이
늘어남에 따라, 거의 대부분의 나라에서 치매로 인한 부담이
늘어나고 있다[2]. 국내에서도 65세 이상 노인의 약 9.8%(약
661,707명)가 치매를 앓고 있는 것으로 추정되고 있으며, 이
로 인해 일인당 일년에 약 20,540,000원의 직, 간접적 비용
이 발생하는 것으로 알려져 있다[3]. 이에 치매환자의 진단,
치료, 관리를 위해 치매안심센터가 설립 및 확장되는 등 치
매에 대한 사회적 관심이 증가하고 있다[3].
치매의 치료 및 관리를 위해, 약물치료는 필수적인 방법
중 하나로 알려져 왔지만, 질병의 경과를 변화시키고 병전
기능을 회복시키는 약제는 아직 실용화된 것이 없다. 이에
현재 치매환자에 대한 약물치료는 경증의 상태를 가능한 오
래 유지시키고, 지속적인 조호가 필요한 시기를 최대한 늦
치매의 약물요법
윤 현 철1,2·정 현 강1,2 | 고려대학교 1의과대학 고려대학교구로병원 정신건강의학과, 2정신건강연구소Pharmacotherapy for dementia
HyunChul Youn, MD1,2 · Hyun-Ghang Jeong, MD1,21Department of Psychiatry, Korea University Guro Hospital, Korea University College of Medicine, Seoul; 2Korea University Research
Institute of Mental Health, Seoul, Korea
Received: December 6, 2018 Accepted: December 13, 2018 Corresponding author: Hyun-Ghang Jeong
E-mail: jeonghg@korea.ac.kr © Korean Medical Association
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons. org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Dementia is a clinical syndrome characterized by a cluster of symptoms and signs that manifest as difficulties in cognitive functions such as memory, psychological and psychiatric changes, and impairments in activities of daily living. As a result of worldwide trends of population aging, dementia has had a huge impact on public health in almost all countries. Disease modification therapies for dementia have not yet been developed. However, pharmacotherapy is essential in patients with dementia to combat delays in their cognitive and functional decline. In this article, we review the current pharmacotherapy for dementia. Three acetylcholinesterase inhibitors— donepezil, rivastigmine, galantamine—and memantine are the only medications that have been approved for the treatment of dementia. We present the indications, dose recommendations, side effects, and criteria for National Health Insurance coverage in Korea of these medications for dementia treatment. Although the Ministry of Food and Drug Safety in Korea has not approved any medications for managing the behavioral and psychological symptoms of dementia, some antipsychotics and antidepressants have been studied and used clinically for those purposes. Clinicians may consider vitamin E,
Ginkgo biloba
extract, choline alfoscerate, or omega-3 fatty acids as additional treatment options. Non-steroid anti-inflammatory drugs, estrogen hormone therapy, and statins are not generally recommended for dementia treatment. We believe that our findings will aid clinicians in the treatment of patients with cognitive decline.춰 환자의 기능 저하를 최소화하고 사회, 경제적 부담을 줄
이는 것을 주 목표로 한다[1,4]. 국내에서는 크게 두 가지
기전으로 나눌 수 있는 네 종류의 치매 약제가 대표적으로
사용되고 있는데, 아세틸콜린에스테라아제
억제제(acetyl-cholinesterase inhibitor)인 도네페질(donepezil), 리바스
티그민(rivastigmine), 갈란타민(galantamine), NMDA 수
용체 길항제[N-methyl-D-aspartate (NMDA) receptor
antagonist]인 메만틴(memantine)이 그것이다. 본 종설에
서는 치매에 사용되는 약물을 기전 및 종류별로 소개하고,
일반적으로 사용되는 방법에 대해 정리하였다.
아세틸콜린에스테라아제 억제제
아세틸콜린에스테라아제 억제제는 아세틸콜린에스테라아
제를 가역적으로 억제시켜서, 콜린성 기능을 향상시키는 역
할을 한다. 이는 기저핵 내의 신경 퇴행 및 신경세포 소실로
인해 해마, 대뇌피질 등 신경세포 말단이 위치하고 있는 뇌
영역에서 아세틸콜린 결핍이 나타나 기억력 저하를 일으킨
다는 가설에 기반한다[5]. 아세틸콜린에스테라아제 억제제
는 무작위 배정 이중맹검 방법을 사용하여 3-12개월 정도의
기간 동안 진행한 여러 연구에서 인지기능 저하, 일상생활기
능 저하를 늦추고 행동문제를 호전시키는 것으로 나타났다
[6,7]. 몇몇 환자에서는 일시적인 인지기능의 호전이 보고되
기도 하였다. 장기간 진행된 연구는 많지 않은데, 수년이 지
난 후에도 아세틸콜린에스테라아제 억제제 투약이 이득이
있다는 개방연구가 있는 반면, 3년이 지난 후에는 유의한 이
득이 없다는 연구 또한 보고된 바 있어, 아세틸콜린에스테라
아제 억제제 장기간 복용의 효과를 확인하기 위해서는 추가
적인 연구가 필요하다[8,9]. 1993년 미국 식품의약국(Food
and Drug Administration, FDA)에서 최초로 승인된 아세
틸콜린에스테라아제 억제제는 타크린(tacrine)이었으나, 간
독성 문제로 현재는 사용이 제한되고 있다[10].
1. 도네페질
1996년 FDA에서 승인을 받은 도네페질은 하루 5 mg부
터 시작하며, 불면, 근 경련, 피로, 오심, 식욕저하, 설사 등
의 부작용을 고려하여 4-6주 정도 투여 후 10 mg으로 증량
하게 된다[11]. 부작용이 나타날 경우 초기 용량을 2.5 mg
으로 시작할 수도 있다. 부작용은 대부분 일시적이고 경미
한 편이나, 토사드 퐁(Torsade de pointes)과 같은 부정맥,
전도장애 등이 드물게 나타날 수 있어 투약 전 심전도 검사
를 시행하거나 심혈관질환 병력을 확인하는 것이 필요할 수
있다[10,12]. 도네페질 23 mg은 도네페질 10 mg을 적어
도 3개월 이상 사용한 이후 증량을 고려하게 되는데, 중등
도에서 중증 알츠하이머 치매에서 효과가 있는 것으로 보고
되어, 2010년 FDA에서 승인받았다[13]. 도네페질은 반감기
가 약 70시간으로 긴 편이어서 일반적으로 하루 한 차례 투
약한다[4]. 도네페질은 구강 내 붕해형 제제가 있어 투약 협
조가 잘 되지 않거나 연하가 어려운 환자에서 사용하기에 용
이하다[12].
2. 리바스티그민
리바스티그민은 2000년에 FDA에서 승인받은 약제로 아
세틸콜린에스테라아제뿐만 아니라 부티릴콜린에스테라아제
(butyrylcholine esterase)도 동시에 억제한다[14]. 하루 3
mg으로 시작하여, 오심, 구토, 설사 등의 부작용을 고려하
여 하루 12 mg까지 증량하여 복용하는데, 반감기가 짧아 일
반적으로 하루 2회로 분복 한다[4]. 리바스티그민은 하루 한
번 부착하는 부착포 제제가 있다는 것이 장점으로, 많은 약
물을 복용하거나 순응도가 낮은 노인에게 특히 도움이 된다
[15]. 부착포 제제 리바스티그민은 등의 상부 또는 하부, 팔
의 상부, 가슴 등 털이 없고 옷에 의해 떨어질 염려가 적은
부위에 부착하는데, 잠재적인 피부자극을 피하기 위해 24시
간 후 교체할 때는 같은 해부학적 부위일 지라도 다른 위치
에 부착한다[12]. 부착포 제제는 소화기 부작용이 적은 반면,
부착 부위 발진이나 홍반, 가려움이 나타날 수 있어 주의가
필요하며, 알레르기성 접촉피부염이 의심되는 경우에는 투
약 중단을 고려해야 한다[10,15].
3. 갈란타민
갈란타민은 2001년도에 FDA 승인을 받았으며, 아세틸콜
린에스테라아제 외에도 니코틴 수용체(nicotinic receptor)
에 작용하여 아세틸콜린의 분비를 촉진한다[10]. 일반적으로
반감기가 짧아 하루 8-24 mg을 2회로 나누어 투약하지만,
서방형 제제의 경우에는 하루 한 번 복용이 가능하다[16]. 소
화기 부작용이 있는 경우에는 식사와 함께 투약하도록 하고,
용량을 서서히 증량한다[10].
아세틸콜린에스테라아제 억제제는 주로 알츠하이머 치매
에 사용되며, FDA 승인을 받지는 않았지만 혈관성 치매와
관련해서도 다소 효과가 있다는 보고가 있다[17,18]. 또한,
아세틸콜린에스테라아제 억제제는 루이소체 치매와 파킨슨
병 치매에서도 효과가 있다고 알려져 있으며, 특히 파킨슨
병 치매에서의 리바스티그민 사용은 FDA의 승인을 받았다
[17]. 전두측두엽치매에서의 아세틸콜린에스테라아제 억제
제 사용은 유의한 효과가 입증되지 않았을 뿐만 아니라, 부
작용으로 인해 정신심리행동증상이 악화될 가능성이 있어
추천되지 않는다[19]. 국내 식품의약품안전처에서는 도네페
질은 알츠하이머 치매에(23 mg 제형의 경우, 중등도에서 중
증의 알츠하이머 치매), 리바스티그민은 경증에서 중등도 알
츠하이머 및 파킨슨 치매(부착포 제제의 경우, 중증 알츠하
이머 치매 포함)에, 갈란타민은 경증에서 중등도 알츠하이머
치매에 사용을 허가하였다[12]. 투약 시작 시기는 늦게 투약
을 시작할 경우 인지기능에 대한 효과가 떨어질 수 있어, 가
능한 빠른 시기가 추천된다[20]. 그렇지만 경도인지장애에서
의 아세틸콜린에스테라아제 투약은 유의미한 효과가 밝혀지
지 않았다[21]. 약물 중단의 적절한 시기는 알려져 있지 않
으나, 약물로 인한 부작용이 편익을 넘을 경우, 의미 있는 상
호작용이 불가능한 말기 상태 일 경우에는 약물 중단을 고려
해 볼 수 있다[17].
도네페질, 리바스티그민, 갈란타민
은 일반적으로 비슷한 수준의 효과와
부작용을 나타내는 것으로 알려져 있
다[7]. 그러므로 한 종류의 아세틸콜
린에스테라아제 억제제를 사용한 후
부작용이 나타나거나, 효과가 충분하
지 않다고 판단되는 경우 다른 종류
의 아세틸콜린에스테라아제 억제제
로 변경할 수 있다. 변경 시 따로 약효세척 기간은 필요하
지 않다[22].
NMDA 수용체 길항제
알츠하이머 치매와 같은 신경퇴행성 질환에서 NMDA 수
용체가 지속적으로 활성화되었을 때,
글루탐산염(gluta-mate)의 과활성에 의해 신경세포가 손상을 입고 신경 퇴행
이 유발될 수 있다[23]. NMDA 수용체 길항제인 메만틴은
이러한 과정을 억제하는 기전으로 작용하며, 2003년에 중등
도에서 중증 알츠하이머 치매의 치료제로 FDA 승인을 받았
다[23]. 메만틴은 중등도에서 중증 알츠하이머 치매에서 인
지기능 및 정신행동 증상에 효과가 있는 것으로 밝혀진 것과
는 달리, 경도 알츠하이머 치매에서는 아직 효과에 대한 근
거가 부족하다[24,25]. 아세틸콜린에스테라아제 억제제와의
병용요법에 대해서는 일부 이득이 있다는 연구가 있는 반면,
이론도 있어 아직 명확하게 정립되지는 않았다[25,26]. 메만
틴은 중증도 치매 단계에 들어서는 즉시 투약을 시작하는 것
이 더 치료적 이득이 있는 것으로 알려져 있다[27]. 투약 시
에는 하루 5 mg으로 시작하여 초조, 요실금, 설사, 불면 등
의 부작용에 주의하면서 20 mg까지 증량하여 복용한다[10].
메만틴에서 또한, 투약 협조가 잘 되지 않거나 연하가 어려
운 환자가 복용하기 편리한 구강 내 붕해형 제제가 개발되어
있다[12]. 국내 식품의약품안전처에서는 중등도에서 중증의
알츠하이머 치매에서 메만틴 사용을 허가하였으며, 각 약제
의 투여 기준에 맞는 경우 아세틸콜린에스테라아제 억제제
와의 병용 투여 또한 인정하였다[12]. Table 1에서 아세틸콜
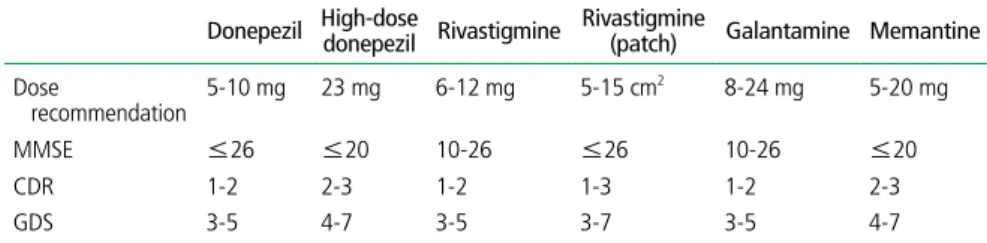
Table 1. Criteria for National Health Insurance coverage in Korea and dose recommendations for acetyl-cholinesterase inhibitors and memantine for dementia treatment
Donepezil High-dose donepezil Rivastigmine Rivastigmine (patch) Galantamine Memantine Dose recommendation 5-10 mg 23 mg 6-12 mg 5-15 cm 2 8-24 mg 5-20 mg MMSE ≤26 ≤20 10-26 ≤26 10-26 ≤20 CDR 1-2 2-3 1-2 1-3 1-2 2-3 GDS 3-5 4-7 3-5 3-7 3-5 4-7
린에스테라아제 억제제 및 메만틴의 사용 용량 및 보험인정
기준을 제시하였다.
정신심리행동증상의 치료
치매환자에서 불면, 불안, 초조, 공격성, 우울, 망상, 환각,
배회 등과 같은 정신심리행동 증상이 나타날 수 있다. 이러
한 정신심리행동 증상의 일차적 치료로 추천되는 것은 지지
체계를 확립하고 음악치료, 다감각 치료와 같은 비약물적인
접근을 사용하는 것이지만, 증상이 심하거나 조절이 되지 않
는 경우 약물치료를 적용하기도 한다[28]. 정신심리행동 증
상의 약물치료로 항정신병 약물, 항우울제, 항불안제, 기분
조절제 등이 시도되어 왔지만 아직까지 정립된 약물치료 지
침은 없다. 치매환자의 인지기능 개선을 위해 사용되는 아세
틸콜린에스테라아제 억제제의 경우에는 정신심리행동 증상
에 대한 효과가 다소 약한 수준인 것으로 알려져 있다[29].
항정신병 약물은 치매와 관련된 초조 증상 및 공격성을 조
절하기 위해 주로 사용되는데, 아리피프라졸(aripiprazole),
올란자핀(olanzapine), 리스페리돈(risperidone), 쿠에티아
핀(quetiapine), 할로페리돌(haloperidol) 등의 적용에 대한
연구들이 있다[30,31]. 그러나 뇌졸중, 진정, 추체외로 증상,
요실금 등을 포함한 다양한 부작용이 보고되고 있으며, 특히
장기간 복용 시 사망률을 증가시킬 수 있어, 3개월마다 재
평가하여 약물 중단을 고려하는 것이 추천된다[30]. 약물 용
량도 가능한 소용량이 추천되는데, 예를 들어, 리스페리돈
의 경우 주로 1-2 mg의 용량이 권장된다[32]. 쿠에티아핀
은 200 mg 이하의 용량이 주로 사용되는데, 추체외로 부작
용이 적어 파킨슨 증상이 동반된 경우 특히 우선적으로 고려
해 볼 수 있다[31].
우울증상은 치매환자에서 자주 동반될 뿐만 아니라, 알
츠하이머 치매의 전구기 단계에서도 흔히 발견된다. 치매
환자의 우울증상에 대해 선택적 세로토닌 재흡수 억제제
(selective serotonin reuptake inhibitors)가 연구되고 또한
임상적으로 사용되어 왔으며, 치료에 도움이 된다고 알려져
있다[4,33]. 하지만, 위약에 비해 유의한 효과가 없다고 보고
하는 연구들도 있어서, 논란은 남아있다[31]. 아직 충분한 연
구가 이루어진 것은 아니지만, 선택적 세로토닌 재흡수 억제
제가 치매환자의 초조와 정신병적 증상에 효과가 있다는 보
고 또한 발표되었다[31]. 삼환계 항우울제는 효과에 비해 부
작용이 커서 추천되지 않는다[31].
이외에도 벤조디아제핀계(benzodiazepine) 항불안제가
치매환자의 급성 초조 및 불안 증상 조절에 효과가 있다는
보고가 있으나, 어지럼증, 진정, 인지기능 저하, 넘어짐 등
의 부작용이 나타날 수 있어 일반적으로 추천되지는 않는다
[34]. 기분조절제 중에서는 카르바마제핀(carbamazepine)
이 치매환자의 정신심리행동증상에 효과가 있다는 연구가
있지만, 역시 부작용 및 약물 상호작용이 많아 사용이 다소
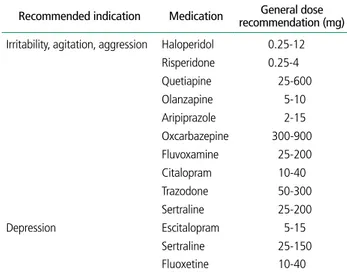
제한적이다[35]. Table 2를 통해 치매의 정신심리행동증상
에 사용할 수 있는 약제들을 정리하였다.
기타 보완적 약물요법
비타민 E는 식물성 오일이나 지방, 아몬드, 해바라기씨 등
에 존재하는데, 항산화 작용을 통해 신경세포 손상을 막아주
는 역할을 하는 것으로 알려져 있다[36]. 이러한 작용을 통해
비타민 E가 치매환자에서도 도움이 될 수 있다는 보고가 있
어, 여러 치매환자들이 특별한 처방 없이 비타민 E를 복용하
Table 2. General dose recommendations of medications for managing the behavioral and psychological symptoms of dementia
Recommended indication Medication recommendation (mg)General dose Irritability, agitation, aggression Haloperidol 0.25-12
Risperidone 0.25-4 Quetiapine 25-600 Olanzapine 5-10 Aripiprazole 2-15 Oxcarbazepine 300-900 Fluvoxamine 25-200 Citalopram 10-40 Trazodone 50-300 Sertraline 25-200 Depression Escitalopram 5-15 Sertraline 25-150 Fluoxetine 10-40
기도 한다[36]. 2014년 발표된 무작위 배정 이중맹검 연구에
서도 비타민 E가 경도 및 중등도 알츠하이머 치매에서 인지
기능 저하를 늦출 수 있다고 보고한 바 있다[37]. 그러나, 아
직 효과에 대해 다소간의 논란이 남아있는 상태이며, 오히려
혈액응고 문제를 일으키거나 사망률을 높일 수도 있기 때문
에 복용 시 주의가 필요하다[36,38].
은행나무 추출물은 뇌혈류 및 시냅스 가소성 개선, 신경
세포 보호 등의 역할을 하는 것으로 알려져 있다[39]. 은행
나무 추출물은 전통적으로 중국에서 약초로 사용되었던 것
으로, 1990년대 이후부터 치매환자에서도 널리 사용되기 시
작하였다. 이에 여러 연구가 발표되었으며, 2017년 기존의
무작위 배정 연구들을 대상으로 분석한 체계적 종설에서는
200 mg 이상의 은행나무 추출물을 5개월 이상 지속적으로
복용했을 때 치매환자에서 편익이 기대된다고 보고하기도
하였다[39]. 그러나 아직까지는 충분한 근거가 발표되지 않
았고 연구마다 결과가 다르게 나타나기도 하여 추가적인 연
구가 필요하다.
아세틸콜린에스테라아제 억제제가 인지기능 개선제로 쓰
이는 것과 마찬가지로, 콜린성 기능을 회복하는 것이 인지기
능 개선에 필요하다는 전제 하에, 콜린성 전구체인 콜린알포
세레이트(choline alphoscerate)가 치매 치료에 있어서 주목
을 받고 있다[40]. 아직 연구가 더 필요하지만, 부작용이 적
고 인지기능 개선에 효과가 있다는 연구가 발표되고 있어 단
독 또는 아세틸콜린에스테라아제 억제제와의 병용요법에 대
한 제안이 이루어지고 있다[40,41].
오메가-3 지방산(omega-3 fatty acids)은 어류와 식물
로부터 유래한 것으로 치매의 진행을 늦추고 뇌기능을 향상
시킬 수 있는 대체 요법으로 기대되었다[42]. 그러나 현재까
지 연구에서 오메가-3 지방산은 부작용이 적지만, 인지기능
개선 효과 또한 뚜렷하지 않은 것으로 나타난 상황이다[42].
그 밖에도 치매 발병 과정에서 염증이 중요한 역할을 할
것이라는 가설 하에 비스테로이드 항염증제가 고려되었으
나, 근거가 부족하여 일반적으로 권고되지는 않는다[10]. 폐
경 후 여성에서 에스트로겐 치료가 인지기능 저하를 늦춘다
는 주장이 있었으나, 알츠하이머 치매 환자에서 시행된 무작
위 배정 이중맹검 연구에서는 유의한 결과가 보고되지 않았
다[43]. 게다가 에스트로겐 투여 시 뇌졸중, 관상동맥질환,
유방암, 폐색전증 등의 위험이 증가하는 것이 보고되어, 위
험 대비 편익을 고려할 때 치매의 예방 및 치료를 위한 에스
트로겐 요법은 추천되지 않는다[44]. 혈액 내 지질을 낮추는
스타틴(statin) 또한 시도되었으나, 오히려 투여 초기 인지
저하가 보고되기도 하는 등, 치매의 예방 및 치료에 유의미
한 효과를 보여주지는 못했다[10,45].
결론
치매의 경과를 변화시켜 병전 기능을 회복시키는 약물
은 아직까지 개발되지 않았으며, 예방에 뚜렷한 효과가 있
다고 밝혀진 약물 또한 아직까지 존재하지 않는다. 그렇지
만 치매환자에서 질환의 진행을 늦추고 기능을 최대한 유
지하며 동반 증상을 완화시키기 위해 약물치료는 필수적이
라고 할 수 있다. 본 종설에서는 현재 치매환자의 치료를
위해 사용되고 있는 약물들을 정리해보았다. 아세틸콜린에
스테라아제 억제제(도네페질, 리바스티그민, 갈란타민) 와
NMDA 수용체 길항제(메만틴)는 인지기능 개선을 위해 임
상에서 가장 흔히 사용되는 약물로, Table 1에 정리된 사
용 용량 및 보험인정기준에 따라 적용이 가능하다. 치매환
자에서 동반될 수 있는 정신심리행동 증상의 경우, 증상에
따라 항정신병 약물 및 선택적 세로토닌 재흡수 억제제 사
용을 고려해 볼 수 있다. 그 밖에도 아직 근거가 다소 부족
하지만, 비타민 E, 은행나무 추출물, 콜린알포세레이트, 오
메가-3 지방산 또한 치매환자의 치료에 있어서 추가를 고
려할 수 있는 선택지이다. 노인환자의 경우 약물 부작용이
쉽게 나타나고 내외과적인 질환을 갖고 있는 경우가 많은
만큼, 치매치료를 위한 약물을 처방할 시에도 약물 상호작
용과 부작용에 대한 고려가 필수적이다. 본 종설은 임상에
서 실제 치매환자가 방문하여 약물치료를 고려할 때 특히
도움이 될 것이다.
찾아보기말:
치매; 약물치료; 콜린에스테라아제 억제제; 메만틴ORCID
HyunChul Youn, https://orcid.org/0000-0002-6557-5628 Hyun-Ghang Jeong, https://orcid.org/0000-0002-0318-5069
REFERENCES
1. Jeong HG, Han C. Diagnosis and treatment of dementia in primary care. J Korean Med Assoc 2013;56:1104-1112. 2. Xu J, Qiu C. Worldwide economic costs and societal burden of
dementia. In: Perneczky R, editor. Biomarkers for preclinical Alzheimerʼs disease. New York: Springer; 2018. p. 3-13. 3. Ministry of Health and Welfare. Korean dementia observatory
2017. Sejong: Ministry of Health and Welfare; 2017.
4. Hahn SJ, Paik NJ. Pharmacological treatment of dementia. Brain Neurorehabil 2015;8:19-23.
5. Francis PT, Palmer AM, Snape M, Wilcock GK. The choliner-gic hypothesis of Alzheimerʼs disease: a review of progress. J Neurol Neurosurg Psychiatry 1999;66:137-147.
6. Birks J. Cholinesterase inhibitors for Alzheimerʼs disease. Cochrane Database Syst Rev 2006;(1):CD005593.
7. Hansen RA, Gartlehner G, Webb AP, Morgan LC, Moore CG, Jonas DE. Efficacy and safety of donepezil, galantamine, and rivastigmine for the treatment of Alzheimerʼs disease: a systematic review and meta-analysis. Clin Interv Aging 2008; 3:211-225.
8. Zhu CW, Livote EE, Scarmeas N, Albert M, Brandt J, Blacker D, Sano M, Stern Y. Long-term associations between cholinesterase inhibitors and memantine use and health out-comes among patients with Alzheimerʼs disease. Alzheimers Dement 2013;9:733-740.
9. Courtney C, Farrell D, Gray R, Hills R, Lynch L, Sellwood E, Edwards S, Hardyman W, Raftery J, Crome P, Lendon C, Shaw H, Bentham P; AD2000 Collaborative Group. Long-term donepezil treatment in 565 patients with Alzheimerʼs disease (AD2000): randomised double-blind trial. Lancet 2004;363: 2105-2115.
10. Korean Association for Geriatric Psychiatry. Geriatric psy-chiatry. 2nd ed. Seoul: ML Communication; 2015.
11. Mendez MF, Cummings JL. Dementia: a clinical approach. Philadelphia: Butterworth-Heinemann; 2003.
12. Ministry of Food and Drug Safety. Online library of medicine [Internet]. Cheongju: Ministry of Food and Drug Safety; 2018 [cited 2018 Nov 1]. Available from: http://drug.mfds.go.kr/ html/index.jsp#n.
13. Farlow MR, Salloway S, Tariot PN, Yardley J, Moline ML, Wang Q, Brand-Schieber E, Zou H, Hsu T, Satlin A. Effective-ness and tolerability of high-dose (23 mg/d) versus standard-dose (10 mg/d) donepezil in moderate to severe Alzheimerʼs disease: a 24-week, randomized, double-blind study. Clin Ther 2010;32:1234-1251.
14. Polinsky RJ. Clinical pharmacology of rivastigmine: a
new-generation acetylcholinesterase inhibitor for the treatment of Alzheimerʼs disease. Clin Ther 1998;20:634-647.
15. Cummings JL, Farlow MR, Meng X, Tekin S, Olin JT. Rivastig-mine transdermal patch skin tolerability: results of a 1-year clinical trial in patients with mild-to-moderate Alzheimerʼs disease. Clin Drug Investig 2010;30:41-49.
16. Seltzer B. Galantamine-ER for the treatment of mild-to-mo-derate Alzheimerʼs disease. Clin Interv Aging 2010;5:1-6. 17. Wong CW. Pharmacotherapy for dementia: a practical
appro-ach to the use of cholinesterase inhibitors and memantine. Drugs Aging 2016;33:451-460.
18. Deschaintre Y, Richard F, Leys D, Pasquier F. Treatment of vascular risk factors is associated with slower decline in Alzheimer disease. Neurology 2009;73:674-680.
19. Kerchner GA, Tartaglia MC, Boxer A. Abhorring the vacuum: use of Alzheimerʼs disease medications in frontotemporal dementia. Expert Rev Neurother 2011;11:709-717.
20. Ngo J, Holroyd-Leduc JM. Systematic review of recent demen-tia practice guidelines. Age Ageing 2015;44:25-33.
21. Tricco AC, Soobiah C, Berliner S, Ho JM, Ng CH, Ashoor HM, Chen MH, Hemmelgarn B, Straus SE. Efficacy and safety of cognitive enhancers for patients with mild cognitive impairment: a systematic review and meta-analysis. CMAJ 2013;185:1393-1401.
22. Emre M. Switching cholinesterase inhibitors in patients with Alzheimerʼs disease. Int J Clin Pract Suppl 2002;(127):64-72. 23. Rogawski MA, Wenk GL. The neuropharmacological basis for
the use of memantine in the treatment of Alzheimerʼs disease. CNS Drug Rev 2003;9:275-308.
24. Schneider LS, Dagerman KS, Higgins JP, McShane R. Lack of evidence for the efficacy of memantine in mild Alzheimer dis-ease. Arch Neurol 2011;68:991-998.
25. Tariot PN, Farlow MR, Grossberg GT, Graham SM, McDo-nald S, Gergel I; Memantine Study Group. Memantine treat-ment in patients with moderate to severe Alzheimer disease already receiving donepezil: a randomized controlled trial. JAMA 2004;291:317-324.
26. Howard R, McShane R, Lindesay J, Ritchie C, Baldwin A, Barber R, Burns A, Dening T, Findlay D, Holmes C, Hughes A, Jacoby R, Jones R, Jones R, McKeith I, Macharouthu A, OʼBrien J, Passmore P, Sheehan B, Juszczak E, Katona C, Hills R, Knapp M, Ballard C, Brown R, Banerjee S, Onions C, Griffin M, Adams J, Gray R, Johnson T, Bentham P, Phillips P. Donepezil and memantine for moderate-to-severe Alzhei-merʼs disease. N Engl J Med 2012;366:893-903.
27. Wilkinson D. A review of the effects of memantine on clinical progression in Alzheimerʼs disease. Int J Geriatr Psychiatry 2012;27:769-776.
28. Azermai M, Petrovic M, Elseviers MM, Bourgeois J, Van Bortel LM, Vander Stichele RH. Systematic appraisal of dementia guidelines for the management of behavioural and psychological symptoms. Ageing Res Rev 2012;11:78-86. 29. Trinh NH, Hoblyn J, Mohanty S, Yaffe K. Efficacy of
choline-sterase inhibitors in the treatment of neuropsychiatric symp-toms and functional impairment in Alzheimer disease: a meta-analysis. JAMA 2003;289:210-216.
30. Azermai M. Dealing with behavioral and psychological symp-toms of dementia: a general overview. Psychol Res Behav Manag 2015;8:181-185.
31. Wang F, Feng TY, Yang S, Preter M, Zhou JN, Wang XP. Drug therapy for behavioral and psychological symptoms of demen-tia. Curr Neuropharmacol 2016;14:307-313.
32. Katz IR, Jeste DV, Mintzer JE, Clyde C, Napolitano J, Brecher M. Comparison of risperidone and placebo for psychosis and behavioral disturbances associated with dementia: a ran-domized, double-blind trial. Risperidone Study Group. J Clin Psychiatry 1999;60:107-115.
33. Bains J, Birks J, Dening T. Antidepressants for treating depression in dementia. Cochrane Database Syst Rev 2002;(4): CD003944.
34. Tampi RR, Tampi DJ. Efficacy and tolerability of benzodia-zepines for the treatment of behavioral and psychological symptoms of dementia: a systematic review of randomized controlled trials. Am J Alzheimers Dis Other Demen 2014;29: 565-574.
35. Pinheiro D. [Anticonvulsant mood stabilizers in the treatment of behavioral and psychological symptoms of dementia (BPSD)]. Encephale 2008;34:409-415.
36. Farina N, Llewellyn D, Isaac MG, Tabet N. Vitamin E for Alzheimerʼs dementia and mild cognitive impairment. Coch-rane Database Syst Rev 2017;1:CD002854.
37. Dysken MW, Sano M, Asthana S, Vertrees JE, Pallaki M, Llorente M, Love S, Schellenberg GD, McCarten JR, Malphurs J, Prieto S, Chen P, Loreck DJ, Trapp G, Bakshi RS, Mintzer JE, Heidebrink JL, Vidal-Cardona A, Arroyo LM, Cruz AR, Zachariah S, Kowall NW, Chopra MP, Craft S, Thielke S, Turvey CL, Woodman C, Monnell KA, Gordon K, Tomaska J, Segal Y, Peduzzi PN, Guarino PD. Effect of vitamin E and memantine on functional decline in Alzheimer disease: the TEAM-AD VA cooperative randomized trial. JAMA 2014; 311:33-44.
38. Bjelakovic G, Nikolova D, Gluud LL, Simonetti RG, Gluud C. Antioxidant supplements for prevention of mortality in healthy participants and patients with various diseases. Coch-rane Database Syst Rev 2012;(3):CD007176.
39. Yuan Q, Wang CW, Shi J, Lin ZX. Effects of Ginkgo biloba on
dementia: an overview of systematic reviews. J Ethnophar-macol 2017;195:1-9.
40. Scapicchio PL. Revisiting choline alphoscerate profile: a new, perspective, role in dementia? Int J Neurosci 2013;123:444-449.
41. Gavrilova SI, Kolykhalov IV, Ponomareva EV, Fedorova YB, Selezneva ND. Clinical efficacy and safety of choline alfosce-rate in the treatment of late-onset cognitive impairment. Zh Nevrol Psikhiatr Im S S Korsakova 2018;118:45-53.
42. Burckhardt M, Herke M, Wustmann T, Watzke S, Langer G, Fink A. Omega-3 fatty acids for the treatment of dementia. Cochrane Database Syst Rev 2016;4:CD009002.
43. Mulnard RA, Cotman CW, Kawas C, van Dyck CH, Sano M, Doody R, Koss E, Pfeiffer E, Jin S, Gamst A, Grundman M, Thomas R, Thal LJ. Estrogen replacement therapy for treat-ment of mild to moderate Alzheimer disease: a randomized controlled trial. Alzheimerʼs Disease Cooperative Study. JAMA 2000;283:1007-1015.
44. Maki PM, Henderson VW. Hormone therapy, dementia, and cognition: the Womenʼs Health Initiative 10 years on. Climac-teric 2012;15:256-262.
45. King DS, Wilburn AJ, Wofford MR, Harrell TK, Lindley BJ, Jones DW. Cognitive impairment associated with atorvastatin and simvastatin. Pharmacotherapy 2003;23:1663-1667.
Peer Reviewers’ Commentary
이 논문은 현재 치매 환자에게 많이 처방되고 있는 대표적 약물 들인 아세틸콜린 분해효소 (acetylcholine esterase, AChE) 억제 제와 NMDA 수용체 억제제, 그리고 정신행동증상 치료제와 보 조 약물들에 대해 근거-기반 의학적 입장에서 정리해 주고 있다. 근거-기반 의학은 임상 연구 결과, 의사의 경험, 환자의 가치를 종합하여 최선의 판단을 내리고자 하는 것으로서, 이 논문에 정 리되어 있는 기존 임상 연구 결과들을 참고하면 적절한 치매 치 료제를 결정하는데 많은 도움이 될 것으로 기대된다. 특히, 흔하 게 처방되고 있는 약물들에 대해서는 용법, 용량, 그리고 부작용 대처법까지 자세하게 기술하고 있어 치매를 처음 진료하고자 하 는 의사들에게도 매우 유용할 것으로 판단된다. [정리: 편집위원회]