pISSN 1598-642X eISSN 2234-7305
표면적이 증가된 분별침전에 의한 paclitaxel의 입자 크기 감소
이지연·김진현*
공주대학교 화학공학부
Received : March 6, 2012 / Revised : April 4, 2012 / Accepted : April 5, 2012
Decrease in the Particle Size of Paclitaxel by Increased Surface Area Fractional Precipitation. Lee, Ji- Yeon and Jin-Hyun Kim*. Department of Chemical Engineering, Kongju National University, Cheonan 330- 717, Korea − In this study, we have for the first time applied increased surface area fractional precipitation in order to decrease the particle size of the anticancer agent paclitaxel from plant cell cultures. When compared with the case where no surface area increasing material was employed, the addition of ion exchange resin as a surface area increasing material resulted in a considerable decrease in the size of the paclitaxel precipitate.
When ion exchange resin was used, the paclitaxel particles were four to five times smaller, having less than a 20 µm radius, than those obtained in the absence of ion exchange resin. This is presumably because the growth of paclitaxel particles was impeded by the addition of ion exchange resin. The size of the paclitaxel precipitate also depended on the material used to increase the surface area, a result considered to be due to differences in the affinity between the particular ion exchange resin used and the paclitaxel particles. The yield of paclitaxel was significantly improved when ion exchange resin was used as a material to increase surface area. Pacli- taxel, with a reduced particle size due to the addition of a surface area increasing material during the fractional precipitation process, is believed to be particularly useful for practical applications of the drug.
Keywords: Paclitaxel, increased surface area fractional precipitation, ion exchange resin, particle size
Paclitaxel은 주목나무(yew tree)의 표피에서 발견된 diterpenoid 계열의 항암물질로 난소암, 유방암, 카포시 종양 (kaposi’s sarcoma), 비소세포성 폐암(non-small cell lung cancer, NSCLC)치료에 대해 FDA(Food and Drug Adminis- tration) 허가를 취득하여 현재 가장 중요한 항암제로 사용되 고 있다[6,10]. 또한 류마티스성 관절염, 알츠하이머 치료 등 의 적응증이 계속 확대되고 여러 다른 치료 방법들과의 복 합처방에 관한 임상시험이 진행 중에 있어 향후 paclitaxel 수요는 계속 늘어날 전망이다.
일반적으로 원료의약품(active pharmaceutical ingredient, API)의 경우 입자 크기를 작게 하여 그 활용도를 높이고자 한다. 입자 크기가 작아질수록 제형 시 용해 속도(dissolution rate), 약물 분산의 균일성(uniformity of drug dispersion), 경구 생체 이용률(oral bioavailability) 등을 향상시킬 수 있 는 장점을 가지고 있기 때문이다[2, 19]. 또한 결정 입자 크 기가 작을수록 정제 후 건조 단계에서 잔류수분 및 잔류용 매 제거에도 상당히 도움이 되기 때문이다[14]. 이러한 측면 에서 본 연구결과인 분별침전공정에서 표면적 증가물질에
의한 paclitaxel 입자 크기의 감소는 의약품의 활용 측면에서 도 유용하게 활용될 수 있을 것으로 판단된다.
입자 크기를 줄이기 위하여 wet milling이나 높은 압력으 로 균질화(high-pressure homogenization)하는 방법이 많이 연구되고 있으나, 많은 시간과 에너지가 요구되며 계면활성 제를 사용하여 제조된 입자를 안정화(응집 방지)시켜야 하는 번거로움도 있다[16]. 또한 입자 크기, 형태, 결정도와 같은 입자의 특성을 조절하기 위하여 결정화, 침전, 용매증발 방 법 등이 보고되고 있다[1, 17, 18]. 하지만 이러한 공정들은 단일공정이지만 낮은 수율과 열에 민감한 의약품의 분해되 는 현상 등 단점이 있다. 또한 나노입자 제조를 위한 다양한 초임계 유체 공정이 보고되었지만 고압 펌프, 온도, 노즐의 경우 높은 압력을 요구하기 때문에 비용이 많이 든다는 단 점이 있다[9].
분별침전 공정은 항암제 paclitaxel을 효율적으로 분리/정 제할 수 있는 매우 간편한 방법으로, 용해도 차이를 이용하 여 높은 순도의 paclitaxel을 고수율로 얻을 수 있는 대표적 인 전 처리 공정으로 사용되어 왔다[5, 7, 8, 11, 15]. 본 연구 에서는 기존의 분별침전공정에서 표면적을 증가시켜 항암물 질 paclitaxel의 입자 크기를 매우 간편하게 감소시키는데 최 초로 활용하고자 하였다. 즉, 표면적 증가물질인 다양한 종 류의 이온교환수지(Amberlite IR 120 H, Amberlite IR 120
*Corresponding author
Tel: +82-41-521-9361, Fax: +82-41-554-2640 E-mail: jinhyun@kongju.ac.kr
으로부터 얻은 세포주(cell line)를 이용하여 배양하였다. T.
chinensis로부터 기원된 현탁액 세포는 24oC 암조건(darkness condition)에서 150 rpm으로 교반하여 배양하였다. 현탁 (suspension) 세포는 수정된 Gambor’s B5 배지, 30 g/L sucrose, 10µm NAA(naphthalene acetic acid), 0.2 µm BA (6-benzylaminopurine), 1 g/L casein hydrolysate, 1 g/L 2- [N-morpholino]ethansulfonicaid(MES)에서 배양하였다. 세포 배양은 2주마다 새로운 배지(medium)로 갈아주었으며 생산 과 배양을 연장시키기 위해 7일과 21일째 되는 날에 1~2%
의 말토오스를 첨가해 주고 elicitor로서 배양 초기에 4 µm 의 AgNO3를 첨가해 주었다[3]. 식물세포배양 후 배양액으 로부터 decanter(Westfalia, CA150 Claritying Decanter)와 고속 원심분리기(α-Laval, BTPX205GD-35CDEEP)를 이용 하여 식물세포와 세포조각(cell debris)을 회수하였다. 식물 세포와 세포조각을 합하여 바이오매스라 하며 ㈜삼양제넥스 에서 제공 받았다.
Paclitaxel 함량 분석을 위해 HPLC 시스템(SCL-10AVP, Shimadzu, Japan)과 Capcell Pak C18 컬럼(250 mm × 4.6 mm; Shiseido, Japan)을 사용하였다. 이동상은 아세토나이트 릴과 증류수 혼합용액(35/65~65/35, v/v, gradient mode)을 유속 1.0 mL/min으로 흘려주었다. 시료 주입양은 20 µL이며 227 nm에서 UV detector에 의해 검출하였다. HPLC 분석은 표준정량곡선을 이용하였으며 표준시료는 Sigma-Aldrich 제 품(순도: 97%)을 사용하였다[13].
식물세포배양액으로부터 회수한 바이오매스와 메탄올의 비율을 1/1(w/v)로 하여 실온(room temperature)에서 4회 반 복 추출하고 추출액을 rotary evaporator(CCA-1100, EYELA, Japan)를 이용하여 농축(원액의 30%)하여 액-액 추출을 수 행하였다. 농축된 메탄올 용액에 메틸렌 클로라이드을 첨가 (메탄올 농축액의 25%)하고, 30 min 동안 교반 후 정체시켜 상 분리를 유도하였다. 액-액 추출을 수행하여 paclitaxel이 포함된 하층인 메틸렌 클로라이드 층으로 paclitaxel을 회수 하여 농축하고 여과지(150 mm, Whatman)로 감압 여과 후 건조하였다. 식물세포 유래 타르/왁스 성분을 제거하기 위하 여 건조된 추출물(crude extract)를 메틸렌 클로라이드에 20%
(v/w) 비율로 녹이고 흡착제(adsorbent)인 sylopute(Fuji Silysia Chemical Ltd., Japan)를 건조된 추출물 대비 50%
(w/w) 비율로 첨가하여 40oC 항온조(PS-1000, EYELA, Japan)에서 30 min동안 교반 하며 반응시킨 후 여과하였다.
여과액은 30oC, 감압상태에서 건조하여 헥산 침전 공정에 이 용하였다. 건조된 시료를 메틸렌 클로라이드에 녹여 헥산에 떨어뜨려 침전을 유도하여 비극성불순물(non-polar impurity)
까지 한 방울씩 천천히 증류수를 떨어뜨린 후 4oC에서 냉장 보관하여 paclitaxel 침전물을 얻었다. 침전 후 침전물을 여과 하고 35oC에서 24 hr 동안 진공 건조하였다. 그리고 HPLC 정제 공정은 ODS C18 컬럼(50 mm × 500 mm, Shiseido, Japan)과 Silica 컬럼(50 mm × 500 mm, Shiseido, Japan)공정 으로 구성되었다. 먼저 ODS 컬럼 HPLC에서 시료 주입량은 50~150 mg/mL(메탄올), 유속은 3~5 cm/min, UV detector의 파장은 227 nm, 용리(elution) 조건은 메탄올/물(65/35, v/v) 로 하였다. 그리고 미량의 불순물들을 제거하기 위한 silica 컬럼 HPLC에서는 시료 주입량은 50~150 mg/mL(메틸렌 클 로라이드), 용리 조건은 메틸렌 클로라이드/메탄올(98/2, v/
v)로 하였으며 UV detector의 파장은 227 nm에서 측정하였 다[8]. 최종 정제된 paclitaxel 순도는 98.7%이었다. 본 연구 의 분별침전을 위한 시료 준비 과정을 나타내었다(Fig. 1).
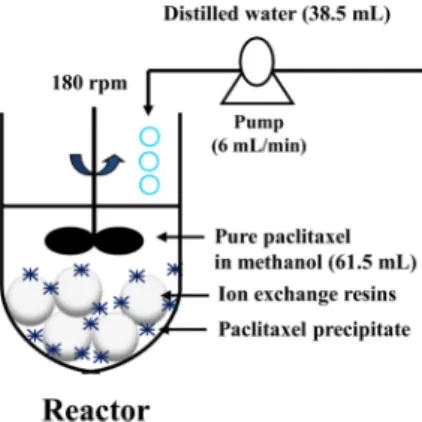
Paclitaxel 입자의 크기 감소를 위한 표면적이 증가된 분 별침전 공정의 개략도를 나타내었다(Fig. 2). 반응액 부피당 표면적(S/V) 증가를 위해 양이온교환수지(Amberlite IR 120 H, Amberlite IR 120 Na, Amberlite 200, Sigma-Aldrich) 와 음이온교환수지(Amberlite IRA 400 OH, Amberlite IRA 400 Cl, Amberlite IRA 910, Sigma-Aldrich)를 각각 사용하였다. 이온교환수지는 35oC에서 하루 동안 건조한 후 실험에 사용하였다. 시료(순수한 paclitaxel의 함량 0.3%, w/
v) 를 메탄올에 녹이고 메탄올이 61.5%가 될 때까지 증류수 를 교반(180 rpm) 하에 한 방울씩 떨어뜨렸다[11]. 그리고 반 응액 부피 당 표면적을 증가시켜 입자의 성장을 저해하기 위 해 이온교환수지를 넣은 후 4oC에서 항온 항습기(KCL- 2000W, EYELA, Japan)에 보관하여 paclitaxel 침전물을 얻 었다. 반응액 부피 당 표면적(S/V)은 선행연구[7]에서 최적 화한 0.428 mm-1으로 고정하여 실험을 수행하였다. 침전 후 침전물을 여과하고 35oC에서 24 hr 동안 진공오븐(UP-2000, EYELA, Japan)에서 건조하였다. 건조된 침전물의 순도와 수 율은 HPLC로 분석하였다.
분별침전 공정에서 paclitaxel 침전물 형태 및 크기를 측 정하기 위해 전자현미경, SV-35 Video Microscope 시스템 (Some Tech., Korea)을 사용하였다[7]. 분별침전 동안 paclitaxel 침전물을 고배율(×100)에서 관찰하였다. 관찰된 paclitaxel 침전물은 IT-Plus 시스템(Some Tech., Korea)에서 동화상으로 확인하였으며 이를 통해 paclitaxel 침전물의 형 태를 확인하고 크기를 측정하였다.
항암물질 paclitaxel의 입자 크기를 감소시키기 위하여 표 면적이 증가된 분별침전을 최초로 응용하였다. 표면적이 증 가된 분별침전에서 침전시간에 따른 침전 양상(paclitaxel 입
자 형태 및 크기, 수율, 순도)에 미치는 영향을 조사하였다.
문헌보고에 의하면, 시료의 순도와 분별침전 시 메탄올 용 액에 녹이는 순수한 paclitaxel의 함량이 증가할수록 과포화 도가 높아져 더 빠른 시간 안에 paclitaxel 침전물을 얻을 수 있음을 알 수 있었다[7]. 따라서 순도 98.7%의 경우 순수한 paclitaxel의 함량 0.4% 이상에서는 침전물이 쉽게 뭉쳐 입 자의 형태 조절에 어려움이 있어(data not shown), 순수한 paclitaxel의 함량 0.3%, (w/v)에서 침전물의 크기를 감소시
키기 위한 분별침전을 수행하였다. 여러 가지 이온교환수지 (Amberlite IR 120 H, Amberlite IR 120 Na, Amberlite 200, Amberlite IRA 400 OH, Amberlite IRA 400 Cl, Amberlite IRA 910)를 사용하여 반응액 부피당 표면적 (surface area per working volume(i.e. volume of reaction solution), S/V)을 증가시켜 분별침전을 수행하였다. 침전 시 간이 경과함에 따라 paclitaxel 침전물의 형태를 전자현미경 을 사용하여 관찰한 결과, 표면적 증가물질을 첨가하지 않 은 경우(Fig. 3A)에는 침전시간 경과에 따라 침전물의 크기 가 점점 커지는 반면 이온교환수지를 첨가한 경우(Fig.
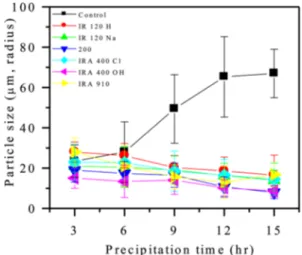
3B~Fig. 3G)에는 침전물 크기가 오히려 작아지는 경향을 나 타내었다. 이러한 결과는 고분자물질 또는 계면활성제를 이 용하여 표면적을 증가시켜 입자의 크기를 감소시킨 연구결 과와 일치하는 것을 알 수 있었다[2]. 또한 침전물의 크기를 각각 측정하여 Fig. 4에 나타내었다. 표면적 증가물질을 첨 가하지 않은 경우 분별침전 시간이 경과할수록 입자 크기가 커지는 반면 이온교환수지를 첨가하였을 경우 표면적 증가 물질과 핵의 충돌 주기가 증가되어 많은 핵이 생성[12]됨에 따라 침전물의 크기가 작아지는 것을 알 수 있었다. 이온교 환수지를 이용하여 표면적이 증가된 경우 표면적 증가물질 을 첨가하지 않을 경우에 비해 4~5배 더 작은 paclitaxel 입 자(<20 µm radius)를 얻을 수 있었다. 이온교환수지 종류에 Fig. 2. Schematic diagram of increased surface area fractional
precipitation with an ion exchange resin in order to decrease the particle size of paclitaxel.
Fig. 1. Preparation of samples for increased surface area fractional precipitation.
따라 paclitaxel 침전물의 크기에 차이를 보였는데 이는 표면 적 증가물질과 paclitaxel 입자와의 친화력(affinity) 차이 때 문으로 판단된다[2, 4, 20]. 즉, 표면적 증가물질과 paclitaxel 입자와의 친화력이 증가할수록 paclitaxel 입자 성장을 저해 하는 더 효과적인 공간적 저해요소(steric barrier) 역할을 하 기 때문에 침전물의 크기가 감소하게 된다. 일반적으로 원 료의약품(active pharmaceutical ingredient, API)의 경우 입 자 크기를 작게 하여 그 활용도를 높이고자 한다. 입자 크기
가 작아질수록 제형 시 용해 속도(dissolution rate), 약물 분 산의 균일성(uniformity of drug dispersion), 경구 생체 이용 률(oral bioavailability) 등을 향상시킬 수 있는 장점을 가지 고 있기 때문이다[19]. 또한 결정 입자 크기가 작을수록 정 제 후 건조 단계에서 잔류수분 및 잔류용매 제거에도 상당 히 도움이 되기 때문이다[14]. 이러한 측면에서 본 연구결과 인 분별침전공정에서 표면적 증가물질에 의한 paclitaxel 입 자 크기의 감소는 의약품의 활용 측면에서도 유용하게 사용 Fig. 3. Electron micrograph of paclitaxel precipitates formed by fractional precipitation at 3 hr~15 hr: Control (A); cation exchange resins Amberlite IR 120 H (B); Amberlite IR 120 Na (C) and Amberlite 200 (D); anion exchange resins Amberlite IRA 400 Cl (E);
Amberlite IRA 400 OH (F) and Amberlite IRA 910 (G). The pure paclitaxel content and purity of crude extract were 0.3% (w/v) and 98.7%, respectively. Scale bar indicates 10 µm.
될 수 있을 것으로 판단된다. 분별침전 시간 경과에 따라 paclitaxel 수율을 확인한 결과, 동일한 분별침전 시간에서 표 면적 증가물질을 첨가하였을 경우에 더 높은 수율을 얻을 수 있었다. 이러한 결과는 표면적 증가물질을 첨가할 경우 분 별침전에 소요되는 시간을 단축시킬 수 있음을 의미한다. 또 한 paclitaxel 순도는 거의 변함이 없음을 알 수 있었다(Fig.
5).
Acknowledgment
This work was supported by a National Research Foun- dation of Korea (NRF) grant funded by the Korean govern- ment (MEST) (No. 2011-0010907).
R
EFERENCES1. Chen, X., T. J. Young, M. Sarkari, R. O. Williams, and K. P.
Johnston. 2002. Preparation of cyclosporine A nanoparticles by evaporative precipitation into aqueous solution. Int. J.
Pharm. 242: 3-14.
2. Cho, E. B., W. K. Cho, K. H. Cha, and J. S. Park. 2010.
Enhanced dissolution of megestrol acetate microcrystals prepared by antisolvent precipitation process using hydro- philic additives. Int. J. Pharm. 396: 91-98.
3. Choi, H. K., T. L. Adams, R. W. Stahlhut, S. I. Kim, J. H.
Yun, B. K. Song, J. H. Kim, S. S. Hong, and H. S. Lee.
1999. Method for mass production of taxol by semi- continuous culture with Taxus chinensis cell culture. US Patent 5,871,979.
4. Dong, Y., W. K. Ng, S. Shen, S. Kim, and R. B. H. Tan.
2009. Preparation and characterization of spironolactone nanoparticles by antisolvent precipitation. Int. J. Pharm.
375: 84-88.
5. Han, M. G., K. Y. Jeon, S. Y. Mun, and J. H. Kim. 2010.
Development of a micelle-fractional precipitation hybrid process for the pre-purification of paclitaxel from plant cell cultures. Process Biochem. 45: 1368-1374.
6. Jeon, K. Y and J. H. Kim. 2008. Effect of surfactant on the micelle process for the pre-purification of paclitaxel. Kor. J.
Biotechnol. Bioeng. 23: 557-560.
7. Jeon, K. Y and J. H. Kim. 2009. Improvement of fractional precipitation process for pre-purification of paclitaxel.
Process Biochem. 44: 736-741.
8. Jeon, S. I., S. Y. Mun, J. H. Kim. 2006. Optimal temperature control in fractional precipitation for paclitaxel pre-purifi- cation. Process Biochem. 41: 276-280.
9. Kawashima, Y and P. York. 2008. Drug delivery applications of supercritical fluid technology. Adv. Drug Deliv. Rev. 60:
297-298.
10. Kim, J. H. 2006. Paclitaxel: recovery and purification in commercialization step. Kor. J. Biotechnol. Bioeng. 21: 1-10.
11. Kim, J. H., I. S. Kang, H. K. Choi, S. S. Hong, H. S. Lee.
Fig. 4. Effect of ion exchange resin used to increase surface area per working volume (S/V: 0.428 mm-1) on the particle size of paclitaxel during fractional precipitation. The pure paclitaxel purity, methanol composition in water, pure paclitaxel content, and precipitation temperature were 98.7%, 61.5% (v/v), 0.3% (w/v) and 4oC, respectively.
Fig. 5. Effect of yield and purity by using the ion exchange res- ins to increase surface area per working volume (S/V: 0.428 mm-1) on the precipitation time of paclitaxel during fractional precipitation. The pure paclitaxel contents, methanol composition in water, pure paclitaxel purity and precipitation temperature were 0.3% (w/v), 61.5% (v/v), 98.7% and 4oC, respectively.
3448.
13. Lee, J. Y. and J. H. Kim. 2011. Development and optimiza- tion of a novel simultaneous microwave-assisted extraction and adsorbent treatment process for separation and recovery of paclitaxel from plant cell cultures. Sep. Purif. Technol. 80:
240-245.
14. Pyo, S. H., M. S. Kim, J. S. Cho, B. K. Song, B. H. Han, and H. J. Choi. 2005. Efficient purification and morphology characterization of paclitaxel from cell cultures of Taxus chinensis. J. Chem. Technol. Biotechnol. 79: 1162-1168.
15. Pyo, S. H., H. B. Park, B. K. Song, B. H. Han, and J. H.
Kim. 2004. A large-scale purification of paclitaxel from cell
17. Vehring, R. 2008. Pharmaceutical particle engineering via spray drying. Pharm. Res. 25: 999-1022.
18. Weers, J. G., T. E. Tarara, and A. R. Clark. 2007. Design of fine particles for pulmonary drug delivery. Expert Opin.
Drug Deliv. 4: 297-313.
19. Yeo, S. D., M. S. Kim, and J. Lee. 2003. Recrystallization of sulfathiazole and chlorpropamide using the supercritical fluid antisolvent process. J. Supercrit. Fluids 25: 143-154.
20. Zhang, H. X., J. X. Wang, Z. B. Zhang, Y. Le, Z. G. Shen, and J. F. Chen. 2009. Micronization of atorvastatin calcium by antisolvent precipitation process. Int. J. Pharm. 374: 106- 113.