임상병리검사과학회지 : 제 28권 제 1 호
1996.
Line Probe Assay를 이 용한 Rifampicin 내 성 결핵균의 신속한 검출
서울의과학연구소 · 서울임상병리검사센터 (SCL) 검은하·주은미·박영석·이규범
Rapid Detection of Rifampicin - Resistant Mycobacterium tuberculosis Using Line Probe Assay
Kim
,Eun-Ha.
,Joo
,Eun-M
i.,Park
,Young-Su
k.,Lee
,Kyu-Pum
Se
oul Medical Scienæ Institute . Seoul Clinical Laboratories( SCL)
Control of tuberculosis are compromised by the increased frequency of multidrug - re- sistant strains of Mycobacterium tuberculosis(M. tuberculosis). Rifampicin is a key compo nent of therapeutic regimens. Resistance to rifampicin results from the substitution of a limited number of highly conserved amino acids encoded by rpo
βthe gene for the ß- subunit of the RNA polymerase. In present study , nested - PCR coupled line probe assay methods were used for rapid detection of rifampicin resistant strain in PCR positive samples with M. tuberculosis. In a total of 10 nested - PCR M. tuberculosis positive sam- ples
,including 8 sputums
,1 pleural fluid and 1 urine
,three rifampicin resistant strains (30%) were detected. Among these, one mutation was found in Sl locus of rpo ß gene, and other two mutations were observed in coinfection state of S2/R5 loci and S4/R4a loci , respectively. This study shows that nested - PCR coupled line probe assay is a rela- tively simple , fast and practical tool for the detection rifampicin resistant M. tuberculosis strains in the routine clinical laboratory wor
k.Key words : Mycobacterium tubercu/osís. rifampicin resistant
, p이 ymerasechain reaction
,line probe assay
1 .
서 론결핵은 1985년까지는 감소하는 추세였으나,
1991 년 이후 단일 결핵균에 의한 감염이 아닌 다약제 내성을 가진 균주가 출현하고, 후천성
면역 결핍증과 결핵의 동시 감염 등 선진국뿐 만 아니라 개발도상국에서도 크게 증가하고 있 다 8, 22) 최근, 감염증 분야에서 획기적인 진단 방법으로 널리 사용되고 있는 최신 분자생물학 적 기법인 중합효소연쇄반응 (PCR) 을 이용한
R4a
R2 R5
S2 54
SI S3 S5
511 513 516 518 앓2 526 531 앓3
C AGC CAG CIG AGC ser Gln 낼앤 Ser 핸~ G멘 phe 빼t ~헬 TTC ATG GAC CAG Gln ~얀 핸!l Asn Pro Leu AAC CCG CTG TgG GGG TTG ACC 훌r GIy Leu Thr Q띤 땐 MG CGC CGA CTG Lys Arg Arg Leu 1윌 활 GCG. CIG GGG C 깨a 낼J,! GIy
Pro Leu V머 (de’) Leu Tyr Trp Pro
A~ Leu
Fig. 1. Wild - type nucleotide and aminoacid sequence of the relevant part of the rpo β
gene.
The positions involved in rifampicin - resistance inducing mutations are underlined. The oligonucleotide probes on the LiP A strips are indicated by horizontal bar.
결핵균 검출에 대한 보고가 다양한 방면에서 활발하게 이루어 지고 있다1. 2) 이 방법은 검체 에 포함된 결핵균 특정 DNA를 수백만 배 이 상 증폭시키는 것으로, 기존에 결핵균 검출을 위해 이용되어 왔던 여러 가지 방법보다 예민 도, 특이도가 월등히 높은 검출 방법이다. 또한 기본적으로 4---8주가 소요되는 결핵균 배양과 정을 거치지 않고 검체로부터 직접 균의 존재 유무를 검출 할 수 있는 신속한 임상실험실 진 단 기법으로서, 본 연구소에서도 이미 그 유용 성에 대해 보고한 바가 있다6.7) 이러한
PCR
반응을 이용하여 결핵균의 빠른 검출이 가능하 게 되었으나, 다약제 내성 검사는 아직까지 배 양법에 의존하고 있는 실정이다 9.14) 다약제 내 성균주의 대표적인 균주인rifampicin
내성 결 핵 균주는, 결핵균 치료를 위해 사용하는 중요 한 조기치료 항결핵제인isoniazid
내성을 동반 하므로, 임상에서rifampicin
내성 결핵균을 조 기에 정확히 검출하는 것은 매우 중요하나lOl9) , 최근까지 임상검체에서 직접rifampicin
내성 결핵균을 검출한 보고는 많지 않다. 본 연구에서는
2
차 중합효소 연쇄반응 (2차 PCR) 과re- verse dot - blot
원 리 를 이 용한line probe assay
방법을 동시에 사용하여rifampicin
내성 결핵균 을 간단하고 신속하게 검출하여 그 결과를 얻 었기에 보고하는 바이다.II.
실험재료 및 방법1.
실험 재료임상 검체로는 결핵으로 의심되는 환자로서 본 기관에 의뢰된 검체 중 양성으로 판명된 10예(객담 8예, 늑막액 1 예, 소변 1예)를 대상 으로 실시하였다. 시약으로 agarose는 미국 FMC사의 제품을 사용하였으며, 제한효소, 전기 영 동
marker ,
Taq polymerase는 미 국Promega
사의 제 품을 사용하였다.PCR
primer 는rifam- plcm
내성 결핵균주에 특이한RN A polymerase
subunit(
rpo 껴) 유전자 부위에서 선택하였다(Fig. 1
)20).Line probe assay
kit는INNO
LiP A rifampicin TB kit
(Innogenetics Co. Bel-
gium) 를 사용하였다.2.
실험 방법1) 검체로부터 결핵균 DNA의 추출
결핵균
DNA
추출에는 일반적으로 사용되고 있는proteinase K/phenol
방법 을 이 용하였 으 며, 검체의 종류에 따라 전처리 과정을 달리 하였다. 객담은 점성이 높기 때문에4N NaOH
와 동량의 검체를 혼합하여 점도를 저하시킨 뒤3
,800
rpm으로 원심분리 후 상충액을 제거 하였고, 늑막액과 소변은4N NaOH
처리를 하 지 않고 바로3
,800
rpm에서 원심분리 후 상충 액을 제거한 뒤, 각 침전물을 세포 용해 완충 액(50 mM Tris-HCl
,pH 7.5
,1 mM EDTA
,1
% Triton X -100) 200
띠와 섞은 다음pro- teinase
K를 최 종 농도가400
땅Iml이 되 도록 혼합하여 370C 에서 1 시간 이상 방치하였다. 이 어phenol/ chlorof
orm을 동량을 넣고1
분간 섞 은 후12
,000
rpm에서10
분간 원심분리를 하고 상충액 을 취 해 다시 chloroform을 넣 고 같은 방 법으로 원심분리를 하였다. 원심분리 후 상충액 을 취 하여0.2 M sodium
acetate와 2배 부피 의100%
에탄올을 넣어 섞은 다음 -200C 에서 1 시 간 이상 방치하였다. 다음으로18
,000
rpm에서 20분간 원심분리 후 침전물을70%
에탄올로 세척하고 원심분리를 한 후 침전물을 건조하였 다. 건조된 침전물을TE
완충액 (TrisEDTA
,pH
7.6) 에 재용해시키고 그 중 일부를 PCR에 사용하였다.2)
1 차 및 2차 중합 효소 연 해 반응PCR
반응의 최종액은 50 여로 하였으며, 반응액 은50 mM KCl , 10 mM Tris - HC
l(pH 8.3) , 2.2 mM MgCl
2, 200 mM
dNTP와1
UTaq polymer-
ase를 사용하였다.
Primer
농도는 l 차 PCR에 서10 pmol
, 2차 PCR에 서 는25
pmol을 사용하 였다.PCR
반응은 1 차 PCR에서 950C 에서1
분, 500C 에서 1 분 30초, 720C 에서 2 분으로
30
회 실시하였다. 그리고 2차 PCR은 950C 에서
1
분, 500C 에서 1 분 30초, 720C 에서 2분동안
30
회 를 자 동
thermal cycler( GeneAmp PCR sys-
tem 480
,Perkin Elmer Cetus
Inc.) 를 이 용하여 증폭하였다.3) Agarose gel
전 기 영 동 및DNA
band의 분석PCR
반응의 확인 을 위 하여 증폭된DNA 10
띠에2
띠의loading buffer( 0.25 % bromo phenol blue , 0.25% xylene cyanol FF , 15%
Ficoll
400) 를 넣은 다음,100
volt에서 30분 동 안2 % agarose gel
전기 영동을 실시하였다.그 후
ethidium
bromide로 염색하여 1 차PCR
에서는
395 bp
, 2차 PCR에서는257 bp
크기의DNA
band를uv
상에서 확인하였다.4) Line Probe Assay
증폭된
PCR
산물10
여를denaturation
용액 10 띠에 담가 200C 에서5
분간 방치한 후 미리 가열한hybridization
용액을1 ml
넣고 혼합하 였다. 다음으로LiPA
strip을 넣고 620C 에서30
분간 방치시킨 다음, 미리 가열한stringent
세척 용액
1
ml로 1 분간 2회 세척하였다. 그 후stringent
세척 용액을1 ml
넣은 뒤 620C 에 서 10 분간 방치 한 후,1
ml의rmse
용액 으로 2회 strip을 세척하고1
ml의conjugate
용액을 넣은 후, 250C 에서 30분간 방치하였다. 이것을1 ml rinse
용액 으로 2회, 1 ml substrate
완충 용액으로1
회 세척한 뒤1 ml substrate
완충 용액 을 가한 다음20
0C --25
0C
온도로 30분간 방치하였다. 마지막으로 멸균한 증류수로 씻어 주고 나서20 0
C -- 25 Oc
온도로 5 분간 방치한 후 결과를 판독하였다.III.
실험성적10예의 임상 검체에서 직접 DNA를 추출 한 후
INNO LiPA rifampicin TB
kit에 포함된1
차
primer(OP1
,OP2)
쌍으로 1 차 PCR을 한 다음, 2차PCR primer
(lP1
,IP2)
쌍으로 2 차 PCR을 실행한 결과2 % agarose gel
상에서10
검체 모두257
bp 의 결핵균 특이DNA
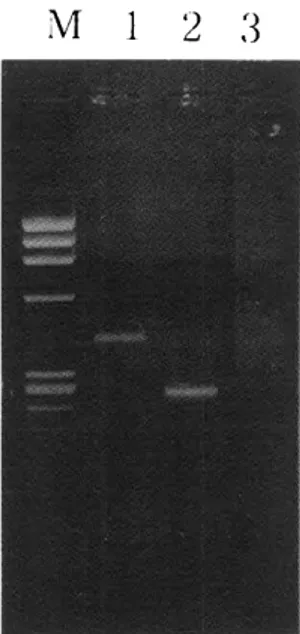
M 1 2 :3
Fig. 2. Amplified DNA products of first PCR and second PCR in rpo
βregion of M tuberculosis.
M : Molecular standard marker(PhiX174/Hae
m)Lane 1 : Amplified product of rpo
βgene by first
PCR(395bp)
Lane 2 : Amplified product of rpo
βgene by sec- ond PCR (25 7bp)
Lane 3 : Negative control
Fig. 3. The strains of rifampicin-resistant
M.tu- berculosis detected by line probe assay system.
Lane 1 : Rifampicin
rstrain : Sl mutation
Lane 2: Rifampicin
rstrain: S4/R4a coinfection mutat
lOn
Lane 3: Rifampicin
rstrain: S2/R5 double muta-
tlOnLane 4-10 : Rifampicin
sstrains
가 확인 된 2차 PCR의 증폭 산물로
reverse dot
hybridization을 실 시 한 결 과, 3예(30%)
에 서rpo
β 유전자에 돌연변이가 일어난 것을 확 인하였다 (Fig.3). 이들 중 한 예는Sl
위치에 서 돌연변이가 일어났음을 알 수 있었고, 또 한 예에서는S4/R4a
위치에서 이중 돌연변이 가 검출되었는데 이것은codon
526 에서 아미 노산histidine
(His) 이 tyrosine(Tyr) 으로 바뀐 경우이다. 나머지 세 번째 예에서는codon 531
에서 아미 노산serine ( Ser
)이leucine
(Leu) 으로바뀌어
S2/R5
위치에서 이중 돌연변이가 일어났음을 알 수 있었다. 본 실험 결과, 2차 PCR과
reverse dot
방법 을 이 용한line probe
assay를 사용하여 임상 검체로부터 신속하고 정확하게rifampicin
내성 결핵균을 검출할 수 있었으며,나아가 이 방법은 향후 임상 검사실에서
rifampi- cm
내성 결핵균의 신속한 진단 방법으로 유용하 게 사용될 수 있을 것으로 사료된다.N. 고 찰
활동성 폐결핵을 가진 환자로부터 다약제 내 성을 가진 결핵균의 증명은 매우 중요한 임상 적 의의를 지닌다 26) 지금까지는 배양에 의한 약제 감수성 검사l2, l4) , 또는 방사선 측정 배양 방법 l3)
,
혹은Bactec 460
기 기 를 이 용한 감수 성 검사 방법 l8, 23) , 결핵균에 대한 특이 항체를 사용하여 결핵균 항원의 양을 측정하는 효소면 역 법 등 17) 을 사용하였다. 이 러 한 방법 들은 검 사 기간이 길다는 단점외에도 고가의 장비와 시약, 결핵균 이외의 오염균에 의한 비특이적 인 반응을 나타낼 수 있는 등 다소 문제점이 있다. 또한 검체의 전처리에 사용되는 화학 물 질에 의한 항원의 변성될 가능성이 있으며, 균 수가 적은 뇌척수액과 같은 임상 검체의 경우 분리가 어렵다는 점들이 지적 되고 있다. 한편 항결핵제를 사용하여 결핵균을 배양했을 때 균 의 성장 정도를 rRNA의 양으로 추정할 수 있 는 방법이 보고되고 있는데, 이는 배양 후3--
5 일 내에 결과 판정이 가능하나, 동위원소의 짧은 반감기 문제와 고가의 장비가 필요하고
M.
tuberculosis와M.
bovis를 구별하기 힘들며,결핵균주가 ml당
6
X10
7 이상이 되어야 검출 이 가능하다는 단점이 있다15) 본 실험에서는DNA
수준에서rifampicin
내성 결핵균을 검출 하기 위하여 임상 검체로부터 직접line probe
assay 를 실시하였다. 이 방법의 원리 는
rifam- picin
내 성 기 전 의 원 인 인RN A polymerase subunit(
rpoß)
유전자 부위에서 선택된2
쌍의 pnmer를 이용하여 2차 PCR을 실시하고 증폭 된 산물을nitrocellulose membrane
strip에 고 정 시 킨10
개 의oligonucleotide
set에 교 잡(hyb
ridization) 하여 그 변이를 검출하는 것이다.
Inno LiP A
strip에는 결핵균의 rpo 껴 유전자의 정상적인 염기서열을 갖는81-85
probe와, 빈 번한 돌연변이가 일어나는 부분의 염기서열을갖는
R2-R5
probe가 미리 고정되어 있으므로, 이 부분의 돌연변이의 검출이 가능하다
(Fig.
1).Rifampicin의 작용은 rpo ß 유전자에 의해 암 호화 되 는
RN A
polymerase의 껴-subunit 부 근에서 조절되는데, 이RN A polymerase ß-
subunit
내에서 돌연변이 (아미 노산의 변화)가일어나면
rifampicin
내성이 생기게 된다 11 , 16, 21 ) 즉 , rpo ß유전자의72
염기 배열내에서 돌연변 이가 일어나는 경우 rifampicin에 대한 민감성 이 상실되어 내성 균주가 된다 24) Rifampicin은lipophilic
ansamycin으로서 소수성 인 세 포벽 을 잘 침투하기 때문에 결핵균에 대해 매우 높은 항균 효과를 나타내므로 조기 치료 항결핵제로 서 사용되는데,rifampicin
내성인 결핵균주들 이 대부분 rpo β 유전자의 돌연 변이를 가지고 있고,rifampicin
내성을 보이는 균주와 다약제 내성을 보이는 결핵균주의 유전적 변이가 거의 일치하므로 , rpo ß유전자의 돌연변이 가rifampi cm
내성의 표지자로서 충분한 의의가 있음이 입 증되 었 다 24, 25) 또한rifampicin
내 성 을 가진 결핵균은 대부분 다른 주요 조기 치료 항결핵 제인isoniazid
내성을 동반하므로 다약제 내성의 표지로써 그 임상적 의의가 크다 27) 본 실 험 에 서 사용한
line probe
assay는 기 존 방법 에 비하여, 방사성 동위원소의 사용이 없고, 빠른 시간 내에DNA
수준에서rifampicin
내성 결 핵균의 검출이 가능하였다. 본 실험에서 고려 해 볼 수 있는 점은, 결핵균PCR
검사를 위해 본 연구소에 의뢰된 임상 검체 중 무작위로 10예의 검체를 선택하여 실험을 실시한 결과3
예 (30%) 에서
rifampicin
내성 결핵균으로 나타 나, 일반적으로 예상되는 것 보다 많은rifam- p
lCm 내성 결핵 균주가 존재함을 알 수 있었 다. 따라서 향후 결핵의 진단에서 결핵균PCR
검사가 양성인 검체의 경우
rifampicin
내성 결 핵균 검사를 동시에 실시한다면, 시간을 절약 할 수 있고 결핵의 진단 및 치료와 예후 추정 에 있어서 많은 도움이 될 수 있을 것이다.v.
결 론Rifampicin
내성 결핵균을 검출하기 위하여,10예의 임상 검체로부터 직접
PCR
증폭 산물 을 얻은 후reverse dot - blot
원리를 이용한line probe
assay를 실시한 결과, rpo 껴 유전자 의81
위치,84/R4a
그리고82/R5
지역에서 돌연변이가 일어난3
예의 내성 균주를 검출할 수 있었다. 본 실혐의 결과로 볼 때, 2차PCR
을 이 용한line probe
assay는 임 상 검 체 로부터 직접rifampicin
내성 균주의 존재를 검출하기 위한 신속하고 간편하며, 정확한 방법임을 알 수 있었으며, 향후 임상에서 활용성이 클 것으 로 사료된다.REFERENCES
1. 김미영, 이무주, 최철석, 이경옥 : 체액에서
nested polymerase chain
reaction을 이 용 한 결핵균의 검출에 관한 고찰. 임상병리 검사과학회지27 : 98-104
,1995.
2.
김상재, 박영길, 조상현, 심명섭 : 핵산 중합 효소 연쇄 반응에 의한 병리검체내 결핵균의 검출. Primer선택과 반응 조건. 대한미 생물학회지
27 : 35-44
,1992.
3.
박정준, 김동언 : 미생물 감염증에서PCR
의 역할. 대한임상병리사회지
26 : 7-14
,1994.
4.
서진태, 김상인 : 결핵균의 신속한 약제 감 수성 검사를 위한 효소면역법 활용에 관한 연구. 대한임상병리학회지13 : 259-269
,1993.
5.
윤경한, 이태윤, 조상래, 김득순, 정동현, 김 주덕 : 가검물내 결핵균 검출에 있어서DNA
분리방법에 따른 중합 효소 연쇄 반 응의 민감도 비교. 대한미생물학회지26 : 159-166 , 199
1.6.
최철석, 김은아, 이경옥 : 임상 가검물에서 중합 효소 연쇄 반응을 이용한 결핵균 진 단의 평가. 대한미생물학회지28 : 381- 389 , 1993.
7.
최철석, 이경옥, 이규범 : PCR을 이용한 결 핵균 진단에 있어서 효과적인 DNA추출법.대한미생물학회지
29 : 147-152
,1994.
8. Bloom B and Murray CJL.: Tuberculosis : commentary on a resurgent killer. Sci- ence 257 : 1055-1064 , 1992.
9. Clarridge JE , Shawar RM , Shinnick TM and Plikaytis BB.: Large scale use of polymerase chain reaction f or detection of Mycobacterium tuberculosis in a routine mycobacteriology laboratory.
JClin Mic- robio l. 31 : 2049-2056 , 1993.
10. Cole ST. : Mycobacterium tuberculosis: drug - resistance mechanism. Trends Microbio l.
2 : 411-415 , 1994.
1
1.Dabbs ER
,Yazawa K
,Mikami Y
,Miyaji M
,Morisaki N and Iwasaki S.: Ribosylation by mycobacterial strains as a new mecha- nism of rifampicin inactivation. Antimicrob Agents Chemother. 39 : 1007 -1009, 1995.
12. Heifets
L.Qualitative and quantitative drug susceptibility tests in mycobacteriology. Am
Res Respir Dis. 17 : 1217 -1222 , 1988.
13. Huebner RE , Good RC and Tokars JI.
Current practices in mycobacteriology:
results of a survey of state public health laboratories. J Clin
λr!icrobiol.31: 771- 775 , 1993.
14. Inderlied CB. Antimycobaterial agents. In : Lorian V , ed. Antibiotics in Laboratory Medicine. 3rd ed. Baltimore: MD. Wil- liams and Wilkins 134-1397 , 199
1.15. Jin D and Gross C. Mapping and se- quencing of mutations in the E. coli rpo
βgene that lead to rifampicin resistance.
JMol Bio l. 202 : 45 - 48 , 1988.
16. Kapur V , Li L and Iordanescu S. Charac- terization by automated DNA sequencing of mutations in the gene (rpo ß) encod- ing the RNA polymerase
βsubunit in the rifampicin resistant Mycobacterium tubercu- losis strains from New Y ork City and Texas. J Clin Microbio l. 32: 1095 -1098 , 1994.
17. Kawa DE , Pennell DR , Kubista LN and Scell RF. Development of rapid method for determining the susceptibility of Mycobacteriun tuberculosis to isoniazid using the gene-probe DNA hybridization system. Antimicrob Agents Chemother. 33 : 1000-1005 , 1989.
18. Kirihara DG , Hillier SL and Coyle MG.
Improved detection times for M. tuberculo- sis in BACTEC radiometric system. J Clin Microbio l. 22 : 841-845 , 1985.
19. Kochi A , Vareldzis B and Styblo K.
Mutidrug-resistant tuberculosis and its contro
l.Res Microbio l. 144: 104-110 , 1993.
20. Lhiang Z , Jannes G and Mijs W. Rapid
detection of rifampicin resistance in spu-
tum and biopsy specimens from tubercu-
losis patients by PCR and line probe assay. Tubercle and Lung Disease 76 : 425
-430 , 1995.
2
1.Miler LM , Crawfold JT and Shinnick TM.
The Mycobacterium tuberculosis rpo ß gene.
Antimicro Agents Chemother 38 : 805 - 811 , 1994.
22. Morris S , Bai GH , Suffyd p , Portillo- Gomez L , Fairchok M and Rouse D. Molecu- lar mechanisms of multidrug resistance in clinical isolates of
}.ψcobacterium tuberculθsis.
J lnfect Dis.171 : 945 - 960 , 1995.
23. Nowak R. WHO calls for action againts TB. Science 267 : 1763 , 1995.
24. Robers GD , Goodman NL , Heifets L , Larsh HW , Linder TH and McClatchy JK. Evalua tion of BACTEC radiometric method for re- covery of mycobacteria and drug sus- ceptibility testing of Mycobacterium tubercu-
losis from acid fast smear positive speci mens. J Clin Microbiol. 18 : 689-696 , 1983.
25. Telanti A , 1mboden P , Marchesi F , Lowrie D, Cole S and Colston MJ. Detec- tion of rifampicin -resistance mutations in Mycobacterium tuberculosis. Lancet 341:
647-650 , 1993.
26. Telanti A , 1mboden P , Marchest F , Schmidheini T and Bodmer T. Direct , au- tomated detection of rifampicin -resistant Mycobacterium tuberculosis by polymerase chain reaction and single strand confor- mational polymorphism. Antimicrob Agents
Cheηwther37: