Porphyromonas gingivalis
에 지속적으로 노출된 구강암 세포의 단백발현 변화위신욱1)#, 우복희1)#, 김다정1,2), 이지혜1,2), 박봉수2,3), 박혜련1,2)*
부산대학교 치의학전문대학원 구강병리학교실1), BK21플러스 사업단2), 구강해부학교실3)
<Abstract>
Changes in Protein Expression of Oral Cancer Cells Continuosly Exposed to
Porphyromonas gingivalis
Sin Wook Wi
1)#, Bok Hee Woo
1)#, Da Jeong Kim
1,2), Ji Hye Lee
1,2), Bong Soo Park
2,3), Hae Ryoun Park
1,2)*Department of Oral Pathology
1), BK21 PLUS Project
2), Department of Oral Anatomy
3), School of Dentistry, Pusan National University
Porphyromonas gingivalis is a gram-negative bacteria of rod shape, and grown in an anerobic condition. It colonizes in subgingival crevice and is known as a major pathogen causing chronic periodontitis. It possesses an invasive property and replicative potential within various cell types, presumably playing an important role in modulating biological behaviors of oral cancer. However, the pathophysiology of P. gingivalis in the malignant transformation of oral cancer has not been fully understood. In this study, we aimed to investigate molecular changes of oral squamous cell carcinoma cells induced by repetitive P. gingivalis infection that clinically resembles chronic periodontitis.
Key words : Porphyromonas gingivalis , Oral Cancer, Periodontitis, L-plastin, S1009A
Korean Journal of Oral and Maxillofacial Pathology 2017;41(1):009-016 ISSN:1225-1577(Print); 2384-0900(Online) Available online at http://journal.kaomp.org https://doi.org/10.17779/KAOMP.2017.41.1.002
# These authors equally contributed to this work.
* Correspondence: Hae Ryoun Park, Department of Oral Pathology, School of Dentistry, Pusan National University
Tel: +82-51-510-8250, Fax: +82-51-510-8249 E-mail: parkhr@pusan.ac.kr
ORCID : 0000-0003-1908-0824
Ⅰ. 서 론
구강 내 만성염증 중 가장 대표적인 것이 치주염이다. 치주 염은 치아 지지조직의 만성염증성 질환이며, 적은 양이지만 혈액 내로 염증매개물질을 유리하여 지속적인 전신염증을 일 으키는 것으로 알려져 있다. 만성 치주염 상태에서 유리하는
염증 매개체들이 세균혈증(bacteremia)을 통해 전신으로 퍼 져나가므로 다양한 전신질환의 발생과 진행에 영향을 미치는 것으로 추정하고 있다. 이를 바탕으로 만성 치주염이 다양한 전신질환에 미치는 영향에 대해 연구되어 왔으며 대표적으로 는 만성 치주염과 죽상경화증의 연관성에 대한 연구가 있 다1,2). 당뇨와의 연관성 연구에 의하면 당뇨환자의 고혈당증 (hyperglycemia)이 치주질환 환자 예후에 나쁜 영향을 미치는 것을 관찰하였으며, 최근 연구에서는 중증 치주질환 환자에서 당뇨발생의 위험성이 증가되는 것으로 보고하고 있다3). 이외 에도 만성치주염과 알츠하이머 치매, 조산, 저체중아 출산, 췌 장암 등과의 연관성에 대한 연구들이 다양한 방법으로 시도되
고 있다4-6). 이와 같이 치주염이 다양한 질환들에 미치는 영향 과 상관관계에 대한 연구들이 매우 많으나 구강암과의 연관성 에 대한 연구는 거의 없다. 구강암의 경우, 치주염과 관련된 요인들에 의해 직접적으로 영향을 받는 위치에 있어 타 질환 에 비해 상호 연관성이 매우 높을 것으로 예상되나, 현재까지 구강암과 만성치주염 간의 상관 관계에 대한 연구는 몇몇의 역학조사에 국한되어 있다7,8). 이러한 역학연구들에 의하면 치주질환자들에서 구강암 발병 빈도가 높은 것으로 보고되고 있으며, 이에 근거하여 만성치주염이 구강암의 발생과 진행에 기여할 수 있음을 짐작할 수 있다.
염증은 면역세포와 이 세포들이 분비하는 사이토카인과 성 장인자들이 관여하는 반응으로 세포의 재생을 촉진하는데 주 로 기여하나, 세포를 구성하는 여러 가지 단백질의 손상을 유 도하기도 한다. 이러한 것들을 고려해보면, 만성 치주염의 대 표적 병원균인 Porphyromonas gingivalis (P. gingivalis) 감염 으로 유발된 염증에 의한 구강편평세포암종 세포의 단백질 발 현 양상 변화를 연구함으로써 구강암의 발병에 관한 가치 있 는 통찰을 얻을 수 있을 것이고, 나아가서 구강암 치료의 극대 화를 가져올 수 있는 치료기법의 개발에 도움을 줄 수 있을 것이다. 기존의 연구에서는 주로 교정용 와이어 결찰로 마우 스 대구치에서 치주염을 유도하는 방법, 마우스에 P.
gingivalis를 경구 투여하여 치주염시 관찰되는 세균혈증을 유 도하는 방법 등이 치주염 유발 모델로 활용되고 있다9,10). 본 연구에서는 구강암세포를 P. gingivalis에 직접적으로 감염시 켜 구강암세포 내에서 일어나는 변화를 단백질 중심으로 관찰 하였다. 이와 같은 실험 연구를 통해 치주염이 구강암에 미치 는 영향에 대해 알아보고, 치주염과 구강암의 상호관계에 대 해 보다 명확히 파악하고자 하였다.
Ⅱ. 재료 및 방법
1.
P. gingivalis배양
yeast extract (1 mg/ml), hemin (5 μg/ml), menadione (1 μg/ml)이 함유된 trypticate soy broth를 이용하여 P. gingivalis strain 381을 37℃ 혐기성 배양기에서 배양하였다.
2. 구강암세포 배양
구강암세포주는 구강편평세포암종 세포주 Ca9-22를 사용하 였다. MEM/F-12(1:1)에 10% fetal bovine serum(GIBCO-BRL, Rockville, MD, USA)이 첨가된 배지를 이용하여 37℃, 5% 이 산화탄소 배양기에서 배양하였다.
3. 구강암 세포내
P. gingivalis감염
인산완충 식염수 용액(phosphate-buffered saline, PBS) 으로 두 번 씻은 P. gingivalis를 감염다중도(multiplicity of infection, MOI) 100 비율로 구강암세포위에 분주하였다. 이후 37℃, 5% 이산화탄소 배양기에서 3시간 배양하여 P. gingivalis 가 구강암세포 내부로 침투될 수 있도록 한 다음, PBS로 씻어 내어 구강암세포 바깥에 남아 있는 P. gingivalis는 제거하였 다. 항생제가 들어 있는 새 배지로 교환 후 이산화탄소 배양기 에서 세포를 배양하였다.
4. 단백질 정제
P. gingivalis로 감염시킨 또는 감염시키지 않은 구강암세 포를 배양접시에서 떼어낸 후 차가운 PBS로 씻고 세포를 모 은 후 원심분리하여 RIPA buffer(20 mM Tris-HCl (pH 7.5), 150 mM NaCl, 1 mM EDTA, 1 mM EGTA, 1% NP-40, 1%
sodium deoxycholate, 2.5 mM sodium pyrophosphate, 1 mM β-glycerophosphate, 1 mM Na3VO4, 1 μg/ml leupeptin) 로 용해시켰다. 용해시킨 세포를 11,000g 속도로 15분간 원심 분리하여 상층액만 모아 새로운 튜브에 옮긴 후, 5X 젤 주입 완충용액(gel loading buffer;0.25% Bromophenol blue, 0.5 M dithiothreitol, 50% glycerol, 10% sodium dodecyl sulfate (SDS), 0.25M Tris-Cl, pH 6.8)를 적용하여 95℃에서 5분간 끓여 냉장 보관하였다.
5. 단백질 분석
젤 주입 완충용액과 함께 끓여 보관하고 있던 단백질을 10% SDS-polyacrylamide gel에서 1차원 전기영동과 2차원 전
Fig. 1. 단백발현 변화 분석 실험 절차
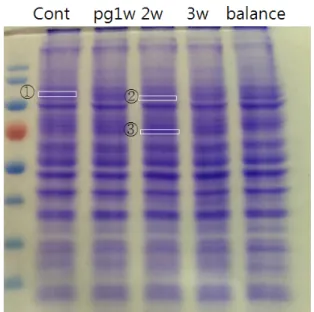
Fig. 2. P. gingivalis로 감염되지 않은 또는 감염된 구강편평 세포암종 세포내 단백질 발현 변화 관찰 소견 (Coomassie blue 염색)
기영동 두 가지 방법으로 각각 분리하였다. 1차원 전기영동 샘플의 경우 Coomassie blue G250 용액으로 염색을 시행하 여 대조군과 뚜렷한 차이를 보이는 밴드를 잘라내어 분석하였 다. 2차원 전기영동을 실시한 젤의 경우 은염색(silver staining) 을 시행 후 Image Master TM2D Platinum(GE healthcare, ver.5.0) 프로그램으로 이미지를 분석하였다. 대조군과 실험 군에서 관찰되는 단백질 스팟(spot) 차이를 확인하고 뚜렷한 차이를 보이는 스팟을 잘라내어 단백질을 분석하였다. 2차원 전기영동의 경우 pH 범위가 3-10, 4-7인 두 가지 조건에서 실 시하였다(Fig. 1).
Ⅲ. 결 과
1.
P. gingivalis가 일으키는 구강편평세포암종 세포내 단백질 변화
치주염은 대표적인 만성 염증성 질환으로 성인의 경우 특 히 나이가 많을수록 오랫동안 지속되는 치주염을 가지고 있었 을 가능성이 높다. 따라서 치주염을 가진 환자의 구강 점막, 치은 및 치주 조직같은 구강내 환경은 치주염 인자에 장기간
노출된 상태이므로 이와 같은 상태를 재현하고자 하였다. 선 행 연구 결과에 따르면, 일회성으로 단기간에 걸쳐 구강편평 세포암종 세포(Ca9-22)와 함께 배양된 P. gingivalis의 경우, 세 포내로 침투한 후 시간이 경과함에 따라 그 감염 정도가 점점 감소하는 것으로 보아 세포내에서 장시간 생존하거나 증식하 지는 못하는 것으로 보였다11). 따라서 Ca9-22 세포를 P.
gingivalis에 반복적으로 오랫동안 노출시켜 만성 염증성 자극 상태를 재현하고자 하였다. 이를 위해 구강암세포를 분주한 후 다음 날 P. gingivalis에 3시간 동안 감염시키고 PBS로 씻는 과정을 일주일에 두 번씩 시행하였으며, 또한 이를 5주간에 걸쳐 지속적으로 반복하였다. 이후 장시간 P. gingivalis에 노 출된 구강암세포들의 단백질 변화를 분석하였다. 1차원 전기 영동에 사용한 샘플의 경우 P. gingivalis에 1주, 2주, 3주 동안 주기적으로 반복 노출된 구강암세포의 단백질을 분석하였으 며, 2차원 전기영동에는 5주까지 지속적으로 P. gingivalis에 반복 노출된 구강암세포를 사용하였다.
1) 1차원 전기영동 결과
1차원 전기영동 후 Coomassie blue로 염색한 결과 육안으 로 증가와 감소가 뚜렷하게 관찰되는 밴드 세 개를 절취하여 분석하였다(Fig. 2). Fig. 2에서 관찰되는 밴드 중 샘플 ①은
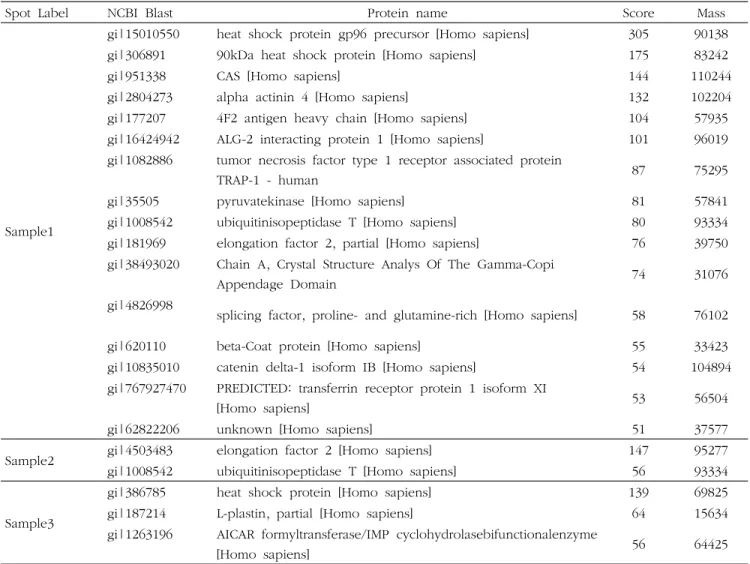
Table 1. Protein analysis of up and down band in cell of repetitive P. gingivalis infected oral sq. cell ca.
Spot Label NCBI Blast Protein name Score Mass
Sample1
gi|15010550 heat shock protein gp96 precursor [Homo sapiens] 305 90138
gi|306891 90kDa heat shock protein [Homo sapiens] 175 83242
gi|951338 CAS [Homo sapiens] 144 110244
gi|2804273 alpha actinin 4 [Homo sapiens] 132 102204
gi|177207 4F2 antigen heavy chain [Homo sapiens] 104 57935
gi|16424942 ALG-2 interacting protein 1 [Homo sapiens] 101 96019 gi|1082886 tumor necrosis factor type 1 receptor associated protein
TRAP-1 - human 87 75295
gi|35505 pyruvatekinase [Homo sapiens] 81 57841
gi|1008542 ubiquitinisopeptidase T [Homo sapiens] 80 93334
gi|181969 elongation factor 2, partial [Homo sapiens] 76 39750
gi|38493020 Chain A, Crystal Structure Analys Of The Gamma-Copi
Appendage Domain 74 31076
gi|4826998
splicing factor, proline- and glutamine-rich [Homo sapiens] 58 76102
gi|620110 beta-Coat protein [Homo sapiens] 55 33423
gi|10835010 catenin delta-1 isoform IB [Homo sapiens] 54 104894
gi|767927470 PREDICTED: transferrin receptor protein 1 isoform XI
[Homo sapiens] 53 56504
gi|62822206 unknown [Homo sapiens] 51 37577
Sample2 gi|4503483 elongation factor 2 [Homo sapiens] 147 95277
gi|1008542 ubiquitinisopeptidase T [Homo sapiens] 56 93334
Sample3
gi|386785 heat shock protein [Homo sapiens] 139 69825
gi|187214 L-plastin, partial [Homo sapiens] 64 15634
gi|1263196 AICAR formyltransferase/IMP cyclohydrolasebifunctionalenzyme
[Homo sapiens] 56 64425
대조군과 비교시 감염군에서 발현이 줄어든 것이며, 샘플 ② 와 ③은 감염군에서 발현 정도가 증가한 것이다. 세 개의 밴드 내 단백질을 분석한 결과는 Table 1에 제시하였다.
2) 2차원 전기영동 결과
2차원 전기영동의 경우 두 가지의 pH 범위(4-7; 3-10)에서 단백질 분리를 시행하고 은염색을 실시하였다. P. gingivalis에 감염되지 않은 대조군과 감염된 군의 단백질 분리 소견을 사 진 촬영하여 비교하였다. pH 3-10 범위에서 단백질을 분리한 겔 이미지 분석 프로그램에서 각 스팟(spot)의 강도를 % volume 값으로 수치화한 후, 대조군과 실험군 이미지 값의 비율(ratio, fold)이 2이상인 스팟만을 선별한 결과, 대조군에 비해 실험군에 발현 증가를 보이는 스팟이 4개, 감소를 보이
는 스팟이 5개, 대조군에서 관찰되지 않으나 실험군에서 새롭 게 나타난 스팟이 3개로 분석되었다(Fig. 3).
pH 범위 4-7에서 2차원 전기영동으로 단백질 분리를 시행 하고 은염색을 실시한 결과는 Fig. 4와 같다. 스팟 이미지 차 이를 분석한 결과 대조군에 비해 실험군에 발현 증가를 보이 는 스팟이 7개, 감소를 보이는 스팟이 4개, 대조군에서 관찰되 지 않으나 실험군에서 새롭게 나타난 스팟이 6개로 분석되었 다(Fig. 4).
두 가지 pH 범위에서 대조군에 비해 실험군에서 그 발현양 이 증가, 혹은 감소되거나 새롭게 나타난 스팟 중, 위치상 중 복되는 것을 구분하여 각 스팟 구성 단백질을 분석한 결과는 Table 2와 같다.
Fig. 3. Comparative expression between P. gingivalis non infected control cell and infected oral sq. cell ca. cell (pH 3-10)
Fig. 4. Comparative expression between P. gingivalis non infected control cell and infected oral sq. cell ca. cell (pH 4-7)
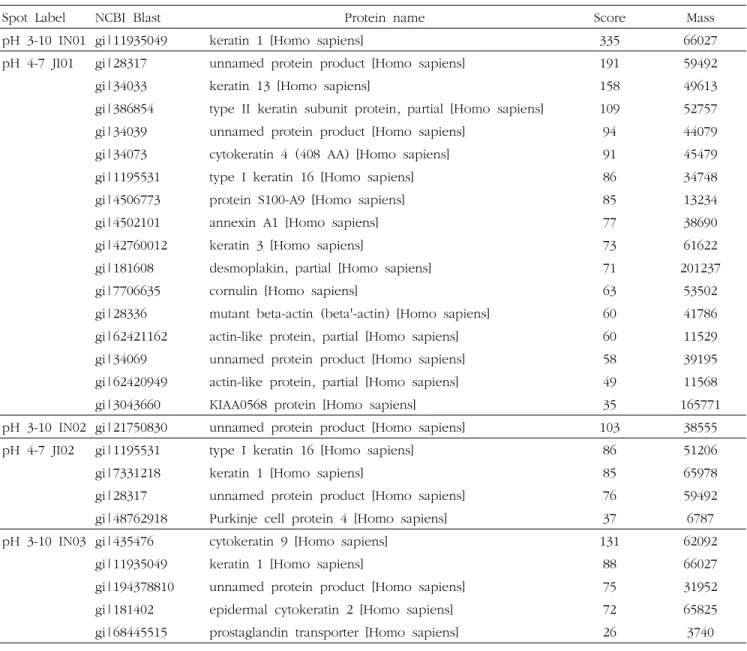
Table 2. Spot protein component analysis
Spot Label NCBI Blast Protein name Score Mass
pH 3-10 IN01 gi|11935049 keratin 1 [Homo sapiens] 335 66027
pH 4-7 JI01 gi|28317 unnamed protein product [Homo sapiens] 191 59492
gi|34033 keratin 13 [Homo sapiens] 158 49613
gi|386854 type II keratin subunit protein, partial [Homo sapiens] 109 52757
gi|34039 unnamed protein product [Homo sapiens] 94 44079
gi|34073 cytokeratin 4 (408 AA) [Homo sapiens] 91 45479
gi|1195531 type I keratin 16 [Homo sapiens] 86 34748
gi|4506773 protein S100-A9 [Homo sapiens] 85 13234
gi|4502101 annexin A1 [Homo sapiens] 77 38690
gi|42760012 keratin 3 [Homo sapiens] 73 61622
gi|181608 desmoplakin, partial [Homo sapiens] 71 201237
gi|7706635 cornulin [Homo sapiens] 63 53502
gi|28336 mutant beta-actin (beta'-actin) [Homo sapiens] 60 41786
gi|62421162 actin-like protein, partial [Homo sapiens] 60 11529
gi|34069 unnamed protein product [Homo sapiens] 58 39195
gi|62420949 actin-like protein, partial [Homo sapiens] 49 11568
gi|3043660 KIAA0568 protein [Homo sapiens] 35 165771
pH 3-10 IN02 gi|21750830 unnamed protein product [Homo sapiens] 103 38555
pH 4-7 JI02 gi|1195531 type I keratin 16 [Homo sapiens] 86 51206
gi|7331218 keratin 1 [Homo sapiens] 85 65978
gi|28317 unnamed protein product [Homo sapiens] 76 59492
gi|48762918 Purkinje cell protein 4 [Homo sapiens] 37 6787
pH 3-10 IN03 gi|435476 cytokeratin 9 [Homo sapiens] 131 62092
gi|11935049 keratin 1 [Homo sapiens] 88 66027
gi|194378810 unnamed protein product [Homo sapiens] 75 31952
gi|181402 epidermal cytokeratin 2 [Homo sapiens] 72 65825
gi|68445515 prostaglandin transporter [Homo sapiens] 26 3740
Ⅳ. 고 찰
그람 음성 혐기성 간균인 P. gingivalis는 만성 치주염의 대 표적 병원균으로 다양한 유형의 세포내로 침투해 들어간다는 보고가 있다. 이러한 침윤 능력으로 인해 세포 내 신호 전달 체계를 변화시켜 질환 발생 및 진행에 기여한다고 여기고 있
다12,13). 치주염은 성인에서 비교적 흔한 만성 염증성 질환으
로 구강암 환자에서 함께 발견될 가능성이 높다. 따라서 치주 염의 대표적 병원균인 P. gingivalis가 구강암 주위미세환경 (tumor microenvironment)에 공존할 가능성이 높으며 구강암
세포에 영향을 미칠 것으로 추정된다. 이러한 점에 착안하여 대표적 치주세균인 P. gingivalis가 구강암세포내로 침투하였 을 때의 단백질 변화를 1차원 전기영동으로 분리하여 관찰한 결과를 분석했을 때, L-plastin 단백질 증가가 특징적으로 관찰 되었다. Plastin은 Actin-결합 단백질로 L과 T의 두 가지 아형 (isoform)이 있다. 복제능력이 있는 섬유모세포, 내피세포, 상 피세포나 멜라닌 세포와 같은 고형 조직(solid tissue)에서 발 현되는 T-plastin과는 달리, L-plastin은 조혈계 세포에서만 발 현되는 것으로 알려져 있다. 하지만 악성 종양세포의 경우, 조혈계 세포가 아닌데도 L-plastin의 발현이 관찰되어 고형 조
직의 암 발생에 관여하는 것으로 추정하고 있다. 또한 암의 발생과 진행뿐만 아니라 침윤과 전이, 임상 병기 등의 요인에 도 기여하여 예후와 치료 결과와도 연관성을 가지는 것으로 보고되었다14,15). 최근 방광암을 포함한 여러 종양에서 생표지 자(biomarker)로서의 활용 가능성을 확인하는 등 다양한 연구 가 시도되고 있으나, L-plastin과 종양 발생 및 진행 과정과의 연계성에 대한 연구는 전반적으로 많지 않다16,17). 더욱이 구 강암 영역에서는 L-plastin이 종양 진행과정에서 어떠한 역할 을 하는지, 또는 진단 및 예후 평가시 활용될 수 있는지에 대 한 연구가 전혀 이루어지지 않고 있다. 본 연구에서 관찰한 P. gingivalis에 의한 L-plastin 발현 증가는 구강암 진행 과정에 서 L-plastin의 역할에 대한 가능성을 조사하고 P. gingivalis가 구강암세포에 미치는 영향과 분자생물학적 기전을 파악하는 데 중요한 기초 자료가 될 수 있을 것이다.
P. gingivalis에 감염된 구강암세포의 단백질을 2차원 전기 영동 분리 후 분석하여 증감이 관찰된 여러 후보 물질 중, 암 진행 및 전이와의 연관성이 활발히 연구되고 있는 S100A9 단 백질이 포함되어 있었다. S100A9 단백질의 경우 대장암 발생 과 진행 과정에서 종양 성장을 촉진하는 인자로 보고되었다
18). 최근 한 연구에 의해 S100A9 단백이 wnt/beta-catenin 경 로를 통해 대장암 침윤과 전이를 촉진하는 인자임이 밝혀졌고
19), 전립선암과 위암에서는 종양 성장 및 환자 예후와 연관되 어 있음이 보고되었으나20,21), 최근 한 피부암 연구에서는 종양 진행을 억제하는 인자로 보고되기도 했다22). 한편 S100A9 단 백이 구강암 발생 및 진행에 미치는 영향에 대한 연구는 많지 않다. 최근 Fang 등은 S100A9 단백이 세포외기질로 유리되어 구강암세포의 침윤과 종양 내 혈관신생 등을 촉진하며, 이 과 정에 염증성 사이토카인인 IL-6이 관여하고 있음을 보고하였 다23). S100A9의 암 발생과 악성도 증가 과정에서의 역할에 대한 결론이 아직 명확하지 않고 구강암과의 상호 관련성에 대한 연구는 밝혀진 것이 거의 없으나, 염증과 연계된 암의 생물학적 특성을 변화시키며 예후에 영향을 미친다는 점은 비 교적 잘 알려져있다. Inaba 등의 연구로 치주세균에 의한 평 활근 증식이 S100A9를 통해 일어나는 것은 이미 알려져 있어, P. gingivalis에 의한 S100A9 증가 자체는 새로운 발견이 아니 라고 할 수 있다24). 다만 본 연구 결과를 바탕으로, 구강암세
포 내에서의 S100A9 증가가 구강암 악성도 증진에 미치는 영 향과 기전 규명을 통해 치주세균의 역할을 보다 구체화할 수 있을 것으로 예상한다. 추가 연구를 통해 P. gingivalis에 의해 발현이 증가된 S100A9가 구강편평세포암종에서 일으키는 변 화와 기전을 규명하고, 이를 통해 P. gingivalis가 구강암세포 의 습성(behavior)에서 일으키는 변화, 나아가서 치주염이 구 강암 진행과 예후에 미치는 영향을 밝히는데 기여할 수 있을 것이다.
ACKNOWLEDGEMENT
이 논문은 부산대학교 기본연구지원사업(2년)에 의하여 연 구되었음
REFERENCES